Casodex 50mg Bicalutamide Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Casodex e como é usado?
Casodex é um medicamento de prescrição usado para tratar os sintomas do câncer de próstata. Casodex 50mg pode ser usado sozinho ou com outros medicamentos.
Casodex 50mg pertence a uma classe de medicamentos denominados Antineoplásicos, Antiandrogênicos; Inibidor de CYP3A4, Moderado.
Não se sabe se Casodex é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Casodex?
Casodex pode causar efeitos colaterais graves, incluindo:
- dor ou inchaço mamário,
- sangue na urina,
- febre,
- arrepios,
- dor ou desconforto súbito no peito,
- chiado,
- tosse seca,
- falta de ar,
- pele pálida,
- tontura,
- ritmo cardíaco acelerado,
- dificuldade de concentração,
- náusea,
- dor de estômago superior,
- sentindo-se cansado,
- perda de apetite,
- urina escura,
- fezes cor de barro,
- amarelecimento da pele ou dos olhos (icterícia),
- aumento da sede,
- aumento da micção,
- fome,
- boca seca,
- odor de hálito frutado,
- sonolência,
- pele seca,
- visão turva e
- perda de peso
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Casodex 50mg incluem:
- ondas de calor,
- dor nas costas,
- dor pélvica,
- dor abdominal,
- inchaço nas mãos, tornozelos ou pés,
- aumento da micção noturna,
- fraqueza,
- tontura,
- náusea,
- diarreia, e
- constipação
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Casodex. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
Os comprimidos de CASODEX® (bicalutamida) contêm 50 mg de bicalutamida, um inibidor não esteroidal do receptor de androgênio sem outra atividade endócrina conhecida. O nome químico é propanamida, N[4ciano-3-(trifluorometil)fenil]-3-[(4-fluorofenil)sulfonil]-2-hidroxi-2-metil-,(+-). As fórmulas estruturais e empíricas são:
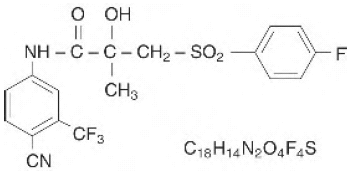
A bicalutamida tem um peso molecular de 430,37. O pKa' é de aproximadamente 12. A bicalutamida é um pó fino branco a esbranquiçado praticamente insolúvel em água a 37°C (5 mg por 1000 mL), ligeiramente solúvel em clorofórmio e etanol absoluto, pouco solúvel em metanol e solúvel em acetona e tetrahidrofurano.
CASODEX é um racemato cuja atividade antiandrogênica é quase exclusivamente exibida pelo enantiômero R da bicalutamida; o enantiômero S é essencialmente inativo.
Os ingredientes inativos dos comprimidos de CASODEX 50mg são lactose, estearato de magnésio, hipromelose, polietilenoglicol, polividona, amidoglicolato de sódio e dióxido de titânio.
INDICAÇÕES
CASODEX 50 mg por dia é indicado para uso em terapia de combinação com um análogo do hormônio liberador do hormônio luteinizante (LHRH) para o tratamento do carcinoma metastático da próstata em estágio D2.
CASODEX 150 mg por dia não é aprovado para uso isolado ou com outros tratamentos [ver Estudos clínicos ].
DOSAGEM E ADMINISTRAÇÃO
Dose e esquema recomendados
A dose recomendada para a terapia com CASODEX 50mg em combinação com um análogo de LHRH é um comprimido de 50mg uma vez ao dia (manhã ou noite), com ou sem alimentos. Recomenda-se que CASODEX 50mg seja tomado à mesma hora todos os dias. O tratamento com CASODEX deve ser iniciado ao mesmo tempo que o tratamento com um análogo de LHRH. Se uma dose de CASODEX 50mg for esquecida, tome a próxima dose no horário programado. Não tome a dose esquecida e não duplique a próxima dose.
Ajuste de Dosagem na Insuficiência Renal
Nenhum ajuste de dose é necessário para pacientes com insuficiência renal [ver Uso em populações específicas ].
Ajuste de Dosagem em Insuficiência Hepática
Não é necessário ajuste de dose para pacientes com insuficiência hepática leve a moderada. Em pacientes com insuficiência hepática grave (n=4), embora tenha havido um aumento de 76% na meia-vida (5,9 e 10,4 dias para pacientes normais e comprometidos, respectivamente) do enantiômero ativo da bicalutamida, nenhum ajuste de dose é necessário. Vejo Uso em populações específicas ].
COMO FORNECIDO
Formas de dosagem e força
CASODEX® (bicalutamida) comprimidos de 50 mg para administração oral.
Comprimidos revestidos por película brancos (identificados em um lado com "CDX50" e no verso com o "logotipo CASODEX") são fornecidos em frascos de dose unitária de 30 comprimidos (0310-0705-30).
Armazenamento e manuseio
Armazenar em temperatura ambiente controlada, 20°-25°C (68°-77°F).
Fabricado para: AstraZeneca Pharmaceuticals LP, Wilmington, DE 19850. Revisado: março de 2017.
EFEITOS COLATERAIS
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
Experiência de Ensaios Clínicos
Em pacientes com câncer de próstata avançado tratados com CASODEX 50mg em combinação com um análogo de LHRH, a reação adversa mais frequente foram ondas de calor (53%).
No ensaio clínico multicêntrico, duplo-cego e controlado comparando CASODEX 50 mg uma vez ao dia com flutamida 250 mg três vezes ao dia, cada uma em combinação com um análogo de LHRH, as seguintes reações adversas com incidência de 5% ou mais, independentemente de causalidade, foram relatados.
Outras reações adversas (maior ou igual a 2%, mas menor que 5%) relatadas no grupo de tratamento com análogo de CASODEX-LHRH estão listadas abaixo por sistema corporal e estão em ordem de frequência decrescente em cada sistema corporal, independentemente da causalidade.
Corpo como um todo: Neoplasia; Dor de pescoço; Febre; Arrepios; Sepse; Hérnia; Cisto
Cardiovascular: Angina Pectoris; Insuficiência Cardíaca Congestiva; Infarto do Miocárdio; Parada Cardíaca; Distúrbio da Artéria Coronária; Síncope
Digestivo: Melena; Hemorragia Retal; Boca seca; Disfagia; Distúrbio Gastrointestinal; Abscesso Periodontal; Carcinoma Gastrointestinal
Metabólico e Nutricional: Edema; BUN aumentado; Creatinina aumentada; Desidratação; Gota; Hipercolesterolemia
Musculoesquelético: Mialgia; Cãibras nas Pernas
Nervoso: Hipertonia; Confusão; Sonolência; Libido diminuída; Neuropatia; Nervosismo
Respiratório: Distúrbio Pulmonar; Asma; Epistaxe; Sinusite
Pele e anexos: Pele seca; Alopecia; Prurido; Herpes Zoster; Carcinoma de Pele; Doença de Pele
Sentidos Especiais: Especificado para catarata
Urogenital: Disúria; Urgência Urinária; Hidronefrose; Distúrbio do Trato Urinário
Valores anormais de testes laboratoriais:
Anormalidades laboratoriais, incluindo: AST, ALT, bilirrubina, BUN e creatinina elevados; e diminuição da hemoglobina e contagem de glóbulos brancos, foram relatados em pacientes tratados com análogo de CASODEX-LHRH e tratados com análogo de flutamida-LHRH.
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de CASODEX. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Distúrbios respiratórios: Doença pulmonar intersticial (algumas fatais), incluindo pneumonite intersticial e fibrose pulmonar, mais frequentemente em doses superiores a 50 mg.
Distúrbios da pele e tecidos subcutâneos: Fotossensibilidade
INTERAÇÕES MEDICAMENTOSAS
Os estudos clínicos não mostraram nenhuma interação medicamentosa entre bicalutamida e análogos de LHRH (gosselina ou leuprolida). Não há evidências de que a bicalutamida induza enzimas hepáticas.
Estudos in vitro demonstraram que a R-bicalutamida é um inibidor do CYP 3A4 com menores efeitos inibitórios sobre a atividade do CYP 2C9, 2C19 e 2D6. Estudos clínicos mostraram que com a coadministração de CASODEX, os níveis médios de midazolam (um substrato do CYP 3A4) podem aumentar 1,5 vezes (para Cmax) e 1,9 vezes (para AUC). Portanto, deve-se ter cautela quando CASODEX 50mg é coadministrado com substratos CYP 3A4.
Estudos in vitro de ligação a proteínas mostraram que a bicalutamida pode deslocar os anticoagulantes cumarínicos dos locais de ligação. Os tempos de protrombina devem ser monitorados de perto em pacientes que já estão recebendo anticoagulantes cumarínicos e que iniciaram CASODEX 50mg e o ajuste da dose de anticoagulante pode ser necessário.
AVISOS
Incluído como parte do "PRECAUÇÕES" Seção
PRECAUÇÕES
Hepatite
Casos de morte ou hospitalização devido a lesão hepática grave (insuficiência hepática) foram relatados pós-comercialização em associação com o uso de CASODEX. A hepatotoxicidade nesses relatos geralmente ocorreu nos primeiros três a quatro meses de tratamento. Hepatite ou aumentos acentuados nas enzimas hepáticas que levaram à descontinuação do medicamento ocorreram em aproximadamente 1% dos pacientes com CASODEX em ensaios clínicos controlados.
Os níveis séricos de transaminases devem ser medidos antes do início do tratamento com CASODEX, em intervalos regulares durante os primeiros quatro meses de tratamento e depois periodicamente. Se ocorrerem sintomas ou sinais clínicos sugestivos de disfunção hepática (p. ALT sérica, deve ser medida imediatamente. Se a qualquer momento um paciente tiver icterícia, ou sua ALT subir acima de duas vezes o limite superior do normal, CASODEX deve ser descontinuado imediatamente com acompanhamento rigoroso da função hepática.
Ginecomastia e dor mamária
Em ensaios clínicos com CASODEX 150 mg como agente único para câncer de próstata, ginecomastia e dor mamária foram relatadas em até 38% e 39% dos pacientes, respectivamente.
Tolerância a glicose
Uma redução na tolerância à glicose foi observada em homens recebendo agonistas de LHRH. Isso pode se manifestar como diabetes ou perda do controle glicêmico em pessoas com diabetes pré-existente. Portanto, deve-se considerar o monitoramento da glicemia em pacientes recebendo CASODEX 50mg em combinação com agonistas de LHRH.
Testes laboratoriais
Avaliações regulares do antígeno prostático específico (PSA) sérico podem ser úteis para monitorar a resposta do paciente. Se os níveis de PSA aumentarem durante a terapia com CASODEX 50mg, o paciente deve ser avaliado quanto à progressão clínica. Para pacientes que apresentam progressão objetiva da doença juntamente com PSA elevado, pode ser considerado um período livre de tratamento com antiandrogênio, enquanto continua o análogo de LHRH.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( INFORMAÇÃO DO PACIENTE ).
Dose e cronograma
Informe os pacientes que a terapia com CASODEX 50mg e o análogo de LHRH deve ser iniciada ao mesmo tempo e que eles não devem interromper ou parar de tomar esses medicamentos sem consultar seu médico [ver DOSAGEM E ADMINISTRAÇÃO ].
Hepatite
Informe os pacientes que CASODEX pode causar hepatite, que pode resultar em insuficiência hepática e morte. Aconselhar os pacientes que os testes de função hepática devem ser monitorados regularmente durante o tratamento e relatar sinais e sintomas de hepatite [ver AVISOS E PRECAUÇÕES ].
Tolerância a glicose
Informe os pacientes que diabetes ou perda do controle glicêmico em pacientes com diabetes pré-existente foi relatada durante o tratamento com agonistas de LHRH. Portanto, deve-se considerar o monitoramento da glicemia em pacientes recebendo CASODEX em combinação com agonistas de LHRH [ver AVISOS E PRECAUÇÕES ].
Sonolência
Durante o tratamento com CASODEX, foi relatada sonolência. Aconselhe os pacientes que apresentam este sintoma a tomar cuidado ao dirigir ou operar máquinas [ver REAÇÕES ADVERSAS ].
Fotossensibilidade
Informe os pacientes que casos de fotossensibilidade foram relatados durante o tratamento com CASODEX e que eles devem evitar a exposição direta à luz solar excessiva ou à exposição à luz UV. Deve-se considerar o uso de protetor solar [ver REAÇÕES ADVERSAS ].
Contracepção e fertilidade
Aconselhar os pacientes do sexo masculino com parceiras do sexo feminino com potencial reprodutivo a usarem métodos contraceptivos eficazes durante o tratamento e por 130 dias após a última dose da terapia com CASODEX 50mg. Avise os pacientes do sexo masculino que CASODEX pode prejudicar a fertilidade [ver Uso em populações específicas ].
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Estudos de carcinogenicidade oral de dois anos foram conduzidos em ratos e camundongos machos e fêmeas com doses de 5, 15 ou 75 mg/kg/dia de bicalutamida. Uma variedade de efeitos tumorais em órgãos-alvo foram identificados e foram atribuídos à antiandrogenicidade da bicalutamida, ou seja, tumores de células intersticiais benignas testiculares (Leydig) em ratos machos em todos os níveis de dose (a concentração plasmática no estado de equilíbrio com a dose de 5 mg/kg/dia é aproximadamente 0,7 vezes a exposição humana na dose recomendada) e adenocarcinoma uterino em ratas a 75 mg/kg/dia (aproximadamente 1,5 vezes a exposição humana na dose recomendada). Não há evidência de hiperplasia das células de Leydig em pacientes; os tumores uterinos não são relevantes para a população de pacientes indicada.
Um pequeno aumento na incidência de carcinoma hepatocelular em camundongos machos que receberam 75 mg/kg/dia de bicalutamida (aproximadamente 4 vezes a exposição humana na dose recomendada) e um aumento na incidência de adenomas benignos de células foliculares da tireoide em ratos que receberam 5 mg/kg /dia (aproximadamente 0,7 vezes a exposição humana na dose recomendada) e acima foram registrados. Estas alterações neoplásicas foram progressões de alterações não neoplásicas relacionadas com a indução de enzimas hepáticas observadas em estudos de toxicidade em animais. A indução enzimática não foi observada após a administração de bicalutamida no homem. Não houve efeitos tumorigênicos sugestivos de carcinogênese genotóxica.
Uma bateria abrangente de testes de genotoxicidade in vitro e in vivo (conversão de genes de levedura, Ames, E. coli, CHO/HGPRT, citogenética de linfócitos humanos, micronúcleo de camundongo e citogenética de medula óssea de rato) demonstrou que a bicalutamida não tem atividade genotóxica .
Em estudos de toxicologia de dose repetida, a atrofia dos túbulos seminíferos dos testículos foi observada para todas as espécies examinadas, o que é um efeito de classe previsto com antiandrogênios. No estudo de ratos de 6 e 12 meses, a atrofia testicular foi observada em aproximadamente 2 vezes a exposição humana na dose recomendada. No estudo de 12 meses em cães, a incidência de atrofia testicular foi observada em aproximadamente 7 vezes a exposição humana na dose recomendada. Em ratos machos administrados 250 mg/kg/dia (aproximadamente 2 vezes a exposição humana na dose recomendada), o intervalo pré-coital e o tempo para o acasalamento bem-sucedido foram aumentados no primeiro pareamento, mas não foram observados efeitos na fertilidade após o acasalamento bem-sucedido. Esses efeitos foram revertidos em 7 semanas após o término de um período de 11 semanas de dosagem.
Ratas fêmeas com doses de 1, 10 e 250 mg/kg/dia (menos de 2 vezes a exposição humana na dose recomendada) aumentaram a irregularidade do ciclo estral, mas não houve efeito sobre a fertilidade.
Em um estudo de desenvolvimento peri e pós-natal, descendentes fêmeas de ratos recebendo doses de 10 mg/kg/dia (aproximadamente 0,7 vezes a exposição humana na dose clínica recomendada) e acima tiveram taxas de gravidez reduzidas. A administração de bicalutamida a fêmeas grávidas resultou na feminização da prole masculina levando a hipospádia em doses de 10 mg/kg/dia (aproximadamente 0,7 vezes a exposição humana na dose recomendada) e acima. A prole masculina afetada também era impotente.
Uso em populações específicas
Gravidez
Resumo do risco
CASODEX é contraindicado para uso em mulheres grávidas, pois pode causar danos ao feto. CASODEX 50mg não é indicado para uso em mulheres. Não há dados em humanos sobre o uso de CASODEX 50mg em mulheres grávidas. Em estudos de reprodução em animais, a administração oral de bicalutamida a ratas grávidas durante a organogênese causou desenvolvimento anormal dos órgãos reprodutivos em fetos do sexo masculino em exposições de aproximadamente 0,7 a 2 vezes a exposição humana na dose recomendada (ver Dados ).
Dados
Dados de animais
Em um estudo de desenvolvimento embriofetal em ratas prenhas administrada durante o período de organogênese dos dias 6 a 15 de gestação, fetos machos reduziram a distância anogenital em doses de 10 mg/kg/dia e acima (aproximadamente 0,7 a 2 vezes a exposição humana em a dose recomendada).
Em um estudo de desenvolvimento pré e pós-natal, as ratas foram doseadas a partir do dia 7-16 da gestação e deixadas para acasalar e criar seus filhotes até o desmame . Filhotes machos de ratos que receberam doses de 10 mg/kg/dia (aproximadamente 0,7 vezes a exposição humana na dose recomendada) e acima, apresentaram redução da distância anogenital.
Em um estudo de desenvolvimento peri e pós-natal, as ratas receberam doses do 16º dia de gestação até o 22º dia de lactação e permitiram que criassem e criassem seus filhotes até o desmame. A sobrevivência e o peso da prole durante a lactação foram reduzidos para ninhadas de ratas maternas que receberam doses de 250 mg/kg/dia (aproximadamente 2 vezes a exposição humana na dose recomendada). Filhotes machos de ratos que receberam doses de 10 mg/kg/dia (aproximadamente 0,7 vezes a exposição humana na dose recomendada) e acima, apresentaram distância anogenital reduzida, órgãos sexuais secundários menores, criptorquidia e hipospádia, resultando em incapacidade de acasalar e engravidam suas parceiras. A prole feminina de ratos que receberam doses de 10 mg/kg/dia (aproximadamente 0,7 vezes a exposição humana na dose recomendada) e superiores tiveram taxas de gravidez reduzidas.
Lactação
Resumo do risco
CASODEX 50mg não é indicado para uso em mulheres grávidas. Não há informações disponíveis sobre a presença de bicalutamida no leite humano, ou sobre os efeitos no lactente ou na produção de leite. A bicalutamida foi detectada em leite de rato.
Fêmeas e Machos com Potencial Reprodutivo
Contracepção
Machos
A terapia antiandrogênica pode causar alterações morfológicas nos espermatozoides [ver Toxicologia não clínica ]. Com base nos achados em estudos de reprodução animal e seu mecanismo de ação, aconselhe os pacientes do sexo masculino com parceiras com potencial reprodutivo a usarem métodos contraceptivos eficazes durante o tratamento e por 130 dias após a dose final de CASODEX [ver Gravidez e FARMACOLOGIA CLÍNICA ].
Infertilidade
Machos

Com base em estudos em animais, CASODEX 50mg pode levar à inibição da espermatogênese e pode prejudicar a fertilidade em machos com potencial reprodutivo. Os efeitos a longo prazo de CASODEX 50mg na fertilidade masculina não foram estudados [ver Toxicologia não clínica ].
Uso Pediátrico
A segurança e eficácia de CASODEX 50mg em pacientes pediátricos não foram estabelecidas.
CASODEX (bicalutamida) comprimido orodispersível foi estudado em combinação com ARIMIDEX (anastrozol) comprimido orodispersível em um estudo aberto, não comparativo, multicêntrico que avaliou a eficácia e segurança deste regime de combinação durante 12 meses no tratamento de gonadotropina independente puberdade precoce em meninos com puberdade precoce familiar limitada ao sexo masculino, também conhecida como testotoxicose. Os pacientes foram incluídos no estudo se tivessem uma idade inicial ≥2 anos e um diagnóstico de testotoxicose com base em características clínicas de puberdade precoce progressiva, aumento testicular simétrico, idade óssea avançada, níveis puberais de testosterona sérica, padrão pré-puberal de secreção de gonadotrofina após um Teste de estimulação com GnRH e ausência de outras causas clínicas e bioquímicas de excesso de testosterona. Treze dos 14 pacientes inscritos completaram 12 meses de tratamento combinado (um paciente foi perdido no seguimento). Se a puberdade precoce central (PPC) se desenvolvesse, um análogo de LHRH deveria ser adicionado. Quatro pacientes foram diagnosticados com CPP durante o estudo de 12 meses e receberam tratamento análogo de LHRH e 2 pacientes adicionais foram diagnosticados no final dos 12 meses e receberam tratamento posteriormente. As características médias ± DP no início do estudo foram as seguintes: idade cronológica: 3,9±1,9 anos; idade óssea 8,8±2,5; relação idade óssea/idade cronológica: 2,06±0,51; taxa de crescimento (cm/ano): 10,81±4,22; escore de desvio padrão da taxa de crescimento (SDS): 0,41±1,36.
dose inicial de CASODEX foi de 12,5 mg. CASODEX foi titulado em cada paciente até que a concentração plasmática de R-bicalutamida (o isômero ativo da bicalutamida) no estado de equilíbrio atingisse 5-15 mcg/mL, que é a faixa de concentrações terapêuticas alcançadas em adultos com câncer de próstata após a administração do medicamento atualmente dose aprovada de CASODEX de 50 mg. A dose diária inicial de anastrozol foi de 0,5 mg. O anastrozol foi titulado independentemente em cada paciente até atingir no estado de equilíbrio uma concentração sérica de estradiol
análise primária de eficácia do estudo foi avaliar a mudança na taxa de crescimento após 12 meses de tratamento, em relação à taxa de crescimento durante ≥6 meses antes de entrar no estudo. As taxas de crescimento pré-estudo foram obtidas retrospectivamente. Não houve evidência estatística de que a taxa de crescimento foi reduzida durante o tratamento. Durante o tratamento com CASODEX/ARIMIDEX a taxa média de crescimento (cm/ano) diminuiu 1,6 cm/ano, IC 95% (-4,7 a 1,5) p=0,28; a taxa de crescimento média SDS diminuiu em 0,1 SD, IC 95% (–1,2 a 1,0) p=0,88. A Tabela 2 mostra os dados descritivos das taxas de crescimento para a população geral e para os subgrupos definidos pela história de tratamento prévio para testotoxicose com cetoconazol, espironolactona, anastrozol ou outros inibidores da aromatase.
As concentrações totais de testosterona aumentaram em média 5 mmol/L ao longo dos 12 meses de tratamento a partir de uma média inicial de 10 mmol/L. As concentrações de estradiol foram iguais ou inferiores ao nível de quantificação (9,81 pmol/L) para 11 de 12 pacientes após 12 meses de tratamento. Seis dos 12 pacientes iniciaram o tratamento com uma concentração de estradiol abaixo do nível de quantificação.
Não houve mortes, eventos adversos graves ou interrupções devido a eventos adversos durante o estudo. Dos 14 pacientes expostos ao tratamento do estudo, 13 (92,9%) apresentaram pelo menos um evento adverso. Os eventos adversos mais frequentemente relatados (> 3 pacientes) foram ginecomastia (7/14, 50%), puberdade precoce central (6/14, 43%), vômitos (5/14, 36%), cefaléia (3/14, 21%), pirexia (3/14, 21%) e infecção do trato respiratório superior (3/14, 21%). As reações adversas consideradas possivelmente relacionadas à bicalutamida pelos investigadores incluíram ginecomastia (6/14, 43%), puberdade precoce central (2/14, 14%), sensibilidade mamária (2/14, 14%), dor mamária (1/14, 7%), astenia (1/14, 7%), aumento da alanina aminotransferase [ALT] (1/14, 7%), aumento da aspartato aminotransferase [AST] (1/14, 7%) e dor torácica musculoesquelética (1 /14, 7%). A cefaleia foi a única reação adversa considerada possivelmente relacionada ao anastrozol pelos investigadores. Para o paciente que desenvolveu ALT e AST elevados, a elevação foi
Uso Geriátrico
Em dois estudos em pacientes que receberam 50 ou 150 mg por dia, não foi demonstrada nenhuma relação significativa entre a idade e os níveis de estado de equilíbrio da bicalutamida total ou do enantiômero R ativo.
Insuficiência hepática
CASODEX deve ser usado com cautela em pacientes com insuficiência hepática moderada a grave. CASODEX é extensamente metabolizado pelo fígado. Dados limitados em indivíduos com insuficiência hepática grave sugerem que a excreção de CASODEX pode ser retardada e pode levar a um maior acúmulo. Testes periódicos de função hepática devem ser considerados para pacientes com insuficiência hepática em terapia de longo prazo [ver AVISOS E PRECAUÇÕES ].
Nenhuma diferença clinicamente significativa na farmacocinética de qualquer enantiômero de bicalutamida foi observada em pacientes com doença hepática leve a moderada em comparação com controles saudáveis. No entanto, a meia-vida do enantiômero R aumentou aproximadamente 76% (5,9 e 10,4 dias para pacientes normais e comprometidos, respectivamente) em pacientes com doença hepática grave (n=4).
Insuficiência renal
insuficiência renal (medida pela depuração da creatinina) não teve efeito significativo na eliminação da bicalutamida total ou do enantiômero R ativo.
SOBREDOSAGEM
Ensaios clínicos de longo prazo foram conduzidos com dosagens de até 200 mg de CASODEX 50 mg por dia e essas dosagens foram bem toleradas. Não foi estabelecida uma dose única de CASODEX 50mg que resulte em sintomas de superdosagem considerados com risco de vida.
Não há antídoto específico; o tratamento de uma sobredosagem deve ser sintomático.
No manejo de uma superdosagem com CASODEX 50mg, o vômito pode ser induzido se o paciente estiver alerta. Deve-se lembrar que, nessa população de pacientes, vários medicamentos podem ter sido usados. A diálise provavelmente não será útil, uma vez que CASODEX é altamente ligado às proteínas e é extensamente metabolizado. São indicados cuidados gerais de suporte, incluindo monitoramento frequente dos sinais vitais e observação cuidadosa do paciente.
CONTRA-INDICAÇÕES
Casodex é contraindicado em:
Hipersensibilidade
CASODEX 50mg é contraindicado em qualquer paciente que tenha apresentado reação de hipersensibilidade ao medicamento ou a qualquer um dos componentes do comprimido. Reações de hipersensibilidade, incluindo edema angioneurótico e urticária, foram relatadas.
Mulheres
CASODEX 50mg não tem indicação para mulheres e não deve ser utilizado nesta população.
Gravidez
CASODEX 50mg pode causar dano fetal quando administrado a uma mulher grávida [ver Uso em populações específicas ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
CASODEX 50mg é um inibidor não esteroidal do receptor androgênico. Inibe competitivamente a ação dos andrógenos ligando-se aos receptores androgênicos do citosol no tecido alvo. O carcinoma prostático é conhecido por ser sensível ao andrógeno e responde ao tratamento que neutraliza o efeito do andrógeno e/ou remove a fonte do andrógeno.
Quando CASODEX 50mg é combinado com terapia com análogo de LHRH, a supressão da testosterona sérica induzida pelo análogo de LHRH não é afetada. No entanto, em ensaios clínicos com CASODEX como agente único para câncer de próstata, foram observados aumentos nos níveis séricos de testosterona e estradiol.
Em um subgrupo de pacientes que foram tratados com CASODEX e um agonista de LHRH, e que descontinuam a terapia com CASODEX 50mg devido ao câncer de próstata avançado progressivo, uma redução no Antígeno Prostático Específico (PSA) e/ou melhora clínica (fenômeno de retirada do antiandrogênio) pode ser observado.
Farmacocinética
Absorção
A bicalutamida é bem absorvida após administração oral, embora a biodisponibilidade absoluta seja desconhecida. A coadministração de bicalutamida com alimentos não tem efeito clinicamente significativo na taxa ou extensão da absorção.
Distribuição
A bicalutamida é altamente ligada às proteínas (96%) [ver INTERAÇÕES MEDICAMENTOSAS ].
Metabolismo/Eliminação
bicalutamida sofre metabolismo estereoespecífico. O isômero S (inativo) é metabolizado principalmente por glucuronidação. O isômero R (ativo) também sofre glucuronidação, mas é predominantemente oxidado a um metabólito inativo seguido por glucuronidação. Tanto os glicuronídeos originais quanto os metabólitos são eliminados na urina e nas fezes. O enantiômero S é rapidamente eliminado em relação ao enantiômero R, com o enantiômero R respondendo por cerca de 99% dos níveis plasmáticos totais em estado de equilíbrio.
A farmacocinética do enantiômero ativo de CASODEX 50mg em homens normais e pacientes com câncer de próstata é apresentada na Tabela 3.
Estudos clínicos
CASODEX 50 mg diariamente em combinação com um LHRH-A
Em um ensaio clínico multicêntrico, duplo-cego e controlado, 813 pacientes com câncer de próstata avançado não tratado previamente foram randomizados para receber CASODEX 50 mg uma vez ao dia (404 pacientes) ou flutamida 250 mg (409 pacientes) três vezes ao dia, cada um em combinação com análogos de LHRH (implante de acetato de goserelina ou depósito de acetato de leuprolida).
Em uma análise realizada após um acompanhamento médio de 160 semanas, 213 (52,7%) pacientes tratados com terapia com análogo de CASODEX-LHRH e 235 (57,5%) pacientes tratados com terapia com análogo de flutamida-LHRH morreram. Não houve diferença significativa na sobrevida entre os grupos de tratamento (ver Figura 1). A razão de risco para tempo até a morte (sobrevivência) foi de 0,87 (intervalo de confiança de 95% 0,72 a 1,05).
Figura 1 - A probabilidade de óbito de Kaplan-Meier para ambos os grupos de tratamento antiandrogênico. 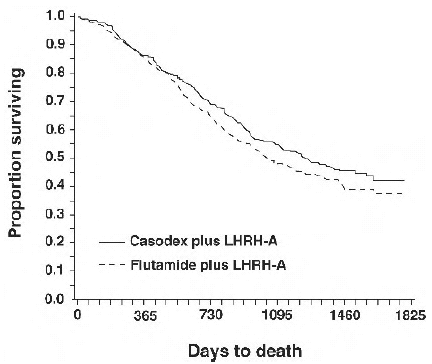
Não houve diferença significativa no tempo para progressão do tumor objetivo entre os grupos de tratamento (ver Figura 2). A progressão tumoral objetiva foi definida como o aparecimento de qualquer metástase óssea ou o agravamento de qualquer metástase óssea existente na cintilografia óssea atribuível à doença metastática, ou um aumento de 25% ou mais de qualquer metástase extraesquelética mensurável existente. A razão de risco para o tempo de progressão de CASODEX mais análogo de LHRH para flutamida mais análogo de LHRH foi de 0,93 (intervalo de confiança de 95%, 0,79 a 1,10).
Figura 2 - Curva de Kaplan-Meier para tempo de progressão para ambos os grupos de tratamento antiandrogênico. 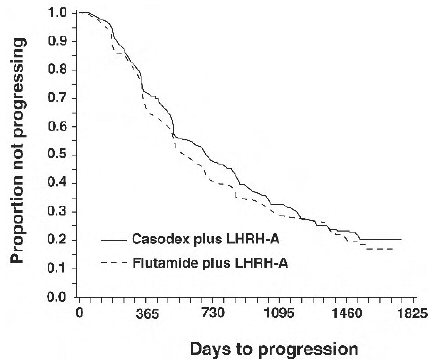
qualidade de vida foi avaliada com questionários auto-administrados ao paciente sobre dor, funcionamento social, bem-estar emocional, vitalidade, limitação de atividades, incapacidade de cama, saúde geral, capacidade física, sintomas gerais e sintomas relacionados ao tratamento. A avaliação dos questionários de Qualidade de Vida não indicou diferenças significativas consistentes entre os dois grupos de tratamento.
Dados de segurança de estudos clínicos usando CASODEX 150 mg
CASODEX 150 mg não está aprovado para uso isolado ou com outros tratamentos.
Dois estudos multicêntricos, randomizados e abertos, idênticos, comparando CASODEX 150 mg diários em monoterapia com castração foram conduzidos em pacientes que tinham câncer de próstata localmente avançado (T3-4, NX, M0) ou metastático (M1).
Monoterapia – Grupo M1
CASODEX 150 mg por dia não está aprovado para uso em pacientes com câncer de próstata M1. Com base em uma análise interina dos dois ensaios para sobrevida, o Data Safety Monitoring Board recomendou que o tratamento CASODEX fosse descontinuado nos pacientes M1 porque o risco de morte era de 25% (HR 1,25, IC 95% 0,87 a 1,81) e 31% ( HR 1,31, IC 95% 0,97 a 1,77) maior no grupo tratado com CASODEX 50mg em comparação ao grupo castrado, respectivamente.
Grupo Localmente Avançado (T3-4, NX, M0)
CASODEX 150 mg por dia não está aprovado para uso em pacientes com câncer de próstata localmente avançado (T3-4, NX, M0). Após a descontinuação de todos os pacientes M1, os estudos continuaram com os pacientes T3-4, NX, M0 até a conclusão do estudo. No estudo maior (N=352), o risco de morte foi 25% (HR 1,25, IC 95% 0,92 a 1,71) maior no grupo CASODEX e no estudo menor (N=140), o risco de morte foi 36 % (HR 0,64, IC 95%, 0,39 a 1,03) menor no grupo CASODEX 50mg.
Além dos dois estudos acima, há outros três estudos clínicos em andamento que fornecem informações adicionais de segurança para CASODEX 150 mg, uma dose que não está aprovada para uso. Estes são três estudos multicêntricos, randomizados, duplo-cegos e de grupos paralelos comparando monoterapia diária de 150 mg de CASODEX (adjuvante à terapia anterior ou sob vigilância) com placebo, para óbito ou tempo de progressão da doença, em uma população de 8.113 pacientes com câncer de próstata localizado ou localmente avançado.
CASODEX 150 mg por dia não está aprovado para uso como terapia para pacientes com câncer de próstata localizado que são candidatos a espera vigilante. Dados de uma análise de subgrupo planejada de dois desses estudos em 1.627 pacientes com câncer de próstata localizado que estavam sob vigilância, revelaram uma tendência de diminuição da sobrevida no braço CASODEX após um acompanhamento médio de 7,4 anos. Houve 294 (37,7%) mortes nos pacientes tratados com CASODEX versus 279 (32,9%) mortes nos pacientes tratados com placebo (grupo de espera vigilante localizado) para uma taxa de risco de 1,16 (IC 95% 0,99 a 1,37).
INFORMAÇÃO DO PACIENTE
CASODEX® [cas–o–dex] (bicalutamida) Comprimido
Leia esta Informação do Paciente antes de começar a tomar CASODEX 50mg e cada vez que receber um reabastecimento. Pode haver novas informações. Este folheto não substitui a conversa com o seu médico sobre a sua condição médica ou o seu tratamento.
O que é CASODEX 50mg?
CASODEX é um medicamento de prescrição chamado inibidor do receptor de andrógeno, usado em combinação com medicamentos do hormônio liberador do hormônio luteinizante (LHRH) para tratar o câncer de próstata metastático em estágio D2.
CASODEX não é para uso em mulheres.
Não se sabe se CASODEX é seguro e eficaz em crianças.
Quem não deve tomar CASODEX 50mg?
Não tome CASODEX 50mg se você:
- é uma mulher.
- estão grávidas ou podem engravidar. CASODEX pode prejudicar o feto.
- são alérgicos a qualquer um dos ingredientes de CASODEX. Consulte o final deste folheto para obter uma lista completa dos ingredientes do CASODEX. Obtenha ajuda médica imediatamente se tiver algum dos seguintes sintomas de uma reação alérgica: comichão, urticária (inchaços), inchaço da face, lábios ou língua, dificuldade em respirar ou engolir.
O que devo dizer ao meu médico antes de tomar CASODEX?
Antes de tomar CASODEX 50mg, informe o seu médico sobre todas as suas condições médicas, incluindo se você:
- tem problemas de fígado.
- tome um medicamento para afinar o sangue. Pergunte ao seu médico ou farmacêutico se não tiver certeza se o seu medicamento é um anticoagulante.
- tem diabetes (foi relatado um controle deficiente do açúcar no sangue em pessoas que tomam CASODEX em combinação com medicamentos para LHRH).
- tem um parceiro que está grávida ou pode engravidar. Você deve usar métodos de controle de natalidade eficazes enquanto estiver tomando CASODEX 50mg e por 130 dias após parar CASODEX. Converse com seu médico se tiver alguma dúvida sobre controle de natalidade.
Informe o seu médico sobre todos os medicamentos que toma, incluindo prescrição e medicamentos de balcão, vitaminas e suplementos de ervas. CASODEX 50mg e outros medicamentos podem afetar uns aos outros causando efeitos colaterais. CASODEX pode afetar o funcionamento de outros medicamentos, e outros medicamentos podem afetar o funcionamento de CASODEX 50mg.
Conheça os medicamentos que você toma. Mantenha uma lista de seus medicamentos com você para mostrar aos seus profissionais de saúde quando receber um novo medicamento.
Como devo tomar CASODEX 50mg?
- Tome CASODEX exatamente como seu médico lhe disse para tomá-lo.
- Tome CASODEX à mesma hora todos os dias.
- O seu tratamento com CASODEX 50mg deve começar ao mesmo tempo que o seu tratamento com o medicamento LHRH.
- Se você esquecer de uma dose, não tome uma dose extra, tome a próxima dose no horário regular. Não tome 2 doses ao mesmo tempo.
- CASODEX 50mg pode ser tomado com ou sem alimentos.
- Se você tomar muito CASODEX, ligue para o seu médico ou Centro de Controle de Intoxicações ou dirija-se ao pronto-socorro do hospital mais próximo imediatamente.
- Não pare de tomar CASODEX a menos que seu médico lhe diga.
- Seu médico pode fazer exames de sangue enquanto você toma CASODEX.
- Seu câncer de próstata pode piorar enquanto estiver tomando CASODEX em combinação com medicamentos para LHRH.
O monitoramento regular de seu câncer de próstata com seu médico é importante para determinar se sua doença é pior.
O que devo evitar ao tomar CASODEX 50mg?
Não conduza, opere máquinas ou faça outras atividades perigosas até saber como CASODEX o afeta.
Algumas pessoas tiveram sensibilidade da pele à luz solar enquanto tomavam CASODEX. Você deve evitar a luz solar ou lâmpadas solares e camas de bronzeamento e considerar o uso de protetor solar durante o tratamento com CASODEX.
Quais são os possíveis efeitos colaterais do CASODEX 50mg?
CASODEX pode causar efeitos colaterais graves, incluindo:
- Problemas hepáticos, incluindo insuficiência hepática que pode precisar ser tratada em um hospital ou que pode levar à morte. Seu médico deve fazer exames de sangue para verificar sua função hepática antes e durante o tratamento com CASODEX. Informe o seu médico imediatamente se tiver algum destes sintomas de um problema de fígado durante o tratamento:
- amarelecimento da pele e dos olhos (icterícia)
- urina escura
- dor de estômago superior direito
- náusea
- vômito
- cansaço
- perda de apetite
- arrepios
- febre
- Dificuldade em respirar com ou sem tosse ou febre. Algumas pessoas que tomam CASODEX 50mg apresentam uma inflamação nos pulmões chamada doença pulmonar intersticial.
- Uma reação alérgica. Os sintomas de uma reação alérgica incluem: comichão na pele, urticária (inchaços), inchaço da face, lábios, língua, garganta ou dificuldade em engolir.
- Aumento da mama (ginecomastia) e dor mamária.
- O controle deficiente do açúcar no sangue pode ocorrer em pessoas que tomam CASODEX 50mg em combinação com medicamentos LHRH. Seu médico pode verificar seu nível de açúcar no sangue durante a terapia com CASODEX 50mg.
Os efeitos colaterais mais comuns de CASODEX 50mg incluem:
- ondas de calor ou curtos períodos de sensação de calor e suor
- dor no corpo inteiro nas costas, pélvis, estômago
- sentindo fraco
- constipação
- infecção
- náusea
- inchaço nos tornozelos, pernas ou pés
- diarréia
- sangue na sua urina
- acordar do sono para urinar à noite
- uma diminuição dos glóbulos vermelhos (anemia)
- sentindo zonzo
Informe o seu médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do CASODEX. Para mais informações, pergunte ao seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar o CASODEX?
Armazene CASODEX em temperatura ambiente entre 20°C e 25°C (68°F a 77°F).
Mantenha CASODEX 50mg e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre o uso seguro e eficaz de CASODEX.
Às vezes, os medicamentos são prescritos para outros fins que não os listados em um folheto informativo para o paciente. Não use CASODEX para uma condição para a qual não foi prescrito. Não dê CASODEX 50mg a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Este folheto informativo do paciente resume as informações mais importantes sobre CASODEX. Se você quiser mais informações sobre CASODEX, fale com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre CASODEX escritas para profissionais de saúde. Para obter mais informações, acesse www.CASODEX.com ou ligue para 1-800-236-9933.
Quais são os ingredientes de CASODEX 50mg?
Ingrediente ativo: bicalutamida.
Ingredientes inativos: lactose, estearato de magnésio, hipromelose, polietilenoglicol, polividona, amidoglicolato de sódio, dióxido de titânio.
Esta informação do paciente foi aprovada pela Food and Drug Administration dos EUA.
