Lexapro 10mg, 20mg, 5mg Escitalopram Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Lexapro e como é usado?
Lexapro é um medicamento de prescrição usado para tratar os sintomas do transtorno depressivo maior e transtorno de ansiedade generalizada. Lexapro pode ser usado sozinho ou com outros medicamentos.
- Lexapro pertence a uma classe de medicamentos chamados antidepressivos, SSRIs.
- Não se sabe se Lexapro 10mg é seguro e eficaz em crianças menores de 12 anos de idade.
Quais são os possíveis efeitos colaterais do Lexapro?
Lexapro pode causar efeitos colaterais graves, incluindo:
- Dor abdominal,
- Sangramento anormal,
- Sonhos anormais,
- Alergia,
- visão embaçada,
- visão de túnel,
- dor no peito,
- concentração diminuída,
- hemostasia,
- dor ou inchaço nos olhos,
- vendo halos ao redor das luzes,
- pensamentos descontrolados,
- comportamento de risco incomum,
- sentimentos de extrema felicidade ou tristeza,
- dor de cabeça,
- azia,
- ondas de calor,
- confusão,
- fala arrastada,
- fraqueza severa,
- vômito,
- perda de coordenação,
- sentindo-se instável,
- músculos muito rígidos (rígidos),
- febre alta,
- sudorese,
- confusão,
- batimentos cardíacos rápidos ou irregulares,
- tremores, e
- tontura
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Lexapro incluem:
- tontura,
- sonolência,
- fraqueza,
- sudorese,
- sentindo-se trêmulo ou ansioso,
- problemas de sono (insônia),
- boca seca,
- perda de apetite,
- náusea,
- constipação,
- bocejando,
- alterações de peso,
- diminuição do desejo sexual,
- impotência, e
- dificuldade em ter um orgasmo
AVISO
SUICIDALIDADE E DROGAS ANTIDEPRESSIVAS
Os antidepressivos aumentaram o risco em comparação ao placebo de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens em estudos de curto prazo de transtorno depressivo maior (TDM) e outros transtornos psiquiátricos. Qualquer pessoa considerando o uso de Lexapro ou qualquer outro antidepressivo em uma criança, adolescente ou adulto jovem deve equilibrar esse risco com a necessidade clínica. Estudos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução no risco com antidepressivos em comparação com placebo em adultos com 65 anos ou mais. A depressão e alguns outros transtornos psiquiátricos estão associados ao aumento do risco de suicídio. Pacientes de todas as idades que iniciam terapia antidepressiva devem ser monitorados adequadamente e observados de perto quanto a piora clínica, suicídio ou mudanças incomuns no comportamento. As famílias e os cuidadores devem ser avisados da necessidade de observação atenta e comunicação com o prescritor. Lexapro 5mg não está aprovado para uso em pacientes pediátricos com menos de 12 anos de idade. [Ver AVISOS E PRECAUÇÕES Agravamento clínico e risco de suicídio, INFORMAÇÃO DO PACIENTE , e Uso em populações específicas : Uso Pediátrico].
DESCRIÇÃO
Lexapro® (oxalato de escitalopram) é um inibidor seletivo da recaptação de serotonina (ISRS) administrado por via oral. O Escitalopram é o Senantiomer puro (isômero único) do citalopram derivado bicíclico racêmico do ftalano. O oxalato de escitalopram é designado oxalato de S-(+)-1-[3(dimetil-amino)propil]-1-(p-fluorofenil)-5-ftalancarbonitrila com a seguinte fórmula estrutural:
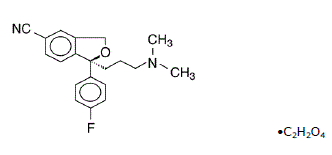
A fórmula molecular é C20H21FN2O • C2H2O4 e o peso molecular é 414,40.
O oxalato de escitalopram ocorre como um pó fino, branco a levemente amarelo e é livremente solúvel em metanol e dimetilsulfóxido (DMSO), solúvel em solução salina isotônica, pouco solúvel em água e etanol, ligeiramente solúvel em acetato de etila e insolúvel em heptano.
Lexapro (oxalato de escitalopram) está disponível em comprimidos ou em solução oral.
Os comprimidos de Lexapro são comprimidos redondos revestidos por película contendo oxalato de escitalopram em dosagens equivalentes a 5 mg, 10 mg e 20 mg de base de escitalopram. Os comprimidos de 10 e 20 mg são marcados. Os comprimidos também contêm os seguintes ingredientes inativos: talco, croscarmelose sódica, celulose microcristalina/dióxido de silício coloidal e estearato de magnésio. O revestimento de filme contém hipromelose, dióxido de titânio e polietilenoglicol.
Lexapro 5mg solução oral contém oxalato de escitalopram equivalente a 1 mg/mL de base de escitalopram. Também contém os seguintes ingredientes inativos: sorbitol, água purificada, ácido cítrico, citrato de sódio, ácido málico, glicerina, propilenoglicol, metilparabeno, propilparabeno e aroma natural de menta.
INDICAÇÕES
Transtorno Depressivo Maior
Lexapro (escitalopram) é indicado para o tratamento agudo e de manutenção do transtorno depressivo maior em adultos e adolescentes de 12 a 17 anos de idade [ver Estudos clínicos ].
Um episódio depressivo maior (DSM-IV) implica um humor deprimido ou disfórico proeminente e relativamente persistente (quase todos os dias por pelo menos 2 semanas) que geralmente interfere no funcionamento diário e inclui pelo menos cinco dos nove sintomas a seguir: humor deprimido, perda de interesse em atividades habituais, alteração significativa no peso e/ou apetite, insônia ou hipersonia, agitação ou retardo psicomotor, aumento da fadiga, sentimentos de culpa ou inutilidade, pensamento lento ou concentração prejudicada, tentativa de suicídio ou ideação suicida.
Distúrbio de ansiedade generalizada
Lexapro 20mg é indicado para o tratamento agudo do Transtorno de Ansiedade Generalizada (TAG) em adultos. Estudos clínicos ].
Transtorno de Ansiedade Generalizada (DSM-IV) é caracterizado por ansiedade e preocupação excessivas (expectativa apreensiva) persistentes por pelo menos 6 meses e que a pessoa tem dificuldade de controlar. Deve estar associado a pelo menos 3 dos seguintes sintomas: inquietação ou sensação de nervosismo, fadiga fácil, dificuldade de concentração ou mente vazia, irritabilidade, tensão muscular e distúrbios do sono.
DOSAGEM E ADMINISTRAÇÃO
Lexapro 5mg deve ser administrado uma vez ao dia, de manhã ou à noite, com ou sem alimentos.
Transtorno Depressivo Maior
Tratamento inicial
Adolescentes
A dose recomendada de Lexapro é de 10 mg uma vez ao dia. Um ensaio de dose flexível de Lexapro (10 a 20 mg/dia) demonstrou a eficácia de Lexapro [ver Estudos clínicos ]. Se a dose for aumentada para 20 mg, isso deve ocorrer após um mínimo de três semanas.
Adultos
dose recomendada de Lexapro 10mg é de 10mg uma vez ao dia. Um ensaio de dose fixa de Lexapro demonstrou a eficácia de 10 mg e 20 mg de Lexapro 5 mg, mas não conseguiu demonstrar um benefício maior de 20 mg em relação a 10 mg [ver Estudos clínicos ]. Se a dose for aumentada para 20 mg, isso deve ocorrer após no mínimo uma semana.
Tratamento de manutenção
É geralmente aceito que episódios agudos de transtorno depressivo maior requerem vários meses ou mais de terapia farmacológica sustentada além da resposta ao episódio agudo. A avaliação sistemática da continuação de Lexapro 10 ou 20 mg/dia em pacientes adultos com transtorno depressivo maior que responderam enquanto tomavam Lexapro durante uma fase de tratamento agudo de 8 semanas demonstrou um benefício de tal tratamento de manutenção [ver Estudos clínicos ]. No entanto, o médico que optar por usar Lexapro 5mg por períodos prolongados deve reavaliar periodicamente a utilidade a longo prazo do medicamento para o paciente individual. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção.
Distúrbio de ansiedade generalizada
Tratamento inicial
Adultos
A dose inicial recomendada de Lexapro é de 10 mg uma vez ao dia. Se a dose for aumentada para 20 mg, isso deve ocorrer após no mínimo uma semana.
Tratamento de manutenção
O transtorno de ansiedade generalizada é reconhecido como uma condição crônica. A eficácia de Lexapro no tratamento de TAG além de 8 semanas não foi sistematicamente estudada. O médico que optar por usar Lexapro por longos períodos deve reavaliar periodicamente a utilidade a longo prazo do medicamento para o paciente individual.
Triagem para transtorno bipolar antes de iniciar Lexapro
Antes de iniciar o tratamento com Lexapro ou outro antidepressivo, rastreie os pacientes quanto a história familiar pessoal de transtorno bipolar, mania ou hipomania [ver AVISOS E PRECAUÇÕES ].
Populações Especiais
10 mg/dia é a dose recomendada para a maioria dos pacientes idosos e pacientes com insuficiência hepática.
Nenhum ajuste de dose é necessário para pacientes com insuficiência renal leve ou moderada. Lexapro deve ser usado com cautela em pacientes com insuficiência renal grave.
Descontinuação do tratamento com Lexapro
Sintomas associados à descontinuação de Lexapro 5mg e outros ISRSs e SNRIs foram relatados [ver AVISOS E PRECAUÇÕES ]. Os pacientes devem ser monitorados quanto a esses sintomas ao descontinuar o tratamento. Recomenda-se uma redução gradual da dose em vez de uma interrupção abrupta sempre que possível. Se ocorrerem sintomas intoleráveis após a diminuição da dose ou após a descontinuação do tratamento, pode-se considerar a retomada da dose prescrita anteriormente. Subsequentemente, o médico pode continuar a diminuir a dose, mas a uma taxa mais gradual.
Troca de um paciente para ou de um inibidor da monoaminoxidase (IMAO) destinado a tratar distúrbios psiquiátricos
Devem decorrer pelo menos 14 dias entre a descontinuação de um IMAO destinado a tratar distúrbios psiquiátricos e o início da terapia com Lexapro. Por outro lado, pelo menos 14 dias devem ser permitidos após a interrupção de Lexapro 20mg antes de iniciar um IMAO destinado a tratar distúrbios psiquiátricos [ver CONTRA-INDICAÇÕES ].
Uso de Lexapro com outros IMAOs, como linezolida ou azul de metileno
Não inicie Lexapro 5mg em um paciente que está sendo tratado com linezolida ou azul de metileno intravenoso porque há um risco aumentado de síndrome serotoninérgica. Em um paciente que requer tratamento mais urgente de uma condição psiquiátrica, outras intervenções, incluindo hospitalização, devem ser consideradas [ver CONTRA-INDICAÇÕES ].
Em alguns casos, um paciente que já esteja recebendo terapia com Lexapro 10mg pode necessitar de tratamento urgente com linezolida ou azul de metileno intravenoso. Se alternativas aceitáveis ao tratamento com linezolida ou azul de metileno intravenoso não estiverem disponíveis e os benefícios potenciais do tratamento com linezolida ou azul de metileno intravenoso forem considerados superiores aos riscos de síndrome serotoninérgica em um determinado paciente, Lexapro deve ser interrompido imediatamente e linezolida ou azul de metileno intravenoso pode ser administrado. O paciente deve ser monitorado quanto a sintomas de síndrome serotoninérgica por 2 semanas ou até 24 horas após a última dose de linezolida ou azul de metileno intravenoso, o que ocorrer primeiro. A terapia com Lexapro pode ser retomada 24 horas após a última dose de linezolida ou azul de metileno intravenoso [ver AVISOS E PRECAUÇÕES ].
risco de administrar azul de metileno por vias não intravenosas (como comprimidos orais ou por injeção local) ou em doses intravenosas muito inferiores a 1 mg/kg com Lexapro 10 mg não é claro. O clínico deve, no entanto, estar ciente da possibilidade de sintomas emergentes da síndrome serotoninérgica com tal uso [ver AVISOS E PRECAUÇÕES ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
Comprimidos
Os comprimidos de Lexapro 10 mg são comprimidos redondos revestidos por película contendo oxalato de escitalopram em dosagens equivalentes a 5 mg, 10 mg e 20 mg de base de escitalopram. Os comprimidos de 10 e 20 mg são marcados. Impresso com "FL" em um lado e "5", "10" ou "20" no outro lado de acordo com suas respectivas forças.
Solução oral
Lexapro solução oral contém oxalato de escitalopram equivalente a 1 mg/mL de base de escitalopram (não sendo comercializado atualmente).
Armazenamento e manuseio
Comprimidos
Comprimidos de 5mg
Garrafa de 100 - NDC # 0456-2005-01
Branco a esbranquiçado, redondo, sem sulcos, revestido por película. Imprima "FL" em um lado do tablet e "5" no outro lado.
Comprimidos de 10 mg
Garrafa de 100 - NDC 0456-2010-01 10 x 10 Unidade de Dose - NDC # 0456-2010-63
Branco a esbranquiçado, redondo, marcado, revestido com película. Impressão no lado marcado com "F" no lado esquerdo e "L" no lado direito. Impressão no lado não marcado com "10".
Comprimidos de 20 mg
Garrafa de 100 - NDC # 0456-2020-01 10 x 10 Unidade de Dose - NDC # 0456-2020-63
Branco a esbranquiçado, redondo, marcado, revestido com película. Impressão no lado marcado com "F" no lado esquerdo e "L" no lado direito. Impressão no lado não marcado com "20".
Solução oral
5 mg/5 mL, sabor de menta (240 mL) - NDC # 0456-2101-08. A solução oral não está sendo comercializada atualmente.
Armazenamento e manuseio
Armazenar a 20°C a 25°C (68°F a 77°F); excursões permitidas de 15 a 30°C (59° a 86°F).
Distribuído por: Allergan USA, Inc. Madison, NJ 07940. Revisado: setembro de 2021
EFEITOS COLATERAIS
Experiência de Ensaios Clínicos
Como os estudos clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos estudos clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos estudos clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
Fontes de dados de ensaios clínicos
Pediatria (6 -17 anos)
Os eventos adversos foram coletados em 576 pacientes pediátricos (286 Lexapro 5mg, 290 placebo) com transtorno depressivo maior em estudos duplo-cegos controlados por placebo. A segurança e eficácia de Lexapro 5mg em pacientes pediátricos com menos de 12 anos de idade não foram estabelecidas.
Adultos
Informações de eventos adversos para Lexapro 5mg foram coletadas de 715 pacientes com transtorno depressivo maior que foram expostos ao escitalopram e de 592 pacientes que foram expostos a placebo em estudos duplo-cegos, controlados por placebo. Outros 284 pacientes com transtorno depressivo maior foram recentemente expostos ao escitalopram em estudos abertos. As informações de eventos adversos para Lexapro em pacientes com TAG foram coletadas de 429 pacientes expostos ao escitalopram e de 427 pacientes expostos ao placebo em estudos duplo-cegos, controlados por placebo.
Os eventos adversos durante a exposição foram obtidos principalmente por inquérito geral e registrados por investigadores clínicos usando terminologia de sua própria escolha. Consequentemente, não é possível fornecer uma estimativa significativa da proporção de indivíduos que experimentam eventos adversos sem primeiro agrupar tipos semelhantes de eventos em um número menor de categorias padronizadas de eventos. Nas tabelas e tabulações a seguir, a terminologia padrão da Organização Mundial da Saúde (OMS) foi usada para classificar os eventos adversos relatados.
As frequências declaradas de reações adversas representam a proporção de indivíduos que experimentaram, pelo menos uma vez, um evento adverso emergente do tratamento do tipo listado. Um evento foi considerado emergente do tratamento se ocorreu pela primeira vez ou piorou durante o tratamento após a avaliação inicial.
Eventos Adversos Associados à Descontinuação do Tratamento
Transtorno Depressivo Maior
Pediatria (6 -17 anos)
Os eventos adversos foram associados à descontinuação de 3,5% dos 286 pacientes que receberam Lexapro e 1% dos 290 pacientes que receberam placebo. O evento adverso mais comum (incidência de pelo menos 1% para Lexapro 10mg e maior que placebo) associado à descontinuação foi insônia (1% Lexapro, 0% placebo).
Adultos
Entre os 715 pacientes deprimidos que receberam Lexapro em estudos controlados com placebo, 6% descontinuaram o tratamento devido a um evento adverso, em comparação com 2% dos 592 pacientes que receberam placebo. Em dois estudos de dose fixa, a taxa de descontinuação por eventos adversos em pacientes que receberam 10 mg/dia de Lexapro 20 mg não foi significativamente diferente da taxa de descontinuação por eventos adversos em pacientes que receberam placebo. A taxa de descontinuação por eventos adversos em pacientes designados para uma dose fixa de 20 mg/dia de Lexapro foi de 10%, o que foi significativamente diferente da taxa de descontinuação por eventos adversos em pacientes que receberam 10 mg/dia de Lexapro (4%) e placebo (3%). Os eventos adversos que foram associados à descontinuação de pelo menos 1% dos pacientes tratados com Lexapro 5mg, e para os quais a taxa foi pelo menos o dobro do placebo, foram náusea (2%) e distúrbio de ejaculação (2% dos pacientes do sexo masculino).
Distúrbio de ansiedade generalizada
Adultos
Entre os 429 pacientes com TAG que receberam Lexapro 10-20 mg/dia em estudos controlados com placebo, 8% descontinuaram o tratamento devido a um evento adverso, em comparação com 4% dos 427 pacientes que receberam placebo. Os eventos adversos que foram associados à descontinuação de pelo menos 1% dos pacientes tratados com Lexapro 20mg, e para os quais a taxa foi pelo menos duas vezes a taxa de placebo, foram náusea (2%), insônia (1%) e fadiga (1 %).
Incidência de Reações Adversas em Ensaios Clínicos Controlados por Placebo
Transtorno Depressivo Maior
Pediatria (6 -17 anos)
O perfil geral de reações adversas em pacientes pediátricos foi geralmente semelhante ao observado em estudos em adultos, conforme mostrado na Tabela 2. ) foram relatados em uma incidência de pelo menos 2% para Lexapro e maior que placebo: dor nas costas, infecção do trato urinário, vômitos e congestão nasal.
Adultos
As reações adversas mais comumente observadas em pacientes com Lexapro 10mg (incidência de aproximadamente 5% ou mais e aproximadamente o dobro da incidência em pacientes com placebo) foram insônia, distúrbio da ejaculação (principalmente atraso ejaculatório), náusea, aumento da sudorese, fadiga e sonolência.
A Tabela 2 enumera a incidência, arredondada para o percentual mais próximo, de eventos adversos emergentes do tratamento que ocorreram entre 715 pacientes deprimidos que receberam Lexapro 20mg em doses variando de 10 a 20 mg/dia em estudos controlados por placebo. Os eventos incluídos são aqueles que ocorrem em 2% ou mais dos pacientes tratados com Lexapro 20mg e para os quais a incidência em pacientes tratados com Lexapro 10mg foi maior do que a incidência em pacientes tratados com placebo.
TABELA 2 Reações Adversas Emergentes do Tratamento observadas com uma frequência ≥ 2% e maior que o placebo para Transtorno Depressivo Maior
Distúrbio de ansiedade generalizada
Adultos
As reações adversas mais comumente observadas em pacientes com Lexapro (incidência de aproximadamente 5% ou mais e aproximadamente duas vezes a incidência em pacientes com placebo) foram náuseas, distúrbios da ejaculação (principalmente atraso ejaculatório), insônia, fadiga, diminuição da libido e anorgasmia.
enumera a incidência, arredondada para a porcentagem mais próxima de eventos adversos emergentes do tratamento que ocorreram entre 429 pacientes com TAG que receberam Lexapro 10 a 20 mg/dia em estudos controlados por placebo. Os eventos incluídos são aqueles que ocorrem em 2% ou mais dos pacientes tratados com Lexapro e para os quais a incidência em pacientes tratados com Lexapro foi maior do que a incidência em pacientes tratados com placebo.
TABELA 3 Reações Adversas Emergentes do Tratamento observadas com uma frequência ≥ 2% e maior que o placebo para Transtorno de Ansiedade Generalizada
Dependência de Dose de Reações Adversas
dependência potencial da dose de reações adversas comuns (definidas como uma taxa de incidência de ≥5% nos grupos de 10 mg ou 20 mg de Lexapro) foi examinada com base na incidência combinada de reações adversas em dois ensaios de dose fixa. As taxas gerais de incidência de eventos adversos em pacientes tratados com 10 mg de Lexapro (66%) foram semelhantes às dos pacientes tratados com placebo (61%), enquanto a taxa de incidência em pacientes tratados com 20 mg/dia de Lexapro foi maior (86 %). A Tabela 4 mostra as reações adversas comuns que ocorreram no grupo Lexapro 20 mg/dia com uma incidência que foi aproximadamente o dobro do grupo Lexapro 10 mg/dia 10 mg/dia e aproximadamente o dobro do grupo placebo.
TABELA 4 Incidência de Reações Adversas Comuns em Pacientes com Transtorno Depressivo Maior
Disfunção sexual masculina e feminina com ISRSs
Embora as alterações no desejo sexual, desempenho sexual e satisfação sexual ocorram frequentemente como manifestações de um transtorno psiquiátrico, elas também podem ser consequência do tratamento farmacológico. Em particular, algumas evidências sugerem que os ISRSs podem causar tais experiências sexuais desagradáveis.
Estimativas confiáveis da incidência e gravidade de experiências indesejáveis envolvendo desejo sexual, desempenho e satisfação são difíceis de obter, no entanto, em parte porque pacientes e médicos podem relutar em discuti-las. Consequentemente, as estimativas da incidência de experiência sexual e desempenho indesejáveis citados na rotulagem do produto provavelmente subestimam sua incidência real.
TABELA 5 Incidência de efeitos colaterais sexuais em ensaios clínicos controlados por placebo
Não existem estudos adequadamente desenhados que examinem a disfunção sexual com o tratamento com escitalopram.
Priapismo foi relatado com todos os ISRSs.
Embora seja difícil saber o risco preciso de disfunção sexual associado ao uso de ISRSs, os médicos devem perguntar rotineiramente sobre esses possíveis efeitos colaterais.
Mudanças nos sinais vitais
Os grupos Lexapro 5mg e placebo foram comparados com relação a (1) alteração média da linha de base nos sinais vitais (pulso, pressão arterial sistólica e pressão arterial diastólica) e (2) a incidência de pacientes que atendem aos critérios para alterações potencialmente clinicamente significativas da linha de base em essas variáveis. Essas análises não revelaram alterações clinicamente importantes nos sinais vitais associados ao tratamento com Lexapro 20mg. Além disso, uma comparação das medidas dos sinais vitais em posição supina e em pé em indivíduos que receberam Lexapro 20mg indicou que o tratamento com Lexapro não está associado a alterações ortostáticas.
Alterações de peso
Os pacientes tratados com Lexapro em estudos controlados não diferiram dos pacientes tratados com placebo em relação à alteração clinicamente importante no peso corporal.
Alterações laboratoriais
Os grupos Lexapro 5mg e placebo foram comparados em relação a (1) alteração média da linha de base em várias variáveis de química sérica, hematologia e exame de urina e (2) a incidência de pacientes que atendem aos critérios para alterações potencialmente clinicamente significativas da linha de base nessas variáveis. Essas análises não revelaram alterações clinicamente importantes nos parâmetros de testes laboratoriais associados ao tratamento com Lexapro.
Alterações de ECG
Os eletrocardiogramas dos grupos Lexapro (N = 625) e placebo (N = 527) foram comparados em relação aos valores discrepantes definidos como indivíduos com alterações de QTc acima de 60 mseg da linha de base ou valores absolutos acima de 500 mseg após a dose, e indivíduos com aumento da frequência cardíaca para acima de 100 bpm ou diminui para menos de 50 bpm com uma alteração de 25% da linha de base (outliers taquicárdicos ou bradicárdicos, respectivamente). Nenhum dos pacientes do grupo Lexapro 20mg apresentou intervalo QTcF > 500 mseg ou prolongamento > 60 mseg em comparação com 0,2% dos pacientes no grupo placebo. A incidência de valores discrepantes taquicárdicos foi de 0,2% no grupo Lexapro 5mg e placebo. A incidência de valores discrepantes bradicárdicos foi de 0,5% no grupo Lexapro 10mg e 0,2% no grupo placebo.
intervalo QTcF foi avaliado em um estudo randomizado, controlado com placebo e ativo (moxifloxacina 400 mg) controlado, com escalonamento de doses múltiplas em 113 indivíduos saudáveis. A diferença média máxima (limite de confiança superior de 95%) do braço placebo foi de 4,5 (6,4) e 10,7 (12,7) ms para 10 mg e 30 mg de escitalopram supraterapêutico administrado uma vez ao dia, respectivamente. Com base na relação exposição-resposta estabelecida, a alteração prevista de QTcF do braço placebo (intervalo de confiança de 95%) abaixo da Cmax para a dose de 20 mg é de 6,6 (7,9) mseg. Escitalopram 30 mg administrado uma vez ao dia resultou em Cmax média 1,7 vezes maior do que a Cmax média para a dose terapêutica máxima recomendada no estado de equilíbrio (20 mg). A exposição sob a dose supraterapêutica de 30 mg é semelhante às concentrações de estado de equilíbrio esperadas em metabolizadores fracos de CYP2C19 após uma dose terapêutica de 20 mg.
Outras reações observadas durante a avaliação pré-comercialização do Lexapro
seguir está uma lista de eventos adversos emergentes do tratamento, conforme definido na introdução ao REAÇÕES ADVERSAS seção, relatada pelos 1.428 pacientes tratados com Lexapro por períodos de até um ano em ensaios clínicos duplo-cegos ou abertos durante sua avaliação pré-comercialização. A listagem não inclui os eventos já listados naqueles eventos para os quais a causa do medicamento foi remota e a uma taxa inferior a 1% ou menor que o placebo, os eventos que foram tão gerais que não foram informativos e os eventos relatados apenas uma vez que não tinha uma probabilidade substancial de ser uma ameaça aguda à vida. Os eventos são categorizados por sistema corporal. Eventos de grande importância clínica são descritos no AVISOS E PRECAUÇÕES seção.
Cardiovascular -hipertensão, palpitação.
Distúrbios do Sistema Nervoso Central e Periférico - sensação de tontura, enxaqueca.
Problemas gastrointestinais -cólicas abdominais, azia, gastroenterite.
Em geral - alergia, dor no peito, febre, afrontamentos, dor nos membros.
Distúrbios metabólicos e nutricionais -aumento de peso.
Distúrbios do sistema musculoesquelético - artralgia, mialgia rigidez da mandíbula.
Distúrbios psiquiátricos aumento do apetite, diminuição da concentração, irritabilidade.
Distúrbios Reprodutivos/Feminino - cólicas menstruais, distúrbios menstruais.
Distúrbios do Sistema Respiratório - bronquite, tosse, congestão nasal, congestão nasal, dor de cabeça sinusal.
Distúrbios da Pele e Apêndices - irritação na pele.
Sentidos Especiais - visão turva, zumbido.
Distúrbios do Sistema Urinário -frequência urinária, infecção do trato urinário.
Experiência pós-marketing
Reações adversas relatadas após a comercialização do Escitalopram
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de Lexapro. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Distúrbios do Sangue e do Sistema Linfático: anemia, agranulocitose, anemia aplástica, anemia hemolítica, púrpura trombocitopenia idiopática, leucopenia, trombocitopenia.
Distúrbios cardíacos: fibrilação atrial, bradicardia, insuficiência cardíaca, infarto do miocárdio, taquicardia, torsade de pointes, arritmia ventricular, taquicardia ventricular.
Distúrbios do ouvido e do labirinto: vertigem
Distúrbios Endócrinos: diabetes mellitus, hiperprolactinemia, SIADH.
Distúrbios oculares: glaucoma de ângulo fechado, diplopia, midríase, distúrbio visual.
Distúrbios gastrointestinais: disfagia, hemorragia gastrointestinal, refluxo gastroesofágico, pancreatite, hemorragia retal.
Distúrbios Gerais e Condições do Local de Administração: marcha anormal, astenia, edema, queda, sensação anormal, mal-estar.
Distúrbios hepatobiliares: hepatite fulminante, insuficiência hepática, necrose hepática, hepatite.
Distúrbios do sistema imunológico: reação alérgica, anafilaxia.
Investigações: aumento da bilirrubina, diminuição do peso, prolongamento do intervalo QT no eletrocardiograma, aumento das enzimas hepáticas, hipercolesterolemia, aumento do INR, diminuição da protrombina.
Distúrbios do Metabolismo e Nutrição: hiperglicemia, hipoglicemia, hipocalemia, hiponatremia.
Distúrbios musculoesqueléticos e do tecido conjuntivo: cãibras musculares, rigidez muscular, fraqueza muscular, rabdomiólise.
Distúrbios do sistema nervoso: acatisia, amnésia, ataxia, coreoatetose, acidente vascular cerebral, disartria, discinesia, distonia, distúrbios extrapiramidais, convulsões (ou convulsões) de grande mal, hipoestesia, mioclonia, nistagmo, parkinsonismo, pernas inquietas, convulsões, síncope, discinesia tardia, tremor.
Gravidez, Puerpério e Condições Perinatais: aborto espontâneo.
Distúrbios psiquiátricos: psicose aguda, agressão, agitação, raiva, ansiedade, apatia, suicídio consumado, confusão, despersonalização, depressão agravada, delírio, delírio, desorientação, sensação irreal, alucinações (visuais e auditivas), alterações de humor, nervosismo, pesadelo, reação de pânico, paranóia , inquietação, automutilação ou pensamentos de automutilação, tentativa de suicídio, ideação suicida, tendência suicida.
Distúrbios Renais e Urinários: insuficiência renal aguda, disúria, retenção urinária.
Distúrbios do sistema reprodutor e da mama: menorragia, priapismo.
Distúrbios respiratórios, torácicos e mediastinais: dispneia, epistaxe, embolia pulmonar, hipertensão pulmonar do recém-nascido. Distúrbios da pele e tecidos subcutâneos: alopecia, angioedema, dermatite, equimose, eritema multiforme, reação de fotossensibilidade, síndrome de Stevens Johnson, necrólise epidérmica tóxica, urticária.
Distúrbios Vasculares: trombose venosa profunda, rubor, crise hipertensiva, hipotensão, hipotensão ortostática, flebite, trombose.
INTERAÇÕES MEDICAMENTOSAS
Inibidores da Monoamino Oxidase (IMAO)
[Ver DOSAGEM E ADMINISTRAÇÃO e , CONTRA-INDICAÇÕES e AVISOS E PRECAUÇÕES ].
Drogas serotoninérgicas
[Ver DOSAGEM E ADMINISTRAÇÃO e , CONTRA-INDICAÇÕES e AVISOS E PRECAUÇÕES ].
Triptanos
Houve raros relatos pós-comercialização de síndrome serotoninérgica com o uso de um ISRS e um triptano. Se o tratamento concomitante de Lexapro 10mg com um triptano for clinicamente justificado, recomenda-se a observação cuidadosa do paciente, particularmente durante o início do tratamento e aumentos de dose [ver AVISOS E PRECAUÇÕES ].
Drogas do SNC
Dados os efeitos primários do escitalopram no SNC, deve-se ter cautela quando for administrado em combinação com outros medicamentos de ação central.
Álcool
Embora Lexapro não tenha potencializado os efeitos cognitivos e motores do álcool em um ensaio clínico, como acontece com outros medicamentos psicotrópicos, o uso de álcool por pacientes em uso de Lexapro não é recomendado.
Medicamentos que interferem na hemostasia (AINEs, aspirina, varfarina, etc.)
A liberação de serotonina pelas plaquetas desempenha um papel importante na hemostasia. Estudos epidemiológicos de desenho caso-controle e coorte que demonstraram associação entre o uso de psicofármacos que interferem na recaptação de serotonina e a ocorrência de hemorragia digestiva alta também mostraram que o uso concomitante de AINE ou aspirina pode potencializar o risco de sangramento. Efeitos anticoagulantes alterados, incluindo aumento do sangramento, foram relatados quando SSRIs e SNRIs são coadministrados com varfarina. Pacientes recebendo terapia com varfarina devem ser cuidadosamente monitorados quando Lexapro é iniciado ou descontinuado.
Cimetidina
Em indivíduos que receberam 21 dias de 40 mg/dia de citalopram racêmico, a administração combinada de 400 mg de cimetidina duas vezes ao dia por 8 dias resultou em um aumento na AUC e Cmax do citalopram de 43% e 39%, respectivamente. O significado clínico destes resultados é desconhecido.
Digoxina
Em indivíduos que receberam 21 dias de 40 mg/dia de citalopram racêmico, a administração combinada de citalopram e digoxina (dose única de 1 mg) não afetou significativamente a farmacocinética de citalopram ou digoxina.
Lítio
A coadministração de citalopram racêmico (40 mg/dia por 10 dias) e lítio (30 mmol/dia por 5 dias) não teve efeito significativo na farmacocinética de citalopram ou lítio. No entanto, os níveis plasmáticos de lítio devem ser monitorados com ajuste adequado da dose de lítio de acordo com a prática clínica padrão. Como o lítio pode aumentar os efeitos serotoninérgicos do escitalopram, deve-se ter cautela quando Lexapro 5mg e lítio são coadministrados.
Pimozida e Celexa
Em um estudo controlado, uma dose única de 2 mg de pimozida coadministrada com 40 mg de citalopram racêmico administrado uma vez ao dia por 11 dias foi associada a um aumento médio nos valores de QTc de aproximadamente 10 ms em comparação com a pimozida administrada isoladamente. O citalopram racêmico não alterou a AUC média ou Cmax da pimozida. O mecanismo desta interação farmacodinâmica não é conhecido.
Sumatriptano
Houve raros relatos pós-comercialização descrevendo pacientes com fraqueza, hiperreflexia e incoordenação após o uso de um ISRS e sumatriptano. Se o tratamento concomitante com sumatriptano e um ISRS (por exemplo, fluoxetina, fluvoxamina, paroxetina, sertralina, citalopram, escitalopram) for clinicamente justificado, aconselha-se a observação apropriada do paciente.
Teofilina
administração combinada de citalopram racêmico (40 mg/dia por 21 dias) e o substrato CYP1A2 teofilina (dose única de 300 mg) não afetou a farmacocinética da teofilina. O efeito da teofilina na farmacocinética do citalopram não foi avaliado.
Varfarina
A administração de 40 mg/dia de citalopram racêmico por 21 dias não afetou a farmacocinética da varfarina, um substrato do CYP3A4. O tempo de protrombina foi aumentado em 5%, cujo significado clínico é desconhecido.
Carbamazepina
A administração combinada de citalopram racêmico (40 mg/dia por 14 dias) e carbamazepina (titulada para 400 mg/dia por 35 dias) não afetou significativamente a farmacocinética da carbamazepina, um substrato do CYP3A4. Embora os níveis plasmáticos mínimos de citalopram não tenham sido afetados, dadas as propriedades indutoras enzimáticas da carbamazepina, a possibilidade de que a carbamazepina possa aumentar a depuração do escitalopram deve ser considerada se os dois medicamentos forem coadministrados.
Triazolam
administração combinada de citalopram racêmico (titulado para 40 mg/dia por 28 dias) e o substrato CYP3A4 triazolam (dose única de 0,25 mg) não afetou significativamente a farmacocinética de citalopram ou triazolam.
Cetoconazol
A administração combinada de citalopram racêmico (40 mg) e cetoconazol (200 mg), um potente inibidor do CYP3A4, diminuiu a Cmax e a AUC do cetoconazol em 21% e 10%, respectivamente, e não afetou significativamente a farmacocinética do citalopram.
Ritonavir
A administração combinada de uma dose única de ritonavir (600 mg), um substrato do CYP3A4 e um potente inibidor do CYP3A4, e escitalopram (20 mg) não afetou a farmacocinética de ritonavir ou escitalopram.
Inibidores de CYP3A4 e -2C19
Estudos in vitro indicaram que CYP3A4 e -2C19 são as enzimas primárias envolvidas no metabolismo do escitalopram. No entanto, a coadministração de escitalopram (20 mg) e ritonavir (600 mg), um potente inibidor do CYP3A4, não afetou significativamente a farmacocinética do escitalopram. Como o escitalopram é metabolizado por vários sistemas enzimáticos, a inibição de uma única enzima pode não diminuir consideravelmente a depuração do escitalopram.
Drogas Metabolizadas pelo Citocromo P4502D6
Os estudos in vitro não revelaram um efeito inibitório do escitalopram no CYP2D6. Além disso, os níveis de estado de equilíbrio de citalopram racêmico não foram significativamente diferentes em metabolizadores fracos e metabolizadores extensos de CYP2D6 após administração de doses múltiplas de citalopram, sugerindo que a coadministração, com escitalopram, de um medicamento que inibe CYP2D6, provavelmente não terá efeitos clinicamente significativos sobre metabolismo do escitalopram. No entanto, existem dados in vivo limitados sugerindo um efeito inibitório modesto do CYP2D6 para escitalopram, ou seja, a coadministração de escitalopram (20 mg/dia por 21 dias) com o antidepressivo tricíclico desipramina (dose única de 50 mg), um substrato para CYP2D6, resultou em um aumento de 40% na Cmax e um aumento de 100% na AUC da desipramina. O significado clínico deste achado é desconhecido. No entanto, recomenda-se cautela na coadministração de escitalopram e drogas metabolizadas pelo CYP2D6.
Metoprolol
administração de 20 mg/dia de Lexapro 20 mg por 21 dias em voluntários saudáveis resultou em um aumento de 50% na Cmax e de 82% na AUC do bloqueador beta-adrenérgico metoprolol (administrado em dose única de 100 mg). O aumento dos níveis plasmáticos de metoprolol tem sido associado à diminuição da cardiosseletividade. A coadministração de Lexapro 5mg e metoprolol não teve efeitos clinicamente significativos na pressão arterial ou na frequência cardíaca.
Eletroconvulsoterapia (ECT)
Não há estudos clínicos do uso combinado de ECT e escitalopram.
Abuso e Dependência de Drogas
Abuso e dependência
Dependência Física e Psicológica
Estudos em animais sugerem que o risco de abuso do citalopram racêmico é baixo. Lexapro 10mg não foi sistematicamente estudado em humanos por seu potencial de abuso, tolerância ou dependência física. A experiência clínica de pré-comercialização com Lexapro não revelou nenhum comportamento de busca de drogas. No entanto, essas observações não foram sistemáticas e não é possível prever com base nesta experiência limitada até que ponto uma droga ativa no SNC será mal utilizada, desviada e/ou abusada uma vez comercializada. Consequentemente, os médicos devem avaliar cuidadosamente os pacientes com Lexapro quanto ao histórico de abuso de drogas e acompanhá-los de perto, observando-os quanto a sinais de uso indevido ou abuso (por exemplo, desenvolvimento de tolerância, aumentos de dose, comportamento de busca de drogas).
AVISOS
Incluído como parte do "PRECAUÇÕES" Seção
PRECAUÇÕES
Pensamentos e Comportamentos Suicidas em Adolescentes e Jovens Adultos
Em análises agrupadas de estudos controlados por placebo de medicamentos antidepressivos (ISRSs e outras classes de antidepressivos) que incluíram aproximadamente 77.000 pacientes adultos e 4.500 pacientes pediátricos, a incidência de pensamentos e comportamentos suicidas em pacientes tratados com antidepressivos com 24 anos ou menos foi maior do que em pacientes tratados com placebo. Houve variação considerável no risco de pensamentos e comportamentos suicidas entre os medicamentos, mas houve um risco aumentado identificado em pacientes jovens para a maioria dos medicamentos estudados. Houve diferenças no risco absoluto de pensamentos e comportamentos suicidas entre as diferentes indicações, com maior incidência em pacientes com TDM. As diferenças droga-placebo no número de casos de pensamentos e comportamentos suicidas por 1.000 pacientes tratados são fornecidas em
Não se sabe se o risco de pensamentos e comportamentos suicidas em crianças, adolescentes e adultos jovens se estende ao uso a longo prazo, ou seja, além de quatro meses. No entanto, há evidências substanciais de ensaios de manutenção controlados por placebo em adultos com TDM de que os antidepressivos retardam a recorrência da depressão e que a própria depressão é um fator de risco para pensamentos e comportamentos suicidas.
Monitorar todos os pacientes tratados com antidepressivos para qualquer indicação de piora clínica e surgimento de pensamentos e comportamentos suicidas, especialmente durante os primeiros meses de terapia medicamentosa e em momentos de mudanças de dosagem. Aconselhar os familiares ou cuidadores de pacientes a monitorar mudanças de comportamento e alertar o profissional de saúde. Considere mudar o regime terapêutico, incluindo possivelmente a descontinuação de Lexapro, em pacientes cuja depressão é persistentemente pior, ou que estão experimentando pensamentos ou comportamentos suicidas emergentes.
Síndrome da serotonina
desenvolvimento de uma síndrome serotoninérgica potencialmente fatal foi relatado com SNRIs e SSRIs, incluindo Lexapro, sozinho, mas particularmente com o uso concomitante de outros medicamentos serotoninérgicos (incluindo triptanos, antidepressivos tricíclicos, fentanil, lítio, tramadol, triptofano, buspirona, anfetaminas, e Erva de São João) e com medicamentos que prejudicam o metabolismo da serotonina (em particular, IMAOs, tanto aqueles destinados a tratar distúrbios psiquiátricos quanto outros, como linezolida e azul de metileno intravenoso).
Os sintomas da síndrome serotoninérgica podem incluir alterações do estado mental (p. ex., agitação, alucinações, delírio e coma), instabilidade autonômica (p. mioclonia, hiperreflexia, incoordenação) convulsões e/ou sintomas gastrointestinais (por exemplo, náuseas, vômitos, diarreia). Os pacientes devem ser monitorados quanto ao surgimento de síndrome serotoninérgica.
uso concomitante de Lexapro 10mg com IMAOs destinados ao tratamento de distúrbios psiquiátricos é contraindicado. Lexapro 5mg também não deve ser iniciado em um paciente que esteja sendo tratado com IMAOs, como linezolida ou azul de metileno intravenoso. Todos os relatos com azul de metileno que forneceram informações sobre a via de administração envolveram administração intravenosa na faixa de dose de 1 mg/kg a 8 mg/kg. Nenhum relato envolveu a administração de azul de metileno por outras vias (como comprimidos orais ou injeção local no tecido) ou em doses mais baixas. Pode haver circunstâncias em que seja necessário iniciar o tratamento com um IMAO, como linezolida ou azul de metileno intravenoso em um paciente tomando Lexapro. Lexapro deve ser descontinuado antes de iniciar o tratamento com o IMAO [ver CONTRA-INDICAÇÕES e DOSAGEM E ADMINISTRAÇÃO ].
Se o uso concomitante de Lexapro 5mg com outros medicamentos serotoninérgicos, incluindo triptanos, antidepressivos tricíclicos, fentanil, lítio, tramadol, buspirona, triptofano, anfetamina e Erva de São João for clinicamente justificado, os pacientes devem ser informados de um risco potencial aumentado de síndrome serotoninérgica , particularmente durante o início do tratamento e aumentos de dose.
O tratamento com Lexapro e quaisquer agentes serotoninérgicos concomitantes deve ser descontinuado imediatamente se ocorrerem os eventos acima e o tratamento sintomático de suporte deve ser iniciado.
Descontinuação do tratamento com Lexapro
Durante a comercialização de Lexapro e outros SSRIs e SNRIs (inibidores da recaptação de serotonina e norepinefrina), houve relatos espontâneos de eventos adversos ocorridos após a descontinuação desses medicamentos, particularmente quando abrupta, incluindo o seguinte: humor disfórico, irritabilidade, agitação, tontura, distúrbios (por exemplo, parestesias como sensações de choque elétrico), ansiedade, confusão, dor de cabeça, letargia, labilidade emocional, insônia e hipomania. Embora esses eventos sejam geralmente autolimitados, houve relatos de sintomas graves de descontinuação.
Os pacientes devem ser monitorados quanto a esses sintomas ao descontinuar o tratamento com Lexapro. Recomenda-se uma redução gradual da dose em vez de uma interrupção abrupta sempre que possível. Se ocorrerem sintomas intoleráveis após a diminuição da dose ou após a descontinuação do tratamento, pode-se considerar a retomada da dose prescrita anteriormente. Subsequentemente, o médico pode continuar a diminuir a dose, mas a uma taxa mais gradual [ver DOSAGEM E ADMINISTRAÇÃO ].
Convulsões
Embora os efeitos anticonvulsivantes do citalopram racêmico tenham sido observados em estudos com animais, Lexapro não foi sistematicamente avaliado em pacientes com distúrbios convulsivos. Esses pacientes foram excluídos dos estudos clínicos durante os testes de pré-comercialização do produto. Em ensaios clínicos de Lexapro 5mg, casos de convulsão foram relatados em associação com o tratamento com Lexapro. Como outros medicamentos eficazes no tratamento do transtorno depressivo maior, Lexapro 20mg deve ser introduzido com cuidado em pacientes com histórico de transtorno convulsivo.
Ativação de mania ou hipomania
Em pacientes com transtorno bipolar, o tratamento de um episódio depressivo com Lexapro ou outro antidepressivo pode precipitar um episódio misto/maníaco. Em estudos controlados por placebo de Lexapro 20mg em transtorno depressivo maior, a ativação de mania/hipomania foi relatada em um (0,1%) de 715 pacientes tratados com Lexapro 20mg e em nenhum dos 592 pacientes tratados com placebo. Um caso adicional de hipomania foi relatado em associação com o tratamento com Lexapro 10mg. A ativação de mania/hipomania também foi relatada em uma pequena proporção de pacientes com transtornos afetivos maiores tratados com citalopram racêmico e outros medicamentos comercializados eficazes no tratamento do transtorno depressivo maior. Antes de iniciar o tratamento com Lexapro, rastreie os pacientes para qualquer história pessoal ou familiar de transtorno bipolar, mania ou hipomania [ver DOSAGEM E ADMINISTRAÇÃO ].
Hiponatremia
hiponatremia pode ocorrer como resultado do tratamento com ISRSs e SNRIs, incluindo Lexapro. Em muitos casos, essa hiponatremia parece ser resultado da síndrome da secreção inapropriada do hormônio antidiurético (SIADH), e foi reversível com a descontinuação de Lexapro 20mg. Casos com sódio sérico inferior a 110 mmol/L foram relatados. Pacientes idosos podem estar em maior risco de desenvolver hiponatremia com SSRIs e SNRIs. Além disso, pacientes em uso de diuréticos ou com depleção de volume podem estar em maior risco [ver Uso Geriátrico ]. A descontinuação de Lexapro deve ser considerada em pacientes com hiponatremia sintomática e intervenção médica apropriada deve ser instituída.
Sinais e sintomas de hiponatremia incluem dor de cabeça, dificuldade de concentração, comprometimento da memória, confusão, fraqueza e instabilidade, o que pode levar a quedas. Sinais e sintomas associados a casos mais graves e/ou agudos incluem alucinação, síncope, convulsão, coma, parada respiratória e morte.
Sangramento Anormal
ISRSs e SNRIs, incluindo Lexapro 20mg, podem aumentar o risco de eventos hemorrágicos. O uso concomitante de aspirina, antiinflamatórios não esteroides, varfarina e outros anticoagulantes pode aumentar o risco. Relatos de casos e estudos epidemiológicos (caso-controle e desenho de coorte) têm demonstrado associação entre o uso de drogas que interferem na recaptação de serotonina e a ocorrência de sangramento gastrointestinal. Os eventos hemorrágicos relacionados ao uso de ISRSs e IRSNs variam de equimoses, hematomas, epistaxe e petéquias a hemorragias com risco de vida.
Os pacientes devem ser alertados sobre o risco de sangramento associado ao uso concomitante de Lexapro 20mg e AINEs, aspirina ou outros medicamentos que afetem a coagulação.
Interferência com o desempenho cognitivo e motor
Em um estudo em voluntários normais, Lexapro 10 mg/dia não produziu comprometimento da função intelectual ou desempenho psicomotor. Como qualquer droga psicoativa pode prejudicar o julgamento, o pensamento ou as habilidades motoras, no entanto, os pacientes devem ser alertados sobre a operação de máquinas perigosas, incluindo automóveis, até que tenham certeza razoável de que a terapia com Lexapro não afeta sua capacidade de se envolver em tais atividades.
Glaucoma de ângulo fechado
Glaucoma de fechamento angular: A dilatação pupilar que ocorre após o uso de muitos medicamentos antidepressivos, incluindo Lexapro 20mg, pode desencadear um ataque de fechamento angular em um paciente com ângulos anatomicamente estreitos que não tenha uma iridectomia patente.
Uso em pacientes com doenças concomitantes
A experiência clínica com Lexapro em pacientes com certas doenças sistêmicas concomitantes é limitada. Recomenda-se cautela no uso de Lexapro 5mg em pacientes com doenças ou condições que produzem metabolismo alterado ou respostas hemodinâmicas.
Lexapro não foi sistematicamente avaliado em pacientes com história recente de infarto do miocárdio ou doença cardíaca instável. Os pacientes com esses diagnósticos foram geralmente excluídos dos estudos clínicos durante os testes de pré-comercialização do produto.
Em indivíduos com insuficiência hepática, a depuração do citalopram racêmico foi diminuída e as concentrações plasmáticas aumentaram. A dose recomendada de Lexapro em pacientes com insuficiência hepática é de 10 mg/dia [ver DOSAGEM E ADMINISTRAÇÃO ].
Como o escitalopram é extensamente metabolizado, a excreção do fármaco inalterado na urina é uma via de eliminação menor. Até que um número adequado de pacientes com insuficiência renal grave tenha sido avaliado durante o tratamento crônico com Lexapro 20mg, no entanto, ele deve ser usado com cautela nesses pacientes. DOSAGEM E ADMINISTRAÇÃO ].
Disfunção Sexual
O uso de ISRSs, incluindo Lexapro, pode causar sintomas de disfunção sexual [ver REAÇÕES ADVERSAS ]. Em pacientes do sexo masculino, o uso de ISRS pode resultar em atraso ou falha ejaculatória, diminuição da libido e disfunção erétil. Em pacientes do sexo feminino, o uso de ISRS pode resultar em diminuição da libido e orgasmo atrasado ou ausente.
É importante que os prescritores perguntem sobre a função sexual antes do início do Lexapro e perguntem especificamente sobre as alterações na função sexual durante o tratamento, porque a função sexual pode não ser relatada espontaneamente. Ao avaliar as alterações na função sexual, é importante obter uma história detalhada (incluindo o momento do início dos sintomas) porque os sintomas sexuais podem ter outras causas, incluindo o transtorno psiquiátrico subjacente. Discutir estratégias de gestão potenciais para apoiar os pacientes na tomada de decisões informadas sobre o tratamento.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( Guia de Medicação ).
Pensamentos e Comportamentos Suicidas
Aconselhe os pacientes, seus familiares e cuidadores a procurar o surgimento de ideação e comportamento suicida, especialmente durante o tratamento e quando a dose for ajustada para cima ou para baixo, e instrua-os a relatar esses sintomas ao seu médico [ver AVISO DE CAIXA e AVISOS E PRECAUÇÕES ].
Síndrome da serotonina
Os pacientes devem ser alertados sobre o risco de síndrome serotoninérgica com o uso concomitante de Lexapro com outros medicamentos serotoninérgicos, incluindo triptanos, antidepressivos tricíclicos, fentanil, lítio, tramadol, triptofano, buspirona, anfetaminas e erva de São João, e com medicamentos que prejudicam o metabolismo de serotonina (em particular, IMAOs, tanto aqueles destinados a tratar distúrbios psiquiátricos quanto outros, como linezolida) [ver AVISOS E PRECAUÇÕES ].
Ativação de mania ou hipomania
Aconselhe os pacientes e seus cuidadores a observar sinais de ativação de mania/hipomania e instrua-os a relatar tais sintomas ao profissional de saúde [ver AVISOS E PRECAUÇÕES ].
Sangramento Anormal
Os pacientes devem ser alertados sobre o uso concomitante de Lexapro 5mg e AINEs, aspirina, varfarina ou outros medicamentos que afetem a coagulação, uma vez que o uso combinado de psicotrópicos que interferem na recaptação de serotonina e esses agentes tem sido associado a um risco aumentado de sangramento. AVISOS E PRECAUÇÕES ].
Glaucoma de ângulo fechado
Os pacientes devem ser alertados de que tomar Lexapro 5mg pode causar dilatação pupilar leve, que em indivíduos suscetíveis, pode levar a um episódio de glaucoma de ângulo fechado. O glaucoma pré-existente é quase sempre o glaucoma de ângulo aberto porque o glaucoma de ângulo fechado, quando diagnosticado, pode ser tratado definitivamente com iridectomia. O glaucoma de ângulo aberto não é um fator de risco para o glaucoma de ângulo fechado. Os pacientes podem querer ser examinados para determinar se são suscetíveis ao fechamento do ângulo e realizar um procedimento profilático (por exemplo, iridectomia), se forem suscetíveis [ver AVISOS E PRECAUÇÕES ].
Disfunção Sexual
Aconselhe os pacientes que o uso de Lexapro pode causar sintomas de disfunção sexual em pacientes do sexo masculino e feminino. Informe os pacientes que eles devem discutir quaisquer alterações na função sexual e possíveis estratégias de manejo com seu médico [ver AVISOS E PRECAUÇÕES ].
Medicamentos Concomitantes
Como o escitalopram é o isômero ativo do citalopram racêmico (Celexa), os dois agentes não devem ser coadministrados. Os pacientes devem ser aconselhados a informar seu médico se estiverem tomando ou planejam tomar qualquer medicamento prescrito ou de venda livre, pois há potencial para interações.
Continuando a Terapia Prescrita
Embora os pacientes possam notar melhora com a terapia com Lexapro 10mg em 1 a 4 semanas, eles devem ser aconselhados a continuar a terapia conforme indicado.
Interferência com o desempenho psicomotor
Como as drogas psicoativas podem prejudicar o julgamento, o pensamento ou as habilidades motoras, os pacientes devem ser alertados sobre a operação de máquinas perigosas, incluindo automóveis, até que tenham certeza razoável de que a terapia com Lexapro não afeta sua capacidade de se envolver em tais atividades.
Álcool
Os pacientes devem ser informados de que, embora Lexapro 5mg não tenha demonstrado em experimentos com indivíduos normais aumentar as deficiências mentais e motoras causadas pelo álcool, o uso concomitante de Lexapro 20mg e álcool em pacientes deprimidos não é recomendado.
Gravidez
Aconselhe as mulheres grávidas a notificarem seus profissionais de saúde se engravidarem ou pretendem engravidar durante o tratamento com LEXAPRO. Aconselhar as pacientes que o uso de LEXAPRO 10mg mais tarde na gravidez pode levar a um risco aumentado de complicações neonatais que requerem hospitalização prolongada, suporte respiratório, alimentação por sonda e/ou hipertensão pulmonar persistente (HPPRN) do recém-nascido [ver Uso em populações específicas ].
Aconselhar as mulheres que existe um registro de exposição à gravidez que monitora os resultados da gravidez em mulheres expostas ao LEXAPRO durante a gravidez [ver Uso em populações específicas ].
Lactação
Aconselhe as mulheres que amamentam usando LEXAPRO a monitorar os bebês quanto a sedação excessiva, inquietação, agitação, má alimentação e baixo ganho de peso e a procurar atendimento médico se notarem esses sinais [ver Uso em populações específicas ].
Necessidade de Programa de Tratamento Abrangente
Lexapro 20mg é indicado como parte integrante de um programa de tratamento total para TDM que pode incluir outras medidas (psicológicas, educacionais, sociais) para pacientes com esta síndrome. O tratamento medicamentoso pode não ser indicado para todos os adolescentes com essa síndrome. A segurança e a eficácia de Lexapro 10mg em MDD não foram estabelecidas em pacientes pediátricos com menos de 12 anos de idade. Os antidepressivos não se destinam ao uso em adolescentes que apresentam sintomas secundários a fatores ambientais e/ou outros transtornos psiquiátricos primários. A colocação educacional apropriada é essencial e a intervenção psicossocial é muitas vezes útil. Quando as medidas corretivas por si só são insuficientes, a decisão de prescrever medicação antidepressiva dependerá da avaliação do médico sobre a cronicidade e gravidade dos sintomas do paciente.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Carcinogênese
Citalopram racêmico foi administrado na dieta a camundongos da linhagem NMRI/BOM e ratos da linhagem COBS WI por 18 e 24 meses, respectivamente. Não houve evidência de carcinogenicidade do citalopram racêmico em camundongos recebendo até 240 mg/kg/dia. Houve um aumento da incidência de carcinoma do intestino delgado em ratos que receberam 8 ou 24 mg/kg/dia de citalopram racêmico. Uma dose sem efeito para este achado não foi estabelecida. A relevância desses achados para humanos é desconhecida.
Mutagênese
citalopram racêmico foi mutagênico no ensaio de mutação reversa bacteriana in vitro (teste de Ames) em 2 de 5 cepas bacterianas (Salmonella TA98 e TA1537) na ausência de ativação metabólica. Foi clastogênico no ensaio in vitro de células pulmonares de hamster chinês para aberrações cromossômicas na presença e ausência de ativação metabólica. O citalopram racêmico não foi mutagênico no ensaio de mutação genética direta em mamíferos (HPRT) in vitro em células de linfoma de camundongo ou em um ensaio de síntese de DNA não programado (UDS) acoplado in vitro/in vivo em fígado de rato. Não foi clastogênico no ensaio in vitro de aberrações cromossômicas em linfócitos humanos ou em dois ensaios in vivo de micronúcleos em camundongos.
Prejuízo da Fertilidade
Quando o citalopram racêmico foi administrado oralmente a 16 ratos machos e 24 fêmeas antes e durante o acasalamento e gestação em doses de 32, 48 e 72 mg/kg/dia, o acasalamento foi reduzido em todas as doses e a fertilidade foi diminuída em doses ≥ 32 mg/kg/dia. A duração da gestação foi aumentada em 48 mg/kg/dia.
Uso em populações específicas
Gravidez
Registro de Exposição à Gravidez
Existe um registro de exposição à gravidez que monitora os resultados da gravidez em mulheres expostas a antidepressivos durante a gravidez. Os profissionais de saúde são incentivados a registrar pacientes ligando para o National Pregnancy Registry for Antidepressants em 1-844-405-6185 ou visitando on-line em https://womensmentalhealth.org/clnical-and-research-programs/pregnancyregistry/antidepressants/
Resumo do risco
Os dados disponíveis de estudos epidemiológicos publicados e relatórios pós-comercialização não estabeleceram um risco aumentado de defeitos congênitos maiores ou aborto espontâneo. Existem riscos de hipertensão pulmonar persistente do recém-nascido (HPPRN) (ver Dados ) e má adaptação neonatal (ver Considerações Clínicas ) com exposição a inibidores seletivos de recaptação de serotonina (ISRSs), incluindo LEXAPRO 5mg, durante a gravidez. Existem riscos associados à depressão não tratada na gravidez (ver Considerações Clínicas ).
Em estudos de reprodução em animais, tanto o escitalopram quanto o citalopram racêmico demonstraram ter efeitos adversos no desenvolvimento embrio/fetal e pós-natal, incluindo anormalidades estruturais fetais, quando administrados em doses superiores às doses terapêuticas humanas (ver Dados ).
O risco de fundo estimado de defeitos congênitos graves e aborto espontâneo para a população indicada é desconhecido. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e aborto nas gestações clinicamente reconhecidas é de 2 a 4% e 15 a 20%, respectivamente.
Considerações Clínicas
Risco materno associado à doença e/ou risco embrio/fetal
As mulheres que descontinuam os antidepressivos são mais propensas a ter uma recaída de depressão maior do que as mulheres que continuam os antidepressivos. Esse achado é de um estudo longitudinal prospectivo com 201 gestantes com histórico de depressão maior, eutímicas e em uso de antidepressivos no início da gravidez. Considere o risco de depressão não tratada ao interromper ou alterar o tratamento com medicação antidepressiva durante a gravidez e pós-parto.
Reações adversas fetais/neonatais
Recém-nascidos expostos a SSRIs ou SNRIs, incluindo Lexapro 5mg, no final do terceiro trimestre desenvolveram complicações que requerem hospitalização prolongada, suporte respiratório e alimentação por sonda. Tais complicações podem surgir imediatamente após o parto. Os achados clínicos relatados incluíram desconforto respiratório, cianose, apnéia, convulsões, instabilidade de temperatura, dificuldade de alimentação, vômitos, hipoglicemia, hipotonia, hipertonia, hiperreflexia, tremor, nervosismo, irritabilidade e choro constante. Essas características são consistentes com um efeito tóxico direto de SSRIs e SNRIs ou, possivelmente, uma síndrome de descontinuação da droga. Deve-se notar que, em alguns casos, o quadro clínico é compatível com síndrome serotoninérgica [ver AVISOS E PRECAUÇÕES ].
Dados
Dados humanos
A exposição a ISRSs, particularmente mais tarde na gravidez, pode aumentar o risco de HPPN. A HPPN ocorre em 1-2 por 1.000 nascidos vivos na população geral e está associada a uma substancial morbidade e mortalidade neonatal.
Dados de animais
Em um estudo de desenvolvimento embrionário/fetal em ratos, a administração oral de escitalopram (56, 112 ou 150 mg/kg/dia) a animais prenhes durante o período de organogênese resultou em diminuição do peso corporal fetal e atrasos associados na ossificação nas duas doses mais altas [aproximadamente ≥ 55 vezes a dose humana máxima recomendada (MRHD) de 20 mg/dia com base em mg/m2]. A toxicidade materna (sinais clínicos e diminuição do ganho de peso corporal e consumo alimentar), leve a 56 mg/kg/dia, estava presente em todos os níveis de dose. A dose sem efeito de desenvolvimento de 56 mg/kg/dia é aproximadamente 27 vezes a MRHD de 20 mg com base em mg/m2. Não foram observadas malformações em nenhuma das doses testadas (até 73 vezes o MRHD em uma base de mg/m2).
Quando ratas foram tratadas com escitalopram (6, 12, 24 ou 48 mg/kg/dia) durante a gravidez e durante o desmame, observou-se um ligeiro aumento da mortalidade da prole e retardo do crescimento em 48 mg/kg/dia, que é aproximadamente 23 vezes o MRHD de 20 mg na base de mg/m2. Foi observada uma ligeira toxicidade materna (sinais clínicos e diminuição do ganho de peso corporal e consumo alimentar) com esta dose. A mortalidade da prole ligeiramente aumentada também foi observada com 24 mg/kg/dia. A dose sem efeito foi de 12 mg/kg/dia que é aproximadamente 6 vezes a MRHD de 20 mg numa base de mg/m2.
Em dois estudos de desenvolvimento embrio/fetal em ratos, a administração oral de citalopram racêmico (32, 56 ou 112 mg/kg/dia) a animais prenhes durante o período de organogênese resultou em diminuição do crescimento e sobrevivência embrionário/fetal e aumento da incidência de anormalidades (incluindo defeitos cardiovasculares e esqueléticos) na dose alta, que é aproximadamente 18 vezes a MRHD de 60 mg/dia com base em mg/m2. Esta dose também foi associada à toxicidade materna (sinais clínicos, diminuição do ganho de peso corporal). A dose de desenvolvimento sem efeito foi de 56 mg/kg/dia é aproximadamente 9 vezes a MRHD em uma base de mg/m2. Em um estudo em coelhos, não foram observados efeitos adversos no desenvolvimento embrionário/fetal com doses de citalopram racêmico de até 16 mg/kg/dia, ou aproximadamente 5 vezes a MRHD em uma base de mg/m2. Assim, os efeitos no desenvolvimento do citalopram racêmico foram observados em uma dose materna tóxica no rato e não foram observados no coelho.
Quando as ratas foram tratadas com citalopram racêmico (4,8, 12,8 ou 32 mg/kg/dia) desde o final da gestação até o desmame, observou-se aumento da mortalidade da prole durante os primeiros 4 dias após o nascimento e retardo persistente do crescimento da prole na dose mais alta, que é aproximadamente 5 vezes a MRHD de 60 mg numa base de mg/m2. A dose sem efeito foi de 12,8 mg/kg/dia é aproximadamente 2 vezes a MRHD em uma base de mg/m2. Efeitos semelhantes na mortalidade e crescimento da prole foram observados quando as mães foram tratadas durante a gestação e início da lactação em doses ≥ 24 mg/kg/dia, aproximadamente 4 vezes a MRHD em uma base de mg/m2. Uma dose sem efeito não foi determinada nesse estudo.
Lactação
Resumo do risco
Dados da literatura publicada relatam a presença de escitalopram e desmetilescitalopram no leite humano (ver Dados ). Há relatos de sedação excessiva, inquietação, agitação, má alimentação e baixo ganho de peso em lactentes expostos ao escitalopram, através do leite materno (ver Considerações Clínicas ),. Não há dados sobre os efeitos do escitalopram ou de seus metabólitos na produção de leite. Os benefícios da amamentação para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de LEXAPRO 5mg e quaisquer potenciais efeitos adversos na criança amamentada por LEXAPRO ou pela condição materna subjacente.
Considerações Clínicas
Lactentes expostos a LEXAPRO 20mg devem ser monitorados quanto a sedação excessiva, inquietação, agitação, má alimentação e baixo ganho de peso.
Dados
Um estudo com 8 nutrizes em uso de escitalopram com doses diárias de 10-20 mg/dia mostrou que bebês amamentados exclusivamente recebem aproximadamente 3,9% da dose de escitalopram ajustada ao peso materno e 1,7% da dose ajustada ao peso materno de desmetilcitalopram .
Uso Pediátrico
A segurança e eficácia de Lexapro 10mg foram estabelecidas em adolescentes (12 a 17 anos de idade) para o tratamento de transtorno depressivo maior [ver Estudos clínicos ]. Embora a eficácia de manutenção em pacientes adolescentes com transtorno depressivo maior não tenha sido sistematicamente avaliada, a eficácia de manutenção pode ser extrapolada de dados de adultos juntamente com comparações de parâmetros farmacocinéticos de escitalopram em pacientes adultos e adolescentes.
A segurança e eficácia de Lexapro não foram estabelecidas em pacientes pediátricos (com menos de 12 anos de idade) com transtorno depressivo maior. Em um estudo de segurança aberto de 24 semanas em 118 crianças (de 7 a 11 anos) com transtorno depressivo maior, os achados de segurança foram consistentes com o perfil de segurança e tolerabilidade conhecido para Lexapro.
A segurança e a eficácia de Lexapro não foram estabelecidas em pacientes pediátricos com menos de 18 anos de idade com Transtorno de Ansiedade Generalizada.
diminuição do apetite e a perda de peso foram observadas em associação com o uso de ISRSs. Consequentemente, o monitoramento regular do peso e do crescimento deve ser realizado em crianças e adolescentes tratados com um ISRS como o Lexapro.
Uso Geriátrico
Aproximadamente 6% dos 1.144 pacientes que receberam escitalopram em estudos controlados de Lexapro 10mg em transtorno depressivo maior e TAG tinham 60 anos de idade ou mais; pacientes idosos nestes estudos receberam doses diárias de Lexapro entre 10 e 20 mg. O número de pacientes idosos nesses estudos foi insuficiente para avaliar adequadamente possíveis medidas de eficácia e segurança diferenciais com base na idade. No entanto, não se pode descartar maior sensibilidade de alguns idosos aos efeitos do Lexapro.
ISRSs e SNRIs, incluindo Lexapro 5mg, foram associados a casos de hiponatremia clinicamente significativa em pacientes idosos, que podem estar em maior risco para esse evento adverso [ver Hiponatremia ].
Em dois estudos farmacocinéticos, a meia-vida do escitalopram foi aumentada em aproximadamente 50% em indivíduos idosos em comparação com indivíduos jovens e a Cmax permaneceu inalterada. FARMACOLOGIA CLÍNICA ]. 10 mg/dia é a dose recomendada para pacientes idosos [ver DOSAGEM E ADMINISTRAÇÃO ].
Dos 4.422 pacientes em estudos clínicos de citalopram racêmico, 1.357 tinham 60 anos ou mais, 1.034 tinham 65 anos ou mais e 457 tinham 75 anos ou mais. Não foram observadas diferenças gerais na segurança ou eficácia entre esses indivíduos e indivíduos mais jovens, e outras experiências clínicas relatadas não identificaram diferenças nas respostas entre pacientes idosos e pacientes mais jovens, mas, novamente, uma maior sensibilidade de alguns indivíduos idosos não pode ser descartada.
SOBREDOSAGEM
O seguinte foi relatado com superdosagem de comprimidos de Lexapro:
- Convulsões, que podem ser retardadas, e estado mental alterado, incluindo coma.
- Toxicidade cardiovascular, que pode ser retardada, incluindo prolongamento do intervalo QRS e QTc, taquiarritmias de complexo largo e torsade de pointes. A hipertensão é mais comumente observada, mas raramente pode ocorrer hipotensão isoladamente ou com co-ingestantes, incluindo álcool.
- Síndrome serotoninérgica (pacientes com superdosagem de múltiplos medicamentos com outros medicamentos proserotonérgicos podem ter um risco maior).
O monitoramento cardíaco prolongado é recomendado em ingestões de superdosagem de Lexapro devido ao risco de arritmia.
A descontaminação gastrointestinal com carvão ativado deve ser considerada em pacientes que se apresentam precocemente após uma superdosagem de Lexapro.
Considere entrar em contato com um centro de intoxicação (1-800-221-2222) ou um toxicologista médico para recomendações de gerenciamento de superdosagem.
CONTRA-INDICAÇÕES
Inibidores da Monoamino Oxidase (IMAO)
O uso de IMAOs destinados a tratar distúrbios psiquiátricos com Lexapro ou dentro de 14 dias após a interrupção do tratamento com Lexapro 5mg é contraindicado devido a um risco aumentado de síndrome serotoninérgica. O uso de Lexapro 20mg dentro de 14 dias após a interrupção de um IMAO destinado a tratar distúrbios psiquiátricos também é contraindicado [ver DOSAGEM E ADMINISTRAÇÃO , e AVISOS E PRECAUÇÕES ].
Iniciar Lexapro 20mg em um paciente que está sendo tratado com IMAOs, como linezolida ou azul de metileno intravenoso, também é contraindicado devido ao risco aumentado de síndrome serotoninérgica [ver DOSAGEM E ADMINISTRAÇÃO , e AVISOS E PRECAUÇÕES ].
Pimozida
O uso concomitante em pacientes em uso de pimozida é contraindicado [ver INTERAÇÕES MEDICAMENTOSAS ].
Hipersensibilidade ao Escitalopram ou Citalopram
Lexapro 20mg é contraindicado em pacientes com hipersensibilidade ao escitalopram ou citalopram ou a qualquer um dos ingredientes inativos do Lexapro.
FARMACOLOGIA CLÍNICA
Mecanismo de ação
Presume-se que o mecanismo de ação antidepressiva do escitalopram, o enantiômero S do citalopram racêmico, esteja ligado à potencialização da atividade serotoninérgica no sistema nervoso central (SNC) resultante de sua inibição da recaptação neuronal de serotonina (5-HT) no SNC.
Farmacodinâmica
Estudos in vitro e in vivo em animais sugerem que o escitalopram é um inibidor altamente seletivo da recaptação de serotonina (ISRS) com efeitos mínimos na recaptação neuronal de norepinefrina e dopamina. O escitalopram é pelo menos 100 vezes mais potente que o enantiômero R em relação à inibição da recaptação de 5-HT e inibição da taxa de disparo neuronal de 5-HT. A tolerância a um modelo de efeito antidepressivo em ratos não foi induzida pelo tratamento a longo prazo (até 5 semanas) com escitalopram. Escitalopram tem nenhuma ou muito baixa afinidade para serotoninérgicos (5-HT1-7) ou outros receptores, incluindo alfa e beta-adrenérgico, dopamina (D1-5), histamina (H1-3), muscarínico (M1-5) e benzodiazepina receptores. O escitalopram também não se liga ou tem baixa afinidade para vários canais iônicos, incluindo canais de Na+, K+, Cl- e Ca++. O antagonismo de receptores muscarínicos, histaminérgicos e adrenérgicos tem sido associado a vários efeitos colaterais anticolinérgicos, sedativos e cardiovasculares de outras drogas psicotrópicas.
Farmacocinética
farmacocinética de dose única e múltipla de escitalopram é linear e proporcional à dose em uma faixa de dose de 10 a 30 mg/dia. A biotransformação do escitalopram é principalmente hepática, com meia-vida terminal média de cerca de 27-32 horas. Com a administração de uma vez ao dia, as concentrações plasmáticas no estado de equilíbrio são alcançadas em aproximadamente uma semana. No estado de equilíbrio, a extensão do acúmulo de escitalopram no plasma em indivíduos jovens e saudáveis foi 2,2-2,5 vezes as concentrações plasmáticas observadas após uma dose única. As formas farmacêuticas em comprimido e solução oral de oxalato de escitalopram são bioequivalentes.
Absorção e Distribuição
Após uma dose oral única (comprimido ou solução de 20 mg) de escitalopram, os níveis sanguíneos de pico ocorrem em cerca de 5 horas. A absorção de escitalopram não é afetada pelos alimentos.
A biodisponibilidade absoluta do citalopram é de cerca de 80% em relação a uma dose intravenosa, e o volume de distribuição do citalopram é de cerca de 12 L/kg. Dados específicos sobre escitalopram não estão disponíveis.
ligação do escitalopram às proteínas plasmáticas humanas é de aproximadamente 56%.
Metabolismo e eliminação
Após administrações orais de escitalopram, a fração da droga recuperada na urina como escitalopram e S-desmetilcitalopram (S-DCT) é de cerca de 8% e 10%, respectivamente. A depuração oral do escitalopram é de 600 mL/min, sendo aproximadamente 7% devido à depuração renal.
escitalopram é metabolizado em S-DCT e S-didemetilcitalopram (S-DDCT). Em humanos, o escitalopram inalterado é o composto predominante no plasma. No estado de equilíbrio, a concentração do metabólito S-DCT de escitalopram no plasma é aproximadamente um terço da concentração de escitalopram. O nível de S-DDCT não foi detectável na maioria dos indivíduos. Estudos in vitro mostram que o escitalopram é pelo menos 7 e 27 vezes mais potente que S-DCT e S-DDCT, respectivamente, na inibição da recaptação de serotonina, sugerindo que os metabólitos do escitalopram não contribuem significativamente para as ações antidepressivas do escitalopram. S-DCT e SDDCT também têm nenhuma ou muito baixa afinidade para serotoninérgicos (5-HT1-7) ou outros receptores, incluindo alfa e beta-adrenérgico, dopamina (D1-5), histamina (H1-3), muscarínico (M1- 5) e receptores de benzodiazepina. S-DCT e S-DDCT também não se ligam a vários canais iônicos, incluindo canais de Na+, K+, Cl- e Ca++.
Estudos in vitro utilizando microssomas hepáticos humanos indicaram que CYP3A4 e CYP2C19 são as isoenzimas primárias envolvidas na N-desmetilação do escitalopram.
Subgrupos de população
Era
Adolescentes
Em um estudo de dose única de 10 mg de escitalopram, a AUC de escitalopram diminuiu 19% e a Cmax aumentou 26% em adolescentes saudáveis (12 a 17 anos de idade) em comparação com adultos. Após doses múltiplas de 40 mg/dia de citalopram, a meia-vida de eliminação do escitalopram, a Cmax no estado de equilíbrio e a AUC foram semelhantes em pacientes com TDM (12 a 17 anos de idade) em comparação com pacientes adultos. Não é necessário ajuste de dose em pacientes adolescentes.
Idoso
A farmacocinética do escitalopram em indivíduos ≥ 65 anos de idade foi comparada com indivíduos mais jovens em um estudo de dose única e de dose múltipla. A AUC e a meia-vida do escitalopram aumentaram aproximadamente 50% em indivíduos idosos, e a Cmax permaneceu inalterada. 10 mg é a dose recomendada para pacientes idosos [ver DOSAGEM E ADMINISTRAÇÃO ].
Gênero
Com base em dados de estudos de dose única e múltipla medindo escitalopram em idosos, adultos jovens e adolescentes, nenhum ajuste de dose com base no sexo é necessário.
Função hepática reduzida
A depuração oral do citalopram foi reduzida em 37% e a meia-vida foi dobrada em pacientes com função hepática reduzida em comparação com indivíduos normais. 10 mg é a dose recomendada de escitalopram para a maioria dos pacientes com insuficiência hepática [ver DOSAGEM E ADMINISTRAÇÃO ].
Função Renal Reduzida
Em pacientes com insuficiência renal leve a moderada, a depuração oral do citalopram foi reduzida em 17% em comparação com indivíduos normais. Nenhum ajuste de dose para tais pacientes é recomendado. Não há informações disponíveis sobre a farmacocinética do escitalopram em pacientes com função renal gravemente reduzida (clearance de creatinina
Interações Medicamentosas
Os dados de inibição enzimática in vitro não revelaram um efeito inibitório do escitalopram no CYP3A4, -1A2, -2C9, -2C19 e -2E1. Com base em dados in vitro, espera-se que o escitalopram tenha pouco efeito inibitório no metabolismo in vivo mediado por esses citocromos. Embora os dados in vivo para abordar esta questão sejam limitados, os resultados dos estudos de interação medicamentosa sugerem que o escitalopram, na dose de 20 mg, não tem efeito inibitório de 3A4 e um efeito inibitório modesto de 2D6. Ver INTERAÇÕES MEDICAMENTOSAS para obter informações mais detalhadas sobre os dados de interação medicamentosa disponíveis.
Toxicologia e/ou Farmacologia Animal
Alterações da retina em ratos
Alterações patológicas (degeneração/atrofia) foram observadas nas retinas de ratos albinos no estudo de carcinogenicidade de 2 anos com citalopram racêmico. Houve um aumento na incidência e gravidade da patologia da retina em ratos machos e fêmeas que receberam 80 mg/kg/dia. Achados semelhantes não estavam presentes em ratos que receberam 24 mg/kg/dia de citalopram racêmico por dois anos, em camundongos que receberam até 240 mg/kg/dia de citalopram racêmico por 18 meses ou em cães que receberam até 20 mg/kg/dia. dia de citalopram racêmico por um ano.
Estudos adicionais para investigar o mecanismo desta patologia não foram realizados, e o potencial significado deste efeito em humanos não foi estabelecido.
Alterações cardiovasculares em cães
Em um estudo de toxicologia de um ano, 5 de 10 cães beagle recebendo doses orais de citalopram racêmico de 8 mg/kg/dia morreram subitamente entre as semanas 17 e 31 após o início do tratamento. Não foram observadas mortes súbitas em ratos com doses de citalopram racêmico de até 120 mg/kg/dia, que produziram níveis plasmáticos de citalopram e seus metabólitos demetilcitalopram e didemetilcitalopram (DDCT) semelhantes aos observados em cães com 8 mg/kg/dia. Um estudo de dosagem intravenosa subsequente demonstrou que em cães beagle, a DDCT racêmica causou prolongamento do intervalo QT, um fator de risco conhecido para o desfecho observado em cães.
Estudos clínicos
Transtorno Depressivo Maior
Adolescentes
eficácia de Lexapro como tratamento agudo para transtorno depressivo maior em pacientes adolescentes foi estabelecida em um estudo de 8 semanas, com dose flexível, controlado por placebo que comparou Lexapro 10-20 mg/dia com placebo em pacientes ambulatoriais de 12 a 17 anos de idade inclusive quem preenchia os critérios do DSM-IV para transtorno depressivo maior. O desfecho primário foi a mudança da linha de base para o desfecho na Escala de Avaliação de Depressão Infantil - Revisada (CDRS-R). Neste estudo, Lexapro 5mg mostrou melhora média estatisticamente significativa maior em comparação com placebo no CDRS-R.
eficácia de Lexapro no tratamento agudo de transtorno depressivo maior em adolescentes foi estabelecida, em parte, com base na extrapolação do estudo de 8 semanas, dose flexível, controlado por placebo com citalopram racêmico 20-40 mg/dia. Neste estudo ambulatorial em crianças e adolescentes de 7 a 17 anos de idade que preencheram os critérios do DSM-IV para transtorno depressivo maior, o tratamento com citalopram mostrou melhora média maior estatisticamente significativa desde o início, em comparação com placebo, no CDRS-R; os resultados positivos para este estudo vieram em grande parte do subgrupo de adolescentes.
Dois estudos adicionais de MDD com dose flexível e controlados por placebo (um estudo Lexapro em pacientes de 7 a 17 anos e um estudo com citalopram em adolescentes) não demonstraram eficácia.
Embora a eficácia de manutenção em pacientes adolescentes não tenha sido sistematicamente avaliada, a eficácia de manutenção pode ser extrapolada de dados de adultos juntamente com comparações de parâmetros farmacocinéticos de escitalopram em pacientes adultos e adolescentes.
Adultos
eficácia de Lexapro 5mg como tratamento para transtorno depressivo maior foi estabelecida em três estudos de 8 semanas, controlados por placebo, realizados em pacientes ambulatoriais entre 18 e 65 anos de idade que preenchiam os critérios do DSM-IV para transtorno depressivo maior. O desfecho primário em todos os três estudos foi a mudança da linha de base para o desfecho na Escala de Avaliação de Depressão de Montgomery Asberg (MADRS).
Um estudo de dose fixa comparou 10 mg/dia de Lexapro e 20 mg/dia de Lexapro com placebo e 40 mg/dia de citalopram. Os grupos de tratamento de 10 mg/dia e 20 mg/dia de Lexapro 5mg apresentaram melhora média estatisticamente significativa maior em comparação com placebo no MADRS. Os grupos de 10 mg e 20 mg de Lexapro foram semelhantes nesta medida de resultado.
Em um segundo estudo de dose fixa de 10 mg/dia de Lexapro e placebo, o grupo de tratamento com 10 mg/dia de Lexapro apresentou melhora média estatisticamente significativa maior em comparação ao placebo no MADRS.
Em um estudo de dose flexível, comparando Lexapro 20mg, titulado entre 10 e 20 mg/dia, com placebo e citalopram, titulado entre 20 e 40 mg/dia, o grupo de tratamento com Lexapro 5mg apresentou melhora média estatisticamente significativa maior em comparação ao placebo no MADR.
As análises da relação entre o resultado do tratamento e idade, sexo e raça não sugeriram nenhuma resposta diferencial com base nessas características dos pacientes.
Em um estudo de longo prazo, 274 pacientes que preencheram os critérios (DSM-IV) para transtorno depressivo maior, que responderam durante uma fase inicial de tratamento aberto de 8 semanas com Lexapro 10 ou 20 mg/dia, foram randomizados para a continuação do Lexapro na mesma dose, ou placebo, por até 36 semanas de observação para recaída. A resposta durante a fase de rótulo aberto foi definida por uma diminuição da pontuação total MADRS para ≤ 12. A recaída durante a fase duplo-cega foi definida como um aumento da pontuação total MADRS para ≥ 22 ou descontinuação devido a resposta clínica insuficiente . Os pacientes que receberam Lexapro contínuo experimentaram um tempo estatisticamente significativo mais longo para recaída em comparação com aqueles que receberam placebo.
Distúrbio de ansiedade generalizada
eficácia de Lexapro 5mg no tratamento agudo do Transtorno de Ansiedade Generalizada (TAG) foi demonstrada em três estudos de 8 semanas, multicêntricos, de dose flexível, controlados por placebo que compararam Lexapro 10-20 mg/dia com placebo em pacientes ambulatoriais adultos entre 18 e 80 anos de idade que preencheram os critérios do DSM-IV para TAG. Em todos os três estudos, Lexapro mostrou melhora média estatisticamente significativa maior em comparação com placebo na Escala de Ansiedade de Hamilton (HAM-A).
Havia muito poucos pacientes em diferentes grupos étnicos e etários para avaliar adequadamente se Lexapro tem ou não efeitos diferenciais nesses grupos. Não houve diferença na resposta ao Lexapro entre homens e mulheres.
INFORMAÇÃO DO PACIENTE
Lexapro® (leks-a-pro) (escitalopram) Comprimidos/Solução Oral
Leia o Guia de Medicação que acompanha o Lexapro antes de começar a tomá-lo e sempre que receber um reabastecimento. Pode haver novas informações. Este Guia de Medicação não substitui a conversa com seu médico sobre sua condição médica ou tratamento. Converse com seu médico se houver algo que você não entenda ou queira saber mais.
Qual é a informação mais importante que devo saber sobre Lexapro 20mg?
Lexapro 10mg e outros medicamentos antidepressivos podem causar efeitos colaterais graves, incluindo:
Mantenha todas as visitas de acompanhamento com seu médico e ligue entre as visitas se estiver preocupado com os sintomas.
Ligue para o seu médico imediatamente se tiver algum dos seguintes sintomas ou ligue para o 911 em caso de emergência, especialmente se eles forem novos, piores ou se preocuparem:
Ligue para o seu médico imediatamente se tiver algum dos seguintes sintomas ou ligue para o 911 em caso de emergência. Lexapro pode estar associado a estes efeitos colaterais graves:
Os sintomas nos homens podem incluir:
Os sintomas em mulheres podem incluir:
Fale com o seu médico se desenvolver quaisquer alterações na sua função sexual ou se tiver dúvidas ou preocupações sobre problemas sexuais durante o tratamento com Lexapro. Pode haver tratamentos que seu médico pode sugerir.
- Lexapro 5mg e outros medicamentos antidepressivos podem aumentar pensamentos ou ações suicidas em algumas crianças, adolescentes ou adultos jovens dentro da primeiros meses de tratamento ou quando a dose é alterada.
- Depressão ou outras doenças mentais graves são as causas mais importantes de pensamentos ou ações suicidas.
- Fique atento a essas mudanças e ligue para o seu médico imediatamente se notar:
- Mudanças novas ou repentinas no humor, comportamento, ações, pensamentos ou sentimentos, especialmente se forem graves.
- Preste atenção especial a essas alterações quando Lexapro 5mg for iniciado ou quando a dose for alterada.
- tentativas de suicídio
- agindo em impulsos perigosos
- agindo de forma agressiva ou violenta
- pensamentos sobre suicídio ou morte
- depressão nova ou pior
- ansiedade nova ou pior ou ataques de pânico
- sentindo-se agitado, inquieto, irritado ou irritado
- problemas para dormir
- um aumento na atividade ou falar mais do que o normal para você
- outras mudanças incomuns no comportamento ou humor
- agitação, alucinações, coma ou outras alterações no estado mental
- problemas de coordenação ou espasmos musculares (reflexos hiperativos)
- batimentos cardíacos acelerados, pressão arterial alta ou baixa
- sudorese ou febre
- náuseas, vômitos ou diarreia
- rigidez muscular
- Problemas respiratórios
- inchaço da face, língua, olhos ou boca
- erupção cutânea, vergões com comichão (urticária) ou bolhas, sozinho ou com febre ou dor nas articulações
- energia levemente aumentada
- problemas graves para dormir
- pensamentos descontrolados
- comportamento imprudente
- ideias extraordinariamente grandes
- felicidade excessiva ou irritabilidade
- falando mais ou mais rápido do que o habitual
- dor de cabeça
- fraqueza ou sensação instável
- confusão, problemas de concentração ou pensamento ou problemas de memória
Apenas algumas pessoas estão em risco para esses problemas. Você pode querer se submeter a um exame oftalmológico para ver se está em risco e receber tratamento preventivo, se estiver.
- dor nos olhos
- mudanças na visão
- inchaço ou vermelhidão dentro ou ao redor do olho
- Ejaculação retardada ou incapacidade de ter uma ejaculação
- Diminuição do desejo sexual
- Problemas para obter ou manter uma ereção
- Diminuição do desejo sexual
- Orgasmo retardado ou incapacidade de ter um orgasmo
Não interrompa o Lexapro sem primeiro falar com seu médico. Parar Lexapro 5mg muito rapidamente pode causar sintomas graves, incluindo:
- ansiedade, irritabilidade, humor alto ou baixo, sensação de inquietação ou mudanças nos hábitos de sono
- dor de cabeça, sudorese, náusea, tontura
- sensações de choque elétrico, tremores, confusão
O que é Lexapro?
Lexapro 20mg é um medicamento de prescrição usado para tratar a depressão. É importante conversar com seu médico sobre os riscos de tratar a depressão e também os riscos de não tratá-la. Você deve discutir todas as opções de tratamento com seu médico. Lexapro também é usado para tratar:
- Transtorno Depressivo Maior (TDM)
- Transtorno de Ansiedade Generalizada (TAG)
Converse com seu médico se achar que sua condição não está melhorando com o tratamento com Lexapro.
Quem não deve tomar Lexapro 5mg?
Não tome Lexapro 10mg se você:
As pessoas que tomam Lexapro 20mg perto do tempo de um IMAO podem ter efeitos colaterais graves ou até mesmo fatais. Obtenha ajuda médica imediatamente se tiver algum destes sintomas:
- são alérgicos ao escitalopram ou citalopram ou a qualquer um dos ingredientes do Lexapro. Consulte o final deste Guia de Medicação para obter uma lista completa dos ingredientes do Lexapro.
- Tome um inibidor da monoamina oxidase (IMAO). Pergunte ao seu médico ou farmacêutico se não tiver certeza se está tomando um IMAO, incluindo linezolida.
- Não tome um IMAO dentro de 2 semanas após a interrupção do Lexapro 10mg, a menos que seja orientado pelo seu médico
- Não inicie Lexapro 20mg se você parou de tomar um IMAO nas últimas 2 semanas, a menos que seja orientado pelo seu médico.
- febre alta
- espasmos musculares descontrolados
- músculos fortes
- mudanças rápidas na frequência cardíaca ou pressão arterial
- confusão
- perda de consciência (desmaiar)
- Não tome Lexapro com Orap® (pimozida) porque tomar esses dois medicamentos juntos pode causar sérios problemas cardíacos.
O que devo dizer ao meu médico antes de tomar Lexapro 20mg? Pergunte se não tiver certeza.
Antes de iniciar Lexapro 20mg, informe o seu médico se você:
- Está tomando certos medicamentos, como:
- Triptanos usados para tratar a enxaqueca
- Medicamentos usados para tratar distúrbios do humor, ansiedade, psicóticos ou do pensamento, incluindo tricíclicos, lítio, ISRSs, ISRNs, anfetaminas ou antipsicóticos
- Tramadol
- Suplementos de venda livre, como triptofano ou erva de São João
- tem problemas de fígado
- tem problemas renais
- tem problemas cardíacos
- tem ou teve convulsões ou convulsões
- tem transtorno bipolar ou mania
- tem baixos níveis de sódio no sangue
- tem uma história de um acidente vascular cerebral
- tem pressão alta
- tem ou teve problemas de sangramento
- estão grávidas ou planejam engravidar. Tomar LEXAPRO no final da gravidez pode aumentar o risco de certos problemas no recém-nascido. Converse com seu médico sobre os benefícios e riscos do tratamento da depressão durante a gravidez
- Se você engravidar enquanto estiver tomando LEXAPRO, converse com seu médico sobre o registro no Registro Nacional de Gravidez para Antidepressivos. Você pode se inscrever ligando para 1-844-405-6185 ou acesse https://womensmentalhealth.org/clinicaland- researchprograms/gravidezregistry/antidepressants/
- está amamentando ou planeja amamentar. Lexapro pode passar para o leite materno. Converse com seu médico sobre a melhor maneira de alimentar seu bebê se estiver tomando Lexapro.
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos e não prescritos, vitaminas e suplementos de ervas. Lexapro 10mg e alguns medicamentos podem interagir uns com os outros, podem não funcionar tão bem ou podem causar efeitos colaterais graves.
O seu médico ou farmacêutico pode dizer-lhe se é seguro tomar Lexapro 20mg com outros medicamentos. Não inicie ou interrompa qualquer medicamento enquanto estiver tomando Lexapro 10mg sem falar primeiro com seu médico.
Se você toma Lexapro, não deve tomar outros medicamentos que contenham escitalopram ou citalopram, incluindo: Celexa.
Como devo tomar Lexapro?
- Tome Lexapro exatamente como prescrito. Seu médico pode precisar alterar a dose de Lexapro até que seja a dose certa para você.
- Lexapro 5mg pode ser tomado com ou sem alimentos.
- Se você esquecer de uma dose de Lexapro, tome a dose esquecida assim que se lembrar. Se estiver quase na hora da próxima dose, pule a dose esquecida e tome a próxima dose no horário regular. Não tome duas doses de Lexapro ao mesmo tempo.
- Se você tomar muito Lexapro, ligue para seu médico ou centro de controle de envenenamento imediatamente ou obtenha tratamento de emergência.
O que devo evitar ao tomar Lexapro?
Lexapro 5mg pode causar sonolência ou afetar sua capacidade de tomar decisões, pensar com clareza ou reagir rapidamente. Você não deve dirigir, operar máquinas pesadas ou realizar outras atividades perigosas até saber como o Lexapro o afeta. Não beba álcool enquanto estiver usando Lexapro.
Quais são os possíveis efeitos colaterais do Lexapro 20mg?
Lexapro 10mg pode causar efeitos colaterais graves, incluindo todos daqueles descritos na seção intitulada “Qual é a informação mais importante que eu deveria saber sobre Lexapro?”
Os possíveis efeitos colaterais comuns em pessoas que tomam Lexapro 5mg incluem:
- Náusea
- Sonolência
- Fraqueza
- Tontura
- Sentindo-se ansioso
- Problemas para dormir
- Problemas sexuais
- Sudorese
- Tremendo
- Não sentindo fome
- Boca seca
- Constipação
- Infecção
- bocejo
Outros efeitos colaterais em crianças e adolescentes incluem:
- aumento da sede
- aumento anormal no movimento muscular ou agitação
- sangramento nasal
- micção difícil
- períodos menstruais pesados
- possível taxa de crescimento mais lenta e mudança de peso. A altura e o peso do seu filho devem ser monitorados durante o tratamento com Lexapro.
Informe o seu médico se tiver algum efeito colateral que o incomode ou que não desapareça. Estes não são todos os possíveis efeitos colaterais do Lexapro. Para mais informações, pergunte ao seu médico ou farmacêutico.
LIGUE PARA O SEU MÉDICO PARA ACONSELHAMENTO MÉDICO SOBRE EFEITOS COLATERAIS. VOCÊ PODE DENUNCIAR EFEITOS COLATERAIS AO FDA EM 1-800-FDA-1088.
Como devo armazenar Lexapro 20mg?
- Armazene Lexapro de 68°F a 77°F (20°C a 25°C); excursões permitidas de 59°F a 86°F (15°C a 30°C).
- Mantenha o frasco de Lexapro bem fechado.
Mantenha Lexapro 10mg e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre Lexapro
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use Lexapro para uma condição para a qual não foi prescrito. Não dê Lexapro 10mg a outras pessoas, mesmo que tenham a mesma condição. Pode prejudicá-los.
Este Guia de Medicação resume as informações mais importantes sobre Lexapro. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre Lexapro que foram escritas para profissionais de saúde.
Para mais informações sobre Lexapro 20mg ligue 1-800-678-1605 ou acesse www.Lexapro.com.
Quais são os ingredientes de Lexapro 20mg?
Princípio ativo: oxalato de escitalopram Ingredientes inativos:
- talco, croscarmelose sódica, celulose microcristalina/dióxido de silício coloidal e estearato de magnésio. O revestimento de filme contém hipromelose, dióxido de titânio e polietilenoglicol.
- Solução oral: sorbitol, água purificada, ácido cítrico, citrato de sódio, ácido málico, glicerina, propilenoglicol, metilparabeno, propilparabeno e aroma natural de menta (a solução oral não está sendo comercializada atualmente).
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
