Parlodel 2.5mg Bromocriptine Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Parlodel e como é usado?
Parlodel 2,5 mg é um medicamento de prescrição usado para tratar os sintomas de Disfunções Associadas à Hiperprolactinemia, Doença de Parkinson, Acromegalia. Parlodel 2,5mg pode ser usado sozinho ou com outros medicamentos.
Parlodel 2,5mg pertence a uma classe de medicamentos chamados Agentes Antiparkinsonianos, Agonistas da Dopamina; Hiperprolactinemia; Metabólico e Endócrino, Outros.
Não se sabe se Parlodel 2,5 mg é seguro e eficaz em crianças com menos de 10 anos de idade.
Quais são os possíveis efeitos colaterais do Parlodel?
Parlodel pode causar efeitos colaterais graves, incluindo:
- urticária,
- dificuldade para respirar,
- inchaço do rosto, lábios, língua ou garganta,
- problemas de visão,
- nariz escorrendo constante,
- dor no peito,
- dor ao respirar,
- ritmo cardíaco acelerado,
- respiração rápida,
- falta de ar,
- dor nas costas,
- inchaço nos tornozelos ou pés,
- urinar menos ou nada,
- confusão,
- alucinações,
- tontura,
- dor de cabeça,
- fome,
- fraqueza,
- sudorese,
- tremores,
- irritabilidade,
- dificuldade de concentração,
- movimentos musculares involuntários,
- perda de equilíbrio ou coordenação,
- fezes com sangue ou alcatrão,
- tossindo sangue,
- vômito que parece borra de café,
- dor de cabeça severa,
- visão embaçada,
- zumbindo em seus ouvidos,
- ansiedade,
- confusão,
- dor no peito,
- falta de ar,
- batimentos cardíacos irregulares e
- convulsões
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Parlodel 2,5mg incluem:
- tontura,
- sensação de giro,
- sonolência leve,
- cansaço,
- dor de cabeça leve,
- humor deprimido,
- problemas de sono (insônia),
- boca seca,
- nariz entupido,
- dor de estômago,
- náusea,
- vômito,
- dor de estômago,
- perda de apetite,
- diarréia,
- constipação, e
- sensação de frio ou dormência nos dedos
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Parlodel. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
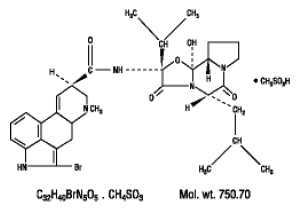
Parlodel® (mesilato de bromocriptina) é um derivado do ergot com potente atividade agonista do receptor de dopamina. Cada comprimido SnapTabs® de Parlodel® (mesilato de bromocriptina) para administração oral contém 2½ mg e cada cápsula contém 5 mg de bromocriptina (como o mesilato). O mesilato de bromocriptina é quimicamente designado como Ergotaman-3',6',18-triona, 2-bromo-12'-hidroxi-2'-(1-metiletil)-5'-( 2-metilpropil)-, (5'α)-monometanossulfonato (sal).
A fórmula estrutural é:
2½ mg SnapTabs®
Ingrediente ativo: mesilato de bromocriptina, USP
Ingredientes inativos: dióxido de silício coloidal, lactose, estearato de magnésio, povidona, amido e outro ingrediente
Cápsulas de 5 mg
Ingrediente ativo: mesilato de bromocriptina, USP
Ingredientes inativos: dióxido de silício coloidal, gelatina, lactose, estearato de magnésio, óxido de ferro vermelho, dióxido de silício, lauril sulfato de sódio, amido, dióxido de titânio, óxido de ferro amarelo e outro ingrediente
INDICAÇÕES
Disfunções Associadas à Hiperprolactinemia
Parlodel (mesilato de bromocriptina) é indicado para o tratamento de disfunções associadas a hiperprolactinemia Incluindo amenorreia com ou sem galactorreia, infertilidade ou hipogonadismo . O tratamento com Parlodel 2,5mg é indicado em pacientes com adenomas secretores de prolactina , que pode ser a endocrinopatia subjacente básica que contribui para as apresentações clínicas acima. Redução dentro tamanho do tumor foi demonstrado em pacientes do sexo masculino e feminino com macroadenomas. Nos casos em que a adenectomia é escolhida, um curso de terapia com Parlodel 2,5 mg pode ser usado para reduzir a massa tumoral antes da cirurgia.
Acromegalia
A terapia com Parlodel 2,5mg é indicada no tratamento da acromegalia. A terapia com Parlodel, isoladamente ou como terapia adjuvante com irradiação hipofisária ou cirurgia, reduz o hormônio de crescimento sérico em 50% ou mais em aproximadamente ½ dos pacientes tratados, embora geralmente não atinja níveis normais.
Uma vez que os efeitos da radiação hipofisária externa podem não se tornar máximos por vários anos, a terapia adjuvante com Parlodel 2,5 mg oferece benefício potencial antes que os efeitos da irradiação se manifestem.
Mal de Parkinson
Parlodel 2,5mg SnapTabs ou cápsulas são indicados no tratamento dos sinais e sintomas da doença de Parkinson idiopática ou pós-encefalítica. Como tratamento adjuvante à levodopa (isolada ou com um inibidor periférico da descarboxilase), a terapia com Parlodel pode fornecer benefícios terapêuticos adicionais naqueles pacientes que atualmente são mantidos em doses ideais de levodopa, aqueles que estão começando a se deteriorar (desenvolvem tolerância) à terapia com levodopa e aqueles que estão experimentando “falha de fim de dose” na terapia com levodopa. A terapia com Parlodel 2,5 mg pode permitir uma redução da dose de manutenção de levodopa e, assim, pode melhorar a ocorrência e/ou gravidade de reações adversas associadas à terapia de longo prazo com levodopa, como movimentos involuntários anormais (por exemplo, discinesias) e as oscilações acentuadas no função motora (fenômeno “on-off”). A eficácia continuada da terapia com Parlodel 2,5 mg durante o tratamento de mais de 2 anos não foi estabelecida.
Os dados são insuficientes para avaliar o benefício potencial do tratamento da doença de Parkinson recém-diagnosticada com Parlodel. Os estudos mostraram, no entanto, significativamente mais reações adversas (principalmente náuseas, alucinações, confusão e hipotensão) em pacientes tratados com Parlodel do que em pacientes tratados com levodopa/carbidopa. Os pacientes que não respondem à levodopa são maus candidatos à terapia com Parlodel.
DOSAGEM E ADMINISTRAÇÃO
Em geral
Recomenda-se que Parlodel (mesilato de bromocriptina) seja tomado com alimentos. Os pacientes devem ser avaliados frequentemente durante o escalonamento da dose para determinar a dosagem mais baixa que produz uma resposta terapêutica.
Indicações hiperprolactinêmicas
A dosagem inicial de Parlodel SnapTabs em adultos é de um comprimido de ½ a um comprimido de 2½ mg por dia. Um comprimido adicional de 2 ½ mg pode ser adicionado ao regime de tratamento conforme tolerado a cada 2 a 7 dias até que uma resposta terapêutica ideal seja alcançada. A dosagem terapêutica variou de 2,5-15 mg por dia em adultos estudados clinicamente.
Com base em dados limitados em crianças de 11 a 15 anos (ver Uso Pediátrico ) a dose inicial é de um comprimido de ½ a um comprimido de 2½ mg por dia. A dosagem pode precisar ser aumentada conforme tolerado até que uma resposta terapêutica seja alcançada. A dosagem terapêutica variou de 2,5-10 mg por dia em crianças com adenomas hipofisários secretores de prolactina.
A fim de reduzir a probabilidade de exposição prolongada a Parlodel caso ocorra uma gravidez insuspeita, um contraceptivo mecânico deve ser usado em conjunto com a terapia com Parlodel 2,5 mg até que os ciclos menstruais ovulatórios normais sejam restaurados. A contracepção pode então ser descontinuada em pacientes que desejam engravidar.
Depois disso, se a menstruação não ocorrer dentro de 3 dias da data prevista, a terapia com Parlodel 2,5 mg deve ser descontinuada e um teste de gravidez realizado.
Acromegalia
Praticamente todos os pacientes acromegálicos que recebem benefício terapêutico de Parlodel 2,5 mg também apresentam reduções nos níveis circulantes de hormônio do crescimento. Portanto, a avaliação periódica dos níveis circulantes do hormônio do crescimento servirá, na maioria dos casos, como guia para determinar o potencial terapêutico de Parlodel. Se, após uma breve tentativa com a terapia com Parlodel, não ocorrer redução significativa nos níveis de hormônio do crescimento, deve ser feita uma avaliação cuidadosa das características clínicas da doença e, se não ocorrer nenhuma alteração, deve-se considerar o ajuste da dose ou a descontinuação da terapia. .
dosagem inicial recomendada é de um comprimido de ½ a um comprimido de Parlodel SnapTabs de 2½ mg ao deitar (com alimentos) por 3 dias. Um comprimido adicional de ½ a 1 SnapTabs deve ser adicionado ao regime de tratamento conforme tolerado a cada 3 a 7 dias até que o paciente obtenha o benefício terapêutico ideal. Os pacientes devem ser reavaliados mensalmente e a dose ajustada com base nas reduções do hormônio do crescimento ou na resposta clínica. A faixa de dosagem terapêutica ideal usual de Parlodel varia de 20-30mg/dia na maioria dos pacientes. A dose máxima não deve exceder 100 mg/dia.
Os pacientes tratados com irradiação hipofisária devem ser retirados da terapia com Parlodel 2,5 mg anualmente para avaliar os efeitos clínicos da radiação no processo da doença, bem como os efeitos da terapia com Parlodel. Normalmente, um período de retirada de 4 a 8 semanas é adequado para esse fim. A recorrência dos sinais/sintomas ou aumentos da hormona do crescimento indicam que o processo da doença ainda está ativo e devem ser considerados novos ciclos de Parlodel.
Mal de Parkinson
princípio básico da terapia com Parlodel 2,5mg é iniciar o tratamento com uma dose baixa e, individualmente, aumentar a dose diária lentamente até que uma resposta terapêutica máxima seja alcançada. A dosagem de levodopa durante este período introdutório deve ser mantida, se possível. A dose inicial de Parlodel 2,5 mg é ½ comprimido de SnapTabs de 2 ½ mg duas vezes ao dia com as refeições. As avaliações são aconselhadas em intervalos de 2 semanas durante a titulação da dose para garantir que a dose mais baixa que produz uma resposta terapêutica ideal não seja excedida. Se necessário, a dose pode ser aumentada a cada 14 a 28 dias em 2½ mg/dia com as refeições. Caso seja aconselhável reduzir a dose de levodopa devido a reações adversas, a dose diária de Parlodel, se aumentada, deve ser realizada gradualmente em pequenos incrementos (2½ mg).
A segurança de Parlodel não foi demonstrada em dosagens superiores a 100 mg/dia.
COMO FORNECIDO
Parlodel (Mesilato de Bromocriptina) SnapTabs
2½mg
Parlodel está disponível em frasco contendo 30 e 100 comprimidos de 2 ½ mg, cada frasco contém um dessecante.
SnapTabs redondos, esbranquiçados, de borda chanfrada, cada um contendo 2½ mg de bromocriptina (como o mesilato). Gravado “PARLODEL 2½” de um lado e “017” do lado marcado. Está em conformidade com o teste de dissolução USP 1.
Pacotes de 30 - NDC 30698-202-30 Pacotes de 100 - NDC 30698-202-01
Cápsulas Parlodel (Mesilato de Bromocriptina)
5 mg
Cápsulas de caramelo e brancas, cada uma contendo 5 mg de bromocriptina (como o mesilato). Impresso em tinta vermelha “PARLODEL 5 mg” em uma metade e “102” na outra metade.
Pacotes de 30 - NDC 30698-201-30 Pacotes de 100 - NDC 30698-201-01
Armazenar e Dispensar
Armazenar a 68° a 77°F (20° a 25°C); excursões permitidas para 59° a 86°F (15° a 30°C) [Consulte USP Controlled Room Temperature].
Dispensar em um recipiente apertado e resistente à luz.
Fabricado para e distribuído por: Validus Pharmaceuticals LLC Parsippany, NJ 07054. Revisado: julho de 2021
EFEITOS COLATERAIS
Reações Adversas de Ensaios Clínicos
Indicações hiperprolactinêmicas
A incidência de efeitos adversos é bastante alta (69%), mas estes são geralmente de grau leve a moderado. A terapia foi descontinuada em aproximadamente 5% dos pacientes devido a efeitos adversos. Estes em ordem decrescente de frequência são: náusea (49%), dor de cabeça (19%), tontura (17%), fadiga (7%), tontura (5%), vômito (5%), cólicas abdominais (4%) , congestão nasal (3%), constipação (3%), diarreia (3%) e sonolência (3%).
Um leve efeito hipotensor pode acompanhar o tratamento com Parlodel (mesilato de bromocriptina). A ocorrência de reações adversas pode ser diminuída reduzindo temporariamente a dosagem para ½ comprimido SnapTabs 2 ou 3 vezes ao dia. Alguns casos de rinorréia no líquido cefalorraquidiano foram relatados em pacientes recebendo Parlodel 2,5 mg para tratamento de grandes prolactinomas. Isso ocorreu raramente, geralmente apenas em pacientes que receberam cirurgia transesfenoidal prévia, radiação hipofisária ou ambos, e que estavam recebendo Parlodel 2,5mg para recorrência do tumor. Também pode ocorrer em pacientes não tratados previamente, cujo tumor se estende até o seio esfenoidal.
Acromegalia
As reações adversas mais frequentes encontradas em pacientes acromegálicos tratados com Parlodel 2,5mg foram: náusea (18%), constipação (14%), hipotensão postural/ortostática (6%), anorexia (4%), boca seca/congestão nasal (4 %), indigestão/dispepsia (4%), vasoespasmo digital (3%), sonolência/cansaço (3%) e vômitos (2%).
As reações adversas menos frequentes (menos de 2%) foram: hemorragia gastrointestinal, tonturas, exacerbação da síndrome de Raynaud, cefaleias e síncope. Raramente (menos de 1%) perda de cabelo, potenciação do álcool, desmaio, tontura, arritmia, taquicardia ventricular, diminuição da necessidade de sono, alucinações visuais, lassidão, falta de ar, bradicardia, vertigem, parestesia, lentidão, ataque vasovagal, psicose delirante, paranóia , insônia, cabeça pesada, tolerância reduzida ao frio, formigamento das orelhas, palidez facial e cãibras musculares foram relatados.
Mal de Parkinson
Em ensaios clínicos nos quais Parlodel 2,5 mg foi administrado com redução concomitante da dose de levodopa/carbidopa, as reações adversas mais comuns que apareceram recentemente foram: náusea, movimentos involuntários anormais, alucinações, confusão, fenômeno “on-off”, tontura, sonolência, desmaio/desmaio, vômitos, astenia, desconforto abdominal, distúrbios visuais, ataxia, insônia, depressão, hipotensão, falta de ar, constipação e vertigem.
As reações adversas menos comuns que podem ser encontradas incluem: anorexia, ansiedade, blefaroespasmo, boca seca, disfagia, edema dos pés e tornozelos, eritromelalgia, convulsão epileptiforme, fadiga, dor de cabeça, letargia, manchas na pele, congestão nasal, nervosismo, pesadelos, parestesia, erupção cutânea, frequência urinária, incontinência urinária, retenção urinária e, raramente, sinais e sintomas de ergotismo, como formigamento nos dedos, pés frios, dormência, cãibras musculares nos pés e pernas ou exacerbação da síndrome de Raynaud.
Anormalidades nos exames laboratoriais podem incluir elevações do nitrogênio ureico no sangue, SGOT, SGPT, GGPT, CPK, fosfatase alcalina e ácido úrico, que geralmente são transitórios e sem significado clínico.
Reações adversas da experiência pós-marketing
As seguintes reações adversas foram relatadas durante o uso pós-aprovação de Parlodel (todas as indicações combinadas). Como as reações adversas de notificações espontâneas são relatadas voluntariamente por uma população de tamanho incerto, geralmente não é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Distúrbios psiquiátricos: Confusão, agitação/excitação psicomotora, alucinações, distúrbios psicóticos, insônia, aumento da libido, hipersexualidade e controle de impulsos/comportamentos compulsivos (incluindo jogos de azar, gastos e outros impulsos intensos).
Distúrbios do sistema nervoso: Dor de cabeça, sonolência, tontura, discinesia, sonolência, parestesia, sonolência diurna excessiva, início súbito de sono.
Distúrbios oculares: Perturbação visual, visão turva.
Distúrbios do ouvido e do labirinto: Zumbido.
Distúrbios cardíacos: Derrame pericárdico, pericardite constritiva, taquicardia, bradicardia, arritmia, fibrose da válvula cardíaca.
Distúrbios vasculares: Hipotensão, hipotensão ortostática (muito raramente levando a síncope), palidez reversível dos dedos das mãos e dos pés induzida pelo frio (especialmente em pacientes com história de fenômeno de Raynaud).
Distúrbios respiratórios, torácicos e mediastinais: Congestão nasal, derrame pleural, fibrose pleural, pleurisia, fibrose pulmonar, dispneia.
Problemas gastrointestinais: Náuseas, constipação, vômitos, boca seca, diarréia, dor abdominal, fibrose retroperitoneal, úlcera gastrointestinal, hemorragia gastrointestinal.
Distúrbios da pele e tecidos subcutâneos: Reações alérgicas na pele, queda de cabelo.
Distúrbios musculoesqueléticos e do tecido conjuntivo: Cãibras nas pernas.
Distúrbios gerais e condições do local de administração: Fadiga, edema periférico, uma síndrome semelhante à Síndrome Neuroléptica Maligna na retirada abrupta de Parlodel, sintomas de abstinência (incluindo apatia, ansiedade, depressão, fadiga, insônia, sudorese e dor) com redução gradual ou após a descontinuação (ver PRECAUÇÕES ).
Eventos Adversos Observados em Outras Condições
Pacientes pós-parto (ver acima AVISOS )
Em estudos pós-parto com Parlodel 2,5 mg, 23 por cento das pacientes pós-parto tratadas tiveram pelo menos 1 efeito colateral, mas eles foram geralmente de grau leve a moderado. A terapia foi descontinuada em aproximadamente 3% dos pacientes. As reações adversas mais frequentes foram: cefaleia (10%), tontura (8%), náusea (7%), vômito (3%), fadiga (1,0%), síncope (0,7%), diarreia (0,4%) e cãibras (0,4%). Diminuições na pressão arterial (≥ 20 mm Hg sistólica e ≥ 10 mm Hg diastólica) ocorreram em 28% das pacientes pelo menos uma vez durante os primeiros 3 dias pós-parto; estes eram geralmente de natureza transitória. Relatos de desmaios no puerpério possivelmente podem estar relacionados a esse efeito. Na experiência pós-comercialização nos EUA, as reações adversas graves relatadas incluem 72 casos de convulsões (incluindo 4 casos de estado de mal epiléptico), 30 casos de acidente vascular cerebral e 9 casos de infarto do miocárdio em pacientes pós-parto. Os casos de convulsão não foram necessariamente acompanhados pelo desenvolvimento de hipertensão. Uma cefaleia persistente e muitas vezes progressivamente intensa, às vezes acompanhada de distúrbios visuais, muitas vezes precedida por horas a dias, muitos casos de convulsão e/ou acidente vascular cerebral. A maioria dos pacientes não mostrou evidência de qualquer um dos distúrbios hipertensivos da gravidez, incluindo eclâmpsia, pré-eclâmpsia ou hipertensão induzida pela gravidez. Um caso de acidente vascular cerebral foi associado à trombose do seio sagital e outro foi associado à vasculite cerebral e cerebelar. Um caso de infarto do miocárdio foi associado à coagulação intravascular disseminada inexplicada e um segundo ocorreu em conjunto com o uso de outro alcalóide do ergot. A relação destas reações adversas com a administração de Parlodel não foi estabelecida.
Em casos raros, eventos adversos graves, incluindo hipertensão, infarto do miocárdio, convulsões, acidente vascular cerebral ou distúrbios psíquicos foram relatados em mulheres no pós-parto tratadas com Parlodel. Em alguns pacientes, o desenvolvimento de convulsões ou acidente vascular cerebral foi precedido por fortes dores de cabeça e/ou distúrbios visuais transitórios. Embora a relação causal desses eventos com o medicamento seja incerta, o monitoramento periódico da pressão arterial é aconselhável em mulheres no pós-parto recebendo Parlodel. Se houver hipertensão, cefaleia grave, progressiva ou contínua (com ou sem distúrbios visuais) ou evidência de toxicidade no SNC, a administração de Parlodel 2,5 mg deve ser descontinuada e o paciente deve ser avaliado imediatamente.
É necessário cuidado especial em pacientes que foram recentemente tratados ou estão em terapia concomitante com medicamentos que podem alterar a pressão arterial, por exemplo, vasoconstritores, como simpaticomiméticos ou alcalóides do ergot, incluindo ergometrina ou metilergometrina, e seu uso concomitante no puerpério não é recomendado.
Para relatar REAÇÕES ADVERSAS SUSPEITAS, entre em contato com a Validus Pharmaceuticals LLC em 1-866-982-5438 ou FDA em 1-800-FDA-1088 ou www.fda.gov/medwatch.
INTERAÇÕES MEDICAMENTOSAS
risco de usar Parlodel em combinação com outros medicamentos não foi sistematicamente avaliado, mas o álcool pode potencializar os efeitos colaterais de Parlodel. Parlodel 2,5 mg pode interagir com antagonistas da dopamina, butirofenonas e alguns outros agentes. Os compostos nessas categorias resultam em uma eficácia diminuída de Parlodel: fenotiazinas, haloperidol, metoclopramida e pimozida. A bromocriptina é um substrato do CYP3A4. Portanto, deve-se ter cautela ao co-administrar medicamentos que são fortes inibidores desta enzima (como antimicóticos azólicos, inibidores da protease do HIV). O uso concomitante de antibióticos macrolídeos, como a eritromicina, mostrou aumentar os níveis plasmáticos de bromocriptina (os valores médios de AUC e Cmax aumentaram 3,7 vezes e 4,6 vezes, respectivamente). níveis de bromocriptina (a AUC da bromocriptina aumentou cerca de 38%).4 Não é recomendado o uso concomitante de Parlodel com outros alcalóides da cravagem do centeio. O ajuste de dose pode ser necessário nos casos em que altas doses de bromocriptina estão sendo usadas (como indicação de doença de Parkinson).
AVISOS
Como a hiperprolactinemia com amenorreia/galactorreia e infertilidade foi encontrada em pacientes com tumores hipofisários, uma avaliação completa da hipófise é indicada antes do tratamento com Parlodel (mesilato de bromocriptina).
Se ocorrer gravidez durante a administração de Parlodel, é obrigatória a observação cuidadosa dessas pacientes. Adenomas secretores de prolactina podem se expandir e pode ocorrer compressão do nervo óptico ou de outros nervos cranianos, tornando-se necessária a cirurgia de emergência da hipófise. Na maioria dos casos, a compactação é resolvida após a entrega. Foi relatado que o reinício do tratamento com Parlodel 2,5 mg produz melhora nos campos visuais de pacientes em que ocorreu compressão do nervo durante a gravidez. A segurança do tratamento com Parlodel 2,5 mg durante a gravidez para a mãe e o feto não foi estabelecida.
Parlodel 2,5 mg foi associado a sonolência e episódios de início súbito de sono, particularmente em pacientes com doença de Parkinson. Foi relatado início súbito de sono durante as atividades diárias, em alguns casos sem consciência ou sinais de alerta. Os pacientes devem ser informados sobre isso e aconselhados a não dirigir ou operar máquinas durante o tratamento com bromocriptina. Pacientes que sofreram sonolência e/ou um episódio de início súbito de sono não devem dirigir ou operar máquinas. Além disso, uma redução da dosagem ou interrupção da terapia pode ser considerada.
Hipotensão sintomática pode ocorrer em pacientes tratados com Parlodel para qualquer indicação. Em estudos pós-parto com Parlodel, foram observadas diminuições nas pressões sistólica e diastólica supina de mais de 20 mm e 10 mm Hg, respectivamente, em quase 30% das pacientes que receberam Parlodel. Na ocasião, a queda na pressão sistólica supina foi de até 50-59 mm de Hg.
Uma vez que, especialmente durante os primeiros dias de tratamento, reações hipotensivas podem ocorrer ocasionalmente e resultar em redução do estado de alerta, deve-se ter cuidado especial ao dirigir veículos ou operar máquinas.
Embora hipotensão durante o início da terapia com Parlodel 2,5 mg ocorra em alguns pacientes, em casos raros, eventos adversos graves, incluindo hipertensão, infarto do miocárdio, convulsões, acidente vascular cerebral, foram relatados em mulheres no pós-parto tratadas com Parlodel 2,5 mg para a inibição da lactação. Hipertensão tem sido relatada, algumas vezes no início da terapia, mas frequentemente se desenvolvendo na segunda semana de terapia; convulsões também foram relatadas com e sem o desenvolvimento prévio de hipertensão; AVC foram relatados principalmente em pacientes pós-parto cujos cursos pré-natais e obstétricos não foram complicados. Muitos desses pacientes que sofreram convulsões (incluindo casos de estado de mal epiléptico) e/ou derrame relataram desenvolver uma dor de cabeça constante e muitas vezes progressivamente intensa horas a dias antes do evento agudo. Alguns casos de derrames e convulsões também foram precedidos por distúrbios visuais (visão turva e cegueira cortical transitória). Casos de infarto agudo do miocárdio também foram relatados.
Embora não tenha sido estabelecida uma relação causal entre a administração de Parlodel e hipertensão, convulsões, acidente vascular cerebral e infarto do miocárdio em mulheres no pós-parto, o uso do medicamento para prevenção da lactação fisiológica ou em pacientes com hipertensão não controlada não é recomendado. Em pacientes em tratamento para hiperprolactinemia, Parlodel 2,5 mg deve ser descontinuado quando a gravidez for diagnosticada (ver PRECAUÇÕES , Estados hiperprolactinêmicos ). Caso Parlodel 2,5mg seja reinstituído para controlar um macroadenoma em rápida expansão (ver PRECAUÇÕES , Estados hiperprolactinêmicos e uma paciente apresenta um distúrbio hipertensivo da gravidez, o benefício de continuar Parlodel deve ser ponderado em relação ao possível risco de seu uso durante um distúrbio hipertensivo da gravidez. Quando Parlodel está sendo usado para tratar acromegalia ou doença de Parkinson em pacientes que engravidaram posteriormente, deve-se decidir se a terapia continua a ser clinicamente necessária ou pode ser retirada. Se for continuado, o medicamento deve ser descontinuado em pacientes que possam apresentar distúrbios hipertensivos da gravidez (incluindo eclâmpsia, pré-eclâmpsia ou hipertensão induzida pela gravidez), a menos que a retirada de Parlodel seja considerada clinicamente contraindicada. Devido à possibilidade de interação entre Parlodel e outros alcalóides do ergot, o uso concomitante desses medicamentos não é recomendado. A monitorização periódica da pressão arterial, particularmente durante as primeiras semanas de terapia, é prudente. Se houver hipertensão, cefaleia grave, progressiva ou contínua (com ou sem distúrbio visual) ou evidência de toxicidade do SNC, a terapia medicamentosa deve ser descontinuada e o paciente deve ser avaliado imediatamente. Atenção especial deve ser dada aos pacientes que foram tratados recentemente ou estão em terapia concomitante com medicamentos que podem alterar a pressão arterial. Seu uso concomitante no puerpério não é recomendado.
Entre os pacientes em tratamento com Parlodel, particularmente em tratamento prolongado e em altas doses, foram relatados derrames pleurais e pericárdicos, bem como fibrose pleural e pulmonar e pericardite constritiva. Pacientes com distúrbios pleuropulmonares inexplicáveis devem ser examinados minuciosamente e a descontinuação da terapia com Parlodel 2,5 mg deve ser considerada. Nos casos em que o tratamento com Parlodel 2,5 mg foi interrompido, as alterações voltaram lentamente ao normal.
Em alguns pacientes em tratamento com Parlodel, particularmente em tratamento prolongado e em altas doses, foi relatada fibrose retroperitoneal. Para garantir o reconhecimento da fibrose retroperitoneal em estágio inicial reversível, recomenda-se que suas manifestações (por exemplo, dor nas costas, edema de membros inferiores, função renal prejudicada) sejam observadas nessa categoria de pacientes. A medicação Parlodel deve ser retirada se houver diagnóstico ou suspeita de alterações fibróticas no retroperitônio.
PRECAUÇÕES
Em geral
Houve relatos de pacientes que experimentaram desejos intensos de jogar, desejos sexuais aumentados, desejos intensos de gastar dinheiro incontrolavelmente e/ou outros desejos intensos e a incapacidade de controlar esses desejos enquanto tomavam um ou mais medicamentos, incluindo Parlodel 2,5 mg , que aumentam o tônus dopaminérgico central. Em alguns casos, embora não em todos, esses impulsos cessaram quando a dose foi reduzida ou a medicação foi descontinuada. Como os pacientes podem não reconhecer esses comportamentos como anormais, é importante que os prescritores perguntem especificamente aos pacientes ou seus cuidadores sobre o desenvolvimento de novos ou maiores impulsos para jogar, impulsos sexuais, gastos descontrolados ou outros impulsos durante o tratamento com Parlodel 2,5mg para a doença de Parkinson ou disfunções associadas à hiperprolactinemia. Os médicos devem considerar a redução da dose ou a interrupção da medicação se um paciente desenvolver tais desejos enquanto estiver tomando Parlodel.
segurança e eficácia de Parlodel (mesilato de bromocriptina) não foram estabelecidas em pacientes com doença renal ou hepática. Deve-se ter cuidado ao administrar a terapia com Parlodel concomitantemente com outros medicamentos conhecidos por reduzir a pressão arterial.
O medicamento deve ser usado com cautela em pacientes com histórico de psicose ou doença cardiovascular. Se pacientes acromegálicas ou pacientes com prolactinoma ou doença de Parkinson estiverem sendo tratadas com Parlodel 2,5 mg durante a gravidez, elas devem ser observadas com cautela, principalmente durante o período pós-parto se tiverem histórico de doença cardiovascular.
Pacientes com problemas hereditários raros de intolerância à galactose, deficiência grave de lactase ou má absorção de glicose-galactose não devem tomar este medicamento.
Estados hiperprolactinêmicos
comprometimento do campo visual é uma complicação conhecida do macroprolactinoma. O tratamento eficaz com Parlodel 2,5 mg leva a uma redução da hiperprolactinemia e, muitas vezes, à resolução da deficiência visual. Em alguns pacientes, no entanto, uma deterioração secundária dos campos visuais pode se desenvolver posteriormente, apesar dos níveis de prolactina normalizados e do encolhimento do tumor, que pode resultar da tração no quiasma óptico que é puxado para baixo na sela agora parcialmente vazia. Nesses casos, o defeito do campo visual pode melhorar com a redução da dosagem de bromocriptina enquanto há alguma elevação da prolactina e alguma reexpansão tumoral. O monitoramento dos campos visuais em pacientes com macroprolactinoma é, portanto, recomendado para um reconhecimento precoce da perda de campo secundária devido à herniação do quiasma e adaptação da dosagem do medicamento.
eficácia relativa de Parlodel versus cirurgia na preservação dos campos visuais não é conhecida. Pacientes com perda de campo visual rapidamente progressiva devem ser avaliados por um neurocirurgião para ajudar a decidir sobre a terapia mais apropriada.
Como a gravidez é frequentemente o objetivo terapêutico em muitos pacientes hiperprolactinêmicos que apresentam amenorreia/galactorreia e hipogonadismo (infertilidade), uma avaliação cuidadosa da hipófise é essencial para detectar a presença de um adenoma secretor de prolactina. Pacientes que não pretendem engravidar ou que apresentam adenomas grandes devem ser aconselhadas a usar medidas contraceptivas, além de contraceptivos orais, durante o tratamento com Parlodel. Como a gravidez pode ocorrer antes do reinício da menstruação, um teste de gravidez é recomendado pelo menos a cada 4 semanas durante o período amenorreico e, uma vez que a menstruação é reiniciada, toda vez que a paciente perder um período menstrual. O tratamento com Parlodel SnapTabs ou cápsulas deve ser descontinuado assim que a gravidez for estabelecida. As pacientes devem ser monitoradas de perto durante a gravidez quanto a sinais e sintomas que possam sinalizar o aumento de um tumor secretor de prolactina previamente não detectado ou existente. A descontinuação do tratamento com Parlodel em pacientes com macroadenomas conhecidos foi associada ao rápido crescimento do tumor e aumento da prolactina sérica na maioria dos casos.
rinorréia do líquido cefalorraquidiano foi observada em alguns pacientes com adenomas secretores de prolactina tratados com Parlodel.
Acromegalia
Vasoespasmo digital sensível ao frio foi observado em alguns pacientes acromegálicos tratados com Parlodel. A resposta, caso ocorra, pode ser revertida pela redução da dose de Parlodel 2,5mg e pode ser prevenida mantendo os dedos aquecidos. Casos de sangramento gastrointestinal grave de úlceras pépticas foram relatados, alguns fatais. Embora não haja evidências de que Parlodel 2,5 mg aumente a incidência de úlceras pépticas em pacientes acromegálicos, os sintomas sugestivos de úlcera péptica devem ser investigados minuciosamente e tratados adequadamente. Pacientes com histórico de úlcera péptica ou sangramento gastrointestinal devem ser observados cuidadosamente durante o tratamento com Parlodel.
possível expansão do tumor durante o tratamento com Parlodel foi relatada em alguns pacientes. Uma vez que a história natural dos tumores secretores de hormônio do crescimento é desconhecida, todos os pacientes devem ser cuidadosamente monitorados e, se houver evidência de expansão tumoral, deve-se considerar a descontinuação do tratamento e procedimentos alternativos.
Mal de Parkinson
A segurança durante o uso prolongado por mais de 2 anos nas doses necessárias para o parkinsonismo não foi estabelecida.
Como em qualquer terapia crônica, recomenda-se a avaliação periódica das funções hepática, hematopoiética, cardiovascular e renal. Pode ocorrer hipotensão sintomática e, portanto, deve-se ter cautela ao tratar pacientes recebendo medicamentos anti-hipertensivos.
Altas doses de Parlodel 2,5mg podem estar associadas a confusão e distúrbios mentais. Uma vez que os pacientes parkinsonianos podem manifestar graus leves de demência, deve-se ter cuidado ao tratar esses pacientes.
Parlodel administrado isoladamente ou concomitantemente com levodopa pode causar alucinações (visuais ou auditivas). As alucinações geralmente desaparecem com a redução da dose; ocasionalmente, é necessária a descontinuação de Parlodel 2,5mg. Raramente, após altas doses, as alucinações persistiram por várias semanas após a descontinuação de Parlodel.
Assim como com a levodopa, deve-se ter cautela ao administrar Parlodel a pacientes com histórico de infarto do miocárdio que apresentam arritmia atrial, nodal ou ventricular residual.
Fibrose retroperitoneal foi relatada em alguns pacientes recebendo terapia de longo prazo (2 a 10 anos) com Parlodel 2,5mg em doses variando de 30-140mg diariamente.
Estudos epidemiológicos mostraram que pacientes com doença de Parkinson têm um risco maior (aproximadamente 6 vezes maior) de desenvolver melanoma do que a população em geral. Se o aumento do risco observado foi devido à doença de Parkinson ou outros fatores, como medicamentos usados para tratar a doença de Parkinson, não está claro. Pelas razões indicadas acima, os pacientes e provedores são aconselhados a monitorar os melanomas com frequência e regularmente ao usar Parlodel para qualquer indicação. Idealmente, os exames periódicos da pele devem ser realizados por indivíduos devidamente qualificados (por exemplo, dermatologistas).
descontinuação de Parlodel deve ser feita gradualmente sempre que possível, mesmo que o paciente permaneça em uso de levodopa. Um complexo de sintomas semelhante à síndrome neuroléptica maligna (caracterizada por temperatura elevada, rigidez muscular, consciência alterada e instabilidade autonômica), sem outra etiologia óbvia, foi relatado em associação com redução rápida da dose, retirada ou alterações na terapia antiparkinsoniana.
Sintomas incluindo apatia, ansiedade, depressão, fadiga, insônia, sudorese e dor foram relatados durante a redução gradual ou após a descontinuação de agonistas dopaminérgicos, incluindo Parlodel. Esses sintomas geralmente não respondem à levodopa. Antes da descontinuação de Parlodel, os pacientes devem ser informados sobre possíveis sintomas de abstinência e monitorados de perto durante e após a descontinuação de Parlodel. Em caso de sintomas de abstinência graves, pode ser considerada a readministração de um agonista da dopamina na dose eficaz mais baixa.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Um estudo de 74 semanas foi realizado em camundongos usando níveis dietéticos de mesilato de bromocriptina equivalentes a doses orais de 10 e 50 mg/kg/dia. Um estudo de 100 semanas em ratos foi realizado usando níveis dietéticos equivalentes a doses orais de 1,7, 9,8 e 44 mg/kg/dia. As doses mais altas testadas em camundongos e ratos foram aproximadamente 2,5 e 4,4 vezes, respectivamente, a dose humana máxima administrada em ensaios clínicos controlados (100 mg/dia) com base na área de superfície corporal. Tumores uterinos malignos, endometriais e miometriais, foram encontrados em ratos da seguinte forma: 0/50 fêmeas controle, 2/50 fêmeas recebendo 1,7 mg/kg diariamente, 7/49 fêmeas recebendo 9,8 mg/kg diariamente e 9/50 fêmeas recebendo 44 mg/kg diariamente. A ocorrência dessas neoplasias é provavelmente atribuída à alta relação estrogênio/progesterona que ocorre em ratos como resultado da ação inibidora da prolactina do mesilato de bromocriptina. Os mecanismos endócrinos que se acredita estarem envolvidos nos ratos não estão presentes em humanos. Não há correlação conhecida entre malignidades uterinas que ocorrem em ratos tratados com bromocriptina e risco humano. Em contraste com os achados em ratos, os úteros de camundongos mortos após 74 semanas de tratamento não apresentaram evidências de alterações relacionadas à droga.
mesilato de bromocriptina foi avaliado quanto ao potencial mutagênico na bateria de testes que incluíram o ensaio de mutação bacteriana de Ames, atividade mutagênica in vitro em fibroblastos de hamster chinês V79, análise citogenética de células de medula óssea de hamster chinês após tratamento in vivo e um teste de micronúcleo in vivo para mutações mutagênicas. potencial em camundongos.
Nenhum efeito mutagênico foi obtido em nenhum desses testes.
A fertilidade e o desempenho reprodutivo em ratas não foram influenciados negativamente pelo tratamento com bromocriptina além da redução prevista no peso dos filhotes devido à supressão da lactação. Nos machos tratados com 50 mg/kg desta droga, o acasalamento e a fertilidade estavam dentro da faixa normal. Aumento da perda perinatal foi produzido nos subgrupos de mães, sacrificadas no dia 21 pós-parto (pp) após o acasalamento com machos tratados com a dose mais alta (50mg/kg).
Gravidez
Categoria B
administração de 10-30 mg/kg de bromocriptina a 2 cepas de ratos nos dias 6 a 15 pós-coito (pc), bem como uma dose única de 10 mg/kg no dia 5 pc interferiu na nidação. Três mg/kg administrados nos dias 6 a 15 não tiveram efeito na nidação e não produziram quaisquer anomalias. Em animais tratados a partir do dia 8-15 pc, isto é, após a implantação, 30 mg/kg produziram aumento da mortalidade pré-natal na forma de aumento da incidência de reabsorção embrionária. Uma anomalia, aplasia de vértebras espinhais e costelas, foi encontrada no grupo de 262 fetos derivados das mães tratadas com 30 mg/kg de bromocriptina. Não foram encontrados efeitos fetotóxicos em descendentes de mães tratadas durante o período peri ou pós-natal.
Dois estudos foram conduzidos em coelhos (2 cepas) para determinar o potencial de interferir na nidação. Níveis de dose de 100 ou 300 mg/kg/dia do dia 1 ao dia 6 pc não afetaram adversamente a nidação. A dose alta foi aproximadamente 63 vezes a dose humana máxima administrada em ensaios clínicos controlados (100 mg/dia), com base na área de superfície corporal. Em coelhos brancos da Nova Zelândia, ocorreu alguma mortalidade embrionária com 300 mg/kg, o que foi um reflexo de toxicidade materna evidente. Três estudos foram conduzidos em 2 cepas de coelhos para determinar o potencial teratológico da bromocriptina em níveis de dose de 3, 10, 30, 100 e 300 mg/kg administrados do dia 6 ao dia 18 pc Em 2 estudos com a cepa Yellow-silver , fenda palatina foi encontrada em 3 e 2 fetos em doses maternas tóxicas de 100 e 300 mg/kg, respectivamente. Um feto controle também exibiu essa anomalia. No terceiro estudo realizado com coelhos brancos da Nova Zelândia usando um protocolo idêntico, não foram produzidas fendas palatinas.
Não foram produzidos efeitos teratológicos ou embriotóxicos da bromocriptina em qualquer dos 6 descendentes de 6 macacos a um nível de dose de 2 mg/kg.
Foram recolhidas informações relativas a 1276 gravidezes em mulheres a tomar Parlodel. Na maioria dos casos, Parlodel foi descontinuado dentro de 8 semanas de gravidez (média de 28,7 dias), no entanto, 8 pacientes receberam o medicamento continuamente durante toda a gravidez. A dose diária média para todos os pacientes foi de 5,8 mg (intervalo de 1-40 mg).
Dessas 1.276 gestações, houve 1.088 partos a termo (4 natimortos), 145 abortos espontâneos (11,4%) e 28 abortos induzidos (2,2%). Além disso, 12 gestações extrauterinas e 3 molas hidatiformes (duas vezes na mesma paciente) causaram interrupção precoce da gravidez. Esses dados se comparam favoravelmente com a taxa de aborto (11% -25%) citada para gestações induzidas por citrato de clomifeno, gonadotrofina menopausal e gonadotrofina coriônica.
Embora os abortos espontâneos muitas vezes não sejam relatados, especialmente antes de 20 semanas de gestação, sua frequência foi estimada em 15%.
A incidência de defeitos congênitos na população varia de 2% a 4,5%. A incidência em 1.109 nascidos vivos de pacientes recebendo bromocriptina é de 3,3%.
Não há sugestão de que Parlodel 2,5mg tenha contribuído para o tipo ou incidência de defeitos congênitos neste grupo de crianças.
Mães que amamentam
Parlodel 2,5mg não deve ser usado durante a lactação em mulheres no pós-parto.
Uso Pediátrico
A segurança e a eficácia da bromocriptina para o tratamento de adenomas hipofisários secretores de prolactina foram estabelecidas em pacientes com idades entre 16 e adultos. Não há dados disponíveis para o uso de bromocriptina em pacientes pediátricos com idade inferior a 8 anos. Um único paciente de 8 anos de idade tratado com bromocriptina para um macroadenoma hipofisário secretor de prolactina foi relatado sem resposta terapêutica.
uso de bromocriptina para o tratamento de adenomas secretores de prolactina em pacientes pediátricos na faixa etária de 11 a 16 anos é apoiado por evidências de estudos bem controlados em adultos, com dados adicionais em um número limitado (n=14) de crianças e adolescentes de 11 a 15 anos de idade com macro e microadenomas hipofisários secretores de prolactina que foram tratados com bromocriptina. Dos 14 pacientes relatados, 9 tiveram resultados bem sucedidos, 3 respostas parciais e 2 não responderam ao tratamento com bromocriptina. O hipopituitarismo crônico complicou o tratamento do macroadenoma em 5 dos respondedores, tanto em pacientes que receberam bromocriptina isoladamente quanto naqueles que receberam bromocriptina em combinação com tratamento cirúrgico e/ou irradiação hipofisária.
A segurança e eficácia da bromocriptina em pacientes pediátricos não foram estabelecidas para nenhuma outra indicação listada na seção INDICAÇÕES E USO.
Uso Geriátrico
Os estudos clínicos para Parlodel 2,5 mg não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se os idosos respondem de forma diferente dos indivíduos mais jovens. No entanto, outras experiências clínicas relatadas, incluindo notificação pós-comercialização de eventos adversos, não identificaram diferenças na resposta ou tolerabilidade entre pacientes idosos e mais jovens. Embora não tenha sido observada variação na eficácia ou perfil de reações adversas em pacientes geriátricos tomando Parlodel 2,5 mg, maior sensibilidade de alguns idosos não pode ser categoricamente descartada. Em geral, a seleção da dose para um paciente idoso deve ser cautelosa, começando na extremidade inferior da faixa de dose, refletindo a maior frequência de diminuição da função hepática, renal ou cardíaca e de doença concomitante ou outra terapia medicamentosa nessa população.
SOBREDOSAGEM
Os sinais e sintomas mais comumente relatados associados à superdosagem aguda de Parlodel (mesilato de bromocriptina) são: náusea, vômito, constipação, sudorese, tontura, palidez, hipotensão grave, mal-estar, confusão, letargia, sonolência, delírios, alucinações e bocejos repetitivos. A dose letal não foi estabelecida e a droga tem uma margem de segurança muito ampla. No entanto, uma morte ocorreu em um paciente que cometeu suicídio com uma quantidade desconhecida de Parlodel 2,5mg e cloroquina.
O tratamento da superdosagem consiste na remoção do fármaco por vômito (se consciente), lavagem gástrica, carvão ativado ou catarse salina. Supervisão cuidadosa e registro da ingestão e eliminação de líquidos são essenciais. A hipotensão deve ser tratada colocando o paciente na posição de Trendelenburg e administrando fluidos intravenosos. Se o alívio satisfatório da hipotensão não puder ser alcançado usando as medidas acima em toda a sua extensão, os vasopressores devem ser considerados.
Houve relatos isolados de crianças que ingeriram acidentalmente Parlodel. Vômitos, sonolência e febre foram relatados como eventos adversos. Os pacientes se recuperaram espontaneamente em poucas horas ou após tratamento adequado.
CONTRA-INDICAÇÕES
Hipersensibilidade à bromocriptina ou a qualquer um dos excipientes de Parlodel (mesilato de bromocriptina), hipertensão não controlada e sensibilidade a qualquer alcalóide do ergot. Em pacientes em tratamento para hiperprolactinemia, Parlodel 2,5 mg deve ser descontinuado quando a gravidez for diagnosticada (ver PRECAUÇÕES , Estados hiperprolactinêmicos ). Caso Parlodel 2,5mg seja reinstituído para controlar um macroadenoma em rápida expansão (ver PRECAUÇÕES , Estados hiperprolactinêmicos e uma paciente apresenta um distúrbio hipertensivo da gravidez, o benefício de continuar Parlodel deve ser ponderado em relação ao possível risco de seu uso durante um distúrbio hipertensivo da gravidez. Quando Parlodel está sendo usado para tratar acromegalia, prolactinoma ou doença de Parkinson em pacientes que engravidam posteriormente, deve-se decidir se a terapia continua a ser clinicamente necessária ou pode ser retirada. Se for continuado, o medicamento deve ser descontinuado em pacientes que possam apresentar distúrbios hipertensivos da gravidez (incluindo eclâmpsia, pré-eclâmpsia ou hipertensão induzida pela gravidez), a menos que a retirada de Parlodel seja considerada clinicamente contraindicada.
O medicamento não deve ser usado durante o período pós-parto em mulheres com histórico de doença arterial coronariana e outras condições cardiovasculares graves, a menos que a retirada seja considerada clinicamente contraindicada. Se o medicamento for usado no período pós-parto, a paciente deve ser observada com cautela.
FARMACOLOGIA CLÍNICA
Parlodel (mesilato de bromocriptina) é um agonista do receptor de dopamina, que ativa os receptores de dopamina pós-sinápticos. Os neurônios dopaminérgicos no processo tuberoinfundibular modulam a secreção de prolactina da hipófise anterior secretando um fator inibidor de prolactina (que se acredita ser dopamina); no corpo estriado, os neurônios dopaminérgicos estão envolvidos no controle da função motora. Clinicamente, Parlodel 2,5 mg reduz significativamente os níveis plasmáticos de prolactina em pacientes com prolactina fisiologicamente elevada, bem como em pacientes com hiperprolactinemia. A inibição da lactação fisiológica, bem como da galactorreia em estados hiperprolactinêmicos patológicos, é obtida em níveis de dose que não afetam a secreção de outros hormônios trópicos da hipófise anterior. Experimentos demonstraram que a bromocriptina induz comportamento estereotipado de longa duração em roedores e comportamento de giro em ratos com lesões unilaterais na substância negra. Essas ações, características daquelas produzidas pela dopamina, são inibidas pelos antagonistas da dopamina e sugerem uma ação direta da bromocriptina sobre os receptores dopaminérgicos estriatais.
mesilato de bromocriptina é um agente não hormonal, não estrogênico, que inibe a secreção de prolactina em humanos, com pouco ou nenhum efeito sobre outros hormônios hipofisários, exceto em pacientes com acromegalia, onde reduz os níveis sanguíneos elevados de hormônio do crescimento na maioria dos pacientes.
O mesilato de bromocriptina produz seu efeito terapêutico no tratamento da doença de Parkinson, quadro clínico caracterizado por deficiência progressiva na síntese de dopamina na substância negra, por estimulação direta dos receptores de dopamina no corpo estriado. Em contraste, a levodopa exerce seu efeito terapêutico somente após a conversão em dopamina pelos neurônios da substância negra, que se sabe estarem numericamente diminuídos nesta população de pacientes.
Farmacocinética
Absorção
Após a administração de dose única de comprimidos de Parlodel 2,5 mg, 2 x 2,5 mg a 5 voluntários saudáveis em jejum, os níveis plasmáticos médios de pico de bromocriptina, o tempo para atingir as concentrações plasmáticas máximas e a meia-vida de eliminação foram de 465 pg/mL ± 226, 2,5 h ± 2 e 4,85 h, respectivamente.1 Foi encontrada uma relação linear entre doses únicas de Parlodel 2,5 mg e Cmax e AUC no intervalo de dose de 1 a 7,5 mg.2 A farmacocinética dos metabólitos da bromocriptina não foi relatada.
Os alimentos não afetaram significativamente a exposição sistêmica da bromocriptina após a administração de comprimidos de Parlodel, 2,5 mg.3 Recomenda-se que Parlodel 2,5 mg seja tomado com alimentos devido à alta porcentagem de indivíduos que vomitam ao receber bromocriptina em jejum.
Após a administração de Parlodel 5 mg duas vezes ao dia por 14 dias, a Cmax e AUC da bromocriptina no estado de equilíbrio foram 628 ± 375 pg/mL e 2377 ± 1186 pg*hr/mL, respectivamente.4
Distribuição
Experimentos in vitro mostraram que a bromocriptina estava 90% -96% ligada à albumina sérica.
Metabolismo
A bromocriptina sofre extensa biotransformação de primeira passagem, refletida por perfis metabólitos complexos e pela ausência quase completa do fármaco original na urina e nas fezes.
Estudos in vitro usando microssomas hepáticos humanos mostraram que a bromocriptina tem uma alta afinidade para CYP3A e hidroxilações no anel prolina da porção ciclopeptídica constituiu uma via metabólica principal.5 Inibidores e/ou substratos potentes para CYP3A4 podem, portanto, inibir a depuração de bromocriptina e chumbo para níveis aumentados. (Vejo PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS seção). A participação de outras enzimas CYP importantes como 2D6, 2C8 e 2C19 no metabolismo da bromocriptina não foi avaliada. A bromocriptina também é um inibidor do CYP3A4 com um valor calculado de IC50 de 1,69 μM.6 Dadas as baixas concentrações terapêuticas de bromocriptina em pacientes (Cmax=0,82 nM), uma alteração significativa do metabolismo de um segundo medicamento cuja depuração é mediada pelo CYP3A4 não deve seja esperado. O efeito potencial da bromocriptina e seus metabólitos para atuar como indutores das enzimas CYP não foi relatado.
Excreção
Cerca de 82% e 5,6% da dose radioativa administrada oralmente foi recuperada nas fezes e na urina, respectivamente. O ácido bromolisérgico e o ácido bromoisolisérgico foram responsáveis por metade da radioatividade na urina.5
Populações Específicas
Efeito do Insuficiência Renal
O efeito da função renal na farmacocinética da bromocriptina não foi avaliado.
Uma vez que o fármaco original e os metabólitos são quase completamente excretados via metabolismo e apenas 6% eliminados por via renal, a insuficiência renal pode não ter um impacto significativo na farmacocinética da bromocriptina e seus metabólitos (ver PRECAUÇÕES , Em geral ).
Efeito do Insuficiência Hepática
O efeito da insuficiência hepática na farmacocinética de Parlodel e seus metabólitos não foi avaliado. Uma vez que Parlodel é eliminado principalmente por metabolismo, a insuficiência hepática pode aumentar os níveis plasmáticos de bromocriptina, portanto, pode ser necessário cautela (ver PRECAUÇÕES , Em geral ).
O efeito da idade, raça e sexo na farmacocinética da bromocriptina e seus metabólitos não foi avaliado.
Estudos clínicos
Em cerca de 75% dos casos de amenorreia e galactorreia, a terapia com Parlodel 2,5mg suprime a galactorreia completamente, ou quase completamente, e reinicia os ciclos menstruais ovulatórios normais.
menstruação geralmente é reiniciada antes da completa supressão da galactorreia; o tempo para isso em média é de 6 a 8 semanas. No entanto, alguns pacientes respondem dentro de alguns dias e outros podem levar até 8 meses.
A galactorreia pode levar mais tempo para controlar dependendo do grau de estimulação do tecido mamário antes da terapia. Pelo menos uma redução de 75% na secreção é geralmente observada após 8 a 12 semanas. Alguns pacientes podem não responder mesmo após 12 meses de terapia.
Em muitos pacientes acromegálicos, Parlodel 2,5mg produz uma redução imediata e sustentada nos níveis circulantes do hormônio do crescimento sérico.
1 Nelson, M. et. al. (1990). Avaliação farmacocinética da eritromicina e cafeína administradas com bromocriptina. Clin Pharmacol Ther; 47(6):694-7.
Schran, HF, Bhuta, SI, Schwartz, et al. (1980). A farmacocinética da bromocriptina no homem. In: Golstein, M. Calne, DB, et. Al (eds). Composto do ergot e função cerebral: aspectos neuroendócrinos e neuropsiquiátricos, pp. 125-139, Nova York, Rave Press.
3 Kopitar, Z., Vrhovac, B., Povsic, L., Plavsic, F., Francetic, I., Urbancic, J. (1991). O efeito de alimentos e metoclopramida na farmacocinética e efeitos colaterais da bromocriptina. Eur J Drug Metab Pharmacokinet; 16(3):177-81
4 Flogstad, AK, Halse, J., Grass, P., Abisch, E., Djoseland, O., Kutz, K., Bodd, E., and Jervell, J., (1994). Uma comparação de octreotida, bromocriptina ou uma combinação de ambas as drogas na acromegalia. Jornal de Endocrinologia Clínica e Metabolismo; Volume 79, 461-465
5 Peyronneau MA, Delaforge M, Riviere R et al. 1994. Alta afinidade de ergopeptídeos para CYP P450 3A. Importância da sua porção peptídica para o reconhecimento de P450 e hidroxilação da bromocriptina. Eur J Biochem 223:947-56.
Wynalda, MA, Wienkers, LC (1997). Avaliação de interações potenciais entre agonistas do receptor de dopamina e várias enzimas do citocromo P450 humano usando uma simples tela de inibição in vitro. Droga Metab Dispos; 25:1211-14.
INFORMAÇÃO DO PACIENTE
Durante os ensaios clínicos, tonturas, sonolência, desmaios, desmaios e síncope foram relatados no início do tratamento com Parlodel 2,5 mg. Em relatos pós-comercialização, Parlodel foi associado a sonolência e episódios de início súbito de sono, particularmente em pacientes com doença de Parkinson. O início súbito de sono durante as atividades diárias, em alguns casos sem consciência ou sinais de alerta, foi relatado muito raramente. Todos os pacientes em tratamento com Parlodel devem ser advertidos com relação ao envolvimento em atividades que exijam respostas rápidas e precisas, como dirigir um automóvel ou operar máquinas. Pacientes em tratamento com Parlodel 2,5 mg e que apresentem sonolência e/ou episódios de sono súbito devem ser aconselhados a não dirigir ou realizar atividades nas quais o estado de alerta prejudicado possa colocar a si ou a outros em risco de ferimentos graves ou morte (por exemplo, operar máquinas).
Pacientes recebendo Parlodel 2,5mg para estados hiperprolactinêmicos associados a macroadenoma ou aqueles que tiveram cirurgia transesfenoidal prévia devem ser orientados a relatar qualquer secreção nasal aquosa persistente ao seu médico. Pacientes recebendo Parlodel 2,5 mg para tratamento de macroadenoma devem ser informados de que a descontinuação do medicamento pode estar associada ao rápido crescimento do tumor e recorrência de seus sintomas originais.
Os pacientes e seus cuidadores devem ser alertados para a possibilidade de que os pacientes possam experimentar desejos intensos de gastar dinheiro incontrolavelmente, desejos intensos de jogar, aumento dos desejos sexuais e outros desejos intensos e a incapacidade de controlar esses desejos enquanto estiver tomando Parlodel. Aconselhe os pacientes e seus cuidadores a informarem seus profissionais de saúde se desenvolverem novos gastos descontrolados ou aumento de gastos, impulsos de jogo, impulsos sexuais ou outros impulsos durante o tratamento com Parlodel [ver PRECAUÇÕES ].
Especialmente durante os primeiros dias de tratamento, reações hipotensivas podem ocorrer ocasionalmente e resultar em diminuição do estado de alerta, devendo-se ter cuidado especial ao dirigir veículos ou operar máquinas.
Aconselhe os pacientes a entrar em contato com seu médico se desejarem descontinuar Parlodel ou diminuir a dose de Parlodel. Aconselhe os pacientes aos quais foi prescrita uma dose mais baixa ou que foram descontinuados do medicamento a notificar seu médico se tiverem sintomas de abstinência, como febre, rigidez muscular, consciência alterada, apatia, ansiedade, depressão, fadiga, insônia, sudorese ou dor (ver PRECAUÇÕES ).
