Wellbutrin 150mg, 300mg Bupropion Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Wellbutrin 150mg e como é usado?
Wellbutrin 150mg é um medicamento de prescrição usado para tratar os sintomas da depressão maior e transtorno afetivo sazonal. Wellbutrin 150mg pode ser usado sozinho ou com outros medicamentos.
Wellbutrin 150mg pertence a uma classe de medicamentos chamados antidepressivos, inibidores da recaptação de dopamina, antidepressivos, outros, auxiliares de cessação do tabagismo.
Quais são os possíveis efeitos colaterais do Wellbutrin 150mg?
Wellbutrin pode causar efeitos colaterais graves, incluindo:
- convulsão (convulsões),
- confusão,
- mudanças incomuns no humor ou comportamento,
- visão embaçada,
- visão de túnel,
- dor ou inchaço nos olhos,
- vendo halos ao redor das luzes,
- batimentos cardíacos rápidos ou irregulares,
- pensamentos descontrolados,
- aumento de energia,
- comportamento imprudente,
- sentindo-se extremamente feliz ou irritado,
- falando mais do que o normal, e
- problemas graves com o sono
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Wellbutrin incluem:
- boca seca,
- nariz entupido,
- problemas de visão,
- problemas de audição,
- náusea,
- vômito,
- constipação,
- problemas de sono (insônia),
- tremores,
- sudorese,
- sentir-se ansioso ou nervoso,
- batimentos cardíacos acelerados,
- confusão,
- agitação,
- hostilidade,
- irritação na pele,
- dor de cabeça,
- tontura, e
- dor nas articulações
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Wellbutrin. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088
AVISO
PENSAMENTOS E COMPORTAMENTOS SUICÍDICOS
SUICIDALIDADE E DROGAS ANTIDEPRESSIVAS
Os antidepressivos aumentaram o risco de pensamentos e comportamentos suicidas em crianças, adolescentes e adultos jovens em estudos de curto prazo. Esses estudos não mostraram um aumento no risco de pensamentos e comportamentos suicidas com o uso de antidepressivos em indivíduos com mais de 24 anos; houve uma redução no risco com o uso de antidepressivos em indivíduos com 65 anos ou mais [ver ADVERTÊNCIAS E PRECAUÇÕES].
Em pacientes de todas as idades que iniciam a terapia antidepressiva, monitore atentamente a piora e o surgimento de pensamentos e comportamentos suicidas. Aconselhe as famílias e os cuidadores sobre a necessidade de observação atenta e comunicação com o prescritor [ver ADVERTÊNCIAS E PRECAUÇÕES].
DESCRIÇÃO
WELLBUTRIN (cloridrato de bupropiona), um antidepressivo da classe das aminocetonas, não está quimicamente relacionado ao inibidor seletivo de recaptação de serotonina tricíclico, tetracíclico, ou outros agentes antidepressivos conhecidos. A sua estrutura assemelha-se muito à da dietilpropiona; está relacionado com as feniletilaminas. É designado como cloridrato de (±)-1-(3-clorofenil)-2-[(1,1-dimetiletil)amino]-1-propanona. O peso molecular é 276,2. A fórmula molecular é C13H18ClNO•HCl. O pó de cloridrato de bupropiona é branco, cristalino e altamente solúvel em água. Tem sabor amargo e produz a sensação de anestesia local na mucosa oral. A fórmula estrutural é:
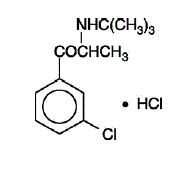
WELLBUTRIN é fornecido para administração oral em comprimidos revestidos por película de 75 mg (ouro amarelo) e 100 mg (vermelho). Cada comprimido contém a quantidade rotulada de cloridrato de bupropiona e os ingredientes inativos: Comprimido de 75 mg – Lago D&C Amarelo Nº 10, Lago FD&C Amarelo Nº 6, hidroxipropilcelulose, hipromelose, celulose microcristalina, polietilenoglicol, talco e dióxido de titânio; Comprimido de 100 mg – Lagoa FD&C Vermelho Nº 40, Lagoa FD&C Amarelo Nº 6, hidroxipropilcelulose, hipromelose, celulose microcristalina, polietilenoglicol, talco e dióxido de titânio.
INDICAÇÕES
WELLBUTRIN (cloridrato de bupropiona) é indicado para o tratamento do transtorno depressivo maior (TDM), conforme definido pelo Manual Diagnóstico e Estatístico (DSM).
A eficácia de WELLBUTRIN 300mg no tratamento de um episódio depressivo maior foi estabelecida em dois estudos controlados de 4 semanas em pacientes internados e um estudo controlado ambulatorial de 6 semanas em indivíduos adultos com TDM [ver Estudos clínicos ].
DOSAGEM E ADMINISTRAÇÃO
Instruções Gerais de Uso
Para minimizar o risco de convulsão, aumente a dose gradualmente [ver AVISOS E PRECAUÇÕES ]. Os aumentos na dose não devem exceder 100 mg/dia em um período de 3 dias. Os comprimidos de Wellbutrin devem ser engolidos inteiros e não esmagados, divididos ou mastigados. WELLBUTRIN 300mg pode ser tomado com ou sem alimentos.
A dose inicial recomendada é de 200 mg/dia, administrada em 100 mg duas vezes ao dia. Após 3 dias de administração, a dose pode ser aumentada para 300 mg/dia, administrada como 100 mg 3 vezes ao dia, com pelo menos 6 horas entre as doses sucessivas. A dosagem acima de 300 mg/dia pode ser realizada usando os comprimidos de 75 ou 100 mg.
Um máximo de 450 mg/dia, administrado em doses divididas de não mais de 150 mg cada, pode ser considerado para pacientes que não apresentam melhora clínica após várias semanas de tratamento com 300 mg/dia. Administrar o comprimido de 100 mg 4 vezes ao dia para não exceder o limite de 150 mg em dose única.
É geralmente aceito que episódios agudos de depressão requerem vários meses ou mais de tratamento com antidepressivos além da resposta no episódio agudo. Não se sabe se a dose de Wellbutrin necessária para o tratamento de manutenção é idêntica à dose que forneceu uma resposta inicial. Reavaliar periodicamente a necessidade de tratamento de manutenção e a dose adequada para tal tratamento.
Ajuste de dose em pacientes com insuficiência hepática
Em pacientes com insuficiência hepática moderada a grave (pontuação de Child-Pugh: 7 a 15), a dose máxima de WELLBUTRIN 150mg é de 75mg/dia. Em pacientes com insuficiência hepática leve (pontuação de Child-Pugh: 5 a 6), considere reduzir a dose e/ou frequência de dosagem [ver Uso em populações específicas , FARMACOLOGIA CLÍNICA ].
Ajuste de dose em pacientes com insuficiência renal
Considere reduzir a dose e/ou frequência de WELLBUTRIN 150mg em pacientes com insuficiência renal (taxa de filtração glomerular menor que 90 mL/min) [ver Uso em populações específicas , FARMACOLOGIA CLÍNICA ].
Mudar um paciente para ou de um antidepressivo inibidor da monoamina oxidase (IMAO)
Devem decorrer pelo menos 14 dias entre a descontinuação de um IMAO destinado a tratar a depressão e o início da terapia com WELLBUTRIN. Por outro lado, pelo menos 14 dias devem ser permitidos após a interrupção do Wellbutrin antes de iniciar um antidepressivo IMAO [ver CONTRA-INDICAÇÕES , INTERAÇÕES MEDICAMENTOSAS ].
Uso de WELLBUTRIN com MAOIs reversíveis, como linezolida ou azul de metileno
Não inicie WELLBUTRIN 300mg em um paciente que esteja sendo tratado com um IMAO reversível, como linezolida ou azul de metileno intravenoso. As interações medicamentosas podem aumentar o risco de reações hipertensivas. Em um paciente que requer tratamento mais urgente de uma condição psiquiátrica, intervenções não farmacológicas, incluindo hospitalização, devem ser consideradas [ver CONTRA-INDICAÇÕES , INTERAÇÕES MEDICAMENTOSAS ].
Em alguns casos, um paciente que já esteja recebendo terapia com Wellbutrin pode necessitar de tratamento urgente com linezolida ou azul de metileno intravenoso. Se alternativas aceitáveis ao tratamento com linezolida ou azul de metileno intravenoso não estiverem disponíveis e os benefícios potenciais do tratamento com linezolida ou azul de metileno intravenoso forem considerados superiores aos riscos de reações hipertensivas em um determinado paciente, Wellbutrin 300 mg deve ser interrompido imediatamente e linezolida ou metileno intravenoso azul pode ser administrado. O paciente deve ser monitorado por 2 semanas ou até 24 horas após a última dose de linezolida ou azul de metileno intravenoso, o que ocorrer primeiro. A terapia com WELLBUTRIN 300mg pode ser retomada 24 horas após a última dose de linezolida ou azul de metileno intravenoso.
risco de administrar azul de metileno por vias não intravenosas (como comprimidos orais ou por injeção local) ou em doses intravenosas muito inferiores a 1 mg/kg com WELLBUTRIN 300 mg não é claro. O clínico deve, no entanto, estar ciente da possibilidade de interação medicamentosa com tal uso [ver CONTRA-INDICAÇÕES , INTERAÇÕES MEDICAMENTOSAS ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
- 75 mg – comprimidos amarelo-ouro, redondos, biconvexos, impressos com “WELLBUTRIN 75”.
- 100 mg – comprimidos vermelhos, redondos, biconvexos, impressos com “WELLBUTRIN 100”.
Armazenamento e manuseio
Os comprimidos de WELLBUTRIN 150 mg, 75 mg de cloridrato de bupropiona, são comprimidos biconvexos amarelo-ouro, redondos, impressos com “WELLBUTRIN 75” em frascos de 100 ( NDC 0173-0177-55).
Os comprimidos de WELLBUTRIN, 100 mg de cloridrato de bupropiona, são comprimidos vermelhos, redondos, biconvexos, impressos com “WELLBUTRIN 100” em frascos de 100 ( NDC 0173-0178-55).
Armazenar à temperatura ambiente, 20° a 25°C (68° a 77°F); excursões permitidas entre 15°C e 30°C (59°F e 86°F) [Consulte Temperatura ambiente controlada USP ]. Proteja da luz e da umidade.
Fabricado para: GlaxoSmithKline, Research Triangle Park,. Revisado: novembro de 2019
EFEITOS COLATERAIS
As seguintes reações adversas são discutidas em mais detalhes em outras seções da bula:
- Pensamentos e comportamentos suicidas em adolescentes e adultos jovens [ver AVISO EM CAIXA , AVISOS E PRECAUÇÕES ]
- Sintomas neuropsiquiátricos e risco de suicídio no tratamento de cessação do tabagismo [ver AVISOS E PRECAUÇÕES ]
- Convulsão [ver AVISOS E PRECAUÇÕES ]
- Hipertensão [ver AVISOS E PRECAUÇÕES ]
- Ativação de mania ou hipomania [ver AVISOS E PRECAUÇÕES ]
- Psicose e outras reações neuropsiquiátricas [ver AVISOS E PRECAUÇÕES ]
- Glaucoma de ângulo fechado [ver AVISOS E PRECAUÇÕES ]
- Reações de hipersensibilidade [ver AVISOS E PRECAUÇÕES ]
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
Reações Adversas que Levam à Descontinuação do Tratamento
As reações adversas foram suficientemente problemáticas para causar a descontinuação do tratamento com WELLBUTRIN em aproximadamente 10% dos 2.400 indivíduos e voluntários saudáveis que participaram de ensaios clínicos durante o desenvolvimento inicial do produto. Os eventos mais comuns que causam descontinuação incluem distúrbios neuropsiquiátricos (3,0%), principalmente agitação e anormalidades no estado mental; distúrbios gastrointestinais (2,1%), principalmente náuseas e vômitos; distúrbios neurológicos (1,7%), principalmente convulsões, dores de cabeça e distúrbios do sono; e problemas dermatológicos (1,4%), principalmente erupções cutâneas. É importante notar, no entanto, que muitos desses eventos ocorreram em doses que excedem a dose diária recomendada.
Reações Adversas Comumente Observadas
As reações adversas comumente encontradas em indivíduos tratados com Wellbutrin são agitação, boca seca, insônia, dor de cabeça/enxaqueca, náusea/vômito, constipação, tremor, tontura, sudorese excessiva, visão turva, taquicardia, confusão, erupção cutânea, hostilidade, arritmia cardíaca e distúrbios auditivos. perturbação.
A Tabela 2 resume as reações adversas que ocorreram em estudos controlados com placebo em uma incidência de pelo menos 1% dos indivíduos que receberam WELLBUTRIN 150mg e com mais frequência nesses indivíduos do que no grupo placebo.
Outras reações adversas observadas durante o desenvolvimento clínico de WELLBUTRIN
As condições e a duração da exposição ao WELLBUTRIN variaram muito, e uma proporção substancial da experiência foi adquirida em ambientes clínicos abertos e não controlados. Durante essa experiência, vários eventos adversos foram relatados; no entanto, sem controles apropriados, é impossível determinar com certeza quais eventos foram ou não causados por WELLBUTRIN. A seguinte enumeração está organizada por sistema de órgãos e descreve os eventos em termos de sua frequência relativa de notificação no banco de dados.
São utilizadas as seguintes definições de frequência: Reacções adversas frequentes são definidas como aquelas que ocorrem em pelo menos 1/100 indivíduos. Reações adversas infrequentes são aquelas que ocorrem em 1/100 a 1/1.000 indivíduos, enquanto eventos raros são aqueles que ocorrem em menos de 1/1.000 indivíduos.
Cardiovascular Frequente foi o edema; infrequentes foram dor torácica, anormalidades no eletrocardiograma (ECG) (batimentos prematuros e alterações ST-T inespecíficas) e falta de ar/dispneia; raros foram rubor e infarto do miocárdio.
Dermatológico: Infrequente era alopecia.
Endócrino: Infrequente foi a ginecomastia; rara foi a glicosúria.
Gastrointestinal: Infrequentes foram disfagia, distúrbio da sede e lesão hepática/icterícia; rara foi a perfuração intestinal.
Geniturinário: Frequente era a noctúria; infrequentes foram irritação vaginal, inchaço testicular, infecção do trato urinário, ereção dolorosa e ejaculação retardada; raros foram enurese e incontinência urinária.
Neurológico: Frequentes foram ataxia/incoordenação, convulsão, mioclonia, discinesia e distonia; infrequentes foram midríase, vertigem e disartria; raras foram anormalidades no eletroencefalograma (EEG) e atenção prejudicada.
Neuropsiquiátrico: Frequentes foram mania/hipomania, aumento da libido, alucinações, diminuição da função sexual e depressão; infrequentes foram comprometimento da memória, despersonalização, psicose, disforia, instabilidade do humor, paranóia e transtorno formal do pensamento; rara era a ideação suicida.
Reclamações orais: Frequente era estomatite; infrequentes foram dor de dente, bruxismo, irritação gengival e edema oral.
Respiratório: Infrequentes foram bronquite e falta de ar/dispneia; rara foi a embolia pulmonar.
Sentidos Especiais: Pouco frequente era a perturbação visual; rara era a diplopia.
Não específico: Frequentes eram sintomas semelhantes aos da gripe; infrequente foi a dor inespecífica; raro foi overdose.
Apetite e peso alterados
Uma perda de peso superior a 5 libras. ocorreu em 28% dos indivíduos que receberam WELLBUTRIN. Esta incidência é aproximadamente o dobro da observada em indivíduos comparáveis tratados com tricíclicos ou placebo. Além disso, enquanto 35% dos indivíduos que receberam antidepressivos tricíclicos ganharam peso, apenas 9,4% dos indivíduos tratados com WELLBUTRIN o fizeram. Consequentemente, se a perda de peso for um sinal importante de apresentação da doença depressiva de um paciente, o potencial anorexígeno e/ou redutor de peso de Wellbutrin deve ser considerado.
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de WELLBUTRIN e não são descritas em outras partes do rótulo. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Corpo (Geral)
Artralgia, mialgia e febre com erupção cutânea e outros sintomas sugestivos de hipersensibilidade tardia. Esses sintomas podem assemelhar-se à doença do soro [ver AVISOS E PRECAUÇÕES ].
Cardiovascular
Hipertensão (em alguns casos grave), hipotensão ortostática, bloqueio cardíaco de terceiro grau.
Endócrino
Hiponatremia, síndrome de secreção inadequada de hormônio antidiurético, hiperglicemia, hipoglicemia.
Gastrointestinal
Esofagite, hepatite.
Hemico e Linfático
Equimose, leucocitose, leucopenia, trombocitopenia. Alterações de PT e/ou INR, raramente associadas a complicações hemorrágicas ou trombóticas, foram observadas quando a bupropiona foi coadministrada com varfarina.
Musculoesquelético
Rigidez muscular/febre/rabdomiólise, fraqueza muscular.
Sistema nervoso
Agressão, coma, suicídio consumado, delírio, anormalidades do sonho, ideação paranóide, parestesia, parkinsonismo, inquietação, tentativa de suicídio, desmascaramento de discinesia tardia.
Pele e anexos
Síndrome de Stevens-Johnson, angioedema, dermatite esfoliativa, urticária.
Sentidos Especiais
Zumbido, aumento da pressão intraocular.
INTERAÇÕES MEDICAMENTOSAS
Potencial para outros medicamentos afetarem WELLBUTRIN
A bupropiona é metabolizada principalmente em hidroxibupropiona pelo CYP2B6. Portanto, existe o potencial de interações medicamentosas entre WELLBUTRIN e medicamentos que são inibidores ou indutores de CYP2B6.
Inibidores de CYP2B6
Ticlopidina e Clopidogrel
O tratamento concomitante com esses medicamentos pode aumentar a exposição à bupropiona, mas diminuir a exposição à hidroxibupropiona. Com base na resposta clínica, o ajuste da dose de Wellbutrin pode ser necessário quando coadministrado com inibidores do CYP2B6 (por exemplo, ticlopidina ou clopidogrel) [ver FARMACOLOGIA CLÍNICA ].
Indutores de CYP2B6
Ritonavir, Lopinavir e Efavirenz
O tratamento concomitante com esses medicamentos pode diminuir a exposição à bupropiona e à hidroxibupropiona. O aumento da dose de Wellbutrin pode ser necessário quando coadministrado com ritonavir, lopinavir ou efavirenz [ver FARMACOLOGIA CLÍNICA ] mas não deve exceder a dose máxima recomendada.
Carbamazepina, Fenobarbital, Fenitoína
Embora não sejam sistematicamente estudados, esses medicamentos podem induzir o metabolismo da bupropiona e diminuir a exposição à bupropiona [ver FARMACOLOGIA CLÍNICA ]. Se a bupropiona for usada concomitantemente com um indutor de CYP, pode ser necessário aumentar a dose de bupropiona, mas a dose máxima recomendada não deve ser excedida.
Potencial para WELLBUTRIN 300mg para afetar outras drogas
Drogas Metabolizadas Por CYP2D6
bupropiona e seus metabólitos (eritrohidrobupropiona, treohidrobupropiona, hidroxibupropiona) são inibidores do CYP2D6. Portanto, a coadministração de WELLBUTRIN com medicamentos que são metabolizados pelo CYP2D6 pode aumentar as exposições de medicamentos que são substratos do CYP2D6. Esses medicamentos incluem certos antidepressivos (por exemplo, venlafaxina, nortriptilina, imipramina, desipramina, paroxetina, fluoxetina e sertralina), antipsicóticos (por exemplo, haloperidol, risperidona, tioridazina), betabloqueadores (por exemplo, metoprolol) e antiarrítmicos do tipo 1C (por exemplo, , propafenona e flecainida). Quando usado concomitantemente com WELLBUTRIN, pode ser necessário diminuir a dose desses substratos do CYP2D6, particularmente para medicamentos com índice terapêutico estreito.
Medicamentos que requerem ativação metabólica pelo CYP2D6 para serem eficazes (por exemplo, tamoxifeno) teoricamente podem ter eficácia reduzida quando administrados concomitantemente com inibidores do CYP2D6, como bupropiona. Pacientes tratados concomitantemente com Wellbutrin e tais medicamentos podem necessitar de doses maiores do medicamento [ver FARMACOLOGIA CLÍNICA ].
Digoxina
A coadministração de Wellbutrin com digoxina pode diminuir os níveis plasmáticos de digoxina. Monitorar os níveis plasmáticos de digoxina em pacientes tratados concomitantemente com WELLBUTRIN e digoxina [ver FARMACOLOGIA CLÍNICA ].
Medicamentos que reduzem o limiar de convulsão
Tenha extremo cuidado ao coadministrar Wellbutrin com outros medicamentos que diminuem o limiar convulsivo (por exemplo, outros produtos de bupropiona, antipsicóticos, antidepressivos, teofilina ou corticosteroides sistêmicos). Use doses iniciais baixas e aumente a dose gradualmente [ver CONTRA-INDICAÇÕES , AVISOS E PRECAUÇÕES ].
Drogas dopaminérgicas (levodopa e amantadina)
Bupropiona, levodopa e amantadina têm efeitos agonistas da dopamina. A toxicidade do SNC foi relatada quando a bupropiona foi coadministrada com levodopa ou amantadina. As reações adversas incluíram inquietação, agitação, tremor, ataxia, distúrbio da marcha, vertigem e tontura. Presume-se que a toxicidade resulte dos efeitos cumulativos dos agonistas da dopamina. Tenha cuidado ao administrar WELLBUTRIN 150mg concomitantemente com esses medicamentos.
Usar com álcool
Na experiência pós-comercialização, houve relatos raros de eventos neuropsiquiátricos adversos ou tolerância reduzida ao álcool em pacientes que ingeriram álcool durante o tratamento com Wellbutrin. O consumo de álcool durante o tratamento com WELLBUTRIN deve ser minimizado ou evitado.
Inibidores da MAO
bupropiona inibe a recaptação de dopamina e norepinefrina. O uso concomitante de IMAOs e bupropiona é contraindicado porque há um risco aumentado de reações hipertensivas se a bupropiona for usada concomitantemente com IMAOs. Estudos em animais demonstram que a toxicidade aguda da bupropiona é aumentada pelo inibidor da MAO fenelzina. Devem decorrer pelo menos 14 dias entre a descontinuação de um IMAO destinado a tratar a depressão e o início do tratamento com WELLBUTRIN. Por outro lado, pelo menos 14 dias devem ser permitidos após a interrupção de WELLBUTRIN 150mg antes de iniciar um antidepressivo IMAO [ver DOSAGEM E ADMINISTRAÇÃO , CONTRA-INDICAÇÕES ].
Interações de testes de laboratório de drogas
Testes de triagem de imunoensaio de urina falso-positivos para anfetaminas foram relatados em pacientes tomando bupropiona. Isso se deve à falta de especificidade de alguns testes de triagem. Resultados de testes falso-positivos podem ocorrer mesmo após a descontinuação da terapia com bupropiona. Testes confirmatórios, como cromatografia gasosa/espectrometria de massa, distinguirão a bupropiona das anfetaminas.
Abuso e Dependência de Drogas
Substância controlada
bupropiona não é uma substância controlada.
Abuso
Humanos
Ensaios clínicos controlados conduzidos em voluntários normais, em indivíduos com histórico de abuso de múltiplas drogas e em indivíduos deprimidos mostraram algum aumento na atividade motora e agitação/excitação, geralmente típicos da atividade estimulante central.
Em uma população de indivíduos com experiência com drogas de abuso, uma dose oral única de 400 mg de bupropiona produziu atividade semelhante à anfetamina leve em comparação com placebo na Subescala de Morfina-Benzedrina do Addiction Research Center Inventories (ARCI) e uma pontuação maior que placebo, mas menos de 15 mg do estimulante dextroanfetamina da Tabela II na Escala de Gosto do ARCI. Essas escalas medem sentimentos gerais de euforia e gosto de drogas que são frequentemente associados ao potencial de abuso.
Os achados em ensaios clínicos, no entanto, não são conhecidos para prever com segurança o potencial de abuso de drogas. No entanto, evidências de ensaios de dose única sugerem que a dose diária recomendada de bupropiona, quando administrada oralmente em doses divididas, provavelmente não reforça significativamente os usuários de anfetaminas ou estimulantes do SNC. No entanto, doses mais altas (que não podem ser testadas devido ao risco de convulsão) podem ser modestamente atraentes para aqueles que abusam de drogas estimulantes do SNC.
WELLBUTRIN destina-se apenas a uso oral. Foi relatada a inalação de comprimidos esmagados ou injeção de bupropiona dissolvida. Convulsões e/ou casos de morte foram relatados quando a bupropiona foi administrada por via intranasal ou por injeção parenteral.
Animais
Estudos em roedores e primatas demonstraram que a bupropiona apresenta algumas ações farmacológicas comuns aos psicoestimulantes. Em roedores, foi demonstrado que aumenta a atividade locomotora, provoca uma resposta comportamental estereotipada leve e aumenta as taxas de resposta em vários paradigmas de comportamento controlados pelo cronograma. Em modelos de primatas avaliando os efeitos de reforço positivo de drogas psicoativas, a bupropiona foi autoadministrada por via intravenosa. Em ratos, a bupropiona produziu efeitos de estímulo discriminativo do tipo anfetamina e cocaína em paradigmas de discriminação de drogas usados para caracterizar os efeitos subjetivos de drogas psicoativas.
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Pensamentos e Comportamentos Suicidas em Crianças, Adolescentes e Jovens Adultos
Pacientes com TDM, tanto adultos quanto pediátricos, podem apresentar piora de sua depressão e/ou surgimento de ideação e comportamento suicida (suicidalidade) ou mudanças incomuns de comportamento, estejam ou não tomando medicamentos antidepressivos, e esse risco pode persistir até que ocorre a remissão. O suicídio é um risco conhecido de depressão e alguns outros distúrbios psiquiátricos, e esses distúrbios são os mais fortes preditores de suicídio. Há uma preocupação de longa data de que os antidepressivos possam ter um papel na indução do agravamento da depressão e do surgimento de tendências suicidas em certos pacientes durante as fases iniciais do tratamento.
Análises conjuntas de ensaios de curto prazo controlados por placebo de medicamentos antidepressivos (inibidores seletivos da recaptação da serotonina [ISRSs] e outros) mostram que esses medicamentos aumentam o risco de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens (com idades de 18 anos). a 24) com TDM e outros transtornos psiquiátricos. Ensaios clínicos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução com antidepressivos em comparação com placebo em adultos com 65 anos ou mais.
As análises agrupadas de estudos controlados por placebo em crianças e adolescentes com TDM, transtorno obsessivo compulsivo (TOC) ou outros transtornos psiquiátricos incluíram um total de 24 estudos de curto prazo de 9 medicamentos antidepressivos em mais de 4.400 indivíduos. As análises agrupadas de estudos controlados por placebo em adultos com TDM ou outros transtornos psiquiátricos incluíram um total de 295 estudos de curto prazo (duração média de 2 meses) de 11 medicamentos antidepressivos em mais de 77.000 indivíduos. Houve variação considerável no risco de suicídio entre as drogas, mas uma tendência de aumento nos indivíduos mais jovens para quase todas as drogas estudadas. Houve diferenças no risco absoluto de suicídio entre as diferentes indicações, com maior incidência no TDM. As diferenças de risco (droga versus placebo), no entanto, foram relativamente estáveis dentro dos estratos de idade e entre as indicações. Essas diferenças de risco (diferença droga-placebo no número de casos de suicídio por 1.000 indivíduos tratados) são fornecidas na Tabela 1.
Nenhum suicídio ocorreu em qualquer um dos ensaios pediátricos. Houve suicídios nos ensaios com adultos, mas o número não foi suficiente para chegar a qualquer conclusão sobre o efeito da droga no suicídio.
Não se sabe se o risco de suicídio se estende ao uso a longo prazo, ou seja, além de vários meses. No entanto, há evidências substanciais de ensaios de manutenção controlados por placebo em adultos com depressão de que o uso de antidepressivos pode retardar a recorrência da depressão.
Todos os pacientes em tratamento com antidepressivos para qualquer indicação devem ser monitorados adequadamente e observados de perto quanto a piora clínica, tendências suicidas e mudanças incomuns de comportamento, especialmente durante os primeiros meses de um curso de terapia medicamentosa, ou em momentos de mudanças de dose, ou aumentos ou diminui [ver AVISO NA CAIXA].
Os seguintes sintomas, ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (agitação psicomotora), hipomania e mania, foram relatados em pacientes adultos e pediátricos em tratamento com antidepressivos para transtorno depressivo maior. quanto a outras indicações, tanto psiquiátricas como não psiquiátricas. Embora não tenha sido estabelecida uma relação causal entre o surgimento de tais sintomas e o agravamento da depressão e/ou o surgimento de impulsos suicidas, existe a preocupação de que tais sintomas possam representar precursores de tendências suicidas emergentes.
Deve-se considerar a mudança do regime terapêutico, incluindo a possibilidade de descontinuação da medicação, em pacientes cuja depressão é persistentemente pior, ou que estão experimentando tendências suicidas emergentes ou sintomas que podem ser precursores de piora da depressão ou tendências suicidas, especialmente se esses sintomas forem graves, abruptos no início, ou não faziam parte dos sintomas de apresentação do paciente.
Familiares e cuidadores de pacientes em tratamento com antidepressivos para TDM ou outras indicações, tanto psiquiátricas quanto não psiquiátricas, devem ser alertados sobre a necessidade de monitorar os pacientes quanto ao surgimento de agitação, irritabilidade, mudanças incomuns de comportamento e outros sintomas descritos acima, como bem como o surgimento de tendências suicidas, e relatar tais sintomas imediatamente aos profissionais de saúde. Tal monitoramento deve incluir observação diária por familiares e cuidadores. As prescrições de WELLBUTRIN 150mg devem ser feitas para a menor quantidade de comprimidos compatível com o bom manejo do paciente, a fim de reduzir o risco de overdose.
Eventos Adversos Neuropsiquiátricos e Risco de Suicídio no Tratamento do Tabagismo
WELLBUTRIN não está aprovado para tratamento de cessação do tabagismo; no entanto, contém o mesmo ingrediente ativo que o medicamento para parar de fumar ZYBAN. Eventos adversos neuropsiquiátricos graves foram relatados em pacientes tomando bupropiona para parar de fumar. Esses relatos pós-comercialização incluíram alterações de humor (incluindo depressão e mania), psicose, alucinações, paranóia, delírios, ideação homicida, agressão, hostilidade, agitação, ansiedade e pânico, bem como ideação suicida, tentativa de suicídio e suicídio consumado. Vejo REAÇÕES ADVERSAS ]. Alguns pacientes que pararam de fumar podem apresentar sintomas de abstinência de nicotina, incluindo humor deprimido. Depressão, raramente incluindo ideação suicida, foi relatada em fumantes submetidos a uma tentativa de parar de fumar sem medicação. No entanto, alguns desses eventos adversos ocorreram em pacientes em uso de bupropiona que continuaram a fumar.
Eventos adversos neuropsiquiátricos ocorreram em pacientes sem e com doença psiquiátrica pré-existente; alguns pacientes experimentaram o agravamento de suas doenças psiquiátricas. Observar os pacientes quanto à ocorrência de eventos adversos neuropsiquiátricos. Aconselhar os pacientes e cuidadores de que o paciente deve parar de tomar Wellbutrin 300mg e entrar em contato com um profissional de saúde imediatamente se forem observadas agitação, humor deprimido ou alterações no comportamento ou pensamento que não sejam típicos do paciente, ou se o paciente desenvolver ideação ou comportamento suicida . Em muitos casos pós-comercialização, foi relatada a resolução dos sintomas após a descontinuação da bupropiona. No entanto, os sintomas persistiram em alguns casos; portanto, monitoramento contínuo e cuidados de suporte devem ser fornecidos até que os sintomas desapareçam.
Apreensão
WELLBUTRIN 300mg pode causar convulsões. O risco de convulsão está relacionado à dose. A dose não deve exceder 450 mg/dia. Aumente a dose gradualmente. Interrompa WELLBUTRIN 150mg e não reinicie o tratamento se o paciente apresentar uma convulsão.
O risco de convulsões também está relacionado a fatores do paciente, situações clínicas e medicamentos concomitantes que diminuem o limiar convulsivo. Considere estes riscos antes de iniciar o tratamento com WELLBUTRIN. WELLBUTRIN 300mg é contraindicado em pacientes com transtorno convulsivo, diagnóstico atual ou anterior de anorexia nervosa ou bulimia, ou submetidos a descontinuação abrupta de álcool, benzodiazepínicos, barbitúricos e drogas antiepilépticas. CONTRA-INDICAÇÕES , INTERAÇÕES MEDICAMENTOSAS ]. As seguintes condições também podem aumentar o risco de convulsão: traumatismo craniano grave; malformação arteriovenosa; Tumor do SNC ou infecção do SNC; acidente vascular cerebral grave; uso concomitante de outros medicamentos que diminuem o limiar convulsivo (por exemplo, outros produtos de bupropiona, antipsicóticos, antidepressivos tricíclicos, teofilina e corticosteroides sistêmicos); distúrbios metabólicos (por exemplo, hipoglicemia, hiponatremia, insuficiência hepática grave e hipóxia); uso de drogas ilícitas (por exemplo, cocaína); ou abuso ou uso indevido de medicamentos prescritos, como estimulantes do SNC. Condições predisponentes adicionais incluem diabetes mellitus tratada com hipoglicemiantes orais ou insulina; uso de anorexígenos; e uso excessivo de álcool, benzodiazepínicos, sedativos/hipnóticos ou opiáceos.
Incidência de convulsão com uso de bupropiona
bupropiona está associada a convulsões em aproximadamente 0,4% (4/1.000) dos pacientes tratados com doses de até 450 mg/dia. A incidência estimada de convulsões para WELLBUTRIN aumenta quase 10 vezes entre 450 e 600 mg/dia.
O risco de convulsão pode ser reduzido se a dose de WELLBUTRIN 300mg não exceder 450mg/dia, administrada em 150mg 3 vezes ao dia, e a taxa de titulação for gradual.
Hipertensão
O tratamento com WELLBUTRIN pode resultar em pressão arterial elevada e hipertensão. Avalie a pressão arterial antes de iniciar o tratamento com WELLBUTRIN 150mg e monitore periodicamente durante o tratamento. O risco de hipertensão aumenta se WELLBUTRIN 150mg for usado concomitantemente com IMAOs ou outros medicamentos que aumentam a atividade dopaminérgica ou noradrenérgica [ver CONTRA-INDICAÇÕES ].
Dados de um estudo comparativo da formulação de liberação sustentada de bupropiona HCl, sistema transdérmico de nicotina (NTS), a combinação de bupropiona de liberação sustentada mais NTS e placebo como auxílio para a cessação do tabagismo sugerem uma maior incidência de hipertensão emergente do tratamento em pacientes tratados com a combinação de bupropiona de liberação sustentada e NTS. Neste estudo, 6,1% dos indivíduos tratados com a combinação de bupropiona de liberação sustentada e NTS apresentaram hipertensão emergente do tratamento em comparação com 2,5%, 1,6% e 3,1% dos indivíduos tratados com bupropiona de liberação sustentada, NTS e placebo, respectivamente . A maioria desses indivíduos tinha evidência de hipertensão pré-existente. Três indivíduos (1,2%) tratados com a combinação de bupropiona de liberação sustentada e NTS e 1 sujeito (0,4%) tratado com NTS tiveram a medicação do estudo descontinuada devido à hipertensão em comparação com nenhum dos indivíduos tratados com bupropiona de liberação sustentada ou placebo. A monitorização da pressão arterial é recomendada em pacientes que recebem a combinação de bupropiona e reposição de nicotina.
Em um ensaio clínico de liberação imediata de bupropiona em indivíduos com MDD com insuficiência cardíaca congestiva estável (N = 36), a bupropiona foi associada a uma exacerbação de hipertensão pré-existente em 2 indivíduos, levando à descontinuação do tratamento com bupropiona. Não há estudos controlados que avaliem a segurança da bupropiona em pacientes com história recente de infarto do miocárdio ou doença cardíaca instável.
Ativação de mania/hipomania
O tratamento antidepressivo pode precipitar um episódio maníaco, misto ou hipomaníaco. O risco parece estar aumentado em pacientes com transtorno bipolar ou que têm fatores de risco para transtorno bipolar. Antes de iniciar WELLBUTRIN, rastreie os pacientes para uma história de transtorno bipolar e a presença de fatores de risco para transtorno bipolar (por exemplo, história familiar de transtorno bipolar, suicídio ou depressão). WELLBUTRIN 150mg não é aprovado para uso no tratamento da depressão bipolar.
Psicose e outras reações neuropsiquiátricas
Pacientes deprimidos tratados com Wellbutrin apresentaram uma variedade de sinais e sintomas neuropsiquiátricos, incluindo delírios, alucinações, psicose, distúrbios de concentração, paranóia e confusão. Alguns desses pacientes tinham diagnóstico de transtorno bipolar. Em alguns casos, esses sintomas diminuíram com a redução da dose e/ou retirada do tratamento. Instrua os pacientes a entrar em contato com um profissional de saúde se ocorrerem tais reações.
Glaucoma de ângulo fechado
A dilatação pupilar que ocorre após o uso de muitos medicamentos antidepressivos, incluindo WELLBUTRIN 300mg, pode desencadear um ataque de fechamento angular em um paciente com ângulos anatomicamente estreitos que não tenha uma iridectomia patente.
Reações de hipersensibilidade
Reações anafilactóides/anafiláticas ocorreram durante os estudos clínicos com bupropiona. As reações têm sido caracterizadas por prurido, urticária, angioedema e dispneia que requerem tratamento médico. Além disso, houve relatos pós-comercialização raros e espontâneos de eritema multiforme, síndrome de Stevens-Johnson e choque anafilático associado à bupropiona. Instrua os pacientes a descontinuar WELLBUTRIN 150mg e consultar um profissional de saúde se desenvolverem uma reação alérgica ou anafilactóide/anafilática (por exemplo, erupção cutânea, prurido, urticária, dor no peito, edema e falta de ar) durante o tratamento.
Existem relatos de artralgia, mialgia, febre com erupção cutânea e outros sintomas semelhantes à doença do soro sugestivos de hipersensibilidade tardia.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( Guia de Medicação ).
Pensamentos e Comportamentos Suicidas
Orientar os pacientes, seus familiares e/ou seus cuidadores a estarem alertas para o surgimento de ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (inquietação psicomotora), hipomania, mania, outras alterações incomuns de comportamento , agravamento da depressão e ideação suicida, especialmente no início do tratamento antidepressivo e quando a dose é ajustada para cima ou para baixo. Aconselhar familiares e cuidadores de pacientes a observar o surgimento de tais sintomas no dia a dia, pois as alterações podem ser abruptas. Esses sintomas devem ser relatados ao prescritor ou profissional de saúde do paciente, especialmente se forem graves, de início abrupto ou não fizerem parte dos sintomas apresentados pelo paciente. Sintomas como esses podem estar associados a um risco aumentado de pensamento e comportamento suicida e indicam a necessidade de monitoramento muito próximo e possivelmente mudanças na medicação.
Eventos Adversos Neuropsiquiátricos e Risco de Suicídio no Tratamento do Tabagismo
Embora WELLBUTRIN 150mg não seja indicado para o tratamento da cessação do tabagismo, contém o mesmo ingrediente ativo do ZYBAN, aprovado para esse uso. Informar aos pacientes que alguns pacientes experimentaram mudanças de humor (incluindo depressão e mania), psicose, alucinações, paranóia, delírios, ideação homicida, agressão, hostilidade, agitação, ansiedade e pânico, bem como ideação suicida e suicídio ao tentar parar de fumar fumar enquanto estiver a tomar bupropiona. Instruir os pacientes a descontinuar a bupropiona e entrar em contato com um profissional de saúde se apresentarem tais sintomas [ver AVISOS E PRECAUÇÕES , REAÇÕES ADVERSAS ].
Reações alérgicas graves
Educar os pacientes sobre os sintomas de hipersensibilidade e descontinuar WELLBUTRIN 300mg se tiverem uma reação alérgica grave.
Apreensão
Instrua os pacientes a descontinuar e não reiniciar WELLBUTRIN se apresentarem uma convulsão durante o tratamento. Aconselhe os pacientes que o uso excessivo ou a interrupção abrupta de álcool, benzodiazepínicos, drogas antiepilépticas ou sedativos/hipnóticos podem aumentar o risco de convulsão. Aconselhar os pacientes a minimizar ou evitar o uso de álcool.
Glaucoma de ângulo fechado
Os pacientes devem ser avisados de que tomar Wellbutrin 150mg pode causar dilatação pupilar leve, que em indivíduos suscetíveis, pode levar a um episódio de glaucoma de ângulo fechado. O glaucoma pré-existente é quase sempre o glaucoma de ângulo aberto porque o glaucoma de ângulo fechado, quando diagnosticado, pode ser tratado definitivamente com iridectomia. O glaucoma de ângulo aberto não é um fator de risco para o glaucoma de ângulo fechado. Os pacientes podem querer ser examinados para determinar se são suscetíveis ao fechamento do ângulo e realizar um procedimento profilático (por exemplo, iridectomia), se forem suscetíveis [ver AVISOS E PRECAUÇÕES ].
Produtos contendo bupropiona
Eduque os pacientes que WELLBUTRIN 150mg contém o mesmo ingrediente ativo (cloridrato de bupropiona) encontrado em ZYBAN, que é usado como auxiliar no tratamento de cessação do tabagismo, e que WELLBUTRIN 150mg não deve ser usado em combinação com ZYBAN ou qualquer outro medicamento que contenha bupropiona (como como WELLBUTRIN 150mg SR, a formulação de liberação prolongada e WELLBUTRIN XL ou FORFIVO XL, as formulações de liberação prolongada e APLENZIN, a formulação de liberação prolongada de bromidrato de bupropiona). Além disso, existem vários produtos genéricos de bupropiona HCl para as formulações de liberação imediata, prolongada e prolongada.
Potencial para comprometimento cognitivo e motor
Aconselhe os pacientes que qualquer droga ativa no SNC, como WELLBUTRIN, pode prejudicar sua capacidade de realizar tarefas que exijam julgamento ou habilidades motoras e cognitivas. Aconselhe os pacientes que, até que estejam razoavelmente certos de que WELLBUTRIN 300mg não afeta adversamente seu desempenho, eles devem se abster de dirigir automóveis ou operar máquinas complexas e perigosas. WELLBUTRIN 150mg pode levar à diminuição da tolerância ao álcool.
Medicamentos Concomitantes
Aconselhe os pacientes a notificar seu médico se estiverem tomando ou planejam tomar algum medicamento prescrito ou de venda livre, pois WELLBUTRIN 150mg e outros medicamentos podem afetar o metabolismo uns dos outros.
Gravidez
Aconselhe as pacientes a notificarem seu médico se engravidarem ou pretendem engravidar durante o tratamento com WELLBUTRIN. Aconselhe as pacientes que existe um registro de exposição na gravidez que monitora os resultados da gravidez em mulheres expostas a WELLBUTRIN 150mg durante a gravidez [ver Uso em populações específicas ].
Informações de armazenamento
Instrua os pacientes a armazenar WELLBUTRIN à temperatura ambiente, entre 20°C a 25°C (68°F e 77°F) e manter os comprimidos secos e protegidos da luz.
Informações de administração
Instrua os pacientes a tomar WELLBUTRIN em doses igualmente divididas 3 ou 4 vezes ao dia, com doses separadas por pelo menos 6 horas para minimizar o risco de convulsão. Instrua os pacientes, caso percam uma dose, a não tomar um comprimido extra para compensar a dose esquecida e a tomar o próximo comprimido no horário regular devido ao risco de convulsão relacionado à dose. Instrua os pacientes que os comprimidos de Wellbutrin devem ser engolidos inteiros e não esmagados, divididos ou mastigados. WELLBUTRIN pode ser tomado com ou sem alimentos.
WELLBUTRIN, WELLBUTRIN SR, WELLBUTRIN 150mg XL e ZYBAN são marcas registradas de propriedade ou licenciadas para o grupo de empresas GSK. As outras marcas listadas são marcas registradas de propriedade ou licenciadas para seus respectivos proprietários e não são de propriedade ou licenciadas para o grupo de empresas GSK. Os fabricantes dessas marcas não são afiliados e não endossam o grupo de empresas GSK ou seus produtos.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Estudos de carcinogenicidade ao longo da vida foram realizados em ratos e camundongos com doses de bupropiona de até 300 e 150 mg/kg/dia, respectivamente. Essas doses são aproximadamente 6 e 2 vezes a MRHD, respectivamente, na base de mg/m2. No estudo em ratos houve um aumento nas lesões proliferativas nodulares do fígado em doses de 100 a 300 mg/kg/dia (aproximadamente 2 a 6 vezes a MRHD em uma base de mg/m2); doses mais baixas não foram testadas. A questão de saber se tais lesões podem ou não ser precursoras de neoplasias do fígado ainda não está resolvida. Lesões hepáticas semelhantes não foram observadas no estudo com camundongos, e nenhum aumento nos tumores malignos do fígado e de outros órgãos foi observado em nenhum dos estudos.
A bupropiona produziu uma resposta positiva (2 a 3 vezes a taxa de mutação de controle) em 2 de 5 cepas no ensaio de mutagenicidade bacteriana de Ames. A bupropiona produziu um aumento nas aberrações cromossômicas em 1 de 3 estudos citogenéticos de medula óssea de ratos in vivo.
Não houve efeitos na fertilidade de machos e fêmeas quando os ratos receberam doses orais de bupropiona de até 300 mg/kg/dia (aproximadamente 6 vezes o MRHD em uma base de mg/m2) a fêmeas antes do acasalamento e até o dia 13 de gestação ou durante a lactação, e aos machos por 60 dias antes e durante o acasalamento. No entanto, doses de 200 mg/kg/dia (aproximadamente 4 vezes o MRHD em uma base de mg/m2) ou superiores, causaram ataxia transitória ou alterações comportamentais em ratas adultas. Também não houve efeitos adversos na fertilidade, reprodução ou crescimento e desenvolvimento da prole masculina ou feminina.
Uso em populações específicas
Gravidez
Registro de Exposição à Gravidez
Existe um registro independente de exposição à gravidez que monitora os resultados da gravidez em mulheres expostas a quaisquer antidepressivos durante a gravidez. Os profissionais de saúde são incentivados a registrar pacientes ligando para o National Pregnancy Registry for Antidepressants em 1-844-4056185 ou acessando on-line em https://womensmentalhealth.org/clinical-and-researchprograms/pregnancyregistry/antidepressants.
Resumo do risco
Dados de estudos epidemiológicos de mulheres grávidas expostas à bupropiona no primeiro trimestre não identificaram um risco aumentado de malformações congênitas em geral (ver Dados ). Existem riscos para a mãe associados à depressão não tratada na gravidez (ver Considerações Clínicas ). Quando a bupropiona foi administrada a ratas grávidas durante a organogênese, não houve evidência de malformações fetais em doses até aproximadamente 10 vezes a dose humana máxima recomendada (MRHD) de 450 mg/dia. Quando administrado a coelhas grávidas durante a organogénese, foram observados aumentos não relacionados com a dose na incidência de malformações fetais e variações esqueléticas em doses aproximadamente iguais à MRHD e superiores. Pesos fetais diminuídos foram observados em doses duas vezes maiores que a MRHD (ver Dados de animais ).
risco de base estimado para defeitos congênitos graves e aborto é desconhecido para a população indicada. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e de aborto espontâneo em gestações clinicamente reconhecidas é de 2% a 4% e 15% a 20%, respectivamente.
Considerações Clínicas
Risco Materno e/ou Embrião/Fetal Associado à Doença
Um estudo prospectivo e longitudinal acompanhou 201 gestantes com histórico de transtorno depressivo maior eutímicas e em uso de antidepressivos durante a gravidez no início da gravidez. As mulheres que descontinuaram os antidepressivos durante a gravidez eram mais propensas a ter uma recaída de depressão maior do que as mulheres que continuaram os antidepressivos. Considere os riscos para a mãe de depressão não tratada e os efeitos potenciais sobre o feto ao interromper ou alterar o tratamento com medicamentos antidepressivos durante a gravidez e pós-parto.
Dados
Dados humanos
Dados do registro internacional de gravidez de bupropiona (675 exposições no primeiro trimestre) e um estudo de coorte retrospectivo usando o banco de dados United Healthcare (1.213 exposições no primeiro trimestre) não mostraram um risco aumentado de malformações em geral. O Registro não foi projetado ou desenvolvido para avaliar defeitos específicos, mas sugeriu um possível aumento de malformações cardíacas.
Não foi observado aumento do risco de malformações cardiovasculares em geral após a exposição à bupropiona durante o primeiro trimestre. A taxa de malformações cardiovasculares observada prospectivamente em gestações com exposição à bupropiona no primeiro trimestre do Registro Internacional de Gravidez foi de 1,3% (9 malformações cardiovasculares/675 exposições maternas à bupropiona no primeiro trimestre), que é semelhante à taxa de fundo de malformações cardiovasculares (aproximadamente 1%). Dados do banco de dados United Healthcare, que teve um número limitado de casos expostos com malformações cardiovasculares, e um estudo caso-controle (6.853 bebês com malformações cardiovasculares e 5.763 com malformações não cardiovasculares) de uso autorrelatado de bupropiona do National Birth Defects O Estudo de Prevenção (NBDPS) não mostrou um risco aumentado de malformações cardiovasculares em geral após a exposição à bupropiona durante o primeiro trimestre.
Os achados do estudo sobre a exposição à bupropiona durante o primeiro trimestre e o risco de obstrução da via de saída do ventrículo esquerdo (OTVE) são inconsistentes e não permitem conclusões sobre uma possível associação. O banco de dados da United Healthcare não tinha poder suficiente para avaliar essa associação; o NBDPS encontrou risco aumentado para OVE (n = 10; OR ajustado = 2,6; IC 95%: 1,2, 5,7), e o estudo caso-controle Slone Epidemiology não encontrou risco aumentado para OVE.
Os achados do estudo sobre exposição à bupropiona durante o primeiro trimestre e risco de comunicação interventricular (CIV) são inconsistentes e não permitem conclusões sobre uma possível associação. O Slone Epidemiology Study encontrou um risco aumentado para CIV após a exposição materna à bupropiona no primeiro trimestre (n = 17; OR ajustado = 2,5; IC 95%: 1,3, 5,0), mas não encontrou risco aumentado para quaisquer outras malformações cardiovasculares estudadas (incluindo LVOTO como acima de). O estudo de banco de dados NBDPS e United Healthcare não encontrou uma associação entre a exposição materna à bupropiona no primeiro trimestre e o CIV.
Para os achados de LVOTO e CIV, os estudos foram limitados pelo pequeno número de casos expostos, achados inconsistentes entre os estudos e o potencial de achados casuais de comparações múltiplas em estudos de caso-controle.
Dados de animais
Em estudos realizados em ratas e coelhas grávidas, a bupropiona foi administrada por via oral durante o período de organogênese em doses de até 450 e 150 mg/kg/dia, respectivamente (aproximadamente 10 e 6 vezes a MRHD, respectivamente, na base de mg/m2 ). Não houve evidência de malformações fetais em ratos. Quando administrado a coelhas grávidas durante a organogênese, foram observados aumentos não relacionados à dose na incidência de malformações fetais e variações esqueléticas na dose mais baixa testada (25 mg/kg/dia, aproximadamente igual ao MRHD em uma base de mg/m2) e maior. Pesos fetais diminuídos foram observados em doses de 50 mg/kg/dia (aproximadamente 2 vezes a MRHD em uma base de mg/m2) e maiores. Nenhuma toxicidade materna foi evidente em doses de 50 mg/kg/dia ou menos.
Em um estudo de desenvolvimento pré e pós-natal, a bupropiona administrada oralmente a ratas grávidas em doses de até 150 mg/kg/dia (aproximadamente 3 vezes a MRHD em uma base de mg/m2) desde a implantação embrionária até a lactação não teve efeito no crescimento dos filhotes ou desenvolvimento.
Lactação
Resumo do risco
Dados da literatura publicada relatam a presença de bupropiona e seus metabólitos no leite humano (ver Dados ). Não há dados sobre os efeitos da bupropiona ou de seus metabólitos na produção de leite. Dados limitados de relatórios pós-comercialização não identificaram uma associação clara de reações adversas no lactente amamentado. Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica de WELLBUTRIN da mãe e quaisquer efeitos adversos potenciais do WELLBUTRIN na criança amamentada ou da condição materna subjacente.
Dados
Em um estudo de lactação com 10 mulheres, os níveis de bupropiona administrada por via oral e seus metabólitos ativos foram medidos no leite ordenhado. A exposição média diária infantil (assumindo 150 mL/kg de consumo diário) à bupropiona e seus metabólitos ativos foi de 2% da dose materna ajustada ao peso. Relatos pós-comercialização descreveram convulsões em lactentes amamentados. A relação da exposição à bupropiona e essas convulsões não é clara.
Uso Pediátrico
A segurança e a eficácia na população pediátrica não foram estabelecidas [ver AVISO EM CAIXA , AVISOS E PRECAUÇÕES ].
Uso Geriátrico
Dos aproximadamente 6.000 indivíduos que participaram de ensaios clínicos com bupropiona comprimidos de liberação prolongada (ensaios de depressão e cessação do tabagismo), 275 tinham idade ≥65 anos e 47 tinham idade ≥75 anos. Além disso, várias centenas de indivíduos com idade ≥65 anos participaram de ensaios clínicos usando a formulação de liberação imediata de bupropiona (ensaios de depressão). Não foram observadas diferenças globais na segurança ou eficácia entre estes indivíduos e indivíduos mais jovens. A experiência clínica relatada não identificou diferenças nas respostas entre idosos e pacientes mais jovens, mas não se pode descartar uma maior sensibilidade de alguns indivíduos mais velhos.
bupropiona é extensivamente metabolizada no fígado em metabólitos ativos, que são posteriormente metabolizados e excretados pelos rins. O risco de reações adversas pode ser maior em pacientes com insuficiência renal. Como os pacientes idosos são mais propensos a ter função renal diminuída, pode ser necessário considerar esse fator na seleção da dose; pode ser útil monitorar a função renal [ver DOSAGEM E ADMINISTRAÇÃO , Uso em populações específicas , FARMACOLOGIA CLÍNICA ].
Insuficiência renal
Considere uma dose e/ou frequência de dosagem reduzida de Wellbutrin em pacientes com insuficiência renal (Taxa de filtração glomerular: inferior a 90 mL/min). A bupropiona e seus metabólitos são eliminados por via renal e podem se acumular nesses pacientes em maior extensão do que o habitual. Monitore atentamente as reações adversas que possam indicar altas exposições de bupropiona ou metabólitos [ver DOSAGEM E ADMINISTRAÇÃO , FARMACOLOGIA CLÍNICA ].
Insuficiência hepática
Em pacientes com insuficiência hepática moderada a grave (pontuação de Child-Pugh: 7 a 15), a dose máxima de WELLBUTRIN 150mg é de 75mg ao dia. Em pacientes com insuficiência hepática leve (pontuação de Child-Pugh: 5 a 6), considere reduzir a dose e/ou frequência de dosagem [ver DOSAGEM E ADMINISTRAÇÃO , FARMACOLOGIA CLÍNICA ].
SOBREDOSAGEM
Experiência de overdose humana
Foram relatadas overdoses de até 30 gramas ou mais de bupropiona. A convulsão foi relatada em aproximadamente um terço de todos os casos. Outras reações graves relatadas com superdosagem de bupropiona isoladamente incluíram alucinações, perda de consciência, taquicardia sinusal e alterações no ECG, como distúrbios de condução (incluindo prolongamento do QRS) ou arritmias. Febre, rigidez muscular, rabdomiólise, hipotensão, estupor, coma e insuficiência respiratória foram relatados principalmente quando a bupropiona fazia parte de múltiplas superdosagens de medicamentos.
Embora a maioria dos pacientes tenha se recuperado sem sequelas, foram relatadas mortes associadas a overdoses de bupropiona isoladamente em pacientes que ingeriram grandes doses da droga. Múltiplas convulsões não controladas, bradicardia, insuficiência cardíaca e parada cardíaca antes da morte foram relatados nesses pacientes.
Gerenciamento de superdosagem
Consulte um Centro de Controle de Intoxicações Certificado para obter orientações e conselhos atualizados. Os números de telefone dos centros de controle de intoxicação certificados estão listados no Physician's Desk Reference (PDR). Ligue para 1-800-222-1222 ou consulte www.poison.org.
Não existem antídotos conhecidos para a bupropiona. Em caso de superdosagem, forneça cuidados de suporte, incluindo supervisão médica e monitoramento. Considere a possibilidade de overdose de drogas múltiplas. Assegurar vias aéreas, oxigenação e ventilação adequadas. Monitorar o ritmo cardíaco e os sinais vitais. A indução de vômito não é recomendada.
CONTRA-INDICAÇÕES
- WELLBUTRIN 150mg é contraindicado em pacientes com distúrbios convulsivos.
- WELLBUTRIN é contraindicado em pacientes com diagnóstico atual ou prévio de bulimia ou anorexia nervosa, pois foi observada uma incidência mais alta de convulsões nesses pacientes tratados com WELLBUTRIN [ver AVISOS E PRECAUÇÕES ].
- WELLBUTRIN 300mg é contraindicado em pacientes submetidos a descontinuação abrupta de álcool, benzodiazepínicos, barbitúricos e drogas antiepilépticas. AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS ].
- O uso de IMAOs (destinados a tratar distúrbios psiquiátricos) concomitantemente com WELLBUTRIN 300mg ou dentro de 14 dias após a interrupção do tratamento com WELLBUTRIN 150mg é contraindicado. Há um risco aumentado de reações hipertensivas quando Wellbutrin é usado concomitantemente com IMAOs. O uso de WELLBUTRIN dentro de 14 dias após a interrupção do tratamento com um IMAO também é contraindicado. Iniciar WELLBUTRIN 150mg em um paciente tratado com IMAOs reversíveis, como linezolida ou azul de metileno intravenoso, é contraindicado [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS ].
- WELLBUTRIN é contraindicado em pacientes com hipersensibilidade conhecida à bupropiona ou a outros componentes de WELLBUTRIN. Reações anafilactóides/anafiláticas e síndrome de Stevens-Johnson foram relatadas [ver AVISOS E PRECAUÇÕES ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
O mecanismo exato da ação antidepressiva da bupropiona não é conhecido, mas presume-se que esteja relacionado a mecanismos noradrenérgicos e/ou dopaminérgicos. A bupropiona é um inibidor relativamente fraco da recaptação neuronal de norepinefrina e dopamina e não inibe a recaptação de serotonina. A bupropiona não inibe a monoamina oxidase.
Farmacocinética
A bupropiona é uma mistura racêmica. A atividade farmacológica e a farmacocinética dos enantiômeros individuais não foram estudadas. A meia-vida média de eliminação (±DP) da bupropiona após administração crônica é de 21 (±9) horas, e as concentrações plasmáticas de bupropiona no estado de equilíbrio são atingidas em 8 dias.
Absorção
biodisponibilidade absoluta de WELLBUTRIN em humanos não foi determinada porque uma formulação intravenosa para uso humano não está disponível. No entanto, parece provável que apenas uma pequena proporção de qualquer dose administrada por via oral atinja a circulação sistêmica intacta. Em estudos com ratos e cães, a biodisponibilidade da bupropiona variou de 5% a 20%.
Em humanos, após a administração oral de WELLBUTRIN 300mg, as concentrações plasmáticas máximas de bupropiona são geralmente alcançadas em 2 horas. As concentrações plasmáticas de bupropiona são proporcionais à dose após doses únicas de 100 a 250 mg; entretanto, não se sabe se a proporcionalidade entre a dose e o nível plasmático é mantida no uso crônico.
Distribuição
Testes in vitro mostram que a bupropiona está 84% ligada às proteínas plasmáticas humanas em concentrações de até 200 mcg/mL. A extensão da ligação proteica do metabólito hidroxibupropiona é semelhante à da bupropiona, enquanto a extensão da ligação proteica do metabólito treohidrobupropiona é cerca de metade daquela observada com a bupropiona.
Metabolismo
bupropiona é extensivamente metabolizada em humanos. Três metabólitos são ativos: hidroxibupropiona, que é formada por hidroxilação do grupo terc-butil da bupropiona, e os isômeros de aminoálcool treohidrobupropiona e eritrohidrobupropiona, que são formados por redução do grupo carbonila. Os achados in vitro sugerem que a CYP2B6 é a principal isoenzima envolvida na formação da hidroxibupropiona, enquanto as enzimas do citocromo P450 não estão envolvidas na formação da treohidrobupropiona. A oxidação da cadeia lateral da bupropiona resulta na formação de um conjugado de glicina do ácido metaclorobenzóico, que é então excretado como o principal metabólito urinário. A potência e toxicidade dos metabólitos em relação à bupropiona não foram totalmente caracterizadas. No entanto, foi demonstrado em um teste de triagem de antidepressivos em camundongos que a hidroxibupropiona é metade da potência da bupropiona, enquanto a treohidrobupropiona e a eritrohidrobupropiona são 5 vezes menos potentes que a bupropiona. Isso pode ser de importância clínica porque as concentrações plasmáticas dos metabólitos são tão altas ou superiores às da bupropiona.
Após uma dose única em humanos, as concentrações plasmáticas máximas de hidroxibupropiona ocorrem aproximadamente 3 horas após a administração de Wellbutrin e são aproximadamente 10 vezes o nível máximo do medicamento original no estado de equilíbrio. A meia-vida de eliminação da hidroxibupropiona é de aproximadamente 20 (± 5) horas, e sua AUC no estado de equilíbrio é cerca de 17 vezes a da bupropiona. Os tempos de pico das concentrações dos metabólitos eritrohidrobupropiona e treohidrobupropiona são semelhantes aos do metabólito hidroxibupropiona. No entanto, suas meias-vidas de eliminação são mais longas, 33 (±10) e 37 (±13) horas, respectivamente, e as AUCs no estado de equilíbrio são 1,5 e 7 vezes maiores que a da bupropiona, respectivamente.
A bupropiona e seus metabólitos exibem cinética linear após administração crônica de 300 a 450 mg/dia.
Eliminação
Após a administração oral de 200 mg de 14C-bupropiona em humanos, 87% e 10% da dose radioativa foi recuperada na urina e nas fezes, respectivamente. Apenas 0,5% da dose oral foi excretada como bupropiona inalterada.
Populações Específicas
Fatores ou condições que alteram a capacidade metabólica (por exemplo, doença hepática, insuficiência cardíaca congestiva [ICC], idade, medicamentos concomitantes, etc.) ou eliminação podem influenciar o grau e extensão do acúmulo dos metabólitos ativos da bupropiona. A eliminação dos principais metabólitos da bupropiona pode ser afetada pela redução da função renal ou hepática porque são compostos moderadamente polares e provavelmente sofrerão mais metabolismo ou conjugação no fígado antes da excreção urinária.
Pacientes com Insuficiência Renal
Há informações limitadas sobre a farmacocinética da bupropiona em pacientes com insuficiência renal. Uma comparação inter-ensaios entre indivíduos normais e indivíduos com insuficiência renal em estágio terminal demonstrou que os valores de Cmax e AUC do medicamento original foram comparáveis nos 2 grupos, enquanto os metabólitos de hidroxibupropiona e treohidrobupropiona tiveram um aumento de 2,3 e 2,8 vezes, respectivamente, na AUC para indivíduos com insuficiência renal terminal. Um segundo estudo, comparando indivíduos normais e indivíduos com insuficiência renal moderada a grave (TFG 30,9 ± 10,8 mL/min) mostrou que após uma dose única de 150 mg de bupropiona de liberação sustentada, a exposição à bupropiona foi aproximadamente 2 vezes maior em indivíduos com função renal comprometida, enquanto os níveis dos metabólitos de hidroxibupropiona e treo/eritrohidrobupropiona (combinados) foram semelhantes nos 2 grupos. A bupropiona é extensivamente metabolizada no fígado em metabólitos ativos, que são posteriormente metabolizados e subsequentemente excretados pelos rins. A eliminação dos principais metabólitos da bupropiona pode ser reduzida pelo comprometimento da função renal. WELLBUTRIN deve ser usado com cautela em pacientes com insuficiência renal e uma frequência e/ou dose reduzidas devem ser consideradas. Uso em populações específicas ].
Pacientes com Insuficiência Hepática
efeito da insuficiência hepática na farmacocinética da bupropiona foi caracterizado em 2 ensaios de dose única, um em indivíduos com doença hepática alcoólica e outro em indivíduos com cirrose leve a grave. O primeiro estudo demonstrou que a meia-vida da hidroxibupropiona foi significativamente maior em 8 indivíduos com doença hepática alcoólica do que em 8 voluntários saudáveis (32 ± 14 horas versus 21 ± 5 horas, respectivamente). Embora não estatisticamente significativo, as AUCs para bupropiona e hidroxibupropiona foram mais variáveis e tenderam a ser maiores (de 53% a 57%) em voluntários com doença hepática alcoólica. As diferenças na meia-vida da bupropiona e dos outros metabólitos nos 2 grupos foram mínimas.
segundo ensaio não demonstrou diferenças estatisticamente significativas na farmacocinética da bupropiona e seus metabólitos ativos em 9 indivíduos com cirrose hepática leve a moderada em comparação com 8 voluntários saudáveis. No entanto, foi observada mais variabilidade em alguns dos parâmetros farmacocinéticos da bupropiona (AUC, Cmax e Tmax) e seus metabólitos ativos (t½) em indivíduos com cirrose hepática leve a moderada. Em indivíduos com cirrose hepática grave, foram observadas alterações significativas na farmacocinética da bupropiona e seus metabólitos (Tabela 3).
Pacientes com Disfunção Ventricular Esquerda
Durante um ensaio de dosagem crônica com bupropiona em 14 indivíduos deprimidos com disfunção ventricular esquerda (história de ICC ou aumento do coração na radiografia), não houve efeito aparente na farmacocinética da bupropiona ou de seus metabólitos, em comparação com voluntários saudáveis.
Era
Os efeitos da idade sobre a farmacocinética da bupropiona e seus metabólitos não foram totalmente caracterizados, mas uma exploração das concentrações de bupropiona no estado de equilíbrio de vários ensaios de eficácia da depressão envolvendo indivíduos com doses de 300 a 750 mg/dia, em uma dose de 3- horários diários, não revelou relação entre idade (18 a 83 anos) e concentração plasmática de bupropiona. Um ensaio farmacocinético de dose única demonstrou que a disposição da bupropiona e seus metabólitos em indivíduos idosos foi semelhante à de indivíduos mais jovens. Esses dados sugerem que não há efeito proeminente da idade na concentração de bupropiona; no entanto, outro estudo farmacocinético de dose única e múltipla sugeriu que os idosos apresentam risco aumentado de acúmulo de bupropiona e seus metabólitos [ver Uso em populações específicas ].
Pacientes Masculinos e Femininos
análise conjunta dos dados farmacocinéticos da bupropiona de 90 voluntários saudáveis do sexo masculino e 90 saudáveis do sexo feminino não revelou diferenças relacionadas ao sexo nas concentrações plasmáticas máximas de bupropiona. A exposição sistêmica média (AUC) foi aproximadamente 13% maior em voluntários do sexo masculino em comparação com voluntários do sexo feminino. O significado clínico deste achado é desconhecido.
Fumantes
Os efeitos do tabagismo na farmacocinética da bupropiona foram estudados em 34 voluntários saudáveis do sexo masculino e feminino; 17 eram tabagistas crônicos e 17 não tabagistas. Após a administração oral de uma dose única de 150 mg de bupropiona, não houve diferenças estatisticamente significativas na Cmax, meia-vida, Tmax, AUC ou depuração da bupropiona ou seus metabólitos ativos entre fumantes e não fumantes.
Estudos de interação medicamentosa
Potencial para outros medicamentos afetarem WELLBUTRIN
Estudos in vitro indicam que a bupropiona é metabolizada principalmente em hidroxibupropiona pelo CYP2B6. Portanto, existe o potencial de interações medicamentosas entre WELLBUTRIN e medicamentos que são inibidores ou indutores de CYP2B6. Além disso, estudos in vitro sugerem que paroxetina, sertralina, norfluoxetina, fluvoxamina e nelfinavir inibem a hidroxilação da bupropiona.
Inibidores de CYP2B6
Ticlopidina, Clopidogrel: Em um estudo em voluntários saudáveis do sexo masculino, clopidogrel 75 mg uma vez ao dia ou ticlopidina 250 mg duas vezes ao dia aumentaram as exposições (Cmax e AUC) de bupropiona em 40% e 60% para clopidogrel, e em 38% e 85% para ticlopidina , respectivamente. As exposições (Cmax e AUC) da hidroxibupropiona foram reduzidas em 50% e 52%, respectivamente, pelo clopidogrel, e 78% e 84%, respectivamente, pela ticlopidina. Acredita-se que este efeito seja devido à inibição da hidroxilação de bupropiona catalisada por CYP2B6.
Prasugrel: Prasugrel é um inibidor fraco do CYP2B6. Em indivíduos saudáveis, o prasugrel aumentou os valores de Cmax e AUC da bupropiona em 14% e 18%, respetivamente, e diminuiu os valores de Cmax e AUC da hidroxibupropiona, um metabolito ativo da bupropiona, em 32% e 24%, respetivamente.
Cimetidina: O metabólito treohidrobupropiona da bupropiona não parece ser produzido pelas enzimas do citocromo P450. Os efeitos da administração concomitante de cimetidina na farmacocinética da bupropiona e seus metabólitos ativos foram estudados em 24 jovens voluntários saudáveis do sexo masculino. Após a administração oral de 300 mg de bupropiona com e sem cimetidina 800 mg, a farmacocinética da bupropiona e da hidroxibupropiona não foi afetada. No entanto, houve aumentos de 16% e 32% na AUC e Cmax, respectivamente, das porções combinadas de treohidrobupropiona e eritrohidrobupropiona.
Citalopram: Citalopram não afetou a farmacocinética da bupropiona e seus três metabólitos.
Indutores de CYP2B6
Ritonavir e lopinavir: em um estudo com voluntários saudáveis, ritonavir 100 mg duas vezes ao dia reduziu a AUC e a Cmax da bupropiona em 22% e 21%, respectivamente. A exposição do metabólito hidroxibupropiona diminuiu 23%, a treohidrobupropiona diminuiu 38% e a eritrohidrobupropiona diminuiu 48%.
Em um segundo estudo com voluntários saudáveis, o ritonavir na dose de 600 mg duas vezes ao dia diminuiu a AUC e a Cmax da bupropiona em 66% e 62%, respectivamente. A exposição do metabólito hidroxibupropiona diminuiu 78%, a treohidrobupropiona diminuiu 50% e a eritrohidrobupropiona diminuiu 68%.
Em outro estudo com voluntários saudáveis, lopinavir 400 mg/ritonavir 100 mg duas vezes ao dia diminuiu a AUC e a Cmax da bupropiona em 57%. A AUC e Cmax da hidroxibupropiona foram diminuídas em 50% e 31%, respectivamente.
Efavirenz: Em um estudo em voluntários saudáveis, efavirenz 600 mg uma vez ao dia por 2 semanas reduziu a AUC e Cmax da bupropiona em aproximadamente 55% e 34%, respectivamente. A AUC da hidroxibupropiona permaneceu inalterada, enquanto a Cmax da hidroxibupropiona aumentou em 50%.
Carbamazepina, Fenobarbital, Fenitoína: Embora não estudados sistematicamente, esses medicamentos podem induzir o metabolismo da bupropiona.
Potencial para WELLBUTRIN afetar outros medicamentos
Dados em animais indicaram que a bupropiona pode ser um indutor de enzimas metabolizadoras de drogas em humanos. Em um estudo, após a administração crônica de 100 mg de bupropiona três vezes ao dia a 8 voluntários saudáveis do sexo masculino por 14 dias, não houve evidência de indução de seu próprio metabolismo. No entanto, pode haver potencial para alterações clinicamente importantes dos níveis sanguíneos de drogas coadministradas.
Drogas Metabolizadas Por CYP2D6
In vitro, a bupropiona e seus metabólitos (eritrohidrobupropiona, treohidrobupropiona, hidroxibupropiona) são inibidores do CYP2D6. Em um ensaio clínico com 15 indivíduos do sexo masculino (com idades entre 19 e 35 anos) que eram metabolizadores extensivos de CYP2D6, bupropiona 300 mg/dia seguida por uma dose única de 50 mg de desipramina aumentou a Cmax, AUC e t½ da desipramina em uma média de aproximadamente 2, 5 e 2 vezes, respectivamente. O efeito esteve presente por pelo menos 7 dias após a última dose de bupropiona. O uso concomitante de bupropiona com outras drogas metabolizadas pelo CYP2D6 não foi formalmente estudado.
Citalopram: Embora o citalopram não seja metabolizado principalmente pelo CYP2D6, em um estudo, a bupropiona aumentou a Cmax e a AUC do citalopram em 30% e 40%, respectivamente.
Lamotrigina: doses orais múltiplas de bupropiona não tiveram efeitos estatisticamente significativos na farmacocinética de dose única de lamotrigina em 12 voluntários saudáveis.
Digoxina: Dados da literatura mostraram que a exposição à digoxina foi diminuída quando uma dose oral única de 0,5 mg de digoxina foi administrada 24 horas após uma dose oral única de 150 mg de bupropiona de liberação prolongada em voluntários saudáveis.
Estudos clínicos
eficácia de WELLBUTRIN 150mg no tratamento do transtorno depressivo maior foi estabelecida em dois estudos controlados por placebo de 4 semanas em pacientes adultos internados com TDM (Ensaios 1 e 2 na Tabela 4) e em um estudo controlado por placebo de 6 semanas em pacientes ambulatoriais adultos com TDM (Ensaio 3 na Tabela 4). No primeiro ensaio, o intervalo de dose de WELLBUTRIN 300mg foi de 300mg a 600mg/dia administrado em 3 doses divididas; 78% dos indivíduos foram tratados com doses de 300 mg a 450 mg/dia. O estudo demonstrou a eficácia de WELLBUTRIN 300mg conforme medido pela pontuação total da Escala de Avaliação de Depressão de Hamilton (HDRS), o item de humor deprimido HDRS (Item 1) e a pontuação de gravidade de Impressões Clínicas Globais (CGI-S). O segundo ensaio incluiu 2 doses de WELLBUTRIN (300 e 450 mg/dia) e placebo. Este estudo demonstrou a eficácia do WELLBUTRIN 150mg apenas para a dose de 450mg/dia. Os resultados de eficácia foram estatisticamente significativos para o escore total do HDRS e o escore CGI-S, mas não para o item 1 do HDRS. No terceiro estudo, os pacientes ambulatoriais foram tratados com 300 mg/dia de WELLBUTRIN. Este estudo demonstrou a eficácia do WELLBUTRIN 150mg conforme medido pela pontuação total do HDRS, o HDRS Item 1, a Escala de Avaliação de Depressão de Montgomery-Asberg (MADRS), a pontuação CGI-S e a pontuação CGI-Improvement Scale (CGI-I) . A eficácia de WELLBUTRIN 300mg em uso prolongado, ou seja, por mais de 6 semanas, não foi avaliada sistematicamente em estudos controlados.
INFORMAÇÃO DO PACIENTE
BAUTRINO (WELL byu-trin) (cloridrato de bupropiona) Comprimidos
IMPORTANTE: Certifique-se de ler as três seções deste Guia de Medicação. A primeira seção é sobre o risco de pensamentos e ações suicidas com medicamentos antidepressivos; a segunda seção trata do risco de alterações de pensamento e comportamento, depressão e pensamentos ou ações suicidas com medicamentos usados para parar de fumar; e a terceira seção é intitulada “Que outras informações importantes devo saber sobre WELLBUTRIN 150mg?”
Medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas
Esta seção do Guia de Medicação trata apenas do risco de pensamentos e ações suicidas com medicamentos antidepressivos.
Qual é a informação mais importante que devo saber sobre medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas?
1. Os medicamentos antidepressivos podem aumentar o risco de pensamentos ou ações suicidas em algumas crianças, adolescentes ou adultos jovens nos primeiros meses de tratamento.
2. Depressão ou outras doenças mentais graves são as causas mais importantes de pensamentos e ações suicidas. Algumas pessoas podem ter um risco particularmente alto de ter pensamentos ou ações suicidas. Estes incluem pessoas que têm (ou têm histórico familiar de) doença bipolar (também chamada de doença maníaco-depressiva) ou pensamentos ou ações suicidas.
3. Como posso vigiar e tentar prevenir pensamentos e ações suicidas em mim ou em um membro da família?
- Preste muita atenção a quaisquer mudanças, especialmente mudanças repentinas, de humor, comportamentos, pensamentos ou sentimentos. Isso é muito importante quando um medicamento antidepressivo é iniciado ou quando a dose é alterada.
- Ligue para o seu médico imediatamente para relatar mudanças novas ou repentinas no humor, comportamento, pensamentos ou sentimentos.
- Mantenha todas as visitas de acompanhamento com seu médico conforme programado. Ligue para o médico entre as visitas, conforme necessário, especialmente se tiver dúvidas sobre os sintomas.
Ligue para o seu médico imediatamente se você ou seu familiar tiver algum dos seguintes sintomas, especialmente se eles forem novos, piores ou se preocuparem:
- pensamentos sobre suicídio ou morte
- tentativas de suicídio
- depressão nova ou pior
- ansiedade nova ou pior
- sentindo-se muito agitado ou inquieto
- ataques de pânico
- problemas para dormir (insônia)
- irritabilidade nova ou pior
- agindo de forma agressiva, com raiva ou violento
- agindo em impulsos perigosos
- um aumento extremo na atividade e na fala (mania)
- outras mudanças incomuns no comportamento ou humor
O que mais eu preciso saber sobre medicamentos antidepressivos?
- Nunca interrompa um medicamento antidepressivo sem primeiro falar com um profissional de saúde. Parar um medicamento antidepressivo de repente pode causar outros sintomas.
- Os antidepressivos são medicamentos usados para tratar a depressão e outras doenças. É importante discutir todos os riscos de tratar a depressão e também os riscos de não tratá-la. Os pacientes e suas famílias ou outros cuidadores devem discutir todas as opções de tratamento com o profissional de saúde, não apenas o uso de antidepressivos.
- medicamentos antidepressivos têm outros efeitos colaterais. Converse com o médico sobre os efeitos colaterais do medicamento prescrito para você ou seu familiar.
- Medicamentos antidepressivos podem interagir com outros medicamentos. Conheça todos os medicamentos que você ou seu familiar toma. Mantenha uma lista de todos os medicamentos para mostrar ao profissional de saúde. Não inicie novos medicamentos sem primeiro consultar seu médico.
Não se sabe se WELLBUTRIN é seguro e eficaz em crianças menores de 18 anos.
Parar de fumar, medicamentos para parar de fumar, mudanças no pensamento e no comportamento, depressão e pensamentos ou ações suicidas
Esta seção do Guia de Medicação trata apenas do risco de mudanças no pensamento e comportamento, depressão e pensamentos ou ações suicidas com drogas usadas para parar de fumar. Embora WELLBUTRIN não seja um tratamento para parar de fumar, ele contém o mesmo ingrediente ativo (cloridrato de bupropiona) que ZYBAN, que é usado para ajudar os pacientes a parar de fumar.
Fale com o seu profissional de saúde ou o profissional de saúde do seu familiar sobre:
- todos os riscos e benefícios dos medicamentos para parar de fumar.
- todas as opções de tratamento para parar de fumar.
Quando você tenta parar de fumar, com ou sem bupropiona, pode ter sintomas que podem ser devidos à abstinência de nicotina, incluindo:
- vontade de fumar
- frustração
- inquietação
- humor deprimido
- raiva
- diminuição da frequência cardíaca
- problemas para dormir
- sentindo ansioso
- aumento do apetite
- irritabilidade
- Dificuldade de concentração
- ganho de peso
Algumas pessoas até experimentaram pensamentos suicidas ao tentar parar de fumar sem medicação.
Às vezes, parar de fumar pode levar ao agravamento de problemas de saúde mental que você já tem, como a depressão.
Algumas pessoas tiveram efeitos colaterais graves ao tomar bupropiona para ajudá-los a parar de fumar, incluindo: Problemas de saúde mental novos ou piores, como mudanças de comportamento ou pensamento, agressão, hostilidade, agitação, depressão ou pensamentos ou ações suicidas. Algumas pessoas tiveram esses sintomas quando começaram a tomar bupropiona e outras os desenvolveram após várias semanas de tratamento ou após a interrupção da bupropiona. Esses sintomas ocorreram com mais frequência em pessoas que tinham histórico de problemas de saúde mental antes de tomar bupropiona do que em pessoas sem histórico de problemas de saúde mental.
Pare de tomar WELLBUTRIN e ligue para o seu médico imediatamente se você, sua família ou cuidador notar algum desses sintomas. Trabalhe com seu médico para decidir se você deve continuar a tomar WELLBUTRIN. Em muitas pessoas, esses sintomas desapareceram após a interrupção do WELLBUTRIN 300mg, mas em algumas pessoas os sintomas continuaram após a interrupção do WELLBUTRIN. É importante que você acompanhe seu médico até que os sintomas desapareçam. Antes de tomar WELLBUTRIN 150mg, informe o seu médico se você já teve depressão ou outros problemas de saúde mental. Você também deve informar seu médico sobre quaisquer sintomas que você teve durante outras vezes em que tentou parar de fumar, com ou sem bupropiona.
Que outras informações importantes devo saber sobre WELLBUTRIN?
- Convulsões: Há uma chance de ter uma convulsão (convulsão, convulsão) com WELLBUTRIN 150mg, especialmente em pessoas:
- com certos problemas médicos.
- que tomam certos medicamentos. A chance de ter convulsões aumenta com doses mais altas de WELLBUTRIN. Para obter mais informações, consulte as seções “Quem não deve tomar WELLBUTRIN?” e “O que devo dizer ao meu médico antes de tomar WELLBUTRIN 300mg?” Informe o seu médico sobre todas as suas condições médicas e todos os medicamentos que você toma. Não tome quaisquer outros medicamentos enquanto estiver a tomar WELLBUTRIN 150 mg, a menos que o seu médico tenha dito que pode tomá-los. Se você tiver uma convulsão enquanto estiver tomando Wellbutrin, pare de tomar os comprimidos e ligue para o seu médico imediatamente. Não tome WELLBUTRIN 150mg novamente se tiver uma convulsão.
- Pressão alta (hipertensão). Algumas pessoas têm pressão alta que pode ser grave, enquanto tomam WELLBUTRIN. chance de pressão alta pode ser maior se você também usar terapia de reposição de nicotina (como um adesivo de nicotina) para ajudá-lo a parar de fumar (consulte a seção deste Guia de Medicação chamada “Como devo tomar WELLBUTRIN 150mg?”).
- Episódios maníacos. Algumas pessoas podem ter períodos de mania enquanto tomam WELLBUTRIN 300mg, incluindo:
- Energia muito aumentada
- Problemas graves para dormir
- Pensamentos descontrolados
- Comportamento imprudente
- Ideias excepcionalmente grandiosas
- Excesso de felicidade ou irritabilidade
- Falando mais ou mais rápido do que o habitual Se você tiver algum dos sintomas de mania acima, ligue para o seu médico.
- Pensamentos ou comportamentos incomuns. Alguns pacientes têm pensamentos ou comportamentos incomuns enquanto tomam Wellbutrin, incluindo delírios (acreditar que você é outra pessoa), alucinações (ver ou ouvir coisas que não existem), paranóia (sentir que as pessoas estão contra você) ou sentir-se confuso. Se isso acontecer com você, ligue para o seu médico.
- Problemas visuais.
- dor nos olhos
- mudanças na visão
- inchaço ou vermelhidão dentro ou ao redor do olho Apenas algumas pessoas correm o risco de ter esses problemas. Você pode querer se submeter a um exame oftalmológico para ver se está em risco e receber tratamento preventivo, se estiver.
- Reações alérgicas graves. Algumas pessoas podem ter reações alérgicas graves ao WELLBUTRIN. Pare de tomar WELLBUTRIN 300mg e ligue para o seu médico imediatamente se tiver erupção cutânea, comichão, urticária, febre, gânglios linfáticos inchados, feridas dolorosas na boca ou à volta dos olhos, inchaço dos lábios ou da língua, dor no peito ou dificuldade em respirar. Estes podem ser sinais de uma reação alérgica grave.
que é WELLBUTRIN?
WELLBUTRIN é um medicamento de prescrição usado para tratar adultos com um certo tipo de depressão chamado transtorno depressivo maior.
Quem não deve tomar WELLBUTRIN 150mg?
Não tome WELLBUTRIN se você
- tem ou teve um distúrbio convulsivo ou epilepsia.
- tem ou teve um transtorno alimentar, como anorexia nervosa ou bulimia.
- estiver tomando outros medicamentos que contenham bupropiona, incluindo ZYBAN (usado para ajudar as pessoas a parar de fumar), WELLBUTRIN 300mg SR, WELLBUTRIN 150mg XL, APLENZIN ou FORFIVO XL. A bupropiona é o mesmo ingrediente ativo que está no WELLBUTRIN.
- Beba muito álcool e pare de beber abruptamente, ou use medicamentos chamados sedativos (estes deixam você com sono), benzodiazepínicos ou medicamentos anticonvulsivos, e você para de usá-los de repente.
- tomar um inibidor da monoamina oxidase (IMAO). Pergunte ao seu médico ou farmacêutico se não tiver certeza se está tomando um IMAO, incluindo o antibiótico linezolida.
- não tome um IMAO dentro de 2 semanas após a interrupção do WELLBUTRIN, a menos que seja instruído a fazê-lo pelo seu médico.
- não inicie WELLBUTRIN 150mg se você parou de tomar um IMAO nas últimas 2 semanas, a menos que seja orientado pelo seu médico.
- são alérgicos ao ingrediente ativo de WELLBUTRIN 300mg, bupropiona, ou a qualquer um dos ingredientes inativos. Consulte o final deste Guia de Medicação para obter uma lista completa dos ingredientes do WELLBUTRIN.
O que devo dizer ao meu médico antes de tomar WELLBUTRIN?
Informe o seu médico se você já teve depressão, pensamentos ou ações suicidas ou outros problemas de saúde mental. Consulte “Medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas”.
- Informe o seu médico sobre suas outras condições médicas, incluindo se você:
- tem problemas de fígado, especialmente cirrose do fígado.
- tem problemas renais.
- tem ou teve um transtorno alimentar, como anorexia nervosa ou bulimia.
- tiveram um ferimento na cabeça.
- teve uma convulsão (convulsão, ataque).
- tem um tumor no seu sistema nervoso (cérebro ou coluna).
- teve um ataque cardíaco, problemas cardíacos ou pressão alta.
- é diabético tomando insulina ou outros medicamentos para controlar o açúcar no sangue.
- beber álcool.
- abuso de medicamentos prescritos ou drogas de rua.
- estão grávidas ou planejam engravidar. Converse com seu médico sobre o risco para o feto se você tomar WELLBUTRIN 300mg durante a gravidez.
- Informe o seu médico se engravidar ou achar que está grávida durante o tratamento com Wellbutrin.
- Se você engravidar durante o tratamento com WELLBUTRIN, converse com seu médico sobre o registro no Registro Nacional de Gravidez para Antidepressivos. Você pode se registrar ligando para 1-844-405-6185.
- está amamentando ou planeja amamentar durante o tratamento com WELLBUTRIN. WELLBUTRIN passa para o seu leite. Converse com seu médico sobre a melhor maneira de alimentar seu bebê durante o tratamento com WELLBUTRIN.
Informe o seu médico sobre todos os medicamentos que toma, incluindo prescrição, medicamentos de venda livre, vitaminas e suplementos de ervas. Muitos medicamentos aumentam suas chances de ter convulsões ou outros efeitos colaterais graves se você os tomar enquanto estiver tomando WELLBUTRIN.
Como devo tomar WELLBUTRIN 300mg?
- Tome WELLBUTRIN 300mg exatamente como prescrito pelo seu médico. Não altere sua dose ou pare de tomar WELLBUTRIN sem falar primeiro com seu médico.
- Engula os comprimidos de WELLBUTRIN inteiros. Não mastigue, corte ou esmague os comprimidos de WELLBUTRIN 300mg.
- Tome WELLBUTRIN 300mg à mesma hora todos os dias.
- Tome suas doses de WELLBUTRIN 300mg com pelo menos 6 horas de intervalo.
- Você pode tomar WELLBUTRIN com ou sem alimentos.
- Se você perder uma dose, não tome uma dose extra para compensar a dose que você esqueceu. Aguarde e tome a próxima dose no horário regular. Isto é muito importante. Excesso de WELLBUTRIN pode aumentar sua chance de ter uma convulsão.
- Se você tomar muito WELLBUTRIN, ou overdose, ligue para o pronto-socorro local ou centro de controle de envenenamento imediatamente.
- Não tome outros medicamentos enquanto estiver a tomar WELLBUTRIN 300mg, a menos que o seu médico lhe diga que está tudo bem.
- Se estiver a tomar WELLBUTRIN 150 mg para o tratamento da perturbação depressiva major, pode demorar várias semanas até sentir que WELLBUTRIN 150 mg está a funcionar. Assim que se sentir melhor, é importante continuar a tomar WELLBUTRIN exatamente como indicado pelo seu médico. Ligue para o seu médico se achar que WELLBUTRIN não está funcionando para você.
O que devo evitar ao tomar WELLBUTRIN 300mg?
- Limite ou evite o uso de álcool durante o tratamento com WELLBUTRIN. Se você costuma beber muito álcool, converse com seu médico antes de parar de repente. Se você parar de beber álcool de repente, pode aumentar o risco de ter convulsões.
- Não conduza um carro ou utilize máquinas pesadas até saber como WELLBUTRIN 150mg o afeta. WELLBUTRIN pode afetar sua capacidade de fazer essas coisas com segurança.
Quais são os possíveis efeitos colaterais do WELLBUTRIN 300mg?
WELLBUTRIN pode causar efeitos colaterais graves. Consulte as seções no início deste Guia de Medicação para obter informações sobre os efeitos colaterais graves do WELLBUTRIN.
Os efeitos colaterais mais comuns do WELLBUTRIN incluem:
- nervosismo
- transpiração intensa
- boca seca
- tremor (tremor)
- constipação
- problemas para dormir
- dor de cabeça
- visão embaçada
- náusea ou vômito
- batimento cardíaco rápido
- tontura
Se tiver náuseas, tome o medicamento com alimentos. Se tiver problemas para dormir, não tome o medicamento muito perto da hora de dormir.
Informe o seu médico imediatamente sobre quaisquer efeitos colaterais que o incomodem.
Estes não são todos os possíveis efeitos colaterais do WELLBUTRIN. Para mais informações, pergunte ao seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Você também pode relatar efeitos colaterais à GlaxoSmithKline pelo telefone 1-888-825-5249.
Como devo armazenar WELLBUTRIN 300mg?
- Armazene WELLBUTRIN em temperatura ambiente entre 20°C e 25°C (68°F e 77°F).
- Mantenha os comprimidos de WELLBUTRIN secos e protegidos da luz.
Mantenha WELLBUTRIN e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre o uso seguro e eficaz de WELLBUTRIN.
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use WELLBUTRIN 300mg para uma condição para a qual não foi prescrito. Não dê WELLBUTRIN a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Se você fizer um teste de triagem de drogas na urina, WELLBUTRIN pode tornar o resultado do teste positivo para anfetaminas. Se você disser à pessoa que está fazendo o teste de triagem de drogas que você está tomando WELLBUTRIN 300mg, ela poderá fazer um teste de triagem de drogas mais específico que não deve ter esse problema.
Este Guia de Medicação resume informações importantes sobre WELLBUTRIN. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre WELLBUTRIN que foram escritas para profissionais de saúde.
Para obter mais informações sobre o WELLBUTRIN, ligue para 1-888-825-5249.
Quais são os ingredientes de WELLBUTRIN 300mg?
Princípio ativo: cloridrato de bupropiona.
Ingredientes inativos: Comprimido de 75 mg – Lago D&C Amarelo Nº 10, Lago FD&C Amarelo Nº 6, hidroxipropilcelulose, hipromelose, celulose microcristalina, polietilenoglicol, talco e dióxido de titânio; Comprimido de 100 mg – Lago FD&C Vermelho Nº 40, Lago FD&C Amarelo Nº 6, hidroxipropilcelulose, hipromelose, celulose microcristalina, polietilenoglicol, talco e dióxido de titânio.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
