Abilify 10mg, 15mg, 20mg Aripiprazole Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.

O que é Abilify 20mg e como é usado?
Abilify é um medicamento de prescrição usado para tratar os sintomas da esquizofrenia, transtorno bipolar I (depressão maníaca) e transtorno depressivo maior. Abilify 10mg pode ser usado sozinho ou com outros medicamentos. Abilify é um agente antipsicótico e antimaníaco.
- Não se sabe se Abilify é seguro e eficaz em crianças com menos de 6 anos de idade.
Quais são os possíveis efeitos colaterais do Abilify 15mg?
Abilify 15mg pode causar efeitos colaterais graves, incluindo:
- agitação ou angústia grave,
- sentindo-se inquieto,
- espasmos ou movimentos incontroláveis de seus olhos, lábios, língua, rosto, braços ou pernas,
- aparência de máscara do rosto,
- dificuldade para engolir,
- problemas de fala,
- convulsão (convulsões),
- pensamentos de suicídio ou automutilação,
- músculos rígidos ou rígidos,
- febre alta,
- sudorese,
- confusão,
- batimentos cardíacos rápidos ou irregulares,
- tremores (tremores),
- sentindo-se tonto,
- arrepios,
- dor de garganta,
- aftas,
- feridas na pele,
- tosse,
- dificuldade para respirar,
- aumento da sede,
- aumento da micção,
- boca seca e
- odor de hálito frutado
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Abilify 20mg incluem:
- movimentos musculares descontrolados,
- ansiedade,
- sentindo-se inquieto,
- ganho de peso,
- náusea,
- vômito,
- constipação,
- aumento do apetite,
- dor de cabeça,
- tontura,
- sonolência,
- sentindo-se cansado,
- problemas de sono (insônia),
- nariz entupido e
- dor de garganta
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Abilify. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
MORTALIDADE AUMENTADA EM PACIENTES IDOSOS COM PSICOSE RELACIONADA À DEMÊNCIA E PENSAMENTOS E COMPORTAMENTOS SUICÍDICOS COM MEDICAMENTOS ANTIDEPRESSIVOS
Pacientes idosos com psicose relacionada à demência tratados com medicamentos antipsicóticos apresentam risco aumentado de morte. ABILIFY 20mg não é aprovado para o tratamento de pacientes com psicose relacionada à demência [ver ADVERTÊNCIAS E PRECAUÇÕES].
Os antidepressivos aumentaram o risco de pensamentos e comportamentos suicidas em crianças, adolescentes e adultos jovens em estudos de curto prazo. Esses estudos não mostraram aumento do risco de pensamentos e comportamentos suicidas com o uso de antidepressivos em pacientes com mais de 24 anos; houve uma redução no risco com o uso de antidepressivos em pacientes com 65 anos ou mais [ver ADVERTÊNCIAS E PRECAUÇÕES].
Em pacientes de todas as idades que iniciam a terapia antidepressiva, monitore atentamente quanto à piora e ao surgimento de pensamentos e comportamentos suicidas. Aconselhe as famílias e os cuidadores sobre a necessidade de observação atenta e comunicação com o prescritor [ver ADVERTÊNCIAS E PRECAUÇÕES].
DESCRIÇÃO
aripiprazol é um medicamento psicotrópico que está disponível como ABILIFY® (aripiprazol) Comprimidos, ABILIFY DISCMELT® (aripiprazol) Comprimidos de Desintegração Oral, ABILIFY® (aripiprazol) Solução Oral e ABILIFY® (aripiprazol) Injetável, uma solução para injeção intramuscular. Aripiprazol é 7-[4-[4-(2,3diclorofenil)-1-piperazinil]butoxi]-3,4-di-hidrocarbostiril. A fórmula empírica é C23H27Cl2N3O2 e seu peso molecular é 448,38. A estrutura química é:
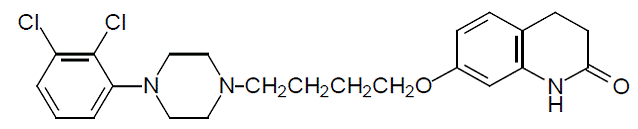
Os comprimidos ABILIFY estão disponíveis nas dosagens de 2 mg, 5 mg, 10 mg, 15 mg, 20 mg e 30 mg. Os ingredientes inativos incluem amido de milho, hidroxipropilcelulose, lactose monohidratada, estearato de magnésio e celulose microcristalina. Os corantes incluem óxido férrico (amarelo ou vermelho) e FD&C Blue No. 2 Aluminum Lake.
ABILIFY 20mg DISCMELT comprimidos de desintegração oral estão disponíveis em dosagens de 10 mg e 15 mg. Os ingredientes inativos incluem acessulfame de potássio, aspartame, silicato de cálcio, croscarmelose sódica, crospovidona, creme de baunilha (aromatizantes naturais e artificiais), estearato de magnésio, celulose microcristalina, dióxido de silício, ácido tartárico e xilitol. Os corantes incluem óxido férrico (amarelo ou vermelho) e FD&C Blue No. 2 Aluminum Lake.
ABILIFY Oral Solution é uma solução límpida, incolor a amarelo-claro, disponível na concentração de 1 mg/mL. Os ingredientes inativos para esta solução incluem edetato dissódico, frutose, glicerina, ácido dl-láctico, metilparabeno, propilenoglicol, propilparabeno, hidróxido de sódio, sacarose e água purificada. A solução oral é aromatizada com creme de laranja natural e outros aromas naturais.
ABILIFY Injection está disponível em frascos de dose única como uma solução aquosa límpida, incolor, estéril, 9,75 mg/1,3 mL (7,5 mg/mL) pronta para uso apenas para uso intramuscular. Os ingredientes inativos para esta solução incluem 199,5 mg de sulfobutiléter β-ciclodextrina (SBECD), 10,4 mg de ácido tartárico, qs para pH 4,3 de hidróxido de sódio e qs para 1,33 mL de água para injeção.
INDICAÇÕES
ABILIFY Comprimidos Orais, Comprimidos de Desintegração Oral e Solução Oral são indicados para o tratamento de:
- Esquizofrenia [ver Estudos clínicos ]
- Tratamento Agudo de Episódios Maníacos e Mistos associados ao Transtorno Bipolar I [ver Estudos clínicos ]
- Tratamento Adjuvante do Transtorno Depressivo Maior [ver Estudos clínicos ]
- Irritabilidade Associada ao Transtorno Autista [ver Estudos clínicos ]
- Tratamento do Transtorno de Tourette [ver Estudos clínicos ]
ABILIFY Injection é indicado para o tratamento de:
- Agitação associada à esquizofrenia ou mania bipolar [ver Estudos clínicos ]
DOSAGEM E ADMINISTRAÇÃO
Esquizofrenia
Adultos
A dose inicial e alvo recomendada para ABILIFY é de 10 ou 15 mg/dia administrados uma vez ao dia, independentemente das refeições. ABILIFY foi sistematicamente avaliado e demonstrou ser eficaz em uma faixa de dose de 10 a 30 mg/dia, quando administrado na forma de comprimido; no entanto, doses superiores a 10 ou 15 mg/dia não foram mais eficazes do que 10 ou 15 mg/dia. Os aumentos de dosagem geralmente não devem ser feitos antes de 2 semanas, o tempo necessário para atingir o estado de equilíbrio [ver Estudos clínicos ].
Tratamento de manutenção: A manutenção da eficácia na esquizofrenia foi demonstrada em um estudo envolvendo pacientes com esquizofrenia que permaneceram sintomaticamente estáveis com outros medicamentos antipsicóticos por períodos de 3 meses ou mais. Esses pacientes foram descontinuados com esses medicamentos e randomizados para ABILIFY 15 mg/dia ou placebo, e observados quanto à recaída [ver Estudos clínicos ]. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade contínua de tratamento de manutenção.
Adolescentes
dose alvo recomendada de ABILIFY é de 10 mg/dia. O aripiprazol foi estudado em pacientes adolescentes de 13 a 17 anos de idade com esquizofrenia em doses diárias de 10 mg e 30 mg. A dose diária inicial da formulação do comprimido nestes pacientes foi de 2 mg, que foi titulada para 5 mg após 2 dias e para a dose alvo de 10 mg após 2 dias adicionais. Os aumentos de dose subsequentes devem ser administrados em incrementos de 5 mg. A dose de 30 mg/dia não se mostrou mais eficaz do que a dose de 10 mg/dia. ABILIFY pode ser administrado independentemente das refeições [ver Estudos clínicos ]. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção.
Mudando de outros antipsicóticos
Não há dados coletados sistematicamente para abordar especificamente a mudança de pacientes com esquizofrenia de outros antipsicóticos para ABILIFY 20 mg ou sobre a administração concomitante com outros antipsicóticos. Embora a descontinuação imediata do tratamento antipsicótico anterior possa ser aceitável para alguns pacientes com esquizofrenia, a descontinuação mais gradual pode ser mais apropriada para outros. Em todos os casos, o período de sobreposição de administração de antipsicóticos deve ser minimizado.
Transtorno Bipolar I
Tratamento Agudo de Episódios Maníacos e Mistos
Adultos
dose inicial recomendada em adultos é de 15 mg administrados uma vez ao dia como monoterapia e 10 mg a 15 mg administrados uma vez ao dia como terapia adjuvante com lítio ou valproato. ABILIFY 10mg pode ser administrado independentemente das refeições. A dose alvo recomendada de ABILIFY é de 15 mg/dia, como monoterapia ou como terapia adjuvante com lítio ou valproato. A dose pode ser aumentada para 30 mg/dia com base na resposta clínica. A segurança de doses acima de 30 mg/dia não foi avaliada em ensaios clínicos.
Pediatria
A dose inicial recomendada em pacientes pediátricos (10 a 17 anos) como monoterapia é de 2 mg/dia, com titulação para 5 mg/dia após 2 dias e uma dose alvo de 10 mg/dia após 2 dias adicionais. A dosagem recomendada como terapia adjuvante ao lítio ou valproato é a mesma. Aumentos de dose subsequentes, se necessários, devem ser administrados em incrementos de 5 mg/dia. ABILIFY pode ser administrado independentemente das refeições [ver Estudos clínicos ].
Tratamento Adjuvante do Transtorno Depressivo Maior
Adultos
dose inicial recomendada de ABILIFY como tratamento adjuvante para pacientes que já estejam tomando um antidepressivo é de 2 a 5 mg/dia. A faixa de dosagem recomendada é de 2 a 15 mg/dia. Os ajustes de dose de até 5 mg/dia devem ocorrer gradualmente, em intervalos não inferiores a 1 semana [ver Estudos clínicos ]. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade contínua de tratamento de manutenção.
Irritabilidade Associada ao Transtorno Autista
Pacientes pediátricos (6 a 17 anos)
A faixa de dosagem recomendada para o tratamento de pacientes pediátricos com irritabilidade associada ao transtorno autista é de 5 a 15 mg/dia.
A dosagem deve ser iniciada com 2 mg/dia. A dose deve ser aumentada para 5 mg/dia, com aumentos subsequentes para 10 ou 15 mg/dia, se necessário. Os ajustes de dose de até 5 mg/dia devem ocorrer gradualmente, em intervalos não inferiores a 1 semana [ver Estudos clínicos ]. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade contínua de tratamento de manutenção.
Transtorno de Tourette
Pacientes pediátricos (6 a 18 anos)
A faixa de dosagem recomendada para o Transtorno de Tourette é de 5 a 20 mg/dia.
Para pacientes com peso inferior a 50 kg, a dosagem deve ser iniciada com 2 mg/dia com uma dose alvo de 5 mg/dia após 2 dias. A dose pode ser aumentada para 10 mg/dia em pacientes que não atingem o controle ideal dos tiques. Os ajustes de dose devem ocorrer gradualmente em intervalos não inferiores a 1 semana.
Para pacientes com peso igual ou superior a 50 kg, a dosagem deve ser iniciada com 2 mg/dia por 2 dias e depois aumentada para 5 mg/dia por 5 dias, com uma dose alvo de 10 mg/dia no dia 8. A dose pode ser aumentada até 20 mg/dia para pacientes que não atingem o controle ideal dos tiques. Os ajustes de dose devem ocorrer gradualmente em incrementos de 5 mg/dia em intervalos não inferiores a 1 semana. [Ver Estudos clínicos ].
Os pacientes devem ser reavaliados periodicamente para determinar a necessidade contínua de tratamento de manutenção.
Agitação associada à esquizofrenia ou mania bipolar (injeção intramuscular)
Adultos
A dose recomendada nestes doentes é de 9,75 mg. A faixa de dosagem recomendada é de 5,25 a 15 mg. Nenhum benefício adicional foi demonstrado para 15 mg em comparação com 9,75 mg. Uma dose mais baixa de 5,25 mg pode ser considerada quando os fatores clínicos justificarem. Se a agitação que justifica uma segunda dose persistir após a dose inicial, podem ser administradas doses cumulativas até um total de 30 mg/dia. No entanto, a eficácia de doses repetidas de ABILIFY 10mg injetável em pacientes agitados não foi sistematicamente avaliada em ensaios clínicos controlados. A segurança de doses diárias totais superiores a 30 mg ou injeções administradas com mais frequência do que a cada 2 horas não foram adequadamente avaliadas em ensaios clínicos [ver Estudos clínicos ].
Se a terapia contínua com ABILIFY for clinicamente indicada, ABILIFY oral na faixa de 10 a 30 mg/dia deve substituir a injeção de ABILIFY o mais rápido possível [ver DOSAGEM E ADMINISTRAÇÃO ].
Administração da injeção de ABILIFY
Para administrar ABILIFY 10mg Injection, aspire o volume necessário de solução na seringa conforme mostrado na Tabela 1. Descarte qualquer porção não utilizada.
ABILIFY Injection destina-se apenas a uso intramuscular. Não administrar por via intravenosa ou subcutânea. Injete lentamente, profundamente na massa muscular.
Os medicamentos parenterais devem ser inspecionados visualmente quanto a partículas e descoloração antes da administração, sempre que a solução e o recipiente permitirem.
Ajustes de dosagem para considerações do citocromo P450
Os ajustes de dose são recomendados em pacientes que são conhecidos metabolizadores fracos de CYP2D6 e em pacientes que tomam concomitantemente inibidores de CYP3A4 ou inibidores de CYP2D6 ou indutores fortes de CYP3A4 (ver Tabela 2). Quando o medicamento coadministrado é retirado da terapia combinada, a dosagem de ABILIFY 10mg deve ser ajustada ao seu nível original. Quando o indutor de CYP3A4 coadministrado é retirado, a dosagem de ABILIFY deve ser reduzida para o nível original em 1 a 2 semanas. Pacientes que podem estar recebendo uma combinação de inibidores fortes, moderados e fracos de CYP3A4 e CYP2D6 (por exemplo, um inibidor forte de CYP3A4 e um inibidor moderado de CYP2D6 ou um inibidor moderado de CYP3A4 com um inibidor moderado de CYP2D6), a dose pode ser reduzida para um - um quarto (25%) da dose usual inicialmente e depois ajustada para obter uma resposta clínica favorável.
Quando ABILIFY adjuvante é administrado a pacientes com transtorno depressivo maior, ABILIFY 10mg deve ser administrado sem ajuste de dose conforme especificado em Posologia e Administração (2.3).
Dosagem de solução oral
A solução oral pode ser substituída por comprimidos na base de mg por mg até o nível de dose de 25 mg. Pacientes recebendo comprimidos de 30 mg devem receber 25 mg da solução [ver FARMACOLOGIA CLÍNICA ].
Dosagem de comprimidos de desintegração oral
A dosagem de ABILIFY 10mg comprimidos de desintegração oral é a mesma dos comprimidos orais [ver Seções acima ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
Os comprimidos de ABILIFY® (aripiprazol) estão disponíveis conforme descrito na Tabela 3.
Os comprimidos de desintegração oral ABILIFY DISCMELT® (aripiprazol) estão disponíveis conforme descrito na Tabela 4.
ABILIFY® (aripiprazol) Solução Oral (1 mg/mL) é uma solução límpida, incolor a amarelo claro, fornecida em frascos resistentes à abertura por crianças, juntamente com um copo doseador oral calibrado.
ABILIFY® (aripiprazol) Injetável para Uso Intramuscular é uma solução límpida e incolor disponível como solução pronta para uso, 9,75 mg/1,3 mL (7,5 mg/mL) em frascos transparentes de vidro Tipo 1.
Armazenamento e manuseio
ABILIFY® (aripiprazol) Comprimidos têm marcações em um lado e estão disponíveis nas dosagens e embalagens listadas na Tabela 32.
ABILIFY 15mg DISCMELT® (aripiprazol) comprimidos de desintegração oral são comprimidos redondos com marcações em ambos os lados. ABILIFY 15mg DISCMELT está disponível nas dosagens e embalagens listadas na Tabela 33.
ABILIFY® (aripiprazol) Solução Oral (1 mg/mL) é fornecido em frascos resistentes à abertura por crianças, juntamente com um copo doseador oral calibrado. ABILIFY 20mg Solução Oral está disponível da seguinte forma:
Frasco de 150 mL NDC 59148-013-15
ABILIFY® (aripiprazol) Injetável para uso intramuscular está disponível como uma solução pronta para uso, 9,75 mg/1,3 mL (7,5 mg/mL) em frascos transparentes de vidro Tipo 1 da seguinte forma:
Frasco de dose única de 9,75 mg/1,3 mL NDC 59148-016-65
Armazenar
Comprimidos
Armazenar a 25°C (77°F); excursões permitidas entre 15°C a 30°C (59°F a 86°F) [ver Temperatura ambiente controlada USP ].
Solução oral
Armazenar a 25°C (77°F); excursões permitidas entre 15°C a 30°C (59°F a 86°F) [ver Temperatura ambiente controlada USP ]. Os frascos abertos de ABILIFY Solução Oral podem ser usados por até 6 meses após a abertura, mas não além da data de validade no frasco. O frasco e seu conteúdo devem ser descartados após a data de validade.
Injeção
Armazenar a 25°C (77°F); excursões permitidas entre 15°C a 30°C (59°F a 86°F) [ver Temperatura ambiente controlada USP ]. Proteja da luz guardando na embalagem original. Guarde na caixa até o momento do uso.
Distribuído e comercializado pela Otsuka America Pharmaceutical, Inc., Rockville, MD 20850 USA. Otsuka America Pharmaceutical, Inc., Rev agosto 2019
EFEITOS COLATERAIS
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
As seguintes reações adversas são discutidas com mais detalhes em outras seções da bula:
- Aumento da mortalidade em pacientes idosos com psicose relacionada à demência [ver AVISO EM CAIXA e AVISOS E PRECAUÇÕES ]
- Eventos Adversos Cerebrovasculares, Incluindo AVC [ver AVISOS E PRECAUÇÕES ]
- Pensamentos e Comportamentos Suicidas em Crianças, Adolescentes e Jovens Adultos [ver AVISO EM CAIXA e AVISOS E PRECAUÇÕES ]
- Síndrome Neuroléptica Maligna (SNM) [ver AVISOS E PRECAUÇÕES ]
- Discinesia Tardia [ver AVISOS E PRECAUÇÕES ]
- Alterações Metabólicas [ver AVISOS E PRECAUÇÕES ]
- Jogo patológico e outros comportamentos compulsivos [ver AVISOS E PRECAUÇÕES ]
- Hipotensão ortostática [ver AVISOS E PRECAUÇÕES ]
- Cataratas [ver AVISOS E PRECAUÇÕES ]
- Leucopenia, neutropenia e agranulocitose [ver AVISOS E PRECAUÇÕES ]
- Convulsões/convulsões [ver AVISOS E PRECAUÇÕES ]
- Potencial para Comprometimento Cognitivo e Motor [ver AVISOS E PRECAUÇÕES ]
- Regulação da temperatura corporal [ver AVISOS E PRECAUÇÕES ]
- Suicídio [ver AVISOS E PRECAUÇÕES ]
- Disfagia [ver AVISOS E PRECAUÇÕES ]
As reações adversas mais comuns em pacientes adultos em ensaios clínicos (≥10%) foram náuseas, vômitos, constipação, dor de cabeça, tontura, acatisia, ansiedade, insônia e inquietação.
As reações adversas mais comuns nos ensaios clínicos pediátricos (≥10%) foram sonolência, cefaleia, vómitos, perturbações extrapiramidais, fadiga, aumento do apetite, insónia, náuseas, nasofaringite e aumento de peso.
ABILIFY foi avaliado quanto à segurança em 13.543 pacientes adultos que participaram de ensaios clínicos de dose múltipla em esquizofrenia, transtorno bipolar, transtorno depressivo maior, demência do tipo Alzheimer, doença de Parkinson e alcoolismo, e que tiveram aproximadamente 7.619 pacientes-ano de exposição a ABILIFY oral 10mg e 749 pacientes com exposição à injeção de ABILIFY. Um total de 3.390 pacientes foram tratados com ABILIFY oral por pelo menos 180 dias e 1.933 pacientes tratados com ABILIFY oral tiveram pelo menos 1 ano de exposição.
ABILIFY 15mg foi avaliado quanto à segurança em 1.686 pacientes (6 a 18 anos) que participaram de ensaios clínicos de dose múltipla em esquizofrenia, mania bipolar, transtorno autista ou transtorno de Tourette e que tiveram aproximadamente 1.342 pacientes-ano de exposição ao ABILIFY oral . Um total de 959 pacientes pediátricos foram tratados com ABILIFY oral por pelo menos 180 dias e 556 pacientes pediátricos tratados com ABILIFY 10mg oral tiveram pelo menos 1 ano de exposição.
As condições e a duração do tratamento com ABILIFY (monoterapia e terapia adjuvante com antidepressivos ou estabilizadores de humor) incluíram (em categorias sobrepostas) estudos duplo-cegos, comparativos e não comparativos abertos, estudos de internação e ambulatorial, estudos de dose fixa e flexível, e exposição de curto e longo prazo.
Experiência de Ensaios Clínicos
Pacientes adultos com esquizofrenia
Os achados a seguir são baseados em um conjunto de cinco estudos controlados por placebo (quatro de 4 semanas e um de 6 semanas) nos quais ABILIFY 15mg oral foi administrado em doses variando de 2 a 30 mg/dia.
Reações Adversas Comumente Observadas
A única reação adversa comumente observada associada ao uso de ABILIFY 20mg em pacientes com esquizofrenia (incidência de 5% ou mais e incidência de ABILIFY pelo menos o dobro do placebo) foi acatisia (ABILIFY 8%; placebo 4%).
Pacientes adultos com mania bipolar
Monoterapia
Os achados a seguir são baseados em um conjunto de ensaios de mania bipolar de 3 semanas, controlados por placebo, nos quais ABILIFY 15mg oral foi administrado em doses de 15 ou 30 mg/dia.
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao uso de ABILIFY em pacientes com mania bipolar (incidência de 5% ou mais e incidência de ABILIFY 15mg pelo menos o dobro do placebo) são mostradas na Tabela 16.
Reações adversas menos comuns em adultos
A Tabela 17 enumera a incidência combinada, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até 6 semanas na esquizofrenia e até 3 semanas na mania bipolar), incluindo apenas aquelas reações que ocorreram em 2% ou mais dos doentes tratados com ABILIFY (doses ≥2 mg/dia) e para os quais a incidência em doentes tratados com ABILIFY 20 mg foi superior à incidência em doentes tratados com placebo no conjunto de dados combinado.
Um exame de subgrupos populacionais não revelou nenhuma evidência clara de incidência diferencial de reações adversas com base na idade, sexo ou raça.
Pacientes adultos com terapia adjuvante com mania bipolar
Os achados a seguir são baseados em um estudo controlado por placebo de pacientes adultos com transtorno bipolar no qual ABILIFY 15mg foi administrado em doses de 15 ou 30 mg/dia como terapia adjuvante com lítio ou valproato.
Reações Adversas Associadas à Descontinuação do Tratamento
Em um estudo de pacientes que já toleravam lítio ou valproato como monoterapia, as taxas de descontinuação devido a reações adversas foram de 12% para pacientes tratados com ABILIFY adjuvante em comparação com 6% para pacientes tratados com placebo adjuvante. As reações adversas medicamentosas mais comuns associadas à descontinuação nos pacientes tratados com ABILIFY adjuvante em comparação com os pacientes tratados com placebo foram acatisia (5% e 1%, respectivamente) e tremor (2% e 1%, respectivamente).
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao ABILIFY adjuvante e lítio ou valproato em pacientes com mania bipolar (incidência de 5% ou mais e incidência de pelo menos o dobro do placebo adjuvante) foram: acatisia, insônia e distúrbio extrapiramidal.
Reações adversas menos comuns em pacientes adultos com terapia adjuvante na mania bipolar
A Tabela 18 enumera a incidência, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante o tratamento agudo (até 6 semanas), incluindo apenas aquelas reações que ocorreram em 2% ou mais dos pacientes tratados com ABILIFY adjuvante (doses de 15 ou 30 mg/dia) e lítio ou valproato e para os quais a incidência em pacientes tratados com esta combinação foi maior do que a incidência em pacientes tratados com placebo mais lítio ou valproato.
Pacientes pediátricos (13 a 17 anos) com esquizofrenia
Os achados a seguir são baseados em um estudo controlado por placebo de 6 semanas no qual ABILIFY oral foi administrado em doses variando de 2 a 30 mg/dia.
Reações Adversas Associadas à Descontinuação do Tratamento
A incidência de descontinuação devido a reações adversas entre pacientes pediátricos tratados com ABILIFY e tratados com placebo (13 a 17 anos) foi de 5% e 2%, respectivamente.
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao uso de ABILIFY 10mg em pacientes adolescentes com esquizofrenia (incidência de 5% ou mais e incidência de ABILIFY pelo menos o dobro do placebo) foram distúrbios extrapiramidais, sonolência e tremor.
Pacientes pediátricos (10 a 17 anos) com mania bipolar
Os achados a seguir são baseados em um estudo controlado por placebo de 4 semanas no qual ABILIFY oral foi administrado em doses de 10 ou 30 mg/dia.
Reações Adversas Associadas à Descontinuação do Tratamento
A incidência de descontinuação devido a reações adversas entre pacientes pediátricos tratados com ABILIFY e tratados com placebo (10 a 17 anos) foi de 7% e 2%, respectivamente.
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao uso de ABILIFY 20mg em pacientes pediátricos com mania bipolar (incidência de 5% ou mais e incidência de ABILIFY pelo menos o dobro do placebo) são mostradas na Tabela 19.
Pacientes pediátricos (6 a 17 anos) com transtorno autista
Os achados a seguir são baseados em dois estudos de 8 semanas, controlados por placebo, nos quais ABILIFY 20 mg oral foi administrado em doses de 2 a 15 mg/dia.
Reações Adversas Associadas à Descontinuação do Tratamento
A incidência de descontinuação devido a reações adversas entre pacientes pediátricos tratados com ABILIFY e tratados com placebo (6 a 17 anos) foi de 10% e 8%, respectivamente.
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao uso de ABILIFY em pacientes pediátricos com transtorno autista (incidência de 5% ou mais e incidência de ABILIFY 10mg pelo menos o dobro do placebo) são mostradas na Tabela 20.
Pacientes pediátricos (6 a 18 anos) com transtorno de Tourette
Os achados a seguir são baseados em um estudo controlado por placebo de 8 semanas e um de 10 semanas nos quais ABILIFY 15mg oral foi administrado em doses de 2 a 20 mg/dia.
Reações Adversas Associadas à Descontinuação do Tratamento
A incidência de descontinuação devido a reações adversas entre pacientes pediátricos tratados com ABILIFY e tratados com placebo (6 a 18 anos) foi de 7% e 1%, respectivamente.
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao uso de ABILIFY em pacientes pediátricos com transtorno de Tourette (incidência de 5% ou mais e incidência de ABILIFY 10mg pelo menos duas vezes maior que a do placebo) são mostradas na Tabela 21.
Reações adversas menos comuns em pacientes pediátricos (6 a 18 anos) com esquizofrenia, mania bipolar, transtorno autista ou transtorno de Tourette
Tabela 22 enumera a incidência combinada, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até 6 semanas na esquizofrenia, até 4 semanas na mania bipolar, até 8 semanas no transtorno autista e até 10 semanas na doença de Tourette), incluindo apenas as reações que ocorreram em 2% ou mais dos pacientes pediátricos tratados com ABILIFY (doses ≥2 mg/dia) e para as quais a incidência em pacientes tratados com ABILIFY 10mg foi maior do que a incidência em pacientes tratados com placebo.
Pacientes adultos recebendo ABILIFY como tratamento adjuvante do transtorno depressivo maior
Os achados a seguir são baseados em um conjunto de dois estudos controlados por placebo de pacientes com transtorno depressivo maior nos quais ABILIFY 20 mg foi administrado em doses de 2 mg a 20 mg como tratamento adjuvante à terapia antidepressiva continuada.
Reações Adversas Associadas à Descontinuação do Tratamento
incidência de descontinuação devido a reações adversas foi de 6% para pacientes tratados com ABILIFY adjuvante e 2% para pacientes tratados com placebo adjuvante.
Reações Adversas Comumente Observadas
As reações adversas comumente observadas associadas ao uso adjuvante de ABILIFY 15mg em pacientes com transtorno depressivo maior (incidência de 5% ou mais e ABILIFY 15mg incidência de pelo menos o dobro do placebo) foram: acatisia, inquietação, insônia, constipação, fadiga e visão embaçada.
Reações adversas menos comuns em pacientes adultos com transtorno depressivo maior
Tabela 23 enumera a incidência combinada, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até 6 semanas), incluindo apenas as reações adversas que ocorreram em 2% ou mais dos pacientes tratados com ABILIFY adjuvante (doses ≥2 mg/dia) e para os quais a incidência em pacientes tratados com ABILIFY 10 mg adjuvante foi maior do que a incidência em pacientes tratados com placebo adjuvante no conjunto de dados combinado.
Pacientes com agitação associada à esquizofrenia ou mania bipolar (injeção intramuscular)
Os achados a seguir são baseados em um conjunto de três estudos controlados por placebo de pacientes com agitação associada à esquizofrenia ou mania bipolar nos quais ABILIFY 20 mg foi administrado em doses de 5,25 mg a 15 mg.
Reações Adversas Comumente Observadas
Houve uma reação adversa comumente observada (náusea) associada ao uso de ABILIFY 10mg injetável em pacientes com agitação associada à esquizofrenia e mania bipolar (incidência de 5% ou mais e ABILIFY 20mg incidência pelo menos o dobro do placebo).
Reações adversas menos comuns em pacientes com agitação associada à esquizofrenia ou mania bipolar
A Tabela 24 enumera a incidência combinada, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (24 horas), incluindo apenas aquelas reações adversas que ocorreram em 2% ou mais dos pacientes tratados com injeção de ABILIFY (doses ≥5,25 mg /dia) e para os quais a incidência em pacientes tratados com injeção de ABILIFY 15mg foi maior do que a incidência em pacientes tratados com placebo no conjunto de dados combinado.
Reações Adversas Relacionadas à Dose
Esquizofrenia
As relações dose-resposta para a incidência de eventos adversos emergentes do tratamento foram avaliadas a partir de quatro ensaios em pacientes adultos com esquizofrenia comparando várias doses fixas (2, 5, 10, 15, 20 e 30 mg/dia) de ABILIFY oral com placebo. Esta análise, estratificada por estudo, indicou que a única reação adversa a ter uma possível relação dose-resposta, e então mais proeminente apenas com 30 mg, foi sonolência [incluindo sedação]; (as incidências foram placebo, 7,1%; 10 mg, 8,5%; 15 mg, 8,7%; 20 mg, 7,5%; 30 mg, 12,6%).
No estudo de pacientes pediátricos (13 a 17 anos de idade) com esquizofrenia, três reações adversas comuns pareciam ter uma possível relação dose-resposta: distúrbio extrapiramidal (as incidências foram placebo, 5,0%; 10 mg, 13,0%; 30 mg, 21,6 %); sonolência (as incidências foram placebo, 6,0%; 10 mg, 11,0%; 30 mg, 21,6%); e tremor (as incidências foram placebo, 2,0%; 10 mg, 2,0%; 30 mg, 11,8%).
Mania Bipolar
No estudo de pacientes pediátricos (10 a 17 anos de idade) com mania bipolar, quatro reações adversas comuns tiveram uma possível relação dose-resposta em 4 semanas; distúrbio extrapiramidal (as incidências foram placebo, 3,1%; 10 mg, 12,2%; 30 mg, 27,3%); sonolência (as incidências foram placebo, 3,1%; 10 mg, 19,4%; 30 mg, 26,3%); acatisia (as incidências foram placebo, 2,1%; 10 mg, 8,2%; 30 mg, 11,1%); e hipersecreção salivar (as incidências foram placebo, 0%; 10 mg, 3,1%; 30 mg, 8,1%).
Transtorno Autista
Em um estudo de pacientes pediátricos (6 a 17 anos de idade) com transtorno autista, uma reação adversa comum teve uma possível relação dose-resposta: fadiga (as incidências foram placebo, 0%; 5 mg, 3,8%; 10 mg, 22,0%; 15 mg, 18,5%).
Transtorno de Tourette
Em um estudo de pacientes pediátricos (7 a 17 anos de idade) com transtorno de Tourette, nenhuma reação adversa comum teve relação dose-resposta.
Sintomas extrapiramidais
Esquizofrenia
Em estudos de curto prazo controlados por placebo em esquizofrenia em adultos, a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados à acatisia, para pacientes tratados com ABILIFY foi de 13% vs. 12% para placebo; e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY foi de 8% vs. 4% para placebo. No estudo de curto prazo, controlado por placebo, de esquizofrenia em pacientes pediátricos (13 a 17 anos), a incidência de eventos relacionados à EPS relatados, excluindo eventos relacionados à acatisia, para pacientes tratados com ABILIFY foi de 25% vs. 7% para placebo; e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY foi de 9% vs. 6% para placebo.
Os dados coletados objetivamente desses ensaios foram coletados na Simpson Angus Rating Scale (para EPS), na Barnes Akathisia Scale (para acatisia) e nas Assessments of Involuntary Movement Scales (para discinesias). Nos estudos de esquizofrenia em adultos, os dados coletados objetivamente não mostraram diferença entre ABILIFY 10mg e placebo, com exceção da Escala de Acatisia de Barnes (ABILIFY 20mg, 0,08; placebo, -0,05). No estudo de esquizofrenia pediátrico (13 a 17 anos), os dados coletados objetivamente não mostraram diferença entre ABILIFY 20mg e placebo, com exceção da Simpson Angus Rating Scale (ABILIFY 20mg, 0,24; placebo, -0,29).
Da mesma forma, em um estudo de longo prazo (26 semanas), controlado por placebo de esquizofrenia em adultos, dados coletados objetivamente na Simpson Angus Rating Scale (para EPS), na Barnes Akathisia Scale (para acatisia) e nas Avaliações de Involuntary As Escalas de Movimento (para discinesias) não mostraram diferença entre ABILIFY e placebo.
Mania Bipolar
Nos estudos de curto prazo, controlados por placebo em mania bipolar em adultos, a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados à acatisia, para pacientes tratados com ABILIFY em monoterapia foi de 16% vs. 8% para placebo e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY em monoterapia foi de 13% vs. 4% para placebo. No estudo controlado por placebo de 6 semanas em mania bipolar para terapia adjuvante com lítio ou valproato, a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados à acatisia para pacientes tratados com ABILIFY adjuvante foi de 15% vs. 8% para adjuvante placebo e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY adjuvante foi de 19% vs. 5% para placebo adjuvante. No estudo controlado por placebo de curto prazo em mania bipolar em pacientes pediátricos (10 a 17 anos), a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados à acatisia, para pacientes tratados com ABILIFY foi de 26% vs. 5% para placebo e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY foi de 10% vs. 2% para placebo.
Nos estudos de mania bipolar em adultos com ABILIFY em monoterapia, a Simpson Angus Rating Scale e a Barnes Akathisia Scale mostraram uma diferença significativa entre ABILIFY 15mg e placebo (ABILIFY, 0,50; placebo, -0,01 e ABILIFY 10mg, 0,21; placebo, -0,05). As alterações nas avaliações das escalas de movimento involuntário foram semelhantes para os grupos ABILIFY 15mg e placebo. Nos ensaios de mania bipolar com ABILIFY 20mg como terapia adjuvante com lítio ou valproato, a Simpson Angus Rating Scale e a Barnes Akathisia Scale mostraram uma diferença significativa entre ABILIFY adjuvante e placebo adjuvante (ABILIFY 20mg, 0,73; placebo, 0,07 e ABILIFY 10mg, 0,30; placebo, 0,11). As alterações nas avaliações das escalas de movimento involuntário foram semelhantes para ABILIFY 20mg adjuvante e placebo adjuvante. No ensaio de mania bipolar pediátrica (10 a 17 anos), de curto prazo, a Simpson Angus Rating Scale mostrou uma diferença significativa entre ABILIFY 10mg e placebo (ABILIFY 15mg, 0,90; placebo, -0,05). As alterações na Escala de Acatisia de Barnes e nas Escalas de Avaliação de Movimentos Involuntários foram semelhantes para os grupos ABILIFY 20mg e placebo.
Transtorno Depressivo Maior
Nos estudos de curto prazo, controlados por placebo em transtorno depressivo maior, a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados a acatisia, para pacientes tratados com ABILIFY adjuvante foi de 8% vs. 5% para pacientes tratados com placebo adjuvante; e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY adjuvante foi de 25% vs. 4% para pacientes tratados com placebo adjuvante.
Nos estudos de transtorno depressivo maior, a Simpson Angus Rating Scale e a Barnes Akathisia Scale mostraram uma diferença significativa entre ABILIFY adjuvante e placebo adjuvante (ABILIFY 10mg, 0,31; placebo, 0,03 e ABILIFY, 0,22; placebo, 0,02). As alterações nas avaliações das escalas de movimento involuntário foram semelhantes para os grupos adjuvante ABILIFY e placebo adjuvante.
Transtorno Autista
Nos estudos de curto prazo, controlados por placebo em transtorno autista em pacientes pediátricos (6 a 17 anos), a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados à acatisia, para pacientes tratados com ABILIFY foi de 18% vs. 2% para placebo e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY foi de 3% vs. 9% para placebo.
Nos estudos pediátricos (6 a 17 anos) de transtorno autista de curto prazo, a Simpson Angus Rating Scale mostrou uma diferença significativa entre ABILIFY e placebo (ABILIFY 20mg, 0,1; placebo, -0,4). As alterações na Escala de Acatisia de Barnes e nas Escalas de Avaliação de Movimentos Involuntários foram semelhantes para os grupos ABILIFY 10mg e placebo.
Transtorno de Tourette
Nos estudos de curto prazo, controlados por placebo, no transtorno de Tourette em pacientes pediátricos (6 a 18 anos), a incidência de eventos relacionados a EPS relatados, excluindo eventos relacionados à acatisia, para pacientes tratados com ABILIFY foi de 7% vs. 6% para placebo e a incidência de eventos relacionados à acatisia para pacientes tratados com ABILIFY foi de 4% vs. 6% para placebo.
Nos estudos pediátricos (6 a 18 anos) de curto prazo sobre o transtorno de Tourette, as alterações na Escala de Avaliação de Simpson Angus, Escala de Acatisia de Barnes e Escala de Avaliações de Movimento Involuntário não foram clinicamente significativamente diferentes para ABILIFY 15mg e placebo.
Agitação associada à esquizofrenia ou mania bipolar
Nos estudos controlados por placebo em pacientes com agitação associada a esquizofrenia ou mania bipolar, a incidência de eventos relacionados a EPS relatados excluindo eventos relacionados a acatisia para pacientes tratados com ABILIFY foi de 2% vs. 2% para placebo e a incidência de acatisia- eventos relacionados para pacientes tratados com ABILIFY foi de 2% vs. 0% para placebo. Dados coletados objetivamente na Simpson Angus Rating Scale (para EPS) e na Barnes Akathisia Scale (para acatisia) para todos os grupos de tratamento não mostraram diferença entre ABILIFY 10mg e placebo.
Distonia
Sintomas de distonia, contrações anormais prolongadas de grupos musculares, podem ocorrer em indivíduos suscetíveis durante os primeiros dias de tratamento. Os sintomas distônicos incluem: espasmo dos músculos do pescoço, algumas vezes progredindo para aperto na garganta, dificuldade para engolir, dificuldade para respirar e/ou protrusão da língua. Embora esses sintomas possam ocorrer em doses baixas, eles ocorrem com mais frequência e com maior gravidade com alta potência e em doses mais altas de medicamentos antipsicóticos de primeira geração. Um risco elevado de distonia aguda é observado em homens e grupos etários mais jovens.
Achados Adicionais Observados em Ensaios Clínicos
Reações Adversas em Ensaios de Longo Prazo, Duplo-Cego e Controlados por Placebo
As reações adversas relatadas em um estudo duplo-cego de 26 semanas comparando ABILIFY 10mg oral e placebo em pacientes com esquizofrenia foram geralmente consistentes com aquelas relatadas nos estudos controlados por placebo de curto prazo, exceto por uma maior incidência de tremor [8]. % (12/153) para ABILIFY 20mg vs. 2% (3/153) para placebo]. Neste estudo, a maioria dos casos de tremor foi de intensidade leve (8/12 leve e 4/12 moderada), ocorreu no início da terapia (9/12 ≤49 dias) e teve duração limitada (7/12 ≤ 10 dias). O tremor raramente levou à descontinuação (
Outras reações adversas observadas durante a avaliação pré-comercialização de ABILIFY
lista a seguir não inclui reações: 1) já listadas nas tabelas anteriores ou em outro lugar na bula, 2) para as quais a causa do medicamento era remota, 3) que eram tão gerais que não eram informativas, 4) que não foram consideradas como tendo implicações clínicas, ou 5) que ocorreram a uma taxa igual ou inferior ao placebo.
As reações são categorizadas por sistema corporal de acordo com as seguintes definições: reações adversas frequentes são aquelas que ocorrem em pelo menos 1/100 pacientes; reações adversas infrequentes são aquelas que ocorrem em 1/100 a 1/1.000 pacientes; reações raras são aquelas que ocorrem em menos de 1/1.000 pacientes:
Adultos - Administração Oral
Distúrbios do Sangue e do Sistema Linfático: raro - trombocitopenia
Distúrbios cardíacos: infrequentes - bradicardia, palpitações, raros - flutter atrial, parada cardiorrespiratória, bloqueio atrioventricular, fibrilação atrial, angina pectoris, isquemia miocárdica, infarto do miocárdio, insuficiência cardiopulmonar
Distúrbios oculares: infrequente - fotofobia; raro - diplopia
Problemas gastrointestinais: infrequente - doença do refluxo gastroesofágico
Distúrbios Gerais e Condições do Local de Administração: frequente - astenia; infrequente - edema periférico, dor torácica; raro - edema facial
Distúrbios hepatobiliares: raros - hepatite, icterícia
Distúrbios do sistema imunológico : raro - hipersensibilidade
Lesões, Intoxicações e Complicações do Procedimento: infrequente - queda; raro - insolação
Investigações: frequente - diminuição do peso, pouco frequente - aumento da enzima hepática, aumento da glicemia, aumento da lactato desidrogenase sanguínea, aumento da gama glutamil transferase; raros - aumento da prolactina no sangue, aumento da ureia no sangue, aumento da creatinina no sangue, aumento da bilirrubina no sangue, prolongamento do intervalo QT no eletrocardiograma, aumento da hemoglobina glicosilada
Distúrbios do Metabolismo e Nutrição: freqüente - anorexia; raros - hipocalemia, hiponatremia, hipoglicemia
Distúrbios musculoesqueléticos e do tecido conjuntivo: infrequente - fraqueza muscular, rigidez muscular; raros - rabdomiólise, diminuição da mobilidade
Distúrbios do sistema nervoso: infrequente - parkinsonismo, comprometimento da memória, rigidez de roda dentada, hipocinesia, bradicinesia; raros - acinesia, mioclonia, coordenação anormal, distúrbio da fala, convulsão Grand Mal;
Distúrbios psiquiátricos: infrequente - agressão, perda de libido, delírio; raros - aumento da libido, anorgasmia, tiques, ideação homicida, catatonia, sonambulismo
Distúrbios Renais e Urinários: raros - retenção urinária, noctúria
Distúrbios do sistema reprodutor e da mama: infrequente - disfunção erétil; raros - ginecomastia, menstruação irregular, amenorreia, dor mamária, priapismo
Distúrbios respiratórios, torácicos e mediastinais: infrequentes - congestão nasal, dispnéia
Distúrbios da Pele e Tecidos Subcutâneos: infrequente - erupção cutânea, hiperidrose, prurido, reação de fotossensibilidade, alopecia; raro - urticária
Distúrbios Vasculares: pouco frequente - hipotensão, hipertensão
Pacientes Pediátricos - Administração Oral
A maioria dos eventos adversos observados no banco de dados agrupado de 1.686 pacientes pediátricos, com idades entre 6 e 18 anos, também foram observados na população adulta. As reações adversas adicionais observadas na população pediátrica estão listadas abaixo.
Distúrbios oculares infrequente - crise oculogírica
Problemas gastrointestinais: infrequente - língua seca, espasmo da língua
Investigações: frequente - aumento da insulina no sangue
Distúrbios do sistema nervoso: infrequente - dormir falando
Distúrbios Renais e Urinários frequente - enurese
Distúrbios da Pele e Tecidos Subcutâneos: infrequente - hirsutismo
Adultos - Injeção Intramuscular
maioria das reações adversas observadas no banco de dados agrupado de 749 pacientes adultos tratados com a injeção de ABILIFY também foram observadas na população adulta tratada com ABILIFY oral. As reações adversas adicionais observadas na população de injeção de ABILIFY estão listadas abaixo.
Distúrbios Gerais e Condições do Local de Administração: ≥1/100 pacientes - reação no local da injeção; ≥1/1000 pacientes e
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de ABILIFY. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estabelecer uma relação causal com a exposição ao medicamento: ocorrências de reação alérgica (reação anafilática, angioedema, laringoespasmo, prurido/urticária ou espasmo orofaríngeo), jogo patológico , soluços e flutuação da glicose no sangue.
INTERAÇÕES MEDICAMENTOSAS
Medicamentos com interações clinicamente importantes com o ABILIFY
Medicamentos que não têm interações clinicamente importantes com o ABILIFY
Com base em estudos farmacocinéticos, não é necessário ajuste de dose de ABILIFY quando administrado concomitantemente com famotidina, valproato, lítio, lorazepam.
Além disso, nenhum ajuste de dose é necessário para substratos de CYP2D6 (por exemplo, dextrometorfano, fluoxetina, paroxetina ou venlafaxina), CYP2C9 (por exemplo, varfarina), CYP2C19 (por exemplo, omeprazol, varfarina, escitalopram) ou CYP3A4 (por exemplo, dextrometorfano) quando coadministrado com ABILIFY. Além disso, nenhum ajuste de dose é necessário para valproato, lítio, lamotrigina, lorazepam ou sertralina quando coadministrados com ABILIFY [ver FARMACOLOGIA CLÍNICA ].
Abuso e Dependência de Drogas
Substância controlada
ABILIFY não é uma substância controlada.
Abuso
ABILIFY não foi sistematicamente estudado em humanos por seu potencial de abuso, tolerância ou dependência física. Consequentemente, os pacientes devem ser avaliados cuidadosamente quanto a histórico de abuso de drogas, e esses pacientes devem ser observados atentamente quanto a sinais de uso indevido ou abuso de ABILIFY 20mg (por exemplo, desenvolvimento de tolerância, aumento da dose, comportamento de busca de drogas).
Dependência
Em estudos de dependência física em macacos, foram observados sintomas de abstinência após a interrupção abrupta da administração. Embora os ensaios clínicos não tenham revelado qualquer tendência para qualquer comportamento de busca de drogas, essas observações não foram sistemáticas e não é possível prever com base nesta experiência limitada até que ponto um medicamento ativo no SNC será mal utilizado, desviado, e/ou abusado uma vez comercializado.
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Aumento da mortalidade em pacientes idosos com psicose relacionada à demência
Aumento da mortalidade
Pacientes idosos com psicose relacionada à demência tratados com medicamentos antipsicóticos apresentam risco aumentado de morte. ABILIFY (aripiprazol) não está aprovado para o tratamento de pacientes com psicose relacionada à demência [ver ADVERTÊNCIA NA CAIXA].
Experiência de segurança em pacientes idosos com psicose associada à doença de Alzheimer
Em três estudos de 10 semanas controlados por placebo de ABILIFY 10mg em pacientes idosos com psicose associada à doença de Alzheimer (n=938; idade média: 82,4 anos; intervalo: 56-99 anos), as reações adversas que foram relatados com incidência ≥3% e incidência de ABILIFY 15mg pelo menos duas vezes maior que a do placebo foram letargia [placebo 2%, ABILIFY 5%], sonolência (incluindo sedação) [placebo 3%, ABILIFY 8%] e incontinência (principalmente , incontinência urinária) [placebo 1%, ABILIFY 5%], salivação excessiva [placebo 0%, ABILIFY 4%] e tonturas [placebo 1%, ABILIFY 4%].
segurança e eficácia de ABILIFY 15mg no tratamento de pacientes com psicose associada à demência não foram estabelecidas. Se o prescritor optar por tratar esses pacientes com ABILIFY 15mg, avalie o surgimento de dificuldade para engolir ou sonolência excessiva, o que pode predispor a lesão acidental ou aspiração [ver AVISO EM CAIXA ].
Eventos Adversos Cerebrovasculares, Incluindo AVC
Em estudos clínicos controlados por placebo (dois estudos de dose flexível e um estudo de dose fixa) de psicose relacionada à demência, houve um aumento na incidência de eventos adversos cerebrovasculares (por exemplo, acidente vascular cerebral, ataque isquêmico transitório), incluindo fatalidades, em pacientes tratados com ABILIFY ( idade média: 84 anos; intervalo: 78-88 anos). No estudo de dose fixa, houve uma relação dose-resposta estatisticamente significativa para eventos adversos cerebrovasculares em pacientes tratados com ABILIFY. ABILIFY não está aprovado para o tratamento de pacientes com psicose relacionada à demência [ver AVISO EM CAIXA ].
Pensamentos e Comportamentos Suicidas em Crianças, Adolescentes e Jovens Adultos
Pacientes com transtorno depressivo maior (TDM), adultos e pediátricos, podem apresentar piora de sua depressão e/ou surgimento de ideação e comportamento suicida (suicidalidade) ou mudanças incomuns de comportamento, estejam ou não tomando medicamentos antidepressivos, e isso risco pode persistir até que ocorra remissão significativa. O suicídio é um risco conhecido de depressão e alguns outros distúrbios psiquiátricos, e esses distúrbios são os mais fortes preditores de suicídio. Há uma preocupação de longa data, no entanto, de que os antidepressivos possam ter um papel na indução do agravamento da depressão e do surgimento de tendências suicidas em certos pacientes durante as fases iniciais do tratamento. Análises combinadas de estudos de curto prazo, controlados por placebo, de medicamentos antidepressivos (ISRSs e outros) mostraram que esses medicamentos aumentam o risco de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens (18 a 24 anos) com TDM e outros transtornos psiquiátricos. Estudos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução com antidepressivos em comparação com placebo em adultos com 65 anos ou mais.
As análises agrupadas de estudos controlados por placebo em crianças e adolescentes com TDM, Transtorno Obsessivo Compulsivo (TOC) ou outros transtornos psiquiátricos incluíram um total de 24 estudos de curto prazo de 9 medicamentos antidepressivos em mais de 4.400 pacientes. As análises agrupadas de estudos controlados por placebo em adultos com TDM ou outros transtornos psiquiátricos incluíram um total de 295 estudos de curto prazo (duração média de 2 meses) de 11 medicamentos antidepressivos em mais de 77.000 pacientes. Houve variação considerável no risco de suicídio entre as drogas, mas uma tendência de aumento nos pacientes mais jovens para quase todas as drogas estudadas. Houve diferenças no risco absoluto de suicídio entre as diferentes indicações, com maior incidência no TDM. As diferenças de risco (droga versus placebo), no entanto, foram relativamente estáveis dentro dos estratos de idade e entre as indicações. Essas diferenças de risco (diferença droga-placebo no número de casos de suicídio por 1.000 pacientes tratados) são fornecidas na Tabela 5.
Nenhum suicídio ocorreu em qualquer um dos ensaios pediátricos. Houve suicídios nos ensaios com adultos, mas o número não foi suficiente para chegar a qualquer conclusão sobre o efeito da droga no suicídio.
Não se sabe se o risco de suicídio se estende ao uso a longo prazo, ou seja, além de vários meses. No entanto, há evidências substanciais de ensaios de manutenção controlados por placebo em adultos com depressão de que o uso de antidepressivos pode retardar a recorrência da depressão.
Todos os pacientes em tratamento com antidepressivos para qualquer indicação devem ser monitorados adequadamente e observados de perto quanto a piora clínica, tendências suicidas e mudanças incomuns de comportamento, especialmente durante os primeiros meses de um curso de terapia medicamentosa, ou em momentos de mudanças de dose, ou aumentos ou diminui.
Os seguintes sintomas, ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (agitação psicomotora), hipomania e mania, foram relatados em pacientes adultos e pediátricos tratados com antidepressivos para TDM, bem como para outras indicações, tanto psiquiátricas como não psiquiátricas. Embora não tenha sido estabelecida uma relação causal entre o surgimento de tais sintomas e o agravamento da depressão e/ou o surgimento de impulsos suicidas, existe a preocupação de que tais sintomas possam representar precursores de tendências suicidas emergentes.
Deve-se considerar a mudança do regime terapêutico, incluindo a possibilidade de descontinuação da medicação, em pacientes cuja depressão é persistentemente pior, ou que estão experimentando tendências suicidas emergentes ou sintomas que podem ser precursores de piora da depressão ou tendências suicidas, especialmente se esses sintomas forem graves, abruptos no início, ou não faziam parte dos sintomas de apresentação do paciente.
Familiares e cuidadores de pacientes em tratamento com antidepressivos para transtorno depressivo maior ou outras indicações, tanto psiquiátricas quanto não psiquiátricas, devem ser alertados sobre a necessidade de monitorar os pacientes quanto ao surgimento de agitação, irritabilidade, alterações incomuns de comportamento e outros sintomas descritos acima , bem como o surgimento de tendências suicidas, e relatar tais sintomas imediatamente aos profissionais de saúde. Tal monitoramento deve incluir observação diária por familiares e cuidadores. As prescrições de ABILIFY devem ser feitas para a menor quantidade de comprimidos consistente com o bom manejo do paciente, a fim de reduzir o risco de superdosagem.
Triagem de pacientes para transtorno bipolar
Um episódio depressivo maior pode ser a apresentação inicial do transtorno bipolar. Acredita-se geralmente (embora não estabelecido em ensaios controlados) que o tratamento de tal episódio com um antidepressivo sozinho pode aumentar a probabilidade de precipitação de um episódio misto/maníaco em pacientes com risco de transtorno bipolar. Não se sabe se algum dos sintomas descritos acima representa tal conversão. No entanto, antes de iniciar o tratamento com um antidepressivo, os pacientes com sintomas depressivos devem ser examinados adequadamente para determinar se estão em risco de transtorno bipolar; essa triagem deve incluir uma história psiquiátrica detalhada, incluindo uma história familiar de suicídio, transtorno bipolar e depressão.
Deve-se notar que ABILIFY 20mg não está aprovado para uso no tratamento da depressão na população pediátrica.
Síndrome Neuroléptica Maligna (SNM)
Um complexo de sintomas potencialmente fatal, algumas vezes referido como Síndrome Neuroléptica Maligna (SNM), pode ocorrer com a administração de medicamentos antipsicóticos, incluindo ABILIFY. casos raros de SNM ocorreram durante o tratamento com ABILIFY 15mg no banco de dados clínico mundial. As manifestações clínicas da SNM são hiperpirexia, rigidez muscular, estado mental alterado e evidência de instabilidade autonômica (pulso ou pressão arterial irregulares, taquicardia, sudorese e disritmia cardíaca). Sinais adicionais podem incluir creatina fosfoquinase elevada, mioglobinúria (rabdomiólise) e insuficiência renal aguda.
avaliação diagnóstica de pacientes com esta síndrome é complicada. Ao chegar a um diagnóstico, é importante excluir casos em que a apresentação clínica inclui tanto doença médica grave (por exemplo, pneumonia, infecção sistêmica) quanto sinais e sintomas extrapiramidais (SEP) não tratados ou tratados inadequadamente. Outras considerações importantes no diagnóstico diferencial incluem toxicidade anticolinérgica central, insolação, febre medicamentosa e patologia primária do sistema nervoso central.
O manejo da SNM deve incluir: 1) descontinuação imediata de drogas antipsicóticas e outras drogas não essenciais à terapia concomitante; 2) tratamento sintomático intensivo e acompanhamento médico; e 3) tratamento de quaisquer problemas médicos graves concomitantes para os quais existam tratamentos específicos disponíveis. Não existe um acordo geral sobre regimes de tratamento farmacológico específico para SNM não complicada.
Se um paciente necessitar de tratamento medicamentoso antipsicótico após a recuperação da SNM, a potencial reintrodução da terapia medicamentosa deve ser cuidadosamente considerada. O paciente deve ser cuidadosamente monitorado, uma vez que foram relatadas recorrências de SNM.
Discinesia tardia
Uma síndrome de movimentos discinéticos involuntários e potencialmente irreversíveis pode se desenvolver em pacientes tratados com drogas antipsicóticas. Embora a prevalência da síndrome pareça ser maior entre os idosos, especialmente as mulheres idosas, é impossível confiar nas estimativas de prevalência para prever, no início do tratamento antipsicótico, quais pacientes provavelmente desenvolverão a síndrome. Se os medicamentos antipsicóticos diferem em seu potencial para causar discinesia tardia é desconhecido.
Acredita-se que o risco de desenvolver discinesia tardia e a probabilidade de que se torne irreversível aumente à medida que a duração do tratamento e a dose cumulativa total de drogas antipsicóticas administradas ao paciente aumentam. No entanto, a síndrome pode se desenvolver, embora muito menos comumente, após períodos de tratamento relativamente breves com doses baixas.
A discinesia tardia pode regredir, parcial ou completamente, se o tratamento antipsicótico for retirado. O tratamento antipsicótico, no entanto, pode suprimir (ou suprimir parcialmente) os sinais e sintomas da síndrome e, assim, pode mascarar o processo subjacente. O efeito que a supressão sintomática tem sobre o curso a longo prazo da síndrome é desconhecido.
Dadas essas considerações, ABILIFY deve ser prescrito da maneira mais provável de minimizar a ocorrência de discinesia tardia. O tratamento antipsicótico crônico geralmente deve ser reservado para pacientes que sofrem de uma doença crônica que (1) responde aos medicamentos antipsicóticos e (2) para os quais tratamentos alternativos, igualmente eficazes, mas potencialmente menos prejudiciais, não estão disponíveis ou são apropriados. Em pacientes que necessitam de tratamento crônico, deve-se buscar a menor dose e a menor duração do tratamento que produza uma resposta clínica satisfatória. A necessidade de continuação do tratamento deve ser reavaliada periodicamente.
Se surgirem sinais e sintomas de discinesia tardia em um paciente em uso de ABILIFY, a descontinuação do medicamento deve ser considerada. No entanto, alguns pacientes podem necessitar de tratamento com ABILIFY 15mg apesar da presença da síndrome.
Alterações metabólicas
Os antipsicóticos atípicos têm sido associados a alterações metabólicas que incluem hiperglicemia/diabetes mellitus, dislipidemia e ganho de peso corporal. Embora todos os medicamentos da classe tenham demonstrado produzir algumas alterações metabólicas, cada medicamento tem seu próprio perfil de risco específico.
Hiperglicemia/Diabetes Mellitus
Hiperglicemia, em alguns casos extrema e associada a cetoacidose ou coma hiperosmolar ou morte, foi relatada em pacientes tratados com antipsicóticos atípicos. Houve relatos de hiperglicemia em pacientes tratados com ABILIFY [ver REAÇÕES ADVERSAS ]. A avaliação da relação entre o uso de antipsicóticos atípicos e anormalidades da glicose é complicada pela possibilidade de um risco aumentado de diabetes mellitus em pacientes com esquizofrenia e o aumento da incidência de diabetes mellitus na população em geral. Dados esses fatores de confusão, a relação entre o uso de antipsicóticos atípicos e eventos adversos relacionados à hiperglicemia não é completamente compreendida. No entanto, estudos epidemiológicos sugerem um risco aumentado de reações adversas relacionadas à hiperglicemia em pacientes tratados com antipsicóticos atípicos. Como o ABILIFY não foi comercializado no momento em que esses estudos foram realizados, não se sabe se o ABILIFY está associado a esse risco aumentado. Não estão disponíveis estimativas de risco precisas para reações adversas relacionadas à hiperglicemia em pacientes tratados com antipsicóticos atípicos.
Pacientes com diagnóstico estabelecido de diabetes mellitus que iniciaram antipsicóticos atípicos devem ser monitorados regularmente quanto à piora do controle glicêmico. Pacientes com fatores de risco para diabetes mellitus (p. Qualquer paciente tratado com antipsicóticos atípicos deve ser monitorado quanto a sintomas de hiperglicemia, incluindo polidipsia, poliúria, polifagia e fraqueza. Os pacientes que desenvolvem sintomas de hiperglicemia durante o tratamento com antipsicóticos atípicos devem ser submetidos ao teste de glicemia em jejum. Em alguns casos, a hiperglicemia foi resolvida quando o antipsicótico atípico foi descontinuado; entretanto, alguns pacientes necessitaram de continuação do tratamento antidiabético apesar da descontinuação do medicamento suspeito.
Adultos
Em uma análise de 13 estudos de monoterapia controlados por placebo em adultos, principalmente com esquizofrenia ou transtorno bipolar, a alteração média na glicemia de jejum em pacientes tratados com ABILIFY (+4,4 mg/dL; exposição mediana de 25 dias; N = 1.057) não foi significativamente diferente dos pacientes tratados com placebo (+2,5 mg/dL; exposição mediana 22 dias; N=799). A Tabela 6 mostra a proporção de pacientes tratados com ABILIFY com glicemia de jejum normal e limítrofe na linha de base (exposição mediana de 25 dias) que tiveram medições de glicemia de jejum altas emergentes do tratamento em comparação com pacientes tratados com placebo (exposição mediana de 22 dias).
Às 24 semanas, a alteração média na glicemia de jejum em pacientes tratados com ABILIFY não foi significativamente diferente dos pacientes tratados com placebo [+2,2 mg/dL (n=42) e +9,6 mg/dL (n=28), respectivamente] .
alteração média na glicemia de jejum em pacientes tratados com ABILIFY adjuvante com transtorno depressivo maior (+0,7 mg/dL; exposição mediana 42 dias; N=241) não foi significativamente diferente do que em pacientes tratados com placebo (+0,8 mg/dL; mediana exposição 42 dias; N=246). A Tabela 7 mostra a proporção de pacientes adultos com alterações nos níveis de glicose em jejum de dois estudos adjuvantes controlados por placebo (exposição mediana de 42 dias) em pacientes com transtorno depressivo maior.
Pacientes Pediátricos e Adolescentes
Em uma análise de dois estudos controlados por placebo em adolescentes com esquizofrenia (13 a 17 anos) e pacientes pediátricos com transtorno bipolar (10 a 17 anos), a alteração média na glicemia de jejum em pacientes tratados com ABILIFY (+4,8 mg/dL; com uma exposição mediana de 43 dias; N=259) não foi significativamente diferente dos pacientes tratados com placebo (+1,7 mg/dL; com uma exposição mediana de 42 dias; N=123).
Em uma análise de dois estudos controlados por placebo em pacientes pediátricos e adolescentes com irritabilidade associada ao transtorno autista (6 a 17 anos) com exposição mediana de 56 dias, a alteração média na glicemia de jejum em pacientes tratados com ABILIFY (-0,2 mg /dL; N=83) não foi significativamente diferente dos pacientes tratados com placebo (-0,6 mg/dL; N=33).
Em uma análise de dois estudos controlados por placebo em pacientes pediátricos e adolescentes com transtorno de Tourette (6 a 18 anos) com exposição mediana de 57 dias, a alteração média na glicemia de jejum em pacientes tratados com ABILIFY (0,79 mg/dL; N=90) não foi significativamente diferente dos pacientes tratados com placebo (-1,66 mg/dL; N=58).
Tabela 8 mostra a proporção de pacientes com alterações nos níveis de glicose em jejum do grupo de esquizofrenia adolescente e pacientes bipolares pediátricos (exposição mediana de 42-43 dias), de dois estudos controlados por placebo em pacientes pediátricos (6 a 17 anos) com irritabilidade associada com transtorno autista (exposição mediana de 56 dias) e dos dois estudos controlados com placebo em pacientes pediátricos (6 a 18 anos) com transtorno de Tourette (exposição mediana de 57 dias).
Em 12 semanas nos estudos agrupados de esquizofrenia em adolescentes e transtorno bipolar pediátrico, a alteração média na glicemia de jejum em pacientes tratados com ABILIFY não foi significativamente diferente dos pacientes tratados com placebo [+2,4 mg/dL (n=81) e +0,1 mg /dL (n=15), respectivamente].
Dislipidemia
Alterações indesejáveis nos lipídios foram observadas em pacientes tratados com antipsicóticos atípicos.
Não houve diferenças significativas entre os pacientes tratados com ABILIFY e placebo na proporção com alterações de níveis normais para níveis clinicamente significativos para colesterol total em jejum/sem jejum, triglicerídeos em jejum, LDLs em jejum e HDLs em jejum/sem jejum. As análises de pacientes com pelo menos 12 ou 24 semanas de exposição foram limitadas por um pequeno número de pacientes.
Adultos
A Tabela 9 mostra a proporção de pacientes adultos, principalmente de estudos agrupados de monoterapia de esquizofrenia e transtorno bipolar controlados por placebo, com alterações no colesterol total (reunidos de 17 ensaios; exposição mediana de 21 a 25 dias), triglicerídeos em jejum (reunidos de oito ensaios; mediana exposição 42 dias), colesterol LDL em jejum (reunido de oito ensaios; exposição mediana de 39 a 45 dias, exceto para pacientes tratados com placebo com medições normais de LDL em jejum basal, que tiveram exposição mediana ao tratamento de 24 dias) e colesterol HDL (reunido de nove ensaios; exposição mediana de 40 a 42 dias).
Em estudos de monoterapia em adultos, a proporção de pacientes em 12 semanas e 24 semanas com alterações de Normal para Alto no colesterol total (jejum/sem jejum), triglicerídeos em jejum e colesterol LDL em jejum foi semelhante entre os pacientes tratados com ABILIFY e com placebo: em 12 semanas, Colesterol Total (jejum/sem jejum), 1/71 (1,4%) vs. 3/74 (4,1%); Triglicerídeos em jejum, 8/62 (12,9%) vs. 5/37 (13,5%); Colesterol LDL em jejum, 0/34 (0%) vs. 1/25 (4,0%), respectivamente; e às 24 semanas, Colesterol Total (jejum/sem jejum), 1/42 (2,4%) vs. 3/37 (8,1%); Triglicerídeos em jejum, 5/34 (14,7%) vs. 5/20 (25%); Colesterol LDL em jejum, 0/22 (0%) vs. 1/18 (5,6%), respectivamente.
A Tabela 10 mostra a proporção de pacientes com alterações no colesterol total (jejum/sem jejum), triglicerídeos em jejum, colesterol LDL em jejum e colesterol HDL de dois estudos adjuvantes controlados por placebo em pacientes adultos com transtorno depressivo maior (exposição média de 42 dias).
Pacientes Pediátricos e Adolescentes
Tabela 11 mostra a proporção de adolescentes com esquizofrenia (13 a 17 anos) e pacientes pediátricos com transtorno bipolar (10 a 17 anos) com alterações no colesterol total e colesterol HDL (reunidos de dois ensaios controlados por placebo; exposição mediana de 42 a 43 dias ) e triglicerídeos em jejum (reunidos de dois estudos controlados por placebo; exposição mediana de 42 a 44 dias).
Em estudos de monoterapia com adolescentes com esquizofrenia e pacientes pediátricos com transtorno bipolar, a proporção de pacientes em 12 semanas e 24 semanas com alterações de normal para alto no colesterol total (jejum/sem jejum), triglicerídeos em jejum e colesterol LDL em jejum foi semelhante entre ABILIFY - e pacientes tratados com placebo: em 12 semanas, Colesterol Total (jejum/sem jejum), 0/57 Â (0%) vs. 0/15 (0%); Triglicerídeos em jejum, 2/72 (2,8%) vs. 1/14 (7,1%), respectivamente; e às 24 semanas, Colesterol Total (jejum/sem jejum), 0/36 (0%) vs. 0/12 (0%); Triglicerídeos em jejum, 1/47 (2,1%) vs. 1/10 (10,0%), respectivamente.
A Tabela 12 mostra a proporção de pacientes com alterações no colesterol total (jejum/sem jejum) e triglicerídeos em jejum (exposição mediana de 56 dias) e colesterol HDL (exposição mediana de 55 a 56 dias) de dois ensaios controlados por placebo em pacientes pediátricos (6 a 17 anos) com irritabilidade associada ao transtorno autista.
Tabela 13 mostra a proporção de pacientes com alterações no colesterol total (jejum/sem jejum) e triglicerídeos em jejum (exposição mediana de 57 dias) e colesterol HDL (exposição mediana de 57 dias) de dois estudos controlados por placebo em pacientes pediátricos (6 a 18 anos) com Transtorno de Tourette.
Ganho de peso
O ganho de peso foi observado com o uso de antipsicótico atípico. Recomenda-se a monitorização clínica do peso.
Adultos
Em uma análise de 13 estudos de monoterapia controlados por placebo, principalmente de esquizofrenia e transtorno bipolar agrupados, com exposição mediana de 21 a 25 dias, a alteração média no peso corporal em pacientes tratados com ABILIFY foi de +0,3 kg (N = 1.673) em comparação para -0,1 kg (N=1100) em pacientes controlados com placebo. Às 24 semanas, a alteração média da linha de base no peso corporal em pacientes tratados com ABILIFY foi de -1,5 kg (n=73) em comparação com -0,2 kg (n=46) em pacientes tratados com placebo.
Nos ensaios que adicionaram ABILIFY aos antidepressivos, os pacientes receberam primeiro 8 semanas de tratamento antidepressivo, seguido de 6 semanas de ABILIFY 10mg adjuvante ou placebo, além do tratamento antidepressivo em andamento. A alteração média no peso corporal em pacientes que receberam ABILIFY adjuvante foi de +1,7 kg (N=347) em comparação com +0,4 kg (N=330) em pacientes que receberam placebo adjuvante.
A Tabela 14 mostra o percentual de pacientes adultos com ganho de peso ≥7% do peso corporal por indicação.
Pacientes Pediátricos e Adolescentes
Em uma análise de dois estudos controlados por placebo em adolescentes com esquizofrenia (13 a 17 anos) e pacientes pediátricos com transtorno bipolar (10 a 17 anos) com exposição mediana de 42 a 43 dias, a alteração média no peso corporal em pacientes tratados com ABILIFY pacientes foi de +1,6 kg (N=381) comparado a +0,3 kg (N=187) em pacientes tratados com placebo. Às 24 semanas, a alteração média da linha de base no peso corporal em
Os doentes tratados com ABILIFY foi de +5,8 kg (n=62) em comparação com +1,4 kg (n=13) nos doentes tratados com placebo.
Em dois estudos de curto prazo, controlados por placebo em pacientes (6 a 17 anos) com irritabilidade associada ao transtorno autista com exposição mediana de 56 dias, a mudança média no peso corporal em pacientes tratados com ABILIFY foi de +1,6 kg (n=209 ) em comparação com +0,4 kg (n=98) em pacientes tratados com placebo.
Em dois estudos de curto prazo, controlados por placebo em pacientes (6 a 18 anos) com Transtorno de Tourette com exposição mediana de 57 dias, a mudança média no peso corporal em pacientes tratados com ABILIFY foi de +1,5 kg (n=105). ) em comparação com +0,4 kg (n=66) em pacientes tratados com placebo.
A Tabela 15 mostra o percentual de pacientes pediátricos e adolescentes com ganho de peso ≥7% do peso corporal por indicação.
Em um estudo aberto que envolveu pacientes de dois estudos controlados por placebo de adolescentes com esquizofrenia (13 a 17 anos) e pacientes pediátricos com transtorno bipolar (10 a 17 anos), 73,2% dos pacientes (238/325) completaram 26 semanas de terapia com ABILIFY. Após 26 semanas, 32,8% dos pacientes ganharam ≥7% de seu peso corporal, não ajustado para crescimento normal. Para ajustar o crescimento normal, foram derivados escores z (medidos em desvios padrão [DP]), que normalizam para o crescimento natural de pacientes pediátricos e adolescentes em comparação com os padrões populacionais pareados por idade e sexo. Uma alteração no escore z
Em um estudo aberto que envolveu pacientes de dois estudos de curto prazo, controlados por placebo, pacientes (6 a 17 anos) com irritabilidade associada ao transtorno autista, bem como pacientes de novo, 60,3% (199/330) completaram um ano de terapia com ABILIFY. A mudança média no escore z de peso foi de 0,26 DPs para pacientes que receberam > 9 meses de tratamento.
Ao tratar pacientes pediátricos para qualquer indicação, o ganho de peso deve ser monitorado e avaliado em relação ao esperado para o crescimento normal.
Jogo patológico e outros comportamentos compulsivos
Relatos de casos pós-comercialização sugerem que os pacientes podem experimentar desejos intensos, principalmente para jogos de azar, e a incapacidade de controlar esses desejos enquanto tomam aripiprazol. Outros impulsos compulsivos, relatados com menos frequência, incluem: impulsos sexuais, compras, comer ou compulsão alimentar e outros comportamentos impulsivos ou compulsivos. Como os pacientes podem não reconhecer esses comportamentos como anormais, é importante que os prescritores perguntem aos pacientes ou seus cuidadores especificamente sobre o desenvolvimento de novos ou intensos impulsos de jogo, impulsos sexuais compulsivos, compras compulsivas, compulsão alimentar ou compulsão alimentar ou outros impulsos durante o tratamento. com aripiprazol. Deve-se notar que os sintomas de controle de impulsos podem estar associados ao transtorno subjacente. Em alguns casos, embora não em todos, os impulsos cessaram quando a dose foi reduzida ou a medicação foi descontinuada. Comportamentos compulsivos podem resultar em danos ao paciente e a outros se não forem reconhecidos. Considere a redução da dose ou a interrupção da medicação se um paciente desenvolver tais desejos.
Hipotensão ortostática
ABILIFY 20mg pode causar hipotensão ortostática, talvez devido ao seu antagonismo do receptor α1-adrenérgico. A incidência de eventos associados à hipotensão ortostática de estudos de curto prazo, controlados por placebo de pacientes adultos em uso oral de ABILIFY (n=2467) incluiu (incidência de ABILIFY 20mg, incidência de placebo) hipotensão ortostática (1%, 0,3%), tontura postural ( 0,5%, 0,3%) e síncope (0,5%, 0,4%); dos pacientes pediátricos de 6 a 18 anos de idade (n=732) em uso de ABILIFY oral incluíram hipotensão ortostática (0,5%, 0%), tontura postural (0,4%, 0%) e síncope (0,2%, 0%); e dos pacientes em ABILIFY Injection (n=501) incluíram hipotensão ortostática (0,6%, 0%), tontura postural (0,2%, 0,5%) e síncope (0,4%, 0%) [ver REAÇÕES ADVERSAS ].
incidência de uma alteração ortostática significativa na pressão arterial (definida como uma diminuição na pressão arterial sistólica ≥ 20 mmHg acompanhada por um aumento na frequência cardíaca ≥ 25 bpm ao comparar os valores em pé com os valores supino) para ABILIFY não foi significativamente diferente do placebo (incidência de ABILIFY , incidência de placebo): em pacientes adultos tratados com ABILIFY oral (4%, 2%), em
Pacientes tratados com ABILIFY com idade entre 6 e 18 anos (0,4%, 1%), ou em pacientes tratados com injeção de ABILIFY 15mg (3%, 2%).
ABILIFY 20mg deve ser usado com cautela em pacientes com doença cardiovascular conhecida (história de infarto do miocárdio ou doença isquêmica do coração, insuficiência cardíaca ou anormalidades de condução), doença cerebrovascular ou condições que predisponham os pacientes à hipotensão (desidratação, hipovolemia e tratamento com anti-hipertensivos). medicamentos) [ver INTERAÇÕES MEDICAMENTOSAS ].
Se a terapia parenteral com benzodiazepínicos for considerada necessária além do tratamento com injeção de ABILIFY, os pacientes devem ser monitorados para sedação excessiva e hipotensão ortostática [ver INTERAÇÕES MEDICAMENTOSAS ].
Cataratas
Os antipsicóticos, incluindo ABILIFY 10mg, podem causar sonolência, hipotensão postural, instabilidade motora e sensorial, podendo levar a quedas e, consequentemente, fraturas ou outras lesões. Para pacientes com doenças, condições ou medicamentos que possam exacerbar esses efeitos, complete as avaliações de risco de queda ao iniciar o tratamento antipsicótico e recorrentemente para pacientes em terapia antipsicótica de longo prazo.
Leucopenia, neutropenia e agranulocitose
Em ensaios clínicos e/ou experiência pós-comercialização, eventos de leucopenia e neutropenia foram relatados temporariamente relacionados a agentes antipsicóticos, incluindo ABILIFY. Agranulocitose também foi relatada.
Possíveis fatores de risco para leucopenia/neutropenia incluem contagem baixa de glóbulos brancos (WBC)/contagem absoluta de neutrófilos (ANC) pré-existente e história de leucopenia/neutropenia induzida por drogas. Em pacientes com história de WBC/ANC clinicamente significativo ou leucopenia/neutropenia induzida por drogas, realize um hemograma completo (CBC) frequentemente durante os primeiros meses de terapia. Nesses pacientes, considere a descontinuação de ABILIFY ao primeiro sinal de declínio clinicamente significativo nos leucócitos na ausência de outros fatores causais.
Monitore os pacientes com neutropenia clinicamente significativa para febre ou outros sintomas ou sinais de infecção e trate imediatamente se tais sintomas ou sinais ocorrerem. Descontinue ABILIFY 20mg em pacientes com neutropenia grave (contagem absoluta de neutrófilos
Convulsões/convulsões
Em estudos de curto prazo, controlados com placebo, os pacientes com histórico de convulsões excluíram convulsões/convulsões em 0,1% (3/2.467) dos pacientes adultos não diagnosticados tratados com ABILIFY 20mg oral, em 0,1% (1/732) dos pacientes pediátricos (6 a 18 anos) e em 0,2% (1/501) dos pacientes adultos tratados com ABILIFY 15mg.
Assim como outros medicamentos antipsicóticos, ABILIFY 15mg deve ser usado com cautela em pacientes com histórico de convulsões ou com condições que diminuam o limiar convulsivo. Condições que diminuem o limiar convulsivo podem ser mais prevalentes em uma população de 65 anos ou mais.
Potencial para comprometimento cognitivo e motor
ABILIFY, como outros antipsicóticos, pode ter o potencial de prejudicar o julgamento, o pensamento ou as habilidades motoras. Por exemplo, em estudos de curto prazo controlados por placebo, a sonolência (incluindo sedação) foi relatada da seguinte forma (incidência de ABILIFY, incidência de placebo): em pacientes adultos (n=2467) tratados com ABILIFY oral (11%, 6%), em pacientes pediátricos de 6 a 17 anos (n=611) (24%, 6%) e em pacientes adultos (n=501) em ABILIFY Injection (9%, 6%). A sonolência (incluindo sedação) levou à descontinuação em 0,3% (8/2467) dos pacientes adultos e 3% (20/732) dos pacientes pediátricos (6 a 18 anos) em uso oral de ABILIFY 10mg em estudos controlados por placebo de curta duração, mas não levou à descontinuação de nenhum paciente adulto em ABILIFY Injection.
Apesar do aumento relativamente modesto da incidência desses eventos em comparação ao placebo, os pacientes devem ser alertados sobre a operação de máquinas perigosas, incluindo automóveis, até que tenham certeza razoável de que a terapia com ABILIFY 15mg não os afeta adversamente.
Regulação da temperatura corporal
A interrupção da capacidade do corpo de reduzir a temperatura corporal central tem sido atribuída a agentes antipsicóticos. Recomenda-se o cuidado apropriado ao prescrever ABILIFY 10mg para pacientes que apresentarão condições que possam contribuir para uma elevação da temperatura corporal central (por exemplo, exercícios extenuantes, exposição a calor extremo, receber medicação concomitante com atividade anticolinérgica ou estar sujeito a desidratação). [Vejo REAÇÕES ADVERSAS ].
Suicídio
A possibilidade de uma tentativa de suicídio é inerente a doenças psicóticas, transtorno bipolar e transtorno depressivo maior, e a supervisão cuidadosa de pacientes de alto risco deve acompanhar a terapia medicamentosa. As prescrições para ABILIFY devem ser feitas na menor quantidade consistente com o bom manejo do paciente, a fim de reduzir o risco de overdose [ver REAÇÕES ADVERSAS ].
Disfagia
dismotilidade e aspiração esofágica foram associadas ao uso de drogas antipsicóticas, incluindo ABILIFY. A pneumonia aspirativa é uma causa comum de morbidade e mortalidade em pacientes idosos, em particular naqueles com demência de Alzheimer avançada. ABILIFY e outros medicamentos antipsicóticos devem ser usados com cautela em pacientes com risco de pneumonia por aspiração [ver Aumento da Mortalidade em Pacientes Idosos com Psicose Relacionada à Demência  e REAÇÕES ADVERSAS ].
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( Guia de Medicação ).
Discuta as seguintes questões com os pacientes que receberam ABILIFY:
Agravamento clínico da depressão e risco de suicídio
Os pacientes, seus familiares e seus cuidadores devem ser encorajados a estarem alertas para o surgimento de ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (inquietação psicomotora), hipomania, mania, outras alterações incomuns de comportamento , agravamento da depressão e ideação suicida, especialmente no início do tratamento antidepressivo e quando a dose é ajustada para cima ou para baixo. Familiares e cuidadores de pacientes devem ser orientados a procurar diariamente o surgimento de tais sintomas, pois as alterações podem ser abruptas. Tais sintomas devem ser relatados ao prescritor ou profissional de saúde do paciente, especialmente se forem graves, de início abrupto ou não fizerem parte dos sintomas apresentados pelo paciente. Sintomas como esses podem estar associados a um risco aumentado de pensamento e comportamento suicida e indicam a necessidade de monitoramento muito próximo e possivelmente mudanças na medicação [ver AVISOS E PRECAUÇÕES ].
Os prescritores ou outros profissionais de saúde devem informar os pacientes, seus familiares e seus cuidadores sobre os benefícios e riscos associados ao tratamento com ABILIFY e devem aconselhá-los sobre seu uso apropriado. Um Guia de Medicação do paciente incluindo informações sobre “Medicamentos Antidepressivos, Depressão e outras Doenças Mentais Graves e Pensamentos ou Ações Suicidas” está disponível para ABILIFY. O prescritor ou profissional de saúde deve orientar os pacientes, seus familiares e seus cuidadores a ler o Guia de Medicação e auxiliá-los na compreensão de seu conteúdo. Os pacientes devem ter a oportunidade de discutir o conteúdo do Guia de Medicação e obter respostas para quaisquer dúvidas que possam ter. Deve-se notar que ABILIFY não foi aprovado como agente único para o tratamento da depressão e não foi avaliado no transtorno depressivo maior pediátrico.
Jogo patológico e outros comportamentos compulsivos
Aconselhe os pacientes e seus cuidadores sobre a possibilidade de que eles possam experimentar impulsos compulsivos para fazer compras, impulsos intensos para jogar, impulsos sexuais compulsivos, compulsão alimentar e/ou outros impulsos compulsivos e a incapacidade de controlar esses impulsos enquanto estiver tomando aripiprazol. Em alguns casos, mas não em todos, os impulsos cessaram quando a dose foi reduzida ou interrompida [ver AVISOS E PRECAUÇÕES ].
Uso de comprimido de desintegração oral
Não abra o blister até estar pronto para administrar. Para a remoção de um único comprimido, abra a embalagem e retire a película do blister para expor o comprimido. Não empurre o comprimido através da folha, pois isso pode danificar o comprimido. Imediatamente após a abertura do blister, com as mãos secas, retire o comprimido e coloque todo o comprimido desintegrante oral ABILIFY DISCMELT na língua. A desintegração do comprimido ocorre rapidamente na saliva. Recomenda-se que ABILIFY DISCMELT seja tomado sem líquido. No entanto, se necessário, pode ser tomado com líquido. Não tente dividir o tablet.
Interferência com o desempenho cognitivo e motor
Como o ABILIFY pode ter o potencial de prejudicar o julgamento, o pensamento ou as habilidades motoras, os pacientes devem ser alertados sobre a operação de máquinas perigosas, incluindo automóveis, até que tenham certeza razoável de que a terapia com ABILIFY não os afeta adversamente [ver AVISOS E PRECAUÇÕES ].
Medicação concomitante
Os pacientes devem ser aconselhados a informar seus médicos se estiverem tomando ou planejam tomar qualquer medicamento prescrito ou de venda livre, uma vez que existe potencial para interações [ver INTERAÇÕES MEDICAMENTOSAS ].
Exposição ao calor e desidratação
Os pacientes devem ser aconselhados sobre os cuidados apropriados para evitar superaquecimento e desidratação [ver AVISOS E PRECAUÇÕES ].
Conteúdo de açúcar
Os pacientes devem ser informados de que cada mL de ABILIFY 10mg Solução Oral contém 400 mg de sacarose e 200 mg de frutose.
Gravidez
Aconselhe as pacientes a notificarem seu médico se engravidarem ou pretendem engravidar durante o tratamento com ABILIFY. Avise os pacientes que ABILIFY 20mg pode causar sintomas extrapiramidais e/ou de abstinência (agitação, hipertonia, hipotonia, tremor, sonolência, dificuldade respiratória e distúrbio alimentar) em um recém-nascido. Avise as pacientes que existe um registro de gravidez que monitora os resultados da gravidez em mulheres expostas a ABILIFY 15mg durante a gravidez [ver Uso em populações específicas ].
Fenilcetonúricos
A fenilalanina é um componente do aspartame. Cada comprimido de desintegração oral ABILIFY DISCMELT contém as seguintes quantidades: 10 mg, 1,12 mg de fenilalanina e 15 mg, 1,68 mg de fenilalanina.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Carcinogênese
Estudos de carcinogenicidade ao longo da vida foram conduzidos em camundongos ICR, ratos F344 e ratos Sprague-Dawley (SD). Aripiprazol foi administrado por 2 anos na dieta em doses de 1, 3, 10 e 30 mg/kg/dia para camundongos ICR e 1, 3 e 10 mg/kg/dia para ratos F344 (0,2, 0,5, 2 e 5 vezes e 0,3, 1 e 3 vezes a MRHD de 30 mg/dia com base em mg/m² de área de superfície corporal, respectivamente). Além disso, os ratos SD foram administrados oralmente durante 2 anos a 10, 20, 40 e 60 mg/kg/dia, que são 3, 6, 13 e 19 vezes a MRHD com base em mg/m² de área de superfície corporal. O aripiprazol não induziu tumores em camundongos machos ou ratos machos. Em camundongos fêmeas, as incidências de adenomas da glândula pituitária e adenocarcinomas e adenoacantomas da glândula mamária foram aumentadas em doses dietéticas de 3 a 30 mg/kg/dia (0,5 a 5 vezes o MRHD). Em ratas, a incidência de fibroadenomas da glândula mamária aumentou com uma dose dietética de 10 mg/kg/dia (3 vezes a MRHD); e as incidências de carcinomas adrenocorticais e adenomas/carcinomas adrenocorticais combinados aumentaram com uma dose oral de 60 mg/kg/dia (19 vezes a MRHD).
Um aumento de neoplasias mamárias, pituitárias e de pâncreas endócrino foi encontrado em roedores após a administração crônica de outras drogas antipsicóticas e é considerado mediado por antagonismo prolongado do receptor D2 da dopamina e hiperprolactinemia. A prolactina sérica não foi medida nos estudos de carcinogenicidade do aripiprazol. No entanto, foram observados aumentos nos níveis séricos de prolactina em camundongos fêmeas em um estudo dietético de 13 semanas nas doses associadas a tumores de glândula mamária e pituitária. A prolactina sérica não aumentou em ratos fêmeas em estudos dietéticos de 4 semanas e 13 semanas na dose associada a tumores da glândula mamária. A relevância para o risco humano dos achados de tumores endócrinos mediados por prolactina em roedores não é clara.
Mutagênese
potencial mutagênico do aripiprazol foi testado no ensaio de mutação reversa bacteriana in vitro, no ensaio de reparo de DNA bacteriano in vitro, no ensaio de mutação genética direta in vitro em células de linfoma de camundongo, no ensaio de aberração cromossômica in vitro no pulmão de hamster chinês (CHL) células, o ensaio de micronúcleo in vivo em camundongos e o ensaio de síntese de DNA não programado em ratos. O aripiprazol e um metabólito (2,3-DCPP) foram clastogênicos no ensaio de aberração cromossômica in vitro em células CHL com e sem ativação metabólica. O metabólito, 2,3DCPP, aumentou as aberrações numéricas no ensaio in vitro em células CHL na ausência de ativação metabólica. Uma resposta positiva foi obtida no ensaio de micronúcleo in vivo em camundongos; no entanto, a resposta foi devido a um mecanismo não considerado relevante para humanos.
Prejuízo da Fertilidade
Ratas fêmeas foram tratadas por via oral com aripiprazol desde 2 semanas antes do acasalamento até o dia 7 de gestação em doses de 2, 6 e 20 mg/kg/dia, que são 0,6, 2 e 6 vezes a MRHD de 30 mg/dia com base em mg/m² de área de superfície corporal. Irregularidades no ciclo estral e aumento dos corpos lúteos foram observados em todas as doses, mas nenhum comprometimento da fertilidade foi observado. O aumento da perda pré-implantação foi observado em 2 e 6 vezes a MRHD, e a diminuição do peso fetal foi observada em 6 vezes a MRHD.
Ratos machos foram tratados oralmente com aripiprazol de 9 semanas antes do acasalamento até o acasalamento em doses de 20, 40 e 60 mg/kg/dia, que são 6, 13 e 19 vezes a MRHD de 30 mg/dia com base em mg/ m² de superfície corporal. Distúrbios na espermatogênese foram observados em 19 vezes a MRHD e atrofia da próstata foi observada em 13 e 19 vezes a MRHD sem comprometimento da fertilidade.
Uso em populações específicas
Gravidez
Registro de Exposição à Gravidez
Existe um registro de exposição à gravidez que monitora os resultados da gravidez em mulheres expostas a antipsicóticos atípicos, incluindo ABILIFY, durante a gravidez. Os profissionais de saúde são incentivados a registrar pacientes entrando em contato com o Registro Nacional de Gravidez para Antipsicóticos Atípicos em 1-866-961-2388 ou visite http://womensmentalhealth.org/clinical-and-researchprograms/pregnancyregistry/.
Resumo do risco
Os recém-nascidos expostos a medicamentos antipsicóticos, incluindo ABILIFY 20mg, durante o terceiro trimestre de gravidez estão em risco de sintomas extrapiramidais e/ou de abstinência após o parto (ver Considerações Clínicas ). Os dados gerais disponíveis de estudos epidemiológicos publicados de mulheres grávidas expostas ao aripiprazol não estabeleceram um risco associado ao medicamento de defeitos congênitos graves, aborto espontâneo ou resultados maternos ou fetais adversos (ver Dados ). Existem riscos para a mãe associados à esquizofrenia não tratada, transtorno bipolar I ou transtorno depressivo maior e à exposição a antipsicóticos, incluindo ABILIFY, durante a gravidez (ver Considerações Clínicas ).
Em estudos de reprodução animal, a administração oral e intravenosa de aripiprazol durante a organogênese em ratos e/ou coelhos em doses 10 e 19 vezes, respectivamente, a dose humana máxima recomendada (MRHD) de 30 mg/dia com base em mg/m² de área de superfície corporal, produziu morte fetal, peso fetal diminuído, testículos que não desceram, ossificação esquelética retardada, anormalidades esqueléticas e hérnia diafragmática. A administração oral e intravenosa de aripiprazol durante o período pré e pós-natal em ratos em doses 10 vezes a MRHD com base em mg/m² de área de superfície corporal, produziu gestação prolongada, natimortos, diminuição do peso dos filhotes e diminuição da sobrevida dos filhotes (ver Dados ).
risco de fundo estimado de defeitos congênitos graves e aborto espontâneo para a população indicada é desconhecido. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e aborto espontâneo em gestações clinicamente reconhecidas é de 2-4% e 15-20%, respectivamente.
Considerações Clínicas
Risco Materno e/ou Embrião/Fetal Associado à Doença
Existe um risco para a mãe de esquizofrenia não tratada ou transtorno bipolar I, incluindo aumento do risco de recaída, hospitalização e suicídio. A esquizofrenia e o transtorno bipolar I estão associados ao aumento de resultados perinatais adversos, incluindo parto prematuro. Não se sabe se isso é resultado direto da doença ou de outros fatores comórbidos.
Estudo prospectivo, longitudinal, acompanhou 201 gestantes com histórico de transtorno depressivo maior, eutímicas e em uso de antidepressivos no início da gestação. As mulheres que descontinuaram os antidepressivos durante a gravidez eram mais propensas a ter uma recaída de depressão maior do que as mulheres que continuaram os antidepressivos. Considere o risco de depressão não tratada ao interromper ou alterar o tratamento com medicação antidepressiva durante a gravidez e pós-parto.
Reações Adversas Fetais/Neonatais
Sintomas extrapiramidais e/ou de abstinência, incluindo agitação, hipertonia, hipotonia, tremor, sonolência, dificuldade respiratória e distúrbios alimentares foram relatados em recém-nascidos que foram expostos a medicamentos antipsicóticos (incluindo ABILIFY) durante o terceiro trimestre de gravidez. Esses sintomas têm variado em gravidade. Monitore os neonatos quanto a sintomas extrapiramidais e/ou de abstinência e gerencie os sintomas adequadamente. Alguns neonatos se recuperaram em horas ou dias sem tratamento específico; outros necessitaram de hospitalização prolongada.
Dados
Dados humanos
Dados publicados de estudos observacionais, registros de nascimento e relatos de casos sobre o uso de antipsicóticos atípicos durante a gravidez não relatam uma associação clara com antipsicóticos e defeitos congênitos maiores. Um estudo retrospectivo de um banco de dados Medicaid de 9.258 mulheres expostas a antipsicóticos durante a gravidez não indicou um aumento geral do risco de defeitos congênitos graves.
Dados de animais
Em estudos com animais, o aripiprazol demonstrou toxicidade no desenvolvimento, incluindo possíveis efeitos teratogênicos em ratos e coelhos.
Em ratas prenhes tratadas por via oral com aripiprazol durante a organogênese em doses de 3, 10 e 30 mg/kg/dia, que são aproximadamente 1, 3 e 10 vezes a MRHD de 30 mg/dia com base em mg/m² de área de superfície corporal, um ligeiro prolongamento da gestação e atraso no desenvolvimento fetal, como evidenciado pela diminuição do peso fetal e testículos que não desceram, foram observados em 10 vezes a MRHD. A ossificação esquelética tardia foi observada em 3 e 10 vezes a MRHD. A prole entregue teve incidência aumentada de nódulos hepatodiafragmáticos e hérnia diafragmática foi observada em 10 vezes a MRHD (os outros grupos de dose não foram examinados para esses achados). No pós-natal, a abertura vaginal tardia foi observada em 3 e 10 vezes a MRHD. Desempenho reprodutivo prejudicado (taxa de fertilidade diminuída, corpos lúteos, implantes, fetos vivos e aumento da perda pós-implantação, provavelmente mediado por efeitos na prole feminina) foram observados em 10 vezes a MRHD; no entanto, não houve evidências que sugerissem que esses efeitos no desenvolvimento fossem secundários à toxicidade materna.
Em ratas prenhas injetadas intravenosamente com aripiprazol durante a organogênese em doses de 3, 9 e 27 mg/kg/dia, que são 1, 3 e 9 vezes a MRHD de 30 mg/dia com base em mg/m² de área de superfície corporal, diminuiu peso fetal e ossificação esquelética retardada foram observados em 9 vezes a MRHD; esta dose também causou toxicidade materna.
Em coelhas grávidas tratadas por via oral com aripiprazol durante a organogênese em doses de 10, 30 e 100 mg/kg/dia que são 6, 19 e 65 vezes a MRHD de 30 mg/dia com base na área de superfície corporal em mg/m², consumo de alimentos e aumento de abortos, bem como aumento da mortalidade fetal foram observados em 65 vezes o MHRD. A diminuição do peso fetal e o aumento da incidência de esternebras fundidas foram observados em 19 e 65 vezes a MRHD.
Em coelhas grávidas injetadas intravenosamente com aripiprazol durante a organogênese em doses de 3, 10 e 30 mg/kg/dia, que são 2, 6 e 19 vezes a MRHD de 30 mg/dia com base em mg/m² de área de superfície corporal, diminuiu peso fetal, anormalidades fetais aumentadas (principalmente esqueléticas) e ossificação esquelética fetal diminuída foram observados em 19 vezes a MRHD; esta dose também causou toxicidade materna. A dose fetal sem efeito foi de 10 mg/kg/dia, que é 6 vezes a MRHD.
Em ratos tratados por via oral com aripiprazol peri e pós-natal do dia 17 da gestação até o dia 21 pós-parto em doses de 3, 10 e 30 mg/kg/dia que são 1, 3 e 10 vezes a MRHD de 30 mg/dia com base em mg/m² de área de superfície corporal, foram observadas toxicidade materna leve e gestação levemente prolongada em 10 vezes o MHRD. Um aumento nos natimortos e diminuição no peso dos filhotes (persistindo na idade adulta) e na sobrevivência também foram observados com esta dose.
Em ratos injetados por via intravenosa com aripiprazol do 6º dia de gestação até o 20º dia de lactação em doses de 3, 8 e 20 mg/kg/dia, que são 1, 3 e 6 vezes a MRHD de 30 mg/dia com base em mg/m² área de superfície corporal, natimortos aumentados foram observados em 3 e 6 vezes a MRHD; e foram observadas diminuições no peso e sobrevida do filhote pós-natal precoce em 6 vezes a MRHD; essas doses também causaram alguma toxicidade materna. Não houve efeitos no desenvolvimento comportamental e reprodutivo pós-natal.
Lactação
Resumo do risco
Dados limitados da literatura publicada relatam a presença de aripiprazol no leite materno humano, em doses infantis relativas variando entre 0,7% a 8,3% da dose ajustada ao peso materno. Há relatos de baixo ganho de peso em bebês amamentados expostos ao aripiprazol e relatos de suprimento inadequado de leite em mulheres lactantes que tomam aripiprazol.
Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de ABILIFY e quaisquer efeitos adversos potenciais do ABILIFY no lactente ou da condição materna subjacente.
Uso Pediátrico
A segurança e a eficácia em pacientes pediátricos com transtorno depressivo maior ou agitação associada à esquizofrenia ou mania bipolar não foram estabelecidas.
A farmacocinética do aripiprazol e do dehidro-aripiprazol em pacientes pediátricos, de 10 a 17 anos de idade, foi semelhante à de adultos após correção para as diferenças de peso corporal [ver FARMACOLOGIA CLÍNICA ].
Esquizofrenia
A segurança e a eficácia em pacientes pediátricos com esquizofrenia foram estabelecidas em um ensaio clínico controlado por placebo de 6 semanas em 202 pacientes pediátricos com idades entre 13 e 17 anos [ver DOSAGEM E ADMINISTRAÇÃO , REAÇÕES ADVERSAS , e Estudos clínicos ]. Embora a eficácia de manutenção em pacientes pediátricos não tenha sido sistematicamente avaliada, a eficácia de manutenção pode ser extrapolada de dados de adultos juntamente com comparações de parâmetros farmacocinéticos de aripiprazol em pacientes adultos e pediátricos.
Transtorno Bipolar I
A segurança e a eficácia em pacientes pediátricos com mania bipolar foram estabelecidas em um ensaio clínico controlado por placebo de 4 semanas em 197 pacientes pediátricos com idades entre 10 e 17 anos [ver DOSAGEM E ADMINISTRAÇÃO , REAÇÕES ADVERSAS , e Estudos clínicos ]. Embora a eficácia de manutenção em pacientes pediátricos não tenha sido sistematicamente avaliada, a eficácia de manutenção pode ser extrapolada de dados de adultos juntamente com comparações de parâmetros farmacocinéticos de aripiprazol em pacientes adultos e pediátricos.
A eficácia de ABILIFY 10mg adjuvante com lítio ou valproato concomitante no tratamento de episódios maníacos ou mistos em pacientes pediátricos não foi sistematicamente avaliada. No entanto, tal eficácia e falta de interação farmacocinética entre aripiprazol e lítio ou valproato podem ser extrapoladas a partir de dados de adultos, juntamente com comparações de parâmetros farmacocinéticos de aripiprazol em pacientes adultos e pediátricos.
Irritabilidade Associada ao Transtorno Autista
segurança e a eficácia em pacientes pediátricos que demonstram irritabilidade associada ao transtorno autista foram estabelecidas em dois ensaios clínicos de 8 semanas, controlados por placebo, em 212 pacientes pediátricos com idades entre 6 e 17 anos. INDICAÇÕES E USO , DOSAGEM E ADMINISTRAÇÃO , REAÇÕES ADVERSAS , e Estudos clínicos ]. Um estudo de manutenção foi realizado em pacientes pediátricos (6 a 17 anos de idade) com irritabilidade associada ao transtorno autista. A primeira fase deste estudo foi uma fase aberta, com dosagem flexível (aripiprazol 2 a 15 mg/dia) na qual os pacientes foram estabilizados (definido como > 25% de melhora na subescala ABC-I e uma classificação CGI-I de “muito melhorado” ou “muito melhorado”) no ABILIFY por 12 semanas consecutivas. No geral, 85 pacientes foram estabilizados e entraram na segunda fase duplo-cega de 16 semanas, onde foram randomizados para continuar o tratamento com ABILIFY ou mudar para placebo. Neste estudo, a eficácia de ABILIFY para o tratamento de manutenção da irritabilidade associada ao transtorno autista não foi estabelecida.
Transtorno de Tourette
A segurança e eficácia do aripiprazol em pacientes pediátricos com transtorno de Tourette foram estabelecidas em um estudo de 8 semanas (7 a 17 anos) e um estudo de 10 semanas (6 a 18 anos) em 194 pacientes pediátricos [ver DOSAGEM E ADMINISTRAÇÃO , REAÇÕES ADVERSAS , e Estudos clínicos ]. A eficácia de manutenção em pacientes pediátricos não foi sistematicamente avaliada.
Estudos de Animais Juvenis
aripiprazol em ratos juvenis causou mortalidade, sinais clínicos do SNC, comprometimento da memória e aprendizado e atraso na maturação sexual quando administrado em doses orais de 10, 20, 40 mg/kg/dia desde o desmame (21 dias de idade) até a maturidade (80 dias de idade) . Na dose de 40 mg/kg/dia, mortalidade, atividade diminuída, membros posteriores afastados, postura encurvada, ataxia, tremores e outros sinais do SNC foram observados em ambos os sexos. Além disso, a maturação sexual tardia foi observada nos machos. Em todas as doses e de maneira dose-dependente, memória e aprendizagem prejudicadas, atividade motora aumentada e alterações histopatológicas na hipófise (atrofia), supra-renais (hipertrofia adrenocortical), glândulas mamárias (hiperplasia e aumento da secreção) e órgãos reprodutores femininos. mucificação vaginal, atrofia endometrial, diminuição dos corpos lúteos ovarianos). As alterações nos órgãos reprodutores femininos foram consideradas secundárias ao aumento dos níveis séricos de prolactina. Um Nível de Efeito Adverso Não Observado (NOAEL) não pôde ser determinado e, na dose mais baixa testada de 10 mg/kg/dia, não há margem de segurança em relação às exposições sistêmicas (AUC0-24) para aripiprazol ou seu principal metabólito ativo em adolescentes na dose pediátrica máxima recomendada de 15 mg/dia. Todos os efeitos relacionados ao medicamento foram reversíveis após um período de recuperação de 2 meses, e a maioria dos efeitos do medicamento em ratos jovens também foram observados em ratos adultos em estudos realizados anteriormente.
aripiprazol em cães juvenis (2 meses de idade) causou sinais clínicos no SNC de tremores, hipoatividade, ataxia, decúbito e uso limitado dos membros posteriores quando administrado por via oral durante 6 meses a 3, 10, 30 mg/kg/dia. O peso corporal médio e o ganho de peso foram reduzidos em até 18% em mulheres em todos os grupos de drogas em relação aos valores de controle. Um NOAEL não pôde ser determinado e, na dose mais baixa testada de 3 mg/kg/dia, não há margem de segurança em relação às exposições sistêmicas (AUC0-24) para aripiprazol ou seu principal metabólito ativo em adolescentes na dose pediátrica máxima recomendada dose de 15 mg/dia. Todos os efeitos relacionados ao medicamento foram reversíveis após um período de recuperação de 2 meses.
Uso Geriátrico
Nenhum ajuste de dose é recomendado para pacientes idosos [ver AVISO EM CAIXA , AVISOS E PRECAUÇÕES , e FARMACOLOGIA CLÍNICA ].
Dos 13.543 pacientes tratados com ABILIFY 15mg oral em ensaios clínicos, 1.073 (8%) tinham ≥65 anos e 799 (6%) tinham ≥75 anos. Os estudos controlados por placebo de ABILIFY 10mg oral em esquizofrenia, mania bipolar ou transtorno depressivo maior não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se eles respondem de forma diferente dos indivíduos mais jovens.
Dos 749 pacientes tratados com a injeção de ABILIFY em ensaios clínicos, 99 (13%) tinham ≥65 anos e 78 (10%) tinham ≥75 anos. Os estudos controlados por placebo da injeção de ABILIFY em pacientes com agitação associada à esquizofrenia ou mania bipolar não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se eles respondem de forma diferente dos indivíduos mais jovens.
ABILIFY 15mg não está aprovado para o tratamento de pacientes com psicose associada à doença de Alzheimer [ver AVISO EM CAIXA e AVISOS E PRECAUÇÕES ].
Metabolizadores fracos de CYP2D6
ajuste da dose é recomendado em metabolizadores fracos de CYP2D6 conhecidos devido às altas concentrações de aripiprazol. Aproximadamente 8% dos caucasianos e 3-8% dos negros/afro-americanos não podem metabolizar os substratos CYP2D6 e são classificados como metabolizadores fracos (PM) [ver DOSAGEM E ADMINISTRAÇÃO e FARMACOLOGIA CLÍNICA ].
Insuficiência Hepática e Renal
Não é necessário ajuste de dose para ABILIFY com base na função hepática do paciente (insuficiência hepática leve a grave, pontuação de Child-Pugh entre 5 e 15) ou função renal (insuficiência renal leve a grave, taxa de filtração glomerular entre 15 e 15). e 90 mL/minuto) [ver FARMACOLOGIA CLÍNICA ].
Outras populações específicas
Nenhum ajuste de dose de ABILIFY é necessário com base no sexo, raça ou tabagismo do paciente [ver FARMACOLOGIA CLÍNICA ].
SOBREDOSAGEM
A terminologia MedDRA tem sido usada para classificar as reações adversas.
Experiência Humana
Em estudos clínicos e na experiência pós-comercialização, reações adversas de superdosagem deliberada ou acidental com ABILIFY oral foram relatadas em todo o mundo. Estes incluem sobredosagens com ABILIFY 20 mg oral isolado e em combinação com outras substâncias. Nenhuma fatalidade foi relatada apenas com ABILIFY. A maior dose conhecida com um resultado conhecido envolveu a ingestão aguda de 1.260 mg de ABILIFY oral (42 vezes a dose diária máxima recomendada) por um paciente que se recuperou totalmente. Superdosagem deliberada ou acidental também foi relatada em crianças (com 12 anos ou menos) envolvendo ingestões orais de ABILIFY 10 mg até 195 mg sem fatalidades.
As reações adversas comuns (notificadas em pelo menos 5% de todos os casos de sobredosagem) notificadas com a sobredosagem oral de ABILIFY (isoladamente ou em combinação com outras substâncias) incluem vómitos, sonolência e tremores. Outros sinais e sintomas clinicamente importantes observados em um ou mais pacientes com superdosagem de ABILIFY (isolado ou com outras substâncias) incluem acidose, agressão, aumento da aspartato aminotransferase, fibrilação atrial, bradicardia, coma, estado confusional, convulsão, aumento da creatina fosfoquinase no sangue, nível deprimido de consciência, hipertensão, hipocalemia, hipotensão, letargia, perda de consciência, complexo QRS prolongado, QT prolongado, aspiração de pneumonia, parada respiratória, estado de mal epiléptico e taquicardia.
Gerenciamento de superdosagem
Nenhuma informação específica está disponível sobre o tratamento de superdosagem com ABILIFY. Um eletrocardiograma deve ser obtido em caso de superdosagem e se houver prolongamento do intervalo QT, o monitoramento cardíaco deve ser instituído. Caso contrário, o manejo da superdosagem deve se concentrar na terapia de suporte, manutenção de vias aéreas adequadas, oxigenação e ventilação e manejo dos sintomas. A supervisão médica e o monitoramento devem continuar até que o paciente se recupere.
Carvão
Em caso de superdosagem de ABILIFY 10mg, uma administração precoce de carvão pode ser útil para prevenir parcialmente a absorção de aripiprazol. A administração de 50 g de carvão ativado, uma hora após uma dose oral única de 15 mg de ABILIFY, diminuiu a AUC e a Cmax médias do aripiprazol em 50%.
Hemodiálise
Embora não haja informações sobre o efeito da hemodiálise no tratamento de uma superdosagem com ABILIFY, é improvável que a hemodiálise seja útil no controle da superdosagem, uma vez que o aripiprazol é altamente ligado às proteínas plasmáticas.
CONTRA-INDICAÇÕES
ABILIFY 15mg é contraindicado em pacientes com história de reação de hipersensibilidade ao aripiprazol. As reações variaram de prurido/urticária a anafilaxia [ver REAÇÕES ADVERSAS ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
O mecanismo de ação do aripiprazol na esquizofrenia ou mania bipolar não é claro. No entanto, a eficácia do aripiprazol nas indicações listadas pode ser mediada por uma combinação de atividade agonista parcial nos receptores D2 e 5-HT1A e atividade antagonista nos receptores 5-HT2A.
Farmacodinâmica
aripiprazol exibe alta afinidade para os receptores de dopamina D2 e D3, serotonina 5-HT1A e 5-HT2A (valores de Ki de 0,34 nM, 0,8 nM, 1,7 nM e 3,4 nM, respectivamente), afinidade moderada para dopamina D4, serotonina 5-HT2C e 5-HT7, receptores alfa1-adrenérgicos e histamina H1 (valores de Ki de 44 nM, 15 nM, 39 nM, 57 nM e 61 nM, respectivamente) e afinidade moderada para o local de recaptação de serotonina (Ki = 98 nM). O aripiprazol não tem afinidade apreciável pelos receptores muscarínicos colinérgicos (IC50>1000 nM).
Farmacocinética
atividade do ABILIFY é presumivelmente devida principalmente ao fármaco original, aripiprazol e, em menor grau, ao seu principal metabólito, o dehidro-aripiprazol, que demonstrou ter afinidades pelos receptores D2 semelhantes ao medicamento original e representa 40% do medicamento original. exposição a drogas no plasma. As meias-vidas médias de eliminação são cerca de 75 horas e 94 horas para aripiprazol e dehidro-aripiprazol, respectivamente. As concentrações de estado estacionário são alcançadas dentro de 14 dias após a dosagem para ambas as porções ativas. A acumulação de aripiprazol é previsível a partir da farmacocinética de dose única. No estado de equilíbrio, a farmacocinética do aripiprazol é proporcional à dose. A eliminação do aripiprazol ocorre principalmente através do metabolismo hepático envolvendo duas isoenzimas P450, CYP2D6 e CYP3A4. Para metabolizadores fracos de CYP2D6, a meia-vida média de eliminação do aripiprazol é de cerca de 146 horas.
Estudos farmacocinéticos mostraram que ABILIFY 10mg DISCMELT comprimidos de desintegração oral é bioequivalente a ABILIFY 15mg comprimidos.
Administração oral
Absorção
Comprimido: O aripiprazol é bem absorvido após a administração do comprimido, com picos de concentração plasmática ocorrendo dentro de 3 horas a 5 horas; a biodisponibilidade oral absoluta da formulação em comprimido é de 87%. ABILIFY 10mg pode ser administrado com ou sem alimentos. A administração de um comprimido de 15 mg de ABILIFY com uma refeição padrão com alto teor de gordura não afetou significativamente a Cmáx ou AUC do aripiprazol ou de seu metabólito ativo, o desidro-aripiprazol, mas atrasou o Tmáx em 3 horas para o aripiprazol e 12 horas para o dehidro-aripiprazol.
Solução oral: O aripiprazol é bem absorvido quando administrado por via oral como solução. Em doses equivalentes, as concentrações plasmáticas de aripiprazol da solução foram superiores às da formulação em comprimido. Em um estudo de biodisponibilidade relativa comparando a farmacocinética de 30 mg de aripiprazol como solução oral com 30 mg de aripiprazol comprimidos em indivíduos saudáveis, as razões solução/comprimido dos valores médios geométricos de Cmax e AUC foram 122% e 114%, respectivamente [ver DOSAGEM E ADMINISTRAÇÃO ]. A farmacocinética de dose única de aripiprazol foi linear e proporcional à dose entre as doses de 5 mg a 30 mg.
Distribuição
volume de distribuição no estado de equilíbrio do aripiprazol após administração intravenosa é alto (404 L ou 4,9 L/kg), indicando extensa distribuição extravascular. Em concentrações terapêuticas, o aripiprazol e seu principal metabólito ligam-se mais de 99% às proteínas séricas, principalmente à albumina. Em voluntários humanos saudáveis administrados de 0,5 a 30 mg/dia de aripiprazol por 14 dias, houve ocupação do receptor D2 dependente da dose indicando penetração cerebral de aripiprazol em humanos.
Metabolismo e eliminação
aripiprazol é metabolizado principalmente por três vias de biotransformação: desidrogenação, hidroxilação e N-desalquilação. Com base em estudos in vitro, as enzimas CYP3A4 e CYP2D6 são responsáveis pela desidrogenação e hidroxilação do aripiprazol, e a N-desalquilação é catalisada pelo CYP3A4. O aripiprazol é o fármaco predominante na circulação sistêmica. No estado de equilíbrio, o dehidro-aripiprazol, o metabólito ativo, representa cerca de 40% da AUC do aripiprazol no plasma.
Após uma dose oral única de aripiprazol marcado com [14C], aproximadamente 25% e 55% da radioatividade administrada foi recuperada na urina e nas fezes, respectivamente. Menos de 1% do aripiprazol inalterado foi excretado na urina e aproximadamente 18% da dose oral foi recuperada inalterada nas fezes.
Estudos de interação medicamentosa
Os efeitos de outras drogas nas exposições de aripiprazol e dehidro-aripiprazol estão resumidos na Figura 1 e na Figura 2, respectivamente. Com base na simulação, é esperado um aumento de 4,5 vezes nos valores médios de Cmax e AUC no estado de equilíbrio quando metabolizadores extensivos de CYP2D6 são administrados com inibidores fortes de CYP2D6 e CYP3A4. Espera-se um aumento de 3 vezes nos valores médios de Cmax e AUC no estado de equilíbrio em metabolizadores fracos de CYP2D6 administrados com fortes inibidores de CYP3A4.
Figura 1: Os efeitos de outros medicamentos na farmacocinética do aripiprazol 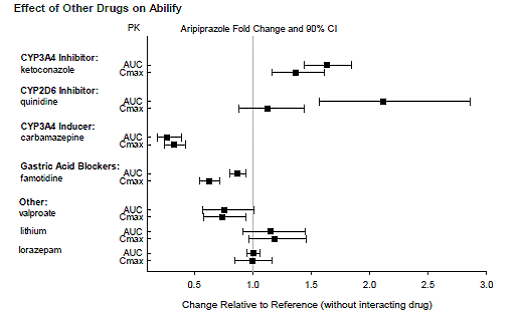
Figura 2: Os efeitos de outros medicamentos na farmacocinética do desidro-aripiprazol 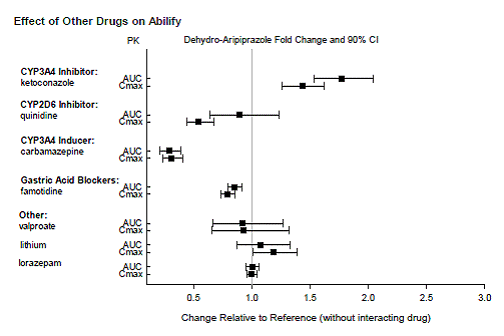
Os efeitos de ABILIFY 15mg nas exposições de outros medicamentos estão resumidos na Figura 3. Uma análise farmacocinética populacional em pacientes com transtorno depressivo maior não mostrou alteração substancial nas concentrações plasmáticas de fluoxetina (20 ou 40 mg/dia), paroxetina CR (37,5 ou 50 mg/dia) ou sertralina (100 ou 150 mg/dia) administrados até o estado de equilíbrio. As concentrações plasmáticas no estado de equilíbrio de fluoxetina e norfluoxetina aumentaram cerca de 18% e 36%, respectivamente, e as concentrações de paroxetina diminuíram cerca de 27%. As concentrações plasmáticas no estado de equilíbrio de sertralina e desmetilsertralina não foram substancialmente alteradas quando essas terapias antidepressivas foram coadministradas com aripiprazol.
Figura 3: Os efeitos do ABILIFY 15mg na farmacocinética de outros medicamentos 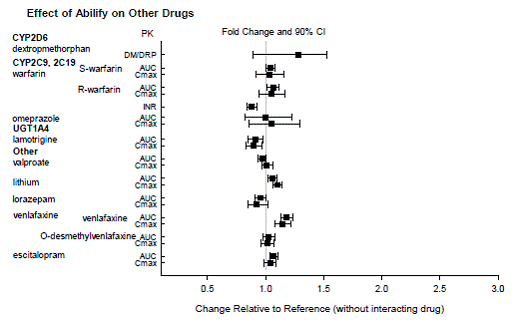
Estudos em populações específicas
As exposições de aripiprazol e dehidro-aripiprazol em populações específicas estão resumidas na Figura 4 e na Figura 5, respectivamente. Além disso, em pacientes pediátricos (10 a 17 anos de idade) administrados com ABILIFY (20 mg a 30 mg), a depuração de aripiprazol corrigida pelo peso corporal foi semelhante à dos adultos.
Figura 4: Efeitos dos fatores intrínsecos na farmacocinética do aripiprazol 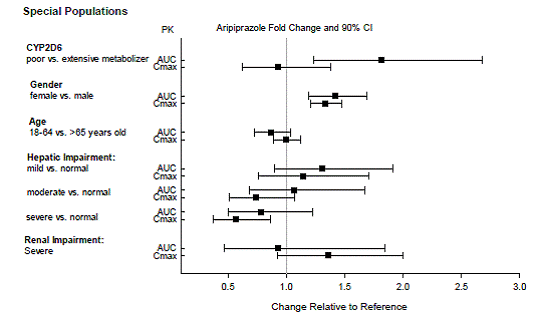
Figura 5: Efeitos dos fatores intrínsecos na farmacocinética do desidro-aripiprazol 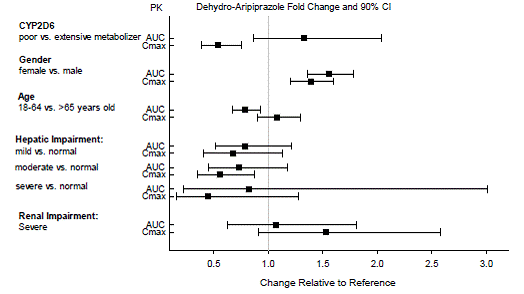
Administração intramuscular
Em dois estudos farmacocinéticos de injeção de aripiprazol administrado por via intramuscular a indivíduos saudáveis, os tempos médios para as concentrações plasmáticas máximas foram de 1 hora e 3 horas. Uma injeção intramuscular de 5 mg de aripiprazol teve uma biodisponibilidade absoluta de 100%. A concentração máxima média geométrica alcançada após uma dose intramuscular foi em média 19% superior à Cmax do comprimido oral. Embora a exposição sistêmica ao longo de 24 horas tenha sido geralmente semelhante entre a injeção de aripiprazol administrada por via intramuscular e após a administração do comprimido oral, a AUC do aripiprazol nas primeiras 2 horas após uma injeção intramuscular foi 90% maior do que a AUC após a mesma dose de um comprimido. Em pacientes estáveis com esquizofrenia ou transtorno esquizoafetivo, a farmacocinética do aripiprazol após administração intramuscular foi linear em uma faixa de dose de 1 mg a 45 mg. Embora o metabolismo da injeção de aripiprazol não tenha sido sistematicamente avaliado, não se espera que a via de administração intramuscular altere as vias metabólicas.
Toxicologia e/ou Farmacologia Animal
O aripiprazol produziu degeneração da retina em ratos albinos em um estudo de toxicidade crônica de 26 semanas com uma dose de 60 mg/kg/dia e em um estudo de carcinogenicidade de 2 anos com doses de 40 e 60 mg/kg/dia que são 13 e 19 vezes a MRHD de 30 mg/dia com base na área de superfície corporal em mg/m². A avaliação das retinas de camundongos albinos e de macacos não revelou evidências de degeneração retiniana. Estudos adicionais para avaliar melhor o mecanismo não foram realizados. A relevância deste achado para o risco humano é desconhecida.
Estudos clínicos
A eficácia das formulações orais de ABILIFY (aripiprazol) foi estabelecida nos seguintes ensaios adequados e bem controlados:
- Quatro ensaios de curto prazo e um ensaio de manutenção em pacientes adultos e um ensaio de curto prazo em adolescentes (13-17 anos) com esquizofrenia [ver Estudos clínicos ]
- Quatro ensaios de monoterapia de curto prazo e um ensaio adjuvante de 6 semanas em pacientes adultos e um ensaio de monoterapia de curto prazo em pacientes pediátricos (1017 anos) com episódios maníacos ou mistos [ver Estudos clínicos ]
- Um estudo de monoterapia de manutenção e um estudo adjuvante de manutenção em pacientes adultos com transtorno bipolar I [ver Estudos clínicos ]
- Dois estudos de curto prazo em pacientes adultos com TDM que tiveram uma resposta inadequada à terapia antidepressiva durante o episódio atual [ver Estudos clínicos ]
- Dois estudos de curta duração em pacientes pediátricos (6-17 anos) para o tratamento da irritabilidade associada ao transtorno autista [ver Estudos clínicos ]
- Dois ensaios de curto prazo em pacientes pediátricos (6-18 anos) com transtorno de Tourette [ver Estudos clínicos ]
A eficácia da formulação injetável de ABILIFY (aripiprazol) foi estabelecida nos seguintes ensaios adequados e bem controlados:
- Três ensaios de 24 horas em pacientes adultos agitados com esquizofrenia ou episódios maníacos/mistos de transtorno bipolar I [ver Estudos clínicos ]
Esquizofrenia
Adultos
A eficácia de ABILIFY 15mg no tratamento da esquizofrenia foi avaliada em cinco estudos de curto prazo (4 semanas e 6 semanas), controlados por placebo, de pacientes internados com recaída aguda que preenchiam predominantemente os critérios do DSM-III/IV para esquizofrenia. Quatro dos cinco estudos foram capazes de distinguir o ABILIFY do placebo, mas um estudo, o menor, não o fez. Três desses estudos também incluíram um grupo de controle ativo composto por risperidona (um estudo) ou haloperidol (dois estudos), mas não foram projetados para permitir uma comparação de ABILIFY 20mg e os comparadores ativos.
Nos quatro ensaios positivos para ABILIFY 10mg, quatro medidas primárias foram usadas para avaliar sinais e sintomas psiquiátricos. A eficácia foi avaliada por meio do escore total da Escala de Síndrome Positiva e Negativa (PANSS). A PANSS é uma escala de 30 itens que mede sintomas positivos de esquizofrenia (7 itens), sintomas negativos de esquizofrenia (7 itens) e psicopatologia geral (16 itens), cada um avaliado em uma escala de 1 (ausente) a 7 (extremo). ; os escores totais da PANSS variam de 30 a 210. A avaliação Clinical Global Impression (CGI) reflete a impressão de um observador habilidoso, totalmente familiarizado com as manifestações da esquizofrenia, sobre o estado clínico geral do paciente.
Em um estudo de 4 semanas (n=414) comparando duas doses fixas de ABILIFY (15 ou 30 mg/dia) com placebo, ambas as doses de ABILIFY 10mg foram superiores ao placebo na pontuação total da PANSS (Estudo 1 na Tabela 26), Subescala positiva PANSS e escore de gravidade CGI. Além disso, a dose de 15 mg foi superior ao placebo na subescala negativa de PANSS.
Em um estudo de 4 semanas (n=404) comparando duas doses fixas de ABILIFY (20 ou 30 mg/dia) com placebo, ambas as doses de ABILIFY foram superiores ao placebo na pontuação total da PANSS (Estudo 2 na Tabela 26), PANSS subescala positiva, subescala negativa da PANSS e escore de gravidade CGI.
Em um estudo de 6 semanas (n=420) comparando três doses fixas de ABILIFY (10, 15 ou 20 mg/dia) com placebo, todas as três doses de ABILIFY foram superiores ao placebo na pontuação total da PANSS (Estudo 3 na Tabela 26), subescala positiva de PANSS e subescala negativa de PANSS.
Em um estudo de 6 semanas (n=367) comparando três doses fixas de ABILIFY (2, 5 ou 10 mg/dia) com placebo, a dose de 10 mg de ABILIFY foi superior ao placebo na pontuação total da PANSS (Estudo 4 em Tabela 26), o desfecho primário do estudo. As doses de 2 e 5 mg não demonstraram superioridade ao placebo na medida de resultado primário.
Assim, a eficácia das doses diárias de 10, 15, 20 e 30 mg foi estabelecida em dois estudos para cada dose. Entre essas doses, não houve evidência de que os grupos de dose mais alta oferecessem qualquer vantagem sobre o grupo de dose mais baixa desses estudos.
Um exame de subgrupos populacionais não revelou nenhuma evidência clara de responsividade diferencial com base na idade, sexo ou raça.
Um estudo de longo prazo recrutou 310 pacientes internados ou ambulatoriais que preenchiam os critérios do DSM-IV para esquizofrenia que eram, pela história, sintomaticamente estáveis com outros medicamentos antipsicóticos por períodos de 3 meses ou mais. Esses pacientes foram descontinuados de seus medicamentos antipsicóticos e randomizados para ABILIFY 15 mg/dia ou placebo por até 26 semanas de observação para recaída. A recaída durante a fase duplo-cega foi definida como pontuação CGI-Melhoria de ≥5 (minimamente pior), pontuação ≥5 (moderadamente grave) nos itens de hostilidade ou não cooperação da PANSS, ou aumento ≥20% na pontuação total da PANSS. Os pacientes que receberam ABILIFY 15 mg/dia tiveram um tempo significativamente maior para recidiva nas 26 semanas subsequentes em comparação com aqueles que receberam placebo (Estudo 5 na Figura 6).
Pacientes pediátricos
eficácia de ABILIFY (aripiprazol) no tratamento da esquizofrenia em pacientes pediátricos (13 a 17 anos de idade) foi avaliada em um estudo controlado por placebo de 6 semanas de pacientes ambulatoriais que preencheram os critérios do DSM-IV para esquizofrenia e tiveram uma pontuação PANSS ≥70 na linha de base. Neste ensaio (n=302) comparando duas doses fixas de ABILIFY (10 ou 30 mg/dia) com placebo, ABILIFY 15mg foi titulado a partir de 2 mg/dia até a dose alvo em 5 dias no braço de tratamento de 10 mg/dia e em 11 dias no braço de tratamento de 30 mg/dia. Ambas as doses de ABILIFY foram superiores ao placebo na pontuação total da PANSS (Estudo 6 na Tabela 26), a medida de resultado primário do estudo. A dose de 30 mg/dia não se mostrou mais eficaz do que a dose de 10 mg/dia. Embora a eficácia de manutenção em pacientes pediátricos não tenha sido sistematicamente avaliada, a eficácia de manutenção pode ser extrapolada de dados de adultos juntamente com comparações de parâmetros farmacocinéticos de aripiprazol em pacientes adultos e pediátricos.
Figura 6: Estimativa de Kaplan-Meier da proporção cumulativa de pacientes com recaída (estudo de esquizofrenia 5) 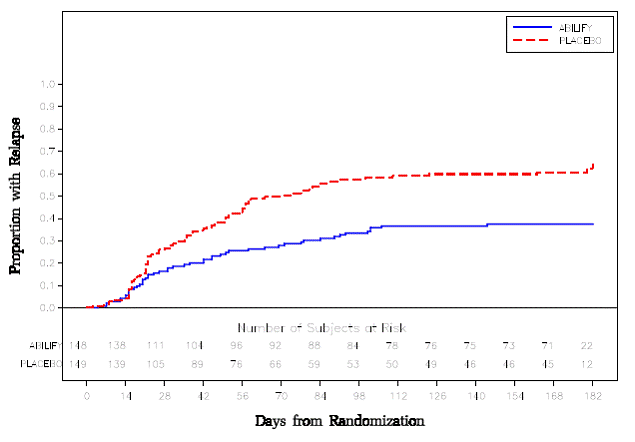
Transtorno bipolar
Tratamento Agudo de Episódios Maníacos e Mistos
Adultos
Monoterapia
A eficácia de ABILIFY 10mg como monoterapia no tratamento agudo de episódios maníacos foi estabelecida em quatro ensaios controlados por placebo de 3 semanas em pacientes hospitalizados que preenchiam os critérios do DSM-IV para transtorno bipolar I com episódios maníacos ou mistos. Esses estudos incluíram pacientes com ou sem características psicóticas e dois dos estudos também incluíram pacientes com ou sem ciclo rápido.
O principal instrumento usado para avaliar os sintomas maníacos foi a Young Mania Rating Scale (Y-MRS), uma escala de 11 itens classificada pelo médico tradicionalmente usada para avaliar o grau de sintomatologia maníaca em uma faixa de 0 (sem características maníacas) a 60 ( pontuação máxima). Um instrumento secundário chave incluiu a escala Clinical Global Impression-Bipolar (CGI-BP).
Nos quatro ensaios positivos, de 3 semanas, controlados por placebo (n=268; n=248; n=480; n=485) que avaliaram ABILIFY em uma faixa de 15 mg a 30 mg, uma vez ao dia (com uma dose inicial de 30 mg/dia em dois estudos e 15 mg/dia em dois estudos), ABILIFY 20 mg foi superior ao placebo na redução da pontuação total Y-MRS (Estudos 1-4 na Tabela 27) e pontuação CGI-BP Severity of Illness score (mania). Nos dois estudos com uma dose inicial de 15 mg/dia, 48% e 44% dos pacientes receberam 15 mg/dia no desfecho. Nos dois estudos com uma dose inicial de 30 mg/dia, 86% e 85% dos pacientes estavam tomando 30 mg/dia no desfecho.
Terapia Adjuvante
eficácia de ABILIFY adjuvante com lítio ou valproato concomitante no tratamento de episódios maníacos ou mistos foi estabelecida em um estudo controlado por placebo de 6 semanas (n=384) com uma fase inicial de 2 semanas de monoterapia com estabilizador de humor em pacientes adultos que preencheram os critérios do DSM-IV para transtorno bipolar I. Este estudo incluiu pacientes com episódios maníacos ou mistos e com ou sem características psicóticas.
Os pacientes foram iniciados com lítio aberto (0,6 a 1,0 mEq/L) ou valproato (50 a 125 μg/mL) em níveis séricos terapêuticos e permaneceram em doses estáveis por 2 semanas. Ao final de 2 semanas, os pacientes que demonstraram resposta inadequada (escore total YMRS ≥16 e ≤25% de melhora no escore total Y-MRS) ao lítio ou valproato foram randomizados para receber ABILIFY (15 mg/dia ou um aumento para 30 mg/dia já no dia 7) ou placebo como terapia adjuvante com lítio ou valproato de rótulo aberto. Na fase de 6 semanas, controlada por placebo, ABILIFY adjuvante iniciando em 15 mg/dia com lítio ou valproato concomitante (em uma faixa terapêutica de 0,6 a 1,0 mEq/L ou 50 a 125 μg/mL, respectivamente) foi superior ao lítio ou valproato com placebo adjuvante na redução da pontuação total YMRS (Estudo 5 na Tabela 27) e pontuação CGI-BP Gravidade da Doença (mania). Setenta e um por cento dos pacientes coadministrados com valproato e 62% dos pacientes coadministrados com lítio estavam em 15 mg/dia no desfecho de 6 semanas.
Pacientes pediátricos
eficácia de ABILIFY 15mg no tratamento do transtorno bipolar I em pacientes pediátricos (10 a 17 anos de idade) foi avaliada em um estudo controlado por placebo de 4 semanas (n=296) de pacientes ambulatoriais que preencheram os critérios do DSM-IV para transtorno bipolar I transtorno maníaco ou episódios mistos com ou sem características psicóticas e tinha uma pontuação Y-MRS ≥20 na linha de base. Este estudo duplo-cego, controlado por placebo, comparou duas doses fixas de ABILIFY (10 ou 30 mg/dia) com placebo. A dose de ABILIFY 20 mg foi iniciada com 2 mg/dia, que foi titulada para 5 mg/dia após 2 dias e para a dose alvo em 5 dias no braço de tratamento de 10 mg/dia e em 13 dias no braço de tratamento de 30 mg/dia. braço de tratamento do dia. Ambas as doses de ABILIFY 10mg foram superiores ao placebo na alteração da linha de base até a semana 4 na pontuação total Y-MRS (Estudo 6 na Tabela 27).
Tratamento de manutenção do transtorno bipolar I
Terapia de manutenção em monoterapia
Um estudo de manutenção foi realizado em pacientes adultos que preenchiam os critérios do DSM-IV para transtorno bipolar I com um episódio maníaco ou misto recente que haviam sido estabilizados com ABILIFY 20mg em rótulo aberto e que haviam mantido uma resposta clínica por pelo menos 6 semanas. A primeira fase deste estudo foi um período de estabilização aberto no qual pacientes internados e ambulatoriais foram estabilizados clinicamente e então mantidos em ABILIFY aberto (15 ou 30 mg/dia, com uma dose inicial de 30 mg/dia) por pelo menos 6 semanas consecutivas. Cento e sessenta e um pacientes ambulatoriais foram então randomizados de forma duplo-cega, para a mesma dose de ABILIFY em que estavam no final do período de estabilização e manutenção ou placebo e foram então monitorados para recaída maníaca ou depressiva. Durante a fase de randomização, o ABILIFY foi superior ao placebo no tempo para o número de recaídas afetivas combinadas (maníacos mais depressivos), o desfecho primário para este estudo (Estudo 7 na Figura 7). Um total de 55 eventos de humor foram observados durante a fase de tratamento duplo-cego. Dezenove eram do grupo ABILIFY e 36 eram do grupo placebo. O número de episódios maníacos observados no grupo ABILIFY 15mg (6) foi menor do que no grupo placebo (19), enquanto o número de episódios depressivos no grupo ABILIFY (9) foi semelhante ao do grupo placebo (11) .
Um exame dos subgrupos populacionais não revelou nenhuma evidência clara de responsividade diferencial com base na idade e sexo; no entanto, houve número insuficiente de pacientes em cada um dos grupos étnicos para avaliar adequadamente as diferenças entre os grupos.
Figura 7: Estimativa de Kaplan-Meier da proporção cumulativa de pacientes com recaída (estudo bipolar 7) 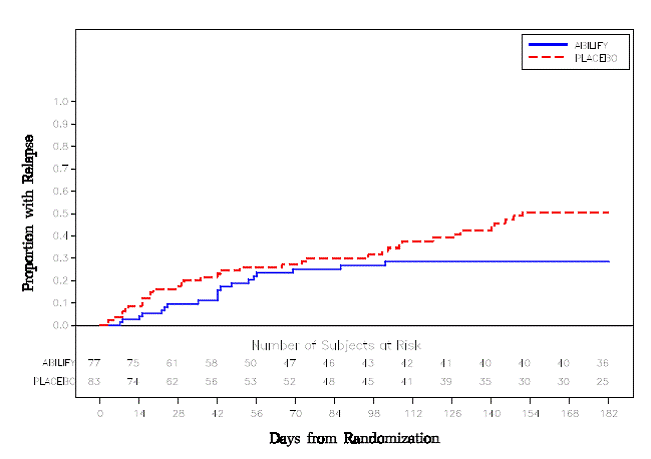
Terapia de Manutenção Adjuvante
Um estudo de manutenção adjuvante foi realizado em pacientes adultos que preencheram os critérios do DSMIV para transtorno bipolar I com um episódio maníaco ou misto recente. Os pacientes foram iniciados com lítio aberto (0,6 a 1,0 mEq/L) ou valproato (50 a 125 μg/mL) em níveis séricos terapêuticos e permaneceram em doses estáveis por 2 semanas. Ao final de 2 semanas, os pacientes que demonstraram resposta inadequada (escore total Y-MRS ≥16 e ≤35% de melhora no escore total Y-MRS) ao lítio ou valproato receberam ABILIFY com uma dose inicial de 15 mg/dia com a opção aumentar para 30 mg ou reduzir para 10 mg já no 4º dia, como terapia adjuvante com lítio ou valproato de rótulo aberto. Antes da randomização, os pacientes que receberam a combinação de ABILIFY simples-cego e lítio ou valproato foram obrigados a manter a estabilidade (escores totais Y-MRS e MADRS ≤12) por 12 semanas consecutivas. Trezentos e trinta e sete pacientes foram então randomizados de forma duplo-cega, para a mesma dose de ABILIFY 20mg em que estavam no final do período de estabilização ou placebo mais lítio ou valproato e foram então monitorados para maníaco, misto ou recaída depressiva por um período máximo de 52 semanas. ABILIFY 15mg foi superior ao placebo no desfecho primário, tempo desde a randomização até a recaída a qualquer evento de humor (Estudo 8 na Figura 8). Um evento de humor foi definido como hospitalização por um episódio maníaco, misto ou depressivo, descontinuação do estudo devido à falta de eficácia acompanhada de escore Y-MRS >16 e/ou MADRS >16, ou um EAS de agravamento da doença acompanhado por Y-MRS Pontuação MRS >16 e/ou MADRS >16. Um total de 68 eventos de humor foram observados durante a fase de tratamento duplo-cego. Vinte e cinco eram do grupo ABILIFY 20mg e 43 eram do grupo placebo. O número de episódios maníacos observados no grupo ABILIFY 15mg (7) foi menor do que no grupo placebo (19), enquanto o número de episódios depressivos no grupo ABILIFY (14) foi semelhante ao do grupo placebo (18) . As curvas de Kaplan-Meier do tempo desde a randomização até a recaída a qualquer evento de humor durante a fase de tratamento duplo-cego de 52 semanas para os grupos ABILIFY 10mg e placebo são mostradas na Figura 8.
Figura 8: Estimativa de Kaplan-Meier da proporção cumulativa de pacientes com recaída a qualquer evento de humor (estudo bipolar 8) 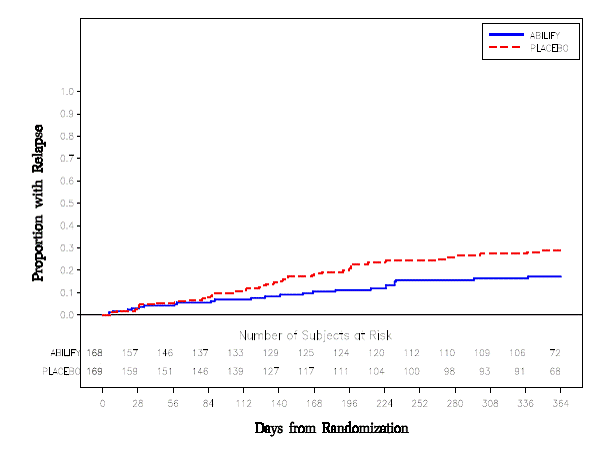
Um exame dos subgrupos populacionais não revelou nenhuma evidência clara de responsividade diferencial com base na idade e sexo; no entanto, houve número insuficiente de pacientes em cada um dos grupos étnicos para avaliar adequadamente as diferenças entre os grupos.
Tratamento Adjuvante do Transtorno Depressivo Maior
Adultos
eficácia de ABILIFY 15mg no tratamento adjuvante do transtorno depressivo maior (TDM) foi demonstrada em dois estudos de curto prazo (6 semanas), controlados por placebo, em pacientes adultos que atenderam aos critérios do DSM-IV para TDM que tiveram uma resposta inadequada ao terapia antidepressiva prévia (1 a 3 ciclos) no episódio atual e que também demonstraram uma resposta inadequada a 8 semanas de terapia antidepressiva prospectiva (paroxetina de liberação controlada, venlafaxina de liberação prolongada, fluoxetina, escitalopram ou sertralina). A resposta inadequada para o tratamento prospectivo foi definida como menos de 50% de melhora na versão de 17 itens da Escala de Avaliação de Depressão de Hamilton (HAMD17), pontuação mínima HAMD17 de 14 e uma classificação de Melhoria de Impressões Globais de não melhor do que uma melhora mínima. A resposta inadequada ao tratamento anterior foi definida como menos de 50% de melhora percebida pelo paciente após um mínimo de 6 semanas de terapia antidepressiva na dose mínima eficaz ou acima dela.
principal instrumento utilizado para avaliar os sintomas depressivos foi a Escala de Avaliação de Depressão de Montgomery-Asberg (MADRS), uma escala de 10 itens avaliada pelo clínico usada para avaliar o grau de sintomatologia depressiva. O principal instrumento secundário foi a Sheehan Disability Scale (SDS), um instrumento de autoavaliação de 3 itens usado para avaliar o impacto da depressão em três domínios de funcionamento com cada item pontuado de 0 (nada) a 10 (extremo).
Nos dois ensaios (n=381, n=362), ABILIFY 15mg foi superior ao placebo na redução dos escores totais médios do MADRS (Estudos 1, 2 na Tabela 28). Em um estudo, o ABILIFY também foi superior ao placebo na redução da pontuação média do SDS.
Em ambos os ensaios, os pacientes receberam ABILIFY 15mg adjuvante aos antidepressivos na dose de 5mg/dia. Com base na tolerabilidade e eficácia, as doses podem ser ajustadas em incrementos de 5 mg, com uma semana de intervalo. As doses permitidas foram: 2, 5, 10, 15 mg/dia, e para pacientes que não estavam em uso de inibidores potentes do CYP2D6 fluoxetina e paroxetina, 20 mg/dia. A dose final média no ponto final para os dois ensaios foi de 10,7 e 11,4 mg/dia.
Um exame de subgrupos populacionais não revelou evidências de resposta diferencial com base na idade, escolha do antidepressivo prospectivo ou raça. Em relação ao sexo, observou-se uma redução média menor no escore total do MADRS no sexo masculino do que no feminino.
Irritabilidade Associada ao Transtorno Autista
Pacientes pediátricos
eficácia de ABILIFY (aripiprazol) no tratamento da irritabilidade associada ao transtorno autista foi estabelecida em dois estudos controlados por placebo de 8 semanas em pacientes pediátricos (6 a 17 anos de idade) que preencheram os critérios do DSM-IV para transtorno autista e comportamentos demonstrados como birras, agressividade, comportamento autolesivo ou uma combinação desses problemas. Mais de 75% desses indivíduos tinham menos de 13 anos de idade.
A eficácia foi avaliada por meio de duas escalas de avaliação: Aberrant Behavior Checklist (ABC) e a escala Clinical Global Impression-Improvement (CGI-I). A medida de resultado primário em ambos os estudos foi a mudança da linha de base para o ponto final na subescala de irritabilidade do ABC (ABC-I). A subescala ABC-I mediu os sintomas de irritabilidade no transtorno autista.
Os resultados destes ensaios são os seguintes:
Em um dos estudos controlados por placebo de 8 semanas, crianças e adolescentes com transtorno autista (n=98), com idades entre 6 e 17 anos, receberam doses diárias de placebo ou ABILIFY 2 a 15 mg/dia. ABILIFY, começando com 2 mg/dia com aumentos permitidos até 15 mg/dia com base na resposta clínica, melhorou significativamente as pontuações na subescala ABC-I e na escala CGI-I em comparação com o placebo. A dose diária média de ABILIFY 10mg no final de 8 semanas de tratamento foi de 8,6 mg/dia (Estudo 1 na Tabela 29).
No outro estudo controlado por placebo de 8 semanas em crianças e adolescentes com transtorno autista (n=218), com idades entre 6 e 17 anos, três doses fixas de ABILIFY (5 mg/dia, 10 mg/dia ou 15 mg/dia dia) foram comparados ao placebo. A dosagem de ABILIFY começou com 2 mg/dia e foi aumentada para 5 mg/dia após uma semana. Após uma segunda semana, foi aumentada para 10 mg/dia para pacientes nos braços de dose de 10 e 15 mg e, após uma terceira semana, foi aumentada para 15 mg/dia no braço de tratamento de 15 mg/dia (Estudo 2 em Tabela 29). Todas as três doses de ABILIFY melhoraram significativamente as pontuações na subescala ABC-I em comparação com o placebo.
Transtorno de Tourette
Pacientes pediátricos
eficácia de ABILIFY (aripiprazol) no tratamento do transtorno de Tourette foi estabelecida em um de 8 semanas (7 a 17 anos de idade) e um de 10 semanas (6 a 18 anos de idade), estudos controlados por placebo em pacientes pediátricos (6 a 18 anos de idade) que preencheram os critérios do DSM-IV para transtorno de Tourette e tiveram uma pontuação total de tic (TTS) ≥ 20 - 22 na Yale Global Tic Severity Scale (YGTSS). O YGTSS é uma escala totalmente validada projetada para medir a gravidade do tique atual. A eficácia foi avaliada usando duas escalas de avaliação: 1) a pontuação total de Tic (TTS) do YGTSS e 2) a Escala de Impressões Globais Clínicas para Síndrome de Tourette (CGI-TS), uma medida resumida determinada pelo clínico que leva em consideração todas as informações disponíveis do paciente. Mais de 65% desses pacientes tinham menos de 13 anos de idade.
medida de resultado primário em ambos os ensaios foi a mudança da linha de base para o desfecho no TTS do YGTSS. As classificações para o TTS são feitas em 5 dimensões diferentes em uma escala de 0 a 5 para tiques motores e vocais cada. A soma dessas 10 pontuações fornece um TTS (ou seja, 0-50).
Os resultados destes ensaios são os seguintes:
No estudo de 8 semanas, controlado por placebo, de dose fixa, crianças e adolescentes com transtorno de Tourette (n=133), com idades entre 7 e 17 anos, foram randomizados 1:1:1 para dose baixa ABILIFY, dose alta ABILIFY 15mg ou placebo. As doses alvo para os grupos de dose baixa e alta de ABILIFY 10mg foram baseadas no peso. Pacientes
Figura 9: Média de Mudança do Mínimo Quadrado da Linha de Base em YGTSS TTS por Semana (Estudo de Transtorno de Tourette 1) 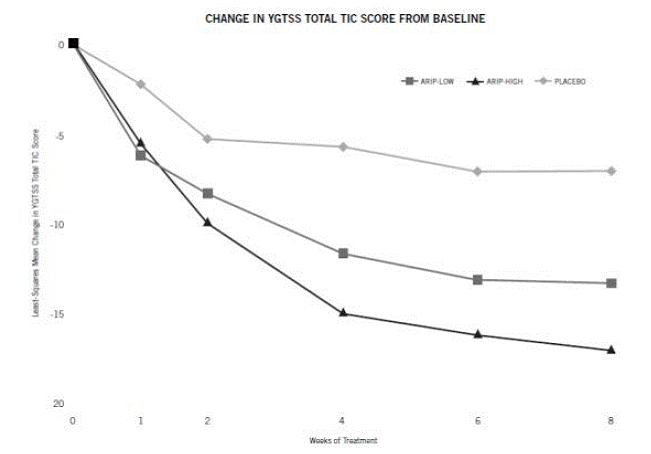
No estudo de dose flexível de 10 semanas, controlado por placebo, em crianças e adolescentes com transtorno de Tourette (n=61), com idades entre 6 e 18 anos, os pacientes receberam doses diárias de placebo ou ABILIFY, começando com 2 mg/dia. dia com aumentos permitidos até 20 mg/dia com base na resposta clínica. ABILIFY demonstrou pontuações estatisticamente significativamente melhores na escala YGTSS TTS em comparação com placebo (Estudo 2 na Tabela 30). A dose diária média de ABILIFY no final de 10 semanas de tratamento foi de 6,54 mg/dia.
Agitação associada à esquizofrenia ou mania bipolar
eficácia de ABILIFY intramuscular para injeção para o tratamento da agitação foi estabelecida em três ensaios de curta duração (24 horas), controlados por placebo, em pacientes agitados internados de dois grupos diagnósticos: esquizofrenia e transtorno bipolar I (episódios maníacos ou mistos, com ou sem características psicóticas). Cada um dos estudos incluiu um único braço de tratamento comparador ativo de injeção de haloperidol (estudos de esquizofrenia) ou injeção de lorazepam (estudo de mania bipolar). Os pacientes podem receber até três injeções durante os períodos de tratamento de 24 horas; no entanto, os pacientes não puderam receber a segunda injeção até após o período inicial de 2 horas, quando a medida de eficácia primária foi avaliada. Os pacientes inscritos nos estudos precisavam ser: (1) julgados pelos investigadores clínicos como clinicamente agitados e candidatos clinicamente apropriados para tratamento com medicação intramuscular e (2) exibindo um nível de agitação que atingisse ou excedesse uma pontuação limite de ≥15 em os cinco itens que compõem o Componente Excitado da Escala de Síndrome Positiva e Negativa (PANSS) (ou seja, itens de controle de impulso ruim, tensão, hostilidade, falta de cooperação e excitação) com pelo menos dois itens individuais pontuações ≥4 usando um sistema de pontuação de 1-7 (1 = ausente, 4 = moderado, 7 = extremo). Nos estudos, a pontuação média inicial do PANSS Excited Component foi de 19, com pontuações variando de 15 a 34 (de uma pontuação máxima de 35), sugerindo assim níveis predominantemente moderados de agitação com alguns pacientes apresentando níveis leves ou graves de agitação. A medida de eficácia primária utilizada para avaliar os sinais e sintomas de agitação nestes ensaios foi a alteração da linha de base no Componente Excitado PANSS 2 horas após a injeção. Uma medida secundária chave foi a Escala de Impressão Clínica Global de Melhoria (CGI-I). Seguem os resultados dos testes:
Em um estudo controlado por placebo em pacientes internados agitados que preenchiam predominantemente os critérios do DSM-IV para esquizofrenia (n = 350), foram avaliadas quatro doses fixas de injeção de ABILIFY 20 mg de 1 mg, 5,25 mg, 9,75 mg e 15 mg. Às 2 horas após a injeção, as doses de 5,25 mg, 9,75 mg e 15 mg foram estatisticamente superiores ao placebo no Componente Excitado PANSS (Estudo 1 na Tabela 31) e na Escala CGII.
Em um segundo estudo controlado por placebo em pacientes internados agitados que preenchiam predominantemente os critérios do DSM-IV para esquizofrenia (n=445), foi avaliada uma dose de injeção fixa de 15 mg de ABILIFY de 9,75 mg. Às 2 horas após a injeção, ABILIFY para injeção foi estatisticamente superior ao placebo no Componente Excitado PANSS (Estudo 2 na Tabela 31) e na Escala CGI-I.
Em um estudo controlado por placebo em pacientes internados agitados que atendem aos critérios do DSMIV para transtorno bipolar I (maníaco ou misto) (n=291), foram avaliadas duas doses fixas de injeção de 10 mg de ABILIFY de 9,75 mg e 15 mg. Às 2 horas após a injeção, ambas as doses foram estatisticamente superiores ao placebo no Componente Excitado PANSS (Estudo 3 na Tabela 31).
O exame de subconjuntos populacionais (idade, raça e sexo) não revelou qualquer responsividade diferencial com base nesses subgrupos.
INFORMAÇÃO DO PACIENTE
ABILIFY® (aripiprazol) Comprimidos
ABILIFY DISCMELT® (aripiprazol) Comprimidos de desintegração oral
ABILIFY® (aripiprazol) Solução Oral
ABILIFY® (aripiprazol) injeção apenas para uso intramuscular
Qual é a informação mais importante que devo saber sobre ABILIFY 20mg?
(Para outros efeitos colaterais, consulte também “Quais são os possíveis efeitos colaterais do ABILIFY?”)
Efeitos colaterais graves podem ocorrer quando você toma ABILIFY, incluindo:
- Aumento do risco de morte em pacientes idosos com psicose relacionada à demência: Medicamentos como ABILIFY 10mg podem aumentar o risco de morte em idosos que perderam o contato com a realidade (psicose) devido à confusão e perda de memória (demência). ABILIFY não está aprovado para o tratamento de pacientes com psicose relacionada à demência.
- Risco de pensamentos ou ações suicidas: Medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas:
1. Os medicamentos antidepressivos podem aumentar os pensamentos ou ações suicidas em algumas crianças, adolescentes e adultos jovens nos primeiros meses de tratamento.
2. Depressão e outras doenças mentais graves são as causas mais importantes de pensamentos e ações suicidas. Algumas pessoas podem ter um risco particularmente alto de ter pensamentos ou ações suicidas. Estes incluem pessoas que têm (ou têm histórico familiar de) doença bipolar (também chamada de doença maníaco-depressiva) ou pensamentos ou ações suicidas.
3. Como posso vigiar e tentar prevenir pensamentos e ações suicidas em mim ou em um membro da família?
- Preste muita atenção a quaisquer mudanças, especialmente mudanças repentinas, de humor, comportamentos, pensamentos ou sentimentos. Isso é muito importante quando um medicamento antidepressivo é iniciado ou quando a dose é alterada.
- Ligue para o profissional de saúde imediatamente para relatar mudanças novas ou repentinas no humor, comportamento, pensamentos ou sentimentos.
- Mantenha todas as visitas de acompanhamento com o profissional de saúde conforme programado. Ligue para o médico entre as visitas, conforme necessário, especialmente se tiver dúvidas sobre os sintomas.
Ligue para um profissional de saúde imediatamente se você ou seu familiar tiver algum dos seguintes sintomas, especialmente se forem novos, piores ou se preocuparem:
- pensamentos sobre suicídio ou morte
- tentativas de suicídio
- depressão nova ou pior
- ansiedade nova ou pior
- sentindo-se muito agitado ou inquieto
- ataques de pânico
- problemas para dormir (insônia)
- irritabilidade nova ou pior
- agindo de forma agressiva, com raiva ou violento
- agindo em impulsos perigosos
- um aumento extremo na atividade e na fala (mania)
- outras mudanças incomuns no comportamento ou humor
O que mais eu preciso saber sobre medicamentos antidepressivos?
- Nunca interrompa um medicamento antidepressivo sem primeiro falar com um profissional de saúde. Parar um medicamento antidepressivo de repente pode causar outros sintomas.
- Os antidepressivos são medicamentos usados para tratar a depressão e outras doenças. É importante discutir todos os riscos de tratar a depressão e também os riscos de não tratá-la. Os pacientes e suas famílias ou outros cuidadores devem discutir todas as opções de tratamento com o profissional de saúde, não apenas o uso de antidepressivos.
- medicamentos antidepressivos têm outros efeitos colaterais. Converse com o médico sobre os efeitos colaterais do medicamento prescrito para você ou seu familiar.
- Medicamentos antidepressivos podem interagir com outros medicamentos. Conheça todos os medicamentos que você ou seu familiar toma. Mantenha uma lista de todos os medicamentos para mostrar ao profissional de saúde. Não inicie novos medicamentos sem primeiro consultar seu médico.
- Nem todos os medicamentos antidepressivos prescritos para crianças são aprovados pela FDA para uso em crianças. Fale com o profissional de saúde do seu filho para obter mais informações.
O que é ABILIFY?
- ABILIFY 20mg comprimidos orais, comprimidos de desintegração oral e solução oral são medicamentos prescritos usados para tratar:
- Esquizofrenia
- episódios maníacos ou mistos que acontecem com transtorno bipolar I
- transtorno depressivo maior (TDM) quando ABILIFY 20mg é usado com medicamentos antidepressivos
- irritabilidade associada ao transtorno autista
- Distúrbio de Tourette
- ABILIFY Injection é um medicamento de prescrição usado para tratar:
- agitação associada à esquizofrenia ou mania bipolar
Não se sabe se ABILIFY 10mg é seguro ou eficaz em crianças:
- menores de 13 anos com esquizofrenia
- menos de 10 anos de idade com transtorno bipolar I
- menores de 6 anos com irritabilidade associada ao transtorno autista
- menores de 6 anos de idade com transtorno de Tourette
Não tome ABILIFY 20mg se você são alérgicos ao aripiprazol ou a qualquer um dos ingredientes de ABILIFY. Consulte o final deste Guia de Medicação para obter uma lista completa dos ingredientes do ABILIFY.
Antes de tomar ABILIFY 15mg, informe o seu médico sobre todas as suas condições médicas, incluindo se você tem ou teve:
- diabetes ou açúcar elevado no sangue em você ou sua família; o seu médico deve verificar o seu nível de açúcar no sangue antes de iniciar ABILIFY 10 mg e também durante o tratamento.
- convulsões (convulsões).
- pressão arterial baixa ou alta.
- problemas cardíacos ou derrame.
- gravidez ou planos de engravidar. Não se sabe se ABILIFY prejudicará o feto.
- Se você engravidar enquanto estiver recebendo ABILIFY 10mg, converse com seu médico sobre o registro no Registro Nacional de Gravidez para Antipsicóticos Atípicos. Você pode se registrar ligando para 1-866-961-2388 ou acesse http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
- amamentando ou planeja amamentar. ABILIFY passa para o leite materno. Converse com seu médico sobre a melhor maneira de alimentar seu bebê se você receber ABILIFY.
- baixa contagem de glóbulos brancos.
- fenilcetonúria. ABILIFY DISCMELT Os comprimidos de desintegração oral contêm fenilalanina.
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos e de venda livre, vitaminas e suplementos de ervas.
ABILIFY e outros medicamentos podem afetar um ao outro causando possíveis efeitos colaterais graves. ABILIFY pode afetar o funcionamento de outros medicamentos e outros medicamentos podem afetar o funcionamento de ABILIFY.
O seu médico pode informá-lo se é seguro tomar ABILIFY com outros medicamentos. Não inicie ou interrompa nenhum medicamento enquanto estiver tomando ABILIFY sem falar primeiro com seu médico. Conheça os medicamentos que você toma. Mantenha uma lista de seus medicamentos para mostrar ao seu médico e farmacêutico quando receber um novo medicamento.
Como devo tomar ABILIFY 20mg?
- Tome ABILIFY 10mg exatamente como seu médico lhe disser para tomá-lo. Não altere a dose nem pare de tomar ABILIFY por conta própria.
- ABILIFY 20mg pode ser tomado com ou sem alimentos.
- Os comprimidos de ABILIFY devem ser engolidos inteiros.
- Se você perder uma dose de ABILIFY 20mg, tome a dose esquecida assim que se lembrar. Se estiver quase na hora da próxima dose, simplesmente pule a dose esquecida e tome a próxima dose no horário regular. Não tome duas doses de ABILIFY 10mg ao mesmo tempo.
- Se lhe foi prescrito ABILIFY DISCMELT, tome-o da seguinte forma:
- Não abra o blister até estar pronto para tomar o comprimido DISCMELT.
- Para remover um comprimido de DISCMELT, abra a embalagem e retire a película do blister para expor o comprimido.
- Não empurre o comprimido através da folha, pois isso pode danificar o comprimido.
- Imediatamente após a abertura do blister, com as mãos secas, retire o comprimido e coloque todo o comprimido desintegrante oral ABILIFY DISCMELT na língua.
- desintegração do comprimido ocorre rapidamente na saliva. Recomenda-se que ABILIFY 10mg DISCMELT seja tomado sem líquido. No entanto, se necessário, pode ser tomado com líquido.
- Não tente dividir o comprimido DISCMELT.
- Se você tomar muito ABILIFY, ligue para o seu médico ou centro de controle de envenenamento em 1-800-222-1222 imediatamente, ou vá para a sala de emergência do hospital mais próximo.
O que devo evitar ao tomar ABILIFY 10mg?
- Não dirija, opere máquinas pesadas ou faça outras atividades perigosas até saber como ABILIFY 10mg o afeta. ABILIFY 20mg pode causar sonolência.
- Evite ficar superaquecido ou desidratado.
- Não exagere.
- Em clima quente, fique dentro de casa em um local fresco, se possível.
- Fique longe do sol. Não use roupas demais ou pesadas.
- Beba bastante água.
Quais são os possíveis efeitos colaterais do ABILIFY?
ABILIFY 10mg pode causar efeitos colaterais graves, incluindo:
- Consulte “Quais são as informações mais importantes que devo saber sobre ABILIFY 10mg?”
- Acidente vascular cerebral em idosos (problemas cerebrovasculares) que podem levar à morte
- Síndrome neuroléptica maligna (SNM). Informe o seu médico imediatamente se tiver alguns ou todos os seguintes sintomas: febre alta, rigidez muscular, confusão, sudorese, alterações no pulso, frequência cardíaca e pressão arterial. Estes podem ser sintomas de uma condição rara e grave que pode levar à morte. Ligue para o seu médico imediatamente se tiver algum destes sintomas.
- Movimentos corporais descontrolados (discinesia tardia). ABILIFY pode causar movimentos que você não pode controlar em seu rosto, língua ou outras partes do corpo. A discinesia tardia pode não desaparecer, mesmo se você parar de receber ABILIFY. A discinesia tardia também pode começar após você parar de receber ABILIFY.
- Problemas com o seu metabolismo, como:
- Açúcar elevado no sangue (hiperglicemia) e diabetes. aumento do açúcar no sangue pode ocorrer em algumas pessoas que tomam ABILIFY. Açúcar no sangue extremamente alto pode levar ao coma ou à morte. Se você tem diabetes ou fatores de risco para diabetes (como excesso de peso ou histórico familiar de diabetes), seu médico deve verificar seu nível de açúcar no sangue antes de iniciar ABILIFY e durante o tratamento.
Ligue para o seu médico se tiver algum destes sintomas de açúcar elevado no sangue enquanto estiver recebendo ABILIFY:
- sinto muita sede
- necessidade de urinar mais do que o habitual
- sinto muita fome
- sentir-se fraco ou cansado
- sentir-se mal do estômago
- sente-se confuso ou seu hálito cheira a fruta
- Aumento dos níveis de gordura (colesterol e triglicerídeos) no sangue.
- Ganho de peso. Você e seu médico devem verificar seu peso regularmente.
- Desejos incomuns. Algumas pessoas que tomaram ABILIFY 15mg tiveram impulsos incomuns, como jogos de azar, compulsão alimentar ou comer que você não pode controlar (compulsivo), compras compulsivas e impulsos sexuais. Se você ou seus familiares perceberem que você está tendo impulsos ou comportamentos incomuns, converse com seu médico.
- Hipotensão ortostática (diminuição da pressão arterial). Tonturas ou desmaios podem ocorrer ao se levantar muito rapidamente de uma posição sentada ou deitada.
- Cataratas. ABILIFY pode deixá-lo sonolento ou tonto, pode causar uma diminuição da pressão arterial ao mudar de posição e pode retardar o pensamento e as habilidades motoras, o que pode levar a quedas que podem causar fraturas ou outras lesões.
- Baixa contagem de glóbulos brancos
- Convulsões (convulsões)
- Problemas com o controle da temperatura corporal, especialmente quando você se exercita muito ou está em uma área muito quente. É importante que você beba água para evitar a desidratação. Consulte “O que devo evitar ao receber ABILIFY 15mg?”
- Dificuldade em engolir que pode fazer com que alimentos ou líquidos entrem nos pulmões.
Os efeitos colaterais mais comuns de ABILIFY 10mg em adultos incluem:
- Náusea
- tontura
- vômito
- ansiedade
- constipação
- insônia
- dor de cabeça
- inquietação
- visão embaçada
- doença respiratória superior
- sensação interior de inquietação/necessidade de movimento (acatisia)
Os efeitos colaterais mais comuns do ABILIFY em crianças incluem:
- sentindo sonolento
- insônia
- dor de cabeça
- náusea
- vômito
- nariz entupido
- fadiga
- ganho de peso
- aumento ou diminuição do apetite
- movimento descontrolado, como inquietação, tremor
- aumento da saliva ou baba
- rigidez muscular
Estes não são todos os possíveis efeitos colaterais do ABILIFY.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar o ABILIFY?
- Armazene ABILIFY 15mg em temperatura ambiente, entre 20°C e 25°C (68°F a 77°F).
- Os frascos abertos de ABILIFY 10mg Solução Oral podem ser usados por até 6 meses após a abertura, mas não além da data de validade no frasco.
Mantenha ABILIFY e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre o uso seguro e eficaz do ABILIFY
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use ABILIFY 20mg para uma condição para a qual não foi prescrito. Não dê ABILIFY 20mg a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los. Você pode pedir ao seu médico ou farmacêutico informações sobre o ABILIFY 10mg que foi escrito para profissionais de saúde.
Quais são os ingredientes do ABILIFY?
Ingrediente ativo: aripiprazol
Ingredientes inativos:
amido de milho, hidroxipropilcelulose, lactose monohidratada, estearato de magnésio e celulose microcristalina. Os corantes incluem óxido férrico (amarelo ou vermelho) e FD&C Blue No. 2 Aluminum Lake
ABILIFY 10mg DISCMELT comprimidos de desintegração oral: acessulfame de potássio, aspartame (que contém fenilalanina), silicato de cálcio, croscarmelose sódica, crospovidona, creme de baunilha (aromatizantes naturais e artificiais), estearato de magnésio, celulose microcristalina, dióxido de silício, ácido tartárico e xilitol. Os corantes incluem óxido férrico (amarelo ou vermelho) e FD&C Blue No. 2 Aluminum Lake
Solução oral ABILIFY: edetato dissódico, frutose (200 mg por mL), glicerina, ácido dl-láctico, metilparabeno, propilenoglicol, propilparabeno, hidróxido de sódio, sacarose (400 mg por mL) e água purificada. A solução oral é aromatizada com creme de laranja natural e outros aromas naturais
Para obter mais informações sobre o ABILIFY, acesse www.abilify.com ou ligue para 1-800-438-6055.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA
