Actos 15mg, 30mg Pioglitazone Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Actos e como é usado?
Actos 15mg é um medicamento de prescrição utilizado para tratar os sintomas da diabetes mellitus tipo 2. Actos pode ser usado sozinho ou com outros medicamentos.
Actos é um medicamento antidiabético, tiazolidinedionas.
Não se sabe se Actos 15mg é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Actos 15mg?
Actos pode causar efeitos colaterais graves, incluindo:
- falta de ar (especialmente ao deitar),
- cansaço incomum,
- inchaço,
- ganho de peso rápido,
- urina rosa ou vermelha,
- micção dolorosa ou difícil,
- vontade nova ou agravada de urinar,
- alterações na visão e
- dor súbita e incomum na mão, braço ou pé
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Actos incluem:
- dor de cabeça,
- dores musculares e
- sintomas de resfriado (nariz entupido, dor sinusal, espirros, dor de garganta)
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Estes não são todos os possíveis efeitos colaterais do Actos. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
INSUFICIÊNCIA CARDÍACA CONGESTIVA
- Tiazolidinedionas, incluindo ACTOS 15mg, causam ou exacerbam insuficiência cardíaca congestiva em alguns pacientes [ver AVISOS E PRECAUÇÕES ].
- Após o início de ACTOS 30mg e após o aumento da dose, monitore os pacientes cuidadosamente quanto a sinais e sintomas de insuficiência cardíaca (por exemplo, ganho de peso excessivo, rápido, dispnéia e/ou edema). Se ocorrer insuficiência cardíaca, ela deve ser tratada de acordo com os padrões atuais de tratamento e deve ser considerada a descontinuação ou redução da dose de ACTOS 15mg.
- ACTOS não é recomendado em pacientes com insuficiência cardíaca sintomática.
- O início de ACTOS em pacientes com insuficiência cardíaca Classe III ou IV da New York Heart Association (NYHA) é contraindicado [ver CONTRA-INDICAÇÕES e AVISOS E PRECAUÇÕES ].
DESCRIÇÃO
Os comprimidos de ACTOS são uma tiazolidinediona e um agonista do receptor ativado por proliferador de peroxissoma (PPAR) gama que contém um medicamento antidiabético oral: pioglitazona.
O monocloridrato de pioglitazona [(±)-5-[[4-[2-(5-etil-2-piridinil) etoxi] fenil] metil]-2,4-] tiazolidinediona contém um carbono assimétrico e o composto é sintetizado e usado como a mistura racêmica. Os dois enantiômeros da pioglitazona se interconvertem in vivo. Não foram encontradas diferenças na atividade farmacológica entre os dois enantiômeros. A fórmula estrutural é a seguinte:
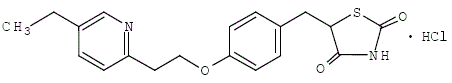
cloridrato de pioglitazona é um pó cristalino branco inodoro que possui uma fórmula molecular de C19H20N2O3S•HCl e um peso molecular de 392,90 daltons. É solúvel em N,Ndimetilformamida, pouco solúvel em etanol anidro, muito pouco solúvel em acetona e acetonitrila, praticamente insolúvel em água e insolúvel em éter.
ACTOS está disponível como um comprimido para administração oral contendo 15 mg, 30 mg ou 45 mg de pioglitazona (como base) formulada com os seguintes excipientes: lactos 30 mg monohidratado NF, hidroxipropilcelulose NF, carboximetilcelulose cálcio NF e estearato de magnésio NF.
INDICAÇÕES
Monoterapia e Terapia Combinada
ACTOS 30mg é indicado como adjuvante à dieta e exercícios para melhorar o controle glicêmico em adultos com diabetes mellitus tipo 2 em vários contextos clínicos [ver Estudos clínicos ].
Limitações importantes de uso
ACTOS 15mg exerce seu efeito anti-hiperglicêmico apenas na presença de insulina endógena. ACTOS 30mg não deve ser usado para tratar diabetes tipo 1 ou cetoacidose diabética, pois não seria eficaz nessas situações.
Tenha cuidado em pacientes com doença hepática [ver AVISOS E PRECAUÇÕES ].
DOSAGEM E ADMINISTRAÇÃO
Recomendações para todos os pacientes
ACTOS 15mg deve ser tomado uma vez ao dia e pode ser tomado independentemente das refeições.
A dose inicial recomendada para pacientes sem insuficiência cardíaca congestiva é de 15 mg ou 30 mg uma vez ao dia.
A dose inicial recomendada para pacientes com insuficiência cardíaca congestiva (NYHA Classe I ou II) é de 15 mg uma vez ao dia.
A dose pode ser titulada em incrementos de 15 mg até um máximo de 45 mg uma vez ao dia com base na resposta glicêmica determinada pela HbA1c.
Após o início de ACTOS 30mg ou com aumento da dose, monitore os pacientes cuidadosamente quanto a reações adversas relacionadas à retenção de líquidos, como ganho de peso, edema e sinais e sintomas de insuficiência cardíaca congestiva [ver AVISO DE CAIXA e AVISOS E PRECAUÇÕES ].
Testes hepáticos (alanina e aspartato aminotransferases séricas, fosfatase alcalina e bilirrubina total) devem ser obtidos antes de iniciar ACTOS. O monitoramento periódico de rotina dos testes hepáticos durante o tratamento com ACTOS 30mg não é recomendado em pacientes sem doença hepática. Os pacientes que apresentam anormalidades nos testes hepáticos antes do início de ACTOS ou que apresentam testes hepáticos anormais durante o tratamento com ACTOS devem ser tratados conforme descrito em Advertências e Precauções [ver AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Uso concomitante com um secretagogo de insulina ou insulina
Se ocorrer hipoglicemia em um paciente que coadministrou ACTOS 30mg e um secretagogo de insulina (por exemplo, sulfonilureia), a dose do secretagogo de insulina deve ser reduzida.
Se ocorrer hipoglicemia em um paciente coadministrado com ACTOS 30mg e insulina, a dose de insulina deve ser diminuída em 10% a 25%. Ajustes adicionais na dose de insulina devem ser individualizados com base na resposta glicêmica.
Uso concomitante com fortes inibidores de CYP2C8
coadministração de ACTOS 30mg e gemfibrozil, um forte inibidor do CYP2C8, aumenta a exposição à pioglitazona em aproximadamente 3 vezes. Portanto, a dose máxima recomendada de ACTOS é de 15 mg por dia quando usado em combinação com gemfibrozil ou outros inibidores fortes de CYP2C8 [ver INTERAÇÕES MEDICAMENTOSAS e FARMACOLOGIA CLÍNICA ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
O comprimido redondo contém pioglitazona da seguinte forma:
- 15 mg: Branco a esbranquiçado, gravado com “ACTOS” de um lado e “15” do outro
- 30 mg: Branco a esbranquiçado, gravado com “ACTOS” de um lado e “30” do outro
- 45 mg: Branco a esbranquiçado, gravado com “ACTOS” de um lado e “45” do outro
Armazenamento e manuseio
ATOS está disponível em comprimidos de 15 mg, 30 mg e 45 mg da seguinte forma:
comprimido de 15mg : Comprimido branco a esbranquiçado, redondo, convexo, sem ranhura, com “ACTOS” de um lado e “15” do outro, disponível em:
NDC 64764-151-04 Garrafas de 30 NDC 64764-151-05 Garrafas de 90 NDC 64764-151-06 Garrafas de 500
comprimido de 30mg Comprimido branco a esbranquiçado, redondo, plano, sem ranhura, com “ACTOS” de um lado e “30” do outro, disponível em:
NDC 64764-301-14 Garrafas de 30 NDC 64764-301-15 Garrafas de 90 NDC 64764-301-16 Garrafas de 500
comprimido de 45mg : Comprimido branco a esbranquiçado, redondo, plano, sem ranhura, com “ACTOS” de um lado e “45” do outro, disponível em:
NDC 64764-451-24 Garrafas de 30 NDC 64764-451-25 Garrafas de 90 NDC 64764-451-26 Garrafas de 500
Armazenar
Armazenar a 25°C (77°F); excursões permitidas para 15-30°C (59-86°F) [veja USP Controlled Room Temperature]. Manter o recipiente bem fechado e proteger da luz, umidade e umidade.
Distribuído por: Takeda Pharmaceuticals America, Inc. Deerfield, IL 60015. Revisado: dezembro de 2017
EFEITOS COLATERAIS
As seguintes reações adversas graves são discutidas em outra parte da bula:
- Insuficiência cardíaca congestiva [ver AVISO DE CAIXA e AVISOS E PRECAUÇÕES ]
- Edema [ver AVISOS E PRECAUÇÕES ]
- Fraturas [ver AVISOS E PRECAUÇÕES ]
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
Mais de 8.500 pacientes com diabetes tipo 2 foram tratados com ACTOS em ensaios clínicos randomizados, duplo-cegos e controlados, incluindo 2.605 pacientes com diabetes tipo 2 e doença macrovascular tratados com ACTOS 30mg no ensaio clínico PROactive. Nesses estudos, mais de 6.000 pacientes foram tratados com ACTOS por seis meses ou mais, mais de 4.500 pacientes foram tratados com ACTOS 15mg por um ano ou mais e mais de 3.000 pacientes foram tratados com ACTOS por pelo menos dois anos.
Em seis ensaios combinados de monoterapia controlada por placebo de 16 a 26 semanas e de terapia combinada de 16 a 24 semanas, a incidência de retiradas devido a eventos adversos foi de 4,5% para pacientes tratados com ACTOS 30mg e 5,8% para o comparador. pacientes tratados. Os eventos adversos mais comuns que levaram à retirada foram relacionados ao controle glicêmico inadequado, embora a incidência desses eventos tenha sido menor (1,5%) com ACTOS 30mg do que com placebo (3,0%).
No ensaio PROactive, a incidência de desistências devido a eventos adversos foi de 9,0% para pacientes tratados com ACTOS 30mg e 7,7% para pacientes tratados com placebo. A insuficiência cardíaca congestiva foi o evento adverso grave mais comum, levando à retirada ocorrendo em 1,3% dos pacientes tratados com ACTOS 30mg e 0,6% dos pacientes tratados com placebo.
Eventos adversos comuns: ensaios de monoterapia de 16 a 26 semanas
Um resumo da incidência e tipo de eventos adversos comuns relatados em três ensaios de monoterapia controlados por placebo de 16 a 26 semanas agrupados de ACTOS é fornecido na Tabela 1. Os termos relatados representam aqueles que ocorreram com uma incidência de >5% e mais comumente em pacientes tratados com ACTOS 15mg do que em pacientes que receberam placebo. Nenhum desses eventos adversos foi relacionado à dose de ACTOS.
Eventos Adversos Comuns: Ensaios de Terapia Complementar Combinada de 16 a 24 semanas
Um resumo da incidência geral e dos tipos de eventos adversos comuns relatados em estudos de ACTOS add-on para sulfonilureia é fornecido na Tabela 2. Os termos relatados representam aqueles que ocorreram com uma incidência >5% e mais comumente com o mais alto testado dose de ACTOS.
Um resumo da incidência geral e dos tipos de eventos adversos comuns relatados em estudos com ACTOS 30mg adicionado à metformina é fornecido na Tabela 3. Os termos relatados representam aqueles que ocorreram com uma incidência > 5% e mais comumente com a maior dose testada de ACTOS.
A Tabela 4 resume a incidência e os tipos de eventos adversos comuns relatados em ensaios de ACTOS add-on à insulina. Os termos relatados representam aqueles que ocorreram com uma incidência >5% e mais comumente com a maior dose testada de ACTOS.
Um resumo da incidência geral e dos tipos de eventos adversos comuns relatados no estudo PROactive é fornecido na Tabela 5. Os termos relatados representam aqueles que ocorreram com uma incidência >5% e mais comumente em pacientes tratados com ACTOS do que em pacientes que recebeu placebo.
Insuficiência Cardíaca Congestiva
Um resumo da incidência de eventos adversos relacionados à insuficiência cardíaca congestiva é fornecido na Tabela 6 para os estudos complementares de 16 a 24 semanas para sulfonilureias, para os estudos complementares de 16 a 24 semanas para insulina e para o add-on de 16 a 24 semanas para ensaios de metformina. Nenhum dos eventos foi fatal.
Pacientes com diabetes tipo 2 e insuficiência cardíaca congestiva classe II da NYHA ou classe III precoce foram randomizados para receber 24 semanas de tratamento duplo-cego com ACTOS 30 mg em doses diárias de 30 mg a 45 mg (n = 262) ou gliburida em doses diárias de 10 mg a 15 mg (n=256). Um resumo da incidência de eventos adversos relacionados à insuficiência cardíaca congestiva relatada neste estudo é fornecido na Tabela 7.
Os eventos de insuficiência cardíaca congestiva que levaram à hospitalização que ocorreram durante o estudo PROactive estão resumidos na Tabela 8.
Segurança cardiovascular
No ensaio PROactive, 5.238 pacientes com diabetes tipo 2 e histórico de doença macrovascular foram randomizados para ACTOS (N = 2.605), com titulação forçada de até 45 mg por dia ou placebo (N = 2.633), além do tratamento padrão. Quase todos os pacientes (95%) estavam recebendo medicamentos cardiovasculares (betabloqueadores, inibidores da ECA, bloqueadores dos receptores da angiotensina II, bloqueadores dos canais de cálcio, nitratos, diuréticos, aspirina, estatinas e fibratos). No início do estudo, os pacientes tinham idade média de 62 anos, duração média do diabetes de 9,5 anos e HbA1c média de 8,1%. A duração média do seguimento foi de 34,5 meses. O objetivo primário deste estudo foi examinar o efeito de ACTOS na mortalidade e morbidade macrovascular em pacientes com diabetes mellitus tipo 2 que estavam em alto risco de eventos macrovasculares. A variável primária de eficácia foi o tempo até a primeira ocorrência de qualquer evento em um desfecho composto cardiovascular que incluiu mortalidade por todas as causas, infarto do miocárdio (IM) não fatal, incluindo infarto do miocárdio silencioso, acidente vascular cerebral, síndrome coronariana aguda, intervenção cardíaca incluindo cirurgia de revascularização do miocárdio ou intervenção percutânea, amputação maior da perna acima do tornozelo e cirurgia de revascularização ou revascularização na perna. Um total de 514 (19,7%) pacientes tratados com ACTOS 15mg e 572 (21,7%) pacientes tratados com placebo apresentaram pelo menos um evento do desfecho composto primário (taxa de risco 0,90; Intervalo de Confiança de 95%: 0,80, 1,02; p=0,10 ).
Embora não tenha havido diferença estatisticamente significativa entre ACTOS e placebo para a incidência de três anos de um primeiro evento dentro deste composto, não houve aumento na mortalidade ou no total de eventos macrovasculares com ACTOS. O número de primeiras ocorrências e o total de eventos individuais que contribuem para o desfecho composto primário é mostrado na Tabela 9.
Ganho de peso
O ganho de peso relacionado à dose ocorre quando ACTOS 30mg é usado sozinho ou em combinação com outros medicamentos antidiabéticos. O mecanismo de ganho de peso não é claro, mas provavelmente envolve uma combinação de retenção de líquidos e acúmulo de gordura.
As Tabelas 10 e 11 resumem as mudanças no peso corporal com ACTOS e placebo nos ensaios de 16 a 26 semanas randomizados, em monoterapia duplo-cego e de 16 a 24 semanas de terapia complementar combinada e no ensaio PROactive.
Edema
edema induzido pelo uso de ACTOS é reversível quando o ACTOS é descontinuado. O edema geralmente não requer hospitalização, a menos que haja insuficiência cardíaca congestiva coexistente. Um resumo da frequência e tipos de eventos adversos de edema que ocorrem em investigações clínicas de ACTOS 30mg é fornecido na Tabela 12.
Efeitos hepáticos
Não houve evidência de hepatotoxicidade induzida com ACTOS no banco de dados de ensaios clínicos controlados com ACTOS até o momento. Um estudo randomizado, duplo-cego de 3 anos comparando ACTOS 15mg à gliburida como adjuvante da metformina e da terapia com insulina foi projetado especificamente para avaliar a incidência de elevação de ALT sérica para mais de três vezes o limite superior do intervalo de referência, medido a cada oito semanas durante as primeiras 48 semanas do ensaio e depois a cada 12 semanas. Um total de 3/1051 (0,3%) pacientes tratados com ACTOS e 9/1046 (0,9%) pacientes tratados com gliburida desenvolveram valores de ALT maiores que três vezes o limite superior do intervalo de referência. Nenhum dos pacientes tratados com ACTOS no banco de dados de ensaios clínicos controlados com ACTOS até o momento teve uma ALT sérica superior a três vezes o limite superior do intervalo de referência e uma bilirrubina total correspondente superior a duas vezes o limite superior do intervalo de referência, um combinação preditiva do potencial de lesão hepática grave induzida por drogas.
Hipoglicemia
Nos ensaios clínicos ACTOS 15mg, eventos adversos de hipoglicemia foram relatados com base no julgamento clínico dos investigadores e não exigiram confirmação com teste de glicose por punção digital.
No estudo complementar de 16 semanas com sulfonilureia, a incidência de hipoglicemia relatada foi de 3,7% com ACTOS 30 mg e 0,5% com placebo. No teste de 16 semanas com insulina, a incidência de hipoglicemia relatada foi de 7,9% com ACTOS 15 mg, 15,4% com ACTOS 30 mg e 4,8% com placebo.
A incidência de hipoglicemia relatada foi maior com ACTOS 45 mg em comparação com ACTOS 30 mg tanto no estudo de 24 semanas com adição de sulfonilureia (15,7% vs. 13,4%) quanto no estudo de 24 semanas com adição de insulina (47,8 % vs. 43,5%).
Três pacientes nestes quatro estudos foram hospitalizados devido à hipoglicemia. Todos os três pacientes estavam recebendo ACTOS 30 mg (0,9%) no teste de 24 semanas com insulina. Outros 14 pacientes relataram hipoglicemia grave (definida como causando interferência considerável nas atividades habituais do paciente) que não exigiu hospitalização. Esses pacientes estavam recebendo ACTOS 45 mg em combinação com sulfonilureia (n=2) ou ACTOS 30 mg ou 45 mg em combinação com insulina (n=12).
Tumores da Bexiga Urinária
Foram observados tumores na bexiga urinária de ratos machos no estudo de carcinogenicidade de dois anos [ver Toxicologia não clínica ]. Durante o ensaio clínico PROactive de três anos, 14 pacientes de 2.605 (0,54%) randomizados para ACTOS e 5 de 2.633 (0,19%) randomizados para placebo foram diagnosticados com câncer de bexiga. Após excluir os pacientes em que a exposição ao medicamento do estudo foi inferior a um ano no momento do diagnóstico de câncer de bexiga, houve 6 (0,23%) casos em ACTOS 15mg e dois (0,08%) casos em placebo. Após a conclusão do estudo, um grande subconjunto de pacientes foi observado por até 10 anos adicionais, com pouca exposição adicional ao ACTOS. Durante os 13 anos de acompanhamento PROactive e observacional, a ocorrência de câncer de bexiga não diferiu entre os pacientes randomizados para ACTOS ou placebo (HR = 1,00; IC 95%: 0,59-1,72) [ver AVISOS E PRECAUÇÕES ].
Anormalidades laboratoriais
Efeitos hematológicos
ACTOS 15mg pode causar diminuição da hemoglobina e do hematócrito. Em ensaios de monoterapia controlados com placebo, os valores médios de hemoglobina diminuíram de 2% a 4% em pacientes tratados com ACTOS em comparação com uma alteração média na hemoglobina de -1% a +1% em pacientes tratados com placebo. Essas mudanças ocorreram principalmente nas primeiras 4 a 12 semanas de terapia e permaneceram relativamente constantes depois disso. Essas alterações podem estar relacionadas ao aumento do volume plasmático associado à terapia com ACTOS 30mg e provavelmente não estão associadas a quaisquer efeitos hematológicos clinicamente significativos.
Creatina Fosfoquinase
Durante a medição específica do protocolo de creatina fosfoquinase sérica (CPK) em ensaios clínicos ACTOS 15mg, uma elevação isolada na CPK para mais de 10 vezes o limite superior do intervalo de referência foi observada em nove (0,2%) pacientes tratados com ACTOS (valores de 2150 a 11400 UI/L) e em pacientes não tratados com comparador. Seis desses nove pacientes continuaram a receber ACTOS 15mg, dois pacientes apresentaram elevação de CPK no último dia de dosagem e um paciente descontinuou ACTOS devido à elevação. Estas elevações foram resolvidas sem quaisquer sequelas clínicas aparentes. A relação desses eventos com a terapia com ACTOS 30mg é desconhecida.
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de ACTOS. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, geralmente não é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
- Edema macular diabético de início recente ou agravamento com diminuição da acuidade visual [ver AVISOS E PRECAUÇÕES ].
- Insuficiência hepática fatal e não fatal [ver AVISOS E PRECAUÇÕES ].
Relatos pós-comercialização de insuficiência cardíaca congestiva foram relatados em pacientes tratados com ACTOS, com e sem doença cardíaca previamente conhecida e com e sem administração concomitante de insulina.
Na experiência pós-comercialização, houve relatos de aumentos de peso extraordinariamente rápidos e aumentos superiores aos geralmente observados em ensaios clínicos. Os pacientes que apresentam tais aumentos devem ser avaliados quanto ao acúmulo de líquido e eventos relacionados ao volume, como edema excessivo e insuficiência cardíaca congestiva [ver AVISO DE CAIXA e AVISOS E PRECAUÇÕES ].
INTERAÇÕES MEDICAMENTOSAS
Inibidores Fortes de CYP2C8
Um inibidor do CYP2C8 (por exemplo, gemfibrozil) aumenta significativamente a exposição (área sob a curva de concentração sérica-tempo ou AUC) e a meia-vida (t½) da pioglitazona. Portanto, a dose máxima recomendada de ACTOS é de 15 mg por dia se usado em combinação com gemfibrozil ou outros inibidores fortes de CYP2C8 [ver DOSAGEM E ADMINISTRAÇÃO e FARMACOLOGIA CLÍNICA ].
Indutores CYP2C8
Um indutor de CYP2C8 (por exemplo, rifampicina) pode diminuir significativamente a exposição (AUC) da pioglitazona. Portanto, se um indutor de CYP2C8 for iniciado ou interrompido durante o tratamento com ACTOS 30 mg, podem ser necessárias alterações no tratamento do diabetes com base na resposta clínica sem exceder a dose diária máxima recomendada de 45 mg para ACTOS [ver FARMACOLOGIA CLÍNICA ].
Topiramato
Uma diminuição na exposição da pioglitazona e seus metabólitos ativos foi observada com a administração concomitante de pioglitazona e topiramato [ver FARMACOLOGIA CLÍNICA ]. A relevância clínica desta diminuição é desconhecida; entretanto, quando ACTOS e topiramato são usados concomitantemente, monitore os pacientes quanto ao controle glicêmico adequado.
AVISOS
Incluído como parte do "PRECAUÇÕES" Seção
PRECAUÇÕES
Insuficiência Cardíaca Congestiva
ACTOS 15mg, como outras tiazolidinedionas, pode causar retenção de líquidos relacionada à dose quando usado sozinho ou em combinação com outros medicamentos antidiabéticos e é mais comum quando ACTOS 30mg é usado em combinação com insulina. A retenção de líquidos pode levar ou exacerbar a insuficiência cardíaca congestiva. Os pacientes devem ser observados quanto a sinais e sintomas de insuficiência cardíaca congestiva. Se ocorrer insuficiência cardíaca congestiva, ela deve ser tratada de acordo com os padrões atuais de tratamento e deve-se considerar a descontinuação ou redução da dose de ACTOS [ver AVISO DE CAIXA , CONTRA-INDICAÇÕES , e REAÇÕES ADVERSAS ].
Hipoglicemia
Pacientes recebendo ACTOS em combinação com insulina ou outros medicamentos antidiabéticos (particularmente secretagogos de insulina, como sulfonilureias) podem estar em risco de hipoglicemia. Uma redução na dose da medicação antidiabética concomitante pode ser necessária para reduzir o risco de hipoglicemia [ver DOSAGEM E ADMINISTRAÇÃO ].
Efeitos hepáticos
Houve relatos pós-comercialização de insuficiência hepática fatal e não fatal em pacientes tomando ACTOS 15mg, embora os relatos contenham informações insuficientes necessárias para estabelecer a causa provável. Não houve evidência de hepatotoxicidade induzida por drogas no banco de dados de ensaios clínicos controlados ACTOS 30mg até o momento [ver REAÇÕES ADVERSAS ].
Pacientes com diabetes tipo 2 podem ter doença hepática gordurosa ou doença cardíaca com insuficiência cardíaca congestiva episódica, ambas as quais podem causar anormalidades nos testes hepáticos, e também podem ter outras formas de doença hepática, muitas das quais podem ser tratadas ou controladas. Portanto, é recomendado obter um painel de teste hepático (alanina aminotransferase sérica [ALT], aspartato aminotransferase [AST], fosfatase alcalina e bilirrubina total) e avaliar o paciente antes de iniciar a terapia com ACTOS. Em pacientes com testes hepáticos anormais, ACTOS 15mg deve ser iniciado com cautela.
Meça os testes hepáticos imediatamente em pacientes que relatam sintomas que podem indicar lesão hepática, incluindo fadiga, anorexia, desconforto abdominal superior direito, urina escura ou icterícia. Neste contexto clínico, se o paciente apresentar testes hepáticos anormais (ALT maior que 3 vezes o limite superior do intervalo de referência), o tratamento com ACTOS 15mg deve ser interrompido e investigação feita para estabelecer a causa provável. ACTOS não deve ser reiniciado nesses pacientes sem outra explicação para as anormalidades nos testes hepáticos.
Pacientes com ALT sérica superior a três vezes o intervalo de referência com bilirrubina total sérica superior a duas vezes o intervalo de referência sem etiologias alternativas correm risco de lesão hepática grave induzida por drogas e não devem ser reiniciados com ACTOS. Para pacientes com elevações menores de ALT ou bilirrubina séricas e com uma causa provável alternativa, o tratamento com ACTOS pode ser usado com cautela.
Tumores da Bexiga Urinária
Foram observados tumores na bexiga urinária de ratos machos no estudo de carcinogenicidade de dois anos [ver Toxicologia não clínica ]. Além disso, durante o ensaio clínico PROactive de três anos, 14 pacientes de 2.605 (0,54%) randomizados para ACTOS 15mg e 5 de 2.633 (0,19%) randomizados para placebo foram diagnosticados com câncer de bexiga. Após excluir os pacientes em que a exposição ao medicamento do estudo foi inferior a um ano no momento do diagnóstico de câncer de bexiga, houve 6 (0,23%) casos em ACTOS 30mg e dois (0,08%) casos em placebo. Após a conclusão do estudo, um grande subconjunto de pacientes foi observado por até 10 anos adicionais, com pouca exposição adicional ao ACTOS. Durante os 13 anos de acompanhamento proativo e observacional, a ocorrência de câncer de bexiga não diferiu entre os pacientes randomizados para ACTOS 30mg ou placebo (HR = 1,00; [IC 95%: 0,59-1,72]).
Os achados sobre o risco de câncer de bexiga em pacientes expostos ao ACTOS variam entre os estudos observacionais; alguns não encontraram um risco aumentado de câncer de bexiga associado ao ACTOS 30mg, enquanto outros o fizeram.
Um grande estudo de coorte observacional prospectivo de 10 anos realizado nos Estados Unidos não encontrou aumento estatisticamente significativo no risco de câncer de bexiga em pacientes diabéticos já expostos a ACTOS, em comparação com aqueles nunca expostos a ACTOS (HR = 1,06 [IC 95% 0,89-1,26 ]).
Um estudo de coorte retrospectivo realizado com dados do Reino Unido encontrou uma associação estatisticamente significativa entre a exposição ao ACTOS e câncer de bexiga (HR: 1,63; [IC 95%: 1,22-2,19]).
Associações entre dose cumulativa ou duração cumulativa de exposição ao ACTOS 15mg e câncer de bexiga não foram detectadas em alguns estudos, incluindo o estudo observacional de 10 anos nos EUA, mas em outros. Achados inconsistentes e limitações inerentes a esses e outros estudos impedem interpretações conclusivas dos dados observacionais.
ACTOS pode estar associado a um aumento no risco de tumores da bexiga urinária. Não existem dados suficientes para determinar se a pioglitazona é um promotor tumoral para tumores da bexiga urinária.
Consequentemente, ACTOS não deve ser usado em pacientes com câncer de bexiga ativo e os benefícios do controle glicêmico versus riscos desconhecidos de recorrência do câncer com ACTOS devem ser considerados em pacientes com história prévia de câncer de bexiga.
Edema
Em ensaios clínicos controlados, o edema foi relatado com mais frequência em pacientes tratados com ACTOS 30mg do que em pacientes tratados com placebo e está relacionado à dose [ver REAÇÕES ADVERSAS ]. Na experiência pós-comercialização, foram recebidos relatos de novo aparecimento ou agravamento de edema.
ACTOS 15mg deve ser usado com cautela em pacientes com edema. Como as tiazolidinedionas, incluindo ACTOS, podem causar retenção de líquidos, o que pode exacerbar ou levar à insuficiência cardíaca congestiva, ACTOS 30mg deve ser usado com cautela em pacientes com risco de insuficiência cardíaca congestiva. Os pacientes tratados com ACTOS devem ser monitorados quanto a sinais e sintomas de insuficiência cardíaca congestiva. AVISO DE CAIXA , Insuficiência Cardíaca Congestiva e INFORMAÇÃO DO PACIENTE ].
Fraturas
No PROactive (o Prospective Pioglitazone Clinical Trial in Macrovascular Events), 5.238 pacientes com diabetes tipo 2 e histórico de doença macrovascular foram randomizados para ACTOS (N = 2.605), titulado com força até 45 mg por dia ou placebo (N = 2.633) além do padrão de atendimento. Durante um seguimento médio de 34,5 meses, a incidência de fratura óssea em mulheres foi de 5,1% (44/870) para ACTOS 30mg versus 2,5% (23/905) para placebo. Essa diferença foi notada após o primeiro ano de tratamento e persistiu durante o curso do estudo. A maioria das fraturas observadas em pacientes do sexo feminino foram fraturas não vertebrais, incluindo membros inferiores e membros superiores distais. Nenhum aumento na incidência de fratura foi observado em homens tratados com ACTOS (1,7%) versus placebo (2,1%). O risco de fratura deve ser considerado no atendimento de pacientes, especialmente pacientes do sexo feminino, tratados com ACTOS e atenção deve ser dada à avaliação e manutenção da saúde óssea de acordo com os padrões atuais de atendimento.
Edema macular
Edema macular foi relatado na experiência pós-comercialização em pacientes diabéticos que estavam tomando ACTOS ou outra tiazolidinediona. Alguns pacientes apresentaram visão turva ou diminuição da acuidade visual, mas outros foram diagnosticados no exame oftalmológico de rotina.
A maioria dos pacientes apresentava edema periférico no momento em que o edema macular foi diagnosticado. Alguns pacientes tiveram melhora do edema macular após a descontinuação da tiazolidinediona.
Pacientes com diabetes devem fazer exames oftalmológicos regulares por um oftalmologista de acordo com os padrões atuais de atendimento. Pacientes com diabetes que relatam quaisquer sintomas visuais devem ser encaminhados imediatamente a um oftalmologista, independentemente dos medicamentos subjacentes do paciente ou de outros achados físicos [ver REAÇÕES ADVERSAS ].
Resultados Macrovasculares
Não houve estudos clínicos estabelecendo evidências conclusivas de redução do risco macrovascular com ACTOS.
Informações de Aconselhamento do Paciente
Consulte Rotulagem de Paciente Aprovada pela FDA ( INFORMAÇÃO DO PACIENTE ).
- É importante instruir os pacientes a seguirem as instruções dietéticas e fazerem exames regulares de glicose no sangue e hemoglobina glicosilada. Durante períodos de estresse, como febre, trauma, infecção ou cirurgia, os requisitos de medicação podem mudar e os pacientes devem ser lembrados de procurar aconselhamento médico imediatamente.
- Pacientes que experimentam um aumento de peso ou edema incomumente rápido ou que desenvolvem falta de ar ou outros sintomas de insuficiência cardíaca durante o tratamento com ACTOS devem relatar imediatamente esses sintomas a um médico.
- Diga aos pacientes que parem imediatamente de tomar ACTOS e procurem aconselhamento médico imediato se houver náuseas, vômitos, dor abdominal inexplicável, fadiga, anorexia ou urina escura, pois esses sintomas podem ser devidos à hepatotoxicidade.
- Diga aos pacientes para relatar imediatamente qualquer sinal de hematúria macroscópica ou outros sintomas, como disúria ou urgência urinária, que se desenvolvam ou aumentem durante o tratamento, pois podem ser decorrentes de câncer de bexiga.
- Diga aos pacientes para tomarem ACTOS 15mg uma vez ao dia. ACTOS 15mg pode ser tomado com ou sem refeições. Se uma dose for esquecida em um dia, a dose não deve ser dobrada no dia seguinte.
- Ao utilizar a terapia combinada com insulina ou outros medicamentos antidiabéticos, os riscos de hipoglicemia, seus sintomas e tratamento e as condições que predispõem ao seu desenvolvimento devem ser explicados ao paciente e seus familiares.
- Informe as pacientes do sexo feminino que o tratamento com ACTOS 30mg, como outras tiazolidinedionas, pode resultar em uma gravidez indesejada em algumas mulheres anovulatórias na pré-menopausa devido ao seu efeito sobre a ovulação [ver Uso em populações específicas ].
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Um estudo de carcinogenicidade de dois anos foi realizado em ratos machos e fêmeas em doses orais de até 63 mg/kg (aproximadamente 14 vezes a dose oral máxima recomendada para humanos de 45 mg com base em mg/m2). Tumores induzidos por drogas não foram observados em nenhum órgão, exceto na bexiga urinária de ratos machos. Neoplasias de células de transição benignas e/ou malignas foram observadas em ratos machos em doses de 4 mg/kg/dia e acima (aproximadamente igual à dose oral humana máxima recomendada com base em mg/m2). Cálculos urinários com subsequente irritação e hiperplasia foram postulados como o mecanismo para tumores de bexiga observados em ratos machos. Um estudo mecanístico de dois anos em ratos machos utilizando a acidificação da dieta para reduzir a formação de cálculos foi concluído em 2009. A acidificação da dieta diminuiu, mas não aboliu as alterações hiperplásicas na bexiga. A presença de cálculos exacerbou a resposta hiperplásica à pioglitazona, mas não foi considerada a causa primária das alterações hiperplásicas.
relevância para os humanos dos achados da bexiga no rato macho não pode ser excluída.
Um estudo de carcinogenicidade de dois anos também foi realizado em camundongos machos e fêmeas em doses orais de até 100 mg/kg/dia (aproximadamente 11 vezes a dose oral humana máxima recomendada com base em mg/m2). Não foram observados tumores induzidos por drogas em nenhum órgão.
O cloridrato de pioglitazona não foi mutagênico em uma bateria de estudos de toxicologia genética, incluindo o ensaio bacteriano Ames, um ensaio de mutação genética de células de mamíferos (CHO/HPRT e AS52/XPRT), um ensaio citogenético in vitro usando células CHL, um ensaio de síntese de DNA não programado , e um ensaio de micronúcleo in vivo.
Não foram observados efeitos adversos sobre a fertilidade em ratos machos e fêmeas em doses orais de até 40 mg/kg de cloridrato de pioglitazona diariamente antes e durante o acasalamento e gestação (aproximadamente nove vezes a dose oral humana máxima recomendada com base em mg/m2).
Uso em populações específicas
Gravidez
Resumo do risco
Dados limitados com ACTOS em mulheres grávidas não são suficientes para determinar um risco associado ao medicamento para defeitos congênitos graves ou aborto espontâneo. Existem riscos para a mãe e o feto associados ao diabetes mal controlado na gravidez [ver Considerações Clínicas ].
Em estudos de reprodução em animais, não foram observados efeitos adversos no desenvolvimento quando a pioglitazona foi administrada a ratas e coelhas grávidas durante a organogênese em exposições de até 5 e 35 vezes a dose clínica de 45 mg, respectivamente, com base na área de superfície corporal [ver Dados ].
O risco de fundo estimado de grandes defeitos congênitos é de 6-10% em mulheres com diabetes pré-gestacional com HbA1c >7 e foi relatado como sendo tão alto quanto 20-25% em mulheres com HbA1c >10. O risco de fundo estimado de aborto para a população indicada é desconhecido. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e aborto espontâneo em gestações clinicamente reconhecidas é de 2-4% e 15-20%, respectivamente.
Considerações Clínicas
Risco materno e/ou embrionário/fetal associado à doença
O diabetes mal controlado na gravidez aumenta o risco materno de cetoacidose diabética, pré-eclâmpsia, abortos espontâneos, parto prematuro, natimorto e complicações no parto. O diabetes mal controlado aumenta o risco fetal de grandes defeitos congênitos, natimortos e morbidade relacionada à macrossomia.
Dados
Dados de animais
pioglitazona administrada a ratas grávidas durante a organogênese não causou efeitos adversos no desenvolvimento na dose de 20 mg/kg (~ 5 vezes a dose clínica de 45 mg), mas atrasou o parto e reduziu a viabilidade embriofetal em 40 e 80 mg/kg, ou ≥ 9 vezes a dose clínica de 45 mg, por área de superfície corporal. Em coelhas grávidas administradas com pioglitazona durante a organogênese, nenhum efeito adverso no desenvolvimento foi observado com 80 mg/kg (~35 vezes a dose clínica de 45 mg), mas reduziu a viabilidade embriofetal em 160 mg/kg, ou ~69 vezes a dose clínica de 45 mg dose, por área de superfície corporal. Quando ratas grávidas receberam pioglitazona durante o final da gestação e lactação, ocorreu atraso no desenvolvimento pós-natal, atribuído à diminuição do peso corporal, na prole em doses maternas de 10 mg/kg e acima ou ≥ 2 vezes a dose clínica de 45 mg, por área de superfície corporal.
Lactação
Resumo do risco
Não há informações sobre a presença de pioglitazona no leite humano, os efeitos no lactente ou os efeitos na produção de leite. A pioglitazona está presente no leite de rato; no entanto, devido a diferenças específicas da espécie na fisiologia da lactação, os dados em animais podem não prever de forma confiável os níveis da droga no leite humano. Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de ACTOS 15mg e quaisquer potenciais efeitos adversos no lactente com ACTOS 30mg ou da condição materna subjacente.
Fêmeas e Machos com Potencial Reprodutivo
Discuta o potencial de gravidez indesejada com mulheres na pré-menopausa, pois a terapia com ACTOS, como outras tiazolidinedionas, pode resultar em ovulação em algumas mulheres anovulatórias.
Uso Pediátrico
A segurança e a eficácia de ACTOS em pacientes pediátricos não foram estabelecidas.
ACTOS 15mg não é recomendado para uso em pacientes pediátricos com base nos efeitos adversos observados em adultos, incluindo retenção de líquidos e insuficiência cardíaca congestiva, fraturas e tumores da bexiga [ver AVISOS E PRECAUÇÕES ].
Uso Geriátrico
Um total de 92 pacientes (15,2%) tratados com ACTOS nos três estudos duplo-cegos, controlados por placebo, em monoterapia de 16 a 26 semanas agrupados tinham ≥65 anos de idade e dois pacientes (0,3%) tinham ≥75 anos de idade. Nos dois estudos combinados de 16 a 24 semanas com adição de sulfonilureia, 201 pacientes (18,7%) tratados com ACTOS 30mg tinham ≥65 anos e 19 (1,8%) tinham ≥75 anos. Nos dois estudos combinados de 16 a 24 semanas de adição à metformina, 155 pacientes (15,5%) tratados com ACTOS tinham ≥65 anos e 19 (1,9%) tinham ≥75 anos. Nos dois ensaios de adição de insulina de 16 a 24 semanas agrupados, 272 pacientes (25,4%) tratados com ACTOS tinham ≥65 anos e 22 (2,1%) tinham ≥75 anos.
No PROactive, 1.068 pacientes (41,0%) tratados com ACTOS tinham ≥65 anos e 42 (1,6%) tinham ≥75 anos.
Em estudos farmacocinéticos com pioglitazona, não foram observadas diferenças significativas nos parâmetros farmacocinéticos entre pacientes idosos e mais jovens [ver FARMACOLOGIA CLÍNICA ].
Embora as experiências clínicas não tenham identificado diferenças na eficácia e segurança entre pacientes idosos (≥65 anos) e pacientes mais jovens, essas conclusões são limitadas pelo pequeno tamanho da amostra para pacientes com idade ≥75 anos.
SOBREDOSAGEM
Durante os ensaios clínicos controlados, foi relatado um caso de superdosagem com ACTOS 30mg. Um paciente do sexo masculino tomou 120 mg por dia durante quatro dias, depois 180 mg por dia durante sete dias. A paciente negou quaisquer sintomas clínicos durante este período.
Em caso de superdosagem, o tratamento de suporte apropriado deve ser iniciado de acordo com os sinais e sintomas clínicos do paciente.
CONTRA-INDICAÇÕES
- Iniciação em pacientes com insuficiência cardíaca Classe III ou IV da NYHA estabelecida [ver AVISO DE CAIXA ].
- Uso em pacientes com hipersensibilidade conhecida à pioglitazona ou a qualquer outro componente de ACTOS.
FARMACOLOGIA CLÍNICA
Mecanismo de ação
ACTOS 15mg é uma tiazolidinediona que depende da presença de insulina para seu mecanismo de ação. ACTOS diminui a resistência à insulina na periferia e no fígado, resultando em maior eliminação de glicose dependente de insulina e diminuição da produção hepática de glicose. A pioglitazona não é um secretagogo de insulina. A pioglitazona é um agonista do receptor gama ativado pelo proliferador de peroxissoma (PPAR?). Os receptores PPAR são encontrados em tecidos importantes para a ação da insulina, como tecido adiposo, músculo esquelético e fígado. Ativação do PPAR? os receptores nucleares modulam a transcrição de vários genes responsivos à insulina envolvidos no controle do metabolismo da glicose e lipídios.
Em modelos animais de diabetes, a pioglitazona reduz a hiperglicemia, hiperinsulinemia e hipertrigliceridemia características de estados resistentes à insulina, como diabetes tipo 2. As alterações metabólicas produzidas pela pioglitazona resultam em aumento da capacidade de resposta dos tecidos dependentes de insulina e são observadas em vários modelos animais de resistência à insulina.
Como a pioglitazona aumenta os efeitos da insulina circulante (diminuindo a resistência à insulina), ela não reduz a glicose no sangue em modelos animais que não possuem insulina endógena.
Farmacodinâmica
Estudos clínicos demonstram que ACTOS 15mg melhora a sensibilidade à insulina em pacientes resistentes à insulina. ACTOS aumenta a resposta celular à insulina, aumenta a eliminação de glicose dependente de insulina e melhora a sensibilidade hepática à insulina. Em pacientes com diabetes tipo 2, a diminuição da resistência à insulina produzida pelo ACTOS resulta em concentrações mais baixas de glicose no plasma, concentrações mais baixas de insulina no plasma e valores mais baixos de HbA1c. Em ensaios clínicos controlados, ACTOS teve um efeito aditivo no controle glicêmico quando usado em combinação com uma sulfonilureia, metformina ou insulina [ver Estudos clínicos ].
Pacientes com anormalidades lipídicas foram incluídos em ensaios clínicos com ACTOS. No geral, os pacientes tratados com ACTOS 15mg apresentaram reduções médias nos triglicerídeos séricos, aumentos médios no colesterol HDL e nenhuma alteração média consistente no LDL e no colesterol total. Não há evidência conclusiva de benefício macrovascular com ACTOS [ver AVISOS E PRECAUÇÕES e REAÇÕES ADVERSAS ].
Em um estudo de monoterapia de 26 semanas, controlado por placebo e variando de dose, os triglicerídeos séricos médios diminuíram nos grupos de dose de 15 mg, 30 mg e 45 mg de ACTOS 15 mg em comparação com um aumento médio no grupo placebo. O colesterol HDL médio aumentou em maior extensão nos pacientes tratados com ACTOS 30mg do que nos pacientes tratados com placebo. Não houve diferenças consistentes para LDL e colesterol total em pacientes tratados com ACTOS em comparação com placebo (ver Tabela 14).
Nos outros dois estudos de monoterapia (16 semanas e 24 semanas) e nos estudos de terapia combinada com sulfonilureia (16 semanas e 24 semanas), metformina (16 semanas e 24 semanas) ou insulina (16 semanas e 24 semanas), os resultados foram geralmente consistente com os dados acima.
Farmacocinética
Após a administração de ACTOS 15mg uma vez ao dia, as concentrações séricas em estado de equilíbrio da pioglitazona e de seus principais metabólitos ativos, M-III (cetoderivado da pioglitazona) e M-IV (derivado hidroxila da pioglitazona), são alcançadas em sete dias. No estado de equilíbrio, M-III e M-IV atingem concentrações séricas iguais ou superiores às da pioglitazona. No estado de equilíbrio, tanto em voluntários saudáveis quanto em pacientes com diabetes tipo 2, a pioglitazona compreende aproximadamente 30% a 50% do pico das concentrações séricas totais de pioglitazona (pioglitazona mais metabólitos ativos) e 20% a 25% da AUC total.
Cmax, AUC e concentrações séricas mínimas (Cmin) para pioglitazona e M-III e M-IV aumentaram proporcionalmente com doses administradas de 15 mg e 30 mg por dia.
Absorção
Após a administração oral de pioglitazona, o Tmax da pioglitazona foi de duas horas. Os alimentos atrasam o Tmax para três a quatro horas, mas não alteram a extensão da absorção (AUC).
Distribuição
volume médio aparente de distribuição (Vd/F) da pioglitazona após administração de dose única é de 0,63 ± 0,41 (média ± SD) L/kg de peso corporal. A pioglitazona liga-se extensivamente às proteínas (>99%) no soro humano, principalmente à albumina sérica. A pioglitazona também se liga a outras proteínas séricas, mas com menor afinidade. M-III e M-IV também estão extensivamente ligados (>98%) à albumina sérica.
Metabolismo
A pioglitazona é extensivamente metabolizada por hidroxilação e oxidação; os metabólitos também se convertem parcialmente em conjugados de glicuronídeo ou sulfato. Os metabólitos M-III e M-IV são os principais metabólitos ativos circulantes em humanos.
Dados in vitro demonstram que múltiplas isoformas de CYP estão envolvidas no metabolismo da pioglitazona, que incluem CYP2C8 e, em menor grau, CYP3A4 com contribuições adicionais de uma variedade de outras isoformas, incluindo principalmente a CYP1A1 extra-hepática. O estudo in vivo de pioglitazona em combinação com gemfibrozil, um forte inibidor do CYP2C8, mostrou que a pioglitazona é um substrato do CYP2C8 [ver DOSAGEM E ADMINISTRAÇÃO e INTERAÇÕES MEDICAMENTOSAS ]. As proporções urinárias de 6β-hidroxicortisol/cortisol medidas em pacientes tratados com ACTOS 30mg mostraram que a pioglitazona não é um forte indutor da enzima CYP3A4.
Excreção e eliminação
Após administração oral, aproximadamente 15% a 30% da dose de pioglitazona é recuperada na urina. A eliminação renal da pioglitazona é insignificante, e a droga é excretada principalmente como metabólitos e seus conjugados. Presume-se que a maior parte da dose oral seja excretada na bile inalterada ou como metabólitos e eliminada nas fezes.
meia-vida sérica média (t1/2) da pioglitazona e seus metabólitos (M-III e M-IV) variam de três a sete horas e 16 a 24 horas, respectivamente. A pioglitazona tem uma depuração aparente, CL/F, calculada em cinco a sete L/h.
Insuficiência renal
A meia-vida de eliminação sérica da pioglitazona, M-III e M-IV permanece inalterada em pacientes com insuficiência renal moderada (clearance de creatinina [CLcr] 30 a 50 mL/min) e grave (CLcr
Insuficiência hepática
Em comparação com controles saudáveis, indivíduos com função hepática prejudicada (Child-Turcotte-Pugh Grau B/C) têm uma redução de aproximadamente 45% na pioglitazona e pioglitazona total (pioglitazona, M-III e M-IV) Cmax média, mas nenhuma alteração na os valores médios de AUC. Portanto, não é necessário ajuste de dose em pacientes com insuficiência hepática.
Existem relatos pós-comercialização de insuficiência hepática com ACTOS e os ensaios clínicos geralmente excluíram pacientes com ALT sérica >2,5 vezes o limite superior do intervalo de referência. Tenha cuidado em pacientes com doença hepática [ver AVISOS E PRECAUÇÕES ].
Pacientes Geriátricos
Em indivíduos idosos saudáveis, a Cmax da pioglitazona não foi significativamente diferente, mas os valores de AUC foram aproximadamente 21% superiores aos alcançados em indivíduos mais jovens. O t1/2 médio da pioglitazona também foi prolongado em indivíduos idosos (cerca de dez horas) em comparação com indivíduos mais jovens (cerca de sete horas). Essas alterações não foram de uma magnitude que seria considerada clinicamente relevante.
Pacientes pediátricos
A segurança e eficácia da pioglitazona em pacientes pediátricos não foram estabelecidas. ACTOS 15mg não é recomendado para uso em pacientes pediátricos [ver Uso em populações específicas ].
Gênero
Os valores médios de Cmax e AUC da pioglitazona aumentaram 20% a 60% nas mulheres em comparação com os homens. Em ensaios clínicos controlados, as diminuições de HbA1c desde o início foram geralmente maiores para as mulheres do que para os homens (diferença média na HbA1c de 0,5%). Como a terapia deve ser individualizada para cada paciente para alcançar o controle glicêmico, nenhum ajuste de dose é recomendado com base apenas no sexo.
Etnia
Dados farmacocinéticos entre vários grupos étnicos não estão disponíveis.
Interações Medicamentosas
Toxicologia e/ou Farmacologia Animal
Aumento do coração foi observado em camundongos (100 mg/kg), ratos (4 mg/kg e acima) e cães (3 mg/kg) tratados oralmente com cloridrato de pioglitazona (aproximadamente 11, 1 e 2 vezes o máximo recomendado para humanos oral dose para camundongos, ratos e cães, respectivamente, com base em mg/m2). Em um estudo de um ano em ratos, a morte precoce relacionada ao medicamento devido a aparente disfunção cardíaca ocorreu com uma dose oral de 160 mg/kg/dia (aproximadamente 35 vezes a dose oral humana máxima recomendada com base em mg/m2). Aumento do coração foi observado em um estudo de 13 semanas em macacos em doses orais de 8,9 mg/kg e acima (aproximadamente quatro vezes a dose oral humana máxima recomendada com base em mg/m2), mas não em um estudo de 52 semanas em doses orais até 32 mg/kg (aproximadamente 13 vezes a dose oral humana máxima recomendada com base em mg/m2).
Estudos clínicos
Monoterapia
Três estudos randomizados, duplo-cegos e controlados por placebo com duração de 16 a 26 semanas foram conduzidos para avaliar o uso de ACTOS como monoterapia em pacientes com diabetes tipo 2. Esses estudos examinaram ACTOS 15mg em doses de até 45mg ou placebo uma vez ao dia em um total de 865 pacientes.
Em um estudo de monoterapia de variação de dose de 26 semanas, 408 pacientes com diabetes tipo 2 foram randomizados para receber 7,5 mg, 15 mg, 30 mg ou 45 mg de ACTOS ou placebo uma vez ao dia. A terapia com qualquer agente antidiabético anterior foi descontinuada oito semanas antes do período duplo-cego. O tratamento com 15 mg, 30 mg e 45 mg de ACTOS 30 mg produziu melhorias estatisticamente significativas na HbA1c e na glicemia de jejum (FPG) no ponto final em comparação com placebo (ver Figura 1, Tabela 17).
A Figura 1 mostra o curso de tempo para mudanças na HbA1c neste estudo de 26 semanas.
Figura 1. Mudança média da linha de base para HbA1c em um estudo de variação de dose controlado por placebo de 26 semanas (valores observados)
Em um estudo de monoterapia controlado por placebo de 24 semanas, 260 pacientes com diabetes tipo 2 foram randomizados para um dos dois grupos de tratamento com titulação forçada ACTOS ou um grupo placebo de titulação simulada. A terapia com qualquer agente antidiabético anterior foi descontinuada seis semanas antes do período duplo-cego. Em um grupo de tratamento com ACTOS 15mg, os pacientes receberam uma dose inicial de 7,5mg uma vez ao dia. Após quatro semanas, a dose foi aumentada para 15 mg uma vez ao dia e após outras quatro semanas, a dose foi aumentada para 30 mg uma vez ao dia pelo restante do estudo (16 semanas). No segundo grupo de tratamento com ACTOS, os pacientes receberam uma dose inicial de 15 mg uma vez ao dia e foram titulados para 30 mg uma vez ao dia e 45 mg uma vez ao dia de maneira semelhante. O tratamento com ACTOS 15mg, conforme descrito, produziu melhorias estatisticamente significativas em HbA1c e FPG no ponto final em comparação com placebo (ver Tabela 18).
Em um estudo de monoterapia de 16 semanas, 197 pacientes com diabetes tipo 2 foram randomizados para tratamento com 30 mg de ACTOS ou placebo uma vez ao dia. A terapia com qualquer agente antidiabético anterior foi descontinuada seis semanas antes do período duplo-cego. O tratamento com 30 mg de ACTOS produziu melhorias estatisticamente significativas em HbA1c e FPG no ponto final em comparação com placebo (ver Tabela 19).
Terapia combinada
Três ensaios clínicos de 16 semanas, randomizados, duplo-cegos e controlados por placebo foram conduzidos para avaliar os efeitos de ACTOS (15 mg e/ou 30 mg) no controle glicêmico em pacientes com diabetes tipo 2 que foram inadequadamente controlados (HbA1c ≥8 %) apesar da terapia atual com uma sulfonilureia, metformina ou insulina. Além disso, três ensaios clínicos randomizados e duplo-cegos de 24 semanas foram conduzidos para avaliar os efeitos de ACTOS 30 mg vs. ACTOS 45 mg no controle glicêmico em pacientes com diabetes tipo 2 que foram inadequadamente controlados (HbA1c ≥8%) apesar da atual terapia com uma sulfonilureia, metformina ou insulina. O tratamento anterior do diabetes pode ter sido monoterapia ou terapia combinada.
Add-On aos Ensaios de Sulfonilureia
Dois ensaios clínicos foram conduzidos com ACTOS em combinação com uma sulfonilureia. Ambos os estudos incluíram pacientes com diabetes tipo 2 em qualquer dose de sulfonilureia, isoladamente ou em combinação com outro agente antidiabético. Todos os outros agentes antidiabéticos foram retirados pelo menos três semanas antes do início do tratamento do estudo.
No primeiro estudo, 560 pacientes foram randomizados para receber 15 mg ou 30 mg de ACTOS 30 mg ou placebo uma vez ao dia por 16 semanas, além do regime de sulfonilureia atual. O tratamento com ACTOS como adjuvante à sulfonilureia produziu melhorias estatisticamente significativas na HbA1c e FPG no ponto final em comparação com o adjuvante placebo à sulfonilureia (ver Tabela 20).
No segundo estudo, 702 pacientes foram randomizados para receber 30 mg ou 45 mg de ACTOS uma vez ao dia por 24 semanas, além do regime de sulfonilureia atual. A redução média da linha de base na Semana 24 na HbA1c foi de 1,6% para a dose de 30 mg e 1,7% para a dose de 45 mg (ver Tabela 21). A redução média da linha de base na Semana 24 na GJ foi de 52 mg/dL para a dose de 30 mg e 56 mg/dL para a dose de 45 mg.
O efeito terapêutico de ACTOS em combinação com sulfonilureia foi observado em pacientes independentemente da dose de sulfonilureia.
Complemento para testes de metformina
Dois ensaios clínicos foram conduzidos com ACTOS 30mg em combinação com metformina. Ambos os ensaios incluíram pacientes com diabetes tipo 2 em qualquer dose de metformina, isoladamente ou em combinação com outro agente antidiabético. Todos os outros agentes antidiabéticos foram retirados pelo menos três semanas antes do início do tratamento do estudo.
No primeiro estudo, 328 pacientes foram randomizados para receber 30 mg de ACTOS ou placebo uma vez ao dia por 16 semanas, além do regime atual de metformina. O tratamento com ACTOS 30mg como adjuvante à metformina produziu melhorias estatisticamente significativas na HbA1c e FPG no desfecho em comparação com o adjuvante placebo à metformina (ver Tabela 22).
No segundo estudo, 827 pacientes foram randomizados para receber 30 mg ou 45 mg de ACTOS 30 mg uma vez ao dia por 24 semanas, além do regime de metformina atual. A redução média da linha de base na Semana 24 na HbA1c foi de 0,8% para a dose de 30 mg e 1,0% para a dose de 45 mg (ver Tabela 23). A redução média da linha de base na Semana 24 na GJ foi de 38 mg/dL para a dose de 30 mg e 51 mg/dL para a dose de 45 mg.
O efeito terapêutico de ACTOS em combinação com metformina foi observado em pacientes independentemente da dose de metformina.
Complemento para testes de insulina
Dois ensaios clínicos foram conduzidos com ACTOS 15mg em combinação com insulina. Ambos os ensaios incluíram pacientes com diabetes tipo 2 em uso de insulina, isoladamente ou em combinação com outro agente antidiabético. Todos os outros agentes antidiabéticos foram retirados antes do início do tratamento do estudo. No primeiro estudo, 566 pacientes foram randomizados para receber 15 mg ou 30 mg de ACTOS 15 mg ou placebo uma vez ao dia por 16 semanas, além do regime de insulina. O tratamento com ACTOS 30mg como complemento da insulina produziu melhorias estatisticamente significativas na HbA1c e FPG no ponto final em comparação com o placebo como complemento da insulina (consulte a Tabela 24). A dose média diária de insulina na linha de base em cada grupo de tratamento foi de aproximadamente 70 unidades. A maioria dos pacientes (75% em geral, 86% tratados com placebo, 77% tratados com ACTOS 15 mg e 61% tratados com ACTOS 30 mg) não tiveram alteração em sua dose diária de insulina desde o início até a visita final do estudo. A alteração média da linha de base na dose diária de insulina (incluindo pacientes sem modificações na dose de insulina) foi de -3 unidades nos pacientes tratados com ACTOS 15 mg, -8 unidades nos pacientes tratados com ACTOS 30 mg e -1 unidade nos pacientes tratados com placebo.
No segundo estudo, 690 pacientes que receberam uma mediana de 60 unidades por dia de insulina foram randomizados para receber 30 mg ou 45 mg de ACTOS uma vez ao dia por 24 semanas, além de seu regime de insulina atual. A redução média da linha de base na Semana 24 na HbA1c foi de 1,2% para a dose de 30 mg e 1,5% para a dose de 45 mg. A redução média da linha de base na Semana 24 na GJ foi de 32 mg/dL para a dose de 30 mg e 46 mg/dL para a dose de 45 mg (ver Tabela 25). A dose média diária de insulina na linha de base em ambos os grupos de tratamento foi de aproximadamente 70 unidades. A maioria dos pacientes (55% em geral, 58% tratados com ACTOS 30 mg e 52% tratados com ACTOS 45 mg) não tiveram alteração em sua dose diária de insulina desde o início até a visita final do estudo. A alteração média da linha de base na dose diária de insulina (incluindo pacientes sem modificações na dose de insulina) foi de -5 unidades nos pacientes tratados com ACTOS 30 mg e -8 unidades nos pacientes tratados com ACTOS 45 mg.
efeito terapêutico de ACTOS em combinação com insulina foi observado em pacientes independentemente da dose de insulina.
INFORMAÇÃO DO PACIENTE
ATOS (ak-TOS) (pioglitazona) Comprimidos
Leia atentamente este Guia de Medicação antes de começar a tomar ACTOS 15mg e sempre que receber uma recarga. Pode haver novas informações. Esta informação não substitui a conversa com seu médico sobre sua condição médica ou seu tratamento. Se você tiver alguma dúvida sobre ACTOS, pergunte ao seu médico ou farmacêutico.
Qual é a informação mais importante que devo saber sobre ACTOS?
ACTOS pode causar efeitos colaterais graves, incluindo insuficiência cardíaca nova ou pior.
- ACTOS 15mg pode fazer com que seu corpo mantenha líquido extra (retenção de líquidos), o que leva ao inchaço (edema) e ganho de peso. O excesso de fluido corporal pode piorar alguns problemas cardíacos ou levar à insuficiência cardíaca. Insuficiência cardíaca significa que seu coração não bombeia sangue o suficiente
- Não tome ACTOS se tiver insuficiência cardíaca grave
- Se você tiver insuficiência cardíaca com sintomas (como falta de ar ou inchaço), mesmo que esses sintomas não sejam graves, ACTOS pode não ser adequado para você
Ligue para o seu médico imediatamente se tiver algum dos seguintes:
- inchaço ou retenção de líquidos, especialmente nos tornozelos ou pernas
- falta de ar ou dificuldade para respirar, especialmente quando você se deita
- um aumento incomumente rápido no peso
- cansaço incomum
ACTOS pode ter outros efeitos colaterais graves. Consulte “Quais são os possíveis efeitos colaterais do ACTOS?”
O que é ACTOS?
ACTOS 15mg é um medicamento de prescrição usado com dieta e exercício para melhorar o controle de açúcar no sangue (glicose) em adultos com diabetes tipo 2. ACTOS é um medicamento para diabetes chamado pioglitazona que pode ser tomado sozinho ou com outros medicamentos para diabetes.
Não se sabe se ACTOS é seguro e eficaz em crianças menores de 18 anos. ACTOS não é recomendado para uso em crianças.
ACTOS não é para pessoas com diabetes tipo 1.
ACTOS 30mg não é para pessoas com cetoacidose diabética (aumento de cetonas no sangue ou na urina).
Quem não deve tomar ACTOS?
Consulte “Quais são as informações mais importantes que devo saber sobre ACTOS 15mg?”
Não tome ACTOS 15mg se você:
- tem insuficiência cardíaca grave
- são alérgicos a qualquer um dos ingredientes de ACTOS. Consulte o final deste Guia de Medicação para obter uma lista completa de ingredientes em ACTOS
Fale com o seu médico antes de tomar ACTOS se tiver uma destas condições.
O que devo dizer ao meu médico antes de tomar ACTOS 30mg?
Antes de tomar ACTOS, informe o seu médico se:
- tem insuficiência cardíaca
- tem diabetes tipo 1 (“juvenil”) ou teve cetoacidose diabética
- tem um tipo de doença ocular diabética que causa inchaço na parte de trás do olho (edema macular)
- tem problemas de fígado
- tem ou teve câncer de bexiga
- estão grávidas ou planejam engravidar. Não se sabe se ACTOS 15mg pode prejudicar o feto. Converse com seu médico se estiver grávida ou planeja engravidar sobre a melhor maneira de controlar seus níveis de glicose no sangue durante a gravidez
- é uma mulher na pré-menopausa (antes da “mudança de vida”) que não menstrua regularmente ou não menstrua. ACTOS 30mg pode aumentar sua chance de engravidar. Converse com seu médico sobre as opções de controle de natalidade enquanto estiver tomando ACTOS. Informe o seu médico imediatamente se engravidar enquanto estiver a tomar ACTOS
- está amamentando ou planeja amamentar. Não se sabe se ACTOS passa para o seu leite e se pode prejudicar o seu bebé. Converse com seu médico sobre a melhor maneira de controlar seus níveis de glicose no sangue durante a amamentação
Informe o seu médico sobre todos os medicamentos que toma incluindo prescrição e medicamentos de balcão, vitaminas e suplementos de ervas.
ACTOS 30mg e alguns de seus outros medicamentos podem afetar um ao outro. Você pode precisar alterar sua dose de ACTOS 15mg ou alguns outros medicamentos.
Conheça os medicamentos que você toma. Mantenha uma lista dos seus medicamentos e mostre-a ao seu médico e farmacêutico antes de iniciar um novo medicamento. Eles lhe dirão se não há problema em tomar ACTOS 15mg com outros medicamentos.
Como devo tomar ACTOS 15mg?
- Tome ACTOS 15mg exatamente como seu médico lhe disse para tomá-lo
- O seu médico pode alterar a sua dose de ACTOS. Não altere sua dose de ACTOS a menos que seu médico lhe diga para
- ACTOS pode ser prescrito sozinho ou com outros medicamentos para diabetes. Isso dependerá de quão bem o seu açúcar no sangue é controlado
- Tome ACTOS 15mg uma vez por dia, com ou sem alimentos
- Se você perder uma dose de ACTOS 15mg, tome sua próxima dose conforme prescrito, a menos que seu médico lhe diga de forma diferente. Não tome duas doses de uma só vez no dia seguinte
- Se você tomar muito ACTOS, ligue para o seu médico ou dirija-se ao pronto-socorro do hospital mais próximo imediatamente
- Se o seu corpo estiver sob estresse, como febre, infecção, acidente ou cirurgia, a dose de seus medicamentos para diabetes pode precisar ser alterada. Ligue para o seu médico imediatamente
- Mantenha-se em sua dieta e programas de exercícios e teste seu açúcar no sangue regularmente enquanto estiver tomando ACTOS
- Seu médico deve fazer alguns exames de sangue antes de você começar e enquanto estiver tomando ACTOS
- Seu médico também deve fazer o teste de hemoglobina A1C para verificar quão bem o açúcar no sangue é controlado com ACTOS
- O seu médico deve verificar os seus olhos regularmente enquanto estiver a tomar ACTOS
Quais são os possíveis efeitos colaterais do ACTOS?
ACTOS pode causar efeitos colaterais graves, incluindo:
- Consulte “Quais são as informações mais importantes que devo saber sobre o ACTOS?”
- baixo nível de açúcar no sangue (hipoglicemia). Isso pode acontecer se você pular refeições, se você também usar outro medicamento que reduz o açúcar no sangue ou se tiver certos problemas médicos. Tonturas, tonturas, tremores ou fome podem acontecer se o açúcar no sangue estiver muito baixo. Ligue para o seu médico se os níveis baixos de açúcar no sangue forem um problema para você
- problemas de fígado. Ligue para o seu médico imediatamente se você tiver:
- náusea ou vômito
- dor de estômago
- cansaço incomum ou inexplicável
- perda de apetite
- urina escura
- amarelecimento da pele ou do branco dos olhos
- Câncer de bexiga. Pode haver uma chance maior de ter câncer de bexiga quando você toma ACTOS. Você não deve tomar ACTOS 15mg se estiver recebendo tratamento para câncer de bexiga. Informe o seu médico imediatamente se tiver algum dos seguintes sintomas de câncer de bexiga:
- sangue ou uma cor vermelha na urina
- um aumento da necessidade de urinar
- dor ao urinar
- ossos quebrados (fraturas). Geralmente na mão, braço ou pé em mulheres. Converse com seu médico para obter conselhos sobre como manter seus ossos saudáveis.
- doença ocular diabética com inchaço na parte de trás do olho (edema macular). Informe o seu médico imediatamente se tiver alguma alteração na sua visão. O seu médico deve verificar os seus olhos regularmente
- liberação de um óvulo de um ovário em uma mulher (ovulação) levando à gravidez. A ovulação pode ocorrer quando as mulheres na pré-menopausa que não têm períodos mensais regulares tomam ACTOS. Isso pode aumentar sua chance de engravidar
- sintomas semelhantes ao resfriado (infecção do trato respiratório superior)
- dor de cabeça
- infecção do sinus
- dor muscular
- dor de garganta
Os efeitos colaterais mais comuns do ACTOS incluem:
Informe o seu médico se tiver algum efeito secundário que o incomode ou que não desapareça.
Estes não são todos os efeitos colaterais do ACTOS. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar o ACTOS 15mg?
- Armazene ACTOS 15mg a 68°F a 77°F (20°C a 25°C). Manter ACTOS na embalagem original e proteger da luz
- Mantenha o frasco de ACTOS bem fechado e mantenha os comprimidos secos
- Mantenha ACTOS e todos os medicamentos fora do alcance das crianças
Informações gerais sobre o uso seguro e eficaz do ACTOS
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use ACTOS para uma condição para a qual não foi prescrito. Não dê ACTOS a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Este Guia de Medicação resume as informações mais importantes sobre ACTOS. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre ACTOS escritas para profissionais de saúde. Para obter mais informações, acesse www.actos.com ou ligue para 1-877-825-3327.
Quais são os ingredientes de ACTOS 15mg?
Princípio ativo: pioglitazona Ingredientes inativos: lactos 15mge monohidratado, hidroxipropilcelulose, carboximetilcelulose cálcio e estearato de magnésio
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
