Fosamax 35mg, 70mg Alendronate Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Fosamax 70mg e como é usado?
Fosamax 35mg é um medicamento de prescrição usado para prevenir e tratar certos tipos de perda óssea (osteoporose) em adultos. Fosamax 70mg pode ser usado sozinho ou com outros medicamentos.
Fosamax é um modificador do metabolismo do cálcio, derivados de bifosfonatos.
Não se sabe se Fosamax é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Fosamax?
Fosamax pode causar efeitos colaterais graves, incluindo:
- dor no peito
- azia nova ou agravada
- dor ou queimação sob as costelas ou nas costas
- azia grave
- dor ardente na parte superior do estômago ou tosse com sangue
- dor nova ou incomum na coxa ou no quadril
- dor na mandíbula
- dormência
- inchaço
- dor severa nas articulações, ossos ou músculos
- espasmos musculares ou cãibras
- dormência ou sensação de formigamento ao redor da boca ou nos dedos das mãos ou dos pés
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Fosamax incluem:
- azia
- dor de estômago
- dor de estômago
- náusea
- diarréia
- constipação
- dor no osso
- dor muscular
- dor nas articulações
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Fosamax. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
FOSAMAX (alendronato de sódio) é um bifosfonato que atua como um inibidor específico da reabsorção óssea mediada por osteoclastos. Os bisfosfonatos são análogos sintéticos do pirofosfato que se ligam à hidroxiapatita encontrada no osso.
O alendronato de sódio é quimicamente descrito como tri-hidrato de sal monossódico do ácido (4-amino-1-hidroxibutilideno).
A fórmula empírica do alendronato de sódio é C4H12NNaO7P2 •3H2O e seu peso de fórmula é 325,12. A fórmula estrutural é:
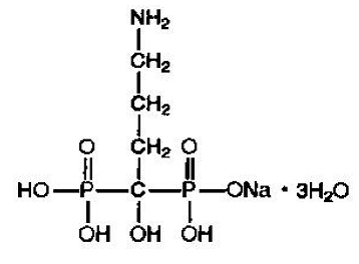
O alendronato de sódio é um pó branco, cristalino e não higroscópico. É solúvel em água, muito pouco solúvel em álcool e praticamente insolúvel em clorofórmio.
FOSAMAX 70 mg comprimidos para administração oral contém 91,37 mg de sal monossódico de alendronato trihidratado, que é o equivalente molar de 70 mg de ácido livre, e os seguintes ingredientes inativos: celulose microcristalina, lactose anidra, croscarmelose sódica e estearato de magnésio.
INDICAÇÕES
Treatment® da osteoporose em mulheres na pós-menopausa
FOSAMAX é indicado para o tratamento da osteoporose em mulheres na pós-menopausa. Em mulheres na pós-menopausa, FOSAMAX 70mg aumenta a massa óssea e reduz a incidência de fraturas, incluindo as do quadril e da coluna (fraturas por compressão vertebral). [Ver Estudos clínicos ]
Prevenção da osteoporose em mulheres na pós-menopausa
FOSAMAX 70mg é indicado para a prevenção da osteoporose pós-menopausa. Estudos clínicos ].
Tratamento para aumentar a massa óssea em homens com osteoporose
FOSAMAX é indicado para o tratamento do aumento da massa óssea em homens com osteoporose [ver Estudos clínicos ].
Tratamento da osteoporose induzida por glicocorticóides
FOSAMAX é indicado para o tratamento da osteoporose induzida por glicocorticóides em homens e mulheres recebendo glicocorticóides em uma dosagem diária equivalente a 7,5 mg ou mais de prednisona e que apresentam baixa densidade mineral óssea [ver Estudos clínicos ].
Tratamento da doença óssea de Paget
FOSAMAX 35mg é indicado para o tratamento da doença óssea de Paget em homens e mulheres. O tratamento é indicado em pacientes com doença óssea de Paget que apresentam fosfatase alcalina pelo menos duas vezes o limite superior do normal, ou aqueles que são sintomáticos, ou aqueles em risco de complicações futuras de sua doença. [Ver Estudos clínicos ]
Limitações importantes de uso
A duração ideal de uso não foi determinada. A segurança e eficácia de FOSAMAX para o tratamento da osteoporose são baseadas em dados clínicos de quatro anos de duração. Todos os pacientes em terapia com bisfosfonatos devem ter a necessidade de terapia continuada reavaliada periodicamente. Pacientes com baixo risco de fratura devem ser considerados para descontinuação do medicamento após 3 a 5 anos de uso. Os pacientes que descontinuam a terapia devem ter seu risco de fratura reavaliado periodicamente.
DOSAGEM E ADMINISTRAÇÃO
Embora os comprimidos de alendronato de 5 mg, 10 mg, 35 mg e 40 mg estejam disponíveis no mercado, FOSAMAX 35 mg não é mais comercializado nas dosagens de 5 mg, 10 mg, 35 mg e 40 mg.
Embora uma solução oral de alendronato possa estar disponível no mercado, FOSAMAX 35mg solução oral não é mais comercializado.
Tratamento da osteoporose em mulheres na pós-menopausa
A dosagem recomendada é:
- um comprimido de 70 mg uma vez por semana ou
- um frasco de 70 mg de solução oral uma vez por semana ou
- um comprimido de 10 mg uma vez ao dia
Prevenção da osteoporose em mulheres na pós-menopausa
A dosagem recomendada é:
- um comprimido de 35 mg uma vez por semana ou
- um comprimido de 5 mg uma vez ao dia
Tratamento para aumentar a massa óssea em homens com osteoporose
A dosagem recomendada é:
- um comprimido de 70 mg uma vez por semana ou
- um frasco de 70 mg de solução oral uma vez por semana ou
- um comprimido de 10 mg uma vez ao dia
Tratamento da osteoporose induzida por glicocorticóides
A dose recomendada é de um comprimido de 5 mg uma vez ao dia, exceto para mulheres na pós-menopausa que não recebem estrogênio, para quem a dose recomendada é de um comprimido de 10 mg uma vez ao dia.
Tratamento da doença óssea de Paget
O regime de tratamento recomendado é de 40 mg uma vez por dia durante seis meses.
Re-tratamento da doença de Paget
novo tratamento com FOSAMAX 35mg pode ser considerado, após um período de avaliação pós-tratamento de seis meses em pacientes que recaíram, com base nos aumentos da fosfatase alcalina sérica, que devem ser medidos periodicamente. O novo tratamento também pode ser considerado naqueles que não conseguiram normalizar sua fosfatase alcalina sérica.
Instruções importantes de administração
Instrua os pacientes a fazer o seguinte:
- Tome FOSAMAX pelo menos meia hora antes da primeira refeição, bebida ou medicamento do dia apenas com água pura [ver Informações de Aconselhamento do Paciente ]. Outras bebidas (incluindo água mineral), alimentos e alguns medicamentos podem reduzir a absorção de FOSAMAX [ver INTERAÇÕES MEDICAMENTOSAS ]. Esperar menos de 30 minutos ou tomar FOSAMAX 70mg com alimentos, bebidas (exceto água pura) ou outros medicamentos diminuirá o efeito de FOSAMAX 70mg, diminuindo sua absorção no corpo.
- Tome FOSAMAX ao acordar para o dia. Para facilitar a entrega ao estômago e, assim, reduzir o potencial de irritação esofágica, um comprimido de FOSAMAX 35mg deve ser engolido com um copo cheio de água (6-8 onças). Para facilitar o esvaziamento gástrico, a solução oral de FOSAMAX 70mg deve ser seguida de pelo menos 2 onças (um quarto de xícara) de água. Os pacientes não devem se deitar por pelo menos 30 minutos e até depois da primeira refeição do dia. FOSAMAX não deve ser tomado ao deitar ou antes de acordar. O não cumprimento destas instruções pode aumentar o risco de experiências adversas esofágicas [ver AVISOS E PRECAUÇÕES e Informações de Aconselhamento do Paciente ].
Recomendações para suplementação de cálcio e vitamina D
Instrua os pacientes a tomarem suplementos de cálcio se a ingestão dietética for inadequada [ver AVISOS E PRECAUÇÕES ]. Pacientes com risco aumentado de insuficiência de vitamina D (por exemplo, com idade superior a 70 anos, internados em casa de repouso ou doentes crônicos) podem precisar de suplementação de vitamina D. Pacientes com síndromes de má absorção gastrintestinal podem necessitar de doses mais altas de suplementação de vitamina D e a dosagem de 25-hidroxivitamina D deve ser considerada.
Pacientes tratados com glicocorticóides devem receber quantidades adequadas de cálcio e vitamina D.
Instruções de administração para doses perdidas
Se uma dose de FOSAMAX uma vez por semana for esquecida, instrua os pacientes a tomarem uma dose na manhã seguinte. Eles não devem tomar duas doses no mesmo dia, mas devem voltar a tomar uma dose uma vez por semana, conforme programado originalmente no dia escolhido.
COMO FORNECIDO
Formas de dosagem e pontos fortes
- Os comprimidos de 70 mg são comprimidos brancos, ovais, não revestidos, com o código 31 de um lado e o contorno de uma imagem óssea do outro.
Armazenamento e manuseio
Nº 3814 - FOSAMAX comprimidos, 70 mg, são comprimidos brancos, ovais, não revestidos com o código 31 de um lado e o contorno de uma imagem óssea do outro:
NDC 0006-0031-44 embalagem blister unidade de uso de 4.
Armazenar
Comprimidos FOSAMAX
Armazene em um recipiente bem fechado à temperatura ambiente, 15-30°C (59-86°F).
Distribuído por: Merck Sharp & Dohme Corp., uma subsidiária da MERCK & CO., INC., Whitehouse Station, NJ 08889, EUA. Revisado: agosto de 2019
EFEITOS COLATERAIS
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos sob condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
Tratamento da osteoporose em mulheres na pós-menopausa
Dosagem Diária
segurança de FOSAMAX 35mg no tratamento da osteoporose pós-menopausa foi avaliada em quatro ensaios clínicos que envolveram 7.453 mulheres com idades entre 44 e 84 anos. O Estudo 1 e o Estudo 2 foram desenhados de forma idêntica, três anos, controlados por placebo, duplo-cegos, multicêntricos (Estados Unidos e Multinacionais n=994); O Estudo 3 foi a coorte de fratura vertebral de três anos do Fracture Intervention Trial [FIT] (n=2027) e o Estudo 4 foi a coorte de fratura clínica de quatro anos do FIT (n=4432). No geral, 3.620 pacientes foram expostos ao placebo e 3.432 pacientes expostos ao FOSAMAX. Pacientes com doença gastrointestinal pré-existente e uso concomitante de anti-inflamatórios não esteroides foram incluídos nestes ensaios clínicos. No Estudo 1 e no Estudo 2 todas as mulheres receberam 500 mg de cálcio elementar como carbonato. No Estudo 3 e no Estudo 4, todas as mulheres com ingestão dietética de cálcio inferior a 1.000 mg por dia receberam 500 mg de cálcio e 250 unidades internacionais de vitamina D por dia.
Entre os pacientes tratados com alendronato 10 mg ou placebo no Estudo 1 e Estudo 2, e todos os pacientes no Estudo 3 e Estudo 4, a incidência de mortalidade por todas as causas foi de 1,8% no grupo placebo e 1,8% no grupo FOSAMAX 35mg. A incidência de eventos adversos graves foi de 30,7% no grupo placebo e 30,9% no grupo FOSAMAX. A porcentagem de pacientes que descontinuaram o estudo devido a qualquer evento adverso clínico foi de 9,5% no grupo placebo e 8,9% no grupo FOSAMAX 70mg. As reações adversas desses estudos considerados pelos pesquisadores como possivelmente, provavelmente ou definitivamente relacionadas ao medicamento em mais ou igual a 1% dos pacientes tratados com FOSAMAX 35mg ou placebo são apresentadas na Tabela 1.
Erupção cutânea e eritema ocorreram.
Reações Adversas Gastrointestinais
Um paciente tratado com FOSAMAX (10 mg/dia), com história de úlcera péptica e gastrectomia e em uso concomitante de aspirina, desenvolveu úlcera anastomótica com hemorragia leve, considerada relacionada ao medicamento. Aspirina e FOSAMAX foram descontinuados e o paciente se recuperou. Nas populações do Estudo 1 e do Estudo 2, 49-54% tinham histórico de distúrbios gastrointestinais no início do estudo e 54-89% usaram anti-inflamatórios não esteróides ou aspirina em algum momento durante os estudos. [Ver AVISOS E PRECAUÇÕES ]
Resultados de testes laboratoriais
Em estudos duplo-cegos, multicêntricos e controlados, foram observadas diminuições assintomáticas, leves e transitórias nos níveis séricos de cálcio e fosfato em aproximadamente 18% e 10%, respectivamente, dos pacientes que receberam FOSAMAX versus aproximadamente 12% e 3% daqueles que receberam placebo. No entanto, as incidências de diminuição do cálcio sérico para menos de 8,0 mg/dL (2,0 mM) e fosfato sérico para menos ou igual a 2,0 mg/dL (0,65 mM) foram semelhantes em ambos os grupos de tratamento.
Dosagem Semanal
segurança de FOSAMAX 70 mg uma vez por semana para o tratamento da osteoporose pós-menopausa foi avaliada em um estudo multicêntrico, duplo-cego, de um ano, comparando FOSAMAX 70 mg uma vez por semana e FOSAMAX 10 mg diariamente. Os perfis gerais de segurança e tolerabilidade de FOSAMAX 70 mg uma vez por semana e FOSAMAX 10 mg por dia foram semelhantes. As reações adversas consideradas pelos investigadores como possivelmente, provavelmente ou definitivamente relacionadas ao medicamento em mais ou igual a 1% dos pacientes em qualquer grupo de tratamento são apresentadas na Tabela 2.
Prevenção da osteoporose em mulheres na pós-menopausa
Dosagem Diária
A segurança de FOSAMAX 5 mg/dia em mulheres na pós-menopausa com 40-60 anos de idade foi avaliada em três estudos duplo-cegos, controlados por placebo, envolvendo mais de 1.400 pacientes randomizados para receber FOSAMAX por dois ou três anos. Nesses estudos, os perfis gerais de segurança de FOSAMAX 5 mg/dia e placebo foram semelhantes. A descontinuação da terapia devido a qualquer evento adverso clínico ocorreu em 7,5% dos 642 pacientes tratados com FOSAMAX 5 mg/dia e 5,7% dos 648 pacientes tratados com placebo.
Dosagem Semanal
segurança de FOSAMAX 35 mg uma vez por semana em comparação com FOSAMAX 5 mg por dia foi avaliada em um estudo multicêntrico, duplo-cego, de um ano com 723 pacientes. Os perfis gerais de segurança e tolerabilidade de FOSAMAX 35 mg uma vez por semana e FOSAMAX 5 mg por dia foram semelhantes.
As reações adversas desses estudos considerados pelos investigadores como possivelmente, provavelmente ou definitivamente relacionadas ao medicamento em mais ou igual a 1% dos pacientes tratados com FOSAMAX 35 mg uma vez por semana, FOSAMAX 5 mg/dia ou placebo são apresentadas na Tabela 3. .
Uso concomitante com terapia de reposição hormonal/estrogênica
Em dois estudos (de um e dois anos de duração) com mulheres osteoporóticas na pós-menopausa (total: n=853), o perfil de segurança e tolerabilidade do tratamento combinado com FOSAMAX 10 mg uma vez ao dia e estrogênio ± progestina (n=354) foi consistente com os dos tratamentos individuais.
Osteoporose em homens
Em dois estudos multicêntricos, duplo-cegos, controlados por placebo em homens (um estudo de dois anos de FOSAMAX 10 mg/dia e um estudo de um ano de FOSAMAX 70 mg uma vez por semana), as taxas de descontinuação da terapia devido a qualquer efeito clínico adverso foram 2,7% para FOSAMAX 10 mg/dia versus 10,5% para placebo e 6,4% para FOSAMAX 70 mg uma vez por semana versus 8,6% para placebo. As reações adversas consideradas pelos pesquisadores como possivelmente, provavelmente ou definitivamente relacionadas ao medicamento em maior ou igual a 2% dos pacientes tratados com FOSAMAX 70mg ou placebo são apresentadas na Tabela 4.
Osteoporose induzida por glicocorticóides
Em dois estudos multicêntricos, duplo-cegos, controlados por placebo, com duração de um ano em pacientes recebendo tratamento com glicocorticoide, os perfis gerais de segurança e tolerabilidade de FOSAMAX 5 e 10 mg/dia foram geralmente semelhantes aos do placebo. As reações adversas consideradas pelos investigadores como possivelmente, provavelmente ou definitivamente relacionadas ao medicamento em maior ou igual a 1% dos pacientes tratados com FOSAMAX 5 ou 10 mg/dia ou placebo são apresentadas na Tabela 5.
O perfil geral de segurança e tolerabilidade na população de osteoporose induzida por glicocorticóides que continuou a terapia pelo segundo ano dos estudos (FOSAMAX: n=147) foi consistente com o observado no primeiro ano.
Doença óssea de Paget
Em estudos clínicos (osteoporose e doença de Paget), os eventos adversos relatados em 175 pacientes tomando FOSAMAX 40 mg/dia por 3-12 meses foram semelhantes aos de mulheres na pós-menopausa tratadas com FOSAMAX 10 mg/dia. Entretanto, houve um aparente aumento na incidência de reações adversas do trato gastrintestinal superior em pacientes tomando FOSAMAX 40 mg/dia (17,7% FOSAMAX versus 10,2% placebo). Um caso de esofagite e dois casos de gastrite resultaram na descontinuação do tratamento.
Além disso, a dor musculoesquelética (óssea, muscular ou articular), que foi descrita em pacientes com doença de Paget tratados com outros bifosfonatos, foi considerada pelos pesquisadores como possivelmente, provavelmente ou definitivamente relacionada ao medicamento em aproximadamente 6% dos pacientes. tratados com FOSAMAX 40 mg/dia versus aproximadamente 1% dos pacientes tratados com placebo, mas raramente resultaram na descontinuação da terapia. A descontinuação da terapia devido a quaisquer eventos adversos clínicos ocorreu em 6,4% dos pacientes com doença de Paget tratados com FOSAMAX 40 mg/dia e 2,4% dos pacientes tratados com placebo.
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de FOSAMAX. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Corpo como um todo: reações de hipersensibilidade incluindo urticária e angioedema. Sintomas transitórios de mialgia, mal-estar, astenia e febre foram relatados com FOSAMAX, geralmente associados ao início do tratamento. Ocorreu hipocalcemia sintomática, geralmente associada a condições predisponentes. Edema periférico.
Gastrointestinal: esofagite, erosões esofágicas, úlceras esofágicas, estenose ou perfuração esofágica e ulceração orofaríngea. Úlceras gástricas ou duodenais, algumas graves e com complicações, também foram relatadas [ver DOSAGEM E ADMINISTRAÇÃO ; AVISOS E PRECAUÇÕES ].
Foi relatada osteonecrose localizada da mandíbula, geralmente associada à extração do dente e/ou infecção local com cicatrização tardia. AVISOS E PRECAUÇÕES ].
Musculoesquelético: dores ósseas, articulares e/ou musculares, ocasionalmente graves e incapacitantes [ver AVISOS E PRECAUÇÕES ]; inchaço nas articulaçoes; fraturas da diáfise femoral de baixa energia e subtrocantéricas [ver AVISOS E PRECAUÇÕES ].
Sistema nervoso: tontura e vertigem.
Pulmonar: exacerbações agudas da asma.
Pele: erupção cutânea (ocasionalmente com fotossensibilidade), prurido, alopecia, reações cutâneas graves, incluindo síndrome de Stevens-Johnson e necrólise epidérmica tóxica.
Sentidos Especiais: uveíte, esclerite ou episclerite. Colesteatoma do meato acústico externo (osteonecrose focal).
INTERAÇÕES MEDICAMENTOSAS
Suplementos de cálcio/antiácidos
A coadministração de FOSAMAX e cálcio, antiácidos ou medicamentos orais contendo cátions multivalentes interferirá na absorção de FOSAMAX. Portanto, instrua os pacientes a esperar pelo menos meia hora após tomar FOSAMAX 35mg antes de tomar qualquer outro medicamento oral.
Aspirina
Em estudos clínicos, a incidência de eventos adversos gastrointestinais superiores foi aumentada em pacientes recebendo terapia concomitante com doses diárias de FOSAMAX 35mg maiores que 10mg e produtos contendo aspirina.
Anti-inflamatórios não esteroides
FOSAMAX 35mg pode ser administrado a pacientes em uso de anti-inflamatórios não esteróides (AINEs). Em um estudo clínico controlado de 3 anos (n=2.027) durante o qual a maioria dos pacientes recebeu AINEs concomitantes, a incidência de eventos adversos gastrointestinais superiores foi semelhante em pacientes que tomaram FOSAMAX 5 ou 10 mg/dia em comparação com aqueles que tomaram placebo. No entanto, uma vez que o uso de AINEs está associado a irritação gastrointestinal, deve-se ter cautela durante o uso concomitante com FOSAMAX.
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Reações Adversas Gastrointestinais Superiores
FOSAMAX 35mg, como outros bisfosfonatos administrados por via oral, pode causar irritação local da mucosa gastrointestinal superior. Devido a esses possíveis efeitos irritantes e ao potencial de agravamento da doença subjacente, deve-se ter cautela quando FOSAMAX é administrado a pacientes com problemas gastrointestinais superiores ativos (como esôfago de Barrett, disfagia, outras doenças esofágicas, gastrite, duodenite ou úlceras).
Experiências adversas esofágicas, como esofagite, úlceras esofágicas e erosões esofágicas, ocasionalmente com sangramento e raramente seguidas de estenose ou perfuração esofágica, foram relatadas em pacientes recebendo tratamento com bifosfonatos orais, incluindo FOSAMAX. Em alguns casos, foram graves e exigiram hospitalização. Os médicos devem, portanto, estar atentos a quaisquer sinais ou sintomas que indiquem uma possível reação esofágica e os pacientes devem ser instruídos a descontinuar FOSAMAX 70mg e procurar atendimento médico se desenvolverem disfagia, odinofagia, dor retroesternal ou pirose recente ou agravada.
risco de eventos adversos esofágicos graves parece ser maior em pacientes que se deitam após tomar bisfosfonatos orais, incluindo FOSAMAX 70mg e/ou que não conseguem engolir bisfosfonatos orais, incluindo FOSAMAX 35mg com o copo cheio recomendado (6-8 onças) de água, e /ou que continuam a tomar bisfosfonatos orais, incluindo FOSAMAX 70mg, após desenvolverem sintomas sugestivos de irritação esofágica. Portanto, é muito importante que as instruções completas de dosagem sejam fornecidas e compreendidas pelo paciente [ver DOSAGEM E ADMINISTRAÇÃO ]. Em pacientes que não podem cumprir as instruções de dosagem devido a deficiência mental, a terapia com FOSAMAX deve ser usada sob supervisão apropriada.
Houve relatos pós-comercialização de úlceras gástricas e duodenais com o uso de bisfosfonatos orais, algumas graves e com complicações, embora nenhum risco aumentado tenha sido observado em ensaios clínicos controlados [ver REAÇÕES ADVERSAS ].
Metabolismo Mineral
A hipocalcemia deve ser corrigida antes de iniciar a terapia com FOSAMAX [ver CONTRA-INDICAÇÕES ]. Outros distúrbios que afetam o metabolismo mineral (como deficiência de vitamina D) também devem ser tratados com eficácia. Em pacientes com essas condições, o cálcio sérico e os sintomas de hipocalcemia devem ser monitorados durante a terapia com FOSAMAX.
Presumivelmente devido aos efeitos de FOSAMAX no aumento da mineralidade óssea, podem ocorrer pequenas diminuições assintomáticas no cálcio e fosfato séricos, especialmente em pacientes com doença de Paget, nos quais a taxa de remodelação óssea pré-tratamento pode ser muito elevada, e em pacientes recebendo glicocorticóides, nos quais a absorção de cálcio pode estar diminuída.
Garantir a ingestão adequada de cálcio e vitamina D é especialmente importante em pacientes com doença óssea de Paget e em pacientes que recebem glicocorticóides.
Dor musculoesquelética
Na experiência pós-comercialização, foram relatadas dores ósseas, articulares e/ou musculares graves e ocasionalmente incapacitantes em pacientes tomando bifosfonatos aprovados para a prevenção e tratamento da osteoporose [ver REAÇÕES ADVERSAS ]. Esta categoria de medicamentos inclui FOSAMAX (alendronato). A maioria dos pacientes eram mulheres na pós-menopausa. O tempo de início dos sintomas variou de um dia a vários meses após o início da droga. Interrompa o uso se desenvolver sintomas graves. A maioria dos pacientes teve alívio dos sintomas após a interrupção. Um subconjunto apresentou recorrência dos sintomas quando reexpostos com a mesma droga ou outro bisfosfonato.
Em estudos clínicos controlados com placebo de FOSAMAX, as porcentagens de pacientes com esses sintomas foram semelhantes nos grupos de FOSAMAX 35mg e placebo.
Osteonecrose da mandíbula
osteonecrose da mandíbula (ONM), que pode ocorrer espontaneamente, geralmente está associada à extração dentária e/ou infecção local com retardo de cicatrização, e foi relatada em pacientes em uso de bifosfonatos, incluindo FOSAMAX. Fatores de risco conhecidos para osteonecrose da mandíbula incluem procedimentos odontológicos invasivos (por exemplo, extração dentária, implantes dentários, cirurgia óssea), diagnóstico de câncer, terapias concomitantes (por exemplo, quimioterapia, corticosteróides, inibidores da angiogênese), má higiene oral e comorbidades desordens (por exemplo, doença periodontal e/ou outra doença dentária pré-existente, anemia, coagulopatia, infecção, dentaduras mal ajustadas). O risco de ONM pode aumentar com a duração da exposição aos bifosfonatos.
Para pacientes que necessitam de procedimentos odontológicos invasivos, a descontinuação do tratamento com bisfosfonatos pode reduzir o risco de ONM. O julgamento clínico do médico assistente e/ou cirurgião oral deve orientar o plano de tratamento de cada paciente com base na avaliação individual de benefício/risco.
Pacientes que desenvolvem osteonecrose da mandíbula durante a terapia com bisfosfonatos devem receber cuidados de um cirurgião oral. Nesses pacientes, a cirurgia odontológica extensa para tratar a ONM pode exacerbar a condição. A descontinuação da terapia com bifosfonatos deve ser considerada com base na avaliação individual de benefício/risco.
Fraturas atípicas subtrocantéricas e diafisárias do fêmur
Fraturas atípicas, de baixa energia ou de baixo trauma da diáfise femoral foram relatadas em pacientes tratados com bisfosfonatos. Essas fraturas podem ocorrer em qualquer lugar da diáfise femoral, desde logo abaixo do trocanter menor até acima do alargamento supracondilar e são transversais ou oblíquas curtas em orientação sem evidência de cominuição. A causalidade não foi estabelecida, pois essas fraturas também ocorrem em pacientes osteoporóticos que não foram tratados com bisfosfonatos.
As fraturas atípicas do fêmur ocorrem mais comumente com trauma mínimo ou nenhum na área afetada. Eles podem ser bilaterais e muitos pacientes relatam dor prodrômica na área afetada, geralmente apresentando-se como dor incômoda e dolorida na coxa, semanas a meses antes de ocorrer uma fratura completa. Vários relatórios observam que os pacientes também estavam recebendo tratamento com glicocorticóides (por exemplo, prednisona) no momento da fratura.
Qualquer paciente com história de exposição a bisfosfonatos que apresente dor na coxa ou na virilha deve ser suspeito de ter uma fratura atípica e deve ser avaliado para descartar uma fratura incompleta do fêmur. Pacientes com fratura atípica também devem ser avaliados quanto a sintomas e sinais de fratura no membro contralateral. A interrupção da terapia com bisfosfonatos deve ser considerada, na pendência de uma avaliação de risco/benefício, individualmente.
Insuficiência renal
FOSAMAX 35mg não é recomendado para pacientes com clearance de creatinina menor que 35 mL/min.
Osteoporose induzida por glicocorticóides
risco versus benefício de FOSAMAX para tratamento em doses diárias de glicocorticóides inferiores a 7,5 mg de prednisona ou equivalente não foi estabelecido [ver INDICAÇÕES E USO ]. Antes de iniciar o tratamento, o estado hormonal gonadal de homens e mulheres deve ser verificado e a reposição apropriada deve ser considerada.
A medição da densidade mineral óssea deve ser feita no início da terapia e repetida após 6 a 12 meses de tratamento combinado com FOSAMAX e glicocorticóide.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( Guia de Medicação ).
Instrua os pacientes a ler o Guia de Medicação antes de iniciar a terapia com FOSAMAX e reler sempre que a prescrição for renovada.
Recomendações para osteoporose, incluindo suplementação de cálcio e vitamina D
Instruir os pacientes a tomar suplementos de cálcio e vitamina D, se a ingestão diária de alimentos for inadequada. O exercício com pesos deve ser considerado juntamente com a modificação de certos fatores comportamentais, como tabagismo e/ou consumo excessivo de álcool, se esses fatores existirem.
Instruções de dosagem
Instrua os pacientes que os benefícios esperados de FOSAMAX 70mg só podem ser obtidos quando tomado com água pura logo ao acordar pelo menos 30 minutos antes da primeira comida, bebida ou medicação do dia. Mesmo a dosagem com suco de laranja ou café demonstrou reduzir acentuadamente a absorção de FOSAMAX [ver FARMACOLOGIA CLÍNICA ].
Instruir os pacientes a não mastigar ou chupar o comprimido devido ao potencial de ulceração orofaríngea.
Instrua os pacientes a engolir cada comprimido de FOSAMAX com um copo cheio de água (6-8 onças) para facilitar a entrega ao estômago e, assim, reduzir o potencial de irritação esofágica. Instrua os pacientes a beber pelo menos 2 onças (um quarto de xícara) de água após tomar FOSAMAX 70mg solução oral, para facilitar o esvaziamento gástrico.
Instruir os pacientes a não se deitarem por pelo menos 30 minutos e até depois da primeira refeição do dia.
Instruir os pacientes a não tomar FOSAMAX na hora de dormir ou antes de acordar. Os pacientes devem ser informados de que o não cumprimento dessas instruções pode aumentar o risco de problemas esofágicos.
Instrua os pacientes que, se desenvolverem sintomas de doença esofágica (como dificuldade ou dor ao engolir, dor retroesternal ou azia nova ou agravada), devem parar de tomar FOSAMAX e consultar seu médico.
Se os pacientes perderem uma dose de FOSAMAX 70mg uma vez por semana, instrua os pacientes a tomarem uma dose na manhã seguinte. Eles não devem tomar duas doses no mesmo dia, mas devem voltar a tomar uma dose uma vez por semana, conforme programado originalmente no dia escolhido.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Os adenomas da glândula Harderian (uma glândula retro-orbital não presente em humanos) foram aumentados em camundongos fêmeas de alta dose (p = 0,003) em um estudo de carcinogenicidade oral de 92 semanas com doses de alendronato de 1, 3 e 10 mg/kg/ dia (homens) ou 1, 2 e 5 mg/kg/dia (mulheres). Essas doses são equivalentes a aproximadamente 0,1 a 1 vez a dose clínica diária mais alta recomendada de 40 mg com base na área de superfície, mg/m². A relevância deste achado para humanos é desconhecida.
Os adenomas de células parafoliculares (tireoide) foram aumentados em ratos machos de alta dose (p = 0,003) em um estudo de carcinogenicidade oral de 2 anos com doses de 1 e 3,75 mg/kg de peso corporal. Essas doses são equivalentes a aproximadamente 0,3 e 1 vez a dose clínica diária de 40 mg com base na área de superfície, mg/m². A relevância desse achado para humanos é desconhecida.
alendronato não foi genotóxico no ensaio de mutagênese microbiana in vitro com e sem ativação metabólica, em um ensaio in vitro de mutagênese em células de mamífero, em um ensaio de eluição alcalina in vitro em hepatócitos de ratos e em um ensaio de aberração cromossômica in vivo em camundongos. Em um ensaio de aberração cromossômica in vitro em células de ovário de hamster chinês, no entanto, o alendronato deu resultados ambíguos.
O alendronato não teve efeito sobre a fertilidade (macho ou fêmea) em ratos em doses orais de até 5 mg/kg/dia (aproximadamente 1 vez a dose clínica diária de 40 mg com base na área de superfície, mg/m²).
Uso em populações específicas
Gravidez
Resumo do risco
Os dados disponíveis sobre o uso de FOSAMAX em mulheres grávidas são insuficientes para informar um risco associado ao medicamento de desfechos maternos ou fetais adversos. Descontinuar FOSAMAX 35mg quando a gravidez for reconhecida.
Em estudos de reprodução animal, a administração oral diária de alendronato a ratos desde antes do acasalamento até o final da gestação ou lactação mostrou diminuição da sobrevida pós-implantação e diminuição do ganho de peso corporal dos filhotes começando com doses equivalentes a menos da metade da dose diária clínica diária mais alta recomendada de 40 mg ( com base na área de superfície corporal, mg/m²). A administração oral de alendronato a ratos durante a organogénese resultou na redução da ossificação fetal a partir de doses 3 vezes a dose clínica diária de 40 mg. Não foram observados efeitos fetais semelhantes em coelhas prenhas administradas oralmente durante a organogênese em doses equivalentes a aproximadamente 10 vezes a dose clínica diária de 40 mg.
Atraso ou falha no parto, parto prolongado e morte materna e fetal no final da gravidez devido à hipocalcemia materna ocorreram em ratos em doses orais tão baixas quanto um décimo da dose clínica diária de 40 mg (ver Dados ).
Os bisfosfonatos são incorporados à matriz óssea, da qual são liberados gradualmente ao longo de um período de anos. A quantidade de bifosfonato incorporada ao osso adulto e disponível para liberação na circulação sistêmica está diretamente relacionada à dose e duração do uso de bifosfonato. Consequentemente, com base no mecanismo de ação dos bisfosfonatos, existe um risco potencial de dano fetal, predominantemente esquelético, se uma mulher engravidar após completar um ciclo de terapia com bisfosfonatos. O impacto de variáveis como o tempo entre a interrupção da terapia com bisfosfonatos até a concepção, o bisfosfonato específico usado e a via de administração (intravenosa versus oral) sobre o risco não foi estudado.
risco de fundo estimado de defeitos congênitos graves e aborto para a(s) população(ões) indicada(s) é desconhecido. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, os riscos de fundo estimados de grandes defeitos congênitos e aborto em gestações clinicamente reconhecidas são de 2-4% e 15-20%, respectivamente.
Dados
Dados de animais
Estudos de reprodução em ratos administrados por via oral desde antes do acasalamento até o final da gestação ou lactação mostraram diminuição da sobrevida pós-implantação a partir de 2 mg/kg/dia e diminuição do ganho de peso corporal a partir de 1 mg/kg/dia, doses equivalentes a menos da metade dos 40 mg dose diária clínica baseada na área de superfície corporal, mg/m². A incidência de ossificação fetal incompleta nos ossos vertebrais, cranianos e esternebrais aumentou em ratos administrados por via oral durante a organogênese começando com 10 mg/kg/dia (aproximadamente 3 vezes a dose clínica diária de 40 mg). Não foram observados efeitos fetais semelhantes em coelhas grávidas com doses oralmente durante a organogênese de até 35 mg/kg/dia (equivalente a aproximadamente 10 vezes a dose clínica diária de 40 mg).
Tanto o cálcio total como o ionizado diminuíram em ratas grávidas que receberam por via oral 15 mg/kg/dia de alendronato (aproximadamente 4 vezes a dose clínica diária de 40 mg), resultando em atrasos e falhas no parto. Parto prolongado devido à hipocalcemia materna foi observado quando os ratos foram tratados desde antes do acasalamento até a gestação começando com 0,5 mg/kg/dia (aproximadamente um décimo da dose clínica diária de 40 mg). Maternotoxicidade (mortes na gravidez tardia) também ocorreu em ratas tratadas oralmente com 15 mg/kg/dia (aproximadamente 4 vezes a dose clínica diária de 40 mg) por períodos de tempo gestacionais variados. Essas mortes maternas foram diminuídas, mas não eliminadas pela interrupção do tratamento. A suplementação de cálcio na água de beber ou por minibomba subcutânea em ratos, dosados por via oral com 15 mg/kg/dia de alendronato, não conseguiu melhorar a hipocalcemia ou prevenir as mortes maternas e neonatais relacionadas à distocia. No entanto, a suplementação intravenosa de cálcio preveniu as mortes maternas, mas não as neonatais.
Lactação
Resumo do risco
Não se sabe se o alendronato está presente no leite materno humano, afeta a produção de leite humano ou tem efeitos no lactente. Os benefícios da amamentação para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de FOSAMAX 70mg e quaisquer potenciais efeitos adversos na criança amamentada de FOSAMAX ou da condição materna subjacente.
Uso Pediátrico
FOSAMAX 70mg não é indicado para uso em pacientes pediátricos.
segurança e eficácia de FOSAMAX foram examinadas em um estudo randomizado, duplo-cego, controlado por placebo de dois anos de 139 pacientes pediátricos, com idades entre 4-18 anos, com osteogênese imperfeita (OI) grave. Cento e nove pacientes foram randomizados para 5 mg de FOSAMAX 35mg por dia (peso menor que 40 kg) ou 10 mg de FOSAMAX 70mg por dia (peso maior ou igual a 40 kg) e 30 pacientes para placebo. O escore Z de DMO da coluna lombar na linha de base média dos pacientes foi de -4,5. A alteração média no escore Z da DMO da coluna lombar desde o início até o mês 24 foi de 1,3 nos pacientes tratados com FOSAMAX 35mg e 0,1 nos pacientes tratados com placebo. O tratamento com FOSAMAX 35mg não reduziu o risco de fratura. Dezesseis por cento dos pacientes com FOSAMAX que sofreram uma fratura confirmada radiologicamente no Mês 12 do estudo tiveram retardo na consolidação da fratura (remodelação do calo) ou não união da fratura quando avaliados radiograficamente no Mês 24 em comparação com 9% dos pacientes tratados com placebo. Em pacientes tratados com FOSAMAX, os dados de histomorfometria óssea obtidos no mês 24 demonstraram diminuição da renovação óssea e atraso no tempo de mineralização; no entanto, não houve defeitos de mineralização. Não houve diferenças estatisticamente significativas entre os grupos FOSAMAX 35mg e placebo na redução da dor óssea. A biodisponibilidade oral em crianças foi semelhante à observada em adultos.
perfil de segurança geral de FOSAMAX em pacientes com osteogênese imperfeita tratados por até 24 meses foi geralmente semelhante ao de adultos com osteoporose tratados com FOSAMAX. No entanto, houve um aumento da ocorrência de vômitos em pacientes com osteogênese imperfeita tratados com FOSAMAX em comparação ao placebo. Durante o período de tratamento de 24 meses, vômitos foram observados em 32 de 109 (29,4%) pacientes tratados com FOSAMAX 70mg e 3 de 30 (10%) pacientes tratados com placebo.
Em um estudo farmacocinético, 6 de 24 pacientes pediátricos com osteogênese imperfeita que receberam uma dose oral única de FOSAMAX 35 ou 70 mg desenvolveram febre, sintomas semelhantes aos da gripe e/ou linfocitopenia leve dentro de 24 a 48 horas após a administração. Esses eventos, com duração não superior a 2 a 3 dias e respondendo ao acetaminofeno, são consistentes com uma resposta de fase aguda que foi relatada em pacientes recebendo bifosfonatos, incluindo FOSAMAX. [Ver REAÇÕES ADVERSAS ]
Uso Geriátrico
Dos pacientes que receberam FOSAMAX no Fracture Intervention Trial (FIT), 71% (n=2302) tinham idade maior ou igual a 65 anos e 17% (n=550) tinham idade maior ou igual a 75 anos. Dos pacientes que receberam FOSAMAX 70mg nos Estados Unidos e estudos multinacionais de tratamento de osteoporose em mulheres, estudos de osteoporose em homens, estudos de osteoporose induzida por glicocorticóides e estudos de doença de Paget [ver Estudos clínicos ], 45%, 54%, 37% e 70%, respectivamente, tinham 65 anos ou mais. Não foram observadas diferenças gerais na eficácia ou segurança entre esses pacientes e pacientes mais jovens, mas a maior sensibilidade de alguns indivíduos mais velhos não pode ser descartada.
Insuficiência renal
FOSAMAX 70mg não é recomendado para pacientes com clearance de creatinina menor que 35 mL/min. Não é necessário ajuste de dose em pacientes com valores de clearance de creatinina entre 35-60 mL/min [ver FARMACOLOGIA CLÍNICA ].
Insuficiência hepática
Como há evidências de que o alendronato não é metabolizado ou excretado na bile, não foram realizados estudos em pacientes com insuficiência hepática. Não é necessário ajuste de dose [ver FARMACOLOGIA CLÍNICA ].
SOBREDOSAGEM
Letalidade significativa após doses orais únicas foi observada em ratos e camundongos fêmeas a 552 mg/kg (3256 mg/m²) e 966 mg/kg (2898 mg/m²), respectivamente. No sexo masculino, esses valores foram ligeiramente superiores, 626 e 1280 mg/kg, respectivamente. Não houve letalidade em cães em doses orais de até 200 mg/kg (4000 mg/m²).
Nenhuma informação específica está disponível sobre o tratamento de superdosagem com FOSAMAX. Hipocalcemia, hipofosfatemia e eventos adversos gastrointestinais superiores, como dor de estômago, azia, esofagite, gastrite ou úlcera, podem resultar de superdosagem oral. Leite ou antiácidos devem ser administrados para ligar o alendronato. Devido ao risco de irritação esofágica, o vômito não deve ser induzido e o paciente deve permanecer totalmente em pé.
A diálise não seria benéfica.
CONTRA-INDICAÇÕES
FOSAMAX 35mg é contraindicado em pacientes com as seguintes condições:
- Anormalidades do esôfago que retardam o esvaziamento esofágico, como estenose ou acalasia [ver AVISOS E PRECAUÇÕES ]
- Incapacidade de ficar em pé ou sentado por pelo menos 30 minutos [ver DOSAGEM E ADMINISTRAÇÃO ; AVISOS E PRECAUÇÕES ]
- Não administre FOSAMAX 35mg solução oral a pacientes com risco aumentado de aspiração.
- Hipocalcemia [ver AVISOS E PRECAUÇÕES ]
- Hipersensibilidade a qualquer componente deste produto. Reações de hipersensibilidade, incluindo urticária e angioedema, foram relatadas [ver REAÇÕES ADVERSAS ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
Estudos em animais indicaram o seguinte modo de ação. Ao nível celular, o alendronato apresenta localização preferencial em locais de reabsorção óssea, especificamente sob osteoclastos. Os osteoclastos aderem normalmente à superfície óssea, mas não possuem a borda enrugada que é indicativa de reabsorção ativa. O alendronato não interfere no recrutamento ou fixação dos osteoclastos, mas inibe a atividade dos osteoclastos. Estudos em camundongos sobre a localização de [3H]alendronato radioativo no osso mostraram uma captação cerca de 10 vezes maior nas superfícies dos osteoclastos do que nas superfícies dos osteoblastos. Ossos examinados 6 e 49 dias após a administração de [3H]alendronato em ratos e camundongos, respectivamente, mostraram que o osso normal foi formado no topo do alendronato, que foi incorporado dentro da matriz. Embora incorporado na matriz óssea, o alendronato não é farmacologicamente ativo. Assim, o alendronato deve ser administrado continuamente para suprimir os osteoclastos nas superfícies de reabsorção recém-formadas. A histomorfometria em babuínos e ratos mostrou que o tratamento com alendronato reduz a renovação óssea (ou seja, o número de locais em que o osso é remodelado). Além disso, a formação óssea excede a reabsorção óssea nesses locais de remodelação, levando a ganhos progressivos de massa óssea.

Farmacodinâmica
alendronato é um bifosfonato que se liga à hidroxiapatita óssea e inibe especificamente a atividade dos osteoclastos, as células de reabsorção óssea. O alendronato reduz a reabsorção óssea sem efeito direto sobre a formação óssea, embora o último processo seja reduzido porque a reabsorção e a formação óssea são acopladas durante a renovação óssea.
Osteoporose em mulheres na pós-menopausa
osteoporose é caracterizada pela baixa massa óssea que leva a um risco aumentado de fratura. O diagnóstico pode ser confirmado pelo achado de baixa massa óssea, evidência de fratura na radiografia, história de fratura osteoporótica ou perda de altura ou cifose, indicativa de fratura vertebral. A osteoporose ocorre em homens e mulheres, mas é mais comum entre as mulheres após a menopausa, quando a renovação óssea aumenta e a taxa de reabsorção óssea excede a de formação óssea. Essas alterações resultam em perda óssea progressiva e levam à osteoporose em uma proporção significativa de mulheres com mais de 50 anos. Fraturas, geralmente da coluna, quadril e punho, são as consequências comuns. Dos 50 aos 90 anos, o risco de fratura de quadril em mulheres brancas aumenta 50 vezes e o risco de fratura vertebral 15 a 30 vezes. Estima-se que aproximadamente 40% das mulheres de 50 anos sofrerão uma ou mais fraturas da coluna, quadril ou punho relacionadas à osteoporose durante suas vidas restantes. As fraturas de quadril, em particular, estão associadas a morbidade, incapacidade e mortalidade substanciais.
Doses orais diárias de alendronato (5, 20 e 40 mg por seis semanas) em mulheres na pós-menopausa produziram alterações bioquímicas indicativas de inibição dose-dependente da reabsorção óssea, incluindo diminuição do cálcio urinário e marcadores urinários de degradação do colágeno ósseo (como deoxipiridinolina e N-telopeptídeos ligados de colágeno tipo I). Essas alterações bioquímicas tenderam a retornar aos valores basais tão cedo quanto 3 semanas após a descontinuação da terapia com alendronato e não diferiram do placebo após 7 meses.
tratamento a longo prazo da osteoporose com FOSAMAX 10 mg/dia (por até cinco anos) reduziu a excreção urinária de marcadores de reabsorção óssea, desoxipiridinolina e N-telopeptídeos reticulados do colágeno tipo I, em aproximadamente 50% e 70%, respectivamente , para atingir níveis semelhantes aos observados em mulheres pré-menopáusicas saudáveis. Diminuições semelhantes foram observadas em pacientes em estudos de prevenção da osteoporose que receberam FOSAMAX 5 mg/dia. A diminuição na taxa de reabsorção óssea indicada por esses marcadores foi evidente já em um mês e em três a seis meses atingiu um platô que foi mantido por toda a duração do tratamento com FOSAMAX. Em estudos de tratamento da osteoporose, FOSAMAX 10 mg/dia diminuiu os marcadores de formação óssea, osteocalcina e fosfatase alcalina específica do osso em aproximadamente 50% e fosfatase alcalina sérica total em aproximadamente 25 a 30% para atingir um platô após 6 a 12 meses. Em estudos de prevenção da osteoporose, FOSAMAX 5 mg/dia diminuiu a osteocalcina e a fosfatase alcalina sérica total em aproximadamente 40% e 15%, respectivamente. Reduções semelhantes na taxa de remodelação óssea foram observadas em mulheres na pós-menopausa durante estudos de um ano com FOSAMAX 70 mg uma vez por semana para o tratamento da osteoporose e FOSAMAX 35 mg uma vez por semana para a prevenção da osteoporose. Esses dados indicam que a taxa de renovação óssea atingiu um novo estado de equilíbrio, apesar do aumento progressivo na quantidade total de alendronato depositado no osso.
Como resultado da inibição da reabsorção óssea, também foram observadas reduções assintomáticas nas concentrações séricas de cálcio e fosfato após o tratamento com FOSAMAX. Nos estudos de longo prazo, as reduções da linha de base no cálcio sérico (aproximadamente 2%) e fosfato (aproximadamente 4 a 6%) foram evidentes no primeiro mês após o início de FOSAMAX 10 mg. Não foram observadas outras diminuições no cálcio sérico durante os cinco anos de tratamento; no entanto, o fosfato sérico retornou aos níveis pré-estudo durante os anos três a cinco. Reduções semelhantes foram observadas com FOSAMAX 5 mg/dia. Em estudos de um ano com FOSAMAX 35 e 70 mg uma vez por semana, reduções semelhantes foram observadas em 6 e 12 meses. A redução do fosfato sérico pode refletir não apenas o balanço mineral ósseo positivo devido ao FOSAMAX 70mg, mas também uma diminuição na reabsorção renal de fosfato.
Osteoporose em homens
tratamento de homens com osteoporose com FOSAMAX 10 mg/dia por dois anos reduziu a excreção urinária de N-telopeptídeos reticulados do colágeno tipo I em aproximadamente 60% e fosfatase alcalina específica do osso em aproximadamente 40%. Reduções semelhantes foram observadas em um estudo de um ano em homens com osteoporose recebendo FOSAMAX 70 mg uma vez por semana.
Osteoporose induzida por glicocorticóides
O uso sustentado de glicocorticóides é comumente associado ao desenvolvimento de osteoporose e fraturas resultantes (especialmente vertebrais, quadril e costelas). Ocorre tanto em homens como em mulheres de todas as idades. A osteoporose ocorre como resultado da formação óssea inibida e do aumento da reabsorção óssea, resultando em perda óssea líquida. O alendronato diminui a reabsorção óssea sem inibir diretamente a formação óssea.
Em estudos clínicos de até dois anos' duração, FOSAMAX 5 e 10 mg/dia reduziram os N-telopeptídeos reticulados do colágeno tipo I (um marcador de reabsorção óssea) em aproximadamente 60% e reduziram a fosfatase alcalina específica do osso e a fosfatase alcalina sérica total (marcadores de formação óssea) por aproximadamente 15 a 30% e 8 a 18%, respectivamente. Como resultado da inibição da reabsorção óssea, FOSAMAX 5 e 10 mg/dia induziram reduções assintomáticas no cálcio sérico (aproximadamente 1 a 2%) e fosfato sérico (aproximadamente 1 a 8%).
Doença óssea de Paget
A doença óssea de Paget é um distúrbio esquelético focal e crônico caracterizado por remodelação óssea muito aumentada e desordenada. A reabsorção óssea osteoclástica excessiva é seguida pela formação de novo osso osteoblástico, levando à substituição da arquitetura óssea normal por uma estrutura óssea desorganizada, aumentada e enfraquecida.
As manifestações clínicas da doença de Paget variam de ausência de sintomas a morbidade grave devido a dor óssea, deformidade óssea, fraturas patológicas e complicações neurológicas e outras. A fosfatase alcalina sérica, o índice bioquímico de atividade da doença mais frequentemente usado, fornece uma medida objetiva da gravidade da doença e da resposta à terapia.
FOSAMAX 70mg diminui a taxa de reabsorção óssea diretamente, o que leva a uma diminuição indireta na formação óssea. Em ensaios clínicos, FOSAMAX 40 mg uma vez ao dia durante seis meses produziu reduções significativas na fosfatase alcalina sérica, bem como nos marcadores urinários de degradação do colágeno ósseo. Como resultado da inibição da reabsorção óssea, FOSAMAX induziu reduções geralmente leves, transitórias e assintomáticas no cálcio e fosfato séricos.
Farmacocinética
Absorção
Em relação a uma dose de referência intravenosa, a biodisponibilidade oral média do alendronato em mulheres foi de 0,64% para doses variando de 5 a 70 mg quando administrado após jejum noturno e duas horas antes de um café da manhã padronizado. A biodisponibilidade oral do comprimido de 10 mg em homens (0,59%) foi semelhante à das mulheres quando administrado após jejum noturno e 2 horas antes do café da manhã.
FOSAMAX 70 mg solução oral e FOSAMAX 70 mg comprimido são igualmente biodisponíveis.
Um estudo que examinou o efeito do horário de uma refeição na biodisponibilidade do alendronato foi realizado em 49 mulheres na pós-menopausa. A biodisponibilidade foi diminuída (em aproximadamente 40%) quando 10 mg de alendronato foram administrados 0,5 ou 1 hora antes de um café da manhã padronizado, em comparação com a dosagem 2 horas antes de comer. Em estudos de tratamento e prevenção da osteoporose, o alendronato foi eficaz quando administrado pelo menos 30 minutos antes do café da manhã.
biodisponibilidade foi insignificante se o alendronato foi administrado com ou até duas horas após um café da manhã padronizado. A administração concomitante de alendronato com café ou suco de laranja reduziu a biodisponibilidade em aproximadamente 60%.
Distribuição
Estudos pré-clínicos (em ratos machos) mostram que o alendronato se distribui transitoriamente para os tecidos moles após a administração intravenosa de 1 mg/kg, mas é rapidamente redistribuído para o osso ou excretado na urina. O volume médio de distribuição no estado de equilíbrio, excluindo os ossos, é de pelo menos 28 L em humanos. As concentrações do fármaco no plasma após doses terapêuticas orais são muito baixas (menos de 5 ng/mL) para detecção analítica. A ligação às proteínas no plasma humano é de aproximadamente 78%.
Metabolismo
Não há evidências de que o alendronato seja metabolizado em animais ou humanos.
Excreção
Após uma dose intravenosa única de [14C]alendronato, aproximadamente 50% da radioatividade foi excretada na urina em 72 horas e pouca ou nenhuma radioatividade foi recuperada nas fezes. Após uma dose intravenosa única de 10 mg, a depuração renal do alendronato foi de 71 mL/min (64, 78; intervalo de confiança de 90% [IC]), e a depuração sistêmica não excedeu 200 mL/min. As concentrações plasmáticas caíram mais de 95% dentro de 6 horas após a administração intravenosa. A meia-vida terminal em humanos é estimada em mais de 10 anos, provavelmente refletindo a liberação de alendronato do esqueleto. Com base no exposto, estima-se que após 10 anos de tratamento oral com FOSAMAX (10 mg diários) a quantidade de alendronato liberada diariamente do esqueleto seja aproximadamente 25% daquela absorvida pelo trato gastrointestinal.
Populações Específicas
Gênero
A biodisponibilidade e a fração de uma dose intravenosa excretada na urina foram semelhantes em homens e mulheres.
Geriátrico
biodisponibilidade e a disposição (excreção urinária) foram semelhantes em pacientes idosos e jovens. Não é necessário ajuste de dose em pacientes idosos.
Corrida
As diferenças farmacocinéticas devido à raça não foram estudadas.
Insuficiência renal
Estudos pré-clínicos mostram que, em ratos com insuficiência renal, quantidades crescentes da droga estão presentes no plasma, rim, baço e tíbia. Em controles saudáveis, a droga que não é depositada no osso é rapidamente excretada na urina. Nenhuma evidência de saturação da absorção óssea foi encontrada após 3 semanas de administração com doses intravenosas cumulativas de 35 mg/kg em ratos machos jovens. Embora nenhum estudo farmacocinético formal de insuficiência renal tenha sido realizado em pacientes, é provável que, como em animais, a eliminação de alendronato via rim seja reduzida em pacientes com função renal comprometida. Portanto, um acúmulo um pouco maior de alendronato no osso pode ser esperado em pacientes com função renal comprometida.
Não é necessário ajuste de dose para pacientes com clearance de creatinina de 35 a 60 mL/min. FOSAMAX 35mg não é recomendado para pacientes com depuração de creatinina inferior a 35 mL/min devido à falta de experiência com alendronato na insuficiência renal.
Insuficiência hepática
Como há evidências de que o alendronato não é metabolizado ou excretado na bile, não foram realizados estudos em pacientes com insuficiência hepática. Não é necessário ajuste de dose.
Interações medicamentosas
A ranitidina intravenosa mostrou duplicar a biodisponibilidade do alendronato oral. O significado clínico desta biodisponibilidade aumentada e se aumentos semelhantes ocorrerão em pacientes que receberam antagonistas H2 orais é desconhecido.
Em indivíduos saudáveis, a prednisona oral (20 mg três vezes ao dia durante cinco dias) não produziu uma alteração clinicamente significativa na biodisponibilidade oral do alendronato (um aumento médio variando de 20 a 44%).
Produtos contendo cálcio e outros cátions multivalentes podem interferir na absorção do alendronato.
Toxicologia e/ou Farmacologia Animal
As atividades inibitórias relativas sobre a reabsorção óssea e mineralização de alendronato e etidronato foram comparadas no ensaio de Schenk, que se baseia no exame histológico das epífises de ratos em crescimento. Neste ensaio, a dose mais baixa de alendronato que interferiu na mineralização óssea (levando à osteomalácia) foi 6.000 vezes a dose antirreabsortiva. A proporção correspondente para o etidronato foi de um para um. Estes dados sugerem que é altamente improvável que o alendronato administrado em doses terapêuticas induza osteomalácia.
Estudos clínicos
Tratamento da osteoporose em mulheres na pós-menopausa
Dosagem Diária
eficácia de FOSAMAX 10 mg por dia foi avaliada em quatro ensaios clínicos. O Estudo 1, um estudo clínico americano de três anos, multicêntrico, duplo-cego, controlado por placebo, envolveu 478 pacientes com escore T de DMO igual ou inferior a menos 2,5 com ou sem fratura vertebral prévia; Estudo 2, um estudo clínico multinacional de três anos, multicêntrico, duplo-cego, controlado por placebo, envolveu 516 pacientes com escore T de DMO igual ou inferior a menos 2,5 com ou sem fratura vertebral prévia; Estudo 3, o Estudo de Três Anos do Ensaio de Intervenção em Fraturas (FIT), um estudo que envolveu 2.027 pacientes na pós-menopausa com pelo menos uma fratura vertebral na linha de base; e Estudo 4, o Estudo de Quatro Anos de FIT: um estudo que envolveu 4.432 pacientes na pós-menopausa com baixa massa óssea, mas sem fratura vertebral basal.
Efeito na incidência de fratura
Para avaliar os efeitos do FOSAMAX na incidência de fraturas vertebrais (detectadas por radiografia digitalizada; aproximadamente um terço destas foram clinicamente sintomáticas), os estudos dos EUA e Multinacionais foram combinados em uma análise que comparou placebo aos grupos de dosagem agrupados de FOSAMAX (5 ou 10 mg por três anos ou 20 mg por dois anos seguidos de 5 mg por um ano). Houve uma redução estatisticamente significativa na proporção de pacientes tratados com FOSAMAX 70mg apresentando uma ou mais novas fraturas vertebrais em relação aos tratados com placebo (3,2% vs. 6,2%; uma redução de risco relativo de 48%). Uma redução no número total de novas fraturas vertebrais (4,2 vs. 11,3 por 100 pacientes) também foi observada. Na análise conjunta, os pacientes que receberam FOSAMAX tiveram uma perda de estatura estatisticamente significativamente menor do que a observada naqueles que receberam placebo (-3,0 mm vs. -4,6 mm).
Fracture Intervention Trial (FIT) consistiu em dois estudos em mulheres na pós-menopausa: o estudo de três anos de pacientes que tiveram pelo menos uma fratura vertebral radiográfica basal e o estudo de quatro anos de pacientes com baixa massa óssea, mas sem fratura vertebral basal. Em ambos os estudos de FIT, 96% dos pacientes randomizados completaram os estudos (ou seja, tiveram uma visita de encerramento no final programado do estudo); aproximadamente 80% dos pacientes ainda estavam tomando a medicação do estudo após a conclusão.
Fracture Intervention Trial: Estudo de três anos (pacientes com pelo menos uma fratura vertebral radiográfica de base)
Este estudo randomizado, duplo-cego, controlado por placebo, com 2.027 pacientes (FOSAMAX 70mg, n=1.022; placebo, n=1.005) demonstrou que o tratamento com FOSAMAX resultou em reduções estatisticamente significativas na incidência de fraturas em três anos, conforme mostrado na Tabela 6 .
Além disso, nesta população de pacientes com fratura vertebral basal, o tratamento com FOSAMAX reduziu significativamente a incidência de hospitalizações (25,0% vs. 30,7%).
No Estudo de Três Anos de FIT, fraturas do quadril ocorreram em 22 (2,2%) de 1.005 pacientes com placebo e 11 (1,1%) de 1.022 pacientes com FOSAMAX, p=0,047. A Figura 1 mostra a incidência cumulativa de fraturas de quadril neste estudo.
Figura 1: Incidência cumulativa de fraturas de quadril no estudo de três anos de FIT (pacientes com fratura vertebral radiográfica na linha de base)
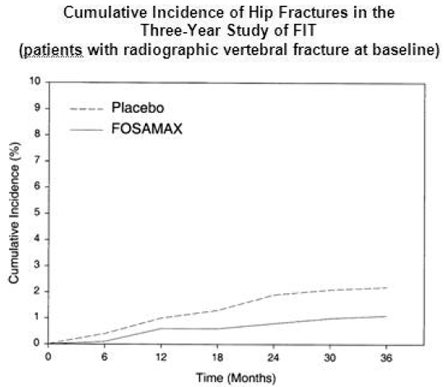
Ensaio de intervenção em fraturas: estudo de quatro anos (pacientes com baixa massa óssea, mas sem fratura vertebral radiográfica basal)
Este estudo randomizado, duplo-cego, controlado por placebo, com 4.432 pacientes (FOSAMAX 70mg, n=2.214; placebo, n=2.218) investigou ainda mais a redução na incidência de fraturas devido ao FOSAMAX. A intenção do estudo foi recrutar mulheres com osteoporose, definida como uma DMO basal do colo do fêmur pelo menos dois desvios padrão abaixo da média para mulheres adultas jovens. No entanto, devido a revisões subsequentes dos valores normativos para a DMO do colo do fêmur, 31% dos pacientes não preencheram esse critério de entrada e, portanto, este estudo incluiu mulheres osteoporóticas e não osteoporóticas. Os resultados são apresentados na Tabela 7 para os pacientes com osteoporose.
Resultados de fraturas em estudos
No Estudo de Três Anos de FIT, FOSAMAX 35mg reduziu a porcentagem de mulheres com pelo menos uma nova fratura vertebral radiográfica de 15,0% para 7,9% (47% de redução do risco relativo, p
O FOSAMAX reduziu a porcentagem de mulheres com múltiplas (duas ou mais) novas fraturas vertebrais de 4,2% para 0,6% (87% de redução do risco relativo, p
Assim, FOSAMAX 35mg reduziu a incidência de fraturas vertebrais radiográficas em mulheres com osteoporose, independentemente de terem ou não uma fratura vertebral radiográfica prévia.
Efeito na densidade mineral óssea
A eficácia da densidade mineral óssea de FOSAMAX 10 mg uma vez ao dia em mulheres na pós-menopausa, de 44 a 84 anos de idade, com osteoporose (densidade mineral óssea da coluna lombar [DMO] de pelo menos 2 desvios padrão abaixo da média da pré-menopausa) foi demonstrada em quatro estudos clínicos cegos, controlados por placebo de dois ou três anos' duração.
A Figura 2 mostra os aumentos médios na DMO da coluna lombar, colo do fêmur e trocânter em pacientes que receberam FOSAMAX 10 mg/dia em relação aos pacientes tratados com placebo em três anos para cada um desses estudos.
Figura 2: Estudos de Tratamento da Osteoporose em Mulheres na Pós-menopausa Aumento da DMO FOSAMAX 10mg/dia em Três Anos
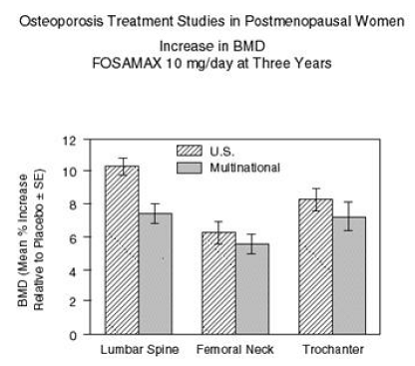
Em três anos, aumentos significativos na DMO, em relação à linha de base e ao placebo, foram observados em cada local de medição em cada estudo em pacientes que receberam FOSAMAX 10 mg/dia. A DMO corporal total também aumentou significativamente em cada estudo, sugerindo que os aumentos na massa óssea da coluna e do quadril não ocorreram às custas de outros locais do esqueleto. Os aumentos na DMO foram evidentes já aos três meses e continuaram ao longo dos três anos de tratamento. (Consulte a Figura 3 para resultados da coluna lombar.) Na extensão de dois anos desses estudos, o tratamento de 147 pacientes com FOSAMAX 10 mg/dia resultou em aumentos contínuos da DMO na coluna lombar e no trocânter (aumentos adicionais absolutos entre os anos 3 e 5: coluna lombar, 0,94%; trocânter, 0,88%). A DMO no colo do fêmur, antebraço e corpo total foram mantidos. FOSAMAX foi igualmente eficaz, independentemente da idade, raça, taxa basal de remodelação óssea e DMO basal na faixa estudada (pelo menos 2 desvios padrão abaixo da média pré-menopausa).
Figura 3: Estudos de tratamento de osteoporose em mulheres na pós-menopausa Curso de tempo do efeito de FOSAMAX 10mg/dia versus placebo: alteração percentual da DMO da coluna lombar em relação à linha de base
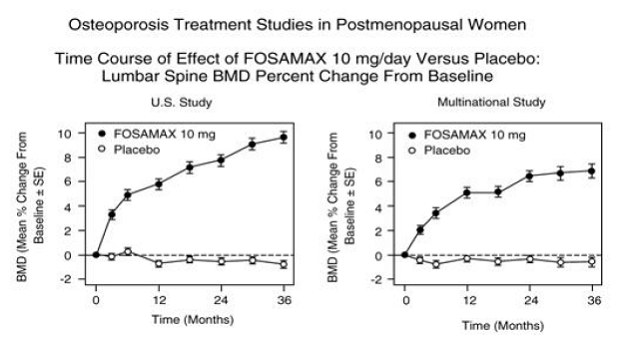
Em pacientes com osteoporose pós-menopausa tratadas com FOSAMAX 10 mg/dia por um ou dois anos, os efeitos da retirada do tratamento foram avaliados. Após a descontinuação, não houve aumentos adicionais na massa óssea e as taxas de perda óssea foram semelhantes às dos grupos placebo.
Histologia Óssea
histologia óssea em 270 pacientes na pós-menopausa com osteoporose tratadas com FOSAMAX em doses variando de 1 a 20 mg/dia por um, dois ou três anos revelou mineralização e estrutura normais, bem como a diminuição esperada na renovação óssea em relação ao placebo. Esses dados, juntamente com a histologia óssea normal e o aumento da resistência óssea observados em ratos e babuínos expostos a tratamento prolongado com alendronato, sustentam a conclusão de que o osso formado durante a terapia com FOSAMAX 35mg é de qualidade normal.
Efeito na altura
FOSAMAX, durante um período de três ou quatro anos, foi associado a reduções estatisticamente significativas na perda de altura versus placebo em pacientes com e sem fraturas vertebrais radiográficas basais. No final dos estudos FIT, as diferenças entre os grupos de tratamento foram de 3,2 mm no estudo de três anos e de 1,3 mm no estudo de quatro anos.
Dosagem Semanal
equivalência terapêutica de FOSAMAX 70 mg uma vez por semana (n=519) e FOSAMAX 10 mg por dia (n=370) foi demonstrada em um estudo multicêntrico, duplo-cego, de um ano de mulheres na pós-menopausa com osteoporose. Na análise primária dos concluintes, os aumentos médios da linha de base na DMO da coluna lombar em um ano foram de 5,1% (4,8, 5,4%; 95% CI) no grupo de 70 mg uma vez por semana (n = 440) e 5,4% ( 5,0, 5,8%; IC 95%) no grupo de 10 mg por dia (n=330). Os dois grupos de tratamento também foram semelhantes em relação aos aumentos da DMO em outros locais do esqueleto. Os resultados da análise de intenção de tratar foram consistentes com a análise primária dos concluintes.
Uso concomitante com terapia de reposição hormonal/estrogênica (TRH)
Os efeitos na DMO do tratamento com FOSAMAX 10 mg uma vez ao dia e estrogênio conjugado (0,625 mg/dia) isoladamente ou em combinação foram avaliados em um estudo de dois anos, duplo-cego, controlado por placebo em mulheres osteoporóticas histerectomizadas na pós-menopausa (n= 425). Em dois anos, os aumentos na DMO da coluna lombar a partir da linha de base foram significativamente maiores com a combinação (8,3%) do que com estrogênio ou FOSAMAX sozinho (ambos 6,0%).
Os efeitos na DMO quando FOSAMAX 35mg foi adicionado a doses estáveis (por pelo menos um ano) de TRH (estrogênio ± progestina) foram avaliados em um estudo duplo-cego, controlado por placebo, de um ano em mulheres pós-menopáusicas com osteoporose (n=428). A adição de FOSAMAX 10 mg uma vez ao dia à TRH produziu, em um ano, aumentos significativamente maiores na DMO da coluna lombar (3,7%) versus TRH isolada (1,1%).
Nesses estudos, aumentos significativos ou tendências favoráveis na DMO para terapia combinada em comparação com TRH isolada foram observados no quadril total, colo do fêmur e trocanter. Nenhum efeito significativo foi observado para a DMO corporal total.
Estudos histomorfométricos de biópsias transilíacas em 92 indivíduos mostraram arquitetura óssea normal. Comparado ao placebo, houve uma supressão de 98% da renovação óssea (avaliada pela superfície de mineralização) após 18 meses de tratamento combinado com FOSAMAX 35mg e TRH, 94% com FOSAMAX 35mg isolado e 78% com TRH isolado. Os efeitos a longo prazo da combinação de FOSAMAX 35mg e TRH na ocorrência e consolidação de fraturas não foram estudados.
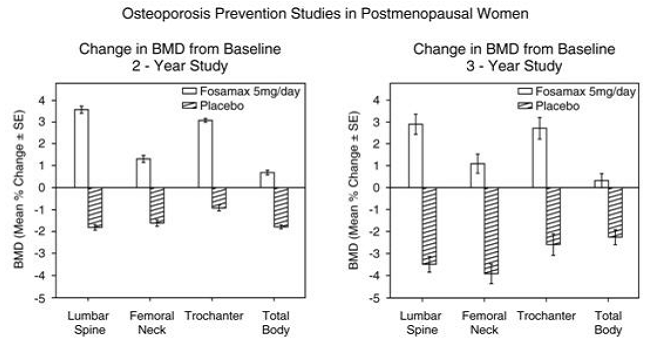
Prevenção da osteoporose em mulheres na pós-menopausa
Dosagem Diária
prevenção da perda óssea foi demonstrada em dois estudos duplo-cegos, controlados por placebo, em mulheres na pós-menopausa com 40-60 anos de idade. Mil e seiscentos e nove pacientes (FOSAMAX 5 mg/dia; n=498) que estavam pelo menos seis meses na pós-menopausa foram incluídos em um estudo de dois anos sem levar em consideração sua DMO basal. No outro estudo, 447 pacientes (FOSAMAX 5 mg/dia; n=88), que estavam entre seis meses e três anos de pós-menopausa, foram tratadas por até três anos. Nos pacientes tratados com placebo, foram observadas perdas de DMO de aproximadamente 1% ao ano na coluna, quadril (colo femoral e trocânter) e corpo total. Em contraste, FOSAMAX 5 mg/dia preveniu a perda óssea na maioria dos pacientes e induziu aumentos significativos na massa óssea média em cada um desses locais (ver Figura 4). Além disso, FOSAMAX 5 mg/dia reduziu a taxa de perda óssea no antebraço em aproximadamente metade em relação ao placebo. FOSAMAX 5 mg/dia foi igualmente eficaz nesta população, independentemente da idade, tempo desde a menopausa, raça e taxa basal de remodelação óssea.
Figura 4: Estudos de prevenção da osteoporose em mulheres na pós-menopausa
Histologia Óssea
A histologia óssea foi normal nos 28 pacientes biopsiados ao final de três anos que receberam FOSAMAX em doses de até 10 mg/dia.
Dosagem Semanal
A equivalência terapêutica de FOSAMAX 35 mg uma vez por semana (n=362) e FOSAMAX 5 mg diariamente (n=361) foi demonstrada em um estudo multicêntrico, duplo-cego, de um ano de mulheres na pós-menopausa sem osteoporose. Na análise primária dos concluintes, os aumentos médios da linha de base na DMO da coluna lombar em um ano foram de 2,9% (2,6, 3,2%; 95% CI) no grupo de 35 mg uma vez por semana (n = 307) e 3,2% ( 2,9, 3,5%; IC 95%) no grupo de 5 mg por dia (n=298). Os dois grupos de tratamento também foram semelhantes em relação aos aumentos da DMO em outros locais do esqueleto. Os resultados da análise de intenção de tratar foram consistentes com a análise primária dos concluintes.
Tratamento para aumentar a massa óssea em homens com osteoporose
A eficácia de FOSAMAX 35mg em homens com osteoporose hipogonadal ou idiopática foi demonstrada em dois estudos clínicos.
Dosagem Diária
Um estudo multicêntrico, duplo-cego, controlado por placebo, de dois anos, de FOSAMAX 10 mg uma vez ao dia, envolveu um total de 241 homens com idades entre 31 e 87 (média, 63). Todos os pacientes do estudo tinham um escore T de DMO menor ou igual a -2 no colo do fêmur e menor ou igual a -1 na coluna lombar, ou uma fratura osteoporótica basal e um escore T de DMO menor ou igual a -1 no colo do fêmur. Em dois anos, os aumentos médios em relação ao placebo na DMO em homens recebendo FOSAMAX 10 mg/dia foram significativos nos seguintes locais: coluna lombar, 5,3%; colo do fêmur, 2,6%; trocanter, 3,1%; e corpo total, 1,6%. O tratamento com FOSAMAX 70mg também reduziu a perda de altura (FOSAMAX, -0,6 mm vs. placebo, -2,4 mm).
Dosagem Semanal
Um estudo multicêntrico, duplo-cego, controlado por placebo, de um ano de duração de FOSAMAX 70 mg uma vez por semana envolveu um total de 167 homens com idades entre 38 e 91 (média, 66). Os pacientes do estudo tinham um escore T de DMO menor ou igual a -2 no colo do fêmur e menor ou igual a -1 na coluna lombar, ou um escore T de DMO menor ou igual a -2 no coluna lombar e menor ou igual a -1 no colo do fêmur, ou uma fratura osteoporótica basal e um escore T de DMO menor ou igual a -1 no colo do fêmur. Em um ano, os aumentos médios em relação ao placebo na DMO em homens recebendo FOSAMAX 70 mg uma vez por semana foram significativos nos seguintes locais: coluna lombar, 2,8%; colo do fêmur, 1,9%; trocanter, 2,0%; e corpo total, 1,2%. Esses aumentos na DMO foram semelhantes aos observados em um ano no estudo de 10 mg uma vez ao dia.
Em ambos os estudos, as respostas da DMO foram semelhantes independentemente da idade (maior ou igual a 65 anos vs. menor que 65 anos), função gonadal (testosterona basal menor que 9 ng/dL vs. maior ou igual a 9 ng/dL) , ou DMO de base (colo do fêmur e coluna lombar T-score menor ou igual a -2,5 vs. maior que -2,5).
Tratamento da osteoporose induzida por glicocorticóides
eficácia de FOSAMAX 5 e 10 mg uma vez ao dia em homens e mulheres recebendo glicocorticóides (pelo menos 7,5 mg/dia de prednisona ou equivalente) foi demonstrada em dois estudos multicêntricos, duplo-cegos, randomizados, controlados por placebo, com duração de um ano. desenho virtualmente idêntico, um realizado nos Estados Unidos e outro em 15 países diferentes (Multinacional [que também incluiu FOSAMAX 2,5 mg/dia]). Esses estudos incluíram 232 e 328 pacientes, respectivamente, com idades entre 17 e 83 anos com uma variedade de doenças que requerem glicocorticóides. Os pacientes receberam suplementos de cálcio e vitamina D. A Figura 5 mostra os aumentos médios em relação ao placebo na DMO da coluna lombar, colo do fêmur e trocânter em pacientes que receberam FOSAMAX 5 mg/dia para cada estudo.
Figura 5: Estudos em Pacientes Tratados com Glicocorticóides Aumento da DMO FOSAMAX 5 mg/dia em Um Ano
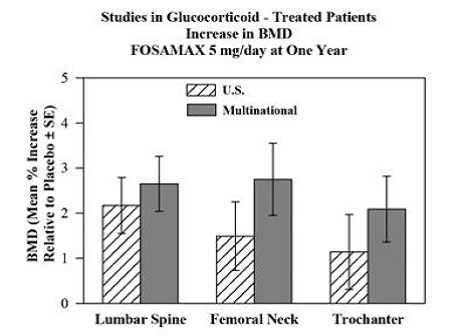
Após um ano, aumentos significativos em relação ao placebo na DMO foram observados nos estudos combinados em cada um desses locais em pacientes que receberam FOSAMAX 5 mg/dia. Nos pacientes tratados com placebo, ocorreu uma diminuição significativa na DMO no colo do fêmur (-1,2%), e diminuições menores foram observadas na coluna lombar e no trocânter. A DMO corporal total foi mantida com FOSAMAX 5 mg/dia. Os aumentos na DMO com FOSAMAX 10 mg/dia foram semelhantes àqueles com FOSAMAX 5 mg/dia em todas as pacientes, exceto para mulheres na pós-menopausa que não receberam terapia com estrogênio. Nessas mulheres, os aumentos (relativos ao placebo) com FOSAMAX 10 mg/dia foram maiores do que aqueles com FOSAMAX 5 mg/dia na coluna lombar (4,1% vs. 1,6%) e trocânter (2,8% vs. 1,7%). mas não em outros sites. FOSAMAX 35mg foi eficaz independentemente da dose ou duração do uso de glicocorticóide. Além disso, FOSAMAX foi igualmente eficaz independentemente da idade (menos de 65 vs. maior ou igual a 65 anos), raça (caucasiana vs. outras raças), sexo, doença subjacente, DMO basal, remodelação óssea basal e uso com um variedade de medicamentos comuns.
histologia óssea foi normal nos 49 pacientes biopsiados ao final de um ano que receberam FOSAMAX em doses de até 10 mg/dia.
Dos 560 pacientes originais nestes estudos, 208 pacientes que permaneceram com pelo menos 7,5 mg/dia de prednisona ou equivalente continuaram em uma extensão duplo-cega de um ano. Após dois anos de tratamento, a DMO da coluna aumentou 3,7% e 5,0% em relação ao placebo com FOSAMAX 5 e 10 mg/dia, respectivamente. Aumentos significativos na DMO (em relação ao placebo) também foram observados no colo do fêmur, trocânter e corpo total.
Após um ano, 2,3% dos pacientes tratados com FOSAMAX 5 ou 10 mg/dia (em conjunto) versus 3,7% daqueles tratados com placebo apresentaram uma nova fratura vertebral (não significativa). No entanto, na população estudada por dois anos, o tratamento com FOSAMAX (grupos de dosagem combinados: 5 ou 10 mg por dois anos ou 2,5 mg por um ano seguido de 10 mg por um ano) reduziu significativamente a incidência de pacientes com uma nova fratura vertebral (FOSAMAX 0,7% vs. placebo 6,8%).
Tratamento da doença óssea de Paget
eficácia de FOSAMAX 40 mg uma vez ao dia durante seis meses foi demonstrada em dois estudos clínicos duplo-cegos de pacientes do sexo masculino e feminino com doença de Paget moderada a grave (fosfatase alcalina pelo menos duas vezes o limite superior do normal): um placebo -estudo multinacional controlado e estudo comparativo americano com etidronato dissódico 400 mg/dia. A Figura 6 mostra as alterações percentuais médias da linha de base na fosfatase alcalina sérica por até seis meses de tratamento randomizado.
Figura 6: Estudos na Doença de Paget do Efeito Ósseo na Fosfatase Alcalina Sérica de FOSAMAX 40mg/dia versus Placebo ou Etidronato 400mg/dia
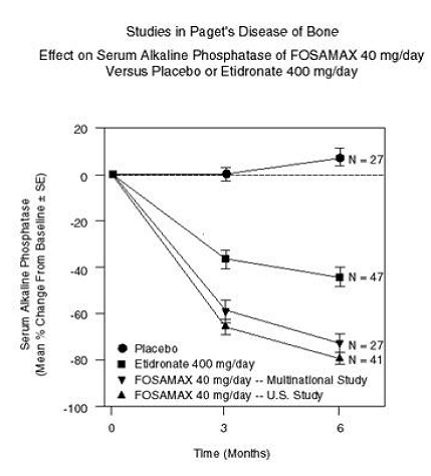
Aos seis meses, a supressão da fosfatase alcalina em pacientes tratados com FOSAMAX foi significativamente maior do que a alcançada com etidronato e contrastou com a completa ausência de resposta em pacientes tratados com placebo. A resposta (definida como normalização da fosfatase alcalina sérica ou diminuição da linha de base maior ou igual a 60%) ocorreu em aproximadamente 85% dos pacientes tratados com FOSAMAX nos estudos combinados versus 30% no grupo etidronato e 0% no placebo grupo. FOSAMAX 70mg foi igualmente eficaz, independentemente da idade, sexo, raça, uso prévio de outros bisfosfonatos ou fosfatase alcalina basal dentro da faixa estudada (pelo menos duas vezes o limite superior do normal).
A histologia óssea foi avaliada em 33 pacientes com doença de Paget tratados com FOSAMAX 40 mg/dia por 6 meses. Como em pacientes tratados para osteoporose [ver Estudos clínicos ], FOSAMAX não prejudicou a mineralização e observou-se a diminuição esperada na taxa de remodelação óssea. O osso lamelar normal foi produzido durante o tratamento com FOSAMAX, mesmo onde o osso preexistente foi tecido e desorganizado. Em geral, os dados de histologia óssea suportam a conclusão de que o osso formado durante o tratamento com FOSAMAX 35mg é de qualidade normal.
INFORMAÇÃO DO PACIENTE
FOSAMAX® (FOSS-ah-max)(alendronato de sódio) Comprimidos
Leia o Guia de Medicação que acompanha o FOSAMAX 70mg antes de começar a tomá-lo e sempre que receber um refil. Pode haver novas informações. Este Guia de Medicação não substitui a conversa com seu médico sobre sua condição médica ou tratamento. Fale com o seu médico se tiver alguma dúvida sobre FOSAMAX.
Qual é a informação mais importante que devo saber sobre FOSAMAX 70mg?
FOSAMAX 70mg pode causar efeitos colaterais graves, incluindo:
1. Problemas de esôfago.
Algumas pessoas que tomam FOSAMAX 35mg podem desenvolver problemas no esôfago (o tubo que conecta a boca e o estômago).
Esses problemas incluem irritação, inflamação ou úlceras do esôfago que às vezes podem sangrar.
- É importante que você tome FOSAMAX 70mg exatamente como prescrito para ajudar a diminuir sua chance de ter problemas de esôfago. (Consulte a seção “Como devo tomar FOSAMAX?”)
- Pare de tomar FOSAMAX e chame seu médico imediatamente se sentir dor no peito, azia nova ou agravada, ou tiver problemas ou dor ao engolir.
2. Níveis baixos de cálcio no sangue (hipocalcemia).
FOSAMAX pode diminuir os níveis de cálcio no sangue. Se você tiver níveis baixos de cálcio no sangue antes de começar a tomar FOSAMAX, isso pode piorar durante o tratamento. Seu baixo nível de cálcio no sangue deve ser tratado antes de você tomar FOSAMAX. A maioria das pessoas com níveis baixos de cálcio no sangue não apresenta sintomas, mas algumas pessoas podem apresentar sintomas. Ligue para o seu médico imediatamente se tiver sintomas de baixo nível de cálcio no sangue, tais como:
- Espasmos, espasmos ou cãibras nos músculos
- Dormência ou formigamento nos dedos das mãos, dedos dos pés ou ao redor da boca
Seu médico pode prescrever cálcio e vitamina D para ajudar a prevenir níveis baixos de cálcio no sangue, enquanto você toma FOSAMAX. Tome cálcio e vitamina D como seu médico lhe disser.
3. Dores ósseas, articulares ou musculares.
Algumas pessoas que tomam FOSAMAX desenvolvem dores ósseas, articulares ou musculares graves.
4. Problemas graves nos ossos da mandíbula (osteonecrose).
Problemas graves nos ossos da mandíbula podem ocorrer quando você toma FOSAMAX. Seu médico deve examinar sua boca antes de iniciar FOSAMAX. O seu médico pode dizer-lhe para consultar o seu dentista antes de iniciar FOSAMAX. É importante que você pratique bons cuidados com a boca durante o tratamento com FOSAMAX.
5. Fraturas incomuns do osso da coxa.
Algumas pessoas desenvolveram fraturas incomuns no osso da coxa. Os sintomas de uma fratura podem incluir dor nova ou incomum no quadril, virilha ou coxa.
Ligue para o seu médico imediatamente se tiver algum destes efeitos secundários.
O que é FOSAMAX 70mg?
- FOSAMAX 70mg é um medicamento de prescrição usado para:
- Tratar ou prevenir a osteoporose em mulheres após a menopausa. Ajuda a reduzir a chance de ter uma fratura do quadril ou da coluna vertebral (quebra).
- Aumentar a massa óssea em homens com osteoporose.
- Trate a osteoporose em homens ou mulheres que estejam tomando medicamentos corticosteróides.
Trate certos homens e mulheres que têm a doença óssea de Paget.
Não se sabe por quanto tempo FOSAMAX 70mg funciona para o tratamento e prevenção da osteoporose. Você deve consultar seu médico regularmente para determinar se FOSAMAX 70mg ainda é adequado para você.
FOSAMAX não é para uso em crianças.
Quem não deve tomar FOSAMAX 70mg?
Não tome FOSAMAX se você:
- Tem certos problemas com o esôfago, o tubo que conecta a boca ao estômago
- Não consegue ficar de pé ou sentado por pelo menos 30 minutos
- Tem baixos níveis de cálcio no sangue
- Tem alergia ao FOSAMAX 70mg ou a qualquer um de seus ingredientes. A lista de ingredientes encontra-se no final deste folheto.
O que devo dizer ao meu médico antes de tomar FOSAMAX 35mg?
Antes de iniciar FOSAMAX, certifique-se de falar com seu médico se você:
- Tem problemas com a deglutição
- Tem problemas estomacais ou digestivos
- Tem baixo cálcio no sangue
- Planeje fazer uma cirurgia dentária ou remover dentes
- Tem problemas renais
- Foi informado que você tem problemas para absorver minerais em seu estômago ou intestinos (síndrome de má absorção)
- Está grávida, tentando engravidar ou suspeita que está grávida. Se engravidar enquanto estiver a tomar FOSAMAX, pare de tomá-lo e contacte o seu médico. Não se sabe se FOSAMAX pode prejudicar o feto.
- Está amamentando ou planeja amamentar. Não se sabe se FOSAMAX passa para o leite e pode prejudicar o bebê.
Informe especialmente o seu médico se estiver a tomar:
- antiácidos
- aspirina
- Medicamentos anti-inflamatórios não esteroides (AINEs)
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos e não prescritos, vitaminas e suplementos de ervas. Certos medicamentos podem afetar o funcionamento de FOSAMAX 70mg.
Conheça os medicamentos que você toma. Mantenha uma lista deles e mostre-a ao seu médico e farmacêutico sempre que receber um novo medicamento.
Como devo tomar FOSAMAX 35mg?
- Tome FOSAMAX 35mg exatamente como indicado pelo seu médico.
- FOSAMAX funciona apenas se tomado com o estômago vazio.
- Tome FOSAMAX 35mg, depois de se levantar para o dia e antes de tomar sua primeira comida, bebida ou outro medicamento.
- Tome FOSAMAX enquanto estiver sentado ou em pé.
- Não mastigue ou chupe um comprimido de FOSAMAX.
- Engula o comprimido de FOSAMAX com um copo cheio (6-8 oz) de água pura.
- Não faça tome FOSAMAX com água mineral, café, chá, refrigerante ou suco.
- Se você tomar Alendronato Diariamente:
- Tome 1 comprimido de alendronato uma vez ao dia, todos os dias depois de se levantar e antes de tomar sua primeira comida, bebida ou outro medicamento.
- Se você tomar FOSAMAX uma vez por semana:
- Escolha o dia da semana que melhor se adapta à sua agenda.
- Tome 1 dose de FOSAMAX todas as semanas no dia escolhido depois de se levantar para o dia e antes de tomar sua primeira comida, bebida ou outro medicamento.
- Se você tomar Alendronato Diariamente:
Após engolir o comprimido de FOSAMAX 35mg, espere pelo menos 30 minutos:
- Antes de deitar. Você pode sentar, ficar de pé ou andar e fazer atividades normais, como ler.
- Antes de tomar sua primeira comida ou bebida, exceto água pura.
- Antes de tomar outros medicamentos, incluindo antiácidos, cálcio e outros suplementos e vitaminas.
Não se deite por pelo menos 30 minutos depois de tomar FOSAMAX e depois de comer sua primeira refeição do dia.
Se você esquecer de uma dose de FOSAMAX 70mg, não a tome no final do dia. Tome a dose esquecida na manhã seguinte depois de se lembrar e depois volte ao seu horário normal. Não tome 2 doses no mesmo dia.
Se você tomar muito FOSAMAX 70mg, ligue para o seu médico. Não tente vomitar. Não se deite.
Quais são os possíveis efeitos colaterais do FOSAMAX 70mg?
FOSAMAX pode causar efeitos colaterais graves.
- Consulte “Quais são as informações mais importantes que devo saber sobre o FOSAMAX?”
Os efeitos colaterais mais comuns de FOSAMAX 70mg são:
- Dor na área do estômago (abdominal)
- Azia
- Constipação
- Diarréia
- Dor de estômago
- Dor nos ossos, articulações ou músculos
- Náusea
Você pode ter reações alérgicas, como urticária ou inchaço do rosto, lábios, língua ou garganta.
Foi relatado o agravamento da asma.
Informe o seu médico se tiver algum efeito secundário que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do FOSAMAX. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar o FOSAMAX?
- Armazene FOSAMAX 35mg em temperatura ambiente, 59°F a 86°F (15°C a 30°C).
- Mantenha FOSAMAX em um recipiente bem fechado.
Mantenha FOSAMAX e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre o uso seguro e eficaz de FOSAMAX.
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use FOSAMAX 35mg para uma condição para a qual não foi prescrito. Não dê FOSAMAX 35mg a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Este Guia de Medicação resume as informações mais importantes sobre FOSAMAX. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre FOSAMAX escritas para profissionais de saúde. Para obter mais informações, acesse: www.FOSAMAX.com ou ligue para 1-800-622-4477 (ligação gratuita).
Quais são os ingredientes do FOSAMAX?
Princípio ativo: alendronato de sódio
Ingredientes inativos: celulose microcristalina, lactose anidra, croscarmelose sódica, estearato de magnésio.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
