Imodium 2mg Loperamide Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Imodium 2mg e como é usado?
Imodium 2mg é um medicamento de prescrição usado para tratar os sintomas de diarréia aguda, diarréia crônica e diarréia do viajante. Imodium pode ser usado sozinho ou com outros medicamentos.
Imodium pertence a uma classe de medicamentos chamados antidiarreicos.
Quais são os possíveis efeitos colaterais do Imodium?
Imodium pode causar efeitos colaterais graves, incluindo:
- diarreia aquosa ou sanguinolenta,
- dor de estômago ou inchaço,
- diarreia contínua ou agravada,
- batimentos cardíacos rápidos ou acelerados,
- vibrando em seu peito,
- falta de ar e
- tontura
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Imodium incluem:
- constipação,
- tontura,
- sonolência,
- náusea, e
- dores de estômago
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Imodium. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
IMODIUM® (cloridrato de loperamida), monocloridrato de 4-(p-clorofenil)-4-hidroxi-N,N-dimetil-a, a-difenil-1-piperidinabutiramida, é um antidiarreico sintético para uso oral.
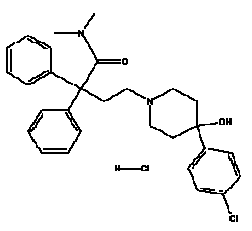
IMODIUM® (loperamida hcl) está disponível em cápsulas de 2mg.
Os ingredientes inativos são: Lactose, amido de milho, talco e estearato de magnésio. As cápsulas de IMODIUM® (loperamida hcl) contêm FD&C Yellow No. 6.
INDICAÇÕES
IMODIUM® (cloridrato de loperamida) é indicado para o controle e alívio sintomático da diarreia aguda inespecífica e da diarreia crônica associada à doença inflamatória intestinal. IMODIUM® (loperamida hcl) também é indicado para reduzir o volume de descarga de ileostomias.
DOSAGEM E ADMINISTRAÇÃO
(1 cápsula = 2 mg)
Os pacientes devem receber reposição adequada de fluidos e eletrólitos conforme necessário.
Diarréia Aguda
Adultos: dose inicial recomendada é de 4 mg (duas cápsulas) seguida de 2 mg (uma cápsula) após cada fezes não formadas. A dose diária não deve exceder 16mg (oito cápsulas). A melhora clínica geralmente é observada em 48 horas.
Crianças: Em crianças de 2 a 5 anos de idade (20 kg ou menos), a formulação líquida sem prescrição (IMODIUM® (loperamida hcl) AD 1 mg/5 mL) deve ser usada; para idades de 6 a 12 anos, podem ser usadas cápsulas de IMODIUM® (loperamida hcl) ou IMODIUM® (loperamida hcl) AD Liquid. Para crianças de 2 a 12 anos de idade, o seguinte esquema para cápsulas ou líquido geralmente atende aos requisitos iniciais de dosagem:
Cronograma de dosagem recomendado para o primeiro dia
Dois a cinco anos: 1 mg três vezes ao dia (dose diária de 3 mg) (13 a 20 kg) Seis a oito anos: 2 mg duas vezes ao dia (dose diária de 4 mg) (20 a 30 kg) Oito a doze anos: 2 mg três vezes ao dia (dose diária de 6 mg) (superior a 30 kg )
Dose Diária Subseqüente Recomendada
Após o primeiro dia de tratamento, recomenda-se que as doses subsequentes de IMODIUM® (loperamida hcl) (1 mg/10 kg de peso corporal) sejam administradas somente após fezes moles. A dosagem diária total não deve exceder as dosagens recomendadas para o primeiro dia.
Diarréia crônica
Crianças: Embora IMODIUM® (loperamida hcl) tenha sido estudado em um número limitado de crianças com diarreia crônica; a dose terapêutica para o tratamento da diarreia crônica em uma população pediátrica não foi estabelecida.
Adultos: A dose inicial recomendada é de 4 mg (duas cápsulas) seguida de 2 mg (uma cápsula) após cada fezes não formadas até que a diarreia seja controlada, após o que a dosagem de IMODIUM® (loperamida hcl) deve ser reduzida para atender às necessidades individuais. Quando a dosagem diária ótima for estabelecida, esta quantidade pode então ser administrada como uma dose única ou em doses divididas.
dose média diária de manutenção em ensaios clínicos foi de 4 a 8 mg (duas a quatro cápsulas). Uma dosagem de 16 mg (oito cápsulas) raramente foi excedida. Se a melhora clínica não for observada após o tratamento com 16 mg por dia por pelo menos 10 dias, é improvável que os sintomas sejam controlados por administração adicional. A administração de IMODIUM® (loperamida hcl) pode ser continuada se a diarreia não puder ser adequadamente controlada com dieta ou tratamento específico.
Crianças menores de 2 anos
O uso de IMODIUM (loperamida hcl) em crianças menores de 2 anos não é recomendado. Houve relatos raros de íleo paralítico associado à distensão abdominal. A maioria desses relatos ocorreu no contexto de disenteria aguda, overdose e com crianças muito pequenas com menos de dois anos de idade.
Idoso
Não foram realizados estudos farmacocinéticos formais em indivíduos idosos. No entanto, não houve grandes diferenças relatadas na disposição do medicamento em pacientes idosos com diarreia em relação a pacientes jovens. Não é necessário ajuste de dose para idosos.
Insuficiência renal
Não há dados farmacocinéticos disponíveis em pacientes com insuficiência renal. Uma vez que os metabólitos e o fármaco inalterado são excretados principalmente nas fezes, não é necessário ajuste de dose para pacientes com insuficiência renal. seção PRECAUÇÕES ).
Insuficiência hepática
Embora não haja dados farmacocinéticos disponíveis em pacientes com insuficiência hepática, IMODIUM (loperamida hcl) deve ser usado com cautela nesses pacientes devido à redução do metabolismo de primeira passagem. (Vejo PRECAUÇÕES ).
COMO FORNECIDO
Cápsulas - cada cápsula contém 2 mg de cloridrato de loperamida. As cápsulas têm um corpo verde claro e uma tampa verde escura com "JANSSEN" impresso em um segmento e "IMODIUM" no outro segmento. As cápsulas de IMODIUM® (loperamida hcl) são fornecidas em frascos de 100.
NDC 50458-400-10.........(100 CÁPSULAS)
Armazenar a 15°-25°C (59°-77°F).
Janssen Pharmaceutica Inc. Revisado em setembro de 1996, julho de 1998. Data de revisão da FDA: 21/10/2005
EFEITOS COLATERAIS
Dados de Ensaios Clínicos
Os efeitos adversos relatados durante as investigações clínicas de IMODIUM® (cloridrato de loperamida) são difíceis de distinguir dos sintomas associados à síndrome diarreica. As experiências adversas registradas durante os estudos clínicos com IMODIUM® (loperamida hcl) foram geralmente de natureza menor e autolimitada. Eles foram mais comumente observados durante o tratamento de diarréia crônica.
Os eventos adversos relatados são resumidos independentemente da avaliação de causalidade dos investigadores.
1) Eventos adversos de 4 estudos controlados com placebo em pacientes com diarreia aguda Os eventos adversos com incidência de 1,0% ou mais, que foram relatados com pelo menos a mesma frequência em pacientes que receberam cloridrato de loperamida como placebo, são apresentados na tabela abaixo.
Os eventos adversos com incidência de 1,0% ou mais, que foram relatados com mais frequência em pacientes com placebo do que com cloridrato de loperamida, foram: boca seca, flatulência, cólica abdominal e cólica.
2) Eventos adversos de 20 estudos controlados por placebo em pacientes com diarreia crônica
Os eventos adversos com incidência de 1,0% ou mais, que foram relatados com pelo menos a mesma frequência em pacientes que receberam cloridrato de loperamida como placebo, são apresentados abaixo na tabela abaixo.
Os eventos adversos com incidência de 1,0% ou mais, que foram relatados com mais frequência em pacientes com placebo do que com cloridrato de loperamida, foram: náusea, vômito, cefaleia, meteorismo, dor abdominal, cólica abdominal e cólica.
3) Eventos adversos de setenta e seis estudos controlados e não controlados em pacientes com diarreia aguda ou crônica
Os eventos adversos com incidência de 1,0% ou mais em pacientes de todos os estudos são apresentados na tabela abaixo.
Experiência pós-marketing
Os seguintes eventos adversos foram relatados:
Distúrbios da pele e tecido subcutâneo
Erupção cutânea, prurido, urticária, angioedema e casos extremamente raros de erupção bolhosa incluindo eritema multiforme, síndrome de Stevens-Johnson e necrólise epidérmica tóxica foram relatados com o uso de IMODIUM (loperamida hcl).
Distúrbios do sistema imunológico
Ocorrências isoladas de reações alérgicas e, em alguns casos, reações de hipersensibilidade graves, incluindo choque anafilático e reações anafilactóides, foram relatadas com o uso de IMODIUM (loperamida hcl).

Problemas gastrointestinais
Boca seca, dor abdominal, distensão ou desconforto, náusea, vômito, flatulência, dispepsia, constipação, íleo paralítico, megacólon, incluindo megacólon tóxico (ver CONTRA-INDICAÇÕES E ADVERTÊNCIAS ).
Distúrbios renais e urinários
Retenção urinária
Distúrbios do sistema nervoso
Sonolência, tontura
Distúrbios gerais e condições do local administrativo
Cansaço
Vários eventos adversos relatados durante as investigações clínicas e a experiência pós-comercialização com loperamida são sintomas frequentes da síndrome diarreica subjacente (dor/desconforto abdominal, náusea, vômito, boca seca, cansaço, sonolência, tontura, constipação e flatulência). . Estes sintomas são muitas vezes difíceis de distinguir dos efeitos indesejáveis das drogas.
Abuso e Dependência de Drogas
Abuso
Um estudo clínico específico projetado para avaliar o potencial de abuso da loperamida em altas doses resultou em um achado de potencial de abuso extremamente baixo.
Dependência
Estudos em macacos dependentes de morfina demonstraram que o cloridrato de loperamida em doses acima das recomendadas para humanos preveniu os sinais de abstinência de morfina. No entanto, em humanos, o teste pupilar de desafio com naloxona, que quando positivo indica efeitos opiáceos, realizado após uma única dose alta, ou após mais de dois anos de uso terapêutico de IMODIUM® (cloridrato de loperamida), foi negativo. O IMODIUM® administrado por via oral (loperamida hcl) (loperamida formulada com estearato de magnésio) é altamente insolúvel e penetra mal no SNC.
INTERAÇÕES MEDICAMENTOSAS
Dados não clínicos mostraram que a loperamida é um substrato da glicoproteína P. A administração concomitante de loperamida (dose única de 16 mg) com uma dose única de 600 mg de quinidina ou ritonavir, ambos inibidores da glicoproteína P, resultou em um aumento de 2 a 3 vezes nos níveis plasmáticos de loperamida. Devido ao potencial de efeitos centrais aumentados quando a loperamida é coadministrada com quinidina e ritonavir, deve-se ter cautela quando a loperamida é administrada nas dosagens recomendadas (2 mg, até 16 mg de dose máxima diária) com inibidores da glicoproteína-P.
Quando uma dose única de 16 mg de loperamida é coadministrada com uma dose única de 600 mg de saquinavir, a loperamida diminuiu a exposição ao saquinavir em 54%, o que pode ter relevância clínica devido à redução da eficácia terapêutica do saquinavir. O efeito do saquinavir na loperamida é de menor importância clínica. Portanto, quando a loperamida é administrada com saquinavir, a eficácia terapêutica do saquinavir deve ser monitorada de perto.
AVISOS
depleção de líquidos e eletrólitos geralmente ocorre em pacientes com diarreia. Nesses casos, a administração de fluidos e eletrólitos apropriados é muito importante. O uso de IMODIUM® (loperamida hcl) não exclui a necessidade de terapia adequada com fluidos e eletrólitos.
Em geral, IMODIUM (loperamida hcl) não deve ser usado quando a inibição do peristaltismo deve ser evitada devido ao possível risco de sequelas significativas, incluindo íleo, megacólon e megacólon tóxico. IMODIUM (loperamida hcl) deve ser descontinuado imediatamente quando ocorrer constipação, distensão abdominal ou íleo.
O tratamento da diarreia com IMODIUM (loperamida hcl) é apenas sintomático. Sempre que uma etiologia subjacente puder ser determinada, o tratamento específico deve ser administrado quando apropriado (ou quando indicado).
Pacientes com AIDS tratados com IMODIUM (loperamida hcl) para diarreia devem ter a terapia interrompida aos primeiros sinais de distensão abdominal. Houve relatos isolados de megacólon tóxico em pacientes com AIDS com colite infecciosa de patógenos virais e bacterianos tratados com cloridrato de loperamida. {ref. EDMS-PSDB-2564186, página 12}
IMODIUM® (loperamida hcl) deve ser usado com cuidado especial em crianças pequenas devido à maior variabilidade de resposta nessa faixa etária. A desidratação, particularmente em crianças mais novas, pode influenciar ainda mais a variabilidade da resposta ao IMODIUM® (loperamida hcl).
PRECAUÇÕES
Em geral
Reações alérgicas extremamente raras, incluindo anafilaxia e choque anafilático, foram relatadas. Na diarreia aguda, se não for observada melhora clínica em 48 horas, a administração de IMODIUM® (cloridrato de loperamida) deve ser descontinuada e os pacientes devem ser aconselhados a consultar seu médico. Embora não haja dados farmacocinéticos disponíveis em pacientes com insuficiência hepática, IMODIUM (loperamida hcl) deve ser usado com cautela nesses pacientes devido à redução do metabolismo de primeira passagem. Pacientes com disfunção hepática devem ser monitorados cuidadosamente quanto a sinais de toxicidade no SNC. Não há dados farmacocinéticos disponíveis em pacientes com insuficiência renal. Uma vez que foi relatado que a maior parte da droga é metabolizada e os metabólitos ou a droga inalterada são excretados principalmente nas fezes, não são necessários ajustes de dosagem em pacientes com insuficiência renal. Não foram realizados estudos formais para avaliar a farmacocinética da loperamida em indivíduos idosos. No entanto, em dois estudos que envolveram pacientes idosos, não houve grandes diferenças na disposição do medicamento em pacientes idosos com diarreia em relação a pacientes jovens.
Carcinogênese, mutagênese, comprometimento da fertilidade
Em um estudo de 18 meses em ratos com doses orais de até 40 mg/kg/dia (21 vezes a dose humana máxima de 16 mg/dia, com base na comparação da área de superfície corporal), não houve evidência de carcinogênese.
A loperamida não foi genotóxica no teste de Ames, no cromoteste SOS em E. coli, no teste letal dominante em camundongos fêmeas ou no ensaio de transformação de células embrionárias de camundongos.
fertilidade e o desempenho reprodutivo foram avaliados em ratos usando doses orais de 2,5, 10 e 40 mg/kg/dia em um estudo e 1, 5, 10, 20 e 40 mg/kg/dia (apenas fêmeas) em um segundo estudar. A administração oral de 20 mg/kg/dia (aproximadamente 11 vezes a dose humana com base na comparação da área de superfície corporal) e superior produziu forte comprometimento da fertilidade feminina. O tratamento de ratas com até 10 mg/kg/dia po (aproximadamente 5 vezes a dose humana com base na comparação da área de superfície corporal) não teve efeito sobre a fertilidade. O tratamento de ratos machos com 40 mg/kg/dia VO (aproximadamente 21 vezes a dose humana com base na comparação da área de superfície corporal) produziu diminuição da fertilidade masculina, enquanto a administração de até 10 mg/kg/dia (aproximadamente 5 vezes a dose humana dose com base em uma comparação da área de superfície corporal) não teve efeito.
Gravidez
Efeitos Teratogênicos Gravidez Categoria C
Estudos de teratologia foram realizados em ratos com doses orais de 2,5, 10 e 40 mg/kg/dia e em coelhos com doses orais de 5, 20 e 40 mg/kg/dia. Esses estudos não revelaram evidência de fertilidade prejudicada ou danos ao feto em doses de até 10 mg/kg/dia em ratos (5 vezes a dose humana com base na comparação da área de superfície corporal) e 40 mg/kg/dia em coelhos (43 vezes a dose humana com base na comparação da área de superfície corporal). O tratamento de ratos com 40 mg/kg/dia po (21 vezes a dose humana com base em uma comparação da área de superfície corporal) produziu uma diminuição acentuada da fertilidade. Os estudos não produziram evidência de atividade teratogênica. Não existem estudos adequados e bem controlados em mulheres grávidas. A loperamida deve ser usada durante a gravidez somente se o benefício potencial justificar o risco potencial para o feto.
Efeitos não teratogênicos
Em um estudo de reprodução peri e pós-natal em ratos, a administração oral de 40 mg/kg/dia produziu comprometimento do crescimento e sobrevivência da prole.
Mães que amamentam
Pequenas quantidades de loperamida podem aparecer no leite materno humano. Portanto, IMODIUM (loperamida hcl) não é recomendado durante a amamentação.
Uso Pediátrico
Veja o " AVISOS "Seção para informações sobre a maior variabilidade de resposta nessa faixa etária.
Em caso de superdosagem acidental de IMODIUM® por crianças, veja " SUPERDOSAGEM " Seção para tratamento sugerido.
SOBREDOSAGEM
Em casos de sobredosagem (incluindo sobredosagem relativa devido a disfunção hepática), podem ocorrer retenção urinária, íleo paralítico e depressão do SNC. As crianças podem ser mais sensíveis aos efeitos do SNC do que os adultos. Ensaios clínicos demonstraram que uma pasta de carvão ativado administrada imediatamente após a ingestão de cloridrato de loperamida pode reduzir a quantidade de droga que é absorvida na circulação sistêmica em até nove vezes. Se o vômito ocorrer espontaneamente após a ingestão, uma pasta de 100 g de carvão ativado deve ser administrada por via oral assim que os líquidos puderem ser retidos.
Se o vômito não ocorrer, deve-se realizar lavagem gástrica seguida da administração de 100 g da pasta de carvão ativado através do tubo gástrico. Em caso de superdosagem, os pacientes devem ser monitorados quanto a sinais de depressão do SNC por pelo menos 24 horas.
Se ocorrerem sintomas de sobredosagem, a naloxona pode ser administrada como antídoto. Se houver resposta à naloxona, os sinais vitais devem ser monitorados cuidadosamente quanto à recorrência dos sintomas de superdosagem do medicamento por pelo menos 24 horas após a última dose de naloxona.
Tendo em vista a ação prolongada da loperamida e a curta duração (uma a três horas) da naloxona, o paciente deve ser monitorado de perto e tratado repetidamente com naloxona conforme indicado. Uma vez que relativamente pouco fármaco é excretado na urina, não se espera que a diurese forçada seja eficaz na superdosagem de IMODIUM® (cloridrato de loperamida).
Em ensaios clínicos, um adulto que tomou três doses de 20 mg em um período de 24 horas sentiu náuseas após a segunda dose e vomitou após a terceira dose. Em estudos projetados para examinar o potencial de efeitos colaterais, a ingestão intencional de até 60 mg de cloridrato de loperamida em uma única dose em indivíduos saudáveis não resultou em efeitos adversos significativos.
CONTRA-INDICAÇÕES
IMODIUM (loperamida hcl) é contraindicado em pacientes com hipersensibilidade conhecida ao cloridrato de loperamida ou a qualquer um dos excipientes.
IMODIUM (loperamida hcl) é contraindicado em pacientes com dor abdominal na ausência de diarreia.
IMODIUM (loperamida hcl) não é recomendado em crianças com menos de 24 meses de idade.
IMODIUM (loperamida hcl) não deve ser usado como terapia primária:
- em pacientes com disenteria aguda, caracterizada por sangue nas fezes e febre alta,
- em doentes com colite ulcerosa aguda,
em pacientes com enterocolite bacteriana causada por organismos invasivos, incluindo Salmonella, Shigella e Campylobacter,
- em pacientes com colite pseudomembranosa associada ao uso de antibióticos de amplo espectro.
FARMACOLOGIA CLÍNICA
Estudos in vitro e em animais mostram que IMODIUM® (cloridrato de loperamida) atua diminuindo a motilidade intestinal e afetando o movimento da água e eletrólitos através do intestino. A loperamida liga-se ao receptor opiáceo na parede intestinal. Consequentemente, inibe a liberação de acetilcolina e prostaglandinas, reduzindo assim o peristaltismo e aumentando o tempo de trânsito intestinal. A loperamida aumenta o tônus do esfíncter anal, reduzindo assim a incontinência e a urgência.
No homem, IMODIUM® (loperamida hcl) prolonga o tempo de trânsito do conteúdo intestinal. Reduz o volume fecal diário, aumenta a viscosidade e a densidade aparente e diminui a perda de líquidos e eletrólitos. A tolerância ao efeito antidiarreico não foi observada. Estudos clínicos indicaram que a meia-vida de eliminação aparente da loperamida no homem é de 10,8 horas com um intervalo de 9,1 a 14,4 horas. Os níveis plasmáticos da droga inalterada permanecem abaixo de 2 nanogramas por mL após a ingestão de uma cápsula de 2mg de IMODIUM® (loperamida hcl). Os níveis plasmáticos são mais altos aproximadamente cinco horas após a administração da cápsula e 2,5 horas após o líquido. Os níveis plasmáticos de pico de loperamida foram semelhantes para ambas as formulações. A eliminação da loperamida ocorre principalmente por N-desmetilação oxidativa. Acredita-se que as isoenzimas do citocromo P450 (CYP450), CYP2C8 e CYP3A4, desempenham um papel importante no processo de N-desmetilação da loperamida, uma vez que a quercetina (inibidor do CYP2C8) e o cetoconazol (inibidor do CYP3A4) inibiram significativamente o processo de N-desmetilação in vitro em 40% e 90%. %, respectivamente. Além disso, CYP2B6 e CYP2D6 parecem desempenhar um papel menor na N-desmetilação da loperamida. A excreção da loperamida inalterada e seus metabólitos ocorre principalmente pelas fezes. Naqueles pacientes nos quais os parâmetros bioquímicos e hematológicos foram monitorados durante os ensaios clínicos, não foram observadas tendências de anormalidade durante a terapia com IMODIUM® (loperamida hcl). Da mesma forma, urinálise, eletrocardiograma e exames clínicos oftalmológicos não mostraram tendências de anormalidade.
INFORMAÇÃO DO PACIENTE
Os pacientes devem ser aconselhados a consultar seu médico se a diarreia não melhorar em 48 horas ou se notar sangue nas fezes, desenvolver febre ou distensão abdominal.
Cansaço, tontura ou sonolência podem ocorrer no contexto de síndromes diarréicas tratadas com IMODIUM (loperamida hcl). Portanto, é aconselhável ter cuidado ao dirigir um carro ou operar máquinas. (Vejo REAÇÕES ADVERSAS ).
