Pamelor 25mg Nortriptyline Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Pamelor 25mg e como é usado?
Pamelor 25mg é um medicamento de prescrição usado para tratar os sintomas da Depressão. Pamelor 25mg pode ser usado sozinho ou com outros medicamentos.
Pamelor pertence a uma classe de medicamentos chamados antidepressivos, TCAs.
Não se sabe se Pamelor é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Pamelor 25mg?
Pamelor pode causar efeitos colaterais graves, incluindo:
- mudanca de humor,
- ansiedade,
- ataques de pânico,
- problemas para dormir,
- comportamento impulsivo,
- irritabilidade,
- agitação,
- hostilidade,
- agressão,
- inquietação,
- hiperatividade (mental ou física),
- aumento da depressão,
- pensamentos sobre se machucar,
- visão embaçada,
- visão de túnel,
- dor ou inchaço nos olhos,
- vendo halos ao redor das luzes,
- movimentos musculares inquietos em seus olhos, língua, mandíbula ou pescoço,
- tontura,
- apreensão,
- dor no peito nova ou agravada,
- batimentos cardíacos acelerados,
- vibrando em seu peito,
- dormência ou fraqueza repentina,
- problemas de visão,
- dificuldade com a fala ou equilíbrio,
- febre,
- dor de garganta,
- contusões fáceis,
- sangramento incomum,
- amarelecimento da pele ou dos olhos (icterícia),
- micção dolorosa ou difícil,
- batimentos cardíacos rápidos,
- reflexos hiperativos,
- náusea,
- vômito,
- diarréia,
- perda de coordenação e
- desmaio
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Pamelor incluem:
- náusea,
- vômito,
- perda de apetite,
- ansiedade,
- problemas de sono (insônia),
- boca seca,
- sabor inusitado,
- pouca ou nenhuma urina,
- constipação,
- alterações na visão,
- inchaço da mama (em homens ou mulheres),
- diminuição do desejo sexual,
- impotência, e
- dificuldade em ter um orgasmo
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Pamelor. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
Suicídio e drogas antidepressivas
Os antidepressivos aumentaram o risco em comparação ao placebo de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens em estudos de curto prazo de transtorno depressivo maior (TDM) e outros transtornos psiquiátricos. Qualquer pessoa considerando o uso de cloridrato de nortriptilina ou qualquer outro antidepressivo em uma criança, adolescente ou adulto jovem deve equilibrar esse risco com a necessidade clínica. Estudos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução no risco com antidepressivos em comparação com placebo em adultos com 65 anos ou mais. A depressão e alguns outros transtornos psiquiátricos estão associados ao aumento do risco de suicídio. Pacientes de todas as idades que iniciam terapia antidepressiva devem ser monitorados adequadamente e observados de perto quanto a piora clínica, suicídio ou mudanças incomuns no comportamento. As famílias e os cuidadores devem ser avisados da necessidade de observação atenta e comunicação com o prescritor. O cloridrato de nortriptilina não está aprovado para uso em pacientes pediátricos (ver AVISOS Agravamento Clínico e Risco de Suicídio; INFORMAÇÃO DO PACIENTE ; e PRECAUÇÕES , Uso Pediátrico).
DESCRIÇÃO
Pamelor™ (nortriptilina HCl) é cloridrato de 1-propanamina, 3-(10,11-di-hidro-5H-dibenzo[a,d]ciclohepten-5-ilideno)-N-metil-.
A fórmula estrutural é a seguinte:
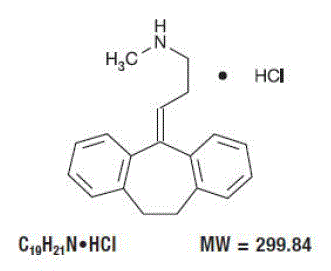
Cápsulas de 10 mg, 25 mg, 50 mg e 75 mg
Ingrediente ativo
cloridrato de nortriptilina USP.
Cápsulas de 10 mg, 25 mg e 75 mg
Ingredientes inativos
D&C Yellow #10, FD&C Yellow #6, gelatina, fluido de silicone, amido e dióxido de titânio.
Cápsulas de 50 mg
Ingredientes inativos
gelatina, fluido de silicone, amido e dióxido de titânio.
INDICAÇÕES
Pamelor™ (nortriptilina HCl) é indicado para o alívio dos sintomas de depressão. As depressões endógenas são mais propensas a serem aliviadas do que outros estados depressivos.
DOSAGEM E ADMINISTRAÇÃO
Pamelor 25mg não é recomendado para crianças.
Pamelor é administrado por via oral na forma de cápsulas. Doses inferiores às usuais são recomendadas para pacientes idosos e adolescentes. Doses mais baixas também são recomendadas para pacientes ambulatoriais do que para pacientes hospitalizados que estarão sob supervisão próxima. O médico deve iniciar a dosagem em um nível baixo e aumentá-la gradualmente, observando cuidadosamente a resposta clínica e qualquer evidência de intolerância. Após a remissão, a medicação de manutenção pode ser necessária por um longo período de tempo na dose mais baixa que manterá a remissão.
Se um paciente desenvolver efeitos colaterais menores, a dosagem deve ser reduzida. O medicamento deve ser descontinuado imediatamente se ocorrerem efeitos adversos de natureza grave ou manifestações alérgicas.
Dose adulta usual
25 mg três ou quatro vezes ao dia; a dosagem deve começar em um nível baixo e ser aumentada conforme necessário. Como regime alternativo, a dosagem diária total pode ser administrada uma vez ao dia. Quando são administradas doses diárias acima de 100 mg, os níveis plasmáticos de nortriptilina devem ser monitorados e mantidos na faixa ideal de 50 a 150 ng/mL. Doses acima de 150 mg/dia não são recomendadas.
Pacientes Idosos e Adolescentes
30 a 50 mg/dia, em doses divididas, ou a dose diária total pode ser administrada uma vez ao dia.
Troca de um paciente para ou de um inibidor da monoaminoxidase (IMAO) destinado a tratar distúrbios psiquiátricos
Devem decorrer pelo menos 14 dias entre a descontinuação de um IMAO destinado a tratar distúrbios psiquiátricos e o início da terapia com Pamelor. Por outro lado, pelo menos 14 dias devem ser permitidos após a interrupção do Pamelor antes de iniciar um IMAO destinado a tratar distúrbios psiquiátricos ( CONTRA-INDICAÇÕES ).
Uso de Pamelor 25mg com outros IMAOs, como linezolida ou azul de metileno
Não inicie Pamelor em um paciente que esteja sendo tratado com linezolida ou azul de metileno intravenoso porque há risco aumentado de síndrome serotoninérgica. Em um paciente que requer tratamento mais urgente de uma condição psiquiátrica, outras intervenções, incluindo hospitalização, devem ser consideradas (ver CONTRA-INDICAÇÕES ).
Em alguns casos, um paciente que já esteja recebendo terapia com Pamelor pode necessitar de tratamento urgente com linezolida ou azul de metileno intravenoso. Se alternativas aceitáveis ao tratamento com linezolida ou azul de metileno intravenoso não estiverem disponíveis e os benefícios potenciais do tratamento com linezolida ou azul de metileno intravenoso forem considerados superiores aos riscos de síndrome serotoninérgica em um determinado paciente, Pamelor 25mg deve ser interrompido imediatamente e linezolida ou metileno intravenoso azul pode ser administrado. O paciente deve ser monitorado quanto a sintomas de síndrome serotoninérgica por duas semanas ou até 24 horas após a última dose de linezolida ou azul de metileno intravenoso, o que ocorrer primeiro. A terapia com Pamelor pode ser retomada 24 horas após a última dose de linezolida ou azul de metileno intravenoso (ver AVISOS ).
risco de administrar azul de metileno por vias não intravenosas (como comprimidos orais ou por injeção local) ou em doses intravenosas muito inferiores a 1 mg/kg com Pamelor 25mg não é claro. O clínico deve, no entanto, estar ciente da possibilidade de sintomas emergentes da síndrome serotoninérgica com tal uso (ver AVISOS ).
COMO FORNECIDO
Cápsulas Pamelor™ (nortriptilina HCl) USP
Cápsulas Pamelor™ (nortriptilina HCl) USP, equivalentes a 10 mg, 25 mg, 50 mg e 75 mg de base, estão disponíveis da seguinte forma:
10 mg : Tampa opaca laranja claro impressa “PAMELOR 10 mg” em corpo opaco preto e branco impresso “M” em preto.
Garrafas de 30: NDC 0406-9910-03
25 mg : Tampa opaca laranja claro impressa “PAMELOR 25 mg” em corpo opaco preto e branco impresso “M” em preto.
Garrafas de 30: NDC 0406-9911-03
50 mg : Tampa opaca branca impressa “PAMELOR 50 mg” em corpo opaco preto e branco impresso “M” em preto.
Garrafas de 30: NDC 0406-9912-03
75 mg Tampa opaca laranja claro impressa “PAMELOR 75 mg” em preto e corpo opaco laranja claro impresso “M” em preto.
Garrafas de 30: NDC 0406-9913-03
Armazenar e Dispensar
Armazene de 20° a 25°C (68° a 77°F) [consulte Temperatura ambiente controlada pela USP].
Dispensar em recipiente hermético (USP) com fecho à prova de crianças.
Mallinckrodt, a marca “M”, o logotipo da Mallinckrodt Pharmaceuticals e outras marcas são marcas registradas de uma empresa Mallinckrodt.
Fabricado por: Patheon Inc. Whitby, Ontário, Canadá. L1N 5Z5. Revisado: outubro de 2016
EFEITOS COLATERAIS
Observação
Incluídas na lista a seguir estão algumas reações adversas que não foram relatadas com este medicamento específico. No entanto, as semelhanças farmacológicas entre os antidepressivos tricíclicos exigem que cada uma das reações seja considerada quando a nortriptilina é administrada.
Cardiovascular
Hipotensão, hipertensão, taquicardia, palpitação, infarto do miocárdio, arritmias, bloqueio cardíaco, acidente vascular cerebral.
Psiquiátrico
Estados de confusão (especialmente em idosos) com alucinações, desorientação, delírios; ansiedade, inquietação, agitação; insônia, pânico, pesadelos; hipomania; exacerbação da psicose.
Neurológico
Dormência, formigamento, parestesias das extremidades; incoordenação, ataxia, tremores; neuropatia periférica; sintomas extrapiramidais; convulsões, alteração nos padrões de EEG; zumbido.
Anticolinérgico
Boca seca e, raramente, adenite sublingual associada; visão turva, perturbação da acomodação, midríase; constipação, íleo paralítico; retenção urinária, micção retardada, dilatação do trato urinário.
Alérgico
Erupção cutânea, petéquias, urticária, prurido, fotossensibilização (evitar exposição excessiva à luz solar); edema (geral ou de face e língua), febre medicamentosa, sensibilidade cruzada com outros medicamentos tricíclicos.
Hematologico
Depressão da medula óssea, incluindo agranulocitose; eosinofilia; púrpura; trombocitopenia.
Gastrointestinal
Náuseas e vômitos, anorexia, desconforto epigástrico, diarréia, gosto peculiar, estomatite, cólicas abdominais, língua negra.
Endócrino
Ginecomastia no homem, aumento mamário e galactorréia na mulher; aumento ou diminuição da libido, impotência; inchaço testicular; elevação ou diminuição dos níveis de açúcar no sangue; síndrome de secreção inapropriada de ADH (hormônio antidiurético).
Outro
Icterícia (simulando obstrução), função hepática alterada; ganho ou perda de peso; transpiração; rubor; frequência urinária, noctúria; sonolência, tontura, fraqueza, fadiga; dor de cabeça; inchaço da parótida; alopecia.
Sintomas de abstinência
Embora estes não sejam indicativos de dependência, a interrupção abrupta do tratamento após terapia prolongada pode produzir náusea, dor de cabeça e mal-estar.
Experiência pós-marketing
seguinte reação adversa ao medicamento foi relatada durante o uso pós-aprovação de Pamelor. Como essa reação é relatada voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança a frequência.
Distúrbios cardíacos - Síndrome de Brugada
Distúrbios oculares - Glaucoma de ângulo fechado
INTERAÇÕES MEDICAMENTOSAS
A administração de reserpina durante a terapia com um antidepressivo tricíclico demonstrou produzir um efeito “estimulante” em alguns pacientes deprimidos.
Supervisão cuidadosa e ajuste cuidadoso da dose são necessários quando Pamelor 25mg é usado com outros anticolinérgicos e simpaticomiméticos.
A administração concomitante de cimetidina e antidepressivos tricíclicos pode produzir aumentos clinicamente significativos nas concentrações plasmáticas do antidepressivo tricíclico. O paciente deve ser informado de que a resposta ao álcool pode ser exagerada.
Um caso de hipoglicemia significativa foi relatado em um paciente diabético tipo II mantido em clorpropamida (250 mg/dia), após a adição de nortriptilina (125 mg/dia).
Drogas Metabolizadas Por P450 2D6
A atividade bioquímica da droga metabolizadora da isozima citocromo P450 2D6 (debrisoquina hidroxilase) é reduzida em um subconjunto da população caucasiana (cerca de 7% a 10% dos caucasianos são chamados de “metabolizadores ruins”); estimativas confiáveis da prevalência da atividade reduzida da isoenzima P450 2D6 entre populações asiáticas, africanas e outras ainda não estão disponíveis. Metabolizadores fracos têm concentrações plasmáticas de antidepressivos tricíclicos (ADTs) maiores do que o esperado quando administrados em doses usuais. Dependendo da fração da droga metabolizada pelo P450 2D6, o aumento na concentração plasmática pode ser pequeno ou bastante grande (aumento de 8 vezes na AUC plasmática do TCA).
Além disso, certas drogas inibem a atividade dessa isoenzima e fazem com que os metabolizadores normais se assemelhem aos metabolizadores ruins. Um indivíduo estável com uma determinada dose de TCA pode tornar-se abruptamente tóxico quando recebe um desses medicamentos inibidores como terapia concomitante. Os medicamentos que inibem o citocromo P450 2D6 incluem alguns que não são metabolizados pela enzima (quinidina; cimetidina) e muitos que são substratos para P450 2D6 (muitos outros antidepressivos, fenotiazinas e os antiarrítmicos tipo 1C propafenona e flecainida). Embora todos os inibidores seletivos da recaptação da serotonina (SSRIs), por exemplo, fluoxetina, sertralina e paroxetina, inibam P450 2D6, eles podem variar na extensão da inibição. A extensão em que as interações do SSRI TCA podem causar problemas clínicos dependerá do grau de inibição e da farmacocinética do SSRI envolvido. No entanto, é indicada cautela na coadministração de ATCs com qualquer um dos ISRS e também na mudança de uma classe para outra. De particular importância, deve decorrer tempo suficiente antes de iniciar o tratamento com TCA em um paciente que está sendo retirado da fluoxetina, dada a longa meia-vida do pai e do metabólito ativo (pelo menos 5 semanas podem ser necessárias).
uso concomitante de antidepressivos tricíclicos com medicamentos que podem inibir o citocromo P450 2D6 pode exigir doses menores do que as normalmente prescritas para o antidepressivo tricíclico ou para o outro medicamento. Além disso, sempre que uma dessas outras drogas é retirada da co-terapia, pode ser necessária uma dose aumentada de antidepressivo tricíclico. É desejável monitorar os níveis plasmáticos de TCA sempre que um TCA for coadministrado com outro medicamento conhecido como inibidor de P450 2D6.
AVISOS
Agravamento clínico e risco de suicídio
Pacientes com transtorno depressivo maior (TDM), adultos e pediátricos, podem apresentar piora de sua depressão e/ou surgimento de ideação e comportamento suicida (suicidalidade) ou mudanças incomuns de comportamento, estejam ou não tomando medicamentos antidepressivos, e isso risco pode persistir até que ocorra remissão significativa. O suicídio é um risco conhecido de depressão e alguns outros distúrbios psiquiátricos, e esses distúrbios são os mais fortes preditores de suicídio. Há uma preocupação de longa data, no entanto, de que os antidepressivos possam ter um papel na indução do agravamento da depressão e do surgimento de tendências suicidas em certos pacientes durante as fases iniciais do tratamento. Análises conjuntas de estudos de curto prazo controlados por placebo de medicamentos antidepressivos (ISRSs e outros) mostraram que esses medicamentos aumentam o risco de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens (de 18 a 24 anos) com depressão maior. (MDD) e outros transtornos psiquiátricos. Estudos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução com antidepressivos em comparação com placebo em adultos com 65 anos ou mais.
As análises agrupadas de estudos controlados por placebo em crianças e adolescentes com TDM, transtorno obsessivo compulsivo (TOC) ou outros transtornos psiquiátricos incluíram um total de 24 estudos de curto prazo de 9 medicamentos antidepressivos em mais de 4.400 pacientes. As análises agrupadas de estudos controlados por placebo em adultos com TDM ou outros transtornos psiquiátricos incluíram um total de 295 estudos de curto prazo (duração média de 2 meses) de 11 medicamentos antidepressivos em mais de 77.000 pacientes. Houve variação considerável no risco de suicídio entre as drogas, mas uma tendência de aumento nos pacientes mais jovens para quase todas as drogas estudadas. Houve diferenças no risco absoluto de suicídio entre as diferentes indicações, com maior incidência no TDM. As diferenças de risco (droga versus placebo), no entanto, foram relativamente estáveis dentro dos estratos de idade e entre as indicações. Essas diferenças de risco (diferença droga-placebo no número de casos de suicídio por 1.000 pacientes tratados) são fornecidas em .
Nenhum suicídio ocorreu em qualquer um dos ensaios pediátricos. Houve suicídios nos ensaios com adultos, mas o número não foi suficiente para chegar a qualquer conclusão sobre o efeito da droga no suicídio.
Não se sabe se o risco de suicídio se estende ao uso a longo prazo, ou seja, além de vários meses. No entanto, há evidências substanciais de ensaios de manutenção controlados por placebo em adultos com depressão de que o uso de antidepressivos pode retardar a recorrência da depressão.
Todos os pacientes em tratamento com antidepressivos para qualquer indicação devem ser monitorados adequadamente e observados de perto quanto a piora clínica, tendências suicidas e mudanças incomuns de comportamento, especialmente durante os primeiros meses de um curso de terapia medicamentosa, ou em momentos de mudanças de dose, ou aumentos ou diminui.
Os seguintes sintomas, ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (agitação psicomotora), hipomania e mania, foram relatados em pacientes adultos e pediátricos em tratamento com antidepressivos para transtorno depressivo maior. quanto a outras indicações, tanto psiquiátricas como não psiquiátricas. Embora não tenha sido estabelecida uma relação causal entre o surgimento de tais sintomas e o agravamento da depressão e/ou o surgimento de impulsos suicidas, existe a preocupação de que tais sintomas possam representar precursores de tendências suicidas emergentes.
Deve-se considerar a mudança do regime terapêutico, incluindo a possibilidade de descontinuação da medicação, em pacientes cuja depressão é persistentemente pior, ou que estão experimentando tendências suicidas emergentes ou sintomas que podem ser precursores de piora da depressão ou tendências suicidas, especialmente se esses sintomas forem graves, abruptos no início, ou não faziam parte dos sintomas de apresentação do paciente.
Familiares e cuidadores de pacientes em tratamento com antidepressivos para transtorno depressivo maior ou outras indicações, tanto psiquiátricas quanto não psiquiátricas, devem ser alertados sobre a necessidade de monitorar os pacientes quanto ao surgimento de agitação, irritabilidade, alterações incomuns de comportamento e outros sintomas descritos acima , bem como o surgimento de tendências suicidas, e relatar tais sintomas imediatamente aos profissionais de saúde. Tal monitoramento deve incluir observação diária por familiares e cuidadores. As prescrições de cloridrato de nortriptilina devem ser feitas para a menor quantidade de cápsulas consistente com o bom manejo do paciente, a fim de reduzir o risco de superdosagem.
Triagem de pacientes para transtorno bipolar
Um episódio depressivo maior pode ser a apresentação inicial do transtorno bipolar. Acredita-se geralmente (embora não estabelecido em ensaios controlados) que o tratamento de tal episódio com um antidepressivo sozinho pode aumentar a probabilidade de precipitação de um episódio misto/maníaco em pacientes com risco de transtorno bipolar. Não se sabe se algum dos sintomas descritos acima representa tal conversão. No entanto, antes de iniciar o tratamento com um antidepressivo, os pacientes com sintomas depressivos devem ser examinados adequadamente para determinar se estão em risco de transtorno bipolar; essa triagem deve incluir uma história psiquiátrica detalhada, incluindo uma história familiar de suicídio, transtorno bipolar e depressão. Deve-se notar que o cloridrato de nortriptilina não é aprovado para uso no tratamento da depressão bipolar.
Pacientes com doença cardiovascular devem receber Pamelor 25mg somente sob supervisão cuidadosa devido à tendência da droga de produzir taquicardia sinusal e prolongar o tempo de condução. Infarto do miocárdio, arritmia e acidentes vasculares cerebrais ocorreram. A ação anti-hipertensiva da guanetidina e de agentes similares pode ser bloqueada. Devido à sua atividade anticolinérgica, Pamelor deve ser usado com muita cautela em pacientes com histórico de retenção urinária. Pacientes com histórico de convulsões devem ser acompanhados de perto quando Pamelor 25mg é administrado, uma vez que esta droga é conhecida por diminuir o limiar convulsivo. É necessário muito cuidado se Pamelor for administrado a pacientes com hipertireoidismo ou que estejam recebendo medicação para tireoide, pois podem desenvolver arritmias cardíacas.
Pamelor pode prejudicar as habilidades mentais e/ou físicas necessárias para o desempenho de tarefas perigosas, como operar máquinas ou dirigir um carro; portanto, o paciente deve ser avisado adequadamente.
consumo excessivo de álcool em combinação com a terapia com nortriptilina pode ter um efeito potencializador, o que pode levar ao risco de aumento de tentativas de suicídio ou superdosagem, especialmente em pacientes com histórico de distúrbios emocionais ou ideação suicida.
A administração concomitante de quinidina e nortriptilina pode resultar em meia-vida plasmática significativamente maior, AUC mais alta e depuração de nortriptilina mais baixa.
Síndrome da serotonina
O desenvolvimento de uma síndrome serotoninérgica potencialmente fatal foi relatado com SNRIs e SSRIs, incluindo Pamelor 25mg, sozinho, mas particularmente com o uso concomitante de outros medicamentos serotoninérgicos (incluindo triptanos, antidepressivos tricíclicos, fentanil, lítio, tramadol, triptofano, buspirona e Erva de São João) e com medicamentos que prejudicam o metabolismo da serotonina (em particular, IMAOs, tanto aqueles destinados a tratar distúrbios psiquiátricos quanto outros, como linezolida e azul de metileno intravenoso).
Os sintomas da síndrome serotoninérgica podem incluir alterações do estado mental (p. mioclonia, hiperreflexia, incoordenação), convulsões e/ou sintomas gastrointestinais (p. Os pacientes devem ser monitorados quanto ao surgimento de síndrome serotoninérgica.
uso concomitante de Pamelor 25mg com IMAOs destinados ao tratamento de distúrbios psiquiátricos é contraindicado. Pamelor também não deve ser iniciado em pacientes que estejam sendo tratados com IMAOs, como linezolida ou azul de metileno intravenoso. Todos os relatos com azul de metileno que forneceram informações sobre a via de administração envolveram administração intravenosa na faixa de dose de 1 mg/kg a 8 mg/kg. Nenhum relato envolveu a administração de azul de metileno por outras vias (como comprimidos orais ou injeção local no tecido) ou em doses mais baixas. Pode haver circunstâncias em que seja necessário iniciar o tratamento com um IMAO, como linezolida ou azul de metileno intravenoso em um paciente tomando Pamelor. Pamelor 25mg deve ser descontinuado antes de iniciar o tratamento com o IMAO (ver CONTRA-INDICAÇÕES e DOSAGEM E ADMINISTRAÇÃO ).
Se o uso concomitante de Pamelor 25mg com outros medicamentos serotoninérgicos, incluindo triptanos, antidepressivos tricíclicos, fentanil, lítio, tramadol, buspirona, triptofano e Erva de São João for clinicamente justificado, os pacientes devem ser alertados sobre um risco potencial aumentado de síndrome serotoninérgica, particularmente durante o início do tratamento e aumentos de dose.
O tratamento com Pamelor 25mg e quaisquer agentes serotoninérgicos concomitantes deve ser descontinuado imediatamente se ocorrerem os eventos acima e tratamento sintomático de suporte deve ser iniciado.
Desmascarando a síndrome de Brugada
Houve relatos pós-comercialização de uma possível associação entre o tratamento com Pamelor e o desmascaramento da síndrome de Brugada. A síndrome de Brugada é um distúrbio caracterizado por síncope, achados eletrocardiográficos (ECG) anormais e risco de morte súbita. Pamelor geralmente deve ser evitado em pacientes com síndrome de Brugada ou com suspeita de síndrome de Brugada.
Glaucoma de ângulo fechado
dilatação pupilar que ocorre após o uso de muitos medicamentos antidepressivos, incluindo Pamelor 25mg, pode desencadear um ataque de fechamento angular em um paciente com ângulos anatomicamente estreitos que não tenha uma iridectomia patente.
Uso na gravidez
O uso seguro de Pamelor durante a gravidez e lactação não foi estabelecido; portanto, quando o medicamento é administrado a pacientes grávidas, lactantes ou mulheres com potencial para engravidar, os benefícios potenciais devem ser ponderados em relação aos possíveis riscos. Estudos de reprodução animal produziram resultados inconclusivos.
PRECAUÇÕES
Informações para pacientes
Os prescritores ou outros profissionais de saúde devem informar os pacientes, seus familiares e seus cuidadores sobre os benefícios e riscos associados ao tratamento com cloridrato de nortriptilina e devem aconselhá-los sobre seu uso adequado. Um paciente Guia de Medicação sobre “Medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas” está disponível para o cloridrato de nortriptilina. O prescritor ou profissional de saúde deve orientar os pacientes, seus familiares e seus cuidadores a ler o Guia de Medicação e auxiliá-los na compreensão de seu conteúdo. Os pacientes devem ter a oportunidade de discutir o conteúdo do Guia de Medicação e obter respostas para quaisquer dúvidas que possam ter. O texto completo do Guia de Medicação é reimpresso no final deste documento.
Os pacientes devem ser avisados sobre os seguintes problemas e solicitados a alertar seu prescritor se ocorrerem enquanto estiverem tomando cloridrato de nortriptilina.
Agravamento clínico e risco de suicídio
Os pacientes, seus familiares e seus cuidadores devem ser encorajados a estarem alertas para o surgimento de ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (inquietação psicomotora), hipomania, mania, outras alterações incomuns de comportamento , agravamento da depressão e ideação suicida, especialmente no início do tratamento antidepressivo e quando a dose é ajustada para cima ou para baixo. Familiares e cuidadores de pacientes devem ser orientados a procurar diariamente o surgimento de tais sintomas, pois as alterações podem ser abruptas. Esses sintomas devem ser relatados ao prescritor ou profissional de saúde do paciente, especialmente se forem graves, de início abrupto ou não fizerem parte dos sintomas apresentados pelo paciente. Sintomas como esses podem estar associados a um risco aumentado de pensamento e comportamento suicida e indicam a necessidade de monitoramento muito próximo e possivelmente mudanças na medicação.
uso de Pamelor em pacientes esquizofrênicos pode resultar em exacerbação da psicose ou pode ativar sintomas esquizofrênicos latentes. Se o fármaco for administrado a pacientes hiperativos ou agitados, pode ocorrer aumento da ansiedade e agitação. Em pacientes maníaco-depressivos, Pamelor pode causar o surgimento de sintomas da fase maníaca.
A hostilidade problemática do paciente pode ser despertada pelo uso de Pamelor. Crises epileptiformes podem acompanhar sua administração, assim como outras drogas de sua classe.
Quando for essencial, a droga pode ser administrada com terapia eletroconvulsiva, embora os riscos possam ser aumentados. Interrompa o medicamento por vários dias, se possível, antes da cirurgia eletiva.
A possibilidade de tentativa de suicídio por paciente deprimido permanece após o início do tratamento; a esse respeito, é importante que a menor quantidade possível de medicamento seja dispensada em um determinado momento.
Tanto a elevação quanto a redução dos níveis de açúcar no sangue foram relatadas.
Os pacientes devem ser alertados de que o uso de Pamelor 25mg pode causar dilatação pupilar leve, que em indivíduos suscetíveis pode levar a um episódio de glaucoma de ângulo fechado. O glaucoma pré-existente é quase sempre o glaucoma de ângulo aberto porque o glaucoma de ângulo fechado, quando diagnosticado, pode ser tratado definitivamente com iridectomia. O glaucoma de ângulo aberto não é um fator de risco para o glaucoma de ângulo fechado. Os pacientes podem desejar ser examinados para determinar se são suscetíveis ao fechamento do ângulo e realizar um procedimento profilático (por exemplo, iridectomia), se forem suscetíveis.
Inibidores da Monoamina Oxidase (IMAOs)
(Ver CONTRA-INDICAÇÕES , AVISOS , e DOSAGEM E ADMINISTRAÇÃO .)
Drogas serotoninérgicas
(Ver CONTRA-INDICAÇÕES , AVISOS , e DOSAGEM E ADMINISTRAÇÃO .)
Uso Pediátrico
A segurança e eficácia na população pediátrica não foram estabelecidas (ver AVISO DE CAIXA e AVISOS , Agravamento Clínico e Risco de Suicídio). Qualquer pessoa considerando o uso de cloridrato de nortriptilina em uma criança ou adolescente deve equilibrar os riscos potenciais com a necessidade clínica.
Uso Geriátrico
Os estudos clínicos do Pamelor não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se eles respondem de forma diferente dos indivíduos mais jovens. Outras experiências clínicas relatadas indicam que, como com outros antidepressivos tricíclicos, eventos adversos hepáticos (caracterizados principalmente por icterícia e enzimas hepáticas elevadas) são observados muito raramente em pacientes geriátricos e mortes associadas a danos hepáticos colestáticos foram relatados em casos isolados. A função cardiovascular, particularmente arritmias e flutuações na pressão arterial, deve ser monitorada. Também houve relatos de estados confusionais após a administração de antidepressivos tricíclicos em idosos. Concentrações plasmáticas mais altas do metabólito ativo da nortriptilina, 10-hidroxinortriptilina, também foram relatadas em pacientes idosos. Assim como com outros antidepressivos tricíclicos, a seleção da dose para um paciente idoso geralmente deve ser limitada à menor dose diária total efetiva (ver DOSAGEM E ADMINISTRAÇÃO ).
SOBREDOSAGEM
Podem ocorrer mortes por superdosagem com esta classe de medicamentos. A ingestão de múltiplas drogas (incluindo álcool) é comum na overdose deliberada de antidepressivos tricíclicos. Como o manejo é complexo e mutável, recomenda-se que o médico entre em contato com um centro de controle de intoxicações para obter informações atualizadas sobre o tratamento. Os sinais e sintomas de toxicidade desenvolvem-se rapidamente após a sobredosagem com antidepressivos tricíclicos, pelo que é necessária monitorização hospitalar o mais rapidamente possível.
Manifestações
As manifestações críticas de sobredosagem incluem: arritmias cardíacas, hipotensão grave, choque, insuficiência cardíaca congestiva, edema pulmonar, convulsões e depressão do SNC, incluindo coma. Alterações no eletrocardiograma, particularmente no eixo ou largura do QRS, são indicadores clinicamente significativos de toxicidade dos antidepressivos tricíclicos.
Outros sinais de superdosagem podem incluir: confusão, inquietação, concentração perturbada, alucinações visuais transitórias, pupilas dilatadas, agitação, reflexos hiperativos, estupor, sonolência, rigidez muscular, vômitos, hipotermia, hiperpirexia ou qualquer um dos sintomas agudos listados em REAÇÕES ADVERSAS . Houve relatos de pacientes se recuperando de overdoses de nortriptilina de até 525 mg.
Gestão
Em geral
Obtenha um ECG e inicie imediatamente a monitorização cardíaca. Proteja as vias aéreas do paciente, estabeleça uma linha intravenosa e inicie a descontaminação gástrica. É necessário um mínimo de seis horas de observação com monitorização cardíaca e observação de sinais de SNC ou depressão respiratória, hipotensão, arritmias cardíacas e/ou bloqueios de condução e convulsões. Se ocorrerem sinais de toxicidade a qualquer momento durante este período, é necessário um monitoramento prolongado. Existem relatos de casos de pacientes que sucumbiram a disritmias fatais tardiamente após a superdosagem; esses pacientes apresentavam evidências clínicas de envenenamento significativo antes da morte e a maioria recebeu descontaminação gastrointestinal inadequada. O monitoramento dos níveis plasmáticos do fármaco não deve orientar o manejo do paciente.
Descontaminação Gastrointestinal
Todos os pacientes com suspeita de overdose de antidepressivos tricíclicos devem receber descontaminação gastrointestinal. Isso deve incluir lavagem gástrica de grande volume seguida de carvão ativado. Se a consciência estiver prejudicada, as vias aéreas devem ser protegidas antes da lavagem. EMESIS É CONTRA-INDICADO.
Cardiovascular
Uma duração máxima do QRS do membro superior de ≥0,10 segundos pode ser a melhor indicação da gravidade da sobredosagem. O bicarbonato de sódio intravenoso deve ser usado para manter o pH sérico na faixa de 7,45 a 7,55. Se a resposta do pH for inadequada, a hiperventilação também pode ser usada. O uso concomitante de hiperventilação e bicarbonato de sódio deve ser feito com extrema cautela, com monitoramento frequente do pH. Um pH > 7,60 ou um pCO
SNC
Em pacientes com depressão do SNC, a intubação precoce é aconselhada devido ao potencial de deterioração abrupta. As convulsões devem ser controladas com benzodiazepínicos ou, se estes forem ineficazes, com outros anticonvulsivantes (por exemplo, fenobarbital, fenitoína). A fisostigmina não é recomendada, exceto para tratar sintomas de risco de vida que não responderam a outras terapias, e somente em consulta com um centro de controle de intoxicações.
Acompanhamento Psiquiátrico
Como a superdosagem é muitas vezes deliberada, os pacientes podem tentar o suicídio por outros meios durante a fase de recuperação. O encaminhamento psiquiátrico pode ser apropriado.
Gestão Pediátrica
Os princípios de gestão de superdosagens em crianças e adultos são semelhantes. É altamente recomendável que o médico entre em contato com o centro de controle de intoxicações local para tratamento pediátrico específico.
CONTRA-INDICAÇÕES
Inibidores da Monoamina Oxidase (IMAOs)
uso de IMAOs destinados a tratar distúrbios psiquiátricos com Pamelor 25mg ou dentro de 14 dias após a interrupção do tratamento com Pamelor 25mg é contraindicado devido ao risco aumentado de síndrome serotoninérgica. O uso de Pamelor 25mg dentro de 14 dias após a interrupção de um IMAO destinado a tratar distúrbios psiquiátricos também é contraindicado (ver AVISOS e DOSAGEM E ADMINISTRAÇÃO ).
Iniciar Pamelor 25mg em um paciente que está sendo tratado com IMAOs, como linezolida ou azul de metileno intravenoso, também é contraindicado devido ao risco aumentado de síndrome serotoninérgica (consulte AVISOS e DOSAGEM E ADMINISTRAÇÃO ).
Hipersensibilidade a antidepressivos tricíclicos
A sensibilidade cruzada entre Pamelor e outras dibenzazepinas é uma possibilidade.
Infarto do miocárdio
Pamelor 25mg é contraindicado durante o período de recuperação aguda após infarto do miocárdio.
FARMACOLOGIA CLÍNICA
mecanismo de elevação do humor por antidepressivos tricíclicos é atualmente desconhecido. Pamelor 25mg não é um inibidor da monoamina oxidase. Inibe a atividade de diversos agentes como histamina, 5-hidroxitriptamina e acetilcolina. Aumenta o efeito pressor da norepinefrina, mas bloqueia a resposta pressora da fenetilamina. Estudos sugerem que Pamelor 25mg interfere no transporte, liberação e armazenamento de catecolaminas. Técnicas de condicionamento operante em ratos e pombos sugerem que Pamelor tem uma combinação de propriedades estimulantes e depressoras.
INFORMAÇÃO DO PACIENTE
Pamelor™ (nortriptilina HCl) Cápsulas USP
Medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas
Leia o Guia de Medicação que acompanha você ou o medicamento antidepressivo de seu familiar. Este Guia de Medicação trata apenas do risco de pensamentos e ações suicidas com medicamentos antidepressivos.
Fale com o seu médico ou com o seu familiar sobre:
- todos os riscos e benefícios do tratamento com medicamentos antidepressivos
- todas as opções de tratamento para depressão ou outra doença mental grave
Qual é a informação mais importante que devo saber sobre medicamentos antidepressivos, depressão e outras doenças mentais graves e pensamentos ou ações suicidas?
- Preste muita atenção a quaisquer mudanças, especialmente mudanças repentinas, de humor, comportamentos, pensamentos ou sentimentos. Isso é muito importante quando um medicamento antidepressivo é iniciado ou quando a dose é alterada.
- Ligue para o profissional de saúde imediatamente para relatar mudanças novas ou repentinas no humor, comportamento, pensamentos ou sentimentos.
- Mantenha todas as visitas de acompanhamento com o profissional de saúde conforme programado. Ligue para o médico entre as visitas, conforme necessário, especialmente se tiver dúvidas sobre os sintomas.
Ligue para um profissional de saúde imediatamente se você ou seu familiar tiver algum dos seguintes sintomas, especialmente se forem novos, piores ou se preocuparem:
- pensamentos sobre suicídio ou morte
- tentativas de suicídio
- depressão nova ou pior
- ansiedade nova ou pior
- sentindo-se muito agitado ou inquieto
- ataques de pânico
- problemas para dormir (insônia)
- irritabilidade nova ou pior
- agindo de forma agressiva, com raiva ou violento
- agindo em impulsos perigosos
- um aumento extremo na atividade e na fala (mania)
- outras mudanças incomuns no comportamento ou humor
Problemas visuais
- dor nos olhos
- mudanças na visão
- inchaço ou vermelhidão dentro ou ao redor do olho
Apenas algumas pessoas estão em risco para esses problemas. Você pode querer se submeter a um exame oftalmológico para ver se está em risco e receber tratamento preventivo, se estiver.
Quem não deve tomar Pamelor?
Não tome Pamelor se você:
- tomar um inibidor da monoamina oxidase (IMAO). Pergunte ao seu médico ou farmacêutico se não tiver certeza se está tomando um IMAO, incluindo o antibiótico linezolida.
- Não tome um IMAO dentro de 2 semanas após a interrupção de Pamelor 25mg, a menos que seja orientado pelo seu médico.
- Não inicie Pamelor 25mg se você parou de tomar um IMAO nas últimas 2 semanas, a menos que seja orientado pelo seu médico.
O que mais eu preciso saber sobre medicamentos antidepressivos?
- Nunca interrompa um medicamento antidepressivo sem primeiro falar com um profissional de saúde. Parar um medicamento antidepressivo de repente pode causar outros sintomas.
- Os antidepressivos são medicamentos usados para tratar a depressão e outras doenças. É importante discutir todos os riscos de tratar a depressão e também os riscos de não tratá-la. Os pacientes e suas famílias ou outros cuidadores devem discutir todas as opções de tratamento com o profissional de saúde, não apenas o uso de antidepressivos.
- medicamentos antidepressivos têm outros efeitos colaterais. Converse com o médico sobre os efeitos colaterais do medicamento prescrito para você ou seu familiar.
- Medicamentos antidepressivos podem interagir com outros medicamentos. Conheça todos os medicamentos que você ou seu familiar toma. Mantenha uma lista de todos os medicamentos para mostrar ao profissional de saúde. Não inicie novos medicamentos sem primeiro consultar seu médico.
- Nem todos os medicamentos antidepressivos prescritos para crianças são aprovados pela FDA para uso em crianças. Fale com o profissional de saúde do seu filho para obter mais informações.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA pelo telefone 1-800-FDA-1088.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
