Cleocin 150mg, 300mg Clindamycin Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que são as cápsulas de cloridrato de Cleocin 300mg?
As cápsulas de Cloridrato de Cleocina contêm um antibiótico indicado no tratamento de infecções graves causadas por bactérias anaeróbicas sensíveis. Cloridrato de Cleocin 150mg também é indicado no tratamento de infecções graves devido a cepas suscetíveis de estreptococos, pneumococos e estafilococos. Seu uso deve ser reservado para pacientes alérgicos à penicilina ou outros pacientes para os quais, no julgamento do médico, uma penicilina é inadequada. Cloridrato de Cleocina está disponível na forma genérica.
Quais são os efeitos colaterais das cápsulas de cloridrato de Cleocin 300mg?
Os efeitos colaterais comuns do Cloridrato de Cleocina incluem:
- colite por Clostridium difficile,
- dor abdominal,
- colite pseudomembranosa,
- esofagite,
- náusea,
- vômito,
- diarréia,
- erupção cutânea,
- urticária,
- reações alérgicas graves (anafilaxia),
- reações de hipersensibilidade,
- coceira,
- corrimento vaginal e desconforto,
- inchaço da pele,
- pele e olhos amarelados (icterícia),
- testes de função hepática anormais, e
- dor nas articulações.
Para reduzir o desenvolvimento de bactérias resistentes a medicamentos e manter a eficácia de CLEOCIN 300mg HCl e outros medicamentos antibacterianos, CLEOCIN 300mg HCl deve ser usado apenas para tratar ou prevenir infecções comprovadas ou fortemente suspeitas de serem causadas por bactérias.
AVISO
Diarreia associada a Clostridium difficile (CDAD) foi relatada com o uso de quase todos os agentes antibacterianos, incluindo CLEOCIN HCl e pode variar em gravidade de diarreia leve a colite fatal. O tratamento com agentes antibacterianos altera a flora normal do cólon, levando ao crescimento excessivo de C. difficle.
Como a terapia com CLEOCIN 150mg HCl foi associada a colite grave que pode terminar fatalmente, deve ser reservada para infecções graves em que agentes antimicrobianos menos tóxicos são inadequados, conforme descrito na INDICAÇÕES E USO seção. Não deve ser usado em pacientes com infecções não bacterianas, como a maioria das infecções do trato respiratório superior.
C. difficle produz toxinas A e B, que contribuem para o desenvolvimento de CDAD. Cepas produtoras de hipertoxina de C. diffile causam aumento da morbidade e mortalidade, pois essas infecções podem ser refratárias à terapia antimicrobiana e podem exigir colectomia. CDAD deve ser considerado em todos os pacientes que apresentam diarreia após o uso de antibióticos. É necessário um histórico médico cuidadoso, pois foi relatado que a CDAD ocorre mais de dois meses após a administração de agentes antibacterianos.
Se houver suspeita ou confirmação de CDAD, o uso contínuo de antibióticos não direcionados contra C. difficle pode precisar ser descontinuado. O manejo adequado de fluidos e eletrólitos, suplementação proteica, tratamento antibiótico de C. difficle e avaliação cirúrgica devem ser instituídos conforme indicação clínica.
DESCRIÇÃO
O cloridrato de clindamicina é o sal cloridrato hidratado de clindamicina. A clindamicina é um antibiótico semissintético produzido por uma substituição 7(S)-cloro do grupo 7(R)-hidroxil do composto original lincomicina.
As cápsulas de CLEOCIN HCl contêm cloridrato de clindamicina equivalente a 75 mg, 150 mg ou 300 mg de clindamicina.
Ingredientes inativos: 75 mg - amido de milho, FD&C azul no. 1, FD&C amarelo no. 5, gelatina, lactose, estearato de magnésio e talco; 150 mg - amido de milho, azul FD&C no. 1, FD&C amarelo no. 5, gelatina, lactose, estearato de magnésio, talco e dióxido de titânio; 300 mg - amido de milho, azul FD&C no. 1, gelatina, lactose, estearato de magnésio, talco e dióxido de titânio.
A fórmula estrutural está representada abaixo:
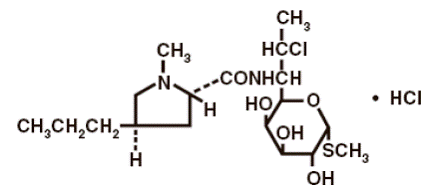
O nome químico do cloridrato de clindamicina é Metil 7-cloro-6,7,8-trideoxi-6-(1-metil-trans-4-propil-L-2-pirrolidinacarboxamido)-1-tio-L-treo-α- Monocloridrato de D-galacto-octopiranósido.
INDICAÇÕES
A clindamicina é indicada no tratamento de infecções graves causadas por bactérias anaeróbicas sensíveis.
clindamicina também é indicada no tratamento de infecções graves devido a cepas suscetíveis de estreptococos, pneumococos e estafilococos. Seu uso deve ser reservado para pacientes alérgicos à penicilina ou outros pacientes para os quais, no julgamento do médico, uma penicilina é inadequada. Devido ao risco de colite, conforme descrito na ADVERTÊNCIA NA CAIXA, antes de selecionar a clindamicina, o médico deve considerar a natureza da infecção e a adequação de alternativas menos tóxicas (por exemplo, eritromicina).
Anaeróbios: Infecções graves do trato respiratório, como empiema, pneumonite anaeróbica e abscesso pulmonar; infecções graves da pele e tecidos moles; septicemia; infecções intra-abdominais, como peritonite e abscesso intra-abdominal (geralmente resultantes de organismos anaeróbios residentes no trato gastrointestinal normal); infecções da pelve feminina e do trato genital, como endometrite, abscesso tubo-ovariano não gonocócico, celulite pélvica e infecção do manguito vaginal pós-cirúrgico.
Estreptococos: Infecções graves do trato respiratório; infecções graves da pele e tecidos moles.
Estafilococos: Infecções graves do trato respiratório; infecções graves da pele e tecidos moles.
Pneumococos: Infecções graves do trato respiratório.
Estudos bacteriológicos devem ser realizados para determinar os organismos causadores e sua suscetibilidade à clindamicina.
Para reduzir o desenvolvimento de bactérias resistentes aos medicamentos e manter a eficácia de CLEOCIN HCl e outros medicamentos antibacterianos, CLEOCIN HCl deve ser usado apenas para tratar ou prevenir infecções comprovadamente ou fortemente suspeitas de serem causadas por bactérias suscetíveis. Quando as informações de cultura e suscetibilidade estiverem disponíveis, elas devem ser consideradas na seleção ou modificação da terapia antibacteriana. Na ausência de tais dados, a epidemiologia local e os padrões de suscetibilidade podem contribuir para a seleção empírica da terapia.
DOSAGEM E ADMINISTRAÇÃO
Se ocorrer diarreia significativa durante o tratamento, este antibiótico deve ser descontinuado (ver AVISO EM CAIXA ).
Adultos
Infecções graves - 150 a 300 mg a cada 6 horas. Infecções mais graves - 300 a 450 mg a cada 6 horas.
Pacientes pediátricos (para crianças que conseguem engolir cápsulas):
Infecções graves 8 a 16 mg/kg/dia (4 a 8 mg/lb/dia) dividido em três ou quatro doses iguais. Infecções mais graves - 16 a 20 mg/kg/dia (8 a 10 mg/lb/dia) dividida em três ou quatro doses iguais.
Para evitar a possibilidade de irritação esofágica, CLEOCIN 300mg HCl cápsulas deve ser tomado com um copo cheio de água.
As cápsulas de CLEOCIN HCl não são adequadas para crianças que não conseguem engoli-las inteiras. As cápsulas não fornecem doses exatas de mg/kg, portanto, pode ser necessário usar a solução oral de palmitato de clindamicina em alguns casos.
Infecções graves devido a bactérias anaeróbicas são geralmente tratadas com solução estéril CLEOCIN PHOSPHATE®. No entanto, em circunstâncias clinicamente apropriadas, o médico pode optar por iniciar o tratamento ou continuar o tratamento com CLEOCIN 150mg HCl Cápsulas.
Em casos de infecções estreptocócicas β-hemolíticas, o tratamento deve continuar por pelo menos 10 dias.
COMO FORNECIDO
Cápsulas de CLEOCINA HCl estão disponíveis nas seguintes forças, cores e tamanhos:
75 mg Garrafas Verdes de 100 NDC 0009-0331-02
150 mg Garrafas Azul Claro e Verde de 100 NDC 0009-0225-02
300 mg Garrafas Azul Claro de 100 NDC 0009-0395-14
Armazenar em temperatura ambiente controlada de 20° a 25° C (68° a 77° F) [consulte USP ].
Distribuído por: Pharmacia & Upjohn Co, Division of Pfizer Inc, NY, NY 10017. Revisado em 2017
EFEITOS COLATERAIS
As seguintes reações foram relatadas com o uso de clindamicina.
Infecções e Infestações: Colite por Clostridium difficile
Gastrointestinal: Dor abdominal, colite pseudomembranosa, esofagite, náuseas, vômitos e diarreia (ver AVISO EM CAIXA ). O início dos sintomas de colite pseudomembranosa pode ocorrer durante ou após o tratamento antibacteriano (ver AVISOS ). Úlcera esofágica foi relatada. Um sabor desagradável ou metálico foi relatado após a administração oral.
Reações de hipersensibilidade: Erupções cutâneas do tipo morbiliforme (maculopapular) generalizadas leves a moderadas são as reações adversas mais frequentemente relatadas. Erupções cutâneas vesiculobolhosas, bem como urticária, foram observadas durante a terapia medicamentosa. Reações cutâneas graves, como necrólise epidérmica tóxica, algumas com desfecho fatal, foram relatadas (consulte AVISOS ). Também foram relatados casos de Pustulose Exantematosa Generalizada Aguda (PEGA), eritema multiforme, alguns semelhantes à síndrome de Stevens-Johnson, choque anafilático, reação anafilática e hipersensibilidade.
Pele e membranas mucosas: Prurido, vaginite, angioedema e casos raros de dermatite esfoliativa foram relatados. (Ver Reações de hipersensibilidade .)
Fígado: Icterícia e anormalidades nos testes de função hepática foram observados durante a terapia com clindamicina.
Renal: Embora nenhuma relação direta da clindamicina com o dano renal tenha sido estabelecida, foi observada disfunção renal como evidenciada por azotemia, oligúria e/ou proteinúria.
Hematopoiético: Neutropenia transitória (leucopenia) e eosinofilia foram relatadas. Foram feitos relatos de agranulocitose e trombocitopenia. Nenhuma relação etiológica direta com a terapia concomitante com clindamicina pode ser feita em qualquer um dos anteriores.
Sistema imunológico: Foram relatados casos de reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS).
Musculoesquelético: Casos de poliartrite foram relatados.
INTERAÇÕES MEDICAMENTOSAS
A clindamicina demonstrou ter propriedades bloqueadoras neuromusculares que podem aumentar a ação de outros agentes bloqueadores neuromusculares. Portanto, deve ser usado com cautela em pacientes recebendo tais agentes.
clindamicina é metabolizada predominantemente pelo CYP3A4 e, em menor grau, pelo CYP3A5, no metabólito principal sulfóxido de clindamicina e no metabólito menor N-desmetilclindamicina. Portanto, os inibidores de CYP3A4 e CYP3A5 podem aumentar as concentrações plasmáticas de clindamicina e os indutores dessas isoenzimas podem reduzir as concentrações plasmáticas de clindamicina. Na presença de inibidores fortes do CYP3A4, monitore as reações adversas. Na presença de indutores fortes do CYP3A4, como a rifampicina, monitore a perda de eficácia.
Estudos in vitro indicam que a clindamicina não inibe CYP1A2, CYP2C9, CYP2C19, CYP2E1 ou CYP2D6 e inibe apenas moderadamente CYP3A4.
Foi demonstrado antagonismo entre a clindamicina e a eritromicina in vitro. Devido ao possível significado clínico, esses dois medicamentos não devem ser administrados concomitantemente.
AVISOS
Ver AVISO EM CAIXA
Diarreia Associada a Clostridium Difficile
Diarreia associada a Clostridium difficile (CDAD) foi relatada com o uso de quase todos os agentes antibacterianos, incluindo CLEOCIN 300mg HCl, e pode variar em gravidade de diarreia leve a colite fatal. O tratamento com agentes antibacterianos altera a flora normal do cólon, levando ao crescimento excessivo de C. difficle.
C. difficle produz toxinas A e B, que contribuem para o desenvolvimento de CDAD. Cepas produtoras de hipertoxina de C. diffile causam aumento da morbidade e mortalidade, pois essas infecções podem ser refratárias à terapia antimicrobiana e podem exigir colectomia. CDAD deve ser considerado em todos os pacientes que apresentam diarreia após o uso de antibióticos. É necessário um histórico médico cuidadoso, pois foi relatado que a CDAD ocorre mais de dois meses após a administração de agentes antibacterianos.
Se houver suspeita ou confirmação de CDAD, o uso contínuo de antibióticos não direcionados contra C. difficle pode precisar ser descontinuado. O manejo adequado de fluidos e eletrólitos, suplementação proteica, tratamento antibiótico de C. difficle e avaliação cirúrgica devem ser instituídos conforme indicação clínica.
Reações anafiláticas e de hipersensibilidade grave
Choque anafilático e reações anafiláticas foram relatados (ver REAÇÕES ADVERSAS ).
Reações graves de hipersensibilidade, incluindo reações cutâneas graves, como necrólise epidérmica tóxica (NET), reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS) e síndrome de Stevens-Johnson (SSJ), algumas com desfecho fatal, foram relatadas (consulte REAÇÕES ADVERSAS ).
Em caso de reação anafilática ou de hipersensibilidade grave, descontinue o tratamento permanentemente e institua a terapia apropriada.
Uma investigação cuidadosa deve ser feita em relação a sensibilidades anteriores a drogas e outros alérgenos.
Uso na meningite
Como a clindamicina não se difunde adequadamente no líquido cefalorraquidiano, a droga não deve ser usada no tratamento da meningite.
PRECAUÇÕES
Em geral
A revisão da experiência até o momento sugere que um subgrupo de pacientes idosos com doença grave associada pode tolerar menos a diarreia. Quando a clindamicina é indicada nesses pacientes, eles devem ser cuidadosamente monitorados quanto a alterações na frequência intestinal.
CLEOCIN 300mg HCl deve ser prescrito com cautela em indivíduos com histórico de doença gastrointestinal, particularmente colite.
CLEOCIN 300mg HCl deve ser prescrito com cautela em indivíduos atópicos.
Os procedimentos cirúrgicos indicados devem ser realizados em conjunto com a antibioticoterapia.
O uso de CLEOCIN 150mg HCl ocasionalmente resulta em supercrescimento de organismos não suscetíveis, particularmente leveduras. Caso ocorram superinfecções, devem ser tomadas as medidas apropriadas conforme indicado pela situação clínica.
modificação da dose de clindamicina pode não ser necessária em pacientes com doença renal. Em pacientes com doença hepática moderada a grave, foi observado prolongamento da meia-vida da clindamicina. No entanto, foi postulado a partir de estudos que, quando administrado a cada oito horas, o acúmulo raramente deve ocorrer. Portanto, a modificação da dosagem em pacientes com doença hepática pode não ser necessária. No entanto, determinações periódicas de enzimas hepáticas devem ser feitas ao tratar pacientes com doença hepática grave.
As cápsulas de 75 mg e 150 mg contêm FD&C amarelo no. 5 (tartrazina), que pode causar reações do tipo alérgico (incluindo asma brônquica) em certos indivíduos suscetíveis. Embora a incidência global de FD&C amarelo não. 5 (tartrazina) na população geral é baixa, é frequentemente observada em pacientes que também têm hipersensibilidade à aspirina.
prescrição de CLEOCIN 150mg HCl na ausência de infecção bacteriana comprovada ou fortemente suspeita ou indicação profilática provavelmente não trará benefícios ao paciente e aumenta o risco de desenvolvimento de bactérias resistentes aos medicamentos.
Testes laboratoriais
Durante a terapia prolongada, testes periódicos de função hepática e renal e hemogramas devem ser realizados.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Estudos de longa duração em animais não foram realizados com clindamicina para avaliar o potencial carcinogênico. Os testes de genotoxicidade realizados incluíram um teste de micronúcleo em ratos e um teste de reversão de Ames Salmonella. Ambos os testes foram negativos.
Estudos de fertilidade em ratos tratados por via oral com até 300 mg/kg/dia (aproximadamente 1,6 vezes a dose humana adulta mais alta recomendada com base em mg/m²) não revelaram efeitos na fertilidade ou na capacidade de acasalamento.
Gravidez
Efeitos teratogênicos
Em ensaios clínicos com mulheres grávidas, a administração sistémica de clindamicina durante o segundo e terceiro trimestres não foi associada a um aumento da frequência de anomalias congénitas.
clindamicina deve ser usada durante o primeiro trimestre de gravidez somente se claramente necessário. Não existem estudos adequados e bem controlados em mulheres grávidas durante o primeiro trimestre de gravidez. Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, este medicamento deve ser usado durante a gravidez somente se claramente necessário.
Estudos de reprodução realizados em ratos e camundongos usando doses orais de clindamicina de até 600 mg/kg/dia (3,2 e 1,6 vezes a dose humana adulta mais alta recomendada com base em mg/m², respectivamente) ou doses subcutâneas de clindamicina de até 250 mg/kg /dia (1,3 e 0,7 vezes a dose humana adulta mais alta recomendada com base em mg/m², respectivamente) não revelou evidência de teratogenicidade.
Mães que amamentam
Foi relatado que a clindamicina aparece no leite materno na faixa de 0,7 a 3,8 mcg/mL. A clindamicina tem o potencial de causar efeitos adversos na flora gastrointestinal do lactente. Se a clindamicina oral ou intravenosa for necessária por uma mãe que amamenta, não é motivo para descontinuar a amamentação, mas um medicamento alternativo pode ser preferido. Monitore a criança quanto a possíveis efeitos adversos na flora gastrointestinal, como diarreia, candidíase (aftas, assaduras) ou, raramente, sangue nas fezes indicando possível colite associada a antibióticos.
Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica de clindamicina da mãe e quaisquer efeitos adversos potenciais da clindamicina na criança amamentada ou da condição materna subjacente.
Uso Pediátrico
Quando CLEOCIN 300mg HCl é administrado à população pediátrica (do nascimento aos 16 anos), é desejável o monitoramento adequado das funções do sistema orgânico.
Uso Geriátrico
Os estudos clínicos de clindamicina não incluíram um número suficiente de pacientes com 65 anos ou mais para determinar se eles respondem de forma diferente dos pacientes mais jovens. No entanto, outras experiências clínicas relatadas indicam que colite e diarreia associadas a antibióticos (devido a Clostridium difficile) observadas em associação com a maioria dos antibióticos ocorrem com mais frequência em idosos (> 60 anos) e podem ser mais graves. Esses pacientes devem ser cuidadosamente monitorados quanto ao desenvolvimento de diarreia.
Estudos farmacocinéticos com clindamicina não mostraram diferenças clinicamente importantes entre indivíduos jovens e idosos com função hepática normal e função renal normal (ajustada à idade) após administração oral ou intravenosa.
SOBREDOSAGEM
Mortalidade significativa foi observada em camundongos com uma dose intravenosa de 855 mg/kg e em ratos com uma dose oral ou subcutânea de aproximadamente 2618 mg/kg. Nos camundongos, foram observadas convulsões e depressão.
hemodiálise e a diálise peritoneal não são eficazes na remoção da clindamicina do soro.
CONTRA-INDICAÇÕES
CLEOCIN 150mg HCl é contraindicado em indivíduos com histórico de hipersensibilidade a preparações contendo clindamicina ou lincomicina.
FARMACOLOGIA CLÍNICA
Farmacologia Humana
Absorção
Estudos de nível sérico com uma dose oral de 150 mg de cloridrato de clindamicina em 24 voluntários adultos normais mostraram que a clindamicina foi rapidamente absorvida após administração oral. Um pico sérico médio de 2,50 mcg/mL foi alcançado em 45 minutos; os níveis séricos foram em média 1,51 mcg/mL em 3 horas e 0,70 mcg/mL em 6 horas. A absorção de uma dose oral é praticamente completa (90%), e a administração concomitante de alimentos não modifica de forma apreciável as concentrações séricas; os níveis séricos têm sido uniformes e previsíveis de pessoa para pessoa e dose a dose. Estudos de nível sérico após múltiplas doses de CLEOCIN 150mg HCl por até 14 dias não mostram evidência de acúmulo ou metabolismo alterado do fármaco. Doses de até 2 gramas de clindamicina por dia durante 14 dias foram bem toleradas por voluntários saudáveis, exceto que a incidência de efeitos colaterais gastrointestinais é maior com as doses mais altas.
Distribuição
As concentrações de clindamicina no soro aumentaram linearmente com o aumento da dose. Os níveis séricos excedem a CIM (concentração inibitória mínima) para a maioria dos organismos indicados por pelo menos seis horas após a administração das doses normalmente recomendadas. A clindamicina é amplamente distribuída nos fluidos e tecidos corporais (incluindo ossos). Não são atingidos níveis significativos de clindamicina no líquido cefalorraquidiano, mesmo na presença de meninges inflamadas.
Metabolismo
Estudos in vitro em microssomas hepáticos e intestinais humanos indicaram que a clindamicina é predominantemente metabolizada pelo citocromo P450 3A4 (CYP3A4), com pequena contribuição do CYP3A5, para formar sulfóxido de clindamicina e um metabólito menor, N-desmetilclindamicina.
Excreção
A meia-vida biológica média é de 2,4 horas. Aproximadamente 10% da bioatividade é excretada na urina e 3,6% nas fezes; o restante é excretado como metabólitos bioinativos.
Populações Especiais
Insuficiência renal
meia-vida sérica da clindamicina é ligeiramente aumentada em pacientes com função renal marcadamente reduzida. A hemodiálise e a diálise peritoneal não são eficazes na remoção da clindamicina do soro.
Uso em idosos
Estudos de farmacocinética em voluntários idosos (61-79 anos) e adultos jovens (18-39 anos) indicam que a idade por si só não altera a farmacocinética da clindamicina (depuração, meia-vida de eliminação, volume de distribuição e área sob a curva concentração sérica-tempo ) após administração IV de fosfato de clindamicina. Após a administração oral de cloridrato de clindamicina, a meia-vida de eliminação é aumentada para aproximadamente 4,0 horas (intervalo de 3,4-5,1 h) em idosos em comparação com 3,2 horas (intervalo de 2,1 - 4,2 h) em adultos mais jovens. A extensão da absorção, no entanto, não é diferente entre as faixas etárias e nenhuma alteração de dosagem é necessária para idosos com função hepática normal e função renal normal (ajustada pela idade)1.
Microbiologia
Mecanismo de ação
clindamicina inibe a síntese de proteínas bacterianas ao se ligar ao RNA 23S da subunidade 50S do ribossomo. A clindamicina é bacteriostática.
Resistência
A resistência à clindamicina é mais frequentemente causada pela modificação de bases específicas do RNA ribossômico 23S. A resistência cruzada entre clindamicina e lincomicina é completa. Como os sítios de ligação para essas drogas antibacterianas se sobrepõem, às vezes é observada resistência cruzada entre lincosamidas, macrolídeos e estreptogramina B. A resistência induzida por macrolídeos à clindamicina ocorre em alguns isolados de bactérias resistentes a macrolídeos. Isolados de estafilococos e estreptococos beta-hemolíticos resistentes a macrolídeos devem ser rastreados para indução de resistência à clindamicina usando o teste da zona D.
Actividade antimicrobiana
A clindamicina demonstrou ser ativa contra a maioria dos isolados dos seguintes microrganismos, tanto in vitro quanto em infecções clínicas, conforme descrito na INDICAÇÕES E USO seção.
Bactérias Gram-positivas
Staphylococcus aureus (cepas sensíveis à meticilina) Streptococcus pneumoniae (cepas sensíveis à penicilina) Streptococcus pyogenes
Bactérias anaeróbicas
Clostridium perfringens Fusobacterium necrophorum Fusobacterium nucleatum Peptostreptococcus anaerobius Prevotella melaninogenica
Pelo menos 90% dos microorganismos listados abaixo exibem concentrações inibitórias mínimas in vitro (CIMs) menores ou iguais ao ponto de corte de CIM suscetível à clindamicina para organismos de um tipo semelhante aos mostrados na Tabela 1. No entanto, a eficácia da clindamicina no tratamento clínico infecções causadas por esses microrganismos não foi estabelecida em ensaios clínicos adequados e bem controlados.
Bactérias Gram-positivas
Staphylococcus epidermidis (cepas sensíveis à meticilina) Streptococcus agalactiae Streptococcus anginosus Streptococcus mitis Streptococcus oralis
Bactérias anaeróbicas
Actinomyces israelii Clostridium clostridioforme Eggerthella lenta Finegoldia (Peptostreptococcus) magna Micromonas (Peptostreptococcus) micros Prevotella bivia Prevotella intermedia Propionibacterium acnes
Métodos de teste de suscetibilidade
Quando disponível, o laboratório de microbiologia clínica deve fornecer ao médico resultados de testes de suscetibilidade in vitro cumulativos para drogas antimicrobianas usadas em hospitais locais e áreas de prática como relatórios periódicos que descrevem o perfil de suscetibilidade de patógenos nosocomiais e adquiridos na comunidade. Esses relatórios devem ajudar o médico a selecionar um medicamento antibacteriano para tratamento.
Técnicas de diluição
Métodos quantitativos são usados para determinar as concentrações inibitórias mínimas antimicrobianas (MICs). Esses MICs fornecem estimativas da suscetibilidade das bactérias aos compostos antimicrobianos. As CIMs devem ser determinadas usando um método de teste padronizado2,3 (caldo e/ou ágar). Os valores de CIM devem ser interpretados de acordo com os critérios fornecidos na Tabela 1.
Técnicas de difusão
Os métodos quantitativos que requerem a medição dos diâmetros das zonas também podem fornecer estimativas reprodutíveis da suscetibilidade das bactérias aos compostos antimicrobianos. O tamanho da zona deve ser determinado usando um método padronizado2,5. Este procedimento utiliza discos de papel impregnados com 2 mcg de clindamicina para testar a suscetibilidade das bactérias à clindamicina. Os pontos de interrupção de difusão de disco são fornecidos na Tabela 1.
Técnicas anaeróbicas
Para bactérias anaeróbicas, a suscetibilidade à clindamicina pode ser determinada por um método de teste padronizado2,4. Os valores de CIM obtidos devem ser interpretados de acordo com os critérios fornecidos na Tabela 1.
Um relato de Suscetível (S ) indica que a droga antimicrobiana provavelmente inibe o crescimento do patógeno se a droga antimicrobiana atingir a concentração usualmente alcançável no local da infecção. Um relatório de Intermediário (I) indica que o resultado deve ser considerado ambíguo e, se o microrganismo não for totalmente suscetível a drogas alternativas e clinicamente viáveis, o teste deve ser repetido. Esta categoria implica em possível aplicabilidade clínica em locais do corpo onde o fármaco está fisiologicamente concentrado ou em situações onde altas dosagens do fármaco podem ser usadas. Esta categoria também fornece uma zona tampão que evita que fatores técnicos pequenos e não controlados causem grandes discrepâncias na interpretação. Um relatório de Resistente (R) indica que a droga antimicrobiana provavelmente não inibe o crescimento do patógeno se a droga antimicrobiana atingir a concentração usualmente alcançável no local da infecção; outra terapia deve ser selecionada.
Controle de qualidade
Os procedimentos de teste de suscetibilidade padronizados requerem o uso de controles laboratoriais para monitorar e garantir a exatidão e precisão dos suprimentos e reagentes usados no ensaio, e as técnicas dos indivíduos que realizam o teste.2,3,4,5 O pó padrão de clindamicina deve fornecer os intervalos de CIM na Tabela 2. Para a técnica de difusão em disco usando o disco de clindamicina de 2 mcg, os critérios fornecidos na Tabela 2 devem ser alcançados.
anaeróbios podem ser testados por métodos de microdiluição em caldo ou diluição em ágar. NA=Não aplicável ATCC® é uma marca registrada da American Type Culture Collection
REFERÊNCIAS
1. Smith RB, Phillips JP: Avaliação de CLEOCIN HCl e CLEOCIN Phosphate em uma população idosa. Upjohn TR 8147-82-9122-021, dezembro de 1982.
2. CLSI. Padrões de desempenho para testes de suscetibilidade antimicrobiana: 26ª ed. Suplemento CLSI M100S. Wayne, PA: Instituto de Padrões Clínicos e Laboratoriais; 2016.
3. CLSI. Métodos para Testes de Susceptibilidade Antimicrobiana de Diluição para Bactérias que Crescem Aerobicamente; Padrão Aprovado - Décima Edição. Documento CLSI M07-A10. Wayne, PA: Instituto de Padrões Clínicos e Laboratoriais; 2015.
4. CLSI. Métodos para Teste de Suscetibilidade Antimicrobiana de Bactérias Anaeróbias; Aprovado Standard-Oitava Edição. Documento CLSI M11-A8. Wayne, PA: Instituto de Padrões Clínicos e Laboratoriais; 2012.
5. CLSI. Padrões de Desempenho para Testes de Susceptibilidade de Disco Antimicrobiano; Padrão Aprovado - Décima Segunda Edição. Documento CLSI M02-A12. Wayne, PA: Instituto de Padrões Clínicos e Laboratoriais; 2015.
INFORMAÇÃO DO PACIENTE
Os pacientes devem ser informados de que medicamentos antibacterianos, incluindo CLEOCIN HCl, devem ser usados apenas para tratar infecções bacterianas. Eles não tratam infecções virais (por exemplo, o resfriado comum). Quando CLEOCIN HCl é prescrito para tratar uma infecção bacteriana, os pacientes devem ser informados de que, embora seja comum sentir-se melhor no início do tratamento, a medicação deve ser tomada exatamente como indicado. Pular doses ou não completar o curso completo da terapia pode (1) diminuir a eficácia do tratamento imediato e (2) aumentar a probabilidade de que as bactérias desenvolvam resistência e não sejam tratáveis por CLEOCIN 150mg HCl ou outros medicamentos antibacterianos no futuro.
diarreia é um problema comum causado por antibióticos que geralmente termina quando o antibiótico é descontinuado. Às vezes, após o início do tratamento com antibióticos, os pacientes podem desenvolver fezes aquosas e sanguinolentas (com ou sem cólicas estomacais e febre), mesmo dois ou mais meses após a última dose do antibiótico. Se isso ocorrer, os pacientes devem entrar em contato com seu médico o mais rápido possível.
