Naprosyn 250mg, 500mg Naproxen Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Naprosyn 500mg e como é usado?
Naprosyn 250mg é um medicamento de prescrição usado para tratar os sintomas de dor ou inflamação causada por artrite, espondilite anquilosante, tendinite, bursite, gota ou cólicas menstruais. Naprosyn pode ser usado sozinho ou com outros medicamentos.
Naprosyn 250mg é um medicamento anti-inflamatório não esteróide (AINE).
Não se sabe se Naprosyn é seguro e eficaz em crianças com menos de 2 anos de idade.
Quais são os possíveis efeitos colaterais do Naprosyn?
Naprosyn pode causar efeitos colaterais graves, incluindo:
- falta de ar,
- inchaço ou ganho de peso rápido,
- erupção cutânea ou bolhas,
- fezes com sangue ou alcatrão,
- tossir sangue ou vômito que parece borra de café,
- náusea,
- dor de estômago superior,
- perda de apetite,
- urina escura,
- fezes cor de barro,
- amarelecimento da pele ou dos olhos (icterícia),
- pouca ou nenhuma micção,
- dor ao urinar,
- inchaço nos pés ou tornozelos,
- anemia (glóbulos vermelhos baixos),
- pele pálida,
- cansaço,
- sentindo-se tonto, e
- mãos ou pés frios
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Naprosyn incluem:
- dor de cabeça,
- indigestão,
- azia, e
- sintomas da gripe
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Naprosyn. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
RISCO DE EVENTOS CARDIOVASCULARES E GASTROINTESTINAIS GRAVES
Eventos Trombóticos Cardiovasculares
- Os anti-inflamatórios não esteroides (AINEs) aumentam o risco de eventos trombóticos cardiovasculares graves, incluindo infarto do miocárdio e acidente vascular cerebral, que podem ser fatais. Este risco pode ocorrer no início do tratamento e pode aumentar com a duração do uso [ver ADVERTÊNCIAS E PRECAUÇÕES].
- NAPROSYN Tablets, EC-NAPROSYN e ANAPROX DS são contraindicados no contexto de cirurgia de revascularização do miocárdio (CRM) [consulte CONTRA-INDICAÇÕES, ADVERTÊNCIAS E PRECAUÇÕES].
Hemorragia, Ulceração e Perfuração Gastrointestinal
- Os AINEs causam um risco aumentado de eventos adversos gastrointestinais (GI) graves, incluindo sangramento, ulceração e perfuração do estômago ou intestinos, que podem ser fatais. Esses eventos podem ocorrer a qualquer momento durante o uso e sem sintomas de aviso. Pacientes idosos e pacientes com história prévia de úlcera péptica e/ou sangramento GI apresentam maior risco de eventos GI graves [ver ADVERTÊNCIAS E PRECAUÇÕES].
DESCRIÇÃO
Os comprimidos de NAPROSYN (naproxeno), os comprimidos de liberação retardada EC-NAPROSYN (naproxeno) e os comprimidos de ANAPROX DS (naproxeno sódico) são medicamentos anti-inflamatórios não esteroides disponíveis da seguinte forma: Os comprimidos de NAPROSYN 250mg estão disponíveis como comprimidos amarelos contendo 500mg de naproxeno para administração oral .
Os comprimidos de liberação retardada de EC-NAPROSYN estão disponíveis como comprimidos brancos com revestimento entérico contendo 375 mg de naproxeno ou 500 mg de naproxeno para administração oral.
Os comprimidos de ANAPROX DS estão disponíveis na forma de comprimidos azuis escuros contendo 550 mg de naproxeno sódico para administração oral.
naproxeno é um derivado do ácido propiônico relacionado ao grupo do ácido arilacético dos anti-inflamatórios não esteroides. Os nomes químicos para naproxeno e naproxeno sódico são ácido (S)-6-metoxi-α-metil-2-naftalenoacético e ácido (S)-6metoxi-α-metil-2-naftalenoacético, sal de sódio, respectivamente. Naproxeno tem um peso molecular de 230,26 e uma fórmula molecular de C14H14O3. Naproxeno sódico tem um peso molecular de 252,23 e uma fórmula molecular de C14H13NaO3. Naproxeno e naproxeno sódico têm as seguintes estruturas, respectivamente:
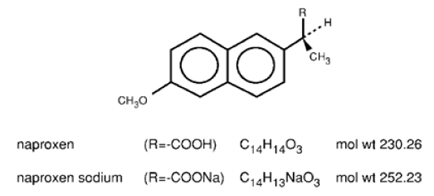
O naproxeno é uma substância cristalina inodora, branca a esbranquiçada. É lipossolúvel, praticamente insolúvel em água em pH baixo e livremente solúvel em água em pH alto. O coeficiente de partição octanol/água do naproxeno a pH 7,4 é de 1,6 a 1,8. O naproxeno sódico é um sólido cristalino branco a branco cremoso, livremente solúvel em água em pH neutro.
Os ingredientes inativos dos comprimidos de NAPROSYN 250mg incluem: croscarmelose sódica, óxidos de ferro, povidona e estearato de magnésio.
Os ingredientes inativos dos comprimidos de liberação retardada de EC-NAPROSYN incluem: croscarmelose sódica, povidona e estearato de magnésio. A dispersão de revestimento entérico contém copolímero de ácido metacrílico, talco, citrato de trietilo, hidróxido de sódio e água purificada. A impressão nas pastilhas é tinta preta. A dissolução deste comprimido de naproxeno com revestimento entérico depende do pH com rápida dissolução acima de pH 6. Não há dissolução abaixo de pH 4.
Os ingredientes inativos dos comprimidos de ANAPROX DS incluem: estearato de magnésio, celulose microcristalina, povidona e talco. A suspensão de revestimento pode conter hidroxipropilmetilcelulose 2910, Opaspray K-1-4227, polietilenoglicol 8000 ou Opadry YS-1-4216.
INDICAÇÕES
Os comprimidos NAPROSYN 500mg, EC-NAPROSYN 250mg e ANAPROX DS são indicados para:
o alívio dos sinais e sintomas de:
- artrite reumatoide
- osteoartrite
- espondilite anquilosante
- Artrite Idiopática Juvenil Poliarticular
Os comprimidos NAPROSYN e ANAPROX DS também são indicados para:
o alívio dos sinais e sintomas de:
- tendinite
- bursite
- gota aguda
a gestão de:
- dor
- dismenorreia primária
DOSAGEM E ADMINISTRAÇÃO
Instruções Gerais de Dosagem
Considere cuidadosamente os benefícios e riscos potenciais dos comprimidos de NAPROSYN, EC-NAPROSYN e ANAPROX DS e outras opções de tratamento antes de decidir usar comprimidos de NAPROSYN 250mg, EC-NAPROSYN 500mg e ANAPROX DS. Use a dose eficaz mais baixa para a duração mais curta consistente com os objetivos individuais do tratamento do paciente [ver AVISOS E PRECAUÇÕES ].
Após observar a resposta à terapia inicial com comprimidos de NAPROSYN 250mg, EC-NAPROSYN 500mg ou ANAPROX DS, a dose e a frequência devem ser ajustadas para atender às necessidades individuais de cada paciente.
Para manter a integridade do revestimento entérico, o comprimido de EC-NAPROSYN não deve ser quebrado, esmagado ou mastigado durante a ingestão.
Produtos contendo naproxeno, como NAPROSYN 500mg, EC-NAPROSYN 250mg e ANAPROX DS, e outros produtos de naproxeno não devem ser usados concomitantemente, pois todos circulam no plasma como ânion naproxeno.
Artrite reumatóide, osteoartrite e espondilite anquilosante
As dosagens recomendadas de comprimidos de NAPROSYN 500mg, ANAPROX DS e EC-NAPROSYN 250mg são mostradas na Tabela 1.
Durante a administração a longo prazo, a dose de naproxeno pode ser ajustada para cima ou para baixo dependendo da resposta clínica do paciente. Uma dose diária mais baixa pode ser suficiente para administração a longo prazo.
As doses da manhã e da noite não precisam ser iguais em tamanho e a administração do medicamento com mais frequência do que duas vezes ao dia geralmente não faz diferença na resposta.
Em pacientes que toleram bem doses mais baixas, a dose pode ser aumentada para naproxeno 1.500 mg/dia por períodos limitados de até 6 meses, quando é necessário um nível mais alto de atividade anti-inflamatória/analgésica. Ao tratar tais pacientes com naproxeno 1.500 mg/dia, o médico deve observar benefícios clínicos aumentados suficientes para compensar o risco potencial aumentado.
Artrite Idiopática Juvenil Poliarticular
As formas farmacêuticas sólidas orais de naproxeno podem não permitir a titulação flexível da dose necessária em pacientes pediátricos com artrite idiopática juvenil poliarticular. Uma formulação líquida pode ser mais apropriada para dosagem baseada no peso e devido à necessidade de flexibilidade de dose em crianças.
Em pacientes pediátricos, doses de 5 mg/kg/dia produziram níveis plasmáticos de naproxeno semelhantes aos observados em adultos tomando 500 mg de naproxeno [ver FARMACOLOGIA CLÍNICA ]. A dose diária total recomendada de naproxeno é de aproximadamente 10 mg/kg, dividida em 2 doses. A dosagem com NAPROSYN Tablets não é apropriada para crianças com peso inferior a 50 kg.
Tratamento da dor, dismenorreia primária e tendinite e bursite agudas
A dose inicial recomendada de ANAPROX DS (naproxeno sódico) comprimidos é de 550 mg, seguido de 550 mg a cada 12 horas ou 275 mg (metade de um comprimido de 550 mg) a cada 6 a 8 horas, conforme necessário. A dose diária total inicial não deve exceder 1375 mg (dois comprimidos e meio) de naproxeno sódico. A partir daí, a dose diária total não deve exceder 1100 mg de naproxeno sódico. Como o sal de sódio do naproxeno é absorvido mais rapidamente, ANAPROX DS é recomendado para o manejo de condições dolorosas agudas quando o início imediato do alívio da dor é desejado. Os comprimidos de NAPROSYN também podem ser usados. A dose inicial recomendada de NAPROSYN comprimidos é de 500 mg, seguida de 250 mg (metade de um comprimido de 500 mg de NAPROSYN) a cada 6-8 horas, conforme necessário. A dose diária total não deve exceder 1250 mg de naproxeno.
EC-NAPROSYN 250mg não é recomendado para o tratamento inicial da dor aguda porque a absorção do naproxeno é retardada em comparação com outros produtos contendo naproxeno [ver FARMACOLOGIA CLÍNICA ].
Gota Aguda
A dose inicial recomendada é de 750 mg (um comprimido e meio) de NAPROSYN 250 mg comprimidos seguidos de 250 mg (meio comprimido) a cada 8 horas até que a crise desapareça. ANAPROX DS também pode ser usado na dose inicial de 825 mg (um comprimido e meio) seguido de 275 mg (meio comprimido) a cada 8 horas. EC-NAPROSYN não é recomendado devido ao atraso na absorção.
Não intercambialidade com outras formulações de naproxeno
Diferentes dosagens e formulações (por exemplo, comprimidos, suspensão) de naproxeno não são intercambiáveis. Essa diferença deve ser levada em consideração ao alterar dosagens ou formulações.
COMO FORNECIDO
Formas de dosagem e pontos fortes
Comprimidos de NAPROSYN® (naproxeno): 500 mg: amarelos, em forma de cápsula, gravados com NPR LE 500 de um lado e sulcados do outro.
EC-NAPROSYN® (naproxeno) comprimidos de liberação retardada: 375 mg: comprimidos revestidos brancos, ovais, biconvexos, impressos com NPR EC 375 em um lado.
EC-NAPROSYN® (naproxeno) comprimidos de liberação retardada: 500 mg: comprimidos revestidos oblongos brancos com NPR EC 500 impresso em um lado.
Comprimidos de ANAPROX® DS (naproxeno sódico): 550 mg: azul escuro, oblongo, gravado com NPS 550 de um lado e ranhurado em ambos os lados.
Armazenamento e manuseio
NAPROSYN (naproxeno) comprimidos 500 mg : comprimidos amarelos em forma de cápsula, gravados com NPR LE 500 numa das faces e ranhurados na outra. Embalado em frascos resistentes à luz de 100. Fornecido como:
NDC 69437-316-01 100's (garrafa)
Armazenar de 15°C a 30°C (59°F a 86°F) em recipientes bem fechados; dispensar em recipientes resistentes à luz.
EC-NAPROSYN (naproxeno) comprimidos de liberação retardada 375 mg : comprimidos revestidos brancos, ovais, biconvexos, impressos com NPR EC 375 em um dos lados. Embalado em frascos resistentes à luz de 100. Fornecido como:
NDC 69437-415-01 100's (garrafa)
500 mg comprimidos revestidos oblongos brancos com NPR EC 500 impresso em um lado. Embalado em frascos resistentes à luz de 100. Fornecido como:
NDC 69437-416-01 100's (garrafa)
Armazenar de 15°C a 30°C (59°F a 86°F) em recipientes bem fechados; dispensar em recipientes resistentes à luz.
ANAPROX DS (naproxeno sódico) Comprimidos 550 mg : comprimidos azuis escuros, oblongos, gravados com NPS 550 numa das faces e ranhurados nas duas faces. Embalado em garrafas de 100. Fornecido como:
NDC 69437-203-01 100's (garrafa)
Armazenar a 15° a 30°C (59° a 86°F) em recipientes bem fechados.
Fabricado para: Atnahs Pharma, Miles Gray Road, Basildon, Essex, SS14 3FR, Reino Unido. Distribuído por: Canton Laboratories, LLC., Alpharetta, GA 30004-5945, Estados Unidos. Revisado: abril de 2021
EFEITOS COLATERAIS
As seguintes reações adversas são discutidas em mais detalhes em outras seções da bula:
- Eventos Trombóticos Cardiovasculares [ver AVISOS E PRECAUÇÕES ]
- Sangramento, Ulceração e Perfuração GI [ver AVISOS E PRECAUÇÕES ]
- Hepatotoxicidade [ver AVISOS E PRECAUÇÕES ]
- Hipertensão [ver AVISOS E PRECAUÇÕES ]
- Insuficiência Cardíaca e Edema [ver AVISOS E PRECAUÇÕES ]
- Toxicidade renal e hipercalemia [ver AVISOS E PRECAUÇÕES ]
- Reações anafiláticas [ver AVISOS E PRECAUÇÕES ]
- Reações cutâneas graves [ver AVISOS E PRECAUÇÕES ]
- Toxicidade hematológica [ver AVISOS E PRECAUÇÕES ]
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
As reações adversas relatadas em ensaios clínicos controlados em 960 pacientes tratados para artrite reumatoide ou osteoartrite estão listadas abaixo. Em geral, as reações em pacientes tratados cronicamente foram relatadas 2 a 10 vezes mais frequentemente do que em estudos de curto prazo nos 962 pacientes tratados para dor leve a moderada ou para dismenorreia. As queixas mais frequentes relatadas estavam relacionadas ao trato gastrointestinal.
Um estudo clínico descobriu que as reações gastrointestinais são mais frequentes e mais graves em pacientes com artrite reumatoide que tomam doses diárias de 1500 mg de naproxeno em comparação com aqueles que tomam 750 mg de naproxeno.
Em ensaios clínicos controlados com cerca de 80 pacientes pediátricos e em estudos abertos e bem monitorados com cerca de 400 pacientes pediátricos com artrite idiopática juvenil poliarticular tratados com naproxeno, a incidência de erupções cutâneas e tempos de sangramento prolongados foram maiores, a incidência de doenças gastrointestinais e centrais as reações do sistema nervoso foram aproximadamente as mesmas, e a incidência de outras reações foi menor em pacientes pediátricos do que em adultos.
Em pacientes que tomaram naproxeno em ensaios clínicos, as experiências adversas mais frequentemente relatadas em aproximadamente 1% a 10% dos pacientes foram:
Experiências gastrointestinais (GI), incluindo: azia*, dor abdominal*, náuseas*, prisão de ventre*, diarreia, dispepsia, estomatite
Sistema nervoso central: dor de cabeça*, tontura*, sonolência*, tontura, vertigem
Dermatológico: prurido (comichão)*, erupções cutâneas*, equimoses*, sudorese, púrpura
Sentidos Especiais: zumbido*, distúrbios visuais, distúrbios auditivos
Cardiovascular: edema*, palpitações
Em geral: dispneia*, sede
*Incidência de reação relatada entre 3% e 9%. As reações que ocorrem em menos de 3% dos pacientes não são marcadas.
Em pacientes tomando AINEs, as seguintes experiências adversas também foram relatadas em aproximadamente 1% a 10% dos pacientes.
Experiências gastrointestinais (GI), incluindo: flatulência, sangramento grave/perfuração, úlceras gastrointestinais (gástricas/duodenais), vômitos
Em geral: função renal anormal, anemia, enzimas hepáticas elevadas, aumento do tempo de sangramento, erupções cutâneas
A seguir estão as experiências adversas adicionais relatadas em
Gastrointestinal: pancreatite, vômito
Hepatobiliar: icterícia
Hemico e Linfático: melena, trombocitopenia, agranulocitose
Sistema nervoso: incapacidade de se concentrar
Dermatológico: erupções cutâneas
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de naproxeno. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
A seguir estão as experiências adversas adicionais relatadas em
Corpo como um todo: reações anafilactóides, edema angioneurótico, distúrbios menstruais, pirexia (calafrios e febre)
Cardiovascular: insuficiência cardíaca congestiva, vasculite, hipertensão, edema pulmonar
Gastrointestinal: inflamação, sangramento (às vezes fatal, particularmente em idosos), ulceração, perfuração e obstrução do trato gastrointestinal superior ou inferior. Esofagite, estomatite, hematêmese, colite, exacerbação de doença inflamatória intestinal (colite ulcerativa, doença de Crohn).
Hepatobiliar: testes de função hepática anormais, hepatite (alguns casos foram fatais)
Hemico e Linfático: eosinofilia, leucopenia, granulocitopenia, anemia hemolítica, anemia aplástica
Metabólico e Nutricional: hiperglicemia, hipoglicemia
Sistema nervoso: depressão, anormalidades dos sonhos, insônia, mal-estar, mialgia, fraqueza muscular, meningite asséptica, disfunção cognitiva, convulsões
Respiratório: pneumonite eosinofílica, asma
Dermatológico: alopecia, urticária, necrólise epidérmica tóxica, eritema multiforme, eritema nodoso, erupção medicamentosa fixa, líquen plano, reação pustulosa, lúpus eritematoso sistêmico, reações bolhosas, incluindo síndrome de Stevens-Johnson, dermatite fotossensível, reações de fotossensibilidade, incluindo casos raros semelhantes a porfiria cutânea tardia (pseudoporfiria) ou epidermólise bolhosa. Se ocorrer fragilidade da pele, bolhas ou outros sintomas sugestivos de pseudoporfiria, o tratamento deve ser descontinuado e o paciente monitorado.
Sentidos Especiais: deficiência auditiva, opacidade da córnea, papilite, neurite óptica retrobulbar, papiledema
Urogenital: nefrite glomerular, hematúria, hipercalemia, nefrite intersticial, síndrome nefrótica, doença renal, insuficiência renal, necrose papilar renal, creatinina sérica elevada
Reprodução (fêmea): infertilidade
Em pacientes tomando AINEs, as seguintes experiências adversas também foram relatadas em
Corpo como um todo: febre, infecção, sepse, reações anafiláticas, alterações do apetite, morte
Cardiovascular: hipertensão, taquicardia, síncope, arritmia, hipotensão, infarto do miocárdio
Gastrointestinal: boca seca, esofagite, úlceras gástricas/pépticas, gastrite, glossite, eructação
Hepatobiliar: hepatite, insuficiência hepática
Hemico e Linfático: sangramento retal, linfadenopatia, pancitopenia
Metabólico e Nutricional: mudanças de peso
Sistema nervoso: ansiedade, astenia, confusão, nervosismo, parestesia, sonolência, tremores, convulsões, coma, alucinações
Respiratório: asma, depressão respiratória, pneumonia
Dermatológico: dermatite esfoliativa
Sentidos Especiais: visão turva, conjuntivite
Urogenital: cistite, disúria, oligúria/poliúria, proteinúria
INTERAÇÕES MEDICAMENTOSAS
Consulte a Tabela 1 para interações medicamentosas clinicamente significativas com naproxeno.
Interações Medicamentos/Testes Laboratoriais
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Eventos Trombóticos Cardiovasculares
Ensaios clínicos de vários AINEs seletivos e não seletivos de COX-2 com duração de até três anos mostraram um risco aumentado de eventos trombóticos cardiovasculares (CV) graves, incluindo infarto do miocárdio (IM) e acidente vascular cerebral, que podem ser fatais. Com base nos dados disponíveis, não está claro que o risco de eventos trombóticos CV seja semelhante para todos os AINEs. O aumento relativo de eventos trombóticos CV graves em relação à linha de base conferida pelo uso de AINEs parece ser semelhante naqueles com e sem doença CV conhecida ou fatores de risco para doença CV. No entanto, pacientes com doença CV conhecida ou fatores de risco tiveram uma incidência absoluta mais alta de excesso de eventos trombóticos CV graves, devido ao aumento da taxa basal. Alguns estudos observacionais descobriram que esse risco aumentado de eventos trombóticos CV graves começou logo nas primeiras semanas de tratamento. O aumento do risco trombótico CV foi observado de forma mais consistente em doses mais elevadas.
Para minimizar o risco potencial de um evento CV adverso em pacientes tratados com AINEs, use a menor dose eficaz pelo menor tempo possível. Médicos e pacientes devem permanecer alertas para o desenvolvimento de tais eventos, durante todo o curso do tratamento, mesmo na ausência de sintomas CV prévios. Os pacientes devem ser informados sobre os sintomas de eventos CV graves e as medidas a serem tomadas se ocorrerem.
Não há evidências consistentes de que o uso concomitante de aspirina reduza o risco aumentado de eventos trombóticos CV graves associados ao uso de AINEs. O uso concomitante de aspirina e um AINE, como o naproxeno, aumenta o risco de eventos gastrointestinais (GI) graves.
Status Pós Cirurgia de Revascularização do Miocárdio (CRM)
Dois grandes ensaios clínicos controlados de um AINE seletivo para COX-2 para o tratamento da dor nos primeiros 10-14 dias após a cirurgia de revascularização do miocárdio encontraram um aumento na incidência de infarto do miocárdio e acidente vascular cerebral. Os AINEs são contraindicados no contexto de CRM [ver CONTRA-INDICAÇÕES ].
Pacientes pós-IM
Estudos observacionais conduzidos no Registro Nacional Dinamarquês demonstraram que pacientes tratados com AINEs no período pós-IM apresentaram risco aumentado de reinfarto, morte relacionada a CV e mortalidade por todas as causas a partir da primeira semana de tratamento. Nesta mesma coorte, a incidência de morte no primeiro ano pós-IAM foi de 20 por 100 pessoas-ano em pacientes tratados com AINEs em comparação com 12 por 100 pessoas-anos em pacientes não expostos a AINEs. Embora a taxa absoluta de morte tenha diminuído um pouco após o primeiro ano pós-IM, o aumento do risco relativo de morte em usuários de AINEs persistiu durante pelo menos os próximos quatro anos de acompanhamento.
Evite o uso de NAPROSYN Tablets, EC-NAPROSYN e ANAPROX DS em pacientes com infarto do miocárdio recente, a menos que se espere que os benefícios superem o risco de eventos trombóticos CV recorrentes. Se os comprimidos de NAPROSYN 250mg, EC-NAPROSYN e ANAPROX DS forem usados em pacientes com infarto do miocárdio recente, monitore os pacientes quanto a sinais de isquemia cardíaca.
Hemorragia, ulceração e perfuração gastrointestinais
Os AINEs, incluindo o naproxeno, causam eventos adversos gastrointestinais (GI) graves, incluindo inflamação, sangramento, ulceração e perfuração do esôfago, estômago, intestino delgado ou intestino grosso, que podem ser fatais. Esses eventos adversos graves podem ocorrer a qualquer momento, com ou sem sintomas de alerta, em pacientes tratados com AINEs.
Apenas um em cada cinco pacientes que desenvolvem um evento adverso grave no trato GI superior na terapia com AINEs é sintomático. Úlceras do trato GI superior, sangramento grave ou perfuração causada por AINEs ocorreram em aproximadamente 1% dos pacientes tratados por 3-6 meses e em cerca de 2%-4% dos pacientes tratados por um ano. No entanto, mesmo a terapia com AINEs de curto prazo não é isenta de riscos.
Fatores de risco para sangramento GI, ulceração e perfuração
Pacientes com história prévia de úlcera péptica e/ou sangramento GI que usaram AINEs tiveram um risco 10 vezes maior de desenvolver sangramento GI em comparação com pacientes sem esses fatores de risco. Outros fatores que aumentam o risco de sangramento GI em pacientes tratados com AINEs incluem maior duração da terapia com AINEs; uso concomitante de corticosteroides orais, aspirina, anticoagulantes ou inibidores seletivos da recaptação da serotonina (ISRS); fumar; uso de álcool; idoso; e mau estado geral de saúde. A maioria dos relatos pós-comercialização de eventos gastrointestinais fatais ocorreu em pacientes idosos ou debilitados. Além disso, pacientes com doença hepática avançada e/ou coagulopatia apresentam risco aumentado de sangramento GI.
Estratégias para minimizar os riscos gastrointestinais em pacientes tratados com AINEs
- Use a dosagem eficaz mais baixa para a duração mais curta possível.
- Evite a administração de mais de um AINE de cada vez.
- Evite o uso em pacientes de alto risco, a menos que se espere que os benefícios superem o risco aumentado de sangramento. Para esses pacientes, bem como aqueles com sangramento GI ativo, considere terapias alternativas além dos AINEs.
- Permaneça alerta para sinais e sintomas de ulceração GI e sangramento durante a terapia com AINEs.
- Se houver suspeita de um evento adverso GI grave, inicie imediatamente a avaliação e o tratamento e descontinue NAPROSYN Tablets, EC-NAPROSYN ou ANAPROX DS até que um evento adverso GI grave seja descartado.
- No caso de uso concomitante de aspirina em baixas doses para profilaxia cardíaca, monitore os pacientes mais de perto quanto a evidências de sangramento GI [ver INTERAÇÕES MEDICAMENTOSAS ].
Hepatotoxicidade
Elevações de ALT ou AST (três ou mais vezes o limite superior do normal [LSN]) foram relatadas em aproximadamente 1% dos pacientes tratados com AINEs em ensaios clínicos. Além disso, casos raros, às vezes fatais, de lesão hepática grave, incluindo hepatite fulminante, necrose hepática e insuficiência hepática foram relatados.
Elevações de ALT ou AST (menos de três vezes o LSN) podem ocorrer em até 15% dos pacientes tratados com AINEs, incluindo naproxeno.
Informe os pacientes sobre os sinais e sintomas de alerta de hepatotoxicidade (p. Se surgirem sinais e sintomas clínicos consistentes com doença hepática, ou se ocorrerem manifestações sistêmicas (por exemplo, eosinofilia, erupção cutânea, etc.), descontinue NAPROSYN 500mg comprimidos, EC-NAPROSYN 250mg ou ANAPROX DS imediatamente e realize uma avaliação clínica do paciente .
Hipertensão
Os AINEs, incluindo NAPROSYN 250mg Comprimidos, EC-NAPROSYN e ANAPROX DS, podem levar a um novo aparecimento de hipertensão ou agravamento de hipertensão pré-existente, qualquer um dos quais pode contribuir para o aumento da incidência de eventos CV. Pacientes em uso de inibidores da enzima conversora de angiotensina (ECA), diuréticos tiazídicos ou diuréticos de alça podem apresentar resposta prejudicada a essas terapias ao tomar AINEs [ver INTERAÇÕES MEDICAMENTOSAS ].
Monitorar a pressão arterial (PA) durante o início do tratamento com AINEs e durante o curso da terapia.
Insuficiência Cardíaca e Edema
A meta-análise do Coxib e a tradicional NSAID Trialists' Collaboration de ensaios clínicos randomizados demonstraram um aumento de aproximadamente duas vezes nas hospitalizações por insuficiência cardíaca em pacientes tratados com COX-2 seletivo e pacientes tratados com NSAID não seletivos em comparação com pacientes tratados com placebo. Em um estudo do Registro Nacional Dinamarquês de pacientes com insuficiência cardíaca, o uso de AINEs aumentou o risco de infarto do miocárdio, hospitalização por insuficiência cardíaca e morte.
Além disso, retenção de líquidos e edema foram observados em alguns pacientes tratados com AINEs. O uso de naproxeno pode atenuar os efeitos CV de vários agentes terapêuticos usados para tratar essas condições médicas (por exemplo, diuréticos, inibidores da ECA ou bloqueadores dos receptores da angiotensina [BRA]) [ver INTERAÇÕES MEDICAMENTOSAS ].
Evite o uso de comprimidos de NAPROSYN 250mg, EC-NAPROSYN ou ANAPROX DS em pacientes com insuficiência cardíaca grave, a menos que se espere que os benefícios superem o risco de agravamento da insuficiência cardíaca. Se NAPROSYN 250mg Comprimidos, EC-NAPROSYN 250mg ou ANAPROX DS for usado em pacientes com insuficiência cardíaca grave, monitore os pacientes quanto a sinais de piora da insuficiência cardíaca.
Como cada comprimido de ANAPROX DS contém 50 mg de sódio (cerca de 2 mEq por cada 500 mg de naproxeno), isso deve ser considerado em pacientes cuja ingestão global de sódio deve ser severamente restrita.
Toxicidade renal e hipercalemia
Toxicidade renal
A administração a longo prazo de AINEs resultou em necrose papilar renal e outras lesões renais.
toxicidade renal também foi observada em pacientes nos quais as prostaglandinas renais têm um papel compensatório na manutenção da perfusão renal. Nesses pacientes, a administração de um AINE pode causar uma redução dose-dependente na formação de prostaglandinas e, secundariamente, no fluxo sanguíneo renal, o que pode precipitar uma descompensação renal evidente. Os pacientes com maior risco dessa reação são aqueles com função renal comprometida, desidratação, hipovolemia, insuficiência cardíaca, disfunção hepática, aqueles que tomam diuréticos e inibidores da ECA ou BRAs e os idosos. A descontinuação da terapia com AINEs geralmente é seguida pela recuperação ao estado pré-tratamento.
Não há informações disponíveis de estudos clínicos controlados sobre o uso de NAPROSYN 500mg comprimidos, EC-NAPROSYN ou ANAPROX DS em pacientes com doença renal avançada. Os efeitos renais de NAPROSYN 500mg comprimidos, EC-NAPROSYN ou ANAPROX DS podem acelerar a progressão da disfunção renal em pacientes com doença renal preexistente.
Corrija o status do volume em pacientes desidratados ou hipovolêmicos antes de iniciar NAPROSYN Tablets, EC-NAPROSYN 250mg ou ANAPROX DS. Monitorar a função renal em pacientes com insuficiência renal ou hepática, insuficiência cardíaca, desidratação ou hipovolemia durante o uso de comprimidos de NAPROSYN 500mg, EC-NAPROSYN e ANAPROX DS [ver INTERAÇÕES MEDICAMENTOSAS ]. Evite o uso de NAPROSYN 250mg comprimidos, EC-NAPROSYN 500mg e ANAPROX DS em pacientes com doença renal avançada, a menos que se espere que os benefícios superem o risco de piora da função renal. Se NAPROSYN 500mg comprimidos, EC-NAPROSYN 500mg ou ANAPROX DS for usado em pacientes com doença renal avançada, monitore os pacientes quanto a sinais de piora da função renal.
Hipercalemia
Aumentos na concentração sérica de potássio, incluindo hipercalemia, foram relatados com o uso de AINEs, mesmo em alguns pacientes sem insuficiência renal. Em pacientes com função renal normal, esses efeitos foram atribuídos a um estado de hiporreninamiquipoaldosteronismo.
Reações anafiláticas
naproxeno tem sido associado a reações anafiláticas em pacientes com e sem hipersensibilidade conhecida ao naproxeno e em pacientes com asma sensível à aspirina. CONTRA-INDICAÇÕES e AVISOS E PRECAUÇÕES ].
Procure ajuda de emergência se ocorrer uma reação anafilática.
Exacerbação da asma relacionada à sensibilidade à aspirina
Uma subpopulação de pacientes com asma pode ter asma sensível à aspirina, que pode incluir rinossinusite crônica complicada por pólipos nasais; broncoespasmo grave e potencialmente fatal; e/ou intolerância à aspirina e outros AINEs.
Como a reatividade cruzada entre aspirina e outros AINEs foi relatada em pacientes sensíveis à aspirina, os comprimidos de NAPROSYN 250mg, EC-NAPROSYN 500mg e ANAPROX DS são contraindicados em pacientes com essa forma de sensibilidade à aspirina [ver CONTRA-INDICAÇÕES ]. Quando os comprimidos de NAPROSYN 250mg, EC-NAPROSYN 250mg ou ANAPROX DS são usados em pacientes com asma preexistente (sem sensibilidade conhecida à aspirina), monitore os pacientes quanto a alterações nos sinais e sintomas da asma.
Reações cutâneas graves
Os AINEs, incluindo o naproxeno, podem causar reações adversas graves na pele, como dermatite esfoliativa, síndrome de Stevens-Johnson (SSJ) e necrólise epidérmica tóxica (NET), que podem ser fatais. Esses eventos graves podem ocorrer sem aviso prévio. Informar os pacientes sobre os sinais e sintomas de reações cutâneas graves e descontinuar o uso de NAPROSYN 250mg comprimidos, EC-NAPROSYN 500mg ou ANAPROX DS ao primeiro aparecimento de erupção cutânea ou qualquer outro sinal de hipersensibilidade. Os comprimidos de NAPROSYN, EC-NAPROSYN e ANAPROX DS são contraindicados em pacientes com reações cutâneas graves prévias a AINEs [ver CONTRA-INDICAÇÕES ].
Reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS)
Reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS) foi relatada em pacientes tomando AINEs, como NAPROSYN Tablets, EC-NAPROSYN 500mg e ANAPROX DS. Alguns desses eventos foram fatais ou com risco de vida. DRESS tipicamente, embora não exclusivamente, apresenta febre, erupção cutânea, linfadenopatia e/ou edema facial. Outras manifestações clínicas podem incluir hepatite, nefrite, anormalidades hematológicas, miocardite ou miosite. Às vezes, os sintomas do DRESS podem se assemelhar a uma infecção viral aguda. A eosinofilia está frequentemente presente. Como esse distúrbio é variável em sua apresentação, outros sistemas orgânicos não mencionados aqui podem estar envolvidos. É importante notar que manifestações precoces de hipersensibilidade, como febre ou linfadenopatia, podem estar presentes, mesmo que a erupção não seja evidente. Se tais sinais ou sintomas estiverem presentes, interrompa os comprimidos de NAPROSYN 500mg, EC-NAPROSYN e ANAPROX DS e avalie o paciente imediatamente.
Toxicidade Fetal
Fechamento prematuro do canal arterial fetal
Evite o uso de AINEs, incluindo comprimidos de NAPROSYN 500mg, EC-NAPROSYN e ANAPROX DS, em mulheres grávidas com cerca de 30 semanas de gestação e mais tarde. AINEs, incluindo NAPROSYN 500mg comprimidos, EC-NAPROSYN e ANAPROX DS, aumentam o risco de fechamento prematuro do canal arterial fetal aproximadamente nesta idade gestacional.
Oligoidrâmnio/Insuficiência Renal Neonatal
uso de AINEs, incluindo comprimidos de NAPROSYN, EC-NAPROSYN 250mg e ANAPROX DS, por volta da 20ª semana de gestação ou mais tarde na gravidez, pode causar disfunção renal fetal levando a oligoidrâmnio e, em alguns casos, insuficiência renal neonatal. Esses resultados adversos são observados, em média, após dias a semanas de tratamento, embora oligoidrâmnios tenham sido relatados com pouca frequência tão logo 48 horas após o início dos AINEs. O oligoidrâmnio é frequentemente, mas nem sempre, reversível com a descontinuação do tratamento. As complicações do oligoidrâmnio prolongado podem, por exemplo, incluir contraturas dos membros e maturação pulmonar retardada. Em alguns casos pós-comercialização de insuficiência renal neonatal, foram necessários procedimentos invasivos, como exsanguineotransfusão ou diálise.
Se o tratamento com AINE for necessário entre cerca de 20 semanas e 30 semanas de gestação, limite o uso de NAPROSYN 250mg comprimidos, EC-NAPROSYN 250mg ou ANAPROX DS à menor dose eficaz e menor duração possível. Considere o monitoramento por ultrassom do líquido amniótico se o tratamento com NAPROSYN Tablets, EC-NAPROSYN ou ANAPROX DS se estender além de 48 horas. Interrompa os comprimidos de NAPROSYN 500mg, EC-NAPROSYN e ANAPROX DS se ocorrer oligoidrâmnio e faça o acompanhamento de acordo com a prática clínica [ver Uso em populações específicas ].
Toxicidade hematológica
Anemia ocorreu em pacientes tratados com AINEs. Isso pode ser devido à perda de sangue oculta ou grosseira, retenção de líquidos ou um efeito descrito de forma incompleta na eritropoiese. Se um paciente tratado com NAPROSYN Tablets, EC-NAPROSYN 500mg ou ANAPROX DS apresentar quaisquer sinais ou sintomas de anemia, monitore a hemoglobina ou o hematócrito.
AINEs, incluindo comprimidos de NAPROSYN, EC-NAPROSYN e ANAPROX DS, podem aumentar o risco de eventos hemorrágicos. Condições comórbidas, como distúrbios de coagulação ou uso concomitante de varfarina e outros anticoagulantes, agentes antiplaquetários (p. Monitore esses pacientes quanto a sinais de sangramento [ver INTERAÇÕES MEDICAMENTOSAS ].
Mascaramento de inflamação e febre
A atividade farmacológica de NAPROSYN Tablets, EC-NAPROSYN 500mg e ANAPROX DS na redução da inflamação e, possivelmente, da febre, pode diminuir a utilidade dos sinais diagnósticos na detecção de infecções.
Uso a longo prazo e monitoramento laboratorial
Como sangramento GI grave, hepatotoxicidade e lesão renal podem ocorrer sem sinais ou sintomas de alerta, considere monitorar os pacientes em tratamento prolongado com AINEs com hemograma e perfil químico periodicamente [ver AVISOS E PRECAUÇÕES ].
Pacientes com valores iniciais de hemoglobina de 10g ou menos que devem receber terapia de longo prazo devem ter os valores de hemoglobina determinados periodicamente.
Devido aos achados oculares adversos em estudos com animais desta classe, recomenda-se a realização de estudos oftalmológicos se ocorrer qualquer alteração ou distúrbio na visão.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler a rotulagem do paciente aprovada pela FDA (Guia de Medicação) que acompanha cada prescrição dispensada. Informe os pacientes, familiares ou seus cuidadores sobre as seguintes informações antes de iniciar a terapia com NAPROSYN Tablets, EC-NAPROSYN ou ANAPROX DS e periodicamente durante o curso da terapia em andamento.
Eventos Trombóticos Cardiovasculares
Aconselhe os pacientes a ficarem alertas para os sintomas de eventos trombóticos cardiovasculares, incluindo dor no peito, falta de ar, fraqueza ou fala arrastada, e relatar qualquer um desses sintomas ao seu médico imediatamente [ver AVISOS E PRECAUÇÕES ].
Hemorragia, ulceração e perfuração gastrointestinais
Aconselhe os pacientes a relatar sintomas de ulcerações e sangramento, incluindo dor epigástrica, dispepsia, melena e hematêmese ao seu médico. No caso de uso concomitante de aspirina em baixas doses para profilaxia cardíaca, informe os pacientes sobre o risco aumentado e os sinais e sintomas de sangramento GI [ver AVISOS E PRECAUÇÕES ].
Hepatotoxicidade
Informe os pacientes sobre os sinais e sintomas de alerta de hepatotoxicidade (p. Se isso ocorrer, instrua os pacientes a interromper os comprimidos de NAPROSYN 500mg, EC-NAPROSYN 250mg ou ANAPROX DS e procurar terapia médica imediata [ver AVISOS E PRECAUÇÕES ].
Insuficiência Cardíaca e Edema
Aconselhe os pacientes a ficarem atentos aos sintomas de insuficiência cardíaca congestiva, incluindo falta de ar, ganho de peso inexplicável ou edema, e a entrar em contato com seu médico se tais sintomas ocorrerem [ver AVISOS E PRECAUÇÕES ].
Reações anafiláticas
Informe os pacientes sobre os sinais de uma reação anafilática (por exemplo, dificuldade em respirar, inchaço da face ou garganta). Instrua os pacientes a procurar ajuda de emergência imediata se isso ocorrer [ver CONTRA-INDICAÇÕES e AVISOS E PRECAUÇÕES ].
Reações cutâneas graves, incluindo DRESS
Aconselhe os pacientes a parar de tomar NAPROSYN 250mg comprimidos, EC-NAPROSYN 500mg ou ANAPROX DS imediatamente se desenvolverem qualquer tipo de erupção cutânea ou febre e entrar em contato com seu médico o mais rápido possível [ver AVISOS E PRECAUÇÕES ].
Fertilidade Feminina
Aconselhe as mulheres com potencial reprodutivo que desejam engravidar que os AINEs, incluindo NAPROSYN Tablets, ECNAPROSYN 250mg e ANAPROX DS, podem estar associados a um atraso reversível na ovulação (ver Uso em populações específicas .]
Toxicidade Fetal
Informar as mulheres grávidas para evitar o uso de comprimidos de NAPROSYN 250mg, EC-NAPROSYN ou ANAPROX DS e outros AINEs a partir de 30 semanas de gestação devido ao risco de fechamento prematuro do canal arterial fetal. Se o tratamento com NAPROSYN Tablets, EC-NAPROSYN 500mg ou ANAPROX DS for necessário para uma gestante entre cerca de 20 a 30 semanas de gestação, informe que ela pode precisar ser monitorada para oligoidrâmnio, se o tratamento continuar por mais de 48 horas [ver AVISOS E PRECAUÇÕES e Uso em populações específicas ].
Evite o uso concomitante de AINEs
Informe os pacientes que o uso concomitante de NAPROSYN Tablets, EC-NAPROSYN 500mg e ANAPROX DS com outros AINEs ou salicilatos (por exemplo, diflunisal, salsalato) não é recomendado devido ao risco aumentado de toxicidade gastrointestinal e pouco ou nenhum aumento na eficácia [ver AVISOS E PRECAUÇÕES e INTERAÇÕES MEDICAMENTOSAS ]. Alertar os pacientes de que os AINEs podem estar presentes em medicamentos de venda livre para o tratamento de resfriados, febre ou insônia.
Uso de AINEs e aspirina em baixas doses
Informe os pacientes para não usar aspirina em baixas doses concomitantemente com NAPROSYN 500mg comprimidos, EC-NAPROSYN e ANAPROX DS até que conversem com seu médico [ver INTERAÇÕES MEDICAMENTOSAS ].
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Carcinogênese
Um estudo de 2 anos foi realizado em ratos para avaliar o potencial carcinogênico do naproxeno em doses de ratos de 8, 16 e 24 mg/kg/dia (0,05, 0,1 e 0,16 vezes a dose diária humana máxima recomendada [MRHD] de 1500 mg/dia com base na comparação da área de superfície corporal). Nenhuma evidência de tumorigenicidade foi encontrada.
Mutagênese
O naproxeno apresentou resultado positivo no ensaio de troca de cromátides irmãs in vivo, mas não foi mutagênico no ensaio de mutação reversa bacteriana in vitro (teste de Ames).
Prejuízo da Fertilidade
Ratos machos foram tratados com 2, 5, 10 e 20 mg/kg de naproxeno por gavagem oral por 60 dias antes do acasalamento e ratos fêmeas foram tratados com as mesmas doses por 14 dias antes do acasalamento e nos primeiros 7 dias de gestação. Não foram observados efeitos adversos na fertilidade (até 0,13 vezes o MRDH com base na área de superfície corporal).
Uso em populações específicas
Gravidez
Resumo do risco
O uso de AINEs, incluindo comprimidos de NAPROSYN 250mg, EC-NAPROSYN e ANAPROX DS, pode causar fechamento prematuro do canal arterial fetal e disfunção renal fetal levando a oligoidrâmnio e, em alguns casos, insuficiência renal neonatal. Devido a esses riscos, limite a dose e a duração do uso de NAPROSYN Tablets, EC-NAPROSYN 500mg ou ANAPROX DS entre cerca de 20 e 30 semanas de gestação e evite o uso de NAPROSYN 500mg Tablets, EC-NAPROSYN e ANAPROX DS em cerca de 30 semanas de gestação e mais tarde na gravidez (ver Considerações Clínicas , Dados ).
Fechamento prematuro do canal arterial fetal
uso de AINEs, incluindo comprimidos de NAPROSYN, EC-NAPROSYN e ANAPROX DS, por volta de 30 semanas de gestação ou mais tarde na gravidez, aumenta o risco de fechamento prematuro do canal arterial fetal.
Oligoidrâmnio/Insuficiência Renal Neonatal
O uso de AINEs com cerca de 20 semanas de gestação ou mais tarde na gravidez tem sido associado a casos de disfunção renal fetal levando a oligoidrâmnio e, em alguns casos, insuficiência renal neonatal.
Os dados de estudos observacionais sobre outros riscos embriofetais potenciais do uso de AINEs em mulheres no primeiro ou segundo trimestre de gravidez são inconclusivos. Em estudos de reprodução animal em ratos, coelhos e camundongos, não há evidência de teratogenicidade ou dano fetal quando o naproxeno foi administrado durante o período de organogênese em doses de 0,13, 0,26 e 0,6 vezes a dose diária humana máxima recomendada de 1.500 mg/dia, respectivamente. Vejo Dados ]. Com base em dados de animais, as prostaglandinas demonstraram ter um papel importante na permeabilidade vascular endometrial, implantação de blastocistos e decidualização. Em estudos com animais, a administração de inibidores da síntese de prostaglandinas, como o naproxeno, resultou em aumento da perda pré e pós-implantação. As prostaglandinas também demonstraram ter um papel importante no desenvolvimento do rim fetal. Em estudos publicados em animais, foi relatado que os inibidores da síntese de prostaglandinas prejudicam o desenvolvimento renal quando administrados em doses clinicamente relevantes.
O risco de fundo estimado de defeitos congênitos graves e aborto para a(s) população(ões) indicada(s) é desconhecido. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e aborto espontâneo em gestações clinicamente reconhecidas é de 2% a 4% e 15% a 20%, respectivamente.
Considerações Clínicas
Reações Adversas Fetais/Neonatais
Fechamento prematuro do canal arterial fetal
Evite o uso de AINEs em mulheres com cerca de 30 semanas de gestação e mais tarde na gravidez, porque os AINEs, incluindo NAPROSYN 500mg comprimidos, EC-NAPROSYN 250mg e ANAPROX DS, podem causar fechamento prematuro do canal arterial fetal (ver Dados ).
Oligoidrâmnio/Insuficiência Renal Neonatal
Se um AINE for necessário por volta da 20ª semana de gestação ou mais tarde na gravidez, limite o uso à menor dose eficaz e à menor duração possível. Se o tratamento com NAPROSYN Tablets, EC-NAPROSYN ou ANAPROX DS se estender por mais de 48 horas, considere o monitoramento com ultrassom para oligoidrâmnio. Se ocorrer oligoidrâmnio, descontinue NAPROSYN 250mg comprimidos, ECNAPROSYN 250mg e ANAPROX DS e faça o acompanhamento de acordo com a prática clínica (consulte Dados ).
Mão de obra ou entrega
Não há estudos sobre os efeitos de NAPROSYN Tablets, EC-NAPROSYN ou ANAPROX DS durante o trabalho de parto ou parto. Em estudos com animais, AINEs, incluindo naproxeno, inibem a síntese de prostaglandinas, causam atraso no parto e aumentam a incidência de natimortos.
Dados
Dados humanos
Há algumas evidências que sugerem que, quando inibidores da síntese de prostaglandinas são usados para retardar o trabalho de parto prematuro, há um risco aumentado de complicações neonatais, como enterocolite necrosante, persistência do canal arterial e hemorragia intracraniana. O tratamento com naproxeno administrado no final da gravidez para retardar o parto tem sido associado a hipertensão pulmonar persistente, disfunção renal e níveis anormais de prostaglandina E em bebês prematuros. Devido aos efeitos conhecidos dos anti-inflamatórios não esteroides no sistema cardiovascular fetal (fechamento do canal arterial), o uso durante a gravidez (particularmente a partir de 30 semanas de gestação ou terceiro trimestre) deve ser evitado.
Fechamento prematuro do canal arterial fetal
A literatura publicada relata que o uso de AINEs em cerca de 30 semanas de gestação e mais tarde na gravidez pode causar fechamento prematuro do canal arterial fetal.
Oligoidrâmnio/Insuficiência Renal Neonatal
Estudos publicados e relatórios pós-comercialização descrevem o uso materno de AINEs em cerca de 20 semanas de gestação ou mais tarde na gravidez associado a disfunção renal fetal levando a oligoidrâmnio e, em alguns casos, insuficiência renal neonatal. Esses resultados adversos são observados, em média, após dias a semanas de tratamento, embora oligoidrâmnios tenham sido relatados com pouca frequência tão logo 48 horas após o início dos AINEs. Em muitos casos, mas não em todos, a diminuição do líquido amniótico foi transitória e reversível com a suspensão da droga. Houve um número limitado de relatos de casos de uso materno de AINEs e disfunção renal neonatal sem oligoidrâmnio, alguns dos quais irreversíveis. Alguns casos de disfunção renal neonatal necessitaram de tratamento com procedimentos invasivos, como exsanguineotransfusão ou diálise.
As limitações metodológicas desses estudos e relatórios pós-comercialização incluem a falta de um grupo de controle; informações limitadas sobre dose, duração e tempo de exposição ao medicamento; e uso concomitante de outros medicamentos. Essas limitações impedem o estabelecimento de uma estimativa confiável do risco de desfechos fetais e neonatais adversos com o uso materno de AINEs. Como os dados de segurança publicados sobre os resultados neonatais envolveram principalmente bebês prematuros, a generalização de certos riscos relatados para o bebê a termo exposto a AINEs pelo uso materno é incerto.
Dados de animais
Estudos de reprodução foram realizados em ratos na dose de 20 mg/kg/dia (0,13 vezes a dose diária humana máxima recomendada de 1500 mg/dia com base na comparação da área de superfície corporal), coelhos na dose de 20 mg/kg/dia (0,26 vezes a dose máxima recomendada humana diária, com base na comparação da área de superfície corporal), e camundongos a 170 mg/kg/dia (0,6 vezes a dose máxima diária humana recomendada com base na comparação da área de superfície corporal) sem evidência de fertilidade prejudicada ou dano ao feto devido a a droga.
Lactação
Resumo do risco
O ânion naproxeno foi encontrado no leite de mulheres lactantes em uma concentração equivalente a aproximadamente 1% da concentração plasmática máxima de naproxeno. Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de NAPROSYN Tablets, EC-NAPROSYN 500mg ou ANAPROX DS e quaisquer potenciais efeitos adversos no bebê amamentado pelos NAPROSYN Tablets, EC-NAPROSYN ou ANAPROX DS ou da condição materna subjacente.
Fêmeas e Machos com Potencial Reprodutivo
Infertilidade
Mulheres
Com base no mecanismo de ação, o uso de AINEs mediados por prostaglandinas, incluindo NAPROSYN Tablets, ECNAPROSYN e ANAPROX DS, pode retardar ou prevenir a ruptura dos folículos ovarianos, que tem sido associada à infertilidade reversível em algumas mulheres. Estudos em animais publicados mostraram que a administração de inibidores da síntese de prostaglandinas tem o potencial de interromper a ruptura folicular mediada por prostaglandinas necessária para a ovulação. Pequenos estudos em mulheres tratadas com AINEs também mostraram um atraso reversível na ovulação. Considerar a retirada de AINEs, incluindo comprimidos de NAPROSYN, EC-NAPROSYN e ANAPROX DS, em mulheres com dificuldades de conceber ou em investigação de infertilidade.
Uso Pediátrico
A segurança e eficácia em pacientes pediátricos com idade inferior a 2 anos não foram estabelecidas. As recomendações de dosagem pediátrica para artrite idiopática juvenil poliarticular são baseadas em estudos bem controlados [ver DOSAGEM E ADMINISTRAÇÃO ]. Não há dados adequados de eficácia ou dose-resposta para outras condições pediátricas, mas a experiência em artrite idiopática juvenil poliarticular e outras experiências de uso estabeleceram que doses únicas de 2,5 a 5 mg/kg como suspensão de naproxeno, com dose diária total não superior a 15 mg/kg/dia, são bem tolerados em pacientes pediátricos com mais de 2 anos de idade.
Uso Geriátrico
A tolerabilidade hepática e renal da administração de naproxeno a longo prazo foi estudada em dois ensaios clínicos duplo-cegos envolvendo 586 pacientes. Dos pacientes estudados, 98 pacientes tinham 65 anos ou mais e 10 dos 98 pacientes tinham 75 anos ou mais. NAPROXEN foi administrado em doses de 375 mg duas vezes ao dia ou 750 mg duas vezes ao dia por até 6 meses. Anormalidades transitórias dos exames laboratoriais que avaliam a função hepática e renal foram observadas em alguns pacientes, embora não tenham sido observadas diferenças na ocorrência de valores anormais entre as diferentes faixas etárias.
Pacientes idosos, em comparação com pacientes mais jovens, estão em maior risco de reações adversas cardiovasculares, gastrointestinais e/ou renais graves associadas aos AINEs. Se o benefício previsto para o paciente idoso superar esses riscos potenciais, inicie a dosagem no limite inferior da faixa de dosagem e monitore os pacientes quanto a efeitos adversos [ver AVISOS E PRECAUÇÕES ].
Estudos indicam que, embora a concentração plasmática total de naproxeno permaneça inalterada, a fração plasmática não ligada de naproxeno está aumentada em idosos. O significado clínico desse achado não é claro, embora seja possível que o aumento na concentração de naproxeno livre possa estar associado a um aumento na taxa de eventos adversos por uma determinada dosagem em alguns pacientes idosos. Recomenda-se cautela quando altas doses são necessárias e alguns ajustes de dosagem podem ser necessários em pacientes idosos. Tal como acontece com outros medicamentos usados em idosos, é prudente usar a menor dose eficaz.
A experiência indica que os pacientes geriátricos podem ser particularmente sensíveis a certos efeitos adversos dos anti-inflamatórios não esteróides. Pacientes idosos ou debilitados parecem tolerar menos ulceração péptica ou sangramento quando esses eventos ocorrem. A maioria das notificações espontâneas de eventos gastrointestinais fatais ocorre na população geriátrica [ver AVISOS E PRECAUÇÕES ].
Sabe-se que o naproxeno é substancialmente excretado pelos rins, e o risco de reações tóxicas a este medicamento pode ser maior em pacientes com função renal comprometida. Como os pacientes idosos são mais propensos a ter função renal diminuída, deve-se ter cuidado na seleção da dose e pode ser útil monitorar a função renal [ver FARMACOLOGIA CLÍNICA ]. Pacientes geriátricos podem estar em maior risco de desenvolver uma forma de toxicidade renal precipitada pela redução da formação de prostaglandinas durante a administração de anti-inflamatórios não esteroides [ver AVISOS E PRECAUÇÕES ].
Insuficiência hepática
Recomenda-se precaução quando são necessárias doses elevadas e pode ser necessário algum ajuste da dose nestes doentes. É prudente usar a menor dose eficaz [ver FARMACOLOGIA CLÍNICA ].
Insuficiência renal
Produtos contendo naproxeno não são recomendados para uso em pacientes com insuficiência renal moderada a grave e grave (clearance de creatinina AVISOS E PRECAUÇÕES , FARMACOLOGIA CLÍNICA ].
SOBREDOSAGEM
Os sintomas após superdosagem aguda de AINEs têm sido tipicamente limitados a letargia, sonolência, náusea, vômito e dor epigástrica, que geralmente são reversíveis com cuidados de suporte. Ocorreu sangramento gastrointestinal. Hipertensão, insuficiência renal aguda, depressão respiratória e coma ocorreram, mas foram raros [ver AVISOS E PRECAUÇÕES ]. Como o naproxeno sódico pode ser rapidamente absorvido, níveis sanguíneos elevados e precoces devem ser antecipados.
Alguns pacientes tiveram convulsões, mas não está claro se foram ou não relacionadas ao medicamento. Não se sabe qual dose da droga seria fatal. [Vejo AVISOS E PRECAUÇÕES ].
Gerencie os pacientes com cuidados sintomáticos e de suporte após uma superdosagem de AINEs. Não existem antídotos específicos.
Considerar êmese e/ou carvão ativado (60 a 100 gramas em adultos, 1 a 2 gramas por kg de peso corporal em pacientes pediátricos) e/ou catártico osmótico em pacientes sintomáticos atendidos dentro de quatro horas após a ingestão ou em pacientes com grande superdosagem. 5 a 10 vezes a dosagem recomendada). Diurese forçada, alcalinização da urina, hemodiálise ou hemoperfusão podem não ser úteis devido à alta ligação proteica.
Para obter informações adicionais sobre o tratamento de superdosagem, entre em contato com um centro de controle de intoxicações (1-800-222-1222).
CONTRA-INDICAÇÕES
Os comprimidos de NAPROSYN 500mg, EC-NAPROSYN e ANAPROX DS são contraindicados nos seguintes pacientes:
- Hipersensibilidade conhecida (por exemplo, reações anafiláticas e reações cutâneas graves) ao naproxeno ou a qualquer componente do medicamento [ver AVISOS E PRECAUÇÕES ]
- História de asma, urticária ou outras reações alérgicas após tomar aspirina ou outros AINEs. Reações anafiláticas graves, às vezes fatais, aos AINEs foram relatadas nesses pacientes [ver AVISOS E PRECAUÇÕES ]
- No cenário de cirurgia de revascularização do miocárdio (CRM) [ver AVISOS E PRECAUÇÕES ]
FARMACOLOGIA CLÍNICA
Mecanismo de ação
O naproxeno tem propriedades analgésicas, anti-inflamatórias e antipiréticas. ANAPROX DS (naproxeno sódico) foi desenvolvido como uma formulação de naproxeno de absorção mais rápida para uso como analgésico.
O mecanismo de ação do naproxeno, como o de outros AINEs, não é completamente compreendido, mas envolve a inibição da ciclooxigenase (COX-1 e COX-2).
O naproxeno é um potente inibidor da síntese de prostaglandinas in vitro. As concentrações de naproxeno atingidas durante a terapia produziram efeitos in vivo. As prostaglandinas sensibilizam os nervos aferentes e potencializam a ação da bradicinina na indução da dor em modelos animais. As prostaglandinas são mediadores da inflamação. Como o naproxeno é um inibidor da síntese de prostaglandinas, seu modo de ação pode ser devido à diminuição das prostaglandinas nos tecidos periféricos.
Farmacodinâmica
Em um estudo com voluntários saudáveis, 10 dias de administração concomitante de naproxeno 220 mg uma vez ao dia com dose baixa de aspirina de liberação imediata (81 mg) mostrou uma interação com a atividade antiplaquetária da aspirina medida pela % de inibição do tromboxano B2 sérico em 24 horas após a dose do dia 10 [98,7% (somente aspirina) vs 93,1% (naproxeno e aspirina)]. A interação foi observada mesmo após a descontinuação do naproxeno no dia 11 (enquanto a dose de aspirina foi continuada), mas normalizada no dia 13. No mesmo estudo, a interação foi maior quando o naproxeno foi administrado 30 minutos antes da aspirina [98,7% vs 87,7%] e mínimo quando a aspirina foi administrada 30 minutos antes do naproxeno [98,7% vs 95,4%].
Após a administração de naproxeno 220 mg duas vezes ao dia com baixa dose de aspirina de liberação imediata (primeira dose de naproxeno administrada 30 minutos antes da aspirina), a interação foi mínima 24 h após a dose do dia 10 [98,7% vs 95,7%]. No entanto, a interação foi mais proeminente após a descontinuação do naproxeno (washout) no dia 11 [98,7% vs 84,3%] e não normalizou completamente no dia 13 [98,5% vs 90,7%]. [Vejo INTERAÇÕES MEDICAMENTOSAS ].
Farmacocinética
naproxeno e o naproxeno sódico são rápida e completamente absorvidos pelo trato gastrointestinal com uma biodisponibilidade in vivo de 95%. As diferentes formas de dosagem de NAPROSYN 250mg são bioequivalentes em termos de extensão de absorção (AUC) e concentração máxima (Cmax); no entanto, os produtos diferem em seu padrão de absorção. Essas diferenças entre os produtos de naproxeno estão relacionadas tanto à forma química do naproxeno utilizada quanto à sua formulação. Mesmo com as diferenças observadas no padrão de absorção, a meia-vida de eliminação do naproxeno permanece inalterada entre os produtos que variam de 12 a 17 horas. Níveis de estado estacionário de naproxeno são alcançados em 4 a 5 dias, e o grau de acúmulo de naproxeno é consistente com essa meia-vida. Isso sugere que as diferenças no padrão de liberação desempenham apenas um papel insignificante na obtenção de níveis plasmáticos em estado estacionário.
Absorção
NAPROSYN Comprimidos/ANAPROX DS
Após a administração de NAPROSYN 500mg comprimidos, os níveis plasmáticos máximos são atingidos em 2 a 4 horas. Após a administração oral de ANAPROX DS, os níveis plasmáticos máximos são atingidos em 1 a 2 horas. A diferença nas taxas entre os dois produtos se deve ao aumento da solubilidade aquosa do sal de sódio do naproxeno usado no ANAPROX DS.
EC-NAPROSYN
EC-NAPROSYN é projetado com um revestimento sensível ao pH para fornecer uma barreira à desintegração no ambiente ácido do estômago e à perda de integridade no ambiente mais neutro do intestino delgado. O revestimento de polímero entérico selecionado para EC-NAPROSYN 250mg dissolve-se acima de pH 6. Quando EC-NAPROSYN foi administrado a indivíduos em jejum, os níveis plasmáticos de pico foram atingidos cerca de 4 a 6 horas após a primeira dose (intervalo: 2 a 12 horas). Um estudo in vivo em humanos usando comprimidos de EC-NAPROSYN 250mg radiomarcados demonstrou que EC-NAPROSYN se dissolve principalmente no intestino delgado e não no estômago, de modo que a absorção da droga é retardada até que o estômago seja esvaziado.
Quando os comprimidos de EC-NAPROSYN e NAPROSYN 500mg foram administrados a indivíduos em jejum (n=24) em um estudo cruzado após 1 semana de dosagem, foram observadas diferenças no tempo para atingir os níveis plasmáticos máximos (Tmax), mas não houve diferenças na absorção total conforme medido por Cmax e AUC:
Efeitos antiácidos
Quando EC-NAPROSYN 250mg foi administrado em dose única com antiácido (capacidade de tamponamento de 54 mEq), os níveis plasmáticos de pico de naproxeno permaneceram inalterados, mas o tempo até o pico foi reduzido (Tmax médio em jejum 5,6 horas, Tmax médio com antiácido 5 horas) , embora não significativamente [ver INTERAÇÕES MEDICAMENTOSAS ].
Efeitos dos alimentos
Quando EC-NAPROSYN 500mg foi administrado em dose única com alimentos, os níveis plasmáticos máximos na maioria dos indivíduos foram alcançados em cerca de 12 horas (intervalo: 4 a 24 horas). O tempo de residência no intestino delgado até a desintegração foi independente da ingestão alimentar. A presença de alimentos prolongou o tempo que os comprimidos permaneceram no estômago, o tempo para os primeiros níveis séricos de naproxeno detectáveis e o tempo para os níveis máximos de naproxeno (Tmax), mas não afetou os níveis de pico de naproxeno (Cmax).
Distribuição
naproxeno tem um volume de distribuição de 0,16 L/kg. Em níveis terapêuticos, o naproxeno é mais de 99% ligado à albumina. Em doses de naproxeno superiores a 500 mg/dia, há um aumento menos que proporcional nos níveis plasmáticos devido a um aumento na depuração causado pela saturação da ligação às proteínas plasmáticas em doses mais altas (média de Css 36,5, 49,2 e 56,4 mg/L com 500, doses diárias de 1.000 e 1.500 mg de naproxeno, respectivamente). O ânion naproxeno foi encontrado no leite de mulheres lactantes em uma concentração equivalente a aproximadamente 1% da concentração plasmática máxima de naproxeno. Uso em populações específicas ].
Eliminação
Metabolismo
O naproxeno é extensamente metabolizado no fígado em 6-0-desmetil naproxeno, e tanto o progenitor quanto os metabólitos não induzem enzimas metabolizadoras. Tanto o naproxeno quanto o 6-0-desmetil naproxeno são posteriormente metabolizados em seus respectivos metabólitos conjugados com acilglicuronídeos.
Excreção
depuração do naproxeno é de 0,13 mL/min/kg. Aproximadamente 95% do naproxeno de qualquer dose é excretado na urina, principalmente como naproxeno ( AVISOS E PRECAUÇÕES ].
Populações Específicas
Pediátrico
Em pacientes pediátricos de 5 a 16 anos com artrite, os níveis plasmáticos de naproxeno após uma dose única de 5 mg/kg de suspensão de naproxeno [ver DOSAGEM E ADMINISTRAÇÃO foram semelhantes aos encontrados em adultos normais após uma dose de 500 mg. A meia-vida terminal parece ser semelhante em pacientes pediátricos e adultos. Não foram realizados estudos farmacocinéticos de naproxeno em pacientes pediátricos com menos de 5 anos de idade. Os parâmetros farmacocinéticos parecem ser semelhantes após a administração de suspensão ou comprimidos de naproxeno em pacientes pediátricos.
Geriátrico
Estudos indicam que, embora a concentração plasmática total de naproxeno permaneça inalterada, a fração plasmática não ligada de naproxeno está aumentada em idosos, embora a fração não ligada seja
Insuficiência hepática
A farmacocinética do naproxeno não foi determinada em indivíduos com insuficiência hepática.
doença hepática alcoólica crônica e provavelmente outras doenças com proteínas plasmáticas diminuídas ou anormais (albumina) reduzem a concentração plasmática total de naproxeno, mas a concentração plasmática de naproxeno não ligado é aumentada.
Insuficiência renal
A farmacocinética do naproxeno não foi determinada em indivíduos com insuficiência renal. Dado que o naproxeno, seus metabólitos e conjugados são excretados principalmente pelo rim, existe o potencial de acúmulo de metabólitos de naproxeno na presença de insuficiência renal. A eliminação do naproxeno está diminuída em pacientes com insuficiência renal grave.
Estudos de interação medicamentosa
Aspirina
Quando os AINEs foram administrados com aspirina, a ligação proteica dos AINEs foi reduzida, embora a depuração do AINE livre não tenha sido alterada. O significado clínico desta interação não é conhecido. Consulte a Tabela 1 para interações medicamentosas clinicamente significativas de AINEs com aspirina [consulte INTERAÇÕES MEDICAMENTOSAS ].
Estudos clínicos
naproxeno foi estudado em pacientes com artrite reumatóide, osteoartrite, artrite idiopática juvenil poliarticular, espondilite anquilosante, tendinite e bursite e gota aguda. A melhora em pacientes tratados para artrite reumatóide foi demonstrada por uma redução no inchaço das articulações, uma redução na duração da rigidez matinal, uma redução na atividade da doença avaliada pelo investigador e pelo paciente e pelo aumento da mobilidade, conforme demonstrado pela redução no tempo de caminhada . Geralmente, a resposta ao naproxeno não depende da idade, sexo, gravidade ou duração da artrite reumatóide.
Em pacientes com osteoartrite, a ação terapêutica do naproxeno foi demonstrada pela redução da dor ou sensibilidade nas articulações, aumento da amplitude de movimento nas articulações do joelho, aumento da mobilidade demonstrado pela redução do tempo de caminhada e melhora na capacidade de realizar atividades da vida diária prejudicada pela doença.
Em um ensaio clínico comparando formulações padrão de naproxeno 375 mg duas vezes ao dia (750 mg ao dia) versus 750 mg duas vezes ao dia (1500 mg/dia), 9 pacientes no grupo de 750 mg interromperam prematuramente devido a eventos adversos. Dezenove pacientes no grupo de 1500 mg terminaram prematuramente devido a eventos adversos. A maioria desses eventos adversos foram eventos gastrointestinais.
Em estudos clínicos em pacientes com artrite reumatoide, osteoartrite e artrite idiopática juvenil poliarticular, o naproxeno demonstrou ser comparável à aspirina e à indometacina no controle das medidas acima mencionadas da atividade da doença, mas a frequência e gravidade dos efeitos adversos gastrointestinais mais leves (náusea , dispepsia, azia) e efeitos adversos no sistema nervoso (zumbido, tontura, tontura) foram menores em pacientes tratados com naproxeno do que naqueles tratados com aspirina ou indometacina.
Em pacientes com espondilite anquilosante, o naproxeno demonstrou diminuir a dor noturna, a rigidez matinal e a dor em repouso. Em estudos duplo-cegos, a droga mostrou-se tão eficaz quanto a aspirina, mas com menos efeitos colaterais.
Em pacientes com gota aguda, uma resposta favorável ao naproxeno foi demonstrada pela eliminação significativa das alterações inflamatórias (p.
naproxeno foi estudado em pacientes com dor leve a moderada secundária a pós-operatório, ortopedia, episiotomia pós-parto e dor de contração uterina e dismenorreia. O início do alívio da dor pode começar dentro de 1 hora em pacientes em uso de naproxeno e em 30 minutos em pacientes em uso de naproxeno sódico. O efeito analgésico foi demonstrado por medidas como redução dos escores de intensidade da dor, aumento dos escores de alívio da dor, diminuição do número de pacientes que necessitam de medicação analgésica adicional e atraso no tempo para remedicação. O efeito analgésico foi encontrado para durar até 12 horas.
naproxeno pode ser usado com segurança em combinação com sais de ouro e/ou corticosteróides; no entanto, em ensaios clínicos controlados, quando adicionado ao regime de pacientes que receberam corticosteróides, não pareceu causar maior melhora em relação ao observado com corticosteróides isolados. Se o naproxeno tem um efeito “poupador de esteróides” não foi adequadamente estudado. Quando adicionado ao regime de pacientes que receberam sais de ouro, o naproxeno resultou em maior melhora. Seu uso em combinação com salicilatos não é recomendado porque há evidências de que a aspirina aumenta a taxa de excreção de naproxeno e os dados são inadequados para demonstrar que naproxeno e aspirina produzem maior melhora em relação à alcançada com aspirina sozinha. Além disso, como com outros AINEs, a combinação pode resultar em maior frequência de eventos adversos do que a demonstrada para qualquer um dos produtos isoladamente.
Em estudos de gastroscopia e perda sanguínea de 51Cr com voluntários normais, a administração diária de 1.000 mg de naproxeno como 1.000 mg de NAPROSYN (naproxeno) ou 1.100 mg de ANAPROX DS (naproxeno sódico) demonstrou causar estatisticamente menos sangramento e erosão gástrica do que 3.250 mg de aspirina.
Três estudos multicêntricos, duplo-cegos, de 6 semanas com EC-NAPROSYN (naproxeno) (375 ou 500 mg duas vezes ao dia, n=385) e NAPROSYN (375 ou 500 mg duas vezes ao dia, n=279) foram conduzidos comparando EC -NAPROSYN com NAPROSYN, incluindo 355 pacientes com artrite reumatoide e osteoartrite que tinham histórico recente de sintomas gastrointestinais relacionados a AINEs. Esses estudos indicaram que EC-NAPROSYN e NAPROSYN 500mg não mostraram diferenças significativas na eficácia ou segurança e tiveram prevalência semelhante de queixas gastrointestinais menores. Pacientes individuais, no entanto, podem achar uma formulação preferível à outra.
Quinhentos e cinquenta e três pacientes receberam EC-NAPROSYN durante ensaios abertos de longa duração (a duração média do tratamento foi de 159 dias). As taxas de úlceras pépticas diagnosticadas clinicamente e sangramentos gastrointestinais foram semelhantes às relatadas historicamente para o uso de AINEs em longo prazo.
INFORMAÇÃO DO PACIENTE
Guia de Medicação para Anti-inflamatórios Não Esteroides (AINEs)
Qual é a informação mais importante que devo saber sobre medicamentos chamados anti-inflamatórios não esteroides (AINEs)?
Os AINEs podem causar efeitos colaterais graves, incluindo:
- Aumento do risco de ataque cardíaco ou acidente vascular cerebral que pode levar à morte. Este risco pode ocorrer no início do tratamento e pode aumentar:
- com doses crescentes de AINEs
- com uso mais prolongado de AINEs
Não tome AINEs antes ou depois de uma cirurgia cardíaca chamada “enxerto de revascularização do miocárdio (CRM)”.
Evite tomar AINEs após um ataque cardíaco recente, a menos que seu médico lhe diga. Você pode ter um risco aumentado de outro ataque cardíaco se tomar AINEs após um ataque cardíaco recente.
- Aumento do risco de sangramento, úlceras e lágrimas (perfuração) do esôfago (tubo que vai da boca ao estômago), estômago e intestinos:
- a qualquer momento durante o uso
- sem sintomas de alerta
- que pode causar a morte
O risco de ter uma úlcera ou sangramento aumenta com:
- história pregressa de úlceras estomacais ou sangramento estomacal ou intestinal com uso de AINEs
- tomar medicamentos chamados “corticosteróides”, “anticoagulantes”, “SSRIs” ou “SNRIs”
- doses crescentes de AINEs
- uso mais prolongado de AINEs
- fumar
- beber álcool
- idoso
- saúde debilitada
- doença hepática avançada
- problemas de sangramento
Os AINEs só devem ser usados:
- exatamente como prescrito
- na dose mais baixa possível para o seu tratamento
- pelo menor tempo necessário
O que são AINEs?
Os AINEs são usados para tratar dor e vermelhidão, inchaço e calor (inflamação) de condições médicas, como diferentes tipos de artrite, cólicas menstruais e outros tipos de dor de curto prazo.
Quem não deve tomar AINEs?
Não tome AINEs:
- se você teve um ataque de asma, urticária ou outra reação alérgica com aspirina ou qualquer outro AINE.
- imediatamente antes ou após a cirurgia de bypass cardíaco.
Antes de tomar AINEs, informe o seu médico sobre todas as suas condições médicas, incluindo se você:
- tem problemas de fígado ou rins
- tem pressão alta
- tem asma
- estão grávidas ou planejam engravidar. Tomar AINEs com cerca de 20 semanas de gravidez ou mais tarde pode prejudicar o feto. Se você precisar tomar AINEs por mais de 2 dias quando estiver entre 20 e 30 semanas de gravidez, seu médico pode precisar monitorar a quantidade de líquido no útero ao redor do bebê. Você não deve tomar AINEs após cerca de 30 semanas de gravidez.
- está amamentando ou planeja amamentar.
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos ou de venda livre, vitaminas ou suplementos de ervas. Os AINEs e alguns outros medicamentos podem interagir entre si e causar efeitos colaterais graves. Não comece a tomar nenhum medicamento novo sem falar primeiro com o seu médico.
Quais são os possíveis efeitos colaterais dos AINEs?
Os AINEs podem causar efeitos colaterais graves, incluindo:
Consulte “Qual é a informação mais importante que devo saber sobre medicamentos chamados anti-inflamatórios não esteroides (AINEs)?”
- pressão alta nova ou pior
- insuficiência cardíaca
- problemas hepáticos, incluindo insuficiência hepática
- problemas renais, incluindo insuficiência renal
- glóbulos vermelhos baixos (anemia)
- reações cutâneas com risco de vida
- reações alérgicas com risco de vida
Outros efeitos colaterais dos AINEs incluem: dor de estômago, constipação, diarréia, gases, azia, náusea, vômito e tontura. Obtenha ajuda de emergência imediatamente se tiver algum dos seguintes sintomas:
- falta de ar ou dificuldade para respirar
- dor no peito
- fraqueza em uma parte ou lado do seu corpo
- fala arrastada
- inchaço do rosto ou garganta
Pare de tomar seu AINE e ligue para seu médico imediatamente se tiver algum dos seguintes sintomas:
- náusea
- mais cansado ou mais fraco do que o habitual
- diarréia
- coceira
- sua pele ou olhos parecem amarelos
- indigestão ou dor de estômago
- sintomas como os da gripe
- vômito de sangue
- há sangue em seu movimento intestinal ou é preto e pegajoso como alcatrão
- ganho de peso incomum
- erupção cutânea ou bolhas com febre
- inchaço dos braços, pernas, mãos e pés
Se você tomar muito do seu AINE, ligue para o seu médico ou procure ajuda médica imediatamente.
Estes não são todos os possíveis efeitos colaterais dos AINEs. Para obter mais informações, pergunte ao seu médico ou farmacêutico sobre AINEs.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Outras informações sobre AINEs
- A aspirina é um AINE, mas não aumenta a chance de ataque cardíaco. A aspirina pode causar sangramento no cérebro, estômago e intestinos. A aspirina também pode causar úlceras no estômago e nos intestinos.
- Alguns AINEs são vendidos em doses mais baixas sem receita médica (sem receita). Converse com seu médico antes de usar AINEs de venda livre por mais de 10 dias.
Informações gerais sobre o uso seguro e eficaz de AINEs
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use AINEs para uma condição para a qual não foi prescrito. Não dê AINEs a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Se você quiser mais informações sobre AINEs, fale com seu médico. Você pode pedir ao seu farmacêutico ou profissional de saúde informações sobre AINEs escritas para profissionais de saúde.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
