Crestor 10mg, 20mg, 5mg Rosuvastatin Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Crestor e como é usado?
Crestor é um medicamento de prescrição usado para diminuir o colesterol LDL (lipoproteína de baixa densidade) e triglicérides no sangue, retardar a progressão da placa nos vasos sanguíneos, reduzir o risco de acidente vascular cerebral e ataque cardíaco. Crestor 20mg pode ser usado sozinho ou com outros medicamentos.
Crestor é um Agentes Redutores de Lipídios, Estatinas, Inibidores da HMG-CoA Redutase.
Não se sabe se Crestor é seguro e eficaz em crianças com menos de 8 anos de idade.
Quais são os possíveis efeitos colaterais do Crestor?
Crestor pode causar efeitos colaterais graves, incluindo:
- dor muscular inexplicável
- sensibilidade muscular
- fraqueza muscular
- confusão
- problemas de memória
- dor de estômago superior
- cansaço
- perda de apetite
- urina escura
- amarelecimento da pele ou dos olhos (icterícia)
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Crestor incluem:
- dor de cabeça
- fraqueza
- dores musculares
- náusea
- dor de estômago
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Crestor. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
CRESTOR (rosuvastatina cálcica) é um agente hipolipemiante sintético para administração oral.
O nome químico da rosuvastatina cálcica é bis[(E)-7-[4-(4-fluorofenil)-6-isopropil-2-[metil(metilsulfonil)amino]pirimidin-5-il](3R,5S)-3 ácido ,5-dihidroxihept-6-enóico] sal de cálcio com a seguinte fórmula estrutural:
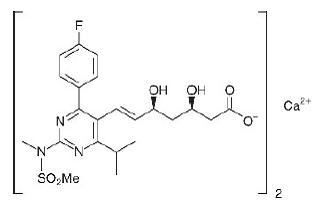
A fórmula empírica da rosuvastatina cálcica é (C22H27FN3O6S)2Ca e o peso molecular é 1001,14. A rosuvastatina cálcica é um pó branco amorfo pouco solúvel em água e metanol e ligeiramente solúvel em etanol. A rosuvastatina cálcica é um composto hidrofílico com coeficiente de partição (octanol/água) de 0,13 em pH de 7,0.
CRESTOR comprimidos para administração oral contém 5, 10, 20 ou 40 mg de rosuvastatina e os seguintes ingredientes inativos: Cada comprimido contém: celulose microcristalina NF, lactose monohidratada NF, fosfato de cálcio tribásico NF, crospovidona NF, estearato de magnésio NF, hipromelose NF, triacetina NF, dióxido de titânio USP, óxido férrico amarelo e óxido férrico vermelho NF.
INDICAÇÕES
Hiperlipidemia e dislipidemia mista
CRESTOR é indicado como terapia adjuvante à dieta para reduzir os níveis elevados de C Total, LDL-C, ApoB, não-HDL-C e triglicerídeos e para aumentar o HDL-C em pacientes adultos com hiperlipidemia primária ou dislipidemia mista. Os agentes que alteram os lipídios devem ser usados em adição a uma dieta restrita em gordura saturada e colesterol quando a resposta à dieta e às intervenções não farmacológicas isoladas for inadequada.
Pacientes pediátricos com hipercolesterolemia familiar
CRESTOR 10mg é indicado como adjuvante da dieta para:
- reduzir os níveis de C Total, LDL-C e ApoB em crianças e adolescentes de 8 a 17 anos de idade com hipercolesterolemia familiar heterozigótica se após uma tentativa adequada de terapia dietética os seguintes achados estiverem presentes: LDL-C >190 mg/dL, ou >160 mg/dL juntamente com uma história familiar positiva de doença cardiovascular prematura (DCV) ou dois ou mais outros fatores de risco de DCV.
- reduzir LDL-C, Total-C, não HDL-C e ApoB em crianças e adolescentes de 7 a 17 anos de idade com hipercolesterolemia familiar homozigótica, isoladamente ou com outros tratamentos hipolipemiantes (por exemplo, aférese de LDL).
Hipertrigliceridemia
CRESTOR é indicado como terapia adjuvante à dieta para o tratamento de pacientes adultos com hipertrigliceridemia.
Disbetalipoproteinemia Primária (Hiperlipoproteinemia Tipo III)
CRESTOR é indicado como adjuvante da dieta para o tratamento de pacientes adultos com disbetalipoproteinemia primária (Hiperlipoproteinemia Tipo III).
Pacientes adultos com hipercolesterolemia familiar homozigótica
CRESTOR é indicado como terapia adjuvante a outros tratamentos hipolipemiantes (p.
Desaceleração da progressão da aterosclerose
CRESTOR 5mg é indicado como terapia adjuvante à dieta para retardar a progressão da aterosclerose em pacientes adultos como parte de uma estratégia de tratamento para reduzir o C Total e o LDL-C para níveis alvo.
Prevenção primária de doenças cardiovasculares
Em indivíduos sem doença coronariana clinicamente evidente, mas com risco aumentado de doença cardiovascular com base na idade ≥50 anos em homens e ≥60 anos em mulheres, PCRhs ≥2 mg/L e presença de pelo menos uma doença cardiovascular adicional fator de risco como hipertensão, HDL-C baixo, tabagismo ou história familiar de doença coronariana prematura, CRESTOR é indicado para:
- reduzir o risco de acidente vascular cerebral
- reduzir o risco de infarto do miocárdio
- reduzir o risco de procedimentos de revascularização arterial
Limitações de uso
CRESTOR não foi estudado nas dislipidemias tipo I e V de Fredrickson.
DOSAGEM E ADMINISTRAÇÃO
Informações gerais de dosagem
O intervalo de dose para CRESTOR 5mg em adultos é de 5 a 40 mg por via oral uma vez ao dia. A dose inicial usual é de 10 a 20 mg uma vez ao dia. A dose inicial usual em pacientes adultos com hipercolesterolemia familiar homozigótica é de 20 mg uma vez ao dia.
dose máxima de 20 mg de CRESTOR de 40 mg deve ser usada apenas para aqueles pacientes que não atingiram sua meta de LDL-C utilizando a dose de 20 mg [ver AVISOS E PRECAUÇÕES ].
CRESTOR 5mg pode ser administrado em dose única a qualquer hora do dia, com ou sem alimentos. O comprimido deve ser engolido inteiro.
Ao iniciar a terapia com CRESTOR ou mudar de outra terapia com inibidor da HMG-CoA redutase, a dose inicial apropriada de CRESTOR 10mg deve ser utilizada primeiro e só então titulada de acordo com a resposta do paciente e o objetivo individualizado da terapia.
Após o início ou após a titulação de CRESTOR, os níveis lipídicos devem ser analisados dentro de 2 a 4 semanas e a dosagem ajustada de acordo.
Dosagem Pediátrica
Na hipercolesterolemia familiar heterozigótica, o intervalo de dose recomendado é de 5 a 10 mg por via oral uma vez ao dia em pacientes de 8 a menos de 10 anos de idade, e 5 a 20 mg por via oral uma vez ao dia em pacientes de 10 a 17 anos de idade.
Na hipercolesterolemia familiar homozigótica, a dose recomendada é de 20 mg por via oral uma vez ao dia em pacientes de 7 a 17 anos de idade.
Dosagem em pacientes asiáticos
Em pacientes asiáticos, considerar o início da terapia com CRESTOR 20 mg com 5 mg uma vez ao dia devido ao aumento das concentrações plasmáticas de rosuvastatina. O aumento da exposição sistêmica deve ser levado em consideração ao tratar pacientes asiáticos não adequadamente controlados com doses de até 20 mg/dia [ver Uso em populações específicas e FARMACOLOGIA CLÍNICA ].
Uso com terapia concomitante
Pacientes que tomam ciclosporina
A dose de CRESTOR 20 mg não deve exceder 5 mg uma vez ao dia [ver AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS e FARMACOLOGIA CLÍNICA ].
Pacientes que tomam Gemfibrozil
Evite o uso concomitante de CRESTOR com gemfibrozil. Se o uso concomitante não puder ser evitado, inicie CRESTOR com 5 mg uma vez ao dia. A dose de CRESTOR não deve exceder 10 mg uma vez ao dia [ver AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS e FARMACOLOGIA CLÍNICA ].
Pacientes que tomam Atazanavir e Ritonavir, Lopinavir e Ritonavir ou Simeprevir
Iniciar terapia CRESTOR 10mg com 5mg uma vez ao dia. A dose de CRESTOR não deve exceder 10 mg uma vez ao dia [ver AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS e FARMACOLOGIA CLÍNICA ].
Dosagem em Pacientes com Insuficiência Renal Grave
Para pacientes com insuficiência renal grave (CLcr Uso em populações específicas e FARMACOLOGIA CLÍNICA ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
5 mg: Comprimidos revestidos amarelos, redondos, biconvexos. Gravado “CRESTOR” e “5” em um lado do comprimido.
10 mg: Comprimidos revestidos cor-de-rosa, redondos, biconvexos. Gravado “CRESTOR” e “10” em um lado do comprimido.
20 mg: Comprimidos revestidos cor-de-rosa, redondos, biconvexos. Gravado “CRESTOR” e “20” em um lado do comprimido.
40 mg: Comprimidos revestidos cor-de-rosa, ovais, biconvexos. Gravado “CRESTOR” de um lado e “40” do outro lado do comprimido.
Armazenamento e manuseio
CRESTOR® (rosuvastatina cálcica) Comprimidos são fornecidos como:
NDC 0310-0755-90: 5mg. Comprimidos revestidos amarelos, redondos, biconvexos. Gravado “CRESTOR” e “5” de um lado; frasco de 90 comprimidos
NDC 0310-0751-90: 10 mg. Comprimidos revestidos cor-de-rosa, redondos, biconvexos. Gravado “CRESTOR” e “10” de um lado; frasco de 90 comprimidos
NDC 0310-0751-39: 10 mg. Comprimidos revestidos cor-de-rosa, redondos, biconvexos. Gravado “CRESTOR” e “10” de um lado; pacotes de dose unitária de 100
NDC 0310-0752-90: 20mg. Comprimidos revestidos cor-de-rosa, redondos, biconvexos. Gravado “CRESTOR” e “20” de um lado; garrafas de 90
NDC 0310-0752-39: 20mg. Comprimidos revestidos cor-de-rosa, redondos, biconvexos. Gravado “CRESTOR” e “20” de um lado; pacotes de dose unitária de 100
NDC 0310-0754-30: 40 mg. Comprimidos revestidos cor-de-rosa, ovais, biconvexos. Gravado “CRESTOR” de um lado e “40” do outro lado; garrafas de 30
Armazenar
Armazenar em temperatura ambiente controlada, 20-25°C (68-77°F) [consulte Temperatura ambiente controlada USP ]. Proteger da umidade.
Distribuído por: AstraZeneca Pharmaceuticals LP Wilmington, DE 19850. Revisado: setembro de 2018
EFEITOS COLATERAIS
As seguintes reações adversas graves são discutidas em mais detalhes em outras seções do rótulo:
- Rabdomiólise com mioglobinúria e insuficiência renal aguda e miopatia (incluindo miosite) [ver AVISOS E PRECAUÇÕES ]
- Anormalidades das enzimas hepáticas [ver AVISOS E PRECAUÇÕES ]
Experiência em Estudos Clínicos
Como os estudos clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos estudos clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos estudos clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
Na base de dados de ensaios clínicos controlados CRESTOR (placebo ou controlados com ativos) de 5.394 pacientes com duração média de tratamento de 15 semanas, 1,4% dos pacientes descontinuaram devido a reações adversas. As reações adversas mais comuns que levaram à descontinuação do tratamento foram:
- mialgia
- dor abdominal
- náusea
As reações adversas mais comumente relatadas (incidência ≥2%) no banco de dados de ensaios clínicos controlados CRESTOR 5mg de 5394 pacientes foram:
- dor de cabeça
- mialgia
- dor abdominal
- astenia
- náusea
As reações adversas notificadas em ≥2% dos doentes em estudos clínicos controlados com placebo e a uma taxa superior à do placebo são apresentadas na Tabela 1. Estes estudos tiveram uma duração de tratamento até 12 semanas.
Outras reações adversas relatadas em estudos clínicos foram dor abdominal, tontura, hipersensibilidade (incluindo erupção cutânea, prurido, urticária e angioedema) e pancreatite. As seguintes anormalidades laboratoriais também foram relatadas: proteinúria positiva na vareta e hematúria microscópica [ver AVISOS E PRECAUÇÕES ]; creatina fosfoquinase elevada, transaminases, glicose, glutamil transpeptidase, fosfatase alcalina e bilirrubina; e anormalidades da função tireoidiana.
No estudo METEOR, envolvendo 981 participantes tratados com 40 mg de rosuvastatina (n=700) ou placebo (n=281) com duração média de tratamento de 1,7 anos, 5,6% dos indivíduos tratados com CRESTOR 5mg versus 2,8% dos indivíduos tratados com placebo descontinuado devido a reações adversas. As reações adversas mais comuns que levaram à descontinuação do tratamento foram: mialgia, aumento das enzimas hepáticas, cefaleia e náuseas [ver Estudos clínicos ].
As reações adversas relatadas em ≥2% dos pacientes e em uma taxa maior que o placebo são mostradas na Tabela 2.
No estudo JUPITER, 17.802 participantes foram tratados com rosuvastatina 20 mg (n=8901) ou placebo (n=8901) por uma duração média de 2 anos. Uma porcentagem maior de pacientes tratados com rosuvastatina versus pacientes tratados com placebo, 6,6% e 6,2%, respectivamente, descontinuaram a medicação do estudo devido a um evento adverso, independentemente da causalidade do tratamento. A mialgia foi a reação adversa mais comum que levou à descontinuação do tratamento.
Em JUPITER, houve uma frequência significativamente maior de diabetes mellitus relatada em pacientes que tomaram rosuvastatina (2,8%) versus pacientes que tomaram placebo (2,3%). A média de HbA1c aumentou significativamente em 0,1% em pacientes tratados com rosuvastatina em comparação com pacientes tratados com placebo. O número de pacientes com HbA1c > 6,5% no final do estudo foi significativamente maior em pacientes tratados com rosuvastatina versus pacientes tratados com placebo [ver AVISOS E PRECAUÇÕES e Estudos clínicos ].
As reações adversas relatadas em ≥2% dos pacientes e em uma taxa maior que o placebo são mostradas na Tabela 3.
Pacientes pediátricos com hipercolesterolemia familiar heterozigótica
Em um estudo controlado de 12 semanas em meninos e meninas pós-menarca de 10 a 17 anos de idade com hipercolesterolemia familiar heterozigótica com CRESTOR 5 a 20 mg por dia [ver Uso em populações específicas e Estudos clínicos ], elevações na creatina fosfoquinase sérica (CK) > 10 x LSN foram observadas com mais frequência em rosuvastatina em comparação com crianças tratadas com placebo. Quatro de 130 (3%) crianças tratadas com rosuvastatina (2 tratadas com 10 mg e 2 tratadas com 20 mg) apresentaram aumento da CK > 10 x LSN, em comparação com 0 de 46 crianças que receberam placebo.
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de CRESTOR: artralgia, insuficiência hepática fatal e não fatal, hepatite, icterícia, trombocitopenia, depressão, distúrbios do sono (incluindo insônia e pesadelos), neuropatia periférica, doença pulmonar intersticial e ginecomastia. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Houve relatos raros de miopatia necrosante imunomediada associada ao uso de estatinas [ver AVISOS E PRECAUÇÕES ].
Houve raros relatos pós-comercialização de comprometimento cognitivo (por exemplo, perda de memória, esquecimento, amnésia, comprometimento da memória e confusão) associados ao uso de estatinas. Esses problemas cognitivos foram relatados para todas as estatinas. Os relatos são geralmente não graves e reversíveis com a descontinuação das estatinas, com tempos variáveis de início dos sintomas (1 dia a anos) e resolução dos sintomas (mediana de 3 semanas).
INTERAÇÕES MEDICAMENTOSAS
Ciclosporina
A ciclosporina aumentou a exposição à rosuvastatina e pode resultar em aumento do risco de miopatia. Portanto, em pacientes em uso de ciclosporina, a dose de CRESTOR 10 mg não deve exceder 5 mg uma vez ao dia [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Gemfibrozil
O gemfibrozil aumentou significativamente a exposição à rosuvastatina. Devido a um risco aumentado observado de miopatia/rabdomiólise, a terapia combinada com CRESTOR e gemfibrozil deve ser evitada. Se usado em conjunto, a dose de CRESTOR 10 mg não deve exceder 10 mg uma vez ao dia [ver FARMACOLOGIA CLÍNICA ].
Inibidores de Protease
coadministração de rosuvastatina com certos inibidores da protease tem efeitos diferentes na exposição à rosuvastatina e pode aumentar o risco de miopatia. O simeprevir, que é um inibidor da protease do vírus da hepatite C (HCV), ou combinações de atazanavir/ritonavir ou lopinavir/ritonavir, que são inibidores da protease do HIV-1, aumentam a exposição à rosuvastatina [Tabela 4 - FARMACOLOGIA CLÍNICA ]. Para estes inibidores de protease, a dose de CRESTOR 5mg não deve exceder 10 mg uma vez ao dia. As combinações de fosamprenavir/ritonavir ou tipranavir/ritonavir, que são inibidores da protease do HIV-1, produzem pouca ou nenhuma alteração na exposição à rosuvastatina. Deve-se ter cautela quando a rosuvastatina é coadministrada com inibidores da protease [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Anticoagulantes cumarínicos
CRESTOR 20mg aumentou significativamente o INR em pacientes recebendo anticoagulantes cumarínicos. Portanto, deve-se ter cautela quando os anticoagulantes cumarínicos são administrados em conjunto com CRESTOR. Em pacientes em uso concomitante de anticoagulantes cumarínicos e CRESTOR, o INR deve ser determinado antes de iniciar CRESTOR e com frequência suficiente durante o início da terapia para garantir que não ocorra alteração significativa do INR [ver AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Niacina
O risco de efeitos no músculo esquelético pode ser aumentado quando CRESTOR 5mg é usado em combinação com doses modificadoras de lipídios (≥1 g/dia) de niacina; deve-se ter cuidado ao prescrever com CRESTOR [ver AVISOS E PRECAUÇÕES ].
Fenofibrato
Quando CRESTOR 20mg foi coadministrado com fenofibrato, não foi observado aumento clinicamente significativo na AUC de rosuvastatina ou fenofibrato. Como se sabe que o risco de miopatia durante o tratamento com inibidores da HMG-CoA redutase aumenta com o uso concomitante de fenofibratos, deve-se ter cautela ao prescrever fenofibratos com CRESTOR [ver AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Colchicina
Casos de miopatia, incluindo rabdomiólise, foram relatados com inibidores da HMG-CoA redutase, incluindo rosuvastatina, coadministrados com colchicina, e deve-se ter cautela ao prescrever CRESTOR com colchicina [ver AVISOS E PRECAUÇÕES ].
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Efeitos do músculo esquelético
Casos de miopatia e rabdomiólise com insuficiência renal aguda secundária à mioglobinúria foram relatados com inibidores da HMG-CoA redutase, incluindo CRESTOR. Esses riscos podem ocorrer em qualquer nível de dose, mas são aumentados na dose mais alta (40 mg).
CRESTOR 5mg deve ser prescrito com cautela em pacientes com fatores predisponentes para miopatia (por exemplo, idade ≥65 anos, hipotireoidismo tratado inadequadamente, insuficiência renal). O risco de miopatia durante o tratamento com CRESTOR 5mg pode ser aumentado com a administração concomitante de algumas outras terapias hipolipemiantes (fibratos ou niacina), gemfibrozil, ciclosporina, atazanavir/ritonavir, lopinavir/ritonavir ou simeprevir [ver DOSAGEM E ADMINISTRAÇÃO e INTERAÇÕES MEDICAMENTOSAS ]. Casos de miopatia, incluindo rabdomiólise, foram relatados com inibidores da HMG-CoA redutase, incluindo rosuvastatina, coadministrados com colchicina, e deve-se ter cautela ao prescrever CRESTOR com colchicinas [ver INTERAÇÕES MEDICAMENTOSAS ].
terapia com CRESTOR deve ser descontinuada se ocorrerem níveis marcadamente elevados de creatina quinase ou se houver diagnóstico ou suspeita de miopatia. A terapia com CRESTOR 5mg também deve ser temporariamente suspensa em qualquer paciente com uma condição aguda e grave sugestiva de miopatia ou predispondo ao desenvolvimento de insuficiência renal secundária à rabdomiólise (p. e distúrbios eletrolíticos ou convulsões não controladas).
Houve relatos raros de miopatia necrosante imunomediada (IMNM), uma miopatia autoimune, associada ao uso de estatinas. O IMNM é caracterizado por: fraqueza muscular proximal e elevação da creatina quinase sérica, que persistem apesar da descontinuação do tratamento com estatinas; biópsia muscular mostrando miopatia necrosante sem inflamação significativa; melhora com imunossupressores.
Todos os pacientes devem ser aconselhados a relatar imediatamente ao seu médico dor muscular inexplicável, sensibilidade ou fraqueza, particularmente se acompanhada de mal-estar ou febre ou se os sinais e sintomas musculares persistirem após a descontinuação de CRESTOR.
Anormalidades das enzimas hepáticas
Recomenda-se a realização de testes de enzimas hepáticas antes do início de CRESTOR 10mg e se ocorrerem sinais ou sintomas de lesão hepática.
Aumentos nas transaminases séricas [AST (SGOT) ou ALT (SGPT)] foram relatados com inibidores da HMG-CoA redutase, incluindo CRESTOR. Na maioria dos casos, as elevações foram transitórias e desapareceram ou melhoraram com a continuação da terapia ou após uma breve interrupção na terapia. Houve dois casos de icterícia, para os quais não foi possível determinar uma relação com a terapia com CRESTOR, que se resolveu após a descontinuação da terapia. Não houve casos de insuficiência hepática ou doença hepática irreversível nestes estudos. Em uma análise conjunta de estudos controlados por placebo, aumentos nas transaminases séricas para >3 vezes o limite superior do normal ocorreram em 1,1% dos pacientes tomando CRESTOR 5mg versus 0,5% dos pacientes tratados com placebo.
Houve raros relatos pós-comercialização de insuficiência hepática fatal e não fatal em pacientes tomando estatinas, incluindo rosuvastatina. Se ocorrer lesão hepática grave com sintomas clínicos e/ou hiperbilirrubinemia ou icterícia durante o tratamento com CRESTOR 20mg, interrompa imediatamente a terapia. Se uma etiologia alternativa não for encontrada, não reinicie o CRESTOR.
CRESTOR 5mg deve ser usado com cautela em pacientes que consomem quantidades substanciais de álcool e/ou têm histórico de doença hepática crônica [ver FARMACOLOGIA CLÍNICA ]. A doença hepática ativa, que pode incluir elevações persistentes e inexplicáveis das transaminases, é uma contraindicação ao uso de CRESTOR [ver CONTRA-INDICAÇÕES ].
Anticoagulantes cumarínicos concomitantes
Deve-se ter cautela quando os anticoagulantes são administrados em conjunto com CRESTOR devido à sua potencialização do efeito dos anticoagulantes do tipo cumarínico no prolongamento do tempo de protrombina/INR. Em pacientes tomando anticoagulantes cumarínicos e CRESTOR concomitantemente, o INR deve ser determinado antes de iniciar CRESTOR 10mg e com frequência suficiente durante o início da terapia para garantir que não ocorra alteração significativa do INR [ver INTERAÇÕES MEDICAMENTOSAS ].
Proteinúria e Hematúria
No programa de ensaios clínicos CRESTOR, foram observadas proteinúria positiva com tira reagente e hematúria microscópica entre os pacientes tratados com CRESTOR. Esses achados foram mais frequentes em pacientes em uso de CRESTOR 40 mg, quando comparados a doses mais baixas de CRESTOR 20 mg ou inibidores da HMG-CoA redutase comparadores, embora geralmente sejam transitórios e não estejam associados a piora da função renal. Embora o significado clínico deste achado seja desconhecido, uma redução da dose deve ser considerada para pacientes em terapia com CRESTOR com proteinúria persistente inexplicada e/ou hematúria durante o exame de urina de rotina.
Efeitos Endócrinos
Aumentos nos níveis de HbA1c e glicose sérica em jejum foram relatados com inibidores da HMG-CoA redutase, incluindo CRESTOR. Com base em dados de ensaios clínicos com CRESTOR, em alguns casos, esses aumentos podem exceder o limite para o diagnóstico de diabetes mellitus [ver REAÇÕES ADVERSAS ].
Embora os estudos clínicos tenham demonstrado que CRESTOR 10mg isoladamente não reduz a concentração plasmática basal de cortisol ou prejudica a reserva adrenal, deve-se ter cautela se CRESTOR for administrado concomitantemente com medicamentos que podem diminuir os níveis ou a atividade dos hormônios esteroides endógenos, como cetoconazol, espironolactona e cimetidina.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( INFORMAÇÃO DO PACIENTE ).
Os pacientes devem ser instruídos a não tomar 2 doses de CRESTOR com intervalo de 12 horas.
Efeitos do músculo esquelético
Os pacientes devem ser aconselhados a relatar imediatamente dor, sensibilidade ou fraqueza muscular inexplicáveis, particularmente se acompanhadas de mal-estar ou febre ou se esses sinais ou sintomas musculares persistirem após a descontinuação de CRESTOR.
Uso concomitante de antiácidos
Ao tomar CRESTOR 5mg com um antiácido combinado de hidróxido de alumínio e magnésio, o antiácido deve ser tomado pelo menos 2 horas após a administração de CRESTOR 10mg.
Toxicidade embriofetal
Aconselhar as mulheres sobre o potencial reprodutivo do risco para o feto, usar contracepção eficaz durante o tratamento e informar seu médico sobre uma gravidez conhecida ou suspeita. [Vejo CONTRA-INDICAÇÕES e Uso em populações específicas ].
Lactação
Aconselhe as mulheres a não amamentar durante o tratamento com CRESTOR [ver CONTRA-INDICAÇÕES e Uso em populações específicas ].
Enzimas do Fígado
Recomenda-se a realização de testes de enzimas hepáticas antes do início de CRESTOR e se ocorrerem sinais ou sintomas de lesão hepática. Todos os pacientes tratados com CRESTOR devem ser aconselhados a relatar imediatamente quaisquer sintomas que possam indicar lesão hepática, incluindo fadiga, anorexia, desconforto abdominal superior direito, urina escura ou icterícia.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Em um estudo de carcinogenicidade de 104 semanas em ratos em níveis de dose de 2, 20, 60 ou 80 mg/kg/dia por gavagem oral, a incidência de pólipos estromais uterinos foi significativamente aumentada em fêmeas com 80 mg/kg/dia em doses sistêmicas. exposição 20 vezes a exposição humana a 40 mg/dia com base na AUC. O aumento da incidência de pólipos não foi observado em doses mais baixas.
Em um estudo de carcinogenicidade de 107 semanas em camundongos que receberam 10, 60 ou 200 mg/kg/dia por gavagem oral, um aumento na incidência de adenoma/carcinoma hepatocelular foi observado em 200 mg/kg/dia em exposições sistêmicas 20 vezes a exposição humana a 40 mg/dia com base na AUC. Uma incidência aumentada de tumores hepatocelulares não foi observada em doses mais baixas.
A rosuvastatina não foi mutagênica ou clastogênica com ou sem ativação metabólica no teste de Ames com Salmonella typhimurium e Escherichia coli, no ensaio de linfoma de camundongo e no ensaio de aberração cromossômica em células de pulmão de hamster chinês. A rosuvastatina foi negativa no teste de micronúcleo em camundongos in vivo.
Em estudos de fertilidade em ratos com doses de gavagem oral de 5, 15, 50 mg/kg/dia, os machos foram tratados por 9 semanas antes e durante o acasalamento e as fêmeas foram tratadas 2 semanas antes do acasalamento e durante todo o acasalamento até o dia 7 de gestação. efeito na fertilidade foi observado com 50 mg/kg/dia (exposições sistêmicas até 10 vezes a exposição humana com 40 mg/dia com base na AUC). Em testículos de cães tratados com rosuvastatina na dose de 30 mg/kg/dia por um mês, foram observadas células gigantes espermátides. Células gigantes espermatídicas foram observadas em macacos após 6 meses de tratamento com 30 mg/kg/dia, além da vacuolação do epitélio tubular seminífero. As exposições no cão foram 20 vezes e no macaco 10 vezes a exposição humana a 40 mg/dia com base na área de superfície corporal. Achados semelhantes foram observados com outras drogas desta classe.
Uso em populações específicas
Gravidez
Resumo do risco
CRESTOR 5mg é contraindicado para uso em mulheres grávidas, uma vez que a segurança em mulheres grávidas não foi estabelecida e não há benefício aparente da terapia com CRESTOR 20mg durante a gravidez. Como os inibidores da HMG-CoA redutase diminuem a síntese de colesterol e possivelmente a síntese de outras substâncias biologicamente ativas derivadas do colesterol, CRESTOR pode causar danos ao feto quando administrado a mulheres grávidas. CRESTOR 5mg deve ser descontinuado assim que a gravidez for reconhecida. CONTRA-INDICAÇÕES ]. Os dados publicados limitados sobre o uso de rosuvastatina são insuficientes para determinar um risco associado ao medicamento de malformações congênitas maiores ou aborto espontâneo. Em estudos de reprodução animal, não houve efeitos adversos no desenvolvimento com a administração oral de rosuvastatina durante a organogênese em exposições sistêmicas equivalentes a uma dose humana máxima recomendada (MRHD) de 40 mg/dia em ratos ou coelhos (com base na AUC e na área de superfície corporal, respectivamente ). Em ratos e coelhos, ocorreu diminuição da sobrevida do filhote/fetal em 12 vezes e equivalente, respectivamente, à MRHD de 40 mg/dia [ver Dados ].
O risco de fundo estimado de defeitos congênitos graves e aborto espontâneo para a população indicada é desconhecido. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e aborto espontâneo em gestações clinicamente reconhecidas é de 2-4% e 15-20%, respectivamente.
Dados
Dados humanos
Dados publicados limitados sobre a rosuvastatina não mostraram um risco aumentado de malformações congênitas maiores ou aborto espontâneo. Raros relatos de anomalias congênitas foram recebidos após exposição intrauterina a outras estatinas. Em uma revisão de aproximadamente 100 gestações acompanhadas prospectivamente em mulheres expostas à sinvastatina ou lovastatina, as incidências de anomalias congênitas, abortos espontâneos e mortes fetais/natimortos não excederam o esperado na população geral. O número de casos é adequado para excluir um aumento ≥3 a 4 vezes nas anomalias congênitas em relação à incidência de base. Em 89% das gestações acompanhadas prospectivamente, o tratamento medicamentoso foi iniciado antes da gravidez e foi descontinuado em algum momento do primeiro trimestre quando a gravidez foi identificada.
Dados de animais
rosuvastatina atravessa a placenta em ratos e coelhos e é encontrada no tecido fetal e no líquido amniótico em 3% e 20%, respectivamente, da concentração plasmática materna após uma dose única oral de 25 mg/kg de gavagem no dia 16 de gestação em ratos. Uma maior distribuição de tecido fetal (concentração plasmática materna de 25%) foi observada em coelhos após uma dose oral única de 1 mg/kg no 18º dia de gestação.
A administração de rosuvastatina não indicou efeito teratogênico em ratos ≤ 25 mg/kg/dia ou em coelhos ≤ 3 mg/kg/dia (doses equivalentes à MRHD de 40 mg/dia com base na AUC e na área de superfície corporal, respectivamente).
Em ratas que receberam 5, 15 e 50 mg/kg/dia antes do acasalamento e continuando até o 7º dia de gestação resultou em diminuição do peso corporal fetal (filhotes fêmeas) e ossificação retardada em 50 mg/kg/dia (10 vezes a exposição humana em a dose de MRHD de 40 mg/dia com base na AUC).
Em ratas prenhas que receberam 2, 10 e 50 mg/kg/dia de rosuvastatina do 7º dia de gestação até o 21º dia de lactação (desmame), ocorreu diminuição da sobrevivência dos filhotes com 50 mg/kg/dia (dose equivalente a 12 vezes a MRHD de 40 mg /dia com base na área de superfície corporal).
Em coelhas grávidas que receberam 0,3, 1 e 3 mg/kg/dia de rosuvastatina do 6º ao 18º dia de gestação, observou-se diminuição da viabilidade fetal e mortalidade materna com 3 mg/kg/dia (dose equivalente à MRHD de 40 mg/ dia com base na área de superfície corporal).
Lactação
Resumo do risco
O uso de rosuvastatina é contraindicado durante a amamentação [ver CONTRA-INDICAÇÕES ]. Dados limitados indicam que CRESTOR está presente no leite humano. Não há informações disponíveis sobre os efeitos do medicamento no lactente ou os efeitos do medicamento na produção de leite. Devido ao potencial de reações adversas graves em um lactente, avise as pacientes que a amamentação não é recomendada durante o tratamento com CRESTOR.
Fêmeas e Machos com Potencial Reprodutivo
Contracepção
CRESTOR pode causar danos ao feto quando administrado a mulheres grávidas [ver Uso em populações específicas ]. Aconselhe as mulheres com potencial reprodutivo a utilizarem métodos contracetivos eficazes durante o tratamento com CRESTOR.
Uso Pediátrico
Em crianças e adolescentes de 8 a 17 anos de idade com hipercolesterolemia familiar heterozigótica, a segurança e eficácia de CRESTOR 10mg como adjuvante da dieta para reduzir os níveis de colesterol total, LDL-C e ApoB quando, após um ensaio adequado de dietoterapia, o LDL -C excede 190 mg/dL ou quando o LDL-C excede 160 mg/dL e há história familiar positiva de DCV prematura ou dois ou mais outros fatores de risco de DCV, foram estabelecidos em um estudo controlado e em um aberto, não controlado julgamento [ver Estudos clínicos ]. A eficácia a longo prazo da terapia com CRESTOR iniciada na infância para reduzir a morbidade e mortalidade na idade adulta não foi estabelecida.
segurança e eficácia de CRESTOR 5mg em crianças e adolescentes de 10 a 17 anos de idade com hipercolesterolemia familiar heterozigótica foram avaliadas em um ensaio clínico controlado de 12 semanas de duração seguido de 40 semanas de exposição aberta. Os pacientes tratados com 5 mg, 10 mg e 20 mg diários de CRESTOR 10 mg tiveram um perfil de experiência adversa geralmente semelhante ao dos pacientes tratados com placebo. Não houve efeito detectável de CRESTOR no crescimento, peso, IMC (índice de massa corporal) ou maturação sexual [ver Estudos clínicos ] em crianças e adolescentes (10 a 17 anos).
CRESTOR não foi estudado em ensaios clínicos controlados envolvendo pacientes pré-púberes ou pacientes com menos de 10 anos de idade com hipercolesterolemia familiar heterozigótica. No entanto, a segurança e a eficácia de CRESTOR foram avaliadas em um estudo aberto não controlado de dois anos que incluiu crianças e adolescentes de 8 a 17 anos de idade com hipercolesterolemia familiar heterozigótica [ver Estudos clínicos ]. A segurança e eficácia de CRESTOR 5mg na redução do LDL-C pareceram geralmente consistentes com as observadas em pacientes adultos, apesar das limitações do desenho do estudo não controlado.
Crianças e adolescentes de 7 a 15 anos de idade com hipercolesterolemia familiar homozigótica foram estudados em um estudo cruzado de 6 semanas, randomizado, controlado por placebo, com CRESTOR 20 mg uma vez ao dia seguido por 12 semanas de tratamento aberto [ver Estudos clínicos ]. Em geral, o perfil de segurança neste estudo foi consistente com o perfil de segurança previamente estabelecido em adultos.
Embora nem todas as reações adversas identificadas na população adulta tenham sido observadas em estudos clínicos com crianças e adolescentes, as mesmas advertências e precauções para adultos devem ser consideradas para crianças e adolescentes. Mulheres adolescentes devem ser aconselhadas sobre métodos contraceptivos apropriados enquanto estiverem em terapia com CRESTOR 5mg [ver Uso em populações específicas ].
Uso Geriátrico
Dos 10.275 pacientes em estudos clínicos com CRESTOR, 3159 (31%) tinham 65 anos ou mais e 698 (6,8%) tinham 75 anos ou mais. Não foram observadas diferenças gerais na segurança ou eficácia entre esses indivíduos e indivíduos mais jovens, e outras experiências clínicas relatadas não identificaram diferenças nas respostas entre os pacientes idosos e os pacientes mais jovens, mas a maior sensibilidade de alguns indivíduos mais velhos não pode ser descartada.
Pacientes idosos apresentam maior risco de miopatia e CRESTOR deve ser prescrito com cautela em idosos [ver AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Insuficiência renal
A exposição à rosuvastatina não é influenciada por insuficiência renal leve a moderada (CLcr ≥30 mL/min/1,73 m²). A exposição à rosuvastatina aumenta de forma clinicamente significativa em pacientes com insuficiência renal grave (CLcr DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Insuficiência hepática
CRESTOR é contraindicado em pacientes com doença hepática ativa, que pode incluir elevações persistentes inexplicáveis dos níveis de transaminases hepáticas. Sabe-se que a doença hepática crônica pelo álcool aumenta a exposição à rosuvastatina; CRESTOR 20mg deve ser usado com cautela nestes pacientes [ver CONTRA-INDICAÇÕES , AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
Pacientes Asiáticos
Estudos farmacocinéticos demonstraram um aumento aproximado de 2 vezes na exposição mediana à rosuvastatina em indivíduos asiáticos quando comparados com controles caucasianos. A dosagem de CRESTOR deve ser ajustada em pacientes asiáticos [ver DOSAGEM E ADMINISTRAÇÃO e FARMACOLOGIA CLÍNICA ].
SOBREDOSAGEM
Não existe tratamento específico em caso de sobredosagem. Em caso de sobredosagem, o doente deve ser tratado sintomaticamente e devem ser instituídas medidas de suporte conforme necessário. A hemodiálise não aumenta significativamente a depuração da rosuvastatina.
CONTRA-INDICAÇÕES
CRESTOR 20mg é contraindicado nas seguintes condições:
- Pacientes com hipersensibilidade conhecida a qualquer componente deste produto. Reações de hipersensibilidade incluindo erupção cutânea, prurido, urticária e angioedema foram relatadas com CRESTOR [ver REAÇÕES ADVERSAS ].
- Pacientes com doença hepática ativa, que pode incluir elevações persistentes inexplicáveis dos níveis de transaminase hepática [ver AVISOS E PRECAUÇÕES ].
- Gravidez [ver Uso em populações específicas ].
- Lactação. Dados limitados indicam que CRESTOR 20mg está presente no leite humano. Como as estatinas têm potencial para reações adversas graves em lactentes, as mulheres que necessitam de tratamento com CRESTOR não devem amamentar seus bebês [ver Uso em populações específicas ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
CRESTOR 10mg é um inibidor seletivo e competitivo da HMG-CoA redutase, a enzima limitante da taxa que converte a 3-hidroxi-3-metilglutaril coenzima A em mevalonato, um precursor do colesterol. Estudos in vivo em animais e estudos in vitro em culturas de células animais e humanas mostraram que a rosuvastatina tem uma alta absorção e seletividade para ação no fígado, o órgão alvo para redução do colesterol. Em estudos in vivo e in vitro, a rosuvastatina produz seus efeitos modificadores de lipídios de duas maneiras. Primeiro, aumenta o número de receptores hepáticos de LDL na superfície celular para aumentar a captação e o catabolismo de LDL. Em segundo lugar, a rosuvastatina inibe a síntese hepática de VLDL, o que reduz o número total de partículas de VLDL e LDL.
Farmacodinâmica
A dose de CRESTOR 5mg reduz de forma dependente o colesterol LDL elevado e reduz o colesterol total e os triglicerídeos e aumenta o colesterol HDL [ver Estudos clínicos ]. Uma resposta terapêutica ao CRESTOR 5mg é evidente dentro de 1 semana após o início da terapia e 90% da resposta máxima é geralmente alcançada em 2 semanas. A resposta máxima geralmente é alcançada em 4 semanas e é mantida após isso. A individualização da dosagem do medicamento deve ser baseada na resposta terapêutica [ver DOSAGEM E ADMINISTRAÇÃO ].
Farmacocinética
Absorção
Em estudos de farmacologia clínica no homem, as concentrações plasmáticas máximas de rosuvastatina foram atingidas 3 a 5 horas após a administração oral. Tanto a Cmax como a AUC aumentaram em proporção aproximada à dose de CRESTOR 10mg. A biodisponibilidade absoluta da rosuvastatina é de aproximadamente 20%.
A administração de CRESTOR com alimentos não afetou a AUC da rosuvastatina.
A AUC da rosuvastatina não difere após a administração do medicamento à noite ou pela manhã.
Distribuição
O volume médio de distribuição no estado de equilíbrio da rosuvastatina é de aproximadamente 134 litros. A rosuvastatina está 88% ligada às proteínas plasmáticas, principalmente albumina. Esta ligação é reversível e independente das concentrações plasmáticas.
Eliminação
rosuvastatina é eliminada principalmente por excreção nas fezes. A meia-vida de eliminação da rosuvastatina é de aproximadamente 19 horas.
Metabolismo
A rosuvastatina não é extensivamente metabolizada; aproximadamente 10% de uma dose radiomarcada é recuperada como metabólito. O principal metabólito é a N-desmetil rosuvastatina, que é formada principalmente pelo citocromo P450 \ 2C9, e estudos in vitro demonstraram que a N-desmetil rosuvastatina tem aproximadamente um sexto a metade da atividade inibitória da HMG-CoA redutase do composto original . No geral, mais de 90% da atividade inibidora da HMG-CoA redutase ativa no plasma é explicada pelo composto original.
Excreção
Após administração oral, a rosuvastatina e seus metabólitos são excretados principalmente nas fezes (90%). Após uma dose intravenosa, aproximadamente 28% da depuração corporal total foi por via renal e 72% por via hepática.
Populações Específicas
Grupos raciais ou étnicos
Uma análise farmacocinética populacional não revelou diferenças clinicamente relevantes na farmacocinética entre os grupos caucasianos, hispânicos e negros ou afro-caribenhos. No entanto, estudos farmacocinéticos, incluindo um realizado nos EUA, demonstraram um aumento aproximado de 2 vezes na exposição mediana (AUC e Cmax) em indivíduos asiáticos quando comparados com um grupo controle caucasiano.
Pacientes Masculinos e Femininos
Não houve diferenças nas concentrações plasmáticas de rosuvastatina entre homens e mulheres.
Pacientes pediátricos
Em uma análise farmacocinética populacional de dois estudos pediátricos envolvendo pacientes com hipercolesterolemia familiar heterozigótica de 10 a 17 anos de idade e 8 a 17 anos de idade, respectivamente, a exposição à rosuvastatina pareceu comparável ou inferior à exposição à rosuvastatina em pacientes adultos.
Pacientes Geriátricos
Não houve diferenças nas concentrações plasmáticas de rosuvastatina entre as populações não idosas e idosas (idade ≥65 anos).
Pacientes com Insuficiência Renal
insuficiência renal leve a moderada (CLcr ≥30 mL/min/1,73 m²) não teve influência nas concentrações plasmáticas de rosuvastatina. No entanto, as concentrações plasmáticas de rosuvastatina aumentaram em extensão clinicamente significativa (cerca de 3 vezes) em pacientes com insuficiência renal grave (CLcr 80 mL/min/ 1,73m²).
Hemodiálise
As concentrações plasmáticas de estado estacionário de rosuvastatina em pacientes em hemodiálise crônica foram aproximadamente 50% maiores em comparação com voluntários saudáveis com função renal normal.
Pacientes com Insuficiência Hepática
Em pacientes com doença hepática alcoólica crônica, as concentrações plasmáticas de rosuvastatina aumentaram modestamente.
Em doentes com doença Child-Pugh A, a Cmax e a AUC aumentaram 60% e 5%, respetivamente, em comparação com doentes com função hepática normal. Em pacientes com doença Child-Pugh B, Cmax e AUC aumentaram 100% e 21%, respectivamente, em comparação com pacientes com função hepática normal.
Estudos de interações medicamentosas
A depuração da rosuvastatina não depende do metabolismo pelo citocromo P450 3A4 numa extensão clinicamente significativa.
A rosuvastatina é um substrato para certas proteínas transportadoras, incluindo a poliproteína transportadora de ânions orgânicos 1B1 do transportador de captação hepática (OATP1B1) e a proteína de resistência ao câncer de mama do transportador de efluxo (BCRP). A administração concomitante de CRESTOR 10mg com medicamentos que são inibidores dessas proteínas transportadoras (por exemplo, ciclosporina, certos inibidores da protease do HIV) pode resultar em aumento das concentrações plasmáticas de rosuvastatina [ver DOSAGEM E ADMINISTRAÇÃO e INTERAÇÕES MEDICAMENTOSAS ].
Farmacogenômica
disposição dos inibidores da HMG-CoA redutase, incluindo a rosuvastatina, envolve OATP1B1 e outras proteínas transportadoras. Concentrações plasmáticas mais elevadas de rosuvastatina foram relatadas em grupos muito pequenos de pacientes (n=3 a 5) que apresentam dois alelos de função reduzida do gene que codifica OATP1B1 (SLCO1B1 521T > C). A frequência deste genótipo (ou seja, SLCO1B1 521 C/C) é geralmente inferior a 5% na maioria dos grupos raciais/étnicos. O impacto deste polimorfismo na eficácia e/ou segurança da rosuvastatina não foi claramente estabelecido.
Toxicologia e/ou Farmacologia Animal
Toxicidade do Sistema Nervoso Central
Lesões vasculares do SNC, caracterizadas por hemorragias perivasculares, edema e infiltração de células mononucleares dos espaços perivasculares, foram observadas em cães tratados com vários outros membros desta classe de drogas. Um fármaco quimicamente semelhante nesta classe produziu degeneração do nervo óptico dose-dependente (degeneração Walleriana das fibras retinogeniculadas) em cães, em uma dose que produziu níveis plasmáticos do fármaco cerca de 30 vezes maiores do que o nível médio do fármaco em humanos tomando a dose mais alta recomendada. Edema, hemorragia e necrose parcial no interstício do plexo coróide foram observados em uma cadela sacrificada moribunda no dia 24 a 90 mg/kg/dia por gavagem oral (exposições sistêmicas 100 vezes a exposição humana a 40 mg/dia com base em AUC). A opacidade da córnea foi observada em cães tratados por 52 semanas a 6 mg/kg/dia por gavagem oral (exposições sistêmicas 20 vezes a exposição humana a 40 mg/dia com base na AUC). A catarata foi observada em cães tratados por 12 semanas por gavagem oral a 30 mg/kg/dia (exposições sistêmicas 60 vezes a exposição humana a 40 mg/dia com base na AUC). Displasia retiniana e perda retiniana foram observadas em cães tratados por 4 semanas por gavagem oral a 90 mg/kg/dia (exposições sistêmicas 100 vezes a exposição humana a 40 mg/dia com base na AUC). Doses ≤ 30 mg/kg/dia (exposições sistêmicas ≤ 60 vezes a exposição humana a 40 mg/dia com base na AUC) não revelaram achados retinianos durante o tratamento por até um ano.
Estudo de toxicologia juvenil
Em um estudo com juvenis, os ratos foram dosados por gavagem oral com 10 ou 50 mg/kg/dia desde o desmame por 9 semanas antes do pareamento, durante todo o pareamento e até o dia anterior à necropsia para machos ou até o dia 7 de gestação para fêmeas. Não foram observados efeitos no desenvolvimento sexual, aparência testicular e epididimal ou fertilidade em qualquer nível de dose (2 vezes ou até 24 vezes a exposição humana (AUC) na dose pediátrica máxima de 20 mg/dia).
Estudos clínicos
Hiperlipidemia e dislipidemia mista
CRESTOR 5mg reduz o C Total, LDL-C, ApoB, não HDL-C e TG, e aumenta o HDL-C, em pacientes adultos com hiperlipidemia e dislipidemia mista.
Estudo de variação de dose
Em um estudo multicêntrico, duplo-cego, controlado por placebo, de variação de dose em pacientes com hiperlipidemia, CRESTOR administrado em dose única diária por 6 semanas reduziu significativamente C Total, C-LDL, C-não-HDL e ApoB, em toda a dose intervalo (Tabela 6).
Estudo controlado ativo
CRESTOR 5mg foi comparado com os inibidores da HMG-CoA redutase atorvastatina, sinvastatina e pravastatina em um estudo multicêntrico, aberto e de variação de dose de 2.240 pacientes com hiperlipidemia ou dislipidemia mista. Após a randomização, os pacientes foram tratados por 6 semanas com uma dose única diária de CRESTOR 20mg, atorvastatina, sinvastatina ou pravastatina (Figura 1 e Tabela 7).
Figura 1: Alteração percentual de LDL-C por dose de CRESTOR 20mg, atorvastatina, sinvastatina e pravastatina na semana 6 em pacientes com hiperlipidemia ou dislipidemia mista 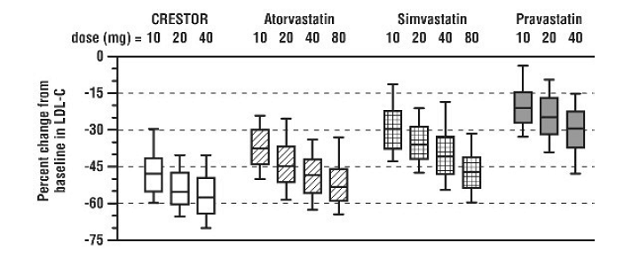
Os gráficos de caixa são uma representação dos valores dos percentis 25, 50 e 75, com bigodes representando os valores dos percentis 10 e 90. LDL-C basal médio: 189 mg/Dl
Hipercolesterolemia Familiar Heterozigótica
Estudo controlado ativo
Em um estudo de pacientes com HF heterozigótica (LDL média basal de 291), os pacientes foram randomizados para CRESTOR 20 mg ou atorvastatina 20 mg. A dose foi aumentada em intervalos de 6 semanas. Reduções significativas de LDL-C desde a linha de base foram observadas em cada dose em ambos os grupos de tratamento (Tabela 8).
Hipertrigliceridemia
Estudo de dose-resposta
Em um estudo de dose-resposta, duplo-cego, controlado por placebo em pacientes com níveis basais de TG de 273 a 817 mg/dL, CRESTOR 10 mg administrado em dose única diária (5 a 40 mg) durante 6 semanas reduziu significativamente os níveis séricos de TG ( Tabela 9).
Disbetalipoproteinemia Primária (Hiperlipoproteinemia Tipo III)
Em um estudo cruzado, randomizado, multicêntrico e duplo-cego, 32 pacientes (27 com ε2/ε2 e 4 com mutação apo E [Arg145Cys] com disbetalipoproteinemia primária (Hiperlipoproteinemia Tipo III) entraram em um período de 6 semanas de introdução alimentar no NCEP Dieta de Mudança de Estilo de Vida Terapêutica (TLC). Após a introdução da dieta, os pacientes foram randomizados para uma sequência de tratamentos em conjunto com a dieta TLC por 6 semanas cada: rosuvastatina 10 mg seguido de rosuvastatina 20 mg ou rosuvastatina 20 mg seguido de rosuvastatina 10 mg CRESTOR reduziu os níveis de lipoproteínas não HDL-C (ponto final primário) e de lipoproteínas remanescentes circulantes.Os resultados são mostrados na tabela abaixo.
Hipercolesterolemia Familiar Homozigótica
Estudo de titulação de dose
Em um estudo aberto de titulação forçada, pacientes homozigotos com HF (n=40, 8-63 anos) foram avaliados quanto à sua resposta a CRESTOR 20 a 40 mg titulados em um intervalo de 6 semanas. Na população geral, a redução média de LDL-C em relação à linha de base foi de 22%. Cerca de um terço dos pacientes se beneficiaram com o aumento da dose de 20 mg para 40 mg com redução adicional do LDL superior a 6%. Nos 27 pacientes com redução de pelo menos 15% no LDL-C, a redução média do LDL-C foi de 30% (redução média de 28%). Entre 13 pacientes com redução de LDL-C
Pacientes pediátricos com hipercolesterolemia familiar homozigótica
CRESTOR foi estudado em um estudo randomizado, duplo-cego, controlado por placebo, multicêntrico, cruzado em 14 crianças e adolescentes com hipercolesterolemia familiar homozigótica. O estudo incluiu uma fase de introdução alimentar de 4 semanas durante a qual os pacientes receberam CRESTOR 10 mg diariamente, uma fase cruzada que incluiu dois períodos de tratamento de 6 semanas com CRESTOR 20 mg ou placebo em ordem aleatória, seguido por um período de 12- semana fase de rótulo aberto durante a qual todos os pacientes receberam CRESTOR 20 mg. Os pacientes tinham idades entre 7 e 15 anos (mediana de 11 anos), 50% eram do sexo masculino, 71% eram caucasianos, 21% eram asiáticos, 7% eram negros e nenhum paciente era de etnia hispânica. Cinquenta por cento estavam em terapia de aférese e 57% estavam em uso de ezetimiba. Os pacientes que entraram no estudo com terapia de aférese ou ezetimiba continuaram o tratamento durante todo o estudo. A média de LDL-C no início do estudo foi de 416 mg/dL (intervalo de 152 a 716 mg/dL). Um total de 13 pacientes completaram os dois períodos de tratamento da fase randomizada cruzada; um paciente retirou o consentimento devido à incapacidade de coletar sangue durante a fase de cruzamento.
CRESTOR 20 mg reduziu significativamente o LDL-C, colesterol total, ApoB e não-HDL-C em comparação com placebo (Tabela 11).
Pacientes pediátricos com hipercolesterolemia familiar heterozigótica
Em um estudo duplo-cego, randomizado, multicêntrico, controlado por placebo, de 12 semanas, 176 (97 homens e 79 mulheres) crianças e adolescentes com hipercolesterolemia familiar heterozigótica foram randomizados para 5, 10 ou 20 mg de rosuvastatina ou placebo diariamente. A idade dos pacientes variava de 10 a 17 anos (idade mediana de 14 anos), com aproximadamente 30% dos pacientes de 10 a 13 anos e aproximadamente 17%, 18%, 40% e 25% nos estágios II, III, IV, e V, respectivamente. As fêmeas estavam pelo menos 1 ano após a menarca. A média de LDL-C no início do estudo foi de 233 mg/dL (intervalo de 129 a 399). A fase duplo-cega de 12 semanas foi seguida por uma fase de titulação de dose aberta de 40 semanas, onde todos os pacientes (n=173) receberam 5 mg, 10 mg ou 20 mg de rosuvastatina diariamente.
rosuvastatina reduziu significativamente os níveis de LDL-C (ponto final primário), colesterol total e ApoB em cada dose em comparação com placebo. Os resultados são mostrados na Tabela 12 abaixo.
Ao final do período de tratamento duplo-cego de 12 semanas, a porcentagem de pacientes que atingiram a meta de LDL-C de menos de 110 mg/dL (2,8 mmol/L) foi de 0% para placebo, 12% para rosuvastatina 5 mg , 41% para rosuvastatina 10 mg e 41% para rosuvastatina 20 mg. Para a fase aberta de 40 semanas, 71% dos pacientes foram titulados para a dose máxima de 20 mg e 41% dos pacientes atingiram a meta de LDL-C de 110 mg/dL.
rosuvastatina também foi estudada em um estudo aberto de dois anos, não controlado, de titulação até o objetivo que incluiu 175 crianças e adolescentes com hipercolesterolemia familiar heterozigótica com 8 a 17 anos de idade (79 meninos e 96 meninas). Todos os pacientes tinham um defeito genético documentado no receptor de LDL ou na ApoB. Aproximadamente 89% eram caucasianos, 7% asiáticos, 1% negros e menos de 1% hispânicos. A média de LDL-C no início do estudo foi de 236 mg/dL. Cinquenta e oito (33%) pacientes eram pré-púberes no início do estudo. A dose inicial de rosuvastatina para todas as crianças e adolescentes foi de 5 mg uma vez ao dia. Crianças de 8 a menos de 10 anos de idade (n=41 na linha de base) podem titular a dose máxima de 10 mg uma vez ao dia, e crianças e adolescentes de 10 a 17 anos de idade podem titular a dose máxima de 20 mg uma vez ao dia.
As reduções no LDL-C desde o início do estudo foram geralmente consistentes em todas as faixas etárias do estudo, bem como com a experiência anterior em estudos controlados em adultos e pediátricos.
eficácia a longo prazo da terapia com rosuvastatina iniciada na infância para reduzir a morbidade e mortalidade na idade adulta não foi estabelecida.
Desaceleração da progressão da aterosclerose
No estudo Measuring Effects on Intima Media Thickness: an Evaluation Of Rosuvastatin 40 mg (METEOR), o efeito da terapia com CRESTOR na aterosclerose carotídea foi avaliado por ultrassonografia modo B em pacientes com LDL-C elevado, de baixo risco (risco de Framingham
taxa anualizada de mudança da linha de base para o grupo placebo foi de +0,0131 mm/ano (p
Em um nível de paciente individual no grupo tratado com CRESTOR, 52,1% dos pacientes demonstraram ausência de progressão da doença (definida como uma taxa de variação anual negativa), em comparação com 37,7% dos pacientes no grupo placebo.
Prevenção primária de doenças cardiovasculares
Na justificativa para o uso de estatinas na prevenção primária: um estudo de Intervention Trial Avaliando Rosuvastatina (JUPITER), o efeito de CRESTOR (rosuvastatina cálcica) na ocorrência de eventos de doenças cardiovasculares (CV) maiores foi avaliado em 17.802 homens (≥50 anos ) e mulheres (≥ 60 anos) sem doença cardiovascular clinicamente evidente, níveis de LDL-C
desfecho primário foi um desfecho composto consistindo do tempo até a primeira ocorrência de qualquer um dos seguintes eventos CV principais: morte CV, infarto do miocárdio não fatal, acidente vascular cerebral não fatal, hospitalização por angina instável ou procedimento de revascularização arterial.
A rosuvastatina reduziu significativamente o risco de eventos cardiovasculares maiores (252 eventos no grupo placebo vs. 142 eventos no grupo rosuvastatina) com uma redução estatisticamente significativa (p
Figura 2: Tempo até a Primeira Ocorrência de Eventos Cardiovasculares Maiores em JÚPITER 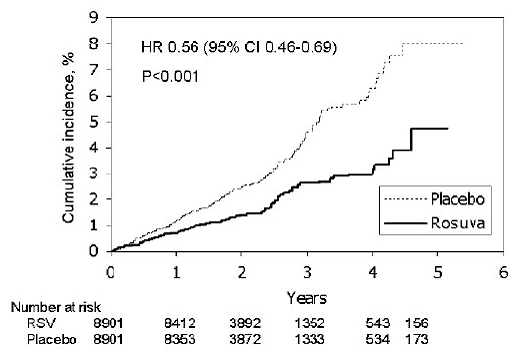
Os componentes individuais do desfecho primário são apresentados na Figura 3. A rosuvastatina reduziu significativamente o risco de infarto do miocárdio não fatal, acidente vascular cerebral não fatal e procedimentos de revascularização arterial. Não houve diferenças significativas de tratamento entre os grupos rosuvastatina e placebo para morte por causas cardiovasculares ou hospitalizações por angina instável.
A rosuvastatina reduziu significativamente o risco de infarto do miocárdio (6 eventos fatais e 62 eventos não fatais em indivíduos tratados com placebo versus 9 eventos fatais e 22 eventos não fatais em indivíduos tratados com rosuvastatina) e o risco de acidente vascular cerebral (6 eventos fatais e 58 eventos não fatais em indivíduos tratados com placebo vs. 3 eventos fatais e 30 eventos não fatais em indivíduos tratados com rosuvastatina).
Em uma análise de subgrupo post-hoc de indivíduos JUPITER (n=1405; rosuvastatina=725, placebo=680) com PCRhs ≥2 mg/L e sem outros fatores de risco tradicionais (tabagismo, PA ≥140/90 ou uso de anti-hipertensivos, baixo HDL-C) além da idade, após ajuste para HDL-C alto, não houve benefício significativo do tratamento com o tratamento com rosuvastatina.
Figura 3: Principais eventos CV por grupo de tratamento em JUPITER 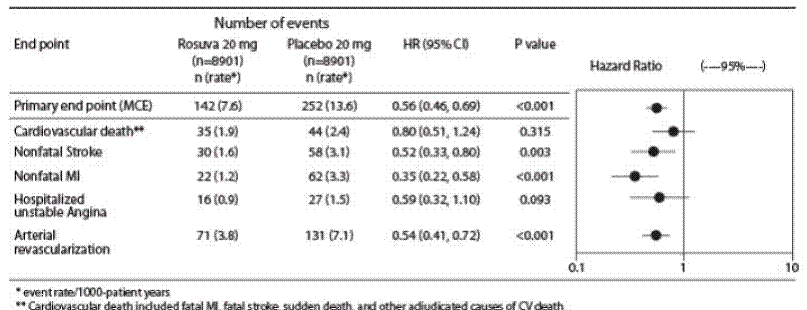
Em um ano, a rosuvastatina aumentou o HDL-C e reduziu o LDL-C, hsCRP, colesterol total e níveis séricos de triglicerídeos (p
INFORMAÇÃO DO PACIENTE
CRESTOR® (Kres-tor) rosuvastatina cálcica comprimidos
Leia atentamente esta Informação do Paciente antes de começar a tomar CRESTOR 20mg e cada vez que receber uma recarga. Se você tiver alguma dúvida sobre CRESTOR, pergunte ao seu médico. Apenas o seu médico pode determinar se CRESTOR é adequado para você.
O que é CRESTOR?
CRESTOR 20mg é um medicamento de prescrição que contém um medicamento para baixar o colesterol chamado rosuvastatina cálcica. A maior parte do colesterol no sangue é produzida no fígado. CRESTOR 20mg funciona reduzindo o colesterol de duas maneiras: CRESTOR 5mg bloqueia uma enzima no fígado fazendo com que o fígado produza menos colesterol, e CRESTOR 20mg aumenta a absorção e degradação pelo fígado do colesterol já no sangue.
- CRESTOR é usado junto com a dieta para:
- diminuir o nível do seu colesterol “ruim” (LDL)
- aumentar o nível do seu colesterol “bom” (HDL)
- diminuir o nível de gordura no sangue (triglicerídeos)
- retardar o acúmulo de depósitos de gordura (placa) nas paredes dos vasos sanguíneos
- CRESTOR é usado para tratar:
- adultos que não podem controlar seus níveis de colesterol apenas com dieta e exercícios
- crianças de 8 a 17 anos de idade com hipercolesterolemia familiar heterozigótica (uma condição hereditária que causa altos níveis de LDL)
- crianças de 7 a 17 anos de idade com hipercolesterolemia familiar homozigótica (uma condição hereditária que causa altos níveis de LDL).
CRESTOR 20mg não está aprovado para uso em crianças com hipercolesterolemia familiar heterozigótica com menos de 8 anos de idade ou para uso em crianças com hipercolesterolemia familiar homozigótica com menos de 7 anos de idade.
CRESTOR 5mg é usado para reduzir o risco de ataques cardíacos e derrames em homens com 50 anos de idade ou mais e mulheres com 60 anos de idade ou mais que não têm doença cardíaca conhecida, mas têm certos fatores de risco adicionais.
Não se sabe se CRESTOR 10mg é seguro e eficaz em pessoas com dislipidemias Fredrickson tipo I e V.
Quem não deve tomar CRESTOR?
Não tome CRESTOR se você:
- são alérgicos à rosuvastatina cálcica ou a qualquer um dos ingredientes de CRESTOR. Consulte o final deste folheto para obter uma lista completa dos ingredientes de CRESTOR.
- tem problemas de fígado.
- está grávida ou pensa que pode estar grávida, ou planeia engravidar. CRESTOR 20mg pode prejudicar o feto. Se engravidar, pare de tomar CRESTOR e contacte o seu médico imediatamente. Se você não planeja engravidar, você deve usar métodos contraceptivos eficazes (contracepção) enquanto estiver tomando CRESTOR.
- estão amamentando. Medicamentos como CRESTOR 5mg podem passar para o leite materno e podem prejudicar seu bebê.
O que devo dizer ao meu médico antes e enquanto estiver tomando CRESTOR?
Informe o seu médico se você:
- tem dores musculares inexplicáveis ou fraqueza
- tem ou teve problemas renais
- tem ou teve problemas de fígado
- beber mais de 2 copos de álcool por dia
- tem problemas de tireóide
- tem 65 anos ou mais
- são de ascendência asiática
- está grávida ou pensa que pode estar grávida, ou está planejando engravidar
- está amamentando
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos e de venda livre, vitaminas e suplementos de ervas.
Fale com o seu médico antes de começar a tomar novos medicamentos.
Tomar CRESTOR 20mg com alguns outros medicamentos podem afetar uns aos outros causando efeitos colaterais. CRESTOR pode afetar a forma como outros medicamentos atuam e outros medicamentos podem afetar a forma como CRESTOR atua.
Informe especialmente o seu médico se estiver a tomar:
- ciclosporina (um medicamento para o seu sistema imunológico)
- gemfibrozil (um medicamento de ácido fíbrico para baixar o colesterol)
- medicamentos antivirais, incluindo inibidores da protease do HIV ou da hepatite C (como lopinavir, ritonavir, fosamprenavir, tipranavir, atazanavir ou simeprevir)
- certos medicamentos antifúngicos (como itraconazol, cetoconazol e fluconazol)
- anticoagulantes cumarínicos (medicamentos que previnem coágulos sanguíneos, como a varfarina)
- niacina ou ácido nicotínico
- derivados de ácido fíbrico (como fenofibrato)
- colchicina (um medicamento usado para tratar a gota)
Peça ao seu médico ou farmacêutico uma lista destes medicamentos se não tiver a certeza.
Conheça todos os medicamentos que toma. Mantenha uma lista deles para mostrar ao seu médico e farmacêutico quando receber um novo medicamento.
Como devo tomar CRESTOR 10mg?
- Tome CRESTOR exatamente como seu médico lhe disse para tomá-lo.
- Tome CRESTOR, por via oral, 1 vez por dia. Engula o comprimido inteiro.
- CRESTOR pode ser tomado a qualquer hora do dia, com ou sem alimentos.
- Não faça altere a sua dose ou pare de CRESTOR 10mg sem falar com o seu médico, mesmo que se sinta bem.
- O seu médico pode fazer análises ao sangue para verificar os seus níveis de colesterol antes e durante o tratamento com CRESTOR. O seu médico pode alterar a sua dose de CRESTOR 10 mg, se necessário.
- O seu médico pode iniciar uma dieta para baixar o colesterol antes de lhe dar CRESTOR. Mantenha-se nesta dieta quando tomar CRESTOR.
- Espere pelo menos 2 horas após tomar CRESTOR para tomar um antiácido que contenha uma combinação de alumínio e hidróxido de magnésio.
- Se você esquecer de uma dose de CRESTOR 10mg, tome-a assim que se lembrar. No entanto, não tome 2 doses de CRESTOR 10mg dentro de 12 horas uma da outra.
- Se você tomar muito CRESTOR 20mg ou overdose, ligue para o seu médico ou dirija-se ao pronto-socorro do hospital mais próximo imediatamente.
Quais são os possíveis efeitos colaterais do CRESTOR 20mg?
CRESTOR 10mg pode causar efeitos colaterais graves, incluindo:
- Dor muscular, sensibilidade e fraqueza (miopatia). Problemas musculares, incluindo ruptura muscular, podem ser graves em algumas pessoas e raramente causam danos nos rins que podem levar à morte. Informe o seu médico imediatamente se:
- você tem dor muscular inexplicável, sensibilidade ou fraqueza, especialmente se tiver febre ou se sentir mais cansado do que o habitual, enquanto estiver tomando CRESTOR.
- tem problemas musculares que não desaparecem mesmo depois de o seu médico lhe ter dito para parar de tomar CRESTOR. Seu médico pode fazer mais testes para diagnosticar a causa de seus problemas musculares.
Suas chances de ter problemas musculares são maiores se você:
- está a tomar alguns outros medicamentos enquanto toma CRESTOR
- tem 65 anos ou mais
- tem problemas de tireóide (hipotireoidismo) que não são controlados
- tem problemas renais
- estão tomando doses mais altas de CRESTOR
- Problemas de fígado. O seu médico deve fazer análises ao sangue para verificar o seu fígado antes de começar a tomar CRESTOR 5 mg e se tiver sintomas de problemas hepáticos enquanto toma CRESTOR. Ligue para o seu médico imediatamente se tiver algum dos seguintes sintomas de problemas no fígado:
- sentir-se extraordinariamente cansado ou fraco
- perda de apetite
- dor de barriga superior
- urina escura
- amarelecimento da pele ou do branco dos olhos
Os efeitos colaterais mais comuns podem incluir: dor de cabeça, dores musculares e dores, dor abdominal, fraqueza e náuseas.
Efeitos colaterais adicionais que foram relatados com CRESTOR incluem perda de memória e confusão.
Informe o seu médico se tiver algum efeito secundário que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do CRESTOR. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar CRESTOR 20mg?
- Armazenar CRESTOR 10mg em temperatura ambiente, entre 20°C e 25°C (68°F a 77°F) e em local seco.
- Jogue fora com segurança os medicamentos que estão desatualizados ou não são mais necessários.
Mantenha CRESTOR 10mg e todos os medicamentos fora do alcance das crianças.
Quais são os ingredientes do CRESTOR?
Ingrediente ativo: rosuvastatina como rosuvastatina cálcica
Ingredientes inativos: celulose microcristalina NF, lactose monohidratada NF, fosfato de cálcio tribásico NF, crospovidona NF, estearato de magnésio NF, hipromelose NF, triacetina NF, dióxido de titânio USP, óxido férrico amarelo e óxido férrico vermelho NF.
Informações gerais sobre o uso seguro e eficaz de CRESTOR
Os medicamentos às vezes são prescritos para outros fins que não os listados em um folheto de informações ao paciente. Não use CRESTOR 10mg para uma condição para a qual não foi prescrito. Não dê CRESTOR 20mg a outras pessoas, mesmo que tenham a mesma condição médica que você. Pode prejudicá-los.
Você pode pedir ao seu farmacêutico ou médico informações sobre CRESTOR 5mg que são escritas para profissionais de saúde.
Esta informação do paciente foi aprovada pela Food and Drug Administration dos EUA, revisada em 9/2018
