Zetia 10mg Ezetimibe Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Zetia e como é usado?
Zetia é um medicamento de prescrição usado para tratar os sintomas de colesterol alto e reduzir o colesterol. Zetia pode ser usado sozinho ou com outros medicamentos.
Zetia pertence a uma classe de medicamentos chamados Agentes Redutores de Lipídios, 2-Azetidinonas.
Não se sabe se Zetia 10mg é seguro e eficaz em crianças com menos de 10 anos de idade.
Quais são os possíveis efeitos colaterais do Zetia?
Zetia pode causar efeitos colaterais graves, incluindo:
- dor muscular,
- sensibilidade ou fraqueza muscular,
- febre,
- cansaço incomum e
- urina de cor escura
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Zetia 10mg incluem:
- dores musculares ou articulares,
- nariz entupido,
- Sinusite,
- dor de garganta,
- diarreia, e
- dor em um braço ou perna
Informe o seu médico se tiver algum efeito secundário que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Zetia. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
ZETIA (ezetimiba) está em uma classe de compostos hipolipemiantes que inibe seletivamente a absorção intestinal de colesterol e fitoesteróis relacionados. O nome químico da ezetimiba é 1-(4-fluorofenil)-3(R)-[3-(4-fluorofenil)-3(S)-hidroxipropil]-4(S)-(4-hidroxifenil)-2-azetidinona . A fórmula empírica é C24H21F2NO3. Seu peso molecular é 409,4 e sua fórmula estrutural é:
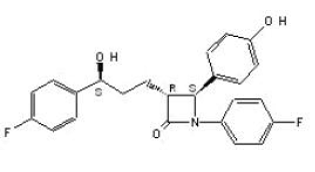
ezetimiba é um pó branco e cristalino que é livremente a muito solúvel em etanol, metanol e acetona e praticamente insolúvel em água. A ezetimiba tem um ponto de fusão de cerca de 163°C e é estável à temperatura ambiente. ZETIA 10mg está disponível na forma de comprimido para administração oral contendo 10 mg de ezetimiba e os seguintes ingredientes inativos: croscarmelose sódica NF, lactose monohidratada NF, estearato de magnésio NF, celulose microcristalina NF, povidona USP e lauril sulfato de sódio NF.
INDICAÇÕES
A terapia com agentes que alteram os lipídios deve ser apenas um componente da intervenção de múltiplos fatores de risco em indivíduos com risco significativamente aumentado de doença vascular aterosclerótica devido à hipercolesterolemia. A terapia medicamentosa é indicada como adjuvante da dieta quando a resposta a uma dieta restrita em gordura saturada e colesterol e outras medidas não farmacológicas isoladas for inadequada.
Hiperlipidemia primária
Monoterapia
ZETIA®, administrado isoladamente, é indicado como terapia adjuvante à dieta para a redução de colesterol total elevado (C total), colesterol de lipoproteína de baixa densidade (LDL-C), apolipoproteína B (Apo B) e colesterol de lipoproteína não de alta densidade (não-HDL-C) em pacientes com hiperlipidemia primária (familiar heterozigótica e não familiar).
Terapia de Combinação com Inibidores da HMG-CoA Redutase (Estatinas)
ZETIA 10mg, administrado em combinação com um inibidor da 3-hidroxi-3-metilglutaril-coenzima A (HMG-CoA) redutase (estatina), é indicado como terapia adjuvante à dieta para a redução dos níveis elevados de C total, LDL-C, Apo B e não-HDL-C em pacientes com hiperlipidemia primária (familiar heterozigótica e não familiar).
Terapia combinada com fenofibrato
ZETIA 10mg, administrado em combinação com fenofibrato, é indicado como terapia adjuvante à dieta para a redução de níveis elevados de C-total, C-LDL, Apo B e C-não-HDL em pacientes adultos com hiperlipidemia mista.
Hipercolesterolemia Familiar Homozigótica (HoFH)
A combinação de ZETIA 10mg e atorvastatina ou sinvastatina é indicada para a redução dos níveis elevados de C-total e C-LDL em pacientes com HFHo, como adjuvante a outros tratamentos hipolipemiantes (por exemplo, aférese de LDL) ou se tais tratamentos não estiverem disponíveis .
Sitosterolemia Homozigótica
ZETIA 10mg é indicado como terapia adjuvante à dieta para a redução dos níveis elevados de sitosterol e campesterol em pacientes com sitosterolemia familiar homozigótica.
Limitações de uso
O efeito de ZETIA na morbidade e mortalidade cardiovascular não foi determinado.
ZETIA não foi estudado nas dislipidemias Fredrickson Tipo I, III, IV e V.
DOSAGEM E ADMINISTRAÇÃO
Informações gerais de dosagem
A dose recomendada de ZETIA é de 10 mg uma vez ao dia.
ZETIA 10mg pode ser administrado com ou sem alimentos.
Terapia concomitante de hipolipemiantes
ZETIA 10mg pode ser administrado com uma estatina (em pacientes com hiperlipidemia primária) ou com fenofibrato (em pacientes com hiperlipidemia mista) para efeito incremental. Por conveniência, a dose diária de ZETIA pode ser tomada ao mesmo tempo que a estatina ou o fenofibrato, de acordo com as recomendações posológicas dos respectivos medicamentos.
Coadminis com sequestrantes de ácidos biliares
A dosagem de ZETIA deve ocorrer ≥2 horas antes ou ≥4 horas após a administração de um sequestrante de ácido biliar [ver INTERAÇÕES MEDICAMENTOSAS ].
Pacientes com Insuficiência Hepática
Não é necessário ajuste de dose em pacientes com insuficiência hepática leve [ver AVISOS E PRECAUÇÕES ].
Pacientes com Insuficiência Renal
Não é necessário ajuste de dose em pacientes com insuficiência renal [ver FARMACOLOGIA CLÍNICA ]. Quando administrado com sinvastatina em pacientes com insuficiência renal moderada a grave (taxa de filtração glomerular estimada Uso em populações específicas ].
Pacientes Geriátricos
Nenhum ajuste de dose é necessário em pacientes geriátricos [ver FARMACOLOGIA CLÍNICA ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
Os comprimidos de 10 mg são comprimidos brancos a esbranquiçados, em forma de cápsula, gravados com “414” numa das faces.
Armazenamento e manuseio
Nº 3861 - Comprimidos ZETIA, 10 mg , são comprimidos brancos a esbranquiçados, em forma de cápsula, com a gravação “414” numa das faces. Eles são fornecidos da seguinte forma:
NDC 66582-414-31 garrafas de 30 NDC 66582-414-54 garrafas de 90 NDC 66582-414-74 garrafas de 500 NDC 66582-414-76 garrafas de 5000 NDC 66582-414-28 embalagens de dose unitária de 100.
Armazenar
Armazenar a 25°C (77°F); excursões permitidas a 15-30°C (59-86°F). [Ver Temperatura ambiente controlada USP .] Proteger da umidade.
Merck Sharp & Dohme Corp., uma subsidiária da MERCK & CO., INC., Whitehouse Station, NJ 08889, EUA. Revisado: agosto de 2013
EFEITOS COLATERAIS
As seguintes reações adversas graves são discutidas em mais detalhes em outras seções do rótulo:
- Anormalidades das enzimas hepáticas [ver AVISOS E PRECAUÇÕES ]
- Rabdomiólise e miopatia [ver AVISOS E PRECAUÇÕES ]
Estudos de monoterapia
No banco de dados de ensaios clínicos controlados com ZETIA 10mg (controlado por placebo) de 2.396 pacientes com duração mediana de tratamento de 12 semanas (intervalo de 0 a 39 semanas), 3,3% dos pacientes com ZETIA 10mg e 2,9% dos pacientes com placebo descontinuaram devido a efeitos adversos reações. As reações adversas mais comuns no grupo de pacientes tratados com ZETIA 10mg que levaram à descontinuação do tratamento e ocorreram em uma taxa maior que o placebo foram:
- Artralgia (0,3%)
- Tonturas (0,2%)
- Gama-glutamiltransferase aumentada (0,2%)
As reações adversas mais comumente relatadas (incidência ≥2% e maior que placebo) no banco de dados de ensaios clínicos controlados por monoterapia com ZETIA de 2.396 pacientes foram: infecção do trato respiratório superior (4,3%), diarreia (4,1%), artralgia (3,0%), sinusite (2,8%) e dor nas extremidades (2,7%).
Estudos de Coadministração de Estatinas
No banco de dados de ensaios clínicos controlados com ZETIA + estatina de 11.308 pacientes com duração mediana de tratamento de 8 semanas (intervalo de 0 a 112 semanas), 4,0% dos pacientes em uso de ZETIA + estatina e 3,3% dos pacientes em tratamento isolado com estatina descontinuaram devido a reações adversas. As reações adversas mais comuns no grupo de pacientes tratados com ZETIA + estatina que levaram à descontinuação do tratamento e ocorreram em uma taxa maior do que a estatina isolada foram:
- Alanina aminotransferase aumentada (0,6%)
- Mialgia (0,5%)
- Fadiga, aumento da aspartato aminotransferase, dor de cabeça e dor nas extremidades (cada a 0,2%)
As reações adversas mais comumente relatadas (incidência ≥2% e maior do que a estatina isolada) no banco de dados de ensaios clínicos controlados com ZETIA + estatina de 11.308 pacientes foram: nasofaringite (3,7%), mialgia (3,2%), infecção do trato respiratório superior (2,9% ), artralgia (2,6%) e diarreia (2,5%).
Experiência de Ensaios Clínicos
Como os estudos clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos estudos clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos estudos clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
Monoterapia
Em 10 ensaios clínicos duplo-cegos, controlados por placebo, 2.396 pacientes com hiperlipidemia primária (faixa etária 9-86 anos, 50% mulheres, 90% caucasianos, 5% negros, 3% hispânicos, 2% asiáticos) e LDL-C elevado foram tratados com ZETIA 10 mg/dia por uma duração média de tratamento de 12 semanas (intervalo de 0 a 39 semanas).
As reações adversas relatadas em ≥2% dos pacientes tratados com ZETIA e com incidência maior do que placebo em estudos controlados por placebo de ZETIA 10mg, independentemente da avaliação de causalidade, são mostradas na Tabela 1.
TABELA 1: Reações Adversas Clínicas Ocorrendo em ≥2% dos Pacientes Tratados com ZETIA 10mg e com Incidência Maior que o Placebo, Independentemente da Causalidade
frequência de reações adversas menos comuns foi comparável entre ZETIA 10mg e placebo.
Combinação com uma estatina
Em 28 ensaios clínicos duplo-cegos, controlados (com placebo ou com controle ativo), 11.308 pacientes com hiperlipidemia primária (faixa etária 10-93 anos, 48% mulheres, 85% caucasianos, 7% negros, 4% hispânicos, 3% asiáticos) e LDL-C elevado foram tratados com ZETIA 10 mg/dia concomitantemente ou adicionados à terapia com estatina em andamento por uma duração média de tratamento de 8 semanas (intervalo de 0 a 112 semanas).
A incidência de transaminases consecutivas aumentadas (≥3 × ULN) foi maior em pacientes que receberam ZETIA 10mg administrado com estatinas (1,3%) do que em pacientes tratados apenas com estatinas (0,4%). [Ver AVISOS E PRECAUÇÕES ]
As reações adversas clínicas relatadas em ≥2% dos pacientes tratados com ZETIA + estatina e com incidência maior que estatina, independentemente da avaliação de causalidade, são mostradas na Tabela 2.
TABELA 2: Reações Adversas Clínicas Ocorrendo em ≥2% dos Pacientes Tratados com ZETIA 10mg Coadministrado com Estatina e com Incidência Maior que Estatina, Independentemente da Causalidade
Combinação com Fenofibrato
Este estudo clínico envolvendo 625 pacientes com dislipidemia mista (faixa etária 20-76 anos, 44% mulheres, 79% caucasianos, 0,1% negros, 11% hispânicos, 5% asiáticos) tratados por até 12 semanas e 576 pacientes tratados por até um adicional de 48 semanas avaliou a coadministração de ZETIA e fenofibrato. Este estudo não foi desenhado para comparar grupos de tratamento para eventos infrequentes. As taxas de incidência (IC de 95%) para elevações clinicamente importantes (≥3 — LSN, consecutivas) nos níveis de transaminase hepática foram 4,5% (1,9, 8,8) e 2,7% (1,2, 5,4) para monoterapia com fenofibrato (n=188) e ZETIA coadministrado com fenofibrato (n=183), respectivamente, ajustado para exposição ao tratamento. As taxas de incidência correspondentes para colecistectomia foram 0,6% (IC 95%: 0,0%, 3,1%) e 1,7% (IC 95%: 0,6%, 4,0%) para monoterapia com fenofibrato e ZETIA 10mg coadministrado com fenofibrato, respectivamente [ver INTERAÇÕES MEDICAMENTOSAS ]. O número de pacientes expostos à terapia de coadministração, bem como à monoterapia com fenofibrato e ezetimiba, foi inadequado para avaliar o risco de doença da vesícula biliar. Não houve elevações de CPK > 10 — LSN em nenhum dos grupos de tratamento.
Experiência pós-marketing
Como as reações abaixo são relatadas voluntariamente por uma população de tamanho incerto, geralmente não é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
As seguintes reações adversas adicionais foram identificadas durante o uso pós-aprovação de ZETIA:
Reações de hipersensibilidade, incluindo anafilaxia, angioedema, erupção cutânea e urticária; eritema multiforme; artralgia; mialgia; creatina fosfoquinase elevada; miopatia/rabdomiólise [ver AVISOS E PRECAUÇÕES ]; elevações nas transaminases hepáticas; hepatite; dor abdominal; trombocitopenia; pancreatite; náusea; tontura; parestesia; depressão; dor de cabeça; colelitíase; colecistite.
INTERAÇÕES MEDICAMENTOSAS
[Ver FARMACOLOGIA CLÍNICA ]
Ciclosporina
Deve-se ter cautela ao usar ZETIA 10mg e ciclosporina concomitantemente devido ao aumento da exposição tanto à ezetimiba quanto à ciclosporina. As concentrações de ciclosporina devem ser monitoradas em pacientes recebendo ZETIA e ciclosporina.
O grau de aumento da exposição à ezetimiba pode ser maior em pacientes com insuficiência renal grave. Em pacientes tratados com ciclosporina, os efeitos potenciais do aumento da exposição à ezetimiba pelo uso concomitante devem ser cuidadosamente ponderados em relação aos benefícios das alterações nos níveis lipídicos fornecidos pela ezetimiba.
Fibratos
A eficácia e segurança da coadministração de ezetimiba com fibratos que não o fenofibrato não foram estudadas.
Os fibratos podem aumentar a excreção de colesterol na bile, levando à colelitíase. Em um estudo pré-clínico em cães, a ezetimiba aumentou o colesterol na bile da vesícula biliar [ver Toxicologia não clínica ]. A coadministração de ZETIA com fibratos que não o fenofibrato não é recomendada até que o uso em pacientes seja adequadamente estudado.
Fenofibrato
Se houver suspeita de colelitíase em um paciente recebendo ZETIA 10mg e fenofibrato, estudos da vesícula biliar são indicados e terapia hipolipemiante alternativa deve ser considerada [ver REAÇÕES ADVERSAS e a rotulagem do produto para fenofibrato].
Colestiramina
A administração concomitante de colestiramina diminuiu a área média sob a curva (AUC) da ezetimiba total em aproximadamente 55%. A redução incremental do LDL-C devido à adição de ezetimiba à colestiramina pode ser reduzida por essa interação.
Anticoagulantes cumarínicos
Se a ezetimiba for adicionada à varfarina, um anticoagulante cumarínico, a Razão Normalizada Internacional (INR) deve ser monitorada adequadamente.
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Uso com estatinas ou fenofibrato
A administração concomitante de ZETIA com uma estatina específica ou fenofibrato deve estar de acordo com a bula do medicamento.
Enzimas do Fígado
Em estudos clínicos controlados de monoterapia, a incidência de elevações consecutivas (≥3 x o limite superior do normal [LSN]) nos níveis de transaminase hepática foi semelhante entre ZETIA (0,5%) e placebo (0,3%).
Em estudos clínicos controlados de combinação de ZETIA 10mg iniciados concomitantemente com uma estatina, a incidência de elevações consecutivas (≥3 x LSN) nos níveis de transaminase hepática foi de 1,3% para pacientes tratados com ZETIA administrado com estatinas e 0,4% para pacientes tratados apenas com estatinas. Essas elevações nas transaminases foram geralmente assintomáticas, não associadas à colestase e retornaram à linha de base após a descontinuação da terapia ou com a continuação do tratamento. Quando ZETIA é coadministrado com uma estatina, testes hepáticos devem ser realizados no início da terapia e de acordo com as recomendações da estatina. Se persistir um aumento de ALT ou AST ≥3 x LSN, considerar a retirada de ZETIA 10mg e/ou da estatina.
Miopatia/Rabdomiólise
Em ensaios clínicos, não houve excesso de miopatia ou rabdomiólise associada a ZETIA 10mg em comparação com o braço de controle relevante (somente placebo ou estatina). No entanto, miopatia e rabdomiólise são reações adversas conhecidas às estatinas e outros medicamentos hipolipemiantes. Em ensaios clínicos, a incidência de creatina fosfoquinase (CPK) > 10 x LSN foi de 0,2% para ZETIA versus 0,1% para placebo e 0,1% para ZETIA coadministrado com uma estatina versus 0,4% para estatinas isoladas. O risco de toxicidade do músculo esquelético aumenta com doses mais altas de estatina, idade avançada (> 65), hipotireoidismo, insuficiência renal e, dependendo da estatina usada, uso concomitante de outros medicamentos.
Na experiência pós-comercialização com ZETIA, foram relatados casos de miopatia e rabdomiólise. A maioria dos pacientes que desenvolveram rabdomiólise estava tomando estatina antes de iniciar ZETIA. No entanto, foi notificada rabdomiólise com ZETIA 10 mg em monoterapia e com a adição de ZETIA 10 mg a agentes que se sabe estarem associados a um risco aumentado de rabdomiólise, tais como fibratos. ZETIA e qualquer estatina ou fibrato que o paciente esteja tomando concomitantemente deve ser imediatamente descontinuado se for diagnosticada ou suspeitar de miopatia. A presença de sintomas musculares e um nível de CPK > 10 x LSN indica miopatia.
Insuficiência hepática
Devido aos efeitos desconhecidos do aumento da exposição à ezetimiba em pacientes com insuficiência hepática moderada a grave, ZETIA não é recomendado para esses pacientes. [Ver FARMACOLOGIA CLÍNICA ]
Informações de Aconselhamento do Paciente
Ver Rotulagem do paciente aprovada pela FDA (INFORMAÇÕES DO PACIENTE).
Os pacientes devem ser aconselhados a aderir à dieta recomendada pelo National Cholesterol Education Program (NCEP), um programa regular de exercícios e testes periódicos de um painel lipídico em jejum.
Dor muscular
Todos os pacientes que iniciam a terapia com ezetimiba devem ser alertados sobre o risco de miopatia e instruídos a relatar imediatamente qualquer dor, sensibilidade ou fraqueza muscular inexplicáveis. O risco de isso ocorrer é aumentado ao tomar certos tipos de medicamentos. Os pacientes devem discutir todos os medicamentos, tanto prescritos quanto de venda livre, com seu médico.
Enzimas do Fígado
Testes hepáticos devem ser realizados quando ZETIA 10mg é adicionado à terapia com estatina e de acordo com as recomendações de estatina.
Gravidez
As mulheres em idade fértil devem ser aconselhadas a usar um método anticoncepcional eficaz para prevenir a gravidez durante o uso de ZETIA adicionado à terapia com estatinas. Discuta planos futuros de gravidez com seus pacientes e discuta quando interromper a terapia combinada com ZETIA 10mg e estatina se eles estiverem tentando engravidar. As pacientes devem ser avisadas de que, se engravidarem, devem parar de tomar a terapia combinada de ZETIA 10mg e estatinas e ligar para seu profissional de saúde.
Amamentação
As mulheres que estão amamentando devem ser aconselhadas a não usar ZETIA adicionado à terapia com estatinas. Pacientes que têm um distúrbio lipídico e estão amamentando devem ser aconselhadas a discutir as opções com seus profissionais de saúde.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Um estudo de carcinogenicidade dietética de 104 semanas com ezetimiba foi realizado em ratos em doses de até 1500 mg/kg/dia (machos) e 500 mg/kg/dia (fêmeas) (~20 x a exposição humana a 10 mg por dia com base na AUC0 -24h para ezetimiba total). Um estudo de carcinogenicidade dietética de 104 semanas com ezetimiba também foi realizado em camundongos em doses de até 500 mg/kg/dia (> 150 x a exposição humana em 10 mg diários com base na AUC0-24h para ezetimiba total). Não houve aumentos estatisticamente significativos na incidência de tumores em ratos ou camundongos tratados com drogas.
Nenhuma evidência de mutagenicidade foi observada in vitro em um teste de mutagenicidade microbiana (Ames) com Salmonella typhimurium e Escherichia coli com ou sem ativação metabólica. Nenhuma evidência de clastogenicidade foi observada in vitro em um ensaio de aberração cromossômica em linfócitos de sangue periférico humano com ou sem ativação metabólica. Além disso, não houve evidência de genotoxicidade no teste de micronúcleo em camundongos in vivo.
Em estudos de fertilidade oral (gavage) de ezetimiba realizados em ratos, não houve evidência de toxicidade reprodutiva em doses de até 1000 mg/kg/dia em ratos machos ou fêmeas (~7 x a exposição humana a 10 mg diariamente com base na AUC0- 24h para ezetimiba total).
Uso em populações específicas
Gravidez
Gravidez Categoria C
Não existem estudos adequados e bem controlados de ezetimiba em mulheres grávidas. A ezetimiba deve ser usada durante a gravidez somente se o benefício potencial justificar o risco para o feto.
Em estudos orais (gavagem) de desenvolvimento embriofetal de ezetimiba realizados em ratos e coelhos durante a organogênese, não houve evidência de efeitos embrioletais nas doses testadas (250, 500, 1000 mg/kg/dia). Em ratos, foram observadas incidências aumentadas de achados esqueléticos fetais comuns (par extra de costelas torácicas, centros vertebrais cervicais não ossificados, costelas encurtadas) com 1000 mg/kg/dia (~10 x a exposição humana a 10 mg diariamente com base na AUC0-24h para ezetimiba total). Em coelhos tratados com ezetimiba, observou-se um aumento da incidência de costelas extratorácicas na dose de 1.000 mg/kg/dia (150 x a exposição humana a 10 mg por dia com base na AUC0-24h para a ezetimiba total). A ezetimiba atravessou a placenta quando ratas e coelhas grávidas receberam doses orais múltiplas.
Estudos de dose múltipla de ezetimiba administrados em combinação com estatinas em ratos e coelhos durante a organogênese resultam em maiores exposições à ezetimiba e às estatinas. Os achados reprodutivos ocorrem em doses mais baixas na terapia combinada em comparação com a monoterapia.
Todas as estatinas são contraindicadas em gestantes e lactantes. Quando ZETIA 10mg é administrado com uma estatina em uma mulher com potencial para engravidar, consulte a categoria de gravidez e a rotulagem do produto para a estatina. [Ver CONTRA-INDICAÇÕES]
Mães que amamentam
Não se sabe se a ezetimiba é excretada no leite materno humano. Em estudos com ratos, a exposição à ezetimiba total em filhotes em amamentação foi até metade da observada no plasma materno. Como muitos medicamentos são excretados no leite humano, deve-se ter cautela quando ZETIA 10mg é administrado a lactantes. ZETIA não deve ser usado em lactantes, a menos que o benefício potencial justifique o risco potencial para o bebê.
Uso Pediátrico
Os efeitos de ZETIA coadministrado com sinvastatina (n=126) em comparação com a monoterapia com sinvastatina (n=122) foram avaliados em meninos e meninas adolescentes com hipercolesterolemia familiar heterozigótica (HeFH). Em um estudo multicêntrico, duplo-cego, controlado seguido por uma fase aberta, 142 meninos e 106 meninas pós-menarca, 10 a 17 anos de idade (idade média de 14,2 anos, 43% mulheres, 82% caucasianos, 4% asiáticos, 2% negros , 13% multirracial) com HeFH foram randomizados para receber ZETIA 10mg coadministrado com sinvastatina ou monoterapia com sinvastatina. A inclusão no estudo exigiu 1) um nível basal de LDL-C entre 160 e 400 mg/dL e 2) uma história médica e apresentação clínica consistentes com HeFH. O valor médio basal de LDL-C foi de 225 mg/dL (intervalo: 161-351 mg/dL) no grupo ZETIA 10 mg coadministrado com sinvastatina em comparação com 219 mg/dL (intervalo: 149-336 mg/dL) na monoterapia com sinvastatina grupo. Os pacientes receberam concomitantemente ZETIA e sinvastatina (10 mg, 20 mg ou 40 mg) ou monoterapia com sinvastatina (10 mg, 20 mg ou 40 mg) por 6 semanas, ZETIA coadministrado e 40 mg de sinvastatina ou 40 mg de sinvastatina em monoterapia por nas 27 semanas seguintes, e coadministrado de forma aberta com ZETIA e sinvastatina (10 mg, 20 mg ou 40 mg) por 20 semanas depois.
Os resultados do estudo na Semana 6 estão resumidos na Tabela 3. Os resultados na Semana 33 foram consistentes com os da Semana 6.
TABELA 3: Diferença Percentual Média na Semana 6 entre o Grupo ZETIA 10mg Agrupado Coadministrado com Sinvastatina e o Grupo de Monoterapia Agrupado com Sinvastatina em Pacientes Adolescentes com Hipercolesterolemia Familiar Heterozigótica
Desde o início do estudo até o final da Semana 33, descontinuações devido a uma reação adversa ocorreram em 7 (6%) pacientes no grupo de ZETIA coadministrado com sinvastatina e em 2 (2%) pacientes no grupo de monoterapia com sinvastatina.
Durante o estudo, ocorreram elevações das transaminases hepáticas (duas medições consecutivas de ALT e/ou AST ≥3 x LSN) em quatro (3%) indivíduos no grupo ZETIA 10mg coadministrado com sinvastatina e em dois (2%) indivíduos no grupo de monoterapia com sinvastatina grupo. Elevações de CPK (≥10 x LSN) ocorreram em dois (2%) indivíduos no grupo ZETIA coadministrado com sinvastatina e em zero indivíduos no grupo de monoterapia com sinvastatina.
Neste estudo controlado limitado, não houve efeito significativo no crescimento ou maturação sexual em meninos ou meninas adolescentes, ou na duração do ciclo menstrual em meninas.
A coadministração de ZETIA 10mg com sinvastatina em doses superiores a 40mg/dia não foi estudada em adolescentes. Além disso, ZETIA 10mg não foi estudado em pacientes com menos de 10 anos de idade ou em meninas pré-menarca.
Com base na ezetimiba total (ezetimiba + ezetimiba-glicuronídeo), não há diferenças farmacocinéticas entre adolescentes e adultos. Os dados farmacocinéticos na população pediátrica
Uso Geriátrico
Estudos de monoterapia
Dos 2.396 pacientes que receberam ZETIA 10mg em estudos clínicos, 669 (28%) tinham 65 anos ou mais e 111 (5%) tinham 75 anos ou mais.
Estudos de Coadministração de Estatinas
Dos 11.308 pacientes que receberam ZETIA + estatina em estudos clínicos, 3.587 (32%) tinham 65 anos ou mais e 924 (8%) tinham 75 anos ou mais.
Não foram observadas diferenças gerais na segurança e eficácia entre esses pacientes e pacientes mais jovens, e outras experiências clínicas relatadas não identificaram diferenças nas respostas entre pacientes idosos e pacientes mais jovens, mas a maior sensibilidade de alguns indivíduos mais velhos não pode ser descartada [ver FARMACOLOGIA CLÍNICA ].
Insuficiência renal
Quando usado como monoterapia, não é necessário ajuste de dose de ZETIA 10mg.
No estudo Study of Heart and Renal Protection (SHARP) de 9.270 pacientes com insuficiência renal moderada a grave (6.247 pacientes sem diálise com creatinina sérica mediana de 2,5 mg/dL e taxa de filtração glomerular estimada mediana de 25,6 mL/min/1,73 m², e 3.023 pacientes em diálise), a incidência de eventos adversos graves, eventos adversos que levaram à descontinuação do tratamento do estudo ou eventos adversos de interesse especial (eventos adversos musculoesqueléticos, anormalidades das enzimas hepáticas, câncer incidente) foi semelhante entre os pacientes já atribuídos a ezetimiba 10 mg mais sinvastatina 20 mg (n=4650) ou placebo (n=4620) durante um seguimento médio de 4,9 anos. No entanto, como a insuficiência renal é um fator de risco para miopatia associada às estatinas, doses de sinvastatina superiores a 20 mg devem ser usadas com cautela e monitoramento cuidadoso quando administradas concomitantemente com ZETIA em pacientes com insuficiência renal moderada a grave.
Insuficiência hepática
ZETIA não é recomendado em pacientes com insuficiência hepática moderada a grave [ver AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
ZETIA 10mg administrado concomitantemente com uma estatina é contraindicado em pacientes com doença hepática ativa ou elevações persistentes inexplicáveis dos níveis de transaminase hepática [ver CONTRA-INDICAÇÕES ; AVISOS E PRECAUÇÕES e FARMACOLOGIA CLÍNICA ].
SOBREDOSAGEM
Em estudos clínicos, a administração de ezetimiba, 50 mg/dia a 15 indivíduos saudáveis por até 14 dias, 40 mg/dia a 18 pacientes com hiperlipidemia primária por até 56 dias e 40 mg/dia a 27 pacientes com sitosterolemia homozigótica por 26 semanas foi geralmente bem tolerada. Uma paciente do sexo feminino com sitosterolemia homozigótica tomou uma overdose acidental de ezetimiba 120 mg/dia por 28 dias sem eventos adversos clínicos ou laboratoriais relatados.
Em caso de sobredosagem, devem ser utilizadas medidas sintomáticas e de suporte.
CONTRA-INDICAÇÕES
ZETIA é contraindicado nas seguintes condições:
- A combinação de ZETIA 10mg com uma estatina é contraindicada em pacientes com doença hepática ativa ou elevações persistentes inexplicáveis nos níveis de transaminases hepáticas.
- Mulheres grávidas ou que possam engravidar. Como as estatinas diminuem a síntese de colesterol e possivelmente a síntese de outras substâncias biologicamente ativas derivadas do colesterol, ZETIA em combinação com uma estatina pode causar dano fetal quando administrado a mulheres grávidas. Além disso, não há benefício aparente da terapia durante a gravidez e a segurança em mulheres grávidas não foi estabelecida. Se a paciente engravidar enquanto estiver tomando este medicamento, a paciente deve ser informada do risco potencial para o feto e da falta de benefício clínico conhecido com o uso continuado durante a gravidez. [Ver Uso em populações específicas ]
- Mães que amamentam. Como as estatinas podem passar para o leite materno e como as estatinas têm o potencial de causar reações adversas graves em lactentes, as mulheres que necessitam de tratamento com ZETIA em combinação com uma estatina devem ser aconselhadas a não amamentar seus bebês [ver Uso em populações específicas ].
- Pacientes com hipersensibilidade conhecida a qualquer componente deste produto. Reações de hipersensibilidade incluindo anafilaxia, angioedema, erupção cutânea e urticária foram relatadas com ZETIA [ver REAÇÕES ADVERSAS ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
A ezetimiba reduz o colesterol no sangue ao inibir a absorção do colesterol pelo intestino delgado. Em um estudo clínico de 2 semanas em 18 pacientes hipercolesterolêmicos, ZETIA 10mg inibiu a absorção intestinal de colesterol em 54%, em comparação com placebo. ZETIA não teve efeito clinicamente significativo nas concentrações plasmáticas das vitaminas lipossolúveis A, D e E (em um estudo de 113 pacientes), e não prejudicou a produção de hormônios esteróides adrenocorticais (em um estudo de 118 pacientes).
conteúdo de colesterol do fígado é derivado predominantemente de três fontes. O fígado pode sintetizar colesterol, retirar colesterol do sangue das lipoproteínas circulantes ou absorver o colesterol absorvido pelo intestino delgado. O colesterol intestinal é derivado principalmente do colesterol secretado na bile e do colesterol da dieta.
A ezetimiba tem um mecanismo de ação diferente de outras classes de compostos redutores de colesterol (estatinas, sequestrantes de ácidos biliares [resinas], derivados de ácido fíbrico e estanóis vegetais). O alvo molecular da ezetimiba demonstrou ser o transportador de esterol, Niemann-Pick C1-Like 1 (NPC1L1), que está envolvido na captação intestinal de colesterol e fitoesteróis.
ezetimiba não inibe a síntese de colesterol no fígado nem aumenta a excreção de ácidos biliares. Em vez disso, a ezetimiba localiza-se na borda em escova do intestino delgado e inibe a absorção de colesterol, levando a uma diminuição na entrega de colesterol intestinal ao fígado. Isso causa uma redução dos estoques de colesterol hepático e um aumento na depuração do colesterol do sangue; este mecanismo distinto é complementar ao das estatinas e do fenofibrato [ver Estudos clínicos ].
Farmacodinâmica
Estudos clínicos demonstraram que níveis elevados de C total, LDL-C e Apo B, a principal proteína constituinte da LDL, promovem a aterosclerose humana. Além disso, níveis diminuídos de HDL-C estão associados ao desenvolvimento de aterosclerose. Estudos epidemiológicos estabeleceram que a morbimortalidade cardiovascular varia diretamente com o nível de C-total e LDL-C e inversamente com o nível de HDL-C. Assim como o LDL, as lipoproteínas ricas em triglicerídeos enriquecidas com colesterol, incluindo lipoproteínas de densidade muito baixa (VLDL), lipoproteínas de densidade intermediária (IDL) e remanescentes, também podem promover aterosclerose. O efeito independente do aumento do HDL-C ou redução dos TG sobre o risco de morbidade e mortalidade coronariana e cardiovascular não foi determinado.
ZETIA reduz o C total, LDL-C, Apo B, não-HDL-C e TG, e aumenta o HDL-C em pacientes com hiperlipidemia. A administração de ZETIA 10mg com uma estatina é eficaz na melhora sérica de C total, LDL-C, Apo B, não-HDL-C, TG e HDL-C além de qualquer tratamento isolado. A administração de ZETIA 10mg com fenofibrato é eficaz na melhora sérica de C-total, C-LDL, Apo B e C-não-HDL em pacientes com hiperlipidemia mista em comparação com qualquer tratamento isolado. Os efeitos da ezetimiba administrada isoladamente ou em associação com uma estatina ou fenofibrato na morbidade e mortalidade cardiovascular não foram estabelecidos.
Farmacocinética
Absorção
Após administração oral, a ezetimiba é absorvida e extensivamente conjugada a um glicuronídeo fenólico farmacologicamente ativo (ezetimiba-glicuronídeo). Após uma dose única de 10 mg de ZETIA 10 mg a adultos em jejum, as concentrações plasmáticas máximas de ezetimiba (Cmax) de 3,4 a 5,5 ng/mL foram atingidas em 4 a 12 horas (Tmax). Valores médios de Cmax de ezetimiba-glicuronídeo de 45 a 71 ng/mL foram alcançados entre 1 e 2 horas (Tmax). Não houve desvio substancial da proporcionalidade da dose entre 5 e 20 mg. A biodisponibilidade absoluta da ezetimiba não pode ser determinada, pois o composto é praticamente insolúvel em meio aquoso adequado para injeção.
Efeito dos Alimentos na Absorção Oral
A administração concomitante de alimentos (refeições com alto teor de gordura ou sem gordura) não teve efeito sobre a extensão da absorção de ezetimiba quando administrado como comprimidos de 10 mg de ZETIA. O valor C da ezetimiba foi aumentado em 38% com o consumo de refeições ricas em gordura. ZETIA pode ser administrado com ou sem alimentos.
Distribuição
ezetimiba e a ezetimiba-glicuronídeo ligam-se fortemente (> 90%) às proteínas plasmáticas humanas.
Metabolismo e Excreção
A ezetimiba é metabolizada principalmente no intestino delgado e no fígado via conjugação de glicuronídeos (uma reação de fase II) com subsequente excreção biliar e renal. Metabolismo oxidativo mínimo (uma reação de fase I) foi observado em todas as espécies avaliadas.
Em humanos, a ezetimiba é rapidamente metabolizada em ezetimiba-glicuronídeo. A ezetimiba e a ezetimibeglucuronida são os principais compostos derivados de drogas detectados no plasma, constituindo aproximadamente 10 a 20% e 80 a 90% da droga total no plasma, respectivamente. Tanto a ezetimiba quanto a ezetimiba-glicuronídeo são eliminadas do plasma com meia-vida de aproximadamente 22 horas tanto para ezetimiba quanto para ezetimibeglicuronídeo. Os perfis de concentração-tempo no plasma exibem múltiplos picos, sugerindo reciclagem entero-hepática.
Após a administração oral de 14C-ezetimiba (20 mg) a seres humanos, a ezetimiba total (ezetimiba + ezetimiba-glicuronídeo) representou aproximadamente 93% da radioatividade total no plasma. Após 48 horas, não havia níveis detectáveis de radioatividade no plasma.
Aproximadamente 78% e 11% da radioatividade administrada foi recuperada nas fezes e na urina, respectivamente, em um período de coleta de 10 dias. A ezetimiba foi o principal componente nas fezes e representou 69% da dose administrada, enquanto a ezetimiba-glicuronídeo foi o principal componente na urina e representou 9% da dose administrada.
Populações Específicas
Pacientes Geriátricos: Em um estudo de dose múltipla com ezetimiba administrado 10 mg uma vez ao dia por 10 dias, as concentrações plasmáticas de ezetimiba total foram cerca de 2 vezes maiores em indivíduos saudáveis mais velhos (≥65 anos) em comparação com indivíduos mais jovens.
Pacientes Pediátricos: [Ver Uso em populações específicas ]
Gênero: Em um estudo de dose múltipla com ezetimiba administrado 10 mg uma vez ao dia por 10 dias, as concentrações plasmáticas de ezetimiba total foram ligeiramente mais altas (
Corrida: Com base em uma meta-análise de estudos farmacocinéticos de dose múltipla, não houve diferenças farmacocinéticas entre indivíduos negros e caucasianos. Estudos em indivíduos asiáticos indicaram que a farmacocinética da ezetimiba foi semelhante à observada em indivíduos caucasianos.
Insuficiência hepática: Após uma dose única de 10 mg de ezetimiba, a AUC média da ezetimiba total aumentou aproximadamente 1,7 vezes em pacientes com insuficiência hepática leve (pontuação de Child-Pugh 5 a 6), em comparação com indivíduos saudáveis. Os valores médios de AUC para ezetimiba total e ezetimiba aumentaram aproximadamente 3 a 4 vezes e 5 a 6 vezes, respectivamente, em pacientes com insuficiência hepática moderada (escore de Child-Pugh 7 a 9) ou grave (escore de Child-Pugh 10 a 15). Em um estudo de dose múltipla de 14 dias (10 mg por dia) em pacientes com insuficiência hepática moderada, os valores médios de AUC para ezetimiba total e ezetimiba aumentaram aproximadamente 4 vezes no Dia 1 e no Dia 14 em comparação com indivíduos saudáveis. Devido aos efeitos desconhecidos do aumento da exposição à ezetimiba em pacientes com insuficiência hepática moderada ou grave, ZETIA não é recomendado nesses pacientes [ver AVISOS E PRECAUÇÕES ].
Insuficiência renal: Após uma dose única de 10 mg de ezetimiba em pacientes com doença renal grave (n=8; CrCl médio ≥ 30 mL/min/1,73 m²), os valores médios de AUC para ezetimiba total, ezetimiba-glicuronídeo e ezetimiba aumentaram aproximadamente 1,5 - vezes, em comparação com indivíduos saudáveis (n=9).
Interações medicamentosas
[Veja também INTERAÇÕES MEDICAMENTOSAS ]
ZETIA 10mg não teve efeito significativo em uma série de drogas sonda (cafeína, dextrometorfano, tolbutamida e midazolam IV) conhecidas por serem metabolizadas pelo citocromo P450 (1A2, 2D6, 2C8/9 e 3A4) em um estudo “coquetel” de doze machos adultos. Isso indica que a ezetimiba não é um inibidor nem um indutor dessas isoenzimas do citocromo P450, e é improvável que a ezetimiba afete o metabolismo de drogas que são metabolizadas por essas enzimas.
TABELA 4: Efeito de Drogas Coadministradas na Ezetimiba Total
TABELA 5: Efeito da coadministração de ezetimiba na exposição sistêmica a outras drogas
Toxicologia e/ou Farmacologia Animal
efeito hipocolesterolêmico da ezetimiba foi avaliado em macacos Rhesus alimentados com colesterol, cães, ratos e modelos de camundongos do metabolismo do colesterol humano. A ezetimiba apresentou um valor de ED50 de 0,5 μg/kg/dia para inibir o aumento dos níveis plasmáticos de colesterol em macacos. Os valores de ED50 em cães, ratos e camundongos foram de 7, 30 e 700 μg/kg/dia, respectivamente. Estes resultados são consistentes com o fato de ZETIA ser um potente inibidor da absorção de colesterol.
Em um modelo de rato, onde o metabólito glicuronídeo de ezetimiba (SCH 60663) foi administrado por via intraduodenal, o metabólito foi tão potente quanto o composto original (SCH 58235) na inibição da absorção de colesterol, sugerindo que o metabólito glicuronídeo tinha atividade semelhante ao do composto original. medicamento.
Em estudos de 1 mês em cães que receberam ezetimiba (0,03 a 300 mg/kg/dia), a concentração de colesterol na bile da vesícula biliar aumentou ~2 a 4 vezes. No entanto, uma dose de 300 mg/kg/dia administrada a cães durante um ano não resultou na formação de cálculos biliares ou quaisquer outros efeitos hepatobiliares adversos. Em um estudo de 14 dias em camundongos que receberam ezetimiba (0,3 a 5 mg/kg/dia) e alimentados com uma dieta pobre em gordura ou rica em colesterol, a concentração de colesterol na bile da vesícula biliar não foi afetada ou reduzida a níveis normais, respectivamente.
Uma série de estudos pré-clínicos agudos foi realizada para determinar a seletividade de ZETIA para inibir a absorção de colesterol. A ezetimiba inibiu a absorção de 14C-colesterol sem efeito sobre a absorção de triglicerídeos, ácidos graxos, ácidos biliares, progesterona, etinilestradiol ou vitaminas lipossolúveis A e D.
Em estudos de toxicidade de 4 a 12 semanas em camundongos, a ezetimiba não induziu as enzimas metabolizadoras do citocromo P450. Em estudos de toxicidade, uma interação farmacocinética de ezetimiba com estatinas (pais ou seus metabólitos hidroxiácidos ativos) foi observada em ratos, cães e coelhos.
Estudos clínicos
Hiperlipidemia primária
ZETIA 10mg reduz o C total, LDL-C, Apo B, não-HDL-C e TG, e aumenta o HDL-C em pacientes com hiperlipidemia. A resposta máxima a quase máxima é geralmente alcançada em 2 semanas e mantida durante a terapia crônica.
Monoterapia
Em dois estudos multicêntricos, duplo-cegos, controlados por placebo, de 12 semanas em 1.719 pacientes com hiperlipidemia primária, ZETIA reduziu significativamente o C total, LDL-C, Apo B, não-HDL-C e TG, e aumentou o HDL- C em comparação com placebo (ver Tabela 6). A redução do LDL-C foi consistente em idade, sexo e LDL-C basal.
TABELA 6: Resposta ao ZETIA 10mg em Pacientes com Hiperlipidemia Primária (% de variação média da linha de base não tratada†)
Combinação com Estatinas
ZETIA 10mg adicionado à terapia com estatinas em andamento
Em um estudo multicêntrico, duplo-cego, controlado por placebo, de 8 semanas, 769 pacientes com hiperlipidemia primária, doença coronariana conhecida ou múltiplos fatores de risco cardiovascular que já estavam recebendo monoterapia com estatina, mas que não atingiram a meta de LDL do NCEP ATP II -C foram randomizados para receber ZETIA 10mg ou placebo, além de sua estatina em andamento.
ZETIA 10mg, adicionado à terapia com estatina em andamento, reduziu significativamente o C total, LDL-C, Apo B, não-HDL-C e TG, e aumentou o HDL-C em comparação com uma estatina administrada isoladamente (consulte a Tabela 7). As reduções de LDL-C induzidas por ZETIA 10mg foram geralmente consistentes em todas as estatinas.
TABELA 7: Resposta à adição de ZETIA 10mg à terapia com estatina em andamento em pacientes com hiperlipidemia (% de alteração média da linha de base tratada‡)
ZETIA iniciado concomitantemente com uma estatina
Em quatro estudos multicêntricos, duplo-cegos, controlados por placebo, de 12 semanas, em 2.382 pacientes hiperlipidêmicos, ZETIA ou placebo foi administrado isoladamente ou com várias doses de atorvastatina, sinvastatina, pravastatina ou lovastatina.
Quando todos os pacientes que receberam ZETIA com uma estatina foram comparados com todos aqueles que receberam apenas a estatina correspondente, ZETIA 10mg reduziu significativamente o C total, LDL-C, Apo B, não-HDL-C e TG e, com exceção da pravastatina , aumento do HDL-C em comparação com a estatina administrada isoladamente. As reduções de LDL-C induzidas por ZETIA 10mg foram geralmente consistentes em todas as estatinas. (Ver nota de rodapé, Tabelas 8 a 11.)
TABELA 8: Resposta a ZETIA 10mg e Atorvastatina Iniciados Simultaneamente em Pacientes com Hiperlipidemia Primária (% de variação média da linha de base não tratada†)
TABELA 9: Resposta ao ZETIA 10mg e Sinvastatina Iniciados Simultaneamente em Pacientes com Hiperlipidemia Primária (% de variação média da linha de base não tratada†)
TABELA 10: Resposta a ZETIA e Pravastatina Iniciados Simultaneamente em Pacientes com Hiperlipidemia Primária (% de Mudança Média da Linha de Base Não Tratada†)
TABELA 11: Resposta a ZETIA e lovastatina iniciadas concomitantemente em pacientes com hiperlipidemia primária (% de variação média da linha de base não tratada†)
Combinação com Fenofibrato
Em um estudo clínico multicêntrico, duplo-cego, controlado por placebo, em pacientes com hiperlipidemia mista, 625 pacientes foram tratados por até 12 semanas e 576 por até 48 semanas adicionais. Os pacientes foram randomizados para receber placebo, ZETIA sozinho, 160 mg de fenofibrato sozinho ou ZETIA 10 mg e 160 mg de fenofibrato no estudo de 12 semanas. Após completar o estudo de 12 semanas, os pacientes elegíveis foram designados para ZETIA coadministrado com fenofibrato ou monoterapia com fenofibrato por mais 48 semanas.
ZETIA 10mg coadministrado com fenofibrato reduziu significativamente o C total, LDL-C, Apo B e não-HDL-C em comparação com o fenofibrato administrado isoladamente. A diminuição percentual em TG e aumento percentual em HDLC para ZETIA coadministrado com fenofibrato foram comparáveis aos do fenofibrato administrado isoladamente (ver Tabela 12).
TABELA 12: Resposta ao ZETIA 10mg e fenofibrato iniciados concomitantemente em pacientes com hiperlipidemia mista (% de alteração média da linha de base não tratada† em 12 semanas†)
As alterações nos parâmetros lipídicos após 48 semanas adicionais de tratamento com ZETIA coadministrado com fenofibrato ou com fenofibrato isolado foram consistentes com os dados de 12 semanas apresentados acima.
Hipercolesterolemia Familiar Homozigótica (HoFH)
Um estudo foi realizado para avaliar a eficácia de ZETIA no tratamento de HoFH. Este estudo duplo-cego, randomizado, de 12 semanas envolveu 50 pacientes com diagnóstico clínico e/ou genotípico de HFHo, com ou sem aférese de LDL concomitante, já recebendo atorvastatina ou sinvastatina (40 mg). Os pacientes foram randomizados para um dos três grupos de tratamento, atorvastatina ou sinvastatina (80 mg), ZETIA 10 mg administrado com atorvastatina ou sinvastatina (40 mg), ou ZETIA administrado com atorvastatina ou sinvastatina (80 mg). Devido à biodisponibilidade diminuída da ezetimiba em pacientes recebendo colestiramina concomitantemente [ver INTERAÇÕES MEDICAMENTOSAS ], a ezetimiba foi administrada pelo menos 4 horas antes ou após a administração das resinas. A média basal de LDL-C foi de 341 mg/dL naqueles pacientes randomizados para atorvastatina 80 mg ou sinvastatina 80 mg isoladamente e 316 mg/dL no grupo randomizado para ZETIA 10 mg mais atorvastatina 40 ou 80 mg ou sinvastatina 40 ou 80 mg. ZETIA 10 mg, administrado com atorvastatina ou sinvastatina (grupos de estatina de 40 e 80 mg, agrupados), reduziu significativamente o LDL-C (21%) em comparação com o aumento da dose de monoterapia com sinvastatina ou atorvastatina de 40 para 80 mg (7%). Naqueles tratados com ZETIA 10 mg mais 80 mg de atorvastatina ou com ZETIA 10 mg mais 80 mg de sinvastatina, o LDL-C foi reduzido em 27%.
Sitosterolemia Homozigótica (Fitosterolemia)
Foi realizado um estudo para avaliar a eficácia de ZETIA no tratamento de sitosterolemia homozigótica. Neste estudo multicêntrico, duplo-cego, controlado por placebo, de 8 semanas, 37 pacientes com homozigose de sitosterolemia com níveis plasmáticos elevados de sitosterol (> 5 mg/dL) em seu regime terapêutico atual (dieta, resinas de ligação aos ácidos biliares, estatinas, cirurgia de bypass ileal e/ou aférese de LDL), foram randomizados para receber ZETIA (n=30) ou placebo (n=7). Devido à biodisponibilidade diminuída da ezetimiba em pacientes recebendo colestiramina concomitantemente [ver INTERAÇÕES MEDICAMENTOSAS ], a ezetimiba foi administrada pelo menos 2 horas antes ou 4 horas após a administração das resinas. Excluindo o indivíduo que recebeu aférese de LDL, ZETIA reduziu significativamente o sitosterol e o campesterol plasmático, em 21% e 24% da linha de base, respectivamente. Em contraste, os pacientes que receberam placebo tiveram aumentos de sitosterol e campesterol de 4% e 3% em relação à linha de base, respectivamente. Para pacientes tratados com ZETIA 10mg, os níveis plasmáticos médios de esteróis vegetais foram reduzidos progressivamente ao longo do estudo. Os efeitos da redução do sitosterol e do campesterol no plasma na redução dos riscos de morbidade e mortalidade cardiovascular não foram estabelecidos.
As reduções no sitosterol e campesterol foram consistentes entre os pacientes que tomaram ZETIA 10mg concomitantemente com sequestrantes de ácidos biliares (n=8) e pacientes que não receberam terapia concomitante com sequestrantes de ácidos biliares (n=21).
Limitações de uso
O efeito de ZETIA 10mg na morbidade e mortalidade cardiovascular não foi determinado.
INFORMAÇÃO DO PACIENTE
ZETIA® (ezetimiba) Comprimidos
Informações do paciente sobre ZETIA (zet´-ea)
Nome genérico: ezetimiba (e-zet´-e-mib)
Leia esta informação com atenção antes de começar a tomar ZETIA® e cada vez que tomar mais ZETIA. Pode haver novas informações. Esta informação não substitui a conversa com seu médico sobre sua condição médica ou seu tratamento. Se você tiver alguma dúvida sobre ZETIA, pergunte ao seu médico. Somente seu médico pode determinar se ZETIA é adequado para você.
O que é ZETIA?
ZETIA é um medicamento utilizado para baixar os níveis de colesterol total e LDL (mau colesterol) no sangue. ZETIA é para pacientes que não conseguem controlar seus níveis de colesterol apenas com dieta e exercícios. Pode ser usado sozinho ou com outros medicamentos para tratar o colesterol alto. Deve manter uma dieta para baixar o colesterol enquanto estiver a tomar este medicamento.
ZETIA trabalha para reduzir a quantidade de colesterol que seu corpo absorve. ZETIA 10mg não ajuda a perder peso. ZETIA 10mg não demonstrou prevenir doenças cardíacas ou ataques cardíacos.
Para obter mais informações sobre colesterol, consulte a seção “O que devo saber sobre colesterol alto?” seção que segue.
Quem não deve tomar ZETIA 10mg?
- Não tome ZETIA 10mg se você é alérgico à ezetimiba, o ingrediente ativo de ZETIA, ou aos ingredientes inativos. Para obter uma lista de ingredientes inativos, consulte a seção “Ingredientes inativos” a seguir.
- Se você tem doença hepática ativa, não tome ZETIA 10mg enquanto estiver tomando medicamentos para baixar o colesterol chamados estatinas.
- Se estiver grávida ou a amamentar, não tome ZETIA enquanto estiver a tomar uma estatina.
- Se você é uma mulher em idade fértil, você deve usar um método eficaz de controle de natalidade para prevenir a gravidez enquanto estiver usando ZETIA adicionado à terapia com estatinas.
ZETIA não foi estudado em crianças com menos de 10 anos.
O que devo dizer ao meu médico antes e enquanto estiver tomando ZETIA 10mg?
Informe o seu médico sobre quaisquer medicamentos prescritos e não prescritos que você esteja tomando ou planeja tomar, incluindo remédios naturais ou fitoterápicos.
Informe o seu médico sobre todas as suas condições médicas, incluindo alergias.
Informe o seu médico se você:
- já teve problemas de fígado. ZETIA 10mg pode não ser adequado para você.
- estão grávidas ou planejam engravidar. O seu médico irá discutir consigo se ZETIA 10mg é adequado para si.
- estão amamentando. Não sabemos se ZETIA 10mg pode passar para o seu bebé através do leite. O seu médico irá discutir consigo se ZETIA 10mg é adequado para si.
- sentir dor muscular inexplicável, sensibilidade ou fraqueza.
Como devo tomar ZETIA 10mg?
- Tome ZETIA uma vez ao dia, com ou sem alimentos. Pode ser mais fácil lembrar-se de tomar a sua dose se o fizer à mesma hora todos os dias, como ao pequeno-almoço, jantar ou ao deitar. Se também tomar outro medicamento para reduzir o colesterol, pergunte ao seu médico se pode tomá-lo ao mesmo tempo.
- Caso se tenha esquecido de tomar ZETIA, tome-o assim que se lembrar. No entanto, não tome mais do que uma dose de ZETIA por dia.
- Continue a seguir uma dieta para baixar o colesterol enquanto estiver tomando ZETIA. Pergunte ao seu médico se você precisa de informações sobre dieta.
- Continue a tomar ZETIA 10mg, a menos que o seu médico lhe diga para parar. É importante que continue a tomar ZETIA 10 mg mesmo que não se sinta doente.
- Consulte seu médico regularmente para verificar seu nível de colesterol e verificar se há efeitos colaterais. O seu médico pode fazer análises ao sangue para verificar o seu fígado antes de começar a tomar ZETIA com uma estatina e durante o tratamento.
Quais são os possíveis efeitos colaterais do ZETIA?
Em estudos clínicos, os pacientes relataram poucos efeitos colaterais enquanto tomavam ZETIA. Estes incluíam diarreia, dores nas articulações e sensação de cansaço.
Os pacientes tiveram problemas musculares graves enquanto tomavam ZETIA 10mg, geralmente quando ZETIA 10mg foi adicionado a uma estatina. Se sentir dor muscular, sensibilidade ou fraqueza inexplicáveis enquanto estiver a tomar ZETIA, contacte o seu médico imediatamente. Você precisa fazer isso imediatamente, porque em raras ocasiões, esses problemas musculares podem ser graves, com ruptura muscular resultando em danos nos rins.
Além disso, os seguintes efeitos colaterais foram relatados no uso geral: reações alérgicas (que podem exigir tratamento imediato) incluindo inchaço da face, lábios, língua e/ou garganta que podem causar dificuldade em respirar ou engolir, erupção cutânea e urticária ; erupção cutânea vermelha elevada, às vezes com lesões em forma de alvo; dor nas articulações; dores musculares; alterações em alguns exames laboratoriais de sangue; problemas de fígado; dor de estômago; inflamação do pâncreas; náusea; tontura; sensação de formigueiro; depressão; dor de cabeça; cálculos biliares; inflamação da vesícula biliar.
Informe o seu médico se tiver estes ou quaisquer outros problemas médicos enquanto estiver a tomar ZETIA. Para obter uma lista completa de efeitos colaterais, pergunte ao seu médico ou farmacêutico.
O que devo saber sobre colesterol alto?
O colesterol é um tipo de gordura encontrada no sangue. Seu colesterol total é composto de colesterol LDL e HDL.
colesterol LDL é chamado de colesterol “ruim” porque pode se acumular na parede das artérias e formar placas. Com o tempo, o acúmulo de placas pode causar um estreitamento das artérias. Esse estreitamento pode retardar ou bloquear o fluxo sanguíneo para o coração, cérebro e outros órgãos. O colesterol LDL elevado é uma das principais causas de doenças cardíacas e uma das causas de acidente vascular cerebral.
O colesterol HDL é chamado de colesterol “bom” porque evita que o colesterol ruim se acumule nas artérias.
Os triglicerídeos também são gorduras encontradas no sangue.
Informações gerais sobre ZETIA
Às vezes, medicamentos são prescritos para condições que não são mencionadas nos folhetos informativos do paciente. Não use ZETIA 10mg para uma condição para a qual não foi prescrito. Não dê ZETIA a outras pessoas, mesmo que tenham a mesma condição que você. Pode prejudicá-los.
Isso resume as informações mais importantes sobre ZETIA. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu farmacêutico ou médico informações sobre ZETIA 10mg que são escritas para profissionais de saúde.
Ingredientes inativos :
Croscarmelose sódica, lactose monohidratada, estearato de magnésio, celulose microcristalina, povidona e lauril sulfato de sódio.
