Microzide 25mg Hydrochlorothiazide Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Microzide 25mg e como é usado?
Microzide é um medicamento de prescrição usado para tratar os sintomas de pressão alta (hipertensão) e inchaço (edema). Microzide pode ser usado sozinho ou com outros medicamentos.
Microzide pertence a uma classe de medicamentos chamados diuréticos, tiazídicos.
Não se sabe se Microzide é seguro e eficaz em crianças com menos de 6 meses de idade.
Quais são os possíveis efeitos colaterais do Microzide?
Microzide pode causar efeitos colaterais graves, incluindo:
- tontura,
- dor nos olhos,
- problemas de visão,
- amarelecimento da pele ou dos olhos (icterícia),
- pele pálida,
- contusões fáceis,
- sangramento incomum (nariz, boca, vagina ou reto),
- falta de ar,
- chiado,
- tosse com muco espumoso,
- dor no peito,
- boca seca,
- sede,
- sonolência,
- falta de energia,
- inquietação,
- dor ou fraqueza muscular,
- ritmo cardíaco acelerado,
- náusea,
- vômito,
- pouca ou nenhuma urina,
- febre,
- dor de garganta,
- inchaço no rosto ou na língua,
- queimando em seus olhos, e
- dor na pele seguida por uma erupção cutânea vermelha ou roxa que se espalha (especialmente no rosto ou na parte superior do corpo) e causa bolhas e descamação
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Microzide incluem:
- náusea,
- vômito,
- perda de apetite,
- diarréia,
- constipação,
- espasmo muscular,
- tontura, e
- dor de cabeça
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Microzide. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
MICROZIDE® (hidroclorotiazida, USP 12,5 mg) é o derivado 3,4-dihidro da clorotiazida. Seu nome químico é 6-cloro-3,4-dihidro-2H-1,2,4-benzotiadiazina-7-sulfonamida 1,1-dióxido. Sua fórmula empírica é C7H8CIN304S2; seu peso molecular é 297,74; e sua fórmula estrutural é:
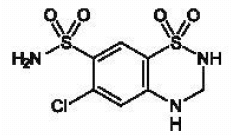
É um pó cristalino branco, ou praticamente branco, ligeiramente solúvel em água, mas livremente solúvel em solução de hidróxido de sódio.
MICROZIDE (cápsula de hidroclorotiazida) é fornecido em cápsulas de 12,5 mg para uso oral.
Ingredientes inativos : dióxido de silício coloidal, amido de milho, lactose monohidratada, estearato de magnésio. As cápsulas de gelatina contêm D&C Vermelho Nº 28, D&C Amarelo Nº 10, FD&C Azul Nº 1, gelatina, dióxido de titânio. As cápsulas são impressas com tinta comestível contendo óxido de ferro preto, D&C Yellow No. 10, FD&C Blue No. 1, FD&C Blue No. 2, FD&C Red No. 40.
INDICAÇÕES
MICROZIDE (cápsula de hidroclorotiazida) é indicado no tratamento da hipertensão como o único agente terapêutico ou em combinação com outros anti-hipertensivos. Ao contrário dos produtos diuréticos combinados poupadores de potássio, MICROZIDE (cápsula de hidroclorotiazida) pode ser usado naqueles pacientes nos quais o desenvolvimento de hipercalemia não pode ser arriscado, incluindo pacientes em uso de inibidores da ECA.
Uso na gravidez
O uso rotineiro de diuréticos em uma mulher saudável é inadequado e expõe a mãe e o feto a riscos desnecessários. Os diuréticos não previnem o desenvolvimento de toxemia da gravidez e não há evidências satisfatórias de que sejam úteis no tratamento da toxemia desenvolvida.
edema durante a gravidez pode surgir de causas patológicas ou das consequências fisiológicas e mecânicas da gravidez. Os diuréticos são indicados na gravidez quando o edema é devido a causas patológicas, assim como na ausência de gravidez. O edema dependente na gravidez decorrente da restrição do retorno venoso pelo útero expandido é devidamente tratado com elevação dos membros inferiores e uso de mangueira de apoio; o uso de diuréticos para diminuir o volume intravascular neste caso é ilógico e desnecessário. Há hipervolemia durante a gravidez normal que não é prejudicial nem para o feto nem para a mãe (na ausência de doença cardiovascular), mas que está associada a edema, incluindo edema generalizado na maioria das gestantes. Se esse edema produzir desconforto, o decúbito aumentado muitas vezes proporcionará alívio. Em casos raros, este edema pode causar desconforto extremo que não é aliviado pelo repouso. Nesses casos, um curso curto de diuréticos pode proporcionar alívio e pode ser apropriado.
DOSAGEM E ADMINISTRAÇÃO
Para controle da hipertensão : A dose inicial de MICROZIDE (cápsula de hidroclorotiazida) para adultos é uma cápsula administrada uma vez ao dia, seja administrada isoladamente ou em combinação com outros anti-hipertensivos. Doses diárias totais superiores a 50 mg não são recomendadas.
COMO FORNECIDO
MICROZIDA (cápsula de hidroclorotiazida) Cápsulas são cápsulas de gelatina dura #4 Teal Opaque/Teal Opaque de duas peças impressas com MICROZIDE (cápsula de hidroclorotiazida) e 12,5 mg em tinta preta. São fornecidos em frascos de 100 com fechos à prova de crianças ( NDC 52544-622-01).
Dispense em um recipiente apertado e resistente à luz, conforme definido na USP.
Mantenha fora do alcance de crianças.
Armazenar a 20°-25°C (68°-77°F). [Consulte a temperatura ambiente controlada pela USP.] Proteja da luz, umidade, congelamento, -20°C (-4°F). Mantenha o recipiente bem fechado.
Envie consultas médicas para: WATSON., Medical Communications PO Box 1953, Morristown, NJ 07962-1953. 800-272-5525. Fabricado por: Watson Pharma Private Limited. Verna, Salcete, Goa 403 722 ÍNDIA. Distribuído por: Watson Pharma, Inc. Morristown, NJ 07962 EUA. Revisado: fevereiro de 2011
EFEITOS COLATERAIS
As reações adversas associadas à hidroclorotiazida demonstraram estar relacionadas com a dose. Em ensaios clínicos controlados, os eventos adversos relatados com doses de 12,5 mg de hidroclorotiazida uma vez ao dia foram comparáveis ao placebo. As seguintes reações adversas foram relatadas para doses de hidroclorotiazida de 25 mg e superiores e, dentro de cada categoria, estão listadas em ordem decrescente de gravidade.
Corpo como um todo : Fraqueza.
Cardiovascular : Hipotensão incluindo hipotensão ortostática (pode ser agravada por álcool, barbitúricos, narcóticos ou medicamentos anti-hipertensivos).
Digestivo Pancreatite, icterícia (icterícia colestática intra-hepática), diarreia, vómitos, sialoadenite, cãibras, obstipação, irritação gástrica, náuseas, anorexia.
Hematologico : Anemia aplástica, agranulocitose, leucopenia, anemia hemolítica, trombocitopenia.
Hipersensibilidade : Reações anafiláticas, angeíte necrosante (vasculite e vasculite cutânea), dificuldade respiratória incluindo pneumonite e edema pulmonar, fotossensibilidade, febre, urticária, erupção cutânea, púrpura.
Metabólico : Desequilíbrio eletrolítico (ver PRECAUÇÕES ), hiperglicemia, glicosúria, hiperuricemia.
Musculoesquelético : Espasmo muscular.
Sistema Nervoso/Psiquiátrico : Vertigem, parestesia, tontura, dor de cabeça, inquietação.
Renal : Insuficiência renal, disfunção renal, nefrite intersticial (ver AVISOS ).
Pele : Eritema multiforme incluindo síndrome de Stevens-Johnson, dermatite esfoliativa incluindo necrólise epidérmica tóxica, alopecia.
Sentidos Especiais Visão turva transitória, xantopsia.
Urogenital : impotência.
Sempre que as reações adversas forem moderadas ou graves, a dosagem de tiazida deve ser reduzida ou a terapia suspensa.
INTERAÇÕES MEDICAMENTOSAS
Quando administrados concomitantemente, os seguintes medicamentos podem interagir com diuréticos tiazídicos:
Álcool, barbitúricos ou narcóticos - pode ocorrer potenciação da hipotensão ortostática.
Medicamentos antidiabéticos - (agentes orais e insulina) pode ser necessário o ajuste da dose do medicamento antidiabético.
Outros medicamentos anti-hipertensivos - efeito aditivo ou potenciação.
Resinas de colestiramina e colestipol - As resinas de colestiramina e colestipol se ligam à hidroclorotiazida e reduzem sua absorção no trato gastrointestinal em até 85 e 43 por cento, respectivamente.
Corticosteróide, ACTH - depleção eletrolítica intensificada, particularmente hipocalemia.
Aminas pressoras (por exemplo, norepinefrina) - possível diminuição da resposta às aminas pressoras, mas não suficiente para impedir seu uso.
Relaxantes do músculo esquelético, não despolarizantes (por exemplo, tubocurarina) possível aumento da capacidade de resposta ao relaxante muscular.
Lítio - geralmente não deve ser administrado com diuréticos. Os agentes diuréticos reduzem a depuração renal do lítio e aumentam muito o risco de toxicidade do lítio. Consulte o folheto informativo das preparações de lítio antes de usar essas preparações com MICROZIDE (cápsula de hidroclorotiazida).
Anti-inflamatórios não esteróides - Em alguns pacientes, a administração de um agente anti-inflamatório não esteroidal pode reduzir os efeitos diuréticos, natriuréticos e anti-hipertensivos dos diuréticos de alça, poupadores de potássio e tiazídicos. Quando MICROZIDE (cápsula de hidroclorotiazida) e agentes anti-inflamatórios não esteroides são usados concomitantemente, os pacientes devem ser observados atentamente para determinar se o efeito desejado do diurético é obtido.
Interações Medicamentos/Testes Laboratoriais
As tiazidas devem ser descontinuadas antes da realização de testes de função da paratireoide (ver PRECAUÇÕES, Geral ).
AVISOS
Diabetes e hipoglicemia: Diabetes mellitus latente pode se manifestar e pacientes diabéticos que recebem tiazidas podem necessitar de ajuste de sua dose de insulina.
Doença renal: Os efeitos cumulativos das tiazidas podem se desenvolver em pacientes com função renal comprometida. Nesses pacientes, as tiazidas podem precipitar a azotemia.
PRECAUÇÕES
Status de equilíbrio de eletrólitos e fluidos
Em estudos publicados, a hipocalemia clinicamente significativa tem sido consistentemente menos comum em pacientes que receberam 12,5 mg de hidroclorotiazida do que em pacientes que receberam doses mais altas. No entanto, a determinação periódica dos eletrólitos séricos deve ser realizada em pacientes que possam estar em risco de desenvolver hipocalemia. Os pacientes devem ser observados quanto a sinais de distúrbios hidroeletrolíticos, ou seja, hiponatremia, alcalose hipoclorêmica e hipocalemia e hipomagnesemia.
Sinais de alerta ou sintomas de desequilíbrio hidroeletrolítico incluem secura da boca, sede, fraqueza, letargia, sonolência, inquietação, dores musculares ou cãibras, fadiga muscular, hipotensão, oligúria, taquicardia e distúrbios gastrointestinais, como náuseas e vômitos.
Pode ocorrer hipocalemia, especialmente com diurese rápida quando há cirrose grave, durante o uso concomitante de corticosteroides ou hormônio adrenocorticotrófico (ACTH) ou após terapia prolongada. A interferência na ingestão adequada de eletrólitos orais também contribuirá para a hipocalemia. A hipocalemia e a hipomagnesemia podem provocar arritmias ventriculares ou sensibilizar ou exagerar a resposta do coração aos efeitos tóxicos dos digitálicos. A hipocalemia pode ser evitada ou tratada com suplementação de potássio ou aumento da ingestão de alimentos ricos em potássio.
hiponatremia dilucional é fatal e pode ocorrer em pacientes edematosos em clima quente; a terapia apropriada é a restrição hídrica em vez da administração de sal, exceto em casos raros quando a hiponatremia é fatal. Na depleção real de sal, a reposição apropriada é a terapia de escolha.
Hiperuricemia
Hiperuricemia ou gota aguda podem ser precipitadas em certos pacientes recebendo diuréticos tiazídicos.
Função hepática prejudicada
As tiazidas devem ser utilizadas com precaução em doentes com insuficiência hepática. Eles podem precipitar coma hepático em pacientes com doença hepática grave.
Doença da paratireóide
A excreção de cálcio é diminuída pelas tiazidas, e alterações patológicas nas glândulas paratireoides, com hipercalcemia e hipofosfatemia, foram observadas em alguns pacientes em terapia prolongada com tiazidas.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Estudos de alimentação de dois anos em camundongos e ratos conduzidos sob os auspícios do Programa Nacional de Toxicologia (NTP) não revelaram evidência de potencial carcinogênico da hidroclorotiazida em camundongos fêmeas (em doses de até aproximadamente 600 mg/kg/dia) ou em camundongos machos. e ratos fêmeas (em doses de aproximadamente 100 mg/kg/dia). O NTP, no entanto, encontrou evidências ambíguas de hepatocarcinogenicidade em camundongos machos. A hidroclorotiazida não foi genotóxica in vitro no ensaio de mutagenicidade de Ames das cepas de Salmonella typhimurium TA 98, TA 100, TA 1535, TA 1537 e TA 1538 e no teste de ovário de hamster chinês (CHO) para aberrações cromossômicas, ou in vivo em ensaios usando cromossomos de células germinais de camundongos, cromossomos de medula óssea de hamster chinês e o gene recessivo de traço letal ligado ao sexo de Drosophila. Os resultados positivos dos testes foram obtidos apenas nos ensaios in vitro CHO Sister Chromatid Exchange (clastogenicidade) e nos ensaios de células de linfoma de camundongo (mutagenicidade), usando concentrações de hidroclorotiazida de 43 a 1300 mcg/mL, e no ensaio de não disjunção de Aspergillus nidulans em uma concentração não especificada.
hidroclorotiazida não teve efeitos adversos na fertilidade de camundongos e ratos de ambos os sexos em estudos em que essas espécies foram expostas, por meio de sua dieta, a doses de até 100 e 4 mg/kg, respectivamente, antes da concepção e durante a gestação.
Gravidez
Efeitos teratogênicos
Gravidez Categoria B: Estudos nos quais a hidroclorotiazida foi administrada oralmente a camundongos e ratas grávidas durante seus respectivos períodos de organogênese importante em doses de até 3.000 e 1.000 mg de hidroclorotiazida/kg, respectivamente, não forneceram evidências de danos ao feto.
No entanto, não existem estudos adequados e bem controlados em mulheres grávidas. Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, este medicamento deve ser usado durante a gravidez somente se for claramente necessário.
Efeitos não teratogênicos
As tiazidas atravessam a barreira placentária e aparecem no sangue do cordão umbilical. Existe o risco de icterícia fetal ou neonatal, trombocitopenia e possivelmente outras reações adversas que ocorreram em adultos.
Mães que amamentam
As tiazidas são excretadas no leite materno. Devido ao potencial de reações adversas graves em lactentes, deve-se decidir entre descontinuar a amamentação ou descontinuar a hidroclorotiazida, levando em consideração a importância do medicamento para a mãe.
Uso Pediátrico
A segurança e eficácia em pacientes pediátricos não foram estabelecidas.
Uso Idoso
Uma maior redução da pressão arterial e um aumento dos efeitos colaterais podem ser observados em idosos (ou seja, > 65 anos) com hidroclorotiazida. Portanto, é recomendado iniciar o tratamento com a dose mais baixa disponível de hidroclorotiazida (12,5 mg). Se for necessária uma titulação adicional, devem ser utilizados incrementos de 12,5 mg.
SOBREDOSAGEM
Os sinais e sintomas mais comuns observados são aqueles causados por depleção eletrolítica (hipocalemia, hipocloremia, hiponatremia) e desidratação decorrente de diurese excessiva. Se digitálicos também foram administrados, a hipocalemia pode acentuar as arritmias cardíacas.
Em caso de superdosagem, medidas sintomáticas e de suporte devem ser empregadas. Emese deve ser induzida ou lavagem gástrica realizada. Corrigir desidratação, desequilíbrio eletrolítico, coma hepático e hipotensão através de procedimentos estabelecidos. Se necessário, administre oxigênio ou respiração artificial para insuficiência respiratória. O grau de remoção da hidroclorotiazida por hemodiálise não foi estabelecido.
A LD50 oral da hidroclorotiazida é superior a 10 g/kg no camundongo e rato.
CONTRA-INDICAÇÕES
A hidroclorotiazida é contraindicada em pacientes com anúria. A hipersensibilidade a este produto ou a outros medicamentos derivados de sulfonamidas também é contraindicada.
FARMACOLOGIA CLÍNICA
hidroclorotiazida bloqueia a reabsorção de íons sódio e cloreto, aumentando assim a quantidade de sódio que atravessa o túbulo distal e o volume de água excretado. Uma porção do sódio adicional apresentado ao túbulo distal é trocada por íons de potássio e hidrogênio. Com o uso continuado de hidroclorotiazida e depleção de sódio, mecanismos compensatórios tendem a aumentar essa troca e podem produzir perda excessiva de íons potássio, hidrogênio e cloreto. A hidroclorotiazida também diminui a excreção de cálcio e ácido úrico, pode aumentar a excreção de iodeto e pode reduzir a taxa de filtração glomerular. As toxicidades metabólicas associadas a alterações eletrolíticas excessivas causadas pela hidroclorotiazida demonstraram estar relacionadas com a dose.
Farmacocinética e Metabolismo
A hidroclorotiazida é bem absorvida (65% a 75%) após administração oral. A absorção de hidroclorotiazida é reduzida em pacientes com insuficiência cardíaca congestiva.
As concentrações plasmáticas máximas são observadas dentro de 1 a 5 horas após a administração e variam de 70 a 490 ng/mL após doses orais de 12,5 a 100 mg. As concentrações plasmáticas estão linearmente relacionadas com a dose administrada. As concentrações de hidroclorotiazida são 1,6 a 1,8 vezes maiores no sangue total do que no plasma. A ligação às proteínas séricas foi relatada como sendo de aproximadamente 40% a 68%. A meia-vida de eliminação plasmática foi relatada como sendo de 6 a 15 horas. A hidroclorotiazida é eliminada principalmente pelas vias renais. Após doses orais de 12,5 a 100 mg, 55% a 77% da dose administrada aparece na urina e mais de 95% da dose absorvida é excretada na urina como droga inalterada. Em pacientes com doença renal, as concentrações plasmáticas de hidroclorotiazida estão aumentadas e a meia-vida de eliminação é prolongada.
Quando MICROZIDE (cápsula de hidroclorotiazida) é administrado com alimentos, sua biodisponibilidade é reduzida em 10%, a concentração plasmática máxima é reduzida em 20% e o tempo até a concentração máxima aumenta de 1,6 para 2,9 horas.
Farmacodinâmica
Acredita-se que os efeitos anti-hipertensivos agudos das tiazidas resultem de uma redução do volume sanguíneo e do débito cardíaco, secundária a um efeito natriurético, embora também tenha sido proposto um mecanismo vasodilatador direto. Com a administração crônica, o volume plasmático volta ao normal, mas a resistência vascular periférica diminui. O mecanismo exato do efeito anti-hipertensivo da hidroclorotiazida não é conhecido.
As tiazidas não afetam a pressão arterial normal. O início da ação ocorre dentro de 2 horas após a administração, o efeito máximo é observado em cerca de 4 horas e a atividade persiste por até 24 horas.
Estudos clínicos
Em um estudo duplo-cego de 4 semanas, duplo-cego, controlado por placebo, em grupo paralelo, com 87 pacientes, os pacientes que receberam MICROZIDE (cápsula de hidroclorotiazida) tiveram reduções na pressão arterial sistólica e diastólica sentadas que foram significativamente maiores do que aquelas observadas em pacientes que receberam placebo. Em estudos controlados por placebo publicados comparando 12,5 mg de hidroclorotiazida a 25 mg, a dose de 12,5 mg preservou a maior parte da redução da pressão arterial corrigida por placebo observada com 25 mg.
INFORMAÇÃO DO PACIENTE
Nenhuma informação fornecida. Por favor, consulte o AVISOS e PRECAUÇÕES Seções.
