Tratamento do Câncer: Nolvadex 10mg, 20mg Tamoxifen Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Nolvadex e como é usado?
Nolvadex 10mg é um medicamento de prescrição usado para tratar os sintomas do câncer de mama. Nolvadex pode ser usado sozinho ou com outros medicamentos.
Nolvadex 20mg pertence a uma classe de medicamentos chamados antineoplásicos, antagonistas dos receptores de estrogênio.
Não se sabe se Nolvadex 20mg é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Nolvadex 20mg?
Nolvadex pode causar efeitos colaterais graves, incluindo:
- alterações na visão,
- dor nos olhos,
- hematomas ou sangramentos fáceis,
- mudanca de humor,
- inchaço dos tornozelos ou pés, e
- cansaço incomum
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Nolvadex incluem:
- ondas de calor,
- rubor,
- alterações nos períodos menstruais,
- náusea,
- cãibras nas pernas,
- cólicas abdominais,
- dor no osso,
- dor muscular,
- tosse,
- inchaço,
- fadiga,
- queda de cabelo,
- dor de cabeça,
- depressão, e
- perda de capacidade/interesse sexual (em homens)
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Nolvadex. Para mais informações, consulte seu médico ou farmacêutico.
AVISO
Para mulheres com carcinoma ductal in situ (DCIS) e mulheres com alto risco de câncer de mama: Eventos graves e com risco de vida associados ao NOLVADEX (citrato de tamoxifeno) no cenário de redução de risco (mulheres com alto risco de câncer e mulheres com CDIS) incluem malignidades uterinas, acidente vascular cerebral e embolia pulmonar. As taxas de incidência para esses eventos foram estimadas a partir do estudo NSABP P-1 (ver FARMACOLOGIA CLÍNICA-Estudos Clínicos - Redução da Incidência de Câncer de Mama em Mulheres de Alto Risco ). As malignidades uterinas consistem em adenocarcinoma endometrial (taxa de incidência por 1.000 mulheres-ano de 2,20 para NOLVADEX (citrato de tamoxifeno) versus 0,71 para placebo) e sarcoma uterino (taxa de incidência por 1.000 mulheres-ano de 0,17 para NOLVADEX (citrato de tamoxifeno) versus 0,4 para placebo)*. Para acidente vascular cerebral, a taxa de incidência por 1.000 mulheres-ano foi de 1,43 para NOLVADEX (citrato de tamoxifeno) versus 1,00 para placebo**. Para embolia pulmonar, a taxa de incidência por 1.000 mulheres-ano foi de 0,75 para NOLVADEX (citrato de tamoxifeno) versus 0,25 para placebo**.
Alguns dos acidentes vasculares cerebrais, embolia pulmonar e malignidades uterinas foram fatais.
Os profissionais de saúde devem discutir os benefícios potenciais versus os riscos potenciais desses eventos graves com mulheres com alto risco de câncer de mama e mulheres com CDIS considerando NOLVADEX (citrato de tamoxifeno) para reduzir o risco de desenvolver câncer de mama.
Os benefícios do NOLVADEX (citrato de tamoxifeno) superam seus riscos em mulheres já diagnosticadas com câncer de mama.
REFERÊNCIAS
*Dados atualizados de acompanhamento de longo prazo (a duração média do acompanhamento é de 6,9 anos) do estudo NSABP P-1. Ver AVISOS: Efeitos sobre o câncer de útero-endométrio e sarcoma uterino .
**Consulte a Tabela 3 abaixo FARMACOLOGIA CLÍNICA-Estudos Clínicos .
DESCRIÇÃO
Os comprimidos de NOLVADEX® (citrato de tamoxifeno), um antiestrogênio não esteroidal, são para administração oral. Os comprimidos de NOLVADEX (citrato de tamoxifeno) estão disponíveis como:
Comprimidos de 10 mg
Cada comprimido contém 15,2 mg de citrato de tamoxifeno que é equivalente a 10 mg de tamoxifeno.
Comprimidos de 20 mg
Cada comprimido contém 30,4 mg de citrato de tamoxifeno que é equivalente a 20 mg de tamoxifeno.
Ingredientes inativos: carboximetilcelulose cálcio, estearato de magnésio, manitol e amido.
Quimicamente, NOLVADEX (citrato de tamoxifeno) é o isômero trans de um derivado de trifeniletileno. O nome químico é (Z)2-[4-(1,2-difenil-1-butenil)fenoxi]-N,N-dimetiletanamina 2 hidroxi-1,2,3-propanotricarboxilato (1:1). As fórmulas estruturais e empíricas são:
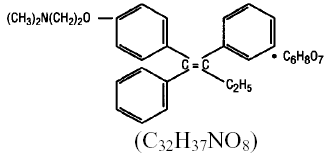
O citrato de tamoxifeno tem um peso molecular de 563,62, o pKa' é 8,85, a solubilidade de equilíbrio em água a 37°C é 0,5 mg/mL e em HCl 0,02 N a 37°C, é 0,2 mg/mL.
INDICAÇÕES
Câncer de mama metastático
NOLVADEX (citrato de tamoxifeno) é eficaz no tratamento do câncer de mama metastático em mulheres e homens. Em mulheres na pré-menopausa com câncer de mama metastático, NOLVADEX (citrato de tamoxifeno) é uma alternativa à ooforectomia ou irradiação ovariana. As evidências disponíveis indicam que os pacientes cujos tumores são positivos para o receptor de estrogênio são mais propensos a se beneficiar da terapia com NOLVADEX (citrato de tamoxifeno).
Tratamento Adjuvante do Câncer de Mama
NOLVADEX (citrato de tamoxifeno) é indicado para o tratamento de câncer de mama com nódulo positivo em mulheres após mastectomia total ou mastectomia segmentar, dissecção axilar e irradiação da mama. Em alguns estudos adjuvantes de NOLVADEX (citrato de tamoxifeno), a maior parte do benefício até o momento foi no subgrupo com quatro ou mais linfonodos axilares positivos.
NOLVADEX (citrato de tamoxifeno) é indicado para o tratamento de câncer de mama com linfonodo axilar negativo em mulheres após mastectomia total ou mastectomia segmentar, dissecção axilar e irradiação da mama.
Os valores dos receptores de estrogênio e progesterona podem ajudar a prever se a terapia adjuvante com NOLVADEX (citrato de tamoxifeno) é provavelmente benéfica.
NOLVADEX (citrato de tamoxifeno) reduz a ocorrência de câncer de mama contralateral em pacientes que recebem terapia adjuvante de NOLVADEX (citrato de tamoxifeno) para câncer de mama.
Carcinoma Ductal in Situ (CDIS)
Em mulheres com CDIS, após cirurgia de mama e radioterapia, NOLVADEX (citrato de tamoxifeno) é indicado para reduzir o risco de câncer de mama invasivo (ver AVISO EM CAIXA no início da etiqueta). A decisão sobre a terapia com NOLVADEX (citrato de tamoxifeno) para a redução da incidência de câncer de mama deve ser baseada em uma avaliação individual dos benefícios e riscos da terapia com NOLVADEX (citrato de tamoxifeno).
Os dados atuais de ensaios clínicos suportam cinco anos de terapia adjuvante NOLVADEX (citrato de tamoxifeno) para pacientes com câncer de mama.
Redução da incidência de câncer de mama em mulheres de alto risco
NOLVADEX (citrato de tamoxifeno) é indicado para reduzir a incidência de câncer de mama em mulheres com alto risco de câncer de mama. Esse efeito foi demonstrado em um estudo de 5 anos de duração planejada com acompanhamento médio de 4,2 anos. Vinte e cinco por cento dos participantes receberam a droga por 5 anos. Os efeitos a longo prazo não são conhecidos. Neste estudo, não houve impacto do tamoxifeno na mortalidade geral ou relacionada ao câncer de mama (ver AVISO EM CAIXA no início da etiqueta).
NOLVADEX (citrato de tamoxifeno) é indicado apenas para mulheres de alto risco. “Alto risco” é definido como mulheres com pelo menos 35 anos de idade com risco previsto de câncer de mama em 5 anos ≥ 1,67%, conforme calculado pelo Modelo Gail.
Exemplos de combinações de fatores que predizem um risco de 5 anos ≥ 1,67% são:
Idade igual ou superior a 35 anos e qualquer uma das seguintes combinações de fatores:
- Um familiar de primeiro grau com história de câncer de mama, 2 ou mais biópsias benignas e história de biópsia de mama mostrando hiperplasia atípica; ou
- Pelo menos 2 parentes de primeiro grau com histórico de câncer de mama e histórico pessoal de pelo menos uma biópsia de mama; ou
- LCIS
Idade igual ou superior a 40 anos e qualquer uma das seguintes combinações de fatores:
- Um parente de primeiro grau com história de câncer de mama, 2 ou mais biópsias benignas, idade do primeiro nascido vivo de 25 anos ou mais e idade da menarca de 11 anos ou menos; ou
- Pelo menos 2 parentes de primeiro grau com histórico de câncer de mama e idade do primeiro nascido vivo de 19 anos ou menos; ou
- Um parente de primeiro grau com história de câncer de mama e história pessoal de biópsia de mama mostrando hiperplasia atípica.
Idade igual ou superior a 45 anos e qualquer uma das seguintes combinações de fatores:
- Pelo menos 2 parentes de primeiro grau com histórico de câncer de mama e idade do primeiro nascido vivo de 24 anos ou menos; ou
- Um parente de primeiro grau com história de câncer de mama com história pessoal de biópsia benigna da mama, idade na menarca de 11 anos ou menos e idade do primeiro nascido vivo de 20 anos ou mais.
Idade igual ou superior a 50 anos e qualquer uma das seguintes combinações de fatores:
- Pelo menos 2 parentes de primeiro grau com histórico de câncer de mama; ou
- História de uma biópsia de mama mostrando hiperplasia atípica e idade do primeiro nascido vivo de 30 anos ou mais e idade da menarca de 11 anos ou menos; ou
- História de pelo menos duas biópsias de mama com história de hiperplasia atípica e idade ao primeiro nascido vivo de 30 anos ou mais.
Idade igual ou superior a 55 anos e qualquer uma das seguintes combinações de fatores:
- Um parente de primeiro grau com história de câncer de mama com história pessoal de biópsia benigna da mama e idade na menarca de 11 anos ou menos; ou
- História de pelo menos 2 biópsias de mama com história de hiperplasia atípica e idade no primeiro nascimento vivo de 20 anos ou mais.
60 anos ou mais e:
- Risco previsto de 5 anos de câncer de mama ≥ 1,67%, calculado pelo Modelo de Gail.
Para mulheres cujos fatores de risco não estão descritos nos exemplos acima, o Modelo Gail é necessário para estimar o risco absoluto de câncer de mama. Os profissionais de saúde podem obter uma ferramenta de avaliação de risco do modelo Gail ligando para 1-800-544-2007.
Não há dados suficientes disponíveis sobre o efeito de NOLVADEX (citrato de tamoxifeno) na incidência de câncer de mama em mulheres com mutações hereditárias (BRCA1, BRCA2) para poder fazer recomendações específicas sobre a eficácia de NOLVADEX (citrato de tamoxifeno) nesses pacientes.
Após uma avaliação do risco de desenvolver câncer de mama, a decisão sobre a terapia com NOLVADEX (citrato de tamoxifeno) para a redução da incidência de câncer de mama deve ser baseada em uma avaliação individual dos benefícios e riscos da terapia com NOLVADEX (citrato de tamoxifeno). No estudo NSABP P-1, o tratamento com NOLVADEX (citrato de tamoxifeno) reduziu o risco de desenvolver câncer de mama durante o período de acompanhamento do estudo, mas não eliminou o risco de câncer de mama (consulte a Tabela 3 em FARMACOLOGIA CLÍNICA ).
DOSAGEM E ADMINISTRAÇÃO
Para pacientes com câncer de mama, a dose diária recomendada é de 20-40 mg. Doses superiores a 20 mg por dia devem ser administradas em doses divididas (manhã e noite).
Em três estudos adjuvantes de agente único em mulheres, um comprimido de 10 mg de NOLVADEX (citrato de tamoxifeno) foi administrado duas (ECOG e NATO) ou três (Toronto) vezes ao dia durante dois anos. No estudo adjuvante NSABP B-14 em mulheres com câncer de mama com linfonodo negativo, um comprimido de 10 mg de NOLVADEX (citrato de tamoxifeno) foi administrado duas vezes ao dia por pelo menos 5 anos. Os resultados do estudo B-14 sugerem que a continuação da terapia além de cinco anos não oferece benefícios adicionais (ver FARMACOLOGIA CLÍNICA ). Na visão geral da EBCTCG de 1995, a redução na recorrência e mortalidade foi maior naqueles estudos que usaram tamoxifeno por cerca de 5 anos do que naqueles que usaram tamoxifeno por um período mais curto de terapia. Não houve indicação de que doses superiores a 20 mg por dia fossem mais eficazes. Os dados atuais de ensaios clínicos suportam 5 anos de terapia adjuvante NOLVADEX (citrato de tamoxifeno) para pacientes com câncer de mama.
Carcinoma Ductal in Situ (CDIS)
A dose recomendada é NOLVADEX (citrato de tamoxifeno) 20 mg por dia durante 5 anos.
Redução da incidência de câncer de mama em mulheres de alto risco
dose recomendada é NOLVADEX (citrato de tamoxifeno) 20 mg por dia durante 5 anos. Não há dados para apoiar o uso de NOLVADEX (citrato de tamoxifeno) além de 5 anos (consulte FARMACOLOGIA CLÍNICA-Estudos Clínicos - Redução da Incidência de Câncer de Mama em Mulheres de Alto Risco ).
COMO FORNECIDO
Comprimidos de 10 mg contendo tamoxifeno como citrato em uma quantidade equivalente a 10 mg de tamoxifeno (comprimido branco redondo, biconvexo, não revestido, identificado com NOLVADEX (citrato de tamoxifeno) 600 gravado em um lado e um camafeu gravado no outro lado) são fornecidos em frascos de 60 comprimidos. NDC 0310-0600-60.
Comprimidos de 20 mg contendo tamoxifeno como citrato em uma quantidade equivalente a 20 mg de tamoxifeno (comprimido branco redondo, biconvexo, não revestido, identificado com NOLVADEX (citrato de tamoxifeno) 604 gravado em um lado e um camafeu gravado no outro lado) são fornecidos em frascos de 30 comprimidos. NDC 0310-0604-30.
Armazenar em temperatura ambiente controlada, 20-25°C (68-77°F) [ver USP]. Dispensar em um recipiente bem fechado e resistente à luz.
*Coumadin® é uma marca registrada da Bristol-Myers Squibb Pharmaceuticals. Todas as outras marcas registradas são propriedade do grupo AstraZeneca, AstraZeneca Pharmaceuticals LP Wilmington, Delaware 19850-5437. Rev. 27-09-05. Data de revisão da FDA: 09/03/2006
EFEITOS COLATERAIS
As reações adversas ao NOLVADEX (citrato de tamoxifeno) são relativamente leves e raramente graves o suficiente para exigir a descontinuação do tratamento em pacientes com câncer de mama.
Estudos clínicos contínuos resultaram em mais informações que indicam melhor a incidência de reações adversas com NOLVADEX (citrato de tamoxifeno) em comparação com placebo.
Câncer de mama metastático
Ocorreu aumento da dor óssea e tumoral e, também, exacerbação local da doença, que às vezes está associada a uma boa resposta tumoral. Pacientes com dor óssea aumentada podem necessitar de analgésicos adicionais. Pacientes com doença de tecidos moles podem ter aumentos súbitos no tamanho de lesões preexistentes, às vezes associados a eritema acentuado dentro e ao redor das lesões e/ou ao desenvolvimento de novas lesões. Quando ocorrem, a dor óssea ou a exacerbação da doença são observadas logo após o início do NOLVADEX (citrato de tamoxifeno) e geralmente desaparecem rapidamente.
Em pacientes tratados com NOLVADEX (citrato de tamoxifeno) para câncer de mama metastático, a reação adversa mais frequente ao NOLVADEX (citrato de tamoxifeno) são ondas de calor.
Outras reações adversas observadas com pouca frequência são hipercalcemia, edema periférico, desgosto por comida, prurido vulvar, depressão, tontura, tontura, dor de cabeça, queda de cabelo e/ou perda parcial de cabelo e secura vaginal.
Mulheres na pré-menopausa
A tabela a seguir resume a incidência de reações adversas relatadas com uma frequência de 2% ou mais em ensaios clínicos (Ingle, Pritchard, Buchanan) que compararam a terapia com NOLVADEX (citrato de tamoxifeno) à ablação ovariana em pacientes na pré-menopausa com câncer de mama metastático.
Câncer de mama masculino
NOLVADEX (citrato de tamoxifeno) é bem tolerado em homens com câncer de mama. Relatos da literatura e relatos de casos sugerem que o perfil de segurança de NOLVADEX (citrato de tamoxifeno) em homens é semelhante ao observado em mulheres. Perda de libido e impotência resultaram na descontinuação da terapia com tamoxifeno em pacientes do sexo masculino. Além disso, em machos oligospérmicos tratados com tamoxifeno, os níveis de LH, FSH, testosterona e estrogênio estavam elevados. Não foram relatadas alterações clínicas significativas.
Câncer de Mama Adjuvante
No estudo NSABP B-14, mulheres com câncer de mama com nódulo axilar negativo foram randomizadas para 5 anos de NOLVADEX (citrato de tamoxifeno) 20 mg/dia ou placebo após a cirurgia primária. Os efeitos adversos relatados estão tabulados abaixo (acompanhamento médio de aproximadamente 6,8 anos) mostrando eventos adversos mais comuns com NOLVADEX (citrato de tamoxifeno) do que com placebo. A incidência de ondas de calor (64% vs. 48%), corrimento vaginal (30% vs. 15%) e menstruação irregular (25% vs. 19%) foram maiores com NOLVADEX (citrato de tamoxifeno) em comparação com placebo. Todos os outros efeitos adversos ocorreram com frequência semelhante nos 2 grupos de tratamento, com exceção de eventos trombóticos; uma incidência maior foi observada em pacientes tratados com NOLVADEX (citrato de tamoxifeno) (até 5 anos, 1,7% vs. 0,4%). Dois dos pacientes tratados com NOLVADEX (citrato de tamoxifeno) que apresentaram eventos trombóticos morreram.
No estudo adjuvante de câncer de mama do Eastern Cooperative Oncology Group (ECOG), NOLVADEX (citrato de tamoxifeno) ou placebo foi administrado por 2 anos a mulheres após a mastectomia. Quando comparado ao placebo, NOLVADEX (citrato de tamoxifeno) mostrou uma incidência significativamente maior de ondas de calor (19% vs. 8% para placebo). A incidência de todas as outras reações adversas foi semelhante nos 2 grupos de tratamento, com exceção da trombocitopenia, onde a incidência de NOLVADEX (citrato de tamoxifeno) foi de 10% versus 3% para placebo, uma observação de significância estatística limítrofe.
Em outros estudos adjuvantes, Toronto e NOLVADEX (citrato de tamoxifeno) Adjuvant Trial Organization (NATO), as mulheres receberam NOLVADEX (citrato de tamoxifeno) ou nenhuma terapia. No estudo de Toronto, ondas de calor foram observadas em 29% dos pacientes para NOLVADEX (citrato de tamoxifeno) versus 1% no grupo não tratado. No estudo da OTAN, ondas de calor e sangramento vaginal foram relatados em 2,8% e 2,0% das mulheres, respectivamente, para NOLVADEX (citrato de tamoxifeno) versus 0,2% para cada no grupo não tratado.
Ensaio Adjuvante Anastrozol - Estudo de Anastrozol em comparação com NOLVADEX (citrato de Tamoxifeno) para Tratamento Adjuvante de Câncer de Mama Inicial (Vejo FARMACOLOGIA CLÍNICA - Estudos clínicos).
Em um acompanhamento médio de 33 meses, a combinação de anastrozol e NOLVADEX (citrato de tamoxifeno) não demonstrou nenhum benefício de eficácia quando comparado à terapia com NOLVADEX (citrato de tamoxifeno) administrada isoladamente em todos os pacientes, bem como na subpopulação positiva para receptores hormonais. Este braço de tratamento foi descontinuado do estudo. A duração mediana do tratamento adjuvante para avaliação de segurança foi de 59,8 meses e 59,6 meses para pacientes que receberam anastrozol 1 mg e NOLVADEX (citrato de tamoxifeno) 20 mg, respectivamente.
Os eventos adversos que ocorrem com incidência de pelo menos 5% em qualquer grupo de tratamento durante o tratamento ou dentro de 14 dias após o término do tratamento são apresentados na tabela a seguir.
Eventos adversos ocorrendo com incidência de pelo menos 5% em qualquer grupo de tratamento durante o tratamento ou dentro de 14 dias após o término do tratamento
Certos eventos adversos e combinações de eventos adversos foram especificados prospectivamente para análise, com base nas propriedades farmacológicas conhecidas e perfis de efeitos colaterais dos dois medicamentos (consulte a tabela a seguir).
Número (%) de pacientes com evento adverso pré-especificado no estudo adjuvante de anastrozol1
Os pacientes que receberam anastrozol tiveram um aumento nos distúrbios articulares (incluindo artrite, artrose e artralgia) em comparação com os pacientes que receberam NOLVADEX (citrato de tamoxifeno). Os pacientes que receberam anastrozol tiveram um aumento na incidência de todas as fraturas (especificamente fraturas da coluna, quadril e punho) [315 (10%)] em comparação com os pacientes que receberam NOLVADEX (citrato de tamoxifeno) [209 (7%)]. As pacientes que receberam anastrozol tiveram uma diminuição nas ondas de calor, sangramento vaginal, corrimento vaginal, câncer de endométrio, eventos tromboembólicos venosos e eventos cerebrovasculares isquêmicos em comparação com pacientes que receberam NOLVADEX (citrato de tamoxifeno).
Os pacientes que receberam NOLVADEX (citrato de tamoxifeno) tiveram uma diminuição da hipercolesterolemia (108 [3,5%]) em comparação com os pacientes que receberam anastrozol (278 [9%]). Angina pectoris foi relatada em 71 [2,3%] pacientes no braço de anastrozol e 51 [1,6%] pacientes no braço de NOLVADEX (citrato de tamoxifeno); infarto do miocárdio foi relatado em 37 [1,2%] pacientes no braço anastrozol e em 34 [1,1%] pacientes no braço NOLVADEX (citrato de tamoxifeno).
Os resultados do subestudo ósseo do ensaio adjuvante, aos 12 e 24 meses, demonstraram que os pacientes que receberam anastrozol tiveram uma diminuição média na coluna lombar e na densidade mineral óssea total do quadril (DMO) em comparação com a linha de base. Os pacientes que receberam NOLVADEX (citrato de tamoxifeno) tiveram um aumento médio na coluna lombar e na DMO total do quadril em comparação com a linha de base.
Carcinoma Ductal in Situ (CDIS)
O tipo e a frequência de eventos adversos no estudo NSABP B-24 foram consistentes com os observados em outros estudos adjuvantes conduzidos com NOLVADEX (citrato de tamoxifeno).
Redução da incidência de câncer de mama em mulheres de alto risco
No ensaio NSABP P-1, houve um aumento de cinco efeitos adversos graves no grupo NOLVADEX (citrato de tamoxifeno): câncer endometrial (33 casos no grupo NOLVADEX (citrato de tamoxifeno) versus 14 no grupo placebo); embolia pulmonar (18 casos no grupo NOLVADEX (citrato de tamoxifeno) vs. 6 no grupo placebo); trombose venosa profunda (30 casos no grupo NOLVADEX (citrato de tamoxifeno) vs. 19 no grupo placebo); acidente vascular cerebral (34 casos no grupo NOLVADEX (citrato de tamoxifeno) vs. 24 no grupo placebo); formação de catarata (540 casos no grupo NOLVADEX (citrato de tamoxifeno) versus 483 no grupo placebo) e cirurgia de catarata (101 casos no grupo NOLVADEX (citrato de tamoxifeno) versus 63 no grupo placebo) (Consulte AVISOS e Tabela 3 em FARMACOLOGIA CLÍNICA ).
A tabela a seguir apresenta os eventos adversos observados no NSABP P-1 por braço de tratamento. Apenas os eventos adversos mais comuns com NOLVADEX (citrato de tamoxifeno) do que com placebo são mostrados.
No estudo NSABP P-1, 15,0% e 9,7% dos participantes que receberam NOLVADEX (citrato de tamoxifeno) e terapia com placebo, respectivamente, se retiraram do estudo por razões médicas. A seguir estão as razões médicas para a retirada de NOLVADEX (citrato de tamoxifeno) e terapia com placebo, respectivamente: Ondas de calor (3,1% vs. 1,5%) e Corrimento Vaginal (0,5% vs. 0,1%).
No estudo NSABP P-1, 8,7% e 9,6% dos participantes que receberam NOLVADEX (citrato de tamoxifeno) e terapia com placebo, respectivamente, desistiram por razões não médicas.
No estudo NSABP P-1, ondas de calor de qualquer gravidade ocorreram em 68% das mulheres que receberam placebo e em 80% das mulheres que receberam NOLVADEX (citrato de tamoxifeno). Ondas de calor graves ocorreram em 28% das mulheres que receberam placebo e 45% das mulheres que receberam NOLVADEX (citrato de tamoxifeno). Corrimento vaginal ocorreu em 35% e 55% das mulheres que receberam placebo e NOLVADEX (citrato de tamoxifeno), respectivamente; e foi grave em 4,5% e 12,3%, respectivamente. Não houve diferença na incidência de sangramento vaginal entre os braços de tratamento.
Pacientes Pediátricos - Síndrome de McCune-Albright
O volume uterino médio aumentou após 6 meses de tratamento e dobrou no final do estudo de um ano. Uma relação causal não foi estabelecida; no entanto, como um aumento na incidência de adenocarcinoma endometrial e sarcoma uterino foi observado em adultos tratados com NOLVADEX (ver AVISO EM CAIXA ), recomenda-se o monitoramento contínuo de pacientes McCune-Albright tratados com NOLVADEX (citrato de tamoxifeno) para efeitos a longo prazo. A segurança e eficácia de NOLVADEX (citrato de tamoxifeno) para meninas de dois a 10 anos com síndrome de McCune-Albright e puberdade precoce não foram estudadas além de um ano de tratamento. Os efeitos a longo prazo da terapia com NOLVADEX (citrato de tamoxifeno) em meninas não foram estabelecidos.
Experiência pós-comercialização
As reações adversas relatadas com menos frequência são sangramento vaginal, corrimento vaginal, irregularidades menstruais, erupções cutâneas e dores de cabeça. Geralmente, estes não foram de gravidade suficiente para exigir redução da dose ou descontinuação do tratamento. Relatos muito raros de eritema multiforme, síndrome de Stevens-Johnson, penfigoide bolhoso, pneumonite intersticial e relatos raros de reações de hipersensibilidade, incluindo angioedema, foram relatados com a terapia com NOLVADEX (citrato de tamoxifeno). Em alguns desses casos, o tempo de início foi superior a um ano. Raramente, a elevação dos níveis séricos de triglicerídeos, em alguns casos com pancreatite, pode estar associada ao uso de NOLVADEX (citrato de tamoxifeno) (ver PRECAUÇÕES - Interações Medicamentosas/Testes Laboratoriais seção).
INTERAÇÕES MEDICAMENTOSAS
Quando NOLVADEX (citrato de tamoxifeno) é usado em combinação com anticoagulantes do tipo cumarínico, pode ocorrer um aumento significativo no efeito anticoagulante. Quando existe tal coadministração, recomenda-se a monitorização cuidadosa do tempo de protrombina do doente.
No estudo NSABP P-1, as mulheres que necessitaram de anticoagulantes do tipo cumarínico por qualquer motivo não foram elegíveis para participação no estudo (ver CONTRA-INDICAÇÕES ).
Existe um risco aumentado de ocorrência de eventos tromboembólicos quando agentes citotóxicos são usados em combinação com NOLVADEX (citrato de tamoxifeno).
tamoxifeno reduziu as concentrações plasmáticas de letrozol em 37%. O efeito do tamoxifeno no metabolismo e excreção de outras drogas antineoplásicas, como a ciclofosfamida e outras drogas que requerem oxidases de função mista para ativação, não é conhecido. Demonstrou-se que as concentrações plasmáticas de tamoxifeno e N-desmetil tamoxifeno são reduzidas quando coadministrados com rifampicina ou aminoglutetimida. A indução do metabolismo mediado pelo CYP3A4 é considerada o mecanismo pelo qual essas reduções ocorrem; outros agentes indutores de CYP3A4 não foram estudados para confirmar este efeito.
Um paciente recebendo NOLVADEX (citrato de tamoxifeno) com fenobarbital concomitante exibiu um nível sérico de tamoxifeno em estado de equilíbrio inferior ao observado para outros pacientes (ou seja, 26 ng/mL versus valor médio de 122 ng/mL). No entanto, o significado clínico deste achado não é conhecido. A rifampicina induziu o metabolismo do tamoxifeno e reduziu significativamente as concentrações plasmáticas de tamoxifeno em 10 pacientes. A aminoglutetimida reduz as concentrações plasmáticas de tamoxifeno e N-desmetil tamoxifeno. A medroxiprogesterona reduz as concentrações plasmáticas de N-desmetil, mas não de tamoxifeno.
A terapia concomitante com bromocriptina demonstrou elevar o tamoxifeno sérico e o N-desmetil tamoxifeno.
Com base nos resultados clínicos e farmacocinéticos do estudo adjuvante com anastrozol, NOLVADEX (citrato de tamoxifeno) não deve ser administrado com anastrozol (ver FARMACOLOGIA CLÍNICA - Interações Medicamentosas seção).
Interações de testes de drogas/laboratórios
Durante a vigilância pós-comercialização, foram relatadas elevações de T4 em algumas pacientes na pós-menopausa, o que pode ser explicado por aumentos na globulina de ligação à tireoide. Essas elevações não foram acompanhadas de hipertireoidismo clínico.
Variações no índice cariopicnótico em esfregaços vaginais e vários graus de efeito de estrogênio em esfregaços de Papanicolaou foram raramente observados em pacientes na pós-menopausa que receberam NOLVADEX (citrato de tamoxifeno).
Na experiência pós-comercialização com NOLVADEX (citrato de tamoxifeno), foram relatados casos infrequentes de hiperlipidemias. O monitoramento periódico de triglicerídeos e colesterol plasmáticos pode ser indicado em pacientes com hiperlipidemias pré-existentes (ver REAÇÕES ADVERSAS-Experiência pós-comercialização seção).
AVISOS
Efeitos em pacientes com câncer de mama metastático
Assim como com outras terapias hormonais aditivas (estrogênios e andrógenos), hipercalcemia foi relatada em alguns pacientes com câncer de mama com metástases ósseas poucas semanas após o início do tratamento com NOLVADEX (citrato de tamoxifeno). Se ocorrer hipercalcemia, medidas apropriadas devem ser tomadas e, se grave, NOLVADEX (citrato de tamoxifeno) deve ser descontinuado.
Efeitos sobre o Câncer Útero-Endométrio e Sarcoma Uterino
Uma incidência aumentada de malignidades uterinas foi relatada em associação com o tratamento com NOLVADEX (citrato de tamoxifeno). O mecanismo subjacente é desconhecido, mas pode estar relacionado ao efeito semelhante ao estrogênio do NOLVADEX (citrato de tamoxifeno). A maioria das malignidades uterinas observadas em associação com NOLVADEX (citrato de tamoxifeno) são classificadas como adenocarcinoma do endométrio. No entanto, sarcomas uterinos raros, incluindo tumores müllerianos mistos malignos (MMMT), também foram relatados. O sarcoma uterino geralmente está associado a um estágio FIGO mais alto (III/IV) no diagnóstico, pior prognóstico e menor sobrevida. Foi relatado que o sarcoma uterino ocorre com mais frequência entre as usuárias de longo prazo (≥ 2 anos) de NOLVADEX (citrato de tamoxifeno) do que as não usuárias. Algumas das malignidades uterinas (carcinoma endometrial ou sarcoma uterino) foram fatais.
No estudo NSABP P-1, entre os participantes randomizados para NOLVADEX (citrato de tamoxifeno), houve um aumento estatisticamente significativo na incidência de câncer endometrial (33 casos de câncer endometrial invasivo, em comparação com 14 casos entre os participantes randomizados para placebo (RR = 2,48 , 95% CI: 1,27-4,92). Os 33 casos em participantes que receberam NOLVADEX (citrato de tamoxifeno) foram FIGO Estágio I, incluindo 20 IA, 12 IB e 1 IC adenocarcinomas endometriais. Em participantes randomizados para placebo, 13 eram FIGO Estágio I (8 IA e 5 IB) e 1 era FIGO Estágio IV. Cinco mulheres em NOLVADEX (citrato de tamoxifeno) e 1 em placebo receberam radioterapia pós-operatória além da cirurgia. Esse aumento foi observado principalmente entre mulheres com pelo menos 50 anos de idade no tempo de randomização (26 casos de câncer de endométrio invasivo, em comparação com 6 casos entre participantes randomizados para placebo (RR = 4,50, IC 95%: 1,78-13,16). Entre mulheres ≤ 49 anos de idade no momento da randomização havia 7 casos de eu câncer endometrial invasivo, em comparação com 8 casos entre os participantes randomizados para placebo (RR = 0,94, IC 95%: 0,28-2,89). Se a idade no momento do diagnóstico for considerada, houve 4 casos de câncer endometrial entre os participantes ≤ 49 randomizados para NOLVADEX (citrato de tamoxifeno) em comparação com 2 entre os participantes randomizados para placebo (RR = 2,21, IC 95%: 0,4-12,0). Para mulheres ≥ 50 no momento do diagnóstico, houve 29 casos entre os participantes randomizados para NOLVADEX (citrato de tamoxifeno) em comparação com 12 entre as mulheres que receberam placebo (RR = 2,5, IC 95%: 1,3-4,9). As razões de risco foram semelhantes nos dois grupos, embora menos eventos tenham ocorrido em mulheres mais jovens. A maioria (29 de 33 casos no grupo NOLVADEX (citrato de tamoxifeno)) de câncer de endométrio foi diagnosticada em mulheres sintomáticas, embora 5 de 33 casos no grupo NOLVADEX (citrato de tamoxifeno) tenham ocorrido em mulheres assintomáticas. Entre as mulheres que receberam NOLVADEX (citrato de tamoxifeno), os eventos apareceram entre 1 e 61 meses (média = 32 meses) desde o início do tratamento.
Em uma revisão atualizada de dados de longo prazo (a duração média do acompanhamento total é de 6,9 anos, incluindo acompanhamento cego) em 8.306 mulheres com útero intacto na randomização no ensaio de redução de risco NSABP P-1, a incidência de ambos adenocarcinomas e sarcomas uterinos raros foi aumentado em mulheres tomando NOLVADEX (citrato de tamoxifeno). Durante o acompanhamento cego, houve 36 casos de adenocarcinoma endometrial FIGO Estágio I (22 foram FIGO Estágio IA, 13 IB e 1 IC) em mulheres que receberam NOLVADEX (citrato de tamoxifeno) e 15 casos em mulheres que receberam placebo [14 foram FIGO Stage I (9 IA e 5 IB) e 1 caso era FIGO Estágio IV]. Das pacientes que receberam NOLVADEX (citrato de tamoxifeno) que desenvolveram câncer de endométrio, uma com estágio IA e 4 com câncer de estágio IB receberam radioterapia. No grupo placebo, um paciente com câncer FIGO Estágio 1B recebeu radioterapia e o paciente com câncer FIGO Estágio IVB recebeu quimioterapia e terapia hormonal. Durante o acompanhamento total, adenocarcinoma endometrial foi relatado em 53 mulheres randomizadas para NOLVADEX (citrato de tamoxifeno) (30 casos de FIGO em Estágio IA, 20 em Estágio IB, 1 em Estágio IC e 2 em Estágio IIIC) e 17 mulheres randomizadas para placebo (9 casos foram FIGO Estágio IA, 6 foram Estágio IB, 1 foi Estágio IIIC e 1 foi Estágio IVB) (incidência por 1.000 mulheres-ano de 2,20 e 0,71, respectivamente). Alguns pacientes receberam radioterapia pós-operatória, além da cirurgia. Sarcomas uterinos foram relatados em 4 mulheres randomizadas para NOLVADEX (citrato de tamoxifeno) (1 foi FIGO IA, 1 foi FIGO IB, 1 foi FIGO IIA e 1 foi FIGO IIIC) e um paciente randomizado para placebo (FIGO 1A); incidência por 1.000 mulheres-ano de 0,17 e 0,04, respectivamente. Dos pacientes randomizados para NOLVADEX (citrato de tamoxifeno), os casos FIGO IA e IB foram MMMT e sarcoma, respectivamente; o FIGO II era um MMMT; e o FIGO III era um sarcoma; e um paciente randomizado para placebo tinha MMMT. Um aumento semelhante na incidência de adenocarcinoma endometrial e sarcoma uterino foi observado entre as mulheres que receberam NOLVADEX (citrato de tamoxifeno) em cinco outros ensaios clínicos NSABP.
Qualquer paciente recebendo ou que tenha recebido anteriormente NOLVADEX (citrato de tamoxifeno) que relatar sangramento vaginal anormal deve ser imediatamente avaliada. Pacientes recebendo ou que receberam anteriormente NOLVADEX (citrato de tamoxifeno) devem fazer exames ginecológicos anuais e devem informar imediatamente seus médicos se apresentarem quaisquer sintomas ginecológicos anormais, por exemplo, irregularidades menstruais, sangramento vaginal anormal, alterações no corrimento vaginal ou dor pélvica ou pressão.
No estudo P-1, a amostragem endometrial não alterou a taxa de detecção de câncer endometrial em comparação com mulheres que não foram submetidas a amostragem endometrial (0,6% com amostragem, 0,5% sem amostragem) para mulheres com útero intacto. Não há dados que sugiram que a amostragem endometrial de rotina em mulheres assintomáticas tomando NOLVADEX (citrato de tamoxifeno) para reduzir a incidência de câncer de mama seria benéfica.
Efeitos não malignos no útero
Uma incidência aumentada de alterações endometriais, incluindo hiperplasia e pólipos, foi relatada em associação com o tratamento com NOLVADEX (citrato de tamoxifeno). A incidência e o padrão desse aumento sugerem que o mecanismo subjacente está relacionado às propriedades estrogênicas do NOLVADEX (citrato de tamoxifeno) .
Houve alguns relatos de endometriose e miomas uterinos em mulheres recebendo NOLVADEX (citrato de tamoxifeno). O mecanismo subjacente pode ser devido ao efeito estrogênico parcial de NOLVADEX (citrato de tamoxifeno). Cistos ovarianos também foram observados em um pequeno número de pacientes na pré-menopausa com câncer de mama avançado que foram tratadas com NOLVADEX (citrato de tamoxifeno).
Foi relatado que NOLVADEX (citrato de tamoxifeno) causa irregularidade menstrual ou amenorreia.
Efeitos tromboembólicos de NOLVADEX (citrato de tamoxifeno)
Há evidências de aumento da incidência de eventos tromboembólicos, incluindo trombose venosa profunda e embolia pulmonar, durante a terapia com NOLVADEX (citrato de tamoxifeno). Quando NOLVADEX (citrato de tamoxifeno) é coadministrado com quimioterapia, pode haver um aumento adicional na incidência de efeitos tromboembólicos. Para o tratamento do câncer de mama, os riscos e benefícios de NOLVADEX (citrato de tamoxifeno) devem ser cuidadosamente considerados em mulheres com histórico de eventos tromboembólicos. Em um pequeno subestudo (N = 81) do estudo NSABP P-1, parece não haver benefício em rastrear mulheres para mutações do Fator V Leiden e Protrombina G20210A como meio de identificar aqueles que podem não ser candidatos apropriados para NOLVADEX (tamoxifeno citrato) terapia.
Os dados do estudo NSABP P-1 mostram que os participantes que receberam NOLVADEX (citrato de tamoxifeno) sem histórico de embolia pulmonar (EP) tiveram um aumento estatisticamente significativo de embolia pulmonar (18-NOLVADEX (citrato de tamoxifeno), 6-placebo, RR = 3,01 , 95% CI: 1,15-9,27). Três dos êmbolos pulmonares, todos no braço NOLVADEX (citrato de tamoxifeno), foram fatais. Oitenta e sete por cento dos casos de embolia pulmonar ocorreram em mulheres com pelo menos 50 anos de idade na randomização. Entre as mulheres que receberam NOLVADEX (citrato de tamoxifeno), os eventos apareceram entre 2 e 60 meses (média = 27 meses) desde o início do tratamento.
Nesta mesma população, um aumento não estatisticamente significativo na trombose venosa profunda (TVP) foi observado no grupo NOLVADEX (citrato de tamoxifeno) (30-NOLVADEX (citrato de tamoxifeno), 19-placebo; RR = 1,59, IC 95%: 0,86 -2,98). O mesmo aumento no risco relativo foi observado em mulheres ≤ 49 e em mulheres ≥ 50, embora menos eventos tenham ocorrido em mulheres mais jovens. Mulheres com eventos tromboembólicos estavam em risco de um segundo evento relacionado (7 de 25 mulheres em placebo, 5 de 48 mulheres em NOLVADEX (citrato de tamoxifeno)) e estavam em risco de complicações do evento e seu tratamento (0/25 em placebo, 4/48 em NOLVADEX (citrato de tamoxifeno)). Entre as mulheres que receberam NOLVADEX (citrato de tamoxifeno), eventos de trombose venosa profunda ocorreram entre 2 e 57 meses (média = 19 meses) desde o início do tratamento.
Houve um aumento não estatisticamente significativo no acidente vascular cerebral entre os pacientes randomizados para NOLVADEX (citrato de tamoxifeno) (24-Placebo; 34-NOLVADEX (citrato de tamoxifeno); RR = 1,42; IC 95% 0,82-2,51). Seis dos 24 AVCs no grupo placebo foram considerados de origem hemorrágica e 10 dos 34 AVCs no grupo NOLVADEX (citrato de tamoxifeno) foram categorizados como hemorrágicos. Dezessete dos 34 AVCs no grupo NOLVADEX (citrato de tamoxifeno) foram considerados oclusivos e 7 foram considerados de etiologia desconhecida. Quatorze dos 24 AVCs no braço placebo foram relatados como oclusivos e 4 de etiologia desconhecida. Entre esses acidentes vasculares cerebrais, 3 acidentes vasculares cerebrais no grupo placebo e 4 acidentes vasculares cerebrais no grupo NOLVADEX (citrato de tamoxifeno) foram fatais. Oitenta e oito por cento dos AVCs ocorreram em mulheres com pelo menos 50 anos de idade no momento da randomização. Entre as mulheres que receberam NOLVADEX (citrato de tamoxifeno), os eventos ocorreram entre 1 e 63 meses (média = 30 meses) desde o início do tratamento.
Efeitos no fígado: câncer de fígado
No estudo sueco usando NOLVADEX adjuvante (citrato de tamoxifeno) 40 mg/dia por 2-5 anos, 3 casos de câncer de fígado foram relatados no grupo tratado com NOLVADEX (citrato de tamoxifeno) versus 1 caso no grupo de observação (ver PRECAUÇÕES - Carcinogênese ). Em outros ensaios clínicos avaliando NOLVADEX (citrato de tamoxifeno), nenhum caso de câncer de fígado foi relatado até o momento.
Um caso de câncer de fígado foi relatado em NSABP P-1 em um participante randomizado para NOLVADEX (citrato de tamoxifeno).
Efeitos no fígado: Efeitos não malignos
NOLVADEX (citrato de tamoxifeno) foi associado a alterações nos níveis de enzimas hepáticas e, em raras ocasiões, a um espectro de anormalidades hepáticas mais graves, incluindo fígado gorduroso, colestase, hepatite e necrose hepática. Alguns desses casos graves incluíram fatalidades. Na maioria dos casos relatados, a relação com NOLVADEX (citrato de tamoxifeno) é incerta. No entanto, algumas reexposições e desexposições positivas foram relatadas.
No ensaio NSABP P-1, foram observadas poucas alterações de grau 3-4 na função hepática (SGOT, SGPT, bilirrubina, fosfatase alcalina) (10 com placebo e 6 com NOLVADEX (citrato de tamoxifeno)). Os lipídios séricos não foram coletados sistematicamente.
Outros cânceres
Vários segundos tumores primários, ocorrendo em outros locais além do endométrio, foram relatados após o tratamento de câncer de mama com NOLVADEX (citrato de tamoxifeno) em ensaios clínicos. Os dados dos estudos NSABP B-14 e P-1 não mostram nenhum aumento em outros cânceres (não uterinos) entre as pacientes que receberam NOLVADEX (citrato de tamoxifeno). Se um risco aumentado para outros cânceres (não uterinos) está associado ao NOLVADEX (citrato de tamoxifeno) ainda é incerto e continua a ser avaliado.
Efeitos nos olhos
Distúrbios oculares, incluindo alterações da córnea, diminuição da percepção da visão de cores, trombose da veia da retina e retinopatia foram relatados em pacientes recebendo NOLVADEX (citrato de tamoxifeno). Uma incidência aumentada de catarata e a necessidade de cirurgia de catarata foram relatadas em pacientes recebendo NOLVADEX (citrato de tamoxifeno).
No estudo NSABP P-1, um risco aumentado de significância limítrofe de desenvolver catarata entre as mulheres sem catarata no início do estudo (540-NOLVADEX (citrato de tamoxifeno); 483-placebo; RR=1,13, IC 95%: 1,00-1,28) foi observado. Entre essas mesmas mulheres, NOLVADEX (citrato de tamoxifeno) foi associado a um risco aumentado de cirurgia de catarata (101-NOLVADEX (citrato de tamoxifeno); 63-placebo; RR = 1,62, IC 95% 1,18-2,22) (consulte a Tabela 3 em FARMACOLOGIA CLÍNICA ). Entre todas as mulheres do estudo (com ou sem catarata no início do estudo), NOLVADEX (citrato de tamoxifeno) foi associado a um risco aumentado de cirurgia de catarata (201-NOLVADEX (citrato de tamoxifeno); 129-placebo; RR=1,58, IC 95% 1,26-1,97). Exames oftalmológicos não foram necessários durante o estudo. Nenhuma outra conclusão sobre eventos oftálmicos sem catarata pode ser feita.
Gravidez Categoria D
NOLVADEX (citrato de tamoxifeno) pode causar dano fetal quando administrado a mulheres grávidas. As mulheres devem ser aconselhadas a não engravidar enquanto estiverem tomando NOLVADEX (citrato de tamoxifeno) ou dentro de 2 meses após a descontinuação de NOLVADEX (citrato de tamoxifeno) e devem usar medidas contraceptivas de barreira ou não hormonais se sexualmente ativas. Tamoxifeno não causa infertilidade, mesmo na presença de irregularidade menstrual. Efeitos nas funções reprodutivas são esperados das propriedades antiestrogênicas da droga. Em estudos reprodutivos em ratos em níveis de dose iguais ou inferiores à dose humana, foram observadas alterações esqueléticas não teratogênicas no desenvolvimento e foram consideradas reversíveis. Além disso, em estudos de fertilidade em ratos e em estudos de teratologia em coelhos com doses iguais ou inferiores às utilizadas em humanos, observou-se uma incidência mais baixa de implantação embrionária e uma incidência mais elevada de morte fetal ou crescimento in utero retardado, com comportamento de aprendizagem mais lento em alguns filhotes de ratos quando comparados a controles históricos. Vários saguis prenhes receberam doses de 10 mg/kg/dia (cerca de 2 vezes a dose máxima diária recomendada para humanos com base em mg/m²) durante a organogênese ou na última metade da gravidez. Não foram observadas deformações e, embora a dose tenha sido alta o suficiente para interromper a gestação em alguns animais, aqueles que mantiveram a gestação não apresentaram evidências de malformações teratogênicas.
Em modelos de roedores de desenvolvimento do trato reprodutivo fetal, o tamoxifeno (em doses de 0,002 a 2,4 vezes a dose máxima diária recomendada em humanos com base em mg/m²) causou alterações em ambos os sexos semelhantes às causadas por estradiol, etinilestradiol e dietilestilbestrol. Embora a relevância clínica dessas alterações seja desconhecida, algumas dessas alterações, especialmente a adenose vaginal, são semelhantes àquelas observadas em mulheres jovens que foram expostas ao dietilestilbestrol in utero e que têm um risco de 1 em 1.000 de desenvolver adenocarcinoma de células claras do útero. vagina ou colo do útero. Até o momento, a exposição in utero ao tamoxifeno não demonstrou causar adenose vaginal ou adenocarcinoma de células claras da vagina ou do colo do útero em mulheres jovens. No entanto, apenas um pequeno número de mulheres jovens foi exposto ao tamoxifeno no útero, e um número menor foi acompanhado por tempo suficiente (até 15-20 anos) para determinar se a neoplasia vaginal ou cervical pode ocorrer como resultado dessa exposição.
Não há estudos adequados e bem controlados de tamoxifeno em mulheres grávidas. Houve um pequeno número de relatos de sangramento vaginal, abortos espontâneos, defeitos congênitos e mortes fetais em mulheres grávidas. Se este medicamento for usado durante a gravidez, ou a paciente engravidar enquanto estiver tomando este medicamento, ou dentro de aproximadamente dois meses após a descontinuação da terapia, a paciente deve ser informada sobre os riscos potenciais para o feto, incluindo o risco potencial a longo prazo de um DES- como síndrome.
Redução da incidência de câncer de mama em mulheres de alto risco - Gravidez Categoria D
Para mulheres sexualmente ativas com potencial para engravidar, a terapia com NOLVADEX (citrato de tamoxifeno) deve ser iniciada durante a menstruação. Em mulheres com irregularidade menstrual, um B-HCG negativo imediatamente antes do início da terapia é suficiente (ver PRECAUÇÕES-INFORMAÇÕES PARA PACIENTES - Redução da incidência de câncer de mama em mulheres de alto risco ).
PRECAUÇÕES
Em geral
Diminuições na contagem de plaquetas, geralmente para 50.000-100.000/mm³, raramente inferiores, foram ocasionalmente relatadas em pacientes tomando NOLVADEX (citrato de tamoxifeno) para câncer de mama. Em pacientes com trombocitopenia significativa, episódios hemorrágicos raros ocorreram, mas é incerto se esses episódios são devidos à terapia com NOLVADEX (citrato de tamoxifeno). Foi observada leucopenia, algumas vezes em associação com anemia e/ou trombocitopenia. Houve relatos raros de neutropenia e pancitopenia em pacientes recebendo NOLVADEX (citrato de tamoxifeno); isso às vezes pode ser grave.
No estudo NSABP P-1, 6 mulheres em uso de NOLVADEX (citrato de tamoxifeno) e 2 em placebo experimentaram quedas de grau 3-4 na contagem de plaquetas (≤ 50.000/mm³).
Informações para Pacientes
Os pacientes devem ser instruídos a ler o Guia de Medicação fornecido conforme exigido por lei quando NOLVADEX 10mg é dispensado. O texto completo do Guia de Medicação é reimpresso no final deste documento.
Redução do câncer de mama invasivo e CDIS em mulheres com CDIS
Mulheres com CDIS tratadas com lumpectomia e radioterapia que estejam considerando NOLVADEX (citrato de tamoxifeno) para reduzir a incidência de um segundo evento de câncer de mama devem avaliar os riscos e benefícios da terapia, uma vez que o tratamento com NOLVADEX (citrato de tamoxifeno) diminuiu a incidência de câncer de mama invasivo câncer, mas não demonstrou afetar a sobrevida (consulte a Tabela 1 em FARMACOLOGIA CLÍNICA ).
Redução da incidência de câncer de mama em mulheres de alto risco
Mulheres com alto risco de câncer de mama podem considerar a terapia com NOLVADEX (citrato de tamoxifeno) para reduzir a incidência de câncer de mama. Se os benefícios do tratamento são considerados superiores aos riscos, depende do histórico de saúde pessoal da mulher e de como ela avalia os benefícios e os riscos. A terapia com NOLVADEX (citrato de tamoxifeno) para reduzir a incidência de câncer de mama pode, portanto, não ser apropriada para todas as mulheres com alto risco de câncer de mama. As mulheres que estão considerando a terapia com NOLVADEX (citrato de tamoxifeno) devem consultar seu profissional de saúde para uma avaliação dos potenciais benefícios e riscos antes de iniciar a terapia para redução da incidência de câncer de mama (ver Tabela 3 em FARMACOLOGIA CLÍNICA ). As mulheres devem entender que NOLVADEX (citrato de tamoxifeno) reduz a incidência de câncer de mama, mas pode não eliminar o risco. NOLVADEX (citrato de tamoxifeno) diminuiu a incidência de pequenos tumores positivos para receptores de estrogênio, mas não alterou a incidência de tumores negativos para receptores de estrogênio ou tumores maiores. Em mulheres com câncer de mama com alto risco de desenvolver um segundo câncer de mama, o tratamento com cerca de 5 anos de NOLVADEX (citrato de tamoxifeno) reduziu a taxa de incidência anual de um segundo câncer de mama em aproximadamente 50%.
Mulheres grávidas ou que planejam engravidar não devem tomar NOLVADEX (citrato de tamoxifeno) para reduzir o risco de câncer de mama. A contracepção não hormonal eficaz deve ser usada por todas as mulheres na pré-menopausa que estejam tomando NOLVADEX (citrato de tamoxifeno) e por aproximadamente dois meses após a descontinuação da terapia se forem sexualmente ativas. Tamoxifeno não causa infertilidade, mesmo na presença de irregularidade menstrual. Para mulheres sexualmente ativas com potencial para engravidar, a terapia com NOLVADEX (citrato de tamoxifeno) deve ser iniciada durante a menstruação. Em mulheres com irregularidade menstrual, um B-HCG negativo imediatamente antes do início da terapia é suficiente (ver ADVERTÊNCIAS - Gravidez Categoria D ).
Dois estudos europeus de tamoxifeno para reduzir o risco de câncer de mama foram conduzidos e não mostraram diferença no número de casos de câncer de mama entre os braços de tamoxifeno e placebo. Esses estudos tinham desenhos de ensaios que diferiam do NSABP P-1, eram menores do que NSABP P-1 e incluíam mulheres com menor risco de câncer de mama do que aquelas em P-1.
Monitoramento durante a terapia com NOLVADEX (citrato de tamoxifeno)
As mulheres que estão tomando ou que já tomaram NOLVADEX (citrato de tamoxifeno) devem ser instruídas a procurar atendimento médico imediato para novos nódulos mamários, sangramento vaginal, sintomas ginecológicos (irregularidades menstruais, alterações no corrimento vaginal ou dor ou pressão pélvica), sintomas de inchaço nas pernas ou sensibilidade, falta de ar inexplicável ou alterações na visão. As mulheres devem informar a todos os profissionais de saúde, independentemente do motivo da avaliação, que tomam NOLVADEX (citrato de tamoxifeno) .
As mulheres que tomam NOLVADEX (citrato de tamoxifeno) para reduzir a incidência de câncer de mama devem fazer um exame de mama, uma mamografia e um exame ginecológico antes do início da terapia. Esses estudos devem ser repetidos em intervalos regulares durante a terapia, de acordo com as boas práticas médicas. As mulheres que tomam NOLVADEX (citrato de tamoxifeno) como terapia adjuvante do câncer de mama devem seguir os mesmos procedimentos de monitoramento que as mulheres que tomam NOLVADEX (citrato de tamoxifeno) para reduzir a incidência de câncer de mama. As mulheres que tomam NOLVADEX (citrato de tamoxifeno) como tratamento para câncer de mama metastático devem revisar este plano de monitoramento com seu médico e selecionar as modalidades apropriadas e o cronograma de avaliação.
Testes laboratoriais
Devem ser obtidos hemogramas completos periódicos, incluindo contagem de plaquetas e testes periódicos de função hepática.
Durante o estudo ATAC, mais pacientes que receberam anastrozol apresentaram níveis séricos elevados de colesterol em comparação com os pacientes que receberam NOLVADEX (citrato de tamoxifeno) (9% versus 3,5%, respectivamente).
Carcinogênese
Um estudo convencional de carcinogênese em ratos com doses de 5, 20 e 35 mg/kg/dia (cerca de uma, três e sete vezes a dose máxima diária recomendada para humanos em uma base de mg/m²) administrada por gavagem oral por até 2 anos ) revelou um aumento significativo do carcinoma hepatocelular em todas as doses. A incidência desses tumores foi significativamente maior entre ratos administrados 20 ou 35 mg/kg/dia (69%) em comparação com aqueles administrados 5 mg/kg/dia (14%). Em um estudo separado, ratos receberam tamoxifeno na dose de 45 mg/kg/dia (cerca de nove vezes a dose máxima diária recomendada em humanos com base em mg/m²); neoplasia hepatocelular foi exibida em 3 a 6 meses.
Tumores ovarianos de células da granulosa e tumores testiculares de células intersticiais foram observados em dois estudos separados em camundongos. Os camundongos receberam as formas trans e racêmica de tamoxifeno por 13 a 15 meses em doses de 5, 20 e 50 mg/kg/dia (cerca de metade, duas e cinco vezes a dose humana diária recomendada em mg/m² base).
Mutagênese
Nenhum potencial genotóxico foi encontrado em uma bateria convencional de testes in vivo e in vitro com sistemas de teste pró e eucarióticos com sistemas de metabolização de drogas. No entanto, níveis aumentados de adutos de DNA foram observados pela pós-marcação com 32P em DNA de fígado de rato e linfócitos humanos cultivados. Tamoxifeno também foi encontrado para aumentar os níveis de formação de micronúcleos in vitro na linha de células linfoblastóides humanas (MCL-5). Com base nesses achados, o tamoxifeno é genotóxico em células MCL-5 de roedores e humanos.
Prejuízo da Fertilidade
Tamoxifeno produziu diminuição da fertilidade e concepção em ratas com doses de 0,04 mg/kg/dia (cerca de 0,01 vezes a dose máxima diária recomendada em humanos com base em mg/m²) quando administrado por duas semanas antes do acasalamento até o dia 7 de gravidez . Com esta dose, os índices de fertilidade e reprodutivos foram significativamente reduzidos com mortalidade fetal total. A mortalidade fetal também aumentou com doses de 0,16 mg/kg/dia (cerca de 0,03 vezes a dose máxima diária recomendada em humanos com base em mg/m²) quando ratas foram administradas nos dias 7-17 de gestação. O tamoxifeno produziu aborto, parto prematuro e morte fetal em coelhos administrados com doses iguais ou superiores a 0,125 mg/kg/dia (cerca de 0,05 vezes a dose humana máxima diária recomendada com base em mg/m²). Não houve alterações teratogênicas em ratos ou coelhos.
Gravidez Categoria D
Ver AVISOS .
Mães que amamentam
Foi relatado que o tamoxifeno inibe a lactação. Dois estudos controlados por placebo em mais de 150 mulheres mostraram que o tamoxifeno inibe significativamente a produção de leite pós-parto precoce. Em ambos os estudos, o tamoxifeno foi administrado dentro de 24 horas após o parto por 5 a 18 dias. O efeito do tamoxifeno na produção de leite estabelecida não é conhecido.
Não há dados que abordem se o tamoxifeno é excretado no leite humano. Se excretado, não há dados sobre os efeitos do tamoxifeno no leite materno em lactentes ou animais amamentados. No entanto, a exposição neonatal direta de tamoxifeno a camundongos e ratos (não via leite materno) produziu 1) lesões do trato reprodutivo em roedores fêmeas (semelhantes às observadas em humanos após exposição intrauterina ao dietilestilbestrol) e 2) defeitos funcionais do trato reprodutivo em machos. roedores, como atrofia testicular e parada da espermatogênese.
Não se sabe se NOLVADEX (citrato de tamoxifeno) é excretado no leite humano. Devido ao potencial de reações adversas graves em lactentes de NOLVADEX (citrato de tamoxifeno), as mulheres que tomam NOLVADEX (citrato de tamoxifeno) não devem amamentar.
Redução na incidência de câncer de mama em mulheres de alto risco com CDIS
Não se sabe se NOLVADEX (citrato de tamoxifeno) é excretado no leite humano. Devido ao potencial de reações adversas graves em lactentes de NOLVADEX (citrato de tamoxifeno), as mulheres que tomam NOLVADEX (citrato de tamoxifeno) não devem amamentar.
Uso Pediátrico
A segurança e eficácia de NOLVADEX (citrato de tamoxifeno) para meninas de dois a 10 anos com síndrome de McCune-Albright e puberdade precoce não foram estudadas além de um ano de tratamento. Os efeitos a longo prazo da terapia com NOLVADEX (citrato de tamoxifeno) para meninas não foram estabelecidos. Em adultos tratados com NOLVADEX (citrato de tamoxifeno), foi observado um aumento na incidência de malignidades uterinas, acidente vascular cerebral e embolia pulmonar (ver AVISO EM CAIXA , e FARMACOLOGIA CLÍNICA-Estudos Clínicos-Síndrome de McCune-Albright subseção).
Uso Geriátrico
No estudo NSABP P-1, a porcentagem de mulheres com pelo menos 65 anos de idade foi de 16%. Mulheres com pelo menos 70 anos de idade representaram 6% dos participantes. Uma redução na incidência de câncer de mama foi observada entre os participantes em cada um dos subgrupos: um total de 28 e 10 cânceres de mama invasivos foram observados entre os participantes com 65 anos ou mais nos grupos placebo e NOLVADEX (citrato de tamoxifeno), respectivamente. Em todos os outros resultados, os resultados neste subconjunto refletem os resultados observados no subconjunto de mulheres com pelo menos 50 anos de idade. Nenhuma diferença geral na tolerabilidade foi observada entre pacientes mais velhos e mais jovens (ver FARMACOLOGIA CLÍNICA - Estudos Clínicos - Redução da Incidência de Câncer de Mama em Mulheres de Alto Risco seção).
No estudo NSABP B-24, a porcentagem de mulheres com pelo menos 65 anos de idade foi de 23%. Mulheres com pelo menos 70 anos de idade representaram 10% dos participantes. Um total de 14 e 12 cânceres de mama invasivos foram observados entre os participantes com 65 anos ou mais nos grupos placebo e NOLVADEX (citrato de tamoxifeno), respectivamente. Este subconjunto é muito pequeno para chegar a qualquer conclusão sobre a eficácia. Em todos os outros parâmetros, os resultados neste subconjunto foram comparáveis aos de mulheres mais jovens inscritas neste estudo. Não foram observadas diferenças globais na tolerabilidade entre pacientes mais velhos e mais jovens.
SOBREDOSAGEM
Os sinais observados nas doses mais altas após estudos para determinar LD50 em animais foram dificuldades respiratórias e convulsões.
Superdosagem aguda em humanos não foi relatada. Em um estudo de pacientes com câncer metastático avançado que determinou especificamente a dose máxima tolerada de NOLVADEX (citrato de tamoxifeno) ao avaliar o uso de doses muito altas para reverter a resistência a múltiplas drogas, observou-se neurotoxicidade aguda manifestada por tremor, hiperreflexia, marcha instável e tontura. Esses sintomas ocorreram dentro de 3-5 dias após o início do NOLVADEX (citrato de tamoxifeno) e desapareceram dentro de 2-5 dias após a interrupção da terapia. Nenhuma toxicidade neurológica permanente foi observada. Um paciente apresentou uma convulsão vários dias após a interrupção do NOLVADEX (citrato de tamoxifeno) e os sintomas neurotóxicos foram resolvidos. A relação causal da convulsão com a terapia com NOLVADEX (citrato de tamoxifeno) é desconhecida. As doses administradas nesses pacientes foram todas superiores a 400 mg/m² da dose de ataque, seguidas por doses de manutenção de 150 mg/m² de NOLVADEX (citrato de tamoxifeno) administradas duas vezes ao dia.
No mesmo estudo, o prolongamento do intervalo QT no eletrocardiograma foi observado quando os pacientes receberam doses superiores a 250 mg/m² da dose de ataque, seguidas por doses de manutenção de 80 mg/m² de NOLVADEX (citrato de tamoxifeno) administradas duas vezes ao dia. Para uma mulher com uma área de superfície corporal de 1,5 m², a dose de carga mínima e as doses de manutenção administradas nas quais os sintomas neurológicos e as alterações QT ocorreram foram pelo menos 6 vezes maiores em relação à dose máxima recomendada.
Nenhum tratamento específico para superdosagem é conhecido; o tratamento deve ser sintomático.
CONTRA-INDICAÇÕES
NOLVADEX (citrato de tamoxifeno) é contraindicado em pacientes com hipersensibilidade conhecida ao medicamento ou a qualquer um de seus componentes.
Redução na incidência de câncer de mama em mulheres de alto risco e mulheres com CDIS
NOLVADEX (citrato de tamoxifeno) é contraindicado em mulheres que necessitam de terapia anticoagulante do tipo cumarínico concomitante ou em mulheres com histórico de trombose venosa profunda ou embolia pulmonar.
FARMACOLOGIA CLÍNICA
NOLVADEX (citrato de tamoxifeno) é um agente não esteroidal que demonstrou potentes propriedades antiestrogênicas em sistemas de testes em animais. Os efeitos antiestrogênicos podem estar relacionados à sua capacidade de competir com o estrogênio por sítios de ligação em tecidos-alvo, como a mama. O tamoxifeno inibe a indução de carcinoma mamário de rato induzido por dimetilbenzantraceno (DMBA) e causa a regressão de tumores induzidos por DMBA já estabelecidos. Neste modelo de rato, o tamoxifeno parece exercer seus efeitos antitumorais ligando-se aos receptores de estrogênio.
Em citossóis derivados de adenocarcinomas de mama humanos, o tamoxifeno compete com o estradiol pela proteína receptora de estrogênio.
Absorção e Distribuição
Após uma dose oral única de 20 mg de tamoxifeno, ocorreu um pico médio de concentração plasmática de 40 ng/mL (intervalo de 35 a 45 ng/mL) aproximadamente 5 horas após a administração. O declínio nas concentrações plasmáticas de tamoxifeno é bifásico com meia-vida de eliminação terminal de cerca de 5 a 7 dias. A concentração plasmática máxima média de N-desmetil tamoxifeno é de 15 ng/mL (intervalo de 10 a 20 ng/mL). A administração crônica de 10 mg de tamoxifeno duas vezes ao dia por 3 meses a pacientes resulta em concentrações plasmáticas médias no estado de equilíbrio de 120 ng/mL (intervalo de 67-183 ng/mL) para tamoxifeno e 336 ng/mL (intervalo de 148-654 ng/mL). mL) para N-desmetil tamoxifeno. As concentrações plasmáticas médias no estado de equilíbrio de tamoxifeno e N-desmetil tamoxifeno após a administração de 20 mg de tamoxifeno uma vez ao dia por 3 meses são 122 ng/mL (intervalo de 71-183 ng/mL) e 353 ng/mL (intervalo de 152-706 ng /mL), respectivamente. Após o início da terapia, as concentrações de estado de equilíbrio de tamoxifeno são alcançadas em cerca de 4 semanas e as concentrações de estado de equilíbrio de N-desmetil tamoxifeno são alcançadas em cerca de 8 semanas, sugerindo uma meia-vida de aproximadamente 14 dias para este metabólito. Em um estudo cruzado de estado de equilíbrio de comprimidos de 10 mg de NOLVADEX (citrato de tamoxifeno) administrados duas vezes ao dia versus um comprimido de 20 mg de NOLVADEX (citrato de tamoxifeno) administrado uma vez ao dia, o comprimido de 20 mg de NOLVADEX (citrato de tamoxifeno) foi bioequivalente aos 10 mg NOLVADEX (citrato de tamoxifeno) comprimidos.
Metabolismo
tamoxifeno é extensamente metabolizado após administração oral. O N-desmetil tamoxifeno é o principal metabólito encontrado no plasma dos pacientes. A atividade biológica do N-desmetil tamoxifeno parece ser semelhante à do tamoxifeno. O 4-hidroxitamoxifeno e um derivado de álcool primário de cadeia lateral do tamoxifeno foram identificados como metabólitos menores no plasma. O tamoxifeno é um substrato do citocromo P-450 3A, 2C9 e 2D6 e um inibidor da P-glicoproteína.
Excreção
Estudos em mulheres que receberam 20 mg de tamoxifeno 14C mostraram que aproximadamente 65% da dose administrada foi excretada do corpo durante um período de 2 semanas com excreção fecal como principal via de eliminação. O fármaco é excretado principalmente como conjugados polares, com o fármaco inalterado e os metabólitos não conjugados representando menos de 30% da radioatividade fecal total.
Populações Especiais
Os efeitos da idade, sexo e raça na farmacocinética do tamoxifeno não foram determinados. Os efeitos da redução da função hepática no metabolismo e farmacocinética do tamoxifeno não foram determinados.
Pacientes pediátricos
A farmacocinética do tamoxifeno e do N-desmetil tamoxifeno foi caracterizada usando uma análise farmacocinética populacional com amostras esparsas por paciente obtidas de 27 pacientes pediátricas do sexo feminino com idades entre 2 e 10 anos matriculadas em um estudo desenhado para avaliar a segurança, eficácia e farmacocinética de NOLVADEX (tamoxifeno citrato) no tratamento da síndrome de McCune-Albright. Dados ricos de dois estudos farmacocinéticos de citrato de tamoxifeno nos quais 59 mulheres na pós-menopausa com câncer de mama completaram os estudos foram incluídos na análise para determinar o modelo farmacocinético estrutural do tamoxifeno. Um modelo de um compartimento forneceu o melhor ajuste aos dados.
Em pacientes pediátricos, um pico médio de concentração plasmática no estado de equilíbrio (Css, max) e AUC foram de 187 ng/mL e 4110 ng h/mL, respectivamente, e Css, max ocorreu aproximadamente 8 horas após a administração. A depuração (CL/F) como peso corporal ajustado em pacientes pediátricas do sexo feminino foi aproximadamente 2,3 vezes maior do que em pacientes do sexo feminino com câncer de mama. Na coorte mais jovem de pacientes pediátricos do sexo feminino (2-6 anos), CL/F foi 2,6 vezes maior; na coorte mais velha (7-10,9 anos) CL/F foi aproximadamente 1,9 vezes maior. A exposição ao N-desmetil tamoxifeno foi comparável entre os pacientes pediátricos e adultos. A segurança e eficácia de NOLVADEX (citrato de tamoxifeno) para meninas de dois a 10 anos com síndrome de McCune-Albright e puberdade precoce não foram estudadas além de um ano de tratamento. Os efeitos a longo prazo da terapia com NOLVADEX (citrato de tamoxifeno) em meninas não foram estabelecidos. Em adultos tratados com NOLVADEX (citrato de tamoxifeno), foi observado um aumento na incidência de malignidades uterinas, acidente vascular cerebral e embolia pulmonar (ver AVISO EM CAIXA ).
Interações Medicamentosas
Estudos in vitro mostraram que eritromicina, ciclosporina, nifedipina e diltiazem inibiram competitivamente a formação de N-desmetil tamoxifeno com K1 aparente de 20, 1, 45 e 30 µM, respectivamente. O significado clínico destes estudos in vitro é desconhecido.
O tamoxifeno reduziu a concentração plasmática de letrozol em 37% quando esses medicamentos foram coadministrados. A rifampicina, um indutor do citocromo P-450 3A4, reduziu a AUC e Cmax do tamoxifeno em 86% e 55%, respectivamente. A aminoglutetimida reduz as concentrações plasmáticas de tamoxifeno e N-desmetil tamoxifeno. A medroxiprogesterona reduz as concentrações plasmáticas de N-desmetil, mas não de tamoxifeno.
No estudo adjuvante de anastrozol, a co-administração de anastrozol e NOLVADEX (citrato de tamoxifeno) em pacientes com câncer de mama reduziu a concentração plasmática de anastrozol em 27% em comparação com os alcançados com anastrozol sozinho; no entanto, a coadministração não afetou a farmacocinética do tamoxifeno ou do N-desmetiltamoxifeno (ver PRECAUÇÕES - INTERAÇÕES MEDICAMENTOSAS ). NOLVADEX (citrato de tamoxifeno) não deve ser coadministrado com anastrozol.
Estudos clínicos
Câncer de mama metastático
Mulheres na pré-menopausa (NOLVADEX (citrato de tamoxifeno) vs. Ablação)
Três estudos prospectivos e randomizados (Ingle, Pritchard, Buchanan) compararam NOLVADEX (citrato de tamoxifeno) à ablação ovariana (ooforectomia ou irradiação ovariana) em mulheres na pré-menopausa com câncer de mama avançado. Embora a taxa de resposta objetiva, o tempo até a falha do tratamento e a sobrevida tenham sido semelhantes em ambos os tratamentos, o acúmulo limitado de pacientes impediu a demonstração de equivalência. Em uma análise geral dos dados de sobrevivência dos 3 estudos, a taxa de risco para morte (NOLVADEX (citrato de tamoxifeno)/ablação ovariana) foi de 1,00 com intervalos de confiança de 95% de 0,73 a 1,37. Estrogênios séricos e plasmáticos elevados foram observados em mulheres na pré-menopausa recebendo NOLVADEX (citrato de tamoxifeno), mas os dados dos estudos randomizados não sugerem um efeito adverso desse aumento. Um número limitado de pacientes na pré-menopausa com progressão da doença durante a terapia com NOLVADEX (citrato de tamoxifeno) respondeu à ablação ovariana subsequente.
Câncer de mama masculino
Resultados publicados de 122 pacientes (119 avaliáveis) e relatos de casos em 16 pacientes (13 avaliáveis) tratados com NOLVADEX (citrato de tamoxifeno) mostraram que NOLVADEX (citrato de tamoxifeno) é eficaz para o tratamento paliativo do câncer de mama masculino. Sessenta e seis desses 132 pacientes avaliáveis responderam ao NOLVADEX (citrato de tamoxifeno), o que constitui uma taxa de resposta objetiva de 50%.
Câncer de Mama Adjuvante
Visão geral
Early Breast Cancer Trialists' Collaborative Group (EBCTCG) conduziu revisões mundiais da terapia adjuvante sistêmica para o câncer de mama inicial em 1985, 1990 e novamente em 1995. Em 1998, dados de resultados de 10 anos foram relatados para 36.689 mulheres em 55 ensaios adjuvante NOLVADEX (citrato de tamoxifeno) usando doses de 20-40 mg/dia por 1-5+ anos. Vinte e cinco por cento dos pacientes receberam 1 ano ou menos de tratamento experimental, 52% receberam 2 anos e 23% receberam cerca de 5 anos. Quarenta e oito por cento dos tumores eram receptores de estrogênio (ER) positivos (> 10 fmol/mg), 21% eram ER pobres (
Entre as mulheres com câncer de mama ER positivo ou desconhecido e linfonodos positivos que receberam cerca de 5 anos de tratamento, a sobrevida global em 10 anos foi de 61,4% para NOLVADEX (citrato de tamoxifeno) versus 50,5% para controle (logrank 2p
efeito da duração programada do tamoxifeno pode ser descrito como segue. Em mulheres com câncer de mama ER positivo ou desconhecido recebendo 1 ano ou menos, 2 anos ou cerca de 5 anos de NOLVADEX (citrato de tamoxifeno), as reduções proporcionais na mortalidade foram de 12%, 17% e 26%, respectivamente (tendência significativa em 2p
O benefício é menos claro para mulheres com câncer de mama pobre em ER nas quais a redução proporcional na recorrência foi de 10% (2p = 0,007) para todas as durações tomadas em conjunto, ou 9% (2p = 0,02) se os cânceres de mama contralaterais forem excluídos. A redução correspondente na mortalidade foi de 6% (NS). Os efeitos de cerca de 5 anos de NOLVADEX (citrato de tamoxifeno) na recorrência e mortalidade foram semelhantes, independentemente da idade e da quimioterapia concomitante. Não houve indicação de que doses superiores a 20 mg por dia fossem mais eficazes.
Anastrozol Adjuvant ATAC Trial - Estudo de Anastrozol em comparação com NOLVADEX (citrato de tamoxifeno) para tratamento adjuvante de câncer de mama precoce - Um estudo adjuvante com anastrozol foi realizado em 9.366 mulheres na pós-menopausa com câncer de mama operável que foram randomizadas para receber tratamento adjuvante com anastrozol 1 mg ao dia, NOLVADEX (citrato de tamoxifeno) 20 mg ao dia ou uma combinação desses dois tratamentos por cinco anos ou até a recorrência da doença. Em um acompanhamento médio de 33 meses, a combinação de anastrozol e NOLVADEX (citrato de tamoxifeno) não demonstrou nenhum benefício de eficácia quando comparado com a terapia com NOLVADEX (citrato de tamoxifeno) isoladamente em todos os pacientes, bem como na subpopulação positiva para receptores hormonais. Este braço de tratamento foi descontinuado do estudo. Por favor consulte FARMACOLOGIA CLÍNICA-Populações Especiais-Interações Medicamentosas , PRECAUÇÕES - Testes de Laboratório , PRECAUÇÕES-Interações medicamentosas e REAÇÕES ADVERSAS seções para informações de segurança deste estudo. Consulte as informações completas de prescrição de ARIMIDEX® (anastrozol) 1 mg comprimidos para obter informações adicionais sobre este estudo.
Os pacientes nos dois braços de monoterapia do estudo ATAC foram tratados por uma média de 60 meses (5 anos) e acompanhados por uma média de 68 meses. A sobrevida livre de doença na população com intenção de tratar foi estatisticamente melhorada [Hazard Ratio (HR) = 0,87, IC 95%: 0,78, 0,97, p = 0,0127] no braço de anastrazol em comparação com o braço de NOLVADEX (citrato de tamoxifeno) .
Nó Positivo - Estudos Individuais
Dois estudos (Hubay e NSABP B-09) demonstraram uma sobrevida livre de doença melhorada após mastectomia radical ou radical modificada em mulheres na pós-menopausa ou mulheres com 50 anos de idade ou mais com câncer de mama cirurgicamente curável com linfonodos axilares positivos quando NOLVADEX (citrato de tamoxifeno) foi adicionado à quimioterapia citotóxica adjuvante. No estudo de Hubay, NOLVADEX (citrato de tamoxifeno) foi adicionado ao CMF de "baixa dose" (ciclofosfamida, metotrexato e fluorouracil). No estudo NSABP B-09, NOLVADEX (citrato de tamoxifeno) foi adicionado ao melfalano [L-fenilalanina mostarda (P)] e fluorouracil (F).
No estudo de Hubay, os pacientes com um receptor de estrogênio positivo (mais de 3 fmol) eram mais propensos a se beneficiar. No estudo NSABP B-09 em mulheres com idade entre 50-59 anos, apenas mulheres com níveis de receptores de estrogênio e progesterona de 10 fmol ou mais claramente se beneficiaram, enquanto houve uma tendência não estatisticamente significativa de efeitos adversos em mulheres com níveis de receptores de estrogênio e progesterona menos de 10 fmol. Em mulheres com idade entre 60-70 anos, houve uma tendência a um efeito benéfico do NOLVADEX (citrato de tamoxifeno) sem qualquer relação clara com o status do receptor de estrogênio ou progesterona.
Três estudos prospectivos (ECOG-1178, Toronto, OTAN) usando NOLVADEX (citrato de tamoxifeno) adjuvantemente como agente único demonstraram uma sobrevida livre de doença melhorada após mastectomia total e dissecção axilar para mulheres na pós-menopausa com linfonodos axilares positivos em comparação com placebo/controles sem tratamento . O estudo da OTAN também demonstrou um benefício geral de sobrevivência.
Nó Negativo - Estudos Individuais
NSABP B-14, um estudo prospectivo, duplo-cego, randomizado, comparou NOLVADEX (citrato de tamoxifeno) com placebo em mulheres com câncer de mama negativo para linfonodo axilar, receptor de estrogênio positivo (≥ 10 fmol/mg de proteína citosol) (como terapia adjuvante , após mastectomia total e dissecção axilar, ou ressecção segmentar
INFORMAÇÃO DO PACIENTE
GUIA DE MEDICAÇÃO
NOLVADEX (citrato de tamoxifeno) ® (NOLE-vah-dex) Comprimidos Nome genérico: tamoxifeno (ta-MOX-I-fen)
Escrito para mulheres que usam NOLVADEX (citrato de tamoxifeno) para diminuir sua alta chance de contrair câncer de mama ou que têm carcinoma ductal in situ (CDIS)
Este Guia de Medicação discute apenas o uso de NOLVADEX (citrato de tamoxifeno) para diminuir a chance de desenvolver câncer de mama em mulheres de alto risco e em mulheres tratadas para CDIS.
Pessoas que tomam NOLVADEX (citrato de tamoxifeno) tratar câncer de mama tem benefícios diferentes e decisões diferentes a serem tomadas do que mulheres de alto risco ou mulheres com carcinoma ductal in situ (CDIS) tomando NOLVADEX (citrato de tamoxifeno) para reduzir a chance de contrair câncer de mama. Se você já tem câncer de mama, converse com seu médico sobre como os benefícios do tratamento do câncer de mama com NOLVADEX (citrato de tamoxifeno) se comparam aos riscos descritos neste documento.
Por que devo ler este Guia de Medicação?
Este guia contém informações para ajudá-lo a decidir se deve usar NOLVADEX (citrato de tamoxifeno) para diminuir sua chance de ter câncer de mama.
Você e seu médico devem conversar sobre se o possível benefício de NOLVADEX (citrato de tamoxifeno) em reduzir sua alta chance de ter câncer de mama é maior do que seus possíveis riscos. Seu médico tem um programa de computador especial ou uma calculadora de mão para saber se você está no grupo de alto risco. Se você tem CDIS e foi tratado com cirurgia e radioterapia, seu médico pode prescrever NOLVADEX (citrato de tamoxifeno) para diminuir sua chance de ter câncer de mama invasivo (disseminado).
Leia este guia cuidadosamente antes de iniciar NOLVADEX (citrato de tamoxifeno). É importante ler a informação que recebe cada vez que recebe mais medicamento. Pode haver algo novo. Este guia não diz tudo sobre NOLVADEX (citrato de tamoxifeno) e não não substituir a conversa com o seu médico.
Somente você e seu médico podem determinar se NOLVADEX (citrato de tamoxifeno) é adequado para você.
Qual é a informação mais importante que devo saber sobre o uso de NOLVADEX (citrato de tamoxifeno) para reduzir a chance de contrair câncer de mama?
NOLVADEX (citrato de tamoxifeno) é um medicamento de prescrição que é como o estrogênio (hormônio feminino) em alguns aspectos e diferente em outros. Na mama, NOLVADEX (citrato de tamoxifeno) pode bloquear os efeitos do estrogênio. Por fazer isso, NOLVADEX (citrato de tamoxifeno) pode bloquear o crescimento de câncer de mama que precisa de estrogênio para crescer (câncer que é positivo para receptor de estrogênio ou progesterona).
NOLVADEX (citrato de tamoxifeno) pode diminuir a chance de ter câncer de mama em mulheres com uma chance maior do que o normal de ter câncer de mama nos próximos cinco anos (mulheres de alto risco) e mulheres com CDIS.
Como as mulheres de alto risco ainda não têm câncer, é importante pensar cuidadosamente se o possível benefício do NOLVADEX (citrato de tamoxifeno) na redução da chance de ter câncer de mama é maior do que seus possíveis riscos.
Este Guia de Medicação analisa os riscos e benefícios do uso de NOLVADEX (citrato de tamoxifeno) para reduzir a chance de contrair câncer de mama em mulheres de alto risco e mulheres com CDIS. Este guia faz não discutir os benefícios e decisões especiais para pessoas que já têm câncer de mama.
Por que mulheres e homens usam NOLVADEX (citrato de tamoxifeno)?
NOLVADEX (citrato de tamoxifeno) tem mais de um uso. NOLVADEX (citrato de tamoxifeno) é usado:
para diminuir a chance de contrair câncer de mama em mulheres com uma chance maior do que o normal de contrair câncer de mama nos próximos 5 anos (mulheres de alto risco)
para diminuir a chance de contrair câncer de mama invasivo (disseminado) em mulheres que fizeram cirurgia e radioterapia para carcinoma ductal in situ (CDIS). DCIS significa que o câncer está apenas dentro dos dutos de leite.
tratar câncer de mama em mulheres após o término do tratamento precoce. O tratamento precoce pode incluir cirurgia, radioterapia e quimioterapia. NOLVADEX (citrato de tamoxifeno) pode impedir que o câncer se espalhe para outras partes do corpo. Também pode reduzir a chance da mulher de ter um novo câncer de mama. em mulheres e homens,
tratar câncer de mama que se espalhou para outras partes do corpo (câncer de mama metastático).
Este guia fala apenas sobre o uso de NOLVADEX (citrato de tamoxifeno) para diminuir a chance de contrair câncer de mama (#1 e #2 acima).
Quais são os benefícios do NOLVADEX (citrato de tamoxifeno) para diminuir a chance de contrair câncer de mama em mulheres de alto risco e em mulheres tratadas para CDIS?
Um grande estudo americano analisou mulheres de alto risco comparou os que tomaram NOLVADEX (citrato de tamoxifeno) por 5 anos com outros que tomaram um comprimido sem NOLVADEX (citrato de tamoxifeno) (placebo). Mulheres de alto risco foram definidas como mulheres que têm 1,7% ou mais de chance de desenvolver câncer de mama nos próximos 5 anos, com base em um programa de computador especial. Neste estudo:
- Em cada 1.000 mulheres de alto risco que tomou um placebo , a cada ano cerca de 7 tem câncer de mama.
- Em cada 1.000 mulheres de alto risco que tomou NOLVADEX (citrato de tamoxifeno) , a cada ano cerca de 4 tem câncer de mama.
O estudo mostrou que, em média, as mulheres de alto risco que tomaram NOLVADEX (citrato de tamoxifeno) reduziram suas chances de contrair câncer de mama em 44%, de 7 em 1.000 para 4 em 1.000.
Outro estudo americano analisou mulheres com CDIS e comparou aqueles que tomaram NOLVADEX (citrato de tamoxifeno) por 5 anos com outros que tomaram placebo. Neste estudo:
- Em cada 1.000 mulheres com CDIS que tomou placebo a cada ano cerca de 17 tem câncer de mama.
- Em cada 1.000 mulheres com CDIS que tomou NOLVADEX (citrato de tamoxifeno) , a cada ano cerca de 10 tem câncer de mama.
O estudo mostrou que, em média, as mulheres com CDIS que tomaram NOLVADEX (citrato de tamoxifeno) reduziram suas chances de contrair câncer de mama invasivo (espalhamento) em 43%, de 17 em 1.000 para 10 em 1.000.
Esses estudos não significam que tomar NOLVADEX (citrato de tamoxifeno) diminuirá sua chance pessoal de ter câncer de mama. Não sabemos quais serão os benefícios para qualquer mulher que tome NOLVADEX (citrato de tamoxifeno) para reduzir sua chance de ter câncer de mama.
Quais são os riscos do NOLVADEX (citrato de tamoxifeno)?
Nos estudos descritos em “Quais são os benefícios do NOLVADEX (citrato de tamoxifeno)?”, as mulheres de alto risco que tomaram NOLVADEX (citrato de tamoxifeno) tiveram certos efeitos colaterais em uma taxa maior do que aquelas que tomaram placebo.
Alguns desses efeitos colaterais podem causar a morte.
Em um estudo, em mulheres que ainda tinham o útero
- De cada 1.000 mulheres que tomaram placebo, a cada ano 1 teve câncer de endométrio (câncer do revestimento do útero) e nenhuma teve sarcoma uterino (câncer do corpo do útero).
- De cada 1.000 mulheres que tomaram NOLVADEX (citrato de tamoxifeno), a cada ano 2 tiveram câncer de endométrio e menos de 1 teve sarcoma uterino.
Esses resultados mostram que, em média, em mulheres de alto risco que ainda tinha seu útero , NOLVADEX (citrato de tamoxifeno) dobrou a chance de contrair câncer endometrial de 1 em 1.000 para 2 em 1.000, e aumentou a chance de contrair sarcoma uterino. Isso não significa que tomar NOLVADEX (citrato de tamoxifeno) dobrará sua chance pessoal de contrair câncer de endométrio ou aumentará sua chance de contrair sarcoma uterino. Não sabemos qual será esse risco para qualquer mulher. O risco é diferente para as mulheres que não têm mais o útero.
Para todas as mulheres neste estudo, tomar NOLVADEX (citrato de tamoxifeno) aumentou o risco de ter um coágulo de sangue em seus pulmões ou veias, ou de ter um acidente vascular cerebral. Em alguns casos, as mulheres morreram devido a esses efeitos.
NOLVADEX (citrato de tamoxifeno) aumentou o risco de contrair catarata (turvação da lente do olho) ou precisar de cirurgia de catarata. (Consulte “Quais são os possíveis efeitos colaterais do NOLVADEX (citrato de tamoxifeno)?” para obter mais detalhes sobre os efeitos colaterais.)
O que não sabemos sobre tomar NOLVADEX (citrato de tamoxifeno) para reduzir a chance de contrair câncer de mama?
Nós não sabemos
- se NOLVADEX (citrato de tamoxifeno) reduz a chance de desenvolver câncer de mama em mulheres com genes anormais de câncer de mama (BRCA1 e BRCA2)
- se tomar NOLVADEX (citrato de tamoxifeno) por 5 anos reduz o número de cânceres de mama que uma mulher terá em sua vida ou se apenas retarda alguns cânceres de mama
- se NOLVADEX (citrato de tamoxifeno) ajuda a mulher a viver mais
- os efeitos de tomar NOLVADEX (citrato de tamoxifeno) com terapia de reposição hormonal (TRH), pílulas anticoncepcionais ou andrógenos (hormônios masculinos)
- os benefícios de tomar NOLVADEX (citrato de tamoxifeno) se você tiver menos de 35 anos
Estudos estão sendo feitos para aprender mais sobre os benefícios e riscos a longo prazo do uso de NOLVADEX (citrato de tamoxifeno) para reduzir a chance de contrair câncer de mama.
Quais são os possíveis efeitos colaterais do NOLVADEX (citrato de tamoxifeno)?
O efeito colateral mais comum do NOLVADEX (citrato de tamoxifeno) são ondas de calor. Isso não é sinal de um problema sério.
O próximo efeito colateral mais comum é o corrimento vaginal. Se a descarga for sanguinolenta, pode ser um sinal de um problema sério. [Consulte “Alterações no revestimento (endométrio) ou corpo do seu útero” abaixo.]
Efeitos colaterais menos comuns, mas graves de NOLVADEX (citrato de tamoxifeno) estão listados abaixo. Estes podem ocorrer a qualquer momento. Ligue para o seu médico imediatamente se tiver quaisquer sinais de efeitos colaterais listados abaixo:
- Alterações no revestimento (endométrio) ou corpo do seu útero. Essas mudanças podem significar que problemas sérios estão começando, incluindo câncer de útero. Os sinais de alterações no útero são:
- Sangramento vaginal ou secreção sanguinolenta que pode ser de cor enferrujada ou marrom. Você deve ligar para o seu médico mesmo se ocorrer apenas uma pequena quantidade de sangramento.
- Alteração no seu sangramento mensal, como na quantidade ou no momento do sangramento ou aumento da coagulação.
- Dor ou pressão na pélvis (abaixo do umbigo).
- Coágulos de sangue em suas veias ou pulmões. Estes podem causar problemas graves, incluindo a morte. Você pode ter coágulos até 2-3 meses após parar de tomar NOLVADEX (citrato de tamoxifeno). Os sinais de coágulos sanguíneos são:
- dor súbita no peito, falta de ar, tosse com sangue
- dor, sensibilidade ou inchaço em uma ou ambas as pernas
- Derrame. O AVC pode causar sérios problemas médicos, incluindo a morte. Os sinais de AVC são:
- fraqueza repentina, formigamento ou dormência no rosto, braço ou perna, especialmente em um lado do corpo
- confusão repentina, dificuldade para falar ou entender
- problemas repentinos para ver em um ou ambos os olhos
- dificuldade súbita para andar, tontura, perda de equilíbrio ou coordenação
- dor de cabeça súbita e intensa sem causa conhecida
- Catarata ou maior chance de precisar de cirurgia de catarata. O sinal desses problemas é o embaçamento lento da visão.
- Problemas hepáticos, incluindo icterícia. Os sinais de problemas no fígado incluem falta de apetite e amarelecimento da pele ou do branco dos olhos.
Estes não são todos os possíveis efeitos colaterais do NOLVADEX (citrato de tamoxifeno). Para obter uma lista completa, pergunte ao seu médico ou farmacêutico.
Quem não deve tomar NOLVADEX (citrato de tamoxifeno)?
Não tome NOLVADEX (citrato de tamoxifeno) por qualquer motivo se você
- Está grávida ou planeja engravidar enquanto estiver tomando NOLVADEX (citrato de tamoxifeno) ou durante os 2 meses após parar de tomar NOLVADEX (citrato de tamoxifeno) . NOLVADEX (citrato de tamoxifeno) pode prejudicar o feto. Demora cerca de 2 meses para limpar NOLVADEX (citrato de tamoxifeno) do seu corpo. Para ter certeza de que não está grávida, você pode começar a tomar NOLVADEX (citrato de tamoxifeno) enquanto estiver menstruada. Ou você pode fazer um teste de gravidez para ter certeza de que não está grávida antes de começar.
- Estão amamentando. Não sabemos se NOLVADEX (citrato de tamoxifeno) pode passar pelo leite e prejudicar o bebê.
- Teve uma reação alérgica a NOLVADEX (citrato de tamoxifeno) ou tamoxifeno (o outro nome para NOLVADEX (citrato de tamoxifeno)), ou a qualquer um de seus ingredientes inativos.
Se engravidar enquanto estiver a tomar NOLVADEX (citrato de tamoxifeno), pare de tomá-lo imediatamente e contacte o seu médico. NOLVADEX (citrato de tamoxifeno) pode prejudicar o feto. Não tome NOLVADEX (citrato de tamoxifeno) para diminuir sua chance de ter câncer de mama se
- Você já teve um coágulo de sangue que precisou de tratamento médico.
- Está a tomar medicamentos para afinar o sangue, como a varfarina (também chamada Coumadin®*).
- Sua capacidade de se movimentar é limitada durante a maior parte de suas horas de vigília.
- Você está em risco de coágulos sanguíneos. O seu médico pode dizer se você está em alto risco de coágulos sanguíneos.
- Você não tem uma chance maior do que o normal de ter câncer de mama. Seu médico pode dizer se você é uma mulher de alto risco.
Como devo tomar NOLVADEX (citrato de tamoxifeno)?
- Engula o(s) comprimido(s) inteiro(s), com água ou outro líquido não alcoólico. Você pode tomar NOLVADEX (citrato de tamoxifeno) com ou sem alimentos. Tome seu remédio todos os dias. Pode ser mais fácil lembrar se você tomá-lo no mesmo horário todos os dias.
- Se você esquecer uma dose, tome-a quando se lembrar e, em seguida, tome a próxima dose como de costume. Se estiver quase na hora da próxima dose ou se você se lembrar da próxima dose, não tome comprimidos extras para compensar a dose esquecida.
- Tome NOLVADEX (citrato de tamoxifeno) por 5 anos, a menos que seu médico lhe diga o contrário.
O que devo evitar ao tomar NOLVADEX (citrato de tamoxifeno)?
- Não engravide enquanto estiver tomando NOLVADEX (citrato de tamoxifeno) ou por 2 meses após parar. NOLVADEX (citrato de tamoxifeno) pode impedir que os métodos hormonais de controle de natalidade funcionem. Os métodos hormonais incluem pílulas anticoncepcionais, adesivos, injeções, anéis e implantes. Portanto, enquanto estiver tomando NOLVADEX (citrato de tamoxifeno), usar métodos de controle de natalidade que não usam hormônios, como preservativos, diafragmas com espermicida ou DIU simples. Se você engravidar, pare de tomar NOLVADEX (citrato de tamoxifeno) imediatamente e ligue para o seu médico.
- Não amamente. Não sabemos se NOLVADEX (citrato de tamoxifeno) pode passar pelo leite e se pode prejudicar o bebê.
O que devo fazer enquanto estiver tomando NOLVADEX (citrato de tamoxifeno)?
- Faça check-ups ginecológicos regulares (“exames femininos”), exames de mama e mamografias. O seu médico irá dizer-lhe com que frequência. Estes irão verificar se há sinais de câncer de mama e câncer de endométrio (revestimento do útero). Como o NOLVADEX (citrato de tamoxifeno) não previne todos os cânceres de mama, e você pode ter outros tipos de câncer, você precisa desses exames para encontrar qualquer câncer o mais cedo possível.
- Como NOLVADEX (citrato de tamoxifeno) pode causar efeitos colaterais graves, preste muita atenção ao seu corpo. Os sinais que você deve procurar estão listados em “Quais são os possíveis efeitos colaterais do NOLVADEX (citrato de tamoxifeno)?”
- Informe a todos os médicos que você vê que está tomando NOLVADEX (citrato de tamoxifeno).
- Informe o seu médico imediatamente se tiver novos nódulos mamários.
Informações gerais sobre o uso seguro e eficaz de NOLVADEX (citrato de tamoxifeno)
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Seu médico prescreveu NOLVADEX (citrato de tamoxifeno) apenas para você. Não dê a outras pessoas, mesmo que tenham uma condição semelhante, pois pode prejudicá-las. Não o use para uma condição para a qual não foi prescrito.
Este Guia de Medicação é um resumo de informações sobre NOLVADEX (citrato de tamoxifeno) para mulheres que usam NOLVADEX (citrato de tamoxifeno) para diminuir sua alta chance de ter câncer de mama ou que têm CDIS. Se você quiser mais informações sobre NOLVADEX (citrato de tamoxifeno), pergunte ao seu médico ou farmacêutico. Eles podem fornecer informações sobre NOLVADEX (citrato de tamoxifeno) escritas para profissionais de saúde. Para obter mais informações sobre NOLVADEX (citrato de tamoxifeno) ou câncer de mama, visite www.NOLVADEX (citrato de tamoxifeno) .com ou ligue para 1-800-236-9933.
Ingredientes: citrato de tamoxifeno, carboximetilcelulose cálcica, estearato de magnésio, manitol e amido.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA
