Asacol 400mg Mesalamine Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
que é Asacol 400mg e como é usado?
Asacol é um medicamento de prescrição utilizado para tratar os sintomas da colite ulcerosa. Asacol 400mg pode ser usado sozinho ou com outros medicamentos.
Asacol pertence a uma classe de medicamentos chamados derivados do ácido 5-aminossalicílico.
Não se sabe se Asacol 400mg é seguro e eficaz em crianças menores de 5 anos de idade.
Quais são os possíveis efeitos colaterais do Asacol 400mg?
Asacol pode causar efeitos colaterais graves, incluindo:
- dor de estômago severa,
- cólicas estomacais,
- diarreia sanguinolenta,
- febre,
- dor de cabeça,
- erupção cutânea,
- fezes com sangue ou alcatrão,
- tossindo sangue,
- vômito que parece borra de café,
- pouca ou nenhuma micção,
- micção dolorosa ou difícil,
- inchaço nos pés ou tornozelos,
- sentindo-se cansado,
- falta de ar,
- perda de apetite,
- dor de estômago superior,
- hematomas ou sangramentos fáceis,
- urina escura,
- fezes cor de barro e
- amarelecimento da pele ou dos olhos (icterícia)
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Asacol incluem:
- náusea,
- vômito,
- dor de estômago,
- diarréia,
- indigestão,
- gás,
- dor de cabeça,
- erupção cutânea, e
- testes de função hepática anormais
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Asacol. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
Cada comprimido de liberação retardada de Asacol (mesalamina) para administração oral contém 400 mg de mesalamina, um aminosalicilato. Asacol (mesalamine) comprimidos de liberação retardada contêm resina à base de acrílico, Eudragit S (copolímero de ácido metacrílico tipo B, NF), que se dissolve em pH 7 ou superior e libera mesalamina no íleo terminal e além para ação anti-inflamatória tópica no cólon . A mesalamina (também conhecida como ácido 5-aminossalicílico ou 5-ASA) tem o nome químico de ácido 5-amino-2-hidroxibenzóico. Sua fórmula estrutural é:
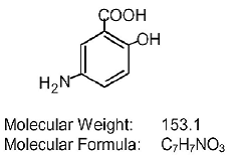
Ingredientes inativos: Cada comprimido contém dióxido de silício coloidal, ftalato de dibutil, tinta preta comestível, óxido férrico vermelho, óxido férrico amarelo, lactose mono-hidratada, estearato de magnésio, copolímero B de ácido metacrílico (Eudragit S), polietilenoglicol, povidona, amidoglicolato de sódio e talco.
INDICAÇÕES
Tratamento da colite ulcerativa leve a moderadamente ativa
Os comprimidos de liberação retardada Asacol® (mesalamina) são indicados para o tratamento da colite ulcerativa leve a moderadamente ativa em pacientes com 5 anos de idade ou mais.
Manutenção da remissão da colite ulcerativa em adultos
Os comprimidos de liberação retardada de asacol (mesalamina) são indicados para a manutenção da remissão da colite ulcerativa em adultos. A segurança e eficácia de Asacol para a manutenção da remissão da colite ulcerosa em doentes pediátricos não foram estabelecidas.
DOSAGEM E ADMINISTRAÇÃO
Dosagem para o tratamento da colite ulcerativa leve a moderadamente ativa
Adultos
Para adultos, a dose recomendada de Asacol 400mg é de dois comprimidos de 400mg, três vezes ao dia, com ou sem alimentos (dose diária total de 2,4 gramas), por um período de 6 semanas. Estudos clínicos ].
Pediatria
Para pacientes pediátricos, a dose diária total recomendada de Asacol é baseada no peso (até um máximo de 2,4 gramas/dia) (ver Tabela 1). Os comprimidos de Asacol 400mg devem ser tomados duas vezes ao dia com ou sem alimentos por um período de 6 semanas [ver Estudos clínicos ].
Dosagem para manutenção da remissão da colite ulcerativa em adultos
Para adultos, a dose recomendada de Asacol é de 1,6 gramas por dia, em doses divididas, com ou sem alimentos [ver Estudos clínicos ].
Instruções importantes de administração
Engula os comprimidos de Asacol inteiros. Não corte, quebre ou mastigue os comprimidos.
Dois comprimidos de Asacol 400 mg não demonstraram ser bioequivalentes a um comprimido de liberação retardada de 800 mg de Asacol® HD (mesalamina) e não devem ser usados alternadamente.
Testes antes da administração de Asacol 400mg
Avalie a função renal antes de iniciar o Asacol [ver AVISOS E PRECAUÇÕES ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
Asacol (mesalamina) Comprimidos de Liberação Retardada: 400 mg (vermelho-marrom, em forma de cápsula e impresso com “0752 DR” em preto).
Armazenamento e manuseio
Asacol (mesalamina) comprimidos de liberação retardada estão disponíveis na forma de comprimidos vermelho-acastanhados em forma de cápsula contendo 400 mg de mesalamina e impressos com “0752 DR” em preto.
NDC 0430-0752-27 Frasco de 180 comprimidos
Armazenar a 20° a 25° C (68° a 77° F); excursões permitidas 15° a 30° C (59° a 86° F) [Consulte Temperatura ambiente controlada USP ].
Fabricado por: Warner Chilcott Deutschland GmbH D-64331 Weiterstadt Alemanha. Comercializado por: Warner Chilcott (EUA), LLC Rockaway, NJ 07866. Revisado: outubro de 2013
EFEITOS COLATERAIS
As reações adversas mais graves observadas nos ensaios clínicos de Asacol ou com outros produtos que contêm mesalamina ou são metabolizados em mesalamina são:
- Insuficiência renal, incluindo insuficiência renal [ver AVISOS E PRECAUÇÕES ]
- Síndrome de intolerância aguda [ver AVISOS E PRECAUÇÕES ]
- Reações de hipersensibilidade [ver AVISOS E PRECAUÇÕES ]
- Insuficiência hepática [ver AVISOS E PRECAUÇÕES ]
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
No total, os comprimidos de Asacol 400mg foram avaliados em 2.690 pacientes com colite ulcerativa em estudos controlados e abertos. As reações adversas apresentadas nas seções a seguir podem ocorrer independentemente da duração da terapia e reações semelhantes foram relatadas em estudos de curto e longo prazo e no cenário pós-comercialização.
Os estudos clínicos que apoiam o uso de Asacol 400mg para o tratamento da colite ulcerativa ativa leve a moderada incluíram dois estudos de 6 semanas, controlados por placebo, randomizados e duplo-cegos em adultos com colite ulcerativa ativa leve a moderada (Estudos 1 e 2) e um Estudo de 6 semanas, randomizado, duplo-cego, de 2 níveis de dose em crianças com colite ulcerativa leve a moderadamente ativa. Os estudos clínicos que apoiam o uso de Asacol 400mg comprimidos na manutenção da remissão da colite ulcerativa incluíram um estudo multicêntrico de 6 meses, randomizado, duplo-cego, controlado por placebo e quatro ensaios de manutenção com controle ativo comparando Asacol 400mg comprimidos com sulfassalazina . Asacol 400mg foi avaliado em 427 adultos e 82 crianças com colite ulcerativa nestes estudos controlados.
Tratamento da colite ulcerativa leve a moderadamente ativa em adultos
Em dois estudos clínicos de 6 semanas controlados por placebo (Estudos 1 e 2) envolvendo 245 pacientes, 155 dos quais foram randomizados para Asacol [ver Estudos clínicos ], 3,2 por cento dos pacientes tratados com Asacol interromperam a terapia por causa de reações adversas em comparação com 2,2 por cento dos pacientes tratados com placebo. A idade média dos pacientes no Estudo 1 foi de 42 anos e 48 por cento dos pacientes eram do sexo masculino. A idade média dos pacientes no Estudo 2 foi de 42 anos e 59 por cento dos pacientes eram do sexo masculino. As reações adversas que levaram à retirada de Asacol incluíram (cada uma em um paciente): diarreia e exacerbação de colite; tontura, náusea, dor nas articulações e dor de cabeça; erupção cutânea, letargia e constipação; boca seca, mal-estar, desconforto lombar, desorientação leve, indigestão leve e cólicas; dor de cabeça, náusea, dor, vômito, cãibras musculares, cabeça entupida, ouvidos entupidos e febre.
As reações adversas em pacientes tratados com Asacol ocorrendo em uma frequência de pelo menos 2 por cento e em uma taxa maior do que placebo em 6 semanas, duplo-cegos, controlados por placebo (Estudos 1 e 2) estão listadas na Tabela 2 abaixo.
Tratamento da colite ulcerativa leve a moderadamente ativa em pacientes pediátricos de 5 a 17 anos
Um estudo randomizado, duplo-cego, de 6 semanas de 2 níveis de dose de Asacol (Estudo 3) foi realizado em 82 pacientes pediátricos de 5 a 17 anos de idade com colite ulcerativa leve a moderadamente ativa. Todos os pacientes foram divididos por categoria de peso corporal (17 a menos de 33 kg, 33 a menos de 54 kg e 54 a 90 kg) e aleatoriamente designados para receber uma dose baixa (1,2, 2,0 e 2,4 g/dia para os respectivos categoria de peso corporal) ou uma dose alta (2,0, 3,6 e 4,8 g/dia).
A dose alta não é uma dosagem aprovada porque não foi considerada mais eficaz do que a dose aprovada [ver DOSAGEM E ADMINISTRAÇÃO e Estudos clínicos ].
duração da exposição à mesalamina entre os 82 pacientes do estudo variou de 12 a 50 dias (média de 40 dias em cada grupo de dose). A maioria (88 por cento) dos pacientes em cada grupo foi tratada por mais de 5 semanas. A Tabela 3 fornece um resumo das reações adversas (RAs) relatadas específicas.
Doze por cento dos pacientes no grupo de baixa dose e 5 por cento dos pacientes no grupo de alta dose tiveram reações adversas graves (ARs). A colite ulcerosa foi relatada como uma RA grave em um sujeito em cada grupo. Outras RAs graves consistiram em sinusite, dor abdominal, índice de massa corporal diminuído, infecção por adenovírus, diarreia sanguinolenta, colangite esclerosante e pancreatite em um indivíduo no grupo de dose baixa e anemia e síncope em um indivíduo no grupo de dose alta.
Sete pacientes foram retirados do estudo por causa de RAs: 5 (12 por cento) no grupo de baixa dose (colite ulcerativa, infecção por adenovírus, colangite esclerosante, pancreatite) e 2 (5 por cento) no grupo de alta dose (aumento da amilase e aumento da lipase , dor abdominal superior).
Em geral, a natureza e a gravidade das reações na população pediátrica foram semelhantes às relatadas em populações adultas de pacientes com colite ulcerativa.
Manutenção da remissão da colite ulcerativa em adultos
Em um estudo de manutenção controlado por placebo de 6 meses envolvendo 264 pacientes (Estudo 4), 177 dos quais foram randomizados para Asacol, seis (3,4%) dos pacientes em uso de Asacol descontinuaram a terapia devido a reações adversas, em comparação com quatro (4,6%) de pacientes em uso de placebo [ver Estudos clínicos ]. A idade média dos pacientes no Estudo 4 foi de 42 anos e 55 por cento dos pacientes eram do sexo masculino. As reações adversas que levaram à retirada do estudo em pacientes usando Asacol incluíram (cada em um paciente): ansiedade; dor de cabeça; prurido; diminuição da libido; artrite reumatoide; e estomatite e astenia.
Além das reações listadas na Tabela 2, as seguintes reações adversas ocorreram em pacientes usando Asacol com uma frequência de 2% ou mais no Estudo 4: aumento abdominal, gastroenterite, hemorragia gastrointestinal, infecção, distúrbio articular, enxaqueca, nervosismo, parestesia, hemorragia retal, anormalidades nas fezes, tenesmo, frequência urinária, vasodilatação e anormalidades da visão.
Em 3.342 pacientes em estudos clínicos não controlados, as seguintes reações adversas ocorreram com uma frequência de 5% ou mais e pareceram aumentar de frequência com o aumento da dose: astenia, febre, síndrome gripal, dor, dor abdominal, dor nas costas, flatulência, sangramento gastrointestinal , artralgia e rinite.
Experiência pós-marketing
Além das reações adversas relatadas acima em ensaios clínicos envolvendo Asacol, as reações adversas listadas abaixo foram identificadas durante o uso pós-aprovação de Asacol 400mg e outros produtos contendo mesalamina. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Corpo como um todo: Dor no pescoço, edema facial, edema, síndrome do tipo lúpus, febre medicamentosa.
Cardiovascular: Pericardite, miocardite [ver AVISOS E PRECAUÇÕES ].
Gastrointestinal: Anorexia, pancreatite, gastrite, aumento do apetite, colecistite, boca seca, úlceras orais, úlcera péptica perfurada diarreia sanguinolenta.
Hematologico: Anemia aplástica por agranulocitose, trombocitopenia, eosinofilia, leucopenia, anemia, linfadenopatia.
Musculoesquelético: Gota.
Nervoso: Depressão, sonolência, labilidade emocional, hiperestesia, vertigem, confusão, tremor, neuropatia periférica, mielite transversa, síndrome de Guillain-Barré.
Renal: Insuficiência renal, nefrite intersticial, nefropatia por alterações mínimas [ver AVISOS E PRECAUÇÕES ].
Respiratório/Pulmonar: Pneumonia eosinofílica, pneumonite intersticial, exacerbação da asma, pleurite.
Pele: Alopecia, psoríase, pioderma gangrenoso, pele seca, eritema nodoso, urticária.
Sentidos Especiais: Dor ocular, alteração do paladar, visão turva, zumbido.
Urogenital: Disúria, urgência urinária, hematúria, epididimite, menorragia, oligospermia reversível.
Anormalidades Laboratoriais: AST (SGOT) ou ALT (SGPT) elevada, fosfatase alcalina elevada, GGT elevada, LDH elevada, bilirrubina elevada, creatinina sérica elevada e BUN.

INTERAÇÕES MEDICAMENTOSAS
Não foram realizados estudos formais de interação medicamentosa usando Asacol 400mg com outros medicamentos. No entanto, as seguintes interações entre produtos contendo mesalamina e outros medicamentos foram relatadas.
Agentes nefrotóxicos, incluindo anti-inflamatórios não esteroides
O uso concomitante de mesalamina com agentes nefrotóxicos conhecidos, incluindo anti-inflamatórios não esteroides (AINEs), pode aumentar o risco de reações renais. AVISOS E PRECAUÇÕES ].
Azatioprina ou 6-mercaptopurina
O uso concomitante de mesalamina com azatioprina ou 6-mercaptopurina pode aumentar o risco de distúrbios sanguíneos.
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Insuficiência renal
Insuficiência renal, incluindo nefropatia por alterações mínimas, nefrite intersticial aguda e crônica e insuficiência renal, foi relatada em pacientes tomando produtos como Asacol 400mg que contêm mesalamina ou são convertidos em mesalamina.
Recomenda-se que os pacientes tenham uma avaliação da função renal antes do início de Asacol 400mg e periodicamente durante o tratamento.
Os prescritores devem avaliar cuidadosamente os riscos e benefícios ao usar Asacol em pacientes com insuficiência renal conhecida ou história de doença renal [ver INTERAÇÕES MEDICAMENTOSAS e Toxicologia não clínica ].
Síndrome de intolerância aguda induzida por mesalamina
A mesalamina tem sido associada a uma síndrome de intolerância aguda que pode ser difícil de distinguir de uma exacerbação da colite ulcerativa. Embora a frequência exata de ocorrência não tenha sido determinada, ocorreu em 3% dos ensaios clínicos controlados de mesalamina ou sulfassalazina. Os sintomas incluem cólicas, dor abdominal, diarreia sanguinolenta e, às vezes, febre, dor de cabeça e erupção cutânea. Observe os pacientes atentamente quanto ao agravamento desses sintomas durante o tratamento. Se houver suspeita de síndrome de intolerância aguda, interrompa imediatamente o tratamento com Asacol.
Reações de hipersensibilidade
Alguns pacientes que experimentaram uma reação de hipersensibilidade à sulfassalazina podem ter uma reação semelhante ao Asacol 400mg ou a outros compostos que contêm ou são convertidos em mesalamina.
Reações de hipersensibilidade cardíaca induzidas pela mesalamina (miocardite e pericardite) foram relatadas com Asacol e outros medicamentos com mesalamina. Deve-se ter cuidado ao prescrever este medicamento a pacientes com condições que os predispõem ao desenvolvimento de miocardite ou pericardite.
Insuficiência Hepática
Houve relatos de insuficiência hepática em pacientes com doença hepática pré-existente que receberam mesalamina. Deve-se ter cautela ao administrar Asacol a pacientes com doença hepática.
Retenção Gástrica Prolongada em Pacientes com Obstrução Gastrointestinal Superior
A obstrução orgânica ou funcional no trato gastrointestinal superior pode causar retenção gástrica prolongada de Asacol 400mg, o que retardaria a liberação de mesalamina no cólon.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Carcinogênese
mesalamina não foi carcinogênica em doses dietéticas de até 480 mg/kg/dia em ratos e 2.000 mg/kg/dia em camundongos, que são cerca de 2,9 e 6,1 vezes a dose máxima de manutenção recomendada de Asacol 400 mg de 1,6 g/dia ou 26,7 mg/kg/dia, com base em 60 kg de peso corporal, respectivamente, com base na área de superfície corporal.
Mutagênese
A mesalamina foi negativa no ensaio de Ames para mutagênese, negativa para indução de trocas de cromátides irmãs (SCE) e aberrações cromossômicas em células de ovário de hamster chinês in vitro e negativa para indução de micronúcleos (MN) em eritrócitos policromáticos de medula óssea de camundongo.
Prejuízo da Fertilidade
A mesalamina, em doses orais de até 480 mg/kg/dia (cerca de 1,9 vezes a dose recomendada para tratamento em humanos com base na área de superfície corporal), não teve efeito na fertilidade ou no desempenho reprodutivo de ratos machos e fêmeas.
Uso em populações específicas
Gravidez
Gravidez Categoria C
Resumo do risco
Não existem estudos adequados e bem controlados sobre o uso de Asacol 400mg em mulheres grávidas. Dados humanos limitados publicados sobre mesalamina não mostram aumento na taxa geral de malformações congênitas. Alguns dados mostram um aumento da taxa de parto prematuro, natimorto e baixo peso ao nascer; no entanto, esses resultados adversos da gravidez também estão associados à doença inflamatória intestinal ativa. Além disso, todas as gestações, independentemente da exposição a drogas, têm uma taxa de fundo de 2 a 4 por cento para malformações maiores e 15 a 20 por cento para perda de gravidez. Nenhuma evidência de dano fetal foi observada em estudos de reprodução animal de mesalamina em ratos e coelhos em doses orais aproximadamente 1,9 vezes (rato) e 3,9 vezes (coelho) a dose humana recomendada. No entanto, o dibutil ftalato (DBP) é um ingrediente inativo no revestimento entérico de Asacol e, em estudos com animais em ratos com doses superiores a 190 vezes a dose humana com base na área de superfície corporal, a DBP materna foi associada a malformações externas e esqueléticas e efeitos adversos na o sistema reprodutor masculino. Asacol 400mg deve ser usado durante a gravidez somente se o benefício potencial justificar o risco potencial para o feto.
Dados humanos
mesalamina atravessa a placenta. Em estudos prospectivos e retrospectivos de mais de 600 mulheres expostas à mesalamina durante a gravidez, a taxa observada de malformações congênitas não aumentou acima da taxa de fundo na população geral. Alguns dados mostram um aumento da taxa de parto prematuro, natimorto e baixo peso ao nascer, mas não está claro se isso foi devido a doença materna subjacente, exposição a drogas ou ambos, já que a doença inflamatória intestinal ativa também está associada a resultados adversos da gravidez.
Dados de animais
Estudos de reprodução com mesalamina foram realizados durante a organogênese em ratos e coelhos em doses orais de até 480 mg/kg/dia. Não houve evidência de diminuição da fertilidade ou dano ao feto. Essas doses de mesalamina foram cerca de 1,9 vezes (rato) e 3,9 vezes (coelho) a dose humana recomendada, com base na área de superfície corporal.
dibutil ftalato (DBP) é um ingrediente inativo no revestimento entérico da Asacol. A ingestão diária humana de DBP da dose máxima recomendada de comprimidos de Asacol é de cerca de 21 mg. Relatos publicados em ratos mostram que filhotes de ratos machos expostos in utero a DBP (maior ou igual a 100 mg/kg/dia, aproximadamente 39 vezes a dose humana com base na área de superfície corporal), exibem aberrações do sistema reprodutivo compatíveis com a interrupção da dependência androgênica desenvolvimento. O significado clínico deste achado em ratos é desconhecido. Em dosagens mais altas (maior ou igual a 500 mg/kg/dia, aproximadamente 194 vezes a dose humana com base na área de superfície corporal), efeitos adicionais, incluindo criptorquidia, hipospádia, atrofia ou agenesia de órgãos acessórios sexuais, lesão testicular, redução diária produção de espermatozóides, retenção permanente dos mamilos e diminuição da distância anogenital são observadas. A prole feminina não é afetada. Altas doses de DBP, administradas a ratas prenhas, foram associadas a maior incidência de anormalidades do desenvolvimento, como fenda palatina (maior ou igual a 630 mg/kg/dia, cerca de 244 vezes a dose humana, com base na área de superfície corporal) e anormalidades (maior ou igual a 750 mg/kg/dia, cerca de 290 vezes a dose humana com base na área de superfície corporal) na prole.
Mães que amamentam
mesalamina e seu metabólito N-acetil estão presentes no leite humano. Em estudos de lactação publicados, as doses maternas de mesalamina de várias formulações e produtos orais e retais variaram de 500 mg a 3 g por dia. A concentração de mesalamina no leite variou de não detectável a 0,11 mg/L. A concentração do metabólito ácido N-acetil-5-aminosalicílico variou de 5 a 18,1 mg/L. Com base nestas concentrações, as doses diárias estimadas para bebês em aleitamento materno exclusivo são de 0 a 0,017 mg/kg/dia de mesalamina e 0,75 a 2,72 mg/kg/dia de ácido N-acetil-5-aminosalicílico.
O dibutil ftalato (DBP), um ingrediente inativo no revestimento entérico dos comprimidos de Asacol 400mg, e seu metabólito primário monobutil ftalato (MBP) são excretados no leite humano. O significado clínico disso não foi determinado.
Os benefícios da amamentação para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de Asacol 400mg e quaisquer potenciais efeitos adversos na criança amamentada pelo medicamento ou pela condição materna subjacente. Tenha cuidado quando Asacol 400mg for administrado a uma mulher que amamenta.
Uso Pediátrico
A segurança e eficácia de Asacol 400mg em pacientes pediátricos de 5 a 17 anos de idade para o tratamento de colite ulcerativa leve a moderadamente ativa foram estabelecidas durante um período de 6 semanas. O uso de Asacol nestas faixas etárias é apoiado por evidências de estudos adequados e bem controlados de Asacol 400mg em adultos e um único estudo em pacientes pediátricos [ver REAÇÕES ADVERSAS , FARMACOLOGIA CLÍNICA e Estudos clínicos ].
Asacol 400mg foi estudado em um estudo randomizado, duplo-cego, de grupos paralelos, de 6 semanas de tratamento de dois níveis de dose de Asacol 400mg em 82 pacientes pediátricos de 5 a 17 anos de idade com colite ulcerativa leve a moderadamente ativa. Todos os pacientes foram divididos por categoria de peso (17 a menos de 33 kg, 33 a menos de 54 kg e 54 a 90 kg) e aleatoriamente designados para receber uma dose baixa (1,2, 2,0 e 2,4 g/dia para o respectivo peso categoria) ou uma dose alta (2,0, 3,6 e 4,8 g/dia). As visitas de linha de base e de triagem foram seguidas por um período de tratamento de 6 semanas [ver DOSAGEM E ADMINISTRAÇÃO ]. A dose alta não foi mais eficaz do que a dose baixa e não é uma dosagem aprovada [ver Estudos clínicos ].
A segurança e eficácia de Asacol em pacientes pediátricos com idade inferior a 5 anos não foram estabelecidas. A segurança e eficácia de Asacol na manutenção da remissão da colite ulcerosa em doentes pediátricos não foram estabelecidas.
Uso Geriátrico
Os estudos clínicos de Asacol não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se eles respondem de forma diferente dos indivíduos mais jovens. Outras experiências clínicas relatadas não identificaram diferenças na resposta entre os pacientes idosos e os mais jovens. Em geral, a maior frequência de diminuição da função hepática, renal ou cardíaca e de doença concomitante ou outra terapia medicamentosa em pacientes idosos deve ser considerada ao prescrever Asacol. Relatos de estudos clínicos não controlados e sistemas de notificação pós-comercialização sugerem uma maior incidência de discrasias sanguíneas, isto é, agranulocitose, neutropenia, pancitopenia, em indivíduos recebendo Asacol com 65 anos ou mais. Deve-se ter cuidado para monitorar de perto as contagens de células sanguíneas durante o tratamento com Asacol.
Insuficiência renal
Sabe-se que a mesalamina é substancialmente excretada pelos rins, e o risco de reações tóxicas a esta droga pode ser maior em pacientes com função renal comprometida. Como os pacientes idosos são mais propensos a ter função renal diminuída, deve-se ter cuidado ao prescrever esta terapia medicamentosa. Recomenda-se que todos os pacientes tenham uma avaliação da função renal antes do início da terapia com Asacol e periodicamente durante a terapia com Asacol [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES ].
SOBREDOSAGEM
Não há antídoto específico para superdosagem de mesalamina e o tratamento para suspeita de toxicidade aguda grave com Asacol deve ser sintomático e de suporte. Isso pode incluir a prevenção da absorção adicional do trato gastrointestinal, correção do desequilíbrio hidroeletrolítico e manutenção da função renal adequada. Asacol 400mg é um produto de liberação retardada dependente do pH e este fator deve ser considerado ao tratar uma suspeita de superdosagem.
CONTRA-INDICAÇÕES
Asacol é contraindicado em pacientes com hipersensibilidade conhecida aos salicilatos ou aminossalicilatos ou a qualquer um dos ingredientes de Asacol [ver AVISOS E PRECAUÇÕES , REAÇÕES ADVERSAS , e DESCRIÇÃO ].
ASACOL (mesalamina) comprimidos de liberação retardada, para uso oral
FARMACOLOGIA CLÍNICA
Mecanismo de ação
O mecanismo de ação da mesalamina é desconhecido, mas parece ser tópico e não sistêmico. A produção mucosa de metabólitos do ácido araquidônico, tanto pelas vias da ciclooxigenase, ou seja, prostanóides, quanto pelas vias da lipoxigenase, ou seja, leucotrienos e ácidos hidroxieicosatetraenóicos, está aumentada em pacientes com colite ulcerativa crônica, e é possível que a mesalamina diminua a inflamação por bloqueando a ciclooxigenase e inibindo a produção de prostaglandinas no cólon.
Farmacocinética
Absorção
Aproximadamente 28 por cento da mesalamina nos comprimidos de Asacol 400mg é absorvida após a ingestão oral. A absorção de mesalamina é semelhante em indivíduos em jejum e alimentados. O T max para mesalamina e seu metabólito, geralmente é retardado, refletindo a liberação retardada, e varia de 4 a 16 horas.
Metabolismo
A mesalamina absorvida é rapidamente acetilada na parede da mucosa intestinal e pelo fígado em ácido N-acetil-5aminosalicílico.
Excreção
A mesalamina absorvida é excretada principalmente pelos rins como ácido N-acetil-5-aminossalicílico. A mesalamina não absorvida é excretada nas fezes.
Após administração intravenosa, a meia-vida de eliminação da mesalamina é de aproximadamente 40 minutos. Após a administração oral, os valores terminais de t½ para mesalamina e ácido N-acetil-5-aminosalicílico são geralmente cerca de 12 horas, mas são variáveis, variando de 2 a 15 horas. Existe uma grande variabilidade inter-individual e intra-individual nas concentrações plasmáticas de mesalamina e ácido N-acetil-5aminosalicílico e nas suas semi-vidas de eliminação após a administração de Asacol.
Populações Específicas
Pacientes pediátricos
Em um estudo farmacocinético de variação de dose avaliando doses de 30, 60 e 90 mg/kg/dia de Asacol 400 mg administradas duas vezes ao dia por quatro semanas, os valores médios de Cavg de mesalamina em pacientes pediátricos com colite ulcerativa variaram de aproximadamente 400 ng/mL a 2100 ng /mL com base em dados de todos os níveis de dose.
Em um estudo em pacientes pediátricos com colite ulcerativa (Estudo 3), as concentrações plasmáticas médias de mesalamina (com base em amostragem esparsa) foram de 820 a 988 ng/mL no nível de dose baixa (ou seja, 1,2, 2,0 ou 2,4 g/dia com base em estratos de peso corporal de 17 a mais de 33 kg, 33 a menos de 54 kg e 54 a menos de 90 kg, respectivamente).
Toxicologia e/ou Farmacologia Animal
Em estudos com animais (ratos, camundongos, cães), o rim foi o principal órgão de toxicidade. (A seguir, as comparações da dosagem animal com a dosagem humana recomendada são baseadas na área de superfície corporal e uma dose de 2,4 g/dia para uma pessoa de 60 kg.)
mesalamina causa necrose papilar renal em ratos em doses únicas de aproximadamente 750 mg/kg a 1.000 mg/kg (aproximadamente 3 a 4 vezes a dose humana recomendada com base na área de superfície corporal). Doses de 170 e 360 mg/kg/dia (cerca de 0,7 e 1,5 vezes a dose humana recomendada com base na área de superfície corporal) administradas a ratos por seis meses produziram necrose papilar, edema papilar, degeneração tubular, mineralização tubular e hiperplasia urotelial.
Em camundongos, doses orais de 4.000 mg/kg/dia de mesalamina (aproximadamente 8 vezes a dose humana recomendada com base na área de superfície corporal) por três meses produziram nefrose tubular, inflamação túbulo-intersticial multifocal/difusa e necrose papilar multifocal/difusa.
Em cães, doses únicas de 6.000 mg (aproximadamente 8 vezes a dose humana recomendada com base na área de superfície corporal) de comprimidos de mesalamina de liberação retardada resultaram em necrose papilar renal, mas não foram fatais. Ocorreram alterações renais em cães que receberam administração crônica de mesalamina em doses de 80 mg/kg/dia (1,1 vezes a dose humana recomendada com base na área de superfície corporal).
Estudos clínicos
Tratamento da colite ulcerativa leve a moderadamente ativa
Adultos
Dois estudos controlados por placebo (Estudos 1 e 2) demonstraram a eficácia de Asacol comprimidos em pacientes com colite ulcerativa leve a moderadamente ativa.
Em um estudo multicêntrico, duplo-cego, randomizado com 158 pacientes (Estudo 1), doses de Asacol de 1,6 g/dia e 2,4 g/dia por 6 semanas foram comparadas ao placebo. O sistema de pontuação para determinação da eficácia do tratamento incluiu a avaliação da frequência das fezes, sangramento retal, achados sigmoidoscópicos, avaliação funcional do paciente e avaliação global do médico. Na dose de 2,4 g/dia, 21 de 43 (49 por cento) pacientes usando comprimidos de Asacol apresentaram melhora na aparência sigmoidoscópica do intestino em comparação com 12 de 44 (27 por cento) pacientes usando placebo (p = 0,048). Além disso, significativamente mais pacientes no grupo de comprimidos de Asacol 2,4 g/dia apresentaram melhora no sangramento retal e na frequência das fezes. A dose de 1,6 g/dia não produziu evidências consistentes de eficácia.
Em um segundo ensaio clínico randomizado, duplo-cego, controlado por placebo de 6 semanas de duração em 87 pacientes (Estudo 2), comprimidos de Asacol, na dose de 4,8 g/dia, por 6 semanas, resultou em melhora sigmoidoscópica em 28 de 38 (74 por cento) pacientes em comparação com 10 de 38 (26 por cento) pacientes com placebo (p menor que 0,001). Além disso, mais pacientes no grupo Asacol 400mg comprimidos 4,8 g/dia do que no grupo placebo apresentaram melhora nos sintomas gerais.
A dose de 4,8 g/dia não é uma dosagem aprovada para o tratamento de colite ulcerativa leve a moderadamente ativa.
Pediatria
A segurança e eficácia de Asacol 400mg em pacientes pediátricos de 5 a 17 anos de idade para o tratamento de colite ulcerativa leve a moderadamente ativa são apoiadas por evidências de estudos adequados e bem controlados de Asacol 400mg em adultos e um único estudo em pacientes pediátricos.
Um estudo randomizado, duplo-cego, de 6 semanas de 2 níveis de dose de Asacol (Estudo 3) foi realizado em 82 pacientes pediátricos de 5 a 17 anos de idade com colite ulcerativa leve ou moderadamente ativa. Todos os pacientes foram divididos por categoria de peso (17 a menos de 33 kg, 33 a menos de 54 kg e 54 a 90 kg) e aleatoriamente designados para receber uma dose baixa (1,2, 2,0 e 2,4 g/dia para o respectivo peso categoria) ou uma dose alta (2,0, 3,6 e 4,8 g/dia). As doses foram administradas a cada 12 horas.
proporção de pacientes que obtiveram sucesso com base no Truncated Mayo Score (TM-Mayo) (com base na frequência de fezes e nos subescores de sangramento retal do Mayo Score) e com base no Pediatric Ulcerative Colitis Activity Index (PUCAI) (que incluiu avaliação de dor abdominal, sangramento retal, consistência e frequência das fezes, presença de evacuações noturnas e nível de atividade) foi medido após 6 semanas de tratamento. O sucesso com base no TM-Mayo foi definido como resposta parcial (melhoria da linha de base na frequência de fezes ou subpontuações de sangramento retal sem piora no outro) ou resposta completa (frequência de fezes e subpontuação de sangramento retal igual a 0). O sucesso com base no PUCAI foi definido como resposta parcial (redução do PUCAI maior ou igual a 20 pontos da Linha de Base até a Semana 6 com pontuação da Semana 6 maior ou igual a 10) ou resposta completa (PUCAI menor que 10 na Semana 6).
Havia 41 pacientes no grupo de baixa dose e 41 pacientes no grupo de alta dose que receberam pelo menos uma dose de Asacol; 36 pacientes em cada grupo de dose completaram o estudo. Os pacientes foram considerados falhas de tratamento se não obtiveram sucesso ou desistiram devido a reação adversa ou falta de eficácia.
Na Semana 6, 73,2 por cento dos pacientes no grupo de baixa dose e 70,0 por cento dos pacientes no grupo de alta dose obtiveram sucesso com base no TM-Mayo; 34,1 por cento dos pacientes no grupo de baixa dose e 42,5 por cento dos pacientes no grupo de alta dose obtiveram resposta completa. Na Semana 6, 56,1 por cento dos pacientes no grupo de baixa dose e 55,0 por cento dos pacientes no grupo de alta dose obtiveram sucesso com base no PUCAI; 46,3 por cento dos pacientes no grupo de baixa dose e 42,5 por cento dos pacientes no grupo de alta dose obtiveram resposta completa.
A dose alta não foi mais eficaz do que a dose baixa e não é uma dosagem aprovada [ver DOSAGEM E ADMINISTRAÇÃO ].
Manutenção da remissão da colite ulcerativa em adultos
Um estudo multicêntrico, randomizado, duplo-cego, controlado por placebo, de 6 meses (Estudo 4) envolveu 264 pacientes tratados com comprimidos de Asacol 400mg 0,8 g/dia (n = 90), 1,6 g/dia (n = 87) , ou placebo (n = 87). No braço de 0,8 g/dia, os pacientes receberam doses duas vezes ao dia; no braço de 1,6 g/dia, os pacientes receberam quatro doses diárias. A proporção de pacientes tratados com 0,8 g/dia que mantiveram remissão endoscópica não foi estatisticamente significativa em comparação ao placebo. A proporção de pacientes em uso de comprimidos de Asacol 1,6 g/dia que mantiveram remissão endoscópica da colite ulcerativa foi de 61 de 87 (70,1 por cento) em comparação com 42 de 87 (48,3 por cento) de pacientes com placebo (p = 0,005).
Uma análise de eficácia combinada de 4 ensaios de manutenção comparou Asacol 400mg comprimidos, em doses de 0,8 g/dia a 2,8 g/dia, em doses divididas variando de duas vezes ao dia a quatro vezes ao dia, com sulfassalazina, em doses de 2 g/dia a 4g/dia. O sucesso do tratamento foi observado em 59 de 98 (59 por cento) pacientes usando comprimidos de Asacol e 70 de 102 (69 por cento) de pacientes usando sulfassalazina, uma diferença não significativa.
INFORMAÇÃO DO PACIENTE
- Instrua os pacientes a engolir os comprimidos de Asacol inteiros, tomando cuidado para não quebrar, cortar ou mastigar os comprimidos, porque o revestimento é uma parte importante da formulação de liberação retardada.
- Informe os pacientes que, se estiverem mudando de uma terapia oral anterior com mesalamina para Asacol, devem descontinuar sua terapia oral anterior com mesalamina e seguir as instruções de dosagem de Asacol. Informe os pacientes que eles não devem substituir dois comprimidos de Asacol 400 mg por um comprimido de Asacol 400 mg HD 800 mg [ver DOSAGEM E ADMINISTRAÇÃO ].
- Informar os pacientes que foram relatados nas fezes, cápsulas intactas, parcialmente intactas e/ou cápsulas de comprimidos. Instrua os pacientes a entrar em contato com seu médico se isso ocorrer repetidamente.
- Instrua os pacientes a proteger os comprimidos de Asacol 400mg da umidade. Instrua os pacientes a fechar bem o recipiente e a deixar quaisquer bolsas dessecantes presentes no frasco junto com os comprimidos.
- Aconselhe as mulheres grávidas, a amamentar ou em idade fértil que Asacol 400 mg contém ftalato de dibutilo, que foi associado a malformações e efeitos adversos no sistema reprodutor masculino em estudos com animais. O dibutilftalato é excretado no leite humano.
