Prometrium 100mg, 200mg Progesterone Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Prometrium 100mg e como é usado?
Prometrium 200mg é um medicamento de prescrição usado para prevenir tratar os sintomas da hiperplasia endometrial e os sintomas da amenorreia secundária (ausência de menstruação ou menstruação). Prometrium pode ser usado sozinho ou com outros medicamentos.
Prometrium pertence a uma classe de medicamentos chamados Progestins.
Não se sabe se Prometrium 200mg é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Prometrium?
Prometrium pode causar efeitos colaterais graves, incluindo:
- sangramento vaginal incomum,
- dor ou ardor ao urinar,
- nódulo na mama,
- problemas de visão súbitos,
- dor de cabeça severa,
- dor atrás dos olhos,
- depressão,
- problemas de sono,
- fraqueza,
- mudanca de humor,
- tontura severa,
- sonolência,
- sensação de giro,
- confusão,
- falta de ar,
- dor ou pressão no peito,
- dor se espalhando para a mandíbula ou ombro,
- náusea,
- sudorese,
- dor de estômago superior,
- coceira,
- cansaço,
- perda de apetite,
- urina de cor escura,
- fezes cor de barro,
- amarelecimento da pele ou dos olhos (icterícia),
- dormência ou fraqueza repentina,
- dor de cabeça súbita e intensa,
- fala arrastada ,
- dificuldade em falar ou se equilibrar,
- tosse repentina,
- chiado,
- respiração rápida,
- tossindo sangue,
- dor na perna,
- inchaço na perna e
- calor ou vermelhidão em uma ou ambas as pernas
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Prometrium 100mg incluem:
- sonolência,
- tontura,
- Dor no peito,
- mudanca de humor,
- dor de cabeça,
- constipação,
- diarréia,
- azia,
- inchaço,
- inchaço nas mãos ou pés,
- dores nas articulações,
- ondas de calor, e
- corrimento vaginal
Informe o seu médico se tiver algum efeito secundário que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Prometrium. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
DISTÚRBIOS CARDIOVASCULARES, CÂNCER DE MAMA E PROVÁVEL DEMÊNCIA PARA TERAPIA COM ESTROGÊNIO MAIS PROGESTINA
Distúrbios Cardiovasculares e Provável Demência
A terapia com estrogênios e progesterona não deve ser usada para a prevenção de doenças cardiovasculares ou demência. (Ver Estudos clínicos e AVISOS , Distúrbios cardiovasculares e demência provável. )
O subestudo da Iniciativa de Saúde da Mulher (WHI) com estrogênio mais progestina relatou riscos aumentados de trombose venosa profunda, embolia pulmonar, acidente vascular cerebral e infarto do miocárdio em mulheres na pós-menopausa (50 a 79 anos de idade) durante 5,6 anos de tratamento com conjugado oral diário estrogênios (CE) [0,625 mg] combinados com acetato de medroxiprogesterona (MPA) [2,5 mg], em relação ao placebo. (Ver Estudos clínicos e AVISOS , Distúrbios cardiovasculares. )
O WHI Memory Study (WHIMS) estudo auxiliar de estrogênio mais progestina do WHI relatou um risco aumentado de desenvolver provável demência em mulheres na pós-menopausa com 65 anos de idade ou mais durante 4 anos de tratamento com CE diário (0,625 mg) combinado com MPA (2,5 mg ), em relação ao placebo. Não se sabe se este achado se aplica a mulheres pós-menopáusicas mais jovens. (Ver Estudos clínicos e AVISOS , Provável demência e PRECAUÇÕES , Uso Geriátrico .)
Câncer de mama
subestudo WHI de estrogênio mais progestina também demonstrou um risco aumentado de câncer de mama invasivo. (Ver Estudos clínicos e AVISOS , Neoplasias malignas, câncer de mama .)
Na ausência de dados comparáveis, esses riscos devem ser considerados semelhantes para outras doses de CE e MPA, e outras combinações e formas de dosagem de estrogênios e progestágenos.
As progestinas com estrogênios devem ser prescritas nas doses efetivas mais baixas e pela menor duração consistente com os objetivos e riscos do tratamento para cada mulher.
DESCRIÇÃO
As cápsulas de PROMETRIUM (progesterona, USP) contêm progesterona micronizada para administração oral. A progesterona tem um peso molecular de 314,47 e uma fórmula molecular de C21H30O2. A progesterona (pregn-4-ene-3, 20-diona) é um pó cristalino branco ou cremoso, inodoro, praticamente insolúvel em água, solúvel em álcool, acetona e dioxano e pouco solúvel em óleos vegetais, estável ao ar, fundindo-se entre 126° e 131°C. A fórmula estrutural é:
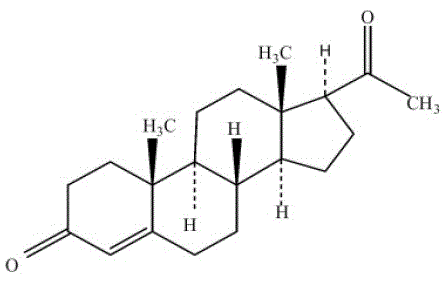
progesterona é sintetizada a partir de um material de partida de uma fonte vegetal e é quimicamente idêntica à progesterona de origem ovariana humana. As cápsulas PROMETRIUM estão disponíveis em várias dosagens para proporcionar flexibilidade de dosagem para um gerenciamento ideal. As cápsulas de PROMETRIUM contêm 100 mg ou 200 mg de progesterona micronizada.
Os ingredientes inativos para PROMETRIUM Cápsulas 100 mg incluem: óleo de amendoim NF, gelatina NF, glicerina USP, lecitina NF, dióxido de titânio USP, FD&C Vermelho Nº 40 e D&C Amarelo Nº 10. Os ingredientes inativos para PROMETRIUM 100 mg Cápsulas 200 mg incluem : óleo de amendoim NF, gelatina NF, glicerina USP, lecitina NF, dióxido de titânio USP, D&C Amarelo nº 10 e FD&C Amarelo nº 6.
INDICAÇÕES
As cápsulas de PROMETRIUM 200mg são indicadas para uso na prevenção da hiperplasia endometrial em mulheres pós-menopáusicas não histerectomizadas que estejam recebendo comprimidos de estrogênios conjugados. Eles também são indicados para uso na amenorreia secundária.
DOSAGEM E ADMINISTRAÇÃO
Prevenção da hiperplasia endometrial
As cápsulas de PROMETRIUM 100mg devem ser administradas em dose única diária ao deitar, 200 mg por via oral durante 12 dias sequencialmente por ciclo de 28 dias, a uma mulher pós-menopáusica com útero que esteja a receber diariamente comprimidos de estrogénios conjugados.
Tratamento da amenorreia secundária
As cápsulas de PROMETRIUM 100mg podem ser administradas em dose única diária de 400 mg ao deitar por 10 dias.
Algumas mulheres podem ter dificuldade em engolir as cápsulas de PROMETRIUM. Para estas mulheres, as cápsulas de PROMETRIUM devem ser tomadas com um copo de água em pé.
COMO FORNECIDO
PROMETRIUM (progesterona, USP) Cápsulas 100 mg são cápsulas redondas, cor de pêssego, marcadas com a impressão preta “SV”.
NDC 0032-1708-01 (Garrafa de 100)
PROMETRIUM (progesterona, USP) Cápsulas 200 mg são cápsulas ovais, de cor amarelo-pálido, marcadas com a impressão preta “SV2”.
NDC 0032-1711-01 (Garrafa de 100)
Armazenar a 25°C (77°F); excursões permitidas de 15° a 30°C (59° a 86°F) [Consulte Temperatura ambiente controlada pela USP].
Proteger da umidade excessiva.
Dispensar em recipiente hermético e resistente à luz, conforme definido em USP/NF, acompanhado de um folheto do paciente.
Mantenha fora do alcance de crianças.
Fabricado por: Catalent Pharma Solutions, São Petersburgo, FL 33716. Revisado: setembro de 2013
EFEITOS COLATERAIS
Ver AVISO DE CAIXA , AVISOS e PRECAUÇÕES .
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
Em um ensaio clínico multicêntrico, randomizado, duplo-cego, controlado por placebo, os efeitos de PROMETRIUM 100mg cápsulas no endométrio foram estudados em um total de 875 mulheres na pós-menopausa. A Tabela 6 lista as reações adversas maiores ou iguais a 2 por cento das mulheres que receberam cápsulas de PROMETRIUM cíclico 200 mg por dia (12 dias por ciclo de mês de calendário) com 0,625 mg de estrogênios conjugados ou placebo.
TABELA 6. Reações adversas (≥ 2%) relatadas em um estudo controlado por placebo de 875 pacientes em mulheres na pós-menopausa ao longo de um período de 3 anos [Porcentagem (%) de relatos de pacientes]
Efeitos sobre a amenorreia secundária
Em um ensaio clínico multicêntrico, randomizado, duplo-cego, controlado por placebo, os efeitos de PROMETRIUM Capsules na amenorreia secundária foram estudados em 49 mulheres pós-menopáusicas preparadas com estrogênio. A Tabela 7 lista as reações adversas maiores ou iguais a 5% das mulheres que receberam PROMETRIUM 100mg Cápsulas ou placebo.
TABELA 7. Reações adversas (≥ 5%) relatadas em pacientes usando 400 mg/dia em um estudo controlado por placebo em mulheres pós-menopáusicas preparadas com estrogênio
Em um estudo de dosagem pós-comercialização multicêntrico, de grupos paralelos, aberto, consistindo em três ciclos de tratamento consecutivos de 28 dias, 220 mulheres na pré-menopausa com amenorreia secundária foram randomizadas para receber terapia diária com estrogênios conjugados (0,625 mg de estrogênios conjugados) e PROMETRIUM 100 mg cápsulas, 300 mg por dia (n=113) ou PROMETRIUM Cápsulas, 400 mg por dia (n=107) por 10 dias de cada ciclo de tratamento. No geral, as reações adversas emergentes do tratamento relatadas com mais frequência, relatadas em mais ou igual a 5% dos indivíduos, foram náusea, fadiga, micose vaginal, nasofaringite, infecção do trato respiratório superior, dor de cabeça, tontura, sensibilidade mamária, distensão abdominal, acne , dismenorreia, alteração de humor e infecção do trato urinário.
Experiência pós-marketing
As seguintes reações adversas adicionais foram relatadas com PROMETRIUM 200mg cápsulas. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança a frequência ou estabelecer uma relação causal com a exposição ao medicamento.
Aparelho geniturinário
carcinoma endometrial, hipospádia, morte intra-uterina, menorragia, distúrbio menstrual, metrorragia, cisto ovariano, aborto espontâneo.
Cardiovascular
colapso circulatório, cardiopatia congênita (incluindo defeito do septo ventricular e persistência do canal arterial), hipertensão, hipotensão, taquicardia.
Gastrointestinal
pancreatite aguda, colestase, hepatite colestática, disfagia, insuficiência hepática, necrose hepática, hepatite, aumento dos testes de função hepática (incluindo aumento da alanina aminotransferase, aumento da aspartato aminotransferase, aumento da gama-glutamil transferase), icterícia, inchaço da língua.
Pele
alopecia, prurido, urticária.
Olhos
visão turva, diplopia, distúrbios visuais.
Sistema nervoso central
agressão, convulsão, despersonalização, consciência deprimida, desorientação, disartria, perda de consciência, parestesia, sedação, estupor, síncope (com e sem hipotensão), ataque isquêmico transitório, ideação suicida.
Durante a terapia inicial, algumas mulheres experimentaram uma constelação de muitos ou todos os seguintes sintomas: tontura extrema e/ou sonolência, visão turva, fala arrastada, dificuldade para andar, perda de consciência, vertigem, confusão, desorientação, sensação de embriaguez e falta de ar.
Diversos
marcha anormal, reação anafilática, artralgia, aumento da glicemia, asfixia, lábio leporino, fenda palatina, dificuldade para andar, dispneia, edema facial, sensação anormal, sensação de embriaguez, hipersensibilidade, asma, cãibras musculares, aperto na garganta, zumbido, vertigem, diminuição do peso , o peso aumentou.
INTERAÇÕES MEDICAMENTOSAS
Interações de testes de laboratório de drogas
Os seguintes resultados laboratoriais podem ser alterados pelo uso de terapia com estrogênio mais progestina:
- Aumento da retenção de sulfobromoftaleína e outros testes de função hepática.
- Testes de coagulação: aumento dos fatores de protrombina VII, VIII, IX e X.
- Determinação de pregnanodiol.
- Função da tireoide: aumento no PBI e iodo ligado à proteína extraível com butanol e diminuição no T3 valores de captação.
AVISOS
Ver AVISO DE CAIXA .
Distúrbios Cardiovasculares
Um risco aumentado de embolia pulmonar, trombose venosa profunda (TVP), acidente vascular cerebral e infarto do miocárdio foi relatado com terapia com estrogênio mais progestina. Caso ocorram ou se suspeite de algum destes casos, a terapia com estrogênio com progesterona deve ser descontinuada imediatamente.
Fatores de risco para doença vascular arterial (por exemplo, hipertensão, diabetes mellitus, tabagismo, hipercolesterolemia e obesidade) e/ou tromboembolismo venoso (por exemplo, história pessoal ou familiar de tromboembolismo venoso [TEV], obesidade e lúpus eritematoso sistêmico ) devem ser gerenciados adequadamente.
Derrame
No subestudo da Women's Health Initiative (WHI) estrogênio mais progestina, um aumento estatisticamente significativo do risco de acidente vascular cerebral foi relatado em mulheres de 50 a 79 anos de idade recebendo CE (0,625 mg) mais MPA (2,5 mg) diariamente em comparação com mulheres da mesma idade grupo que recebeu placebo (33 versus 25 por 10.000 mulheres-ano). O aumento do risco foi demonstrado após o primeiro ano e persistiu. (Ver Estudos clínicos .) Se ocorrer ou houver suspeita de acidente vascular cerebral, a terapia com estrogênio e progesterona deve ser descontinuada imediatamente.
Doença Coronária
No subestudo WHI de estrogênio mais progestina, houve um aumento estatisticamente não significativo do risco de eventos de doença cardíaca coronária (DAC) (definidos como infarto do miocárdio não fatal [IM], MI silencioso ou morte por DAC) relatado em mulheres que receberam CE diariamente (0,625 mg) mais MPA (2,5 mg) em comparação com as mulheres que receberam placebo (41 versus 34 por 10.000 mulheres-ano). Um aumento no risco relativo foi demonstrado no ano 1 e uma tendência de diminuição do risco relativo foi relatada nos anos 2 a 5. (Consulte Estudos clínicos .)
Em mulheres na pós-menopausa com doença cardíaca documentada (n = 2.763, idade média de 66,7 anos), em um ensaio clínico controlado de prevenção secundária de doença cardiovascular (Estudo de reposição de estrogênio/progesterona [HERS]), tratamento com CE diário (0,625 mg) mais MPA (2,5 mg) não demonstraram benefício cardiovascular. Durante um acompanhamento médio de 4,1 anos, o tratamento com CE mais MPA não reduziu a taxa geral de eventos de DAC em mulheres na pós-menopausa com doença cardíaca coronária estabelecida. Houve mais eventos de DAC no grupo tratado com CE mais MPA do que no grupo placebo no ano 1, mas não durante os anos subsequentes. Duas mil trezentas e vinte e uma (2.321) mulheres do estudo HERS original concordaram em participar de uma extensão aberta do HERS, HERS II. O seguimento médio no HERS II foi de 2,7 anos adicionais, totalizando 6,8 anos no total. As taxas de eventos de DAC foram comparáveis entre as mulheres no grupo CE mais MPA e no grupo placebo no HERS, HERS II e em geral.
Tromboembolismo venoso
No subestudo WHI de estrogênio mais progestina, uma taxa estatisticamente significativa 2 vezes maior de TEV (TVP e embolia pulmonar [EP]) foi relatada em mulheres que receberam CE diariamente (0,625 mg) mais MPA (2,5 mg) em comparação com mulheres que receberam placebo ( 35 versus 17 por 10.000 mulheres-ano). Aumentos estatisticamente significativos no risco de TVP (26 versus 13 por 10.000 mulheres-ano) e PE (18 versus 8 por 10.000 mulheres-ano) também foram demonstrados. O aumento do risco de TEV foi demonstrado durante o primeiro ano e persistiu. (Ver Estudos clínicos .) Se ocorrer ou houver suspeita de TEV, a terapia com estrogênio e progesterona deve ser descontinuada imediatamente.
Se possível, os estrogênios com progestágenos devem ser descontinuados pelo menos 4 a 6 semanas antes da cirurgia do tipo associado a um risco aumentado de tromboembolismo ou durante períodos de imobilização prolongada.
Neoplasias malignas
Câncer de mama
ensaio clínico randomizado mais importante que fornece informações sobre câncer de mama em usuárias de estrogênio mais progestina é o subestudo da Women's Health Initiative (WHI) de CE diário (0,625 mg) mais MPA (2,5 mg). Após um acompanhamento médio de 5,6 anos, o subestudo de estrogênio mais progestina relatou um risco aumentado de câncer de mama invasivo em mulheres que tomaram CE mais MPA diariamente. Neste subestudo, o uso prévio de terapia com estrogênio isolado ou estrogênio mais progestina foi relatado por 26% das mulheres. O risco relativo de câncer de mama invasivo foi de 1,24 (95 por cento nCI, 1,01-1,54), e o risco absoluto foi de 41 versus 33 casos por 10.000 mulheres-ano, para CE mais MPA em comparação com placebo. Entre as mulheres que relataram uso prévio de terapia hormonal, o risco relativo de câncer de mama invasivo foi de 1,86, e o risco absoluto foi de 46 versus 25 casos por 10.000 mulheres-ano, para estrogênio mais progesterona em comparação com placebo. Entre as mulheres que não relataram uso prévio de terapia hormonal, o risco relativo de câncer de mama invasivo foi de 1,09, e o risco absoluto foi de 40 versus 36 casos por 10.000 mulheres-ano para CE mais MPA em comparação com placebo. No mesmo subestudo, os cânceres de mama invasivos eram maiores, eram mais propensos a ser linfonodo positivo e foram diagnosticados em um estágio mais avançado no grupo CE (0,625 mg) mais MPA (2,5 mg) em comparação com o grupo placebo. A doença metastática foi rara, sem diferença aparente entre os dois grupos. Outros fatores prognósticos como subtipo histológico, grau e status do receptor hormonal não diferiram entre os grupos. (Ver Estudos clínicos .)
Consistente com os ensaios clínicos do WHI, estudos observacionais também relataram um risco aumentado de câncer de mama para terapia com estrogênio mais progestina, e um risco menor para terapia com estrogênio isolado, após vários anos de uso. O risco aumentou com a duração do uso e pareceu retornar à linha de base cerca de 5 anos após a interrupção do tratamento (somente os estudos observacionais têm dados substanciais sobre o risco após a interrupção). Estudos observacionais também sugerem que o risco de câncer de mama foi maior e se tornou aparente mais cedo, com a terapia com estrogênio mais progestina em comparação com a terapia com estrogênio isolado. No entanto, esses estudos geralmente não encontraram variação significativa no risco de câncer de mama entre diferentes combinações, doses ou vias de administração de estrogênio mais progestina.
Foi relatado que o uso de estrogênio mais progestina resulta em um aumento de mamografias anormais que requerem avaliação adicional. Todas as mulheres devem fazer exames de mama anualmente por um profissional de saúde e realizar autoexames mensais das mamas. Além disso, os exames de mamografia devem ser agendados com base na idade da paciente, fatores de risco e resultados de mamografias anteriores.
Câncer do endométrio
Um risco aumentado de câncer de endométrio foi relatado com o uso de terapia de estrogênio sem oposição em uma mulher com útero. O risco de câncer endometrial relatado entre usuárias de estrogênio sem oposição é cerca de 2 a 12 vezes maior do que em não usuárias e parece depender da duração do tratamento e da dose de estrogênio. A maioria dos estudos não mostra aumento significativo do risco associado ao uso de estrogênios por menos de 1 ano. O maior risco parece estar associado ao uso prolongado, com riscos aumentados de 15 a 24 vezes por 5 a 10 anos ou mais e esse risco persiste por pelo menos 8 a 15 anos após a descontinuação da terapia com estrogênio.
vigilância clínica de todas as mulheres em uso de terapia com estrogênio e progesterona é importante. Medidas diagnósticas adequadas, incluindo amostragem endometrial direcionada ou aleatória quando indicada, devem ser tomadas para descartar malignidade em todos os casos de sangramento genital anormal persistente ou recorrente não diagnosticado. Não há evidências de que o uso de estrogênios naturais resulte em um perfil de risco endometrial diferente dos estrogênios sintéticos de dose equivalente de estrogênio. A adição de uma progestina à terapia com estrogênio em mulheres na pós-menopausa demonstrou reduzir o risco de hiperplasia endometrial, que pode ser um precursor do câncer endometrial.
Cancro do ovário
subestudo WHI de estrogênio mais progestina relatou um aumento estatisticamente não significativo do risco de câncer de ovário. Após um acompanhamento médio de 5,6 anos, o risco relativo de câncer de ovário para CE mais MPA versus placebo foi de 1,58 (95% nCI, 0,77 – 3,24). O risco absoluto de EC mais MPA versus placebo foi de 4 versus 3 casos por 10.000 mulheres-ano. Em alguns estudos epidemiológicos, o uso de estrogênio mais progesterona e produtos apenas com estrogênio, em particular por 5 ou mais anos, foi associado a um risco aumentado de câncer de ovário. No entanto, a duração da exposição associada ao aumento do risco não é consistente em todos os estudos epidemiológicos e alguns relatam nenhuma associação.
Provável demência
No Estudo de Memória da Iniciativa de Saúde da Mulher (WHIMS) de estrogênio mais progestina, um estudo auxiliar do WHI, uma população de 4.532 mulheres na pós-menopausa de 65 a 79 anos de idade foi randomizada para CE diário (0,625 mg) mais MPA (2,5 mg) ou placebo.
No estudo auxiliar WHIMS estrogênio mais progestina, após um acompanhamento médio de 4 anos, 40 mulheres no grupo CE mais MPA e 21 mulheres no grupo placebo foram diagnosticadas com provável demência. O risco relativo de demência provável para estrogênio mais progestina versus placebo foi de 2,05 (IC de 95%, 1,21-3,48). O risco absoluto de demência provável para EC mais MPA versus placebo foi de 45 versus 22 casos por 10.000 mulheres-ano. Não se sabe se esses achados se aplicam a mulheres pós-menopáusicas mais jovens. (Ver Estudos clínicos e PRECAUÇÕES , Uso Geriátrico .)
Anormalidades da Visão
Trombose vascular retiniana foi relatada em pacientes recebendo estrogênio. Interrompa a terapia com estrogênio mais progestina enquanto aguarda o exame se houver perda súbita parcial ou completa da visão, ou se houver um início súbito de proptose, diplopia ou enxaqueca. Se o exame revelar papiledema ou lesões vasculares retinianas, a terapia com estrogênio mais progestina deve ser descontinuada permanentemente.
PRECAUÇÕES
Em geral
Adição de uma progestina quando uma mulher não teve uma histerectomia
Estudos da adição de uma progestina por 10 ou mais dias de um ciclo de administração de estrogênio, ou diariamente com estrogênio em um regime contínuo, relataram uma incidência menor de hiperplasia endometrial do que seria induzida pelo tratamento com estrogênio isolado. A hiperplasia endometrial pode ser um precursor do câncer endometrial.
Existem, no entanto, possíveis riscos que podem estar associados ao uso de progestágenos com estrogênios em comparação com regimes de estrogênio isolado. Estes incluem um risco aumentado de câncer de mama.
Retenção de fluidos
A progesterona pode causar algum grau de retenção de líquidos. Mulheres com condições que podem ser influenciadas por esse fator, como disfunção cardíaca ou renal, merecem observação cuidadosa.
Tontura e sonolência
PROMETRIUM Cápsulas pode causar tontura e sonolência transitórias e deve ser usado com cautela ao dirigir veículos motorizados ou operar máquinas. As cápsulas de PROMETRIUM devem ser tomadas em dose única diária ao deitar.
Informação do paciente
Em geral
Este produto contém óleo de amendoim e não deve ser usado se você for alérgico a amendoim.
Os médicos são aconselhados a discutir o conteúdo do folheto informativo do paciente com os pacientes para os quais prescrevem PROMETRIUM 100mg cápsulas.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
A progesterona não foi testada quanto à carcinogenicidade em animais por via oral de administração. Quando implantada em camundongos fêmeas, a progesterona produziu carcinomas mamários, tumores de células da granulosa ovariana e sarcomas do estroma endometrial. Em cães, injeções intramusculares de longa duração produziram hiperplasia nodular e tumores mamários benignos e malignos. Injeções subcutâneas ou intramusculares de progesterona diminuíram o período de latência e aumentaram a incidência de tumores mamários em ratas previamente tratadas com carcinógeno químico.
progesterona não mostrou evidência de genotoxicidade em estudos in vitro para mutações pontuais ou para danos cromossômicos. Estudos in vivo para danos cromossômicos produziram resultados positivos em camundongos em doses orais de 1.000 mg/kg e 2.000 mg/kg. A progesterona administrada exogenamente demonstrou inibir a ovulação em várias espécies e espera-se que altas doses administradas por um período prolongado prejudiquem a fertilidade até a interrupção do tratamento.
Gravidez
As cápsulas de PROMETRIUM não devem ser utilizadas durante a gravidez. (Ver CONTRA-INDICAÇÕES ).
Gravidez Categoria B
Estudos reprodutivos foram realizados em camundongos com doses de até 9 vezes a dose oral humana, em ratos com doses até 44 vezes a dose oral humana, em coelhos com uma dose de 10 mcg/dia administrada localmente no útero por um dispositivo implantado , em cobaias em doses de aproximadamente metade da dose oral humana e em macacos rhesus em doses aproximadamente da dose humana, todas baseadas na área de superfície corporal, e revelaram pouca ou nenhuma evidência de fertilidade prejudicada ou dano ao feto devido a progesterona.
Mulheres que amamentam
Quantidades detectáveis de progesterona foram identificadas no leite de lactantes recebendo progestinas. Deve-se ter cautela quando as cápsulas de PROMETRIUM 100mg são administradas a uma lactante.
Uso Pediátrico
As cápsulas de PROMETRIUM não são indicadas em crianças. Não foram realizados estudos clínicos na população pediátrica.
Uso Geriátrico
Não houve um número suficiente de mulheres geriátricas envolvidas em estudos clínicos utilizando PROMETRIUM cápsulas para determinar se aquelas com mais de 65 anos de idade diferem de indivíduos mais jovens em sua resposta a PROMETRIUM 200mg cápsulas.
Estudo da Iniciativa de Saúde da Mulher
No subestudo da Women's Health Initiative (WHI) estrogênio mais progestina (CE diário [0,625 mg] mais MPA [2,5 mg] versus placebo), houve um risco relativo maior de acidente vascular cerebral não fatal e câncer de mama invasivo em mulheres com mais de 65 anos de idade . (Ver Estudos clínicos e AVISOS , Distúrbios cardiovasculares e Neoplasias malignas. )
Estudo de Memória da Iniciativa de Saúde da Mulher
No Estudo de Memória da Iniciativa de Saúde da Mulher (WHIMS) de mulheres na pós-menopausa de 65 a 79 anos de idade, houve um risco aumentado de desenvolver provável demência no estudo auxiliar de estrogênio mais progestina quando comparado ao placebo. (Ver Estudos clínicos e AVISOS , Provável demência. )
SOBREDOSAGEM
Não foram realizados estudos sobre superdosagem em humanos. Em caso de superdosagem, PROMETRIUM Capsules deve ser descontinuado e o paciente deve ser tratado sintomaticamente.
CONTRA-INDICAÇÕES
As cápsulas de PROMETRIUM não devem ser usadas em mulheres com qualquer uma das seguintes condições:
FARMACOLOGIA CLÍNICA
As cápsulas PROMETRIUM 200mg são uma forma de dosagem oral de progesterona micronizada que é quimicamente idêntica à progesterona de origem ovariana. A biodisponibilidade oral da progesterona é aumentada através da micronização.
Farmacocinética
Absorção
Após a administração oral de progesterona na forma de cápsula de gelatina mole micronizada, as concentrações séricas máximas foram atingidas em 3 horas. A biodisponibilidade absoluta da progesterona micronizada não é conhecida. A Tabela 1 resume os parâmetros farmacocinéticos médios em mulheres pós-menopáusicas após cinco doses orais diárias de PROMETRIUM Cápsulas 100 mg como uma formulação de cápsula de gelatina mole micronizada.
TABELA 1. Parâmetros Farmacocinéticos das Cápsulas de 200mg de PROMETRIUM
As concentrações séricas de progesterona mostraram-se lineares e proporcionais à dose após a administração de doses múltiplas de PROMETRIUM 200 mg Cápsulas 100 mg na faixa de dose de 100 mg por dia a 300 mg por dia em mulheres na pós-menopausa. Embora não tenham sido estudadas doses superiores a 300 mg por dia em mulheres, as concentrações séricas de um estudo em voluntários do sexo masculino pareceram lineares e proporcionais à dose entre 100 mg por dia e 400 mg por dia. Os parâmetros farmacocinéticos em voluntários do sexo masculino foram geralmente consistentes com os observados em mulheres na pós-menopausa.
Distribuição
A progesterona é aproximadamente 96% a 99% ligada às proteínas séricas, principalmente à albumina sérica (50 a 54%) e transcortina (43 a 48%).
Metabolismo
progesterona é metabolizada principalmente pelo fígado em grande parte em pregnanodiois e pregnanolonas. Pregnanodiois e pregnanolonas são conjugados no fígado com metabólitos glicuronídeos e sulfatos. Os metabólitos da progesterona que são excretados na bile podem ser desconjugados e posteriormente metabolizados no intestino por meio de redução, desidroxilação e epimerização.
Excreção
Os conjugados de glicuronídeo e sulfato de pregnanodiol e pregnanolona são excretados na bile e na urina. Os metabólitos da progesterona são eliminados principalmente pelos rins. Os metabólitos da progesterona que são excretados na bile podem sofrer reciclagem entero-hepática ou podem ser excretados nas fezes.
Populações Especiais
A farmacocinética de PROMETRIUM Cápsulas não foi avaliada em pacientes com baixo peso corporal ou obesos.
Insuficiência Hepática
O efeito da insuficiência hepática na farmacocinética de PROMETRIUM 100mg cápsulas não foi estudado.
Insuficiência renal
O efeito da insuficiência renal na farmacocinética de PROMETRIUM Capsules não foi estudado.
Interação Alimento-Droga
A ingestão concomitante de alimentos aumentou a biodisponibilidade de PROMETRIUM 100mg cápsulas em relação a um estado de jejum quando administrado a mulheres na pós-menopausa na dose de 200 mg.
Interações medicamentosas
O metabolismo da progesterona pelos microssomas hepáticos humanos foi inibido pelo cetoconazol (IC50
coadministração de estrogênios conjugados e PROMETRIUM 200mg cápsulas a 29 mulheres na pós-menopausa durante um período de 12 dias resultou em um aumento nas concentrações totais de estrona (Cmax 3,68 ng/mL a 4,93 ng/mL) e concentrações totais de equilina (Cmax 2,27 ng/mL a 3,22 ng/mL) e uma diminuição nas concentrações circulantes de 17β estradiol (Cmax 0,037 ng/mL a 0,030 ng/mL). A meia-vida dos estrogênios conjugados foi semelhante com a coadministração de PROMETRIUM Capsules. A Tabela 2 resume os parâmetros farmacocinéticos.
TABELA 2. Parâmetros farmacocinéticos médios (± SD) para estradiol, estrona e equilina após coadministração de estrogênios conjugados 0,625 mg e cápsulas de PROMETRIUM 200 mg por 12 dias para mulheres na pós-menopausa
Estudos clínicos
Efeitos sobre o endométrio
Em um ensaio clínico randomizado, duplo-cego, 358 mulheres na pós-menopausa, cada uma com um útero intacto, receberam tratamento por até 36 meses. Os grupos de tratamento foram: PROMETRIUM Cápsulas na dose de 200 mg por dia durante 12 dias por ciclo de 28 dias em combinação com estrogênios conjugados 0,625 mg por dia (n=120); estrogênios conjugados 0,625 mg por dia apenas (n=119); ou placebo (n=119). Os sujeitos em todos os três grupos de tratamento eram principalmente mulheres caucasianas (87 por cento ou mais de cada grupo). Os resultados para a incidência de hiperplasia endometrial em mulheres que receberam até 3 anos de tratamento são mostrados na Tabela 3. Uma comparação do grupo de tratamento com cápsulas de PROMETRIUM mais estrogênios conjugados com o grupo de apenas estrogênios conjugados mostrou uma taxa significativamente menor de hiperplasia (6 por cento produto combinado versus 64 por cento de estrogênio sozinho) no grupo de tratamento PROMETRIUM Cápsulas mais estrogênios conjugados ao longo de 36 meses de tratamento.
TABELA 3. Incidência de Hiperplasia Endometrial em Mulheres Recebendo 3 Anos de Tratamento
Os tempos de diagnóstico de hiperplasia endometrial ao longo de 36 meses de tratamento são mostrados na Figura 1. Esta figura ilustra graficamente que a proporção de pacientes com hiperplasia foi significativamente maior para o grupo de estrogênios conjugados (64 por cento) em comparação com o grupo de estrogênios conjugados mais cápsulas de PROMETRIUM (6 por cento).
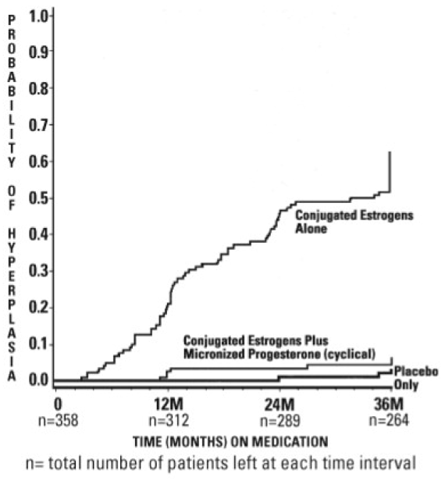
Figura 1. Tempo para Hiperplasia em Mulheres Recebendo até 36 Meses de Tratamento
As taxas de descontinuação devido à hiperplasia ao longo dos 36 meses de tratamento são mostradas na Tabela 4. Para qualquer grau de hiperplasia, a taxa de descontinuação para pacientes que receberam estrogênios conjugados mais PROMETRIUM 100mg cápsulas foi semelhante à do grupo placebo, enquanto o a taxa de descontinuação para pacientes que receberam apenas estrogênios conjugados foi significativamente maior. As mulheres que descontinuaram permanentemente o tratamento devido à hiperplasia foram semelhantes em demografia à população geral do estudo.
TABELA 4. Taxa de descontinuação devido a hiperplasia ao longo de 36 meses de tratamento
Efeitos sobre a amenorreia secundária
Em um estudo clínico de centro único, randomizado e duplo-cego que incluiu mulheres na pré-menopausa com amenorreia secundária por pelo menos 90 dias, a administração de 10 dias de terapia com PROMETRIUM 200mg cápsulas resultou em 80% das mulheres experimentando sangramento de privação dentro de 7 dias após o último dose de PROMETRIUM 100mg Cápsulas, 300 mg por dia (n=20), em comparação com 10 por cento das mulheres com sangramento de privação no grupo placebo (n=21).
Em um estudo de dosagem pós-comercialização multicêntrico, de grupos paralelos, aberto, que incluiu mulheres na pré-menopausa com amenorreia secundária por pelo menos 90 dias, administração de 10 dias de PROMETRIUM 100mg cápsulas durante dois ciclos de tratamento de 28 dias, 300 mg por dia (n= 107) ou 400 mg por dia (n = 99), resultou em 73,8 por cento e 76,8 por cento das mulheres, respectivamente, experimentando sangramento de privação.
taxa de transformação secretora foi avaliada em um estudo clínico multicêntrico, randomizado e duplo-cego em mulheres pós-menopáusicas preparadas com estrogênio. PROMETRIUM 100mg Cápsulas administradas por via oral durante 10 dias a 400 mg por dia (n=22) induziram alterações secretórias completas no endométrio em 45 por cento das mulheres em comparação com 0 por cento no grupo placebo (n=23).
Um segundo estudo de dosagem pós-comercialização multicêntrico, de grupos paralelos e aberto em mulheres na pré-menopausa com amenorreia secundária por pelo menos 90 dias também avaliou a taxa de transformação secretora. Todos os indivíduos receberam diariamente estrogênios conjugados orais durante 3 ciclos de tratamento consecutivos de 28 dias e cápsulas de PROMETRIUM, 300 mg por dia (n=107) ou 400 mg por dia (n=99) por 10 dias de cada ciclo de tratamento. A taxa de transformação completa da secreção foi de 21,5 por cento e 28,3 por cento, respectivamente.
Estudos da Iniciativa de Saúde da Mulher
Women's Health Initiative (WHI) recrutou aproximadamente 27.000 mulheres pós-menopáusicas predominantemente saudáveis em dois subestudos para avaliar os riscos e benefícios dos estrogênios conjugados orais (CE) diários [0,625 mg] sozinhos ou em combinação com acetato de medroxiprogesterona (MPA) [2,5 mg] comparado ao placebo na prevenção de certas doenças crônicas. O desfecho primário foi a incidência de doença coronariana [(DAC) definida como infarto do miocárdio (IM) não fatal, IM silencioso e morte por DAC], com câncer de mama invasivo como principal resultado adverso. Um “índice global” incluiu a ocorrência mais precoce de DAC, câncer de mama invasivo, acidente vascular cerebral, embolia pulmonar (EP), câncer de endométrio (somente no subestudo CE mais MPA), câncer colorretal, fratura de quadril ou morte por outra causa. Esses subestudos não avaliaram os efeitos da CE isoladamente ou da CE mais MPA nos sintomas da menopausa.
Subestudo WHI Estrogen Plus Progestin
subestudo WHI de estrogênio mais progestina foi interrompido precocemente. De acordo com a regra de interrupção predefinida, após um acompanhamento médio de 5,6 anos de tratamento, o aumento do risco de câncer de mama e eventos cardiovasculares excedeu os benefícios especificados incluídos no “índice global”. O excesso de risco absoluto de eventos no “índice global” foi de 19 por 10.000 mulheres-ano.
Para os desfechos incluídos no “índice global” do WHI que alcançaram significância estatística após 5,6 anos de acompanhamento, o excesso de risco absoluto por 10.000 mulheres-ano no grupo tratado com CE mais MPA foi de mais 7 eventos de DAC, mais 8 AVCs, 10 EPs a mais e 8 cânceres de mama mais invasivos, enquanto as reduções de risco absoluto por 10.000 mulheres-anos foram 6 menos cânceres colorretais e 5 menos fraturas de quadril.
Os resultados do subestudo de estrogênio mais progestina, que incluiu 16.608 mulheres (média de 63 anos de idade, faixa de 50 a 79; 83,9 por cento brancas, 6,8 por cento negras, 5,4 por cento hispânicas, 3,9 por cento Outros) são apresentados na Tabela 5. Esses resultados refletem centralmente dados adjudicados após um seguimento médio de 5,6 anos.
TABELA 5. Risco Relativo e Absoluto Observado no Subestudo de Estrogênio Mais Progestina do WHI em uma média de 5,6 anos a, b
O momento do início da terapia com estrogênio e progesterona em relação ao início da menopausa pode afetar o perfil geral de risco-benefício. O subestudo WHI de estrogênio mais progestina estratificado por idade mostrou em mulheres de 50 a 59 anos uma tendência não significativa para reduzir o risco de mortalidade geral [hazard ratio (HR) 0,69 (IC 95%, 0,44-1,07)].
Estudo de Memória da Iniciativa de Saúde da Mulher
estrogênio mais progestina Women's Health Initiative Memory Study (WHIMS), um estudo auxiliar do WHI, recrutou 4.532 mulheres na pós-menopausa predominantemente saudáveis com 65 anos de idade ou mais (47% tinham 65 a 69 anos de idade; 35% tinham 70 a 74 anos de idade). idade; e 18 por cento tinham 75 anos de idade ou mais) para avaliar os efeitos da CE diária (0,625 mg) mais MPA (2,5 mg) na incidência de demência provável (desfecho primário) em comparação com placebo.
Após um acompanhamento médio de 4 anos, o risco relativo de provável demência para EC mais MPA versus placebo foi de 2,05 (IC de 95%, 1,21 – 3,48). O risco absoluto de demência provável para EC mais MPA versus placebo foi de 45 versus 22 por 10.000 mulheres-ano. A demência provável, conforme definida neste estudo, incluiu a doença de Alzheimer (DA), demência vascular (DV) e tipo misto (com características de DA e DV). A classificação mais comum de provável demência no grupo de tratamento e no grupo placebo foi DA. Uma vez que o estudo auxiliar foi realizado em mulheres de 65 a 79 anos de idade, não se sabe se esses achados se aplicam a mulheres pós-menopáusicas mais jovens. (Ver AVISOS , Provável demência e PRECAUÇÕES , Uso Geriátrico .)
INFORMAÇÃO DO PACIENTE
PROMETRIUM® (progesterona, USP) Cápsulas 100 mg e 200 mg
Leia estas INFORMAÇÕES AO PACIENTE antes de começar a tomar PROMETRIUM 200mg cápsulas e leia o que você recebe cada vez que reabastecer sua prescrição de PROMETRIUM 100mg cápsulas. Pode haver novas informações. Esta informação não substitui a conversa com seu médico sobre sua condição médica ou seu tratamento.
QUAL A INFORMAÇÃO MAIS IMPORTANTE QUE DEVO SABER SOBRE PROMETRIUM 100mg CÁPSULAS (A Progesterona Hormônio)?
- As progestinas com estrogênios não devem ser usadas para prevenir doenças cardíacas, ataques cardíacos, derrames ou demência.
- O uso de progestágenos com estrogênios pode aumentar sua chance de ter ataques cardíacos, derrames, câncer de mama e coágulos sanguíneos.
- O uso de progestágenos com estrogênios pode aumentar sua chance de contrair demência, com base em um estudo com mulheres com 65 anos ou mais.
- Você e seu médico devem conversar regularmente sobre se ainda precisa de tratamento com PROMETRIUM 100mg Cápsulas.
ESTE PRODUTO CONTÉM ÓLEO DE AMENDOIM E NÃO DEVE SER USADO SE VOCÊ FOR ALÉRGICO A AMENDOIM.
O que é PROMETRIUM 200mg cápsulas?
As cápsulas de PROMETRIUM 100mg contêm o hormônio feminino chamado progesterona.
Para que serve PROMETRIUM 100mg cápsulas?
Tratamento de irregularidades menstruais
As cápsulas de PROMETRIUM 200mg são usadas para o tratamento da amenorreia secundária (ausência de períodos menstruais em mulheres que já tiveram um período menstrual) devido à diminuição da progesterona. Quando você não produz progesterona suficiente, podem ocorrer irregularidades menstruais. Se o seu médico determinou que seu corpo não produz progesterona suficiente por conta própria, PROMETRIUM 200mg cápsulas pode ser prescrito para fornecer a progesterona que você precisa.
Proteção do Endométrio (Revestimento do Útero)
As cápsulas de PROMETRIUM 200mg são usadas em combinação com medicamentos contendo estrogênio em uma mulher na pós-menopausa com útero (útero). Tomar estrogênio sozinho aumenta a chance de desenvolver uma condição chamada hiperplasia endometrial que pode levar ao câncer do revestimento do útero (útero). A adição de uma progestina é geralmente recomendada para uma mulher com útero para reduzir a chance de contrair câncer de útero (útero).
Quem não deve tomar as cápsulas de PROMETRIUM?
Não comece a tomar PROMETRIUM Capsules se você:
- São alérgicos a amendoim
- Tem sangramento vaginal incomum
- Atualmente tem ou teve certos tipos de câncer O tratamento com estrogênio e progesterona pode aumentar a chance de contrair certos tipos de câncer, incluindo câncer de mama ou útero. Se você tem ou teve câncer, converse com seu médico sobre se você deve tomar PROMETRIUM Capsules.
- Teve um derrame ou ataque cardíaco
- Atualmente tem ou teve coágulos sanguíneos
- Atualmente tem ou teve problemas de fígado
- É alérgico a PROMETRIUM Capsules ou a qualquer um de seus ingredientes Consulte a lista de ingredientes de PROMETRIUM 200mg cápsulas no final deste folheto.
- Acha que pode estar grávida
Informe o seu prestador de cuidados de saúde:
- Se você está amamentando. A hormona nas cápsulas PROMETRIUM 100mg pode passar para o leite materno.
- Sobre todos os seus problemas médicos. Seu médico pode precisar examiná-lo com mais cuidado se você tiver certas condições, como asma (pieira), epilepsia (convulsões), diabetes, enxaqueca, endometriose, lúpus, problemas no coração, fígado, tireoide ou rins, ou se tiver níveis elevados de cálcio no sangue.
- Sobre todos os medicamentos que você toma. Isso inclui medicamentos prescritos e não prescritos, vitaminas e suplementos de ervas. Alguns medicamentos podem afetar o funcionamento de PROMETRIUM 100mg cápsulas. PROMETRIUM Cápsulas também pode afetar o funcionamento de outros medicamentos.
Como devo tomar as cápsulas de PROMETRIUM 200mg?
Quais são os possíveis efeitos colaterais de PROMETRIUM Capsules?
Os efeitos colaterais são agrupados de acordo com a gravidade e a frequência com que ocorrem quando você é tratado:
Efeitos colaterais graves, mas menos comuns incluem:
- Risco para o feto: Casos de fenda palatina, lábio leporino, hipospádia, comunicação interventricular, persistência do canal arterial e outros defeitos cardíacos congênitos.
- Coagulação Sanguínea Anormal: AVC, ataque cardíaco, embolia pulmonar, perda visual ou cegueira.
Alguns dos sinais de alerta de efeitos colaterais graves incluem:
- Alterações na visão ou fala
- Novas dores de cabeça severas repentinas
- Dores graves no peito ou nas pernas com ou sem falta de ar, fraqueza e fadiga
- Tonturas e desmaios
- Vômito
Ligue para o seu médico imediatamente se tiver algum desses sinais de alerta ou quaisquer outros sintomas incomuns que o preocupem.
Efeitos colaterais menos graves, mas comuns incluem:
- Dores de cabeça
- Dor no peito
- Sangramento vaginal irregular ou spotting
- Cólicas estomacais ou abdominais, inchaço
- Nausea e vomito
- Perda de cabelo
- Retenção de fluidos
- Candidíase vaginal
Estes não são todos os possíveis efeitos colaterais das cápsulas de PROMETRIUM 200mg. Para obter mais informações, peça conselhos ao seu médico ou farmacêutico sobre os efeitos colaterais. Você pode relatar os efeitos colaterais à AbbVie Inc. pelo telefone 1-800-633-9110 ou ao FDA pelo telefone 1-800-FDA-1088.
O que posso fazer para diminuir minhas chances de ter um efeito colateral grave com PROMETRIUM 100mg Cápsulas?
- Converse com seu médico regularmente sobre se você deve continuar tomando PROMETRIUM 100mg cápsulas.
- Consulte o seu médico imediatamente se tiver sangramento vaginal incomum enquanto estiver tomando PROMETRIUM Capsules.
- Faça um exame pélvico, exame de mama e mamografia (raio-X da mama) todos os anos, a menos que seu médico lhe diga outra coisa. Se membros da sua família tiveram câncer de mama ou se você já teve nódulos mamários ou uma mamografia anormal, pode ser necessário fazer exames de mama com mais frequência.
- Se você tem pressão alta, colesterol alto (gordura no sangue), diabetes, excesso de peso ou se usa tabaco, pode ter maiores chances de contrair doenças cardíacas. Pergunte ao seu médico sobre maneiras de diminuir suas chances de contrair doenças cardíacas.
Informações gerais sobre o uso seguro e eficaz de PROMETRIUM Capsules
- Às vezes, medicamentos são prescritos para condições que não são mencionadas nos folhetos informativos do paciente. Não tome PROMETRIUM Capsules para condições para as quais não foi prescrito.
- Seu médico prescreveu este medicamento para você e somente para você. Não dê PROMETRIUM Capsules a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
- As cápsulas de PROMETRIUM 200mg devem ser tomadas em dose única diária ao deitar. Algumas mulheres podem sentir tonturas e/ou sonolência extremas durante a terapia inicial. Em alguns casos, os sintomas podem incluir visão turva, dificuldade para falar, dificuldade para caminhar e sensação anormal. Se você tiver esses sintomas, discuta-os imediatamente com seu médico.
- Tenha cuidado ao dirigir um veículo motorizado ou operar máquinas, pois podem ocorrer tonturas ou sonolência.
Mantenha as cápsulas de PROMETRIUM fora do alcance das crianças.
Este folheto fornece um resumo das informações mais importantes sobre PROMETRIUM 100mg Cápsulas. Se você quiser mais informações, fale com seu médico ou farmacêutico. Você pode pedir informações sobre PROMETRIUM 100mg Cápsulas escritas para profissionais de saúde. Você pode obter mais informações ligando para o número gratuito 1-800-633-9110.
Quais são os ingredientes das cápsulas PROMETRIUM?
Princípio ativo: 100 mg ou 200 mg de progesterona micronizada
Os ingredientes inativos para PROMETRIUM Capsules 100 mg incluem: óleo de amendoim NF, gelatina NF, glicerina USP, lecitina NF, dióxido de titânio USP, FD&C Red No. 40 e D&C Yellow No. 10.
Os ingredientes inativos para PROMETRIUM Capsules 200 mg incluem: óleo de amendoim NF, gelatina NF, glicerina USP, lecitina NF, dióxido de titânio USP, D&C Yellow No. 10 e FD&C Yellow No. 6.
COMO FORNECIDO
PROMETRIUM 200mg Cápsulas 100 mg são cápsulas redondas, cor de pêssego, marcadas com a impressão preta “SV”.
PROMETRIUM 100mg Cápsulas 200 mg são cápsulas ovais, de cor amarelo pálido, marcadas com a impressão preta “SV2”.
Armazenar a 25°C (77°F); excursões permitidas de 15° a 30°C (59° a 86°F) [Consulte Temperatura ambiente controlada pela USP].
