Buspar 5mg, 10mg Buspirone Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Buspar e como é usado?
Buspar 5mg é um medicamento de prescrição usado para tratar os sintomas de transtornos de ansiedade. Buspar 5mg pode ser usado sozinho ou com outros medicamentos.
Buspar pertence a uma classe de medicamentos chamados Agentes Ansiolíticos, Ansiolíticos, Não-benzodiazepínicos.
Quais são os possíveis efeitos colaterais do Buspar?
Quais são os possíveis efeitos colaterais do Buspar 5mg?
Buspar pode causar efeitos colaterais graves, incluindo:
- dor no peito,
- falta de ar e
- tontura
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Buspar incluem:
- dor de cabeça,
- tontura,
- sonolência,
- problema do sono (insônia),
- náusea,
- dor de estômago, e
- sentindo-se nervoso ou animado
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Buspar. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
Os comprimidos de cloridrato de buspirona, USP são um agente ansiolítico que não está quimicamente ou farmacologicamente relacionado aos benzodiazepínicos, barbitúricos ou outros medicamentos sedativos/ansiolíticos.
O cloridrato de buspirona, USP é um pó cristalino branco. É muito solúvel em água; livremente solúvel em metanol e em cloreto de metileno; pouco solúvel em etanol e em acetonitrilo; muito pouco solúvel em acetato de etilo e praticamente insolúvel em hexanos. Seu peso molecular é 422. Quimicamente, o cloridrato de buspirona é monocloridrato de 8-[4-[4-(2-pirimidinil)-1-piperazinil]butil]-8-azaspiro[4.5]decano-7,9-diona. A fórmula molecular C21H31N5O2•HCl é representada pela seguinte fórmula estrutural:
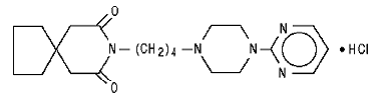
Cada comprimido de cloridrato de buspirona destinado à administração oral contém 5 mg ou 10 mg ou 15 mg ou 30 mg de cloridrato de buspirona (equivalente a 4,6 mg, 9,1 mg, 13,7 mg e 27,4 mg de base livre de buspirona, respectivamente). Além disso, cada comprimido contém os seguintes ingredientes inativos: dióxido de silício coloidal, lactose mono-hidratada, estearato de magnésio, celulose microcristalina e amidoglicolato de sódio. Os comprimidos de 5 mg e 10 mg são marcados para que possam ser divididos ao meio. Assim, o comprimido de 5 mg também pode fornecer uma dose de 2,5 mg e o comprimido de 10 mg pode fornecer uma dose de 5 mg. Os comprimidos de 15 mg e 30 mg são marcados para que possam ser divididos ao meio ou ao meio. Assim, um único comprimido de 15 mg pode fornecer as seguintes doses: 15 mg (comprimido inteiro), 10 mg (dois terços de um comprimido), 7,5 mg (metade de um comprimido) ou 5 mg (um terço de um comprimido) . Um único comprimido de 30 mg pode fornecer as seguintes doses: 30 mg (comprimido inteiro), 20 mg (dois terços de um comprimido), 15 mg (metade de um comprimido) ou 10 mg (um terço de um comprimido).
INDICAÇÕES
Os comprimidos de cloridrato de buspirona são indicados para o tratamento de transtornos de ansiedade ou alívio a curto prazo dos sintomas de ansiedade. A ansiedade ou tensão associada ao estresse da vida cotidiana geralmente não requer tratamento com um ansiolítico.
A eficácia dos comprimidos de cloridrato de buspirona foi demonstrada em ensaios clínicos controlados de pacientes ambulatoriais cujo diagnóstico corresponde aproximadamente ao Transtorno de Ansiedade Generalizada (TAG). Muitos dos pacientes incluídos nesses estudos também apresentavam sintomas depressivos coexistentes e os comprimidos de cloridrato de buspirona aliviavam a ansiedade na presença desses sintomas depressivos coexistentes. Os pacientes avaliados nesses estudos apresentaram sintomas por períodos de 1 mês a mais de 1 ano antes do estudo, com duração média dos sintomas de 6 meses. O Transtorno de Ansiedade Generalizada (300.02) é descrito no Manual Diagnóstico e Estatístico da Associação Americana de Psiquiatria, III1 da seguinte forma:
Ansiedade generalizada e persistente (de pelo menos 1 mês de duração contínua), manifestada por sintomas de três das quatro categorias a seguir:
Tensão do Motor
Tremores, nervosismo, nervosismo, tremores, tensão, dores musculares, fadiga, incapacidade de relaxar, contração das pálpebras, sobrancelhas franzidas, rosto tenso, inquietação, inquietação, sobressalto fácil.
Hiperatividade Autonômica
Sudorese, coração acelerado ou acelerado, mãos frias e úmidas, boca seca, tontura, tontura, parestesias (formigamento nas mãos ou pés), dor de estômago, crises de calor ou frio, micção frequente, diarreia, desconforto na boca do estômago, caroço na garganta, rubor, palidez, pulso alto em repouso e frequência respiratória.
Expectativa Apreensiva
Ansiedade, preocupação, medo, ruminação e antecipação de infortúnio para si ou para os outros.
Vigilância e Escaneamento
Hiperatenção resultando em distração, dificuldade de concentração, insônia, sensação de "no limite", irritabilidade, impaciência.
Os sintomas acima não seriam devidos a outro transtorno mental, como transtorno depressivo ou esquizofrenia. No entanto, sintomas depressivos leves são comuns no TAG.
A eficácia dos comprimidos de cloridrato de buspirona em uso prolongado, ou seja, por mais de 3 a 4 semanas, não foi demonstrada em estudos controlados. Não existe um corpo de evidência disponível que aborde sistematicamente a duração apropriada do tratamento para TAG. No entanto, em um estudo de uso prolongado, 264 pacientes foram tratados com comprimidos de cloridrato de buspirona por 1 ano sem efeito nocivo. Portanto, o médico que optar por usar comprimidos de cloridrato de buspirona por períodos prolongados deve reavaliar periodicamente a utilidade do medicamento para o paciente individual.
DOSAGEM E ADMINISTRAÇÃO
dose inicial recomendada é de 15 mg por dia (7,5 mg bid). Para obter uma resposta terapêutica ideal, em intervalos de 2 a 3 dias, a dosagem pode ser aumentada em 5 mg por dia, conforme necessário. A dose diária máxima não deve exceder 60 mg por dia. Em ensaios clínicos que permitem a titulação da dose, doses divididas de 20 mg a 30 mg por dia foram comumente empregadas.
A biodisponibilidade da buspirona é aumentada quando administrada com alimentos em comparação com o estado de jejum (ver FARMACOLOGIA CLÍNICA ). Conseqüentemente, os pacientes devem tomar buspirona de maneira consistente em relação ao momento da dosagem; sempre com ou sempre sem comida.
Quando a buspirona deve ser administrada com um inibidor potente do CYP3A4, as recomendações de dosagem descritas na INTERAÇÕES MEDICAMENTOSAS seção deve ser seguida.
COMO FORNECIDO
Os comprimidos de cloridrato de buspirona USP, 5 mg, são comprimidos brancos a esbranquiçados, em forma de cápsula, de face plana, com bordas biseladas gravadas com bissecção em um dos lados; um lado do bisect é gravado com 'ZE' e outro é gravado com '36' e o outro lado é liso
Dados do fabricante: N/A. Revisado: maio de 2016
EFEITOS COLATERAIS
Nenhuma informação fornecida.
INTERAÇÕES MEDICAMENTOSAS
Agentes psicotrópicos
Inibidores da MAO
Recomenda-se que os comprimidos de cloridrato de buspirona não sejam usados concomitantemente com inibidores da MAO (ver AVISOS ).
Amitriptilina
Após a adição de buspirona ao regime posológico de amitriptilina, não foram observadas diferenças estatisticamente significativas nos parâmetros farmacocinéticos no estado de equilíbrio (Cmax, AUC e Cmin) da amitriptilina ou de seu metabólito nortriptilina.
Diazepam
Após a adição de buspirona ao regime de dose de diazepam, não foram observadas diferenças estatisticamente significativas nos parâmetros farmacocinéticos no estado de equilíbrio (Cmax, AUC e Cmin) para o diazepam, mas foram observados aumentos de cerca de 15% para o nordiazepam e efeitos clínicos adversos menores (tontura, dor de cabeça e náusea).
Haloperidol
Em um estudo em voluntários normais, a administração concomitante de buspirona e haloperidol resultou em aumento das concentrações séricas de haloperidol. O significado clínico deste achado não é claro.
Nefazodona
[Vejo Inibidores e Indutores do Citocromo P450 3A4 (CYP3A4) ].
Trazodona
Há um relato sugerindo que o uso concomitante de Desyrel®# (cloridrato de trazodona) e buspirona pode ter causado elevações de 3 a 6 vezes na SGPT (ALT) em alguns pacientes. Em um estudo semelhante tentando replicar esse achado, nenhum efeito interativo nas transaminases hepáticas foi identificado.
Triazolam/Flurazepam
coadministração de buspirona com triazolam ou flurazepam não pareceu prolongar ou intensificar os efeitos sedativos de nenhum dos benzodiazepínicos.
Outros psicotrópicos
Como os efeitos da administração concomitante de buspirona com a maioria das outras drogas psicotrópicas não foram estudados, o uso concomitante de buspirona com outras drogas ativas no SNC deve ser abordado com cautela.
Inibidores e indutores do citocromo P450 3A4 (CYP3A4)
A buspirona demonstrou ser metabolizada in vitro pelo CYP3A4. Esta descoberta é consistente com as interações in vivo observadas entre buspirona e o seguinte:
Diltiazem e Verapamil
Em um estudo com nove voluntários saudáveis, a coadministração de buspirona (10 mg em dose única) com verapamil (80 mg três vezes ao dia) ou diltiazem (60 mg três vezes ao dia) aumentou as concentrações plasmáticas de buspirona (verapamil aumentou a AUC e a Cmax da buspirona 3,4 vezes enquanto o diltiazem aumento da AUC e Cmax 5,5 vezes e 4 vezes, respectivamente.) Os eventos adversos atribuíveis à buspirona podem ser mais prováveis durante a administração concomitante com diltiazem ou verapamil. O ajuste subsequente da dose pode ser necessário e deve ser baseado na avaliação clínica.
Eritromicina
Em um estudo em voluntários saudáveis, a coadministração de buspirona (10 mg em dose única) com eritromicina (1,5 g/dia por 4 dias) aumentou as concentrações plasmáticas de buspirona (aumento de 5 vezes na Cmax e aumento de 6 vezes na AUC). Essas interações farmacocinéticas foram acompanhadas por um aumento da incidência de efeitos colaterais atribuíveis à buspirona. Se os dois medicamentos forem usados em combinação, recomenda-se uma dose baixa de buspirona (por exemplo, 2,5 mg duas vezes ao dia). O ajuste subsequente da dose de qualquer um dos medicamentos deve ser baseado na avaliação clínica.
Suco de toranja
Em um estudo em voluntários saudáveis, a coadministração de buspirona (10 mg em dose única) com suco de toranja (200 mL de dose dupla três vezes por 2 dias) aumentou as concentrações plasmáticas de buspirona (aumento de 4,3 vezes na Cmax; aumento de 9,2 vezes na AUC ). Pacientes recebendo buspirona devem ser aconselhados a evitar beber grandes quantidades de suco de toranja.
Itraconazol
Em um estudo em voluntários saudáveis, a coadministração de buspirona (10 mg em dose única) com itraconazol (200 mg/dia por 4 dias) aumentou as concentrações plasmáticas de buspirona (aumento de 13 vezes na Cmax e aumento de 19 vezes na AUC). Essas interações farmacocinéticas foram acompanhadas por um aumento da incidência de efeitos colaterais atribuíveis à buspirona. Se os dois medicamentos forem usados em combinação, recomenda-se uma dose baixa de buspirona (por exemplo, 2,5 mg qd). O ajuste subsequente da dose de qualquer um dos medicamentos deve ser baseado na avaliação clínica.
Nefazodona
Em um estudo de farmacocinética no estado de equilíbrio em voluntários saudáveis, a coadministração de buspirona (2,5 ou 5 mg bid) com nefazodona (250 mg bid) resultou em aumentos acentuados nas concentrações plasmáticas de buspirona (aumento de até 20 vezes na Cmax e até 50 - vezes na AUC) e diminuições estatisticamente significativas (cerca de 50%) nas concentrações plasmáticas do metabólito 1-PP da buspirona. Com doses bid de 5 mg de buspirona, foram observados ligeiros aumentos na AUC para nefazodona (23%) e seus metabólitos hidroxinefazodona (HO-NEF) (17%) e meta-clorofenilpiperazina (9%). Ligeiros aumentos na Cmax foram observados para nefazodona (8%) e seu metabólito HO-NEF (11%).
Indivíduos que receberam buspirona 5 mg bid e nefazodona 250 mg bid experimentaram tontura, astenia, tontura e sonolência, eventos adversos também observados com qualquer uma das drogas isoladamente. Se os dois medicamentos forem usados em combinação, recomenda-se uma dose baixa de buspirona (por exemplo, 2,5 mg qd). O ajuste subsequente da dose de qualquer um dos medicamentos deve ser baseado na avaliação clínica.
Rifampina
Em um estudo em voluntários saudáveis, a coadministração de buspirona (30 mg em dose única) com rifampicina (600 mg/dia por 5 dias) diminuiu as concentrações plasmáticas (redução de 83,7% na Cmax; diminuição de 89,6% na AUC) e os efeitos farmacodinâmicos de buspirona. Se os dois medicamentos forem usados em combinação, a dosagem de buspirona pode precisar ser ajustada para manter o efeito ansiolítico.
Outros inibidores e indutores de CYP3A4
As substâncias que inibem o CYP3A4, como o cetoconazol ou o ritonavir, podem inibir o metabolismo da buspirona e aumentar as concentrações plasmáticas de buspirona, enquanto as substâncias que induzem o CYP3A4, como a dexametasona ou certos anticonvulsivantes (fenitoína, fenobarbital, carbamazepina), podem aumentar a taxa de metabolismo da buspirona. Se um paciente foi titulado para uma dosagem estável de buspirona, um ajuste de dose de buspirona pode ser necessário para evitar eventos adversos atribuíveis à buspirona ou atividade ansiolítica diminuída. Consequentemente, quando administrado com um inibidor potente do CYP3A4, recomenda-se uma dose baixa de buspirona usada com cautela. Quando usado em combinação com um indutor potente do CYP3A4, a dosagem de buspirona pode precisar de ajuste para manter o efeito ansiolítico.
Outras drogas
Cimetidina
A coadministração de buspirona com cimetidina aumentou a Cmax (40%) e a Tmax (2 vezes), mas teve efeitos mínimos na AUC da buspirona.
Ligação proteica
In vitro, a buspirona não desloca drogas fortemente ligadas como fenitoína, propranolol e varfarina das proteínas séricas. No entanto, houve um relato de tempo de protrombina prolongado quando a buspirona foi adicionada ao regime de um paciente tratado com varfarina. O paciente também estava recebendo cronicamente fenitoína, fenobarbital, digoxina e Synthroid®*. In vitro, a buspirona pode deslocar drogas menos firmemente ligadas, como a digoxina. O significado clínico desta propriedade é desconhecido.
Os níveis terapêuticos de aspirina, desipramina, diazepam, flurazepam, ibuprofeno, propranolol, tioridazina e tolbutamida tiveram apenas um efeito limitado na extensão da ligação da buspirona às proteínas plasmáticas (ver FARMACOLOGIA CLÍNICA ).
Interações Medicamentos/Testes Laboratoriais
cloridrato de buspirona pode interferir com o ensaio urinário de metanefrina/catecolamina. Foi erroneamente lido como metanefrina durante o teste de rotina para feocromocitoma, resultando em um resultado laboratorial falso positivo. O cloridrato de buspirona deve, portanto, ser descontinuado por pelo menos 48 horas antes da coleta de urina para catecolaminas.
Abuso e Dependência de Drogas
Classe de substância controlada
O cloridrato de buspirona não é uma substância controlada.
Dependência física e psicológica
Em estudos em humanos e animais, a buspirona não mostrou potencial para abuso ou desvio e não há evidências de que cause tolerância ou dependência física ou psicológica. Voluntários humanos com histórico de uso recreativo de drogas ou álcool foram estudados em duas investigações clínicas duplo-cegas. Nenhum dos indivíduos foi capaz de distinguir entre comprimidos de cloridrato de buspirona e placebo. Por outro lado, os indivíduos mostraram uma preferência estatisticamente significativa por metaqualona e diazepam. Estudos em macacos, camundongos e ratos indicaram que a buspirona não tem potencial para abuso. Após administração crônica no rato, a retirada abrupta da buspirona não resultou na perda de peso corporal comumente observada com substâncias que causam dependência física.
Embora não haja evidência direta de que os comprimidos de cloridrato de buspirona causem dependência física ou comportamento de busca de drogas, é difícil prever a partir de experimentos até que ponto uma droga ativa no SNC será mal utilizada, desviada e/ou abusada uma vez comercializada. Consequentemente, os médicos devem avaliar cuidadosamente os pacientes quanto a um histórico de abuso de drogas e acompanhá-los de perto, observando-os quanto a sinais de uso indevido ou abuso de comprimidos de cloridrato de buspirona (por exemplo, desenvolvimento de tolerância, aumento da dose, comportamento de busca de drogas).
Classe de substância controlada
O cloridrato de buspirona não é uma substância controlada.
Dependência física e psicológica
Em estudos em humanos e animais, a buspirona não mostrou potencial para abuso ou desvio e não há evidências de que cause tolerância ou dependência física ou psicológica. Voluntários humanos com histórico de uso recreativo de drogas ou álcool foram estudados em duas investigações clínicas duplo-cegas. Nenhum dos indivíduos foi capaz de distinguir entre comprimidos de cloridrato de buspirona e placebo. Por outro lado, os indivíduos mostraram uma preferência estatisticamente significativa por metaqualona e diazepam. Estudos em macacos, camundongos e ratos indicaram que a buspirona não tem potencial para abuso. Após administração crônica no rato, a retirada abrupta da buspirona não resultou na perda de peso corporal comumente observada com substâncias que causam dependência física.
Embora não haja evidência direta de que os comprimidos de cloridrato de buspirona causem dependência física ou comportamento de busca de drogas, é difícil prever a partir de experimentos até que ponto uma droga ativa no SNC será mal utilizada, desviada e/ou abusada uma vez comercializada. Consequentemente, os médicos devem avaliar cuidadosamente os pacientes quanto a um histórico de abuso de drogas e acompanhá-los de perto, observando-os quanto a sinais de uso indevido ou abuso de comprimidos de cloridrato de buspirona (por exemplo, desenvolvimento de tolerância, aumento da dose, comportamento de busca de drogas).
AVISOS
A administração de comprimidos de cloridrato de buspirona a um paciente tomando um inibidor da monoaminoxidase (IMAO) pode representar um risco. Houve relatos da ocorrência de pressão arterial elevada quando comprimidos de cloridrato de buspirona foram adicionados a um regime que inclui um IMAO. Portanto, recomenda-se que os comprimidos de cloridrato de buspirona não sejam usados concomitantemente com um IMAO.
Como os comprimidos de cloridrato de buspirona não possuem atividade antipsicótica estabelecida, ele não deve ser utilizado em substituição ao tratamento antipsicótico apropriado.
PRECAUÇÕES
Em geral
Interferência com o desempenho cognitivo e motor
Estudos indicam que os comprimidos de cloridrato de buspirona são menos sedativos do que outros ansiolíticos e que não produz prejuízo funcional significativo. No entanto, seus efeitos no SNC em qualquer paciente individual podem não ser previsíveis. Portanto, os pacientes devem ser advertidos sobre a operação de automóveis ou máquinas complexas até que tenham certeza razoável de que o tratamento com buspirona não os afeta adversamente.
Embora estudos formais da interação do cloridrato de buspirona com álcool indiquem que a buspirona não aumenta o comprometimento do desempenho motor e mental induzido pelo álcool, é prudente evitar o uso concomitante de álcool e buspirona.
Potencial para reações de abstinência em pacientes dependentes de drogas sedativas/hipnóticas/ansiolíticas
Como os comprimidos de cloridrato de buspirona não apresentam tolerância cruzada com benzodiazepínicos e outros medicamentos sedativos/hipnóticos comuns, ele não bloqueará a síndrome de abstinência frequentemente observada com a interrupção da terapia com esses medicamentos. Portanto, antes de iniciar a terapia com comprimidos de cloridrato de buspirona, é aconselhável retirar os pacientes gradualmente, especialmente aqueles que fazem uso crônico de um medicamento depressor do SNC, de seu tratamento anterior. Os sintomas de rebote ou abstinência podem ocorrer em períodos de tempo variados, dependendo em parte do tipo de droga e de sua meia-vida efetiva de eliminação.
A síndrome de abstinência de drogas sedativas/hipnóticas/ansiolíticas pode aparecer como qualquer combinação de irritabilidade, ansiedade, agitação, insônia, tremor, cãibras abdominais, cãibras musculares, vômitos, sudorese, sintomas semelhantes aos da gripe sem febre e, ocasionalmente, até mesmo como convulsões .
Possíveis preocupações relacionadas à ligação da buspirona aos receptores de dopamina
Como a buspirona pode se ligar aos receptores centrais de dopamina, foi levantada uma questão sobre seu potencial de causar alterações agudas e crônicas na função neurológica mediada pela dopamina (por exemplo, distonia, pseudoparkinsonismo, acatisia e discinesia tardia). A experiência clínica em ensaios controlados não conseguiu identificar qualquer atividade neuroléptica significativa; entretanto, uma síndrome de inquietação, aparecendo logo após o início do tratamento, foi relatada em uma pequena fração de pacientes tratados com buspirona. A síndrome pode ser explicada de várias maneiras. Por exemplo, a buspirona pode aumentar a atividade noradrenérgica central; alternativamente, o efeito pode ser atribuído a efeitos dopaminérgicos (ou seja, representam acatisia). Ver REAÇÕES ADVERSAS : Experiência pós-marketing .
Informações para pacientes
Para garantir o uso seguro e eficaz dos comprimidos de cloridrato de buspirona, as seguintes informações e instruções devem ser fornecidas aos pacientes:
Informe o seu médico sobre quaisquer medicamentos, prescrição ou não, álcool ou drogas que você está tomando ou planeja tomar durante o tratamento com comprimidos de cloridrato de buspirona.
Informe o seu médico se estiver grávida, se planeia engravidar ou se engravidar enquanto estiver a tomar comprimidos de cloridrato de buspirona.
Informe o seu médico se estiver amamentando um bebê.
Até sentir como este medicamento o afeta, não dirija um carro ou opere máquinas potencialmente perigosas.
Você deve tomar cloridrato de buspirona de forma consistente, sempre com ou sempre sem alimentos.
Durante o tratamento com comprimidos de cloridrato de buspirona, evite beber grandes quantidades de sumo de toranja.
Testes laboratoriais
Não há testes laboratoriais específicos recomendados.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Nenhuma evidência de potencial carcinogênico foi observada em ratos durante um estudo de 24 meses com aproximadamente 133 vezes a dose oral humana máxima recomendada; ou em camundongos, durante um estudo de 18 meses com aproximadamente 167 vezes a dose oral humana máxima recomendada.
Com ou sem ativação metabólica, a buspirona não induziu mutações pontuais em cinco cepas de Salmonella typhimurium (teste de Ames) ou culturas de células de linfoma de camundongo L5178YTK+, nem foi observado dano ao DNA com buspirona em células humanas Wi-38. Aberrações cromossômicas ou anormalidades não ocorreram nas células da medula óssea de camundongos que receberam uma ou cinco doses diárias de buspirona.
Gravidez
Efeitos teratogênicos
Gravidez Categoria B
Não foram observados problemas de fertilidade ou danos fetais em estudos de reprodução realizados em ratos e coelhos com doses de buspirona de aproximadamente 30 vezes a dose humana máxima recomendada. Em humanos, no entanto, não foram realizados estudos adequados e bem controlados durante a gravidez. Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, este medicamento deve ser usado durante a gravidez somente se for claramente necessário.
Trabalho e entrega
O efeito do cloridrato de buspirona no trabalho de parto e parto em mulheres é desconhecido. Não foram observados efeitos adversos em estudos de reprodução em ratos.
Mães que amamentam
A extensão da excreção no leite humano da buspirona ou de seus metabólitos não é conhecida. Em ratos, no entanto, a buspirona e seus metabólitos são excretados no leite. A administração de comprimidos de cloridrato de buspirona a lactantes deve ser evitada se clinicamente possível.
Uso Pediátrico
segurança e eficácia da buspirona foram avaliadas em dois ensaios de 6 semanas controlados por placebo, envolvendo um total de 559 pacientes pediátricos (variando de 6 a 17 anos de idade) com TAG. As doses estudadas foram de 7,5 mg a 30 mg bid (15 a 60 mg/dia). Não houve diferenças significativas entre buspirona e placebo em relação aos sintomas de TAG após as doses recomendadas para o tratamento de TAG em adultos. Estudos farmacocinéticos mostraram que, para doses idênticas, a exposição plasmática à buspirona e seu metabólito ativo, 1-PP, é igual ou maior em pacientes pediátricos do que em adultos. Nenhum achado de segurança inesperado foi associado à buspirona nesses estudos. Não existem dados de segurança ou eficácia a longo prazo nesta população.
Uso Geriátrico
Em um estudo de 6.632 pacientes que receberam buspirona para o tratamento da ansiedade, 605 pacientes tinham ≥ 65 anos e 41 tinham ≥ 75 anos; os perfis de segurança e eficácia para estes 605 doentes idosos (idade média = 70,8 anos) foram semelhantes aos da população mais jovem (idade média = 43,3 anos). A revisão de eventos clínicos adversos relatados espontaneamente não identificou diferenças entre pacientes idosos e mais jovens, mas a maior sensibilidade de alguns pacientes mais velhos não pode ser descartada.
Não houve efeitos da idade na farmacocinética da buspirona (ver FARMACOLOGIA CLÍNICA , Populações Especiais ).
Uso em pacientes com função hepática ou renal prejudicada
A buspirona é metabolizada pelo fígado e excretada pelos rins. Um estudo farmacocinético em pacientes com insuficiência hepática ou renal demonstrou níveis plasmáticos aumentados e meia-vida prolongada da buspirona. Portanto, a administração de comprimidos de cloridrato de buspirona a pacientes com insuficiência hepática ou renal grave não pode ser recomendada (ver FARMACOLOGIA CLÍNICA ).
SOBREDOSAGEM
Nenhuma informação fornecida.
CONTRA-INDICAÇÕES
Os comprimidos de cloridrato de buspirona são contraindicados em pacientes hipersensíveis ao cloridrato de buspirona.
FARMACOLOGIA CLÍNICA
O mecanismo de ação da buspirona é desconhecido. A buspirona difere dos ansiolíticos benzodiazepínicos típicos, pois não exerce efeitos anticonvulsivantes ou relaxantes musculares. Também não possui o efeito sedativo proeminente associado aos ansiolíticos mais típicos. Estudos pré-clínicos in vitro mostraram que a buspirona tem alta afinidade pelos receptores da serotonina (5-HT1A). A buspirona não tem afinidade significativa pelos receptores de benzodiazepínicos e não afeta a ligação do GABA in vitro ou in vivo quando testada em modelos pré-clínicos.
A buspirona tem afinidade moderada pelos receptores de dopamina D2 do cérebro. Alguns estudos sugerem que a buspirona pode ter efeitos indiretos em outros sistemas de neurotransmissores.
cloridrato de buspirona é rapidamente absorvido no homem e sofre extenso metabolismo de primeira passagem. Em um estudo radiomarcado, a buspirona inalterada no plasma representou apenas cerca de 1% da radioatividade no plasma. Após a administração oral, as concentrações plasmáticas de buspirona inalterada são muito baixas e variáveis entre os indivíduos. Níveis plasmáticos máximos de 1 ng/mL a 6 ng/mL foram observados 40 a 90 minutos após doses orais únicas de 20 mg. A biodisponibilidade de dose única da buspirona inalterada quando tomada na forma de comprimido é, em média, cerca de 90% de uma dose equivalente de solução, mas há grande variabilidade.
Os efeitos dos alimentos sobre a biodisponibilidade dos comprimidos de cloridrato de buspirona foram estudados em oito indivíduos. Eles receberam uma dose de 20 mg com e sem alimentos; a área sob a curva de concentração plasmática-tempo (AUC) e a concentração plasmática máxima (Cmax) de buspirona inalterada aumentaram 84% e 116%, respectivamente, mas a quantidade total de material imunorreativo de buspirona não se alterou. Isso sugere que os alimentos podem diminuir a extensão da depuração pré-sistêmica da buspirona (ver DOSAGEM E ADMINISTRAÇÃO ).
Um estudo de dose múltipla realizado em 15 indivíduos sugere que a buspirona tem farmacocinética não linear. Assim, aumentos de dose e doses repetidas podem levar a níveis sanguíneos de buspirona inalterados um pouco mais altos do que seria previsto pelos resultados de estudos de dose única.
Um estudo de ligação proteica in vitro indicou que aproximadamente 86% da buspirona está ligada às proteínas plasmáticas. Também foi observado que a aspirina aumentou os níveis plasmáticos de buspirona livre em 23%, enquanto o flurazepam diminuiu os níveis plasmáticos de buspirona livre em 20%. No entanto, não se sabe se essas drogas causam efeitos semelhantes nos níveis plasmáticos de buspirona livre in vivo, ou se tais alterações, se ocorrerem, causam diferenças clinicamente significativas no resultado do tratamento. Um estudo in vitro indicou que a buspirona não substituiu drogas altamente ligadas a proteínas, como fenitoína, varfarina e propranolol da proteína plasmática, e que a buspirona pode substituir a digoxina.
A buspirona é metabolizada principalmente por oxidação, que in vitro demonstrou ser mediada pelo citocromo P450 3A4 (CYP3A4) (ver INTERAÇÕES MEDICAMENTOSAS ). Vários derivados hidroxilados e um metabólito farmacologicamente ativo, 1-pirimidinilpiperazina (1-PP), são produzidos. Em modelos animais preditivos de potencial ansiolítico, o 1-PP tem cerca de um quarto da atividade da buspirona, mas está presente em quantidades até 20 vezes maiores. No entanto, isso provavelmente não é importante em humanos: amostras de sangue de humanos expostos cronicamente ao cloridrato de buspirona não apresentam níveis elevados de 1-PP; os valores médios são de aproximadamente 3 ng/mL e o nível sanguíneo humano mais alto registrado entre 108 pacientes cronicamente administrados foi de 17 ng/mL, menos de 1/200 dos níveis de 1-PP encontrados em animais que receberam grandes doses de buspirona sem sinais de toxicidade.
Em um estudo de dose única usando buspirona marcada com 14C, 29% a 63% da dose foi excretada na urina em 24 horas, principalmente como metabólitos; a excreção fecal foi responsável por 18% a 38% da dose. A meia-vida média de eliminação da buspirona inalterada após doses únicas de 10 mg a 40 mg é de cerca de 2 a 3 horas.
Populações Especiais
Efeitos de idade e gênero
Após doses únicas ou múltiplas em adultos, não foram observadas diferenças significativas na farmacocinética da buspirona (AUC e Cmax) entre indivíduos idosos e jovens ou entre homens e mulheres.
Insuficiência hepática
Após a administração de doses múltiplas de buspirona a pacientes com insuficiência hepática, a AUC de buspirona no estado de equilíbrio aumentou 13 vezes em comparação com indivíduos saudáveis (ver PRECAUÇÕES ).
Insuficiência renal
Após a administração de doses múltiplas de buspirona a pacientes com insuficiência renal (Clcr = 10 a 70 mL/min/1,73 m2), a AUC de buspirona no estado de equilíbrio aumentou 4 vezes em comparação com indivíduos saudáveis (Clcr ≥ 80 mL/min/1,73 m2) (Vejo PRECAUÇÕES ).
Efeitos de corrida
Os efeitos da raça na farmacocinética da buspirona não foram estudados.
INFORMAÇÃO DO PACIENTE
Cloridrato de Buspirona Comprimidos, USP Para comprimidos de 15 mg e 30 mg
COMO USAR
A resposta à buspirona varia entre os indivíduos. Seu médico pode achar necessário ajustar sua dosagem para obter a resposta adequada.
Cada comprimido é marcado e pode ser quebrado com precisão.
Para quebrar um comprimido com precisão e facilidade, segure o comprimido entre os polegares e os dedos indicadores perto da ranhura apropriada do comprimido (ranhura). Em seguida, com a ranhura do tablet voltada para você, aplique pressão e separe os segmentos do tablet (segmentos quebrados incorretamente não devem ser usados).
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA pelo telefone 1-800-FDA-1088.
