Glucovance 400/2.50mg, 500/5mg Metformin Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Glucovance 2,50mg e como é usado?
Glucovance 400mg é um medicamento de prescrição usado para tratar os sintomas do Diabetes Mellitus tipo 2. Glucovance pode ser usado sozinho ou com outros medicamentos.
Glucovance pertence a uma classe de medicamentos chamados antidiabéticos, sulfoniluréias/biguanidas.
Não se sabe se Glucovance 2,50mg é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Glucovance 400mg?
Glucovance pode causar efeitos colaterais graves, incluindo:
- urticária,
- dificuldade para respirar,
- inchaço do rosto, lábios, língua ou garganta,
- inchaço,
- ganho de peso rápido,
- falta de ar,
- extrema fraqueza,
- visão embaçada,
- sudorese,
- dificuldade para falar,
- tremores,
- dor de estômago,
- confusão,
- convulsões,
- dores musculares incomuns,
- Problemas respiratórios,
- dor de estômago,
- vômito,
- frequência cardíaca irregular,
- tontura,
- sentindo frio,
- fraqueza, e
- cansaço
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Glucovance incluem:
- Baixo teor de açúcar no sangue,
- náusea,
- diarréia,
- dor de estômago, e
- dor de cabeça
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Glucovance. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
GLUCOVANCE® (Glyburide and Metformin HCl) Comprimidos contém 2 medicamentos anti-hiperglicêmicos orais usados no controle do diabetes tipo 2, gliburida e cloridrato de metformina.
gliburida é um medicamento anti-hiperglicêmico oral da classe das sulfonilureias. O nome químico da gliburida é 1-[[p-[2-(5-cloro-o-anisamido)etil]fenil]sulfonil]-3-ciclo-hexilureia. A gliburida é um composto cristalino branco a esbranquiçado com uma fórmula molecular de C23H28ClN3O5S e um peso molecular de 494,01. A gliburida usada em GLUCOVANCE 5mg tem uma distribuição de tamanho de partícula de 25% de valor de tamanho inferior não superior a 6 μm, 50% de valor de tamanho inferior não superior a 7 a 10 μm e 75% de valor de tamanho inferior não superior a 21 μm. A fórmula estrutural está representada abaixo.
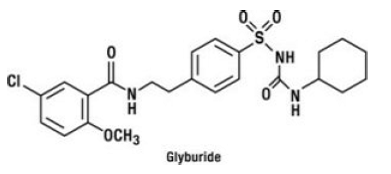
cloridrato de metformina é um medicamento anti-hiperglicêmico oral usado no tratamento do diabetes tipo 2. O cloridrato de metformina (monocloridrato de diamida N,N-dimetilimidodicarbonimida) não está quimicamente ou farmacologicamente relacionado a sulfonilureias, tiazolidinedionas ou inibidores de α-glicosidase. É um composto cristalino branco a esbranquiçado com uma fórmula molecular de C4H12ClN5 (monocloridrato) e um peso molecular de 165,63. O cloridrato de metformina é livremente solúvel em água e praticamente insolúvel em acetona, éter e clorofórmio. O pKa da metformina é 12,4. O pH de uma solução aquosa de cloridrato de metformina a 1% é 6,68. A fórmula estrutural é a seguinte:
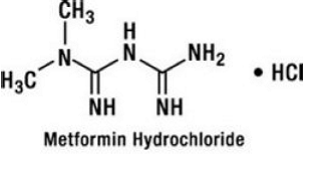
GLUCOVANCE 500 mg está disponível para administração oral em comprimidos contendo 1,25 mg de gliburida com 250 mg de cloridrato de metformina, 2,5 mg de gliburida com 500 mg de cloridrato de metformina e 5 mg de gliburida com 500 mg de cloridrato de metformina. Além disso, cada comprimido contém os seguintes ingredientes inativos: celulose microcristalina, povidona, croscarmelose sódica e estearato de magnésio. Os comprimidos são revestidos por película, o que proporciona diferenciação de cor.
INDICAÇÕES
GLUCOVANCE (Glyburide and Metformin HCl) Tablets é indicado como adjuvante à dieta e exercícios para melhorar o controle glicêmico em adultos com diabetes mellitus tipo 2.
DOSAGEM E ADMINISTRAÇÃO
considerações gerais
A dosagem de GLUCOVANCE deve ser individualizada com base na eficácia e na tolerância, sem exceder a dose diária máxima recomendada de 20 mg de gliburida/2000 mg de metformina. GLUCOVANCE deve ser administrado com as refeições e deve ser iniciado com uma dose baixa, com escalonamento gradual da dose conforme descrito abaixo, para evitar hipoglicemia (principalmente devido à gliburida), reduzir os efeitos colaterais gastrointestinais (principalmente devido à metformina) e permitir a determinação de a dose mínima eficaz para o controle adequado da glicemia para o paciente individual.
Com o tratamento inicial e durante a titulação da dose, o monitoramento adequado da glicemia deve ser usado para determinar a resposta terapêutica ao GLUCOVANCE 2,50mg e para identificar a dose mínima eficaz para o paciente. Depois disso, a HbA1c deve ser medida em intervalos de aproximadamente 3 meses para avaliar a eficácia da terapia. O objetivo terapêutico em todos os pacientes com diabetes tipo 2 é diminuir a GPF, PPG e HbA1c ao normal ou o mais próximo possível do normal. Idealmente, a resposta à terapia deve ser avaliada usando HbA (hemoglobina glicosilada), que é um melhor indicador de controle glicêmico a longo prazo do que o GLP sozinho.
Não foram realizados estudos específicos examinando a segurança e a eficácia da mudança para a terapia com GLUCOVANCE 400 mg em pacientes tomando concomitantemente gliburida (ou outra sulfonilureia) mais metformina. Alterações no controle glicêmico podem ocorrer nesses pacientes, podendo ocorrer hiperglicemia ou hipoglicemia. Qualquer mudança na terapia do diabetes tipo 2 deve ser realizada com cuidado e monitoramento apropriado.
GLUCOVANCE em pacientes com controle glicêmico inadequado em dieta e exercício
Dose inicial recomendada: 1,25 mg/250 mg uma ou duas vezes ao dia com as refeições.
Para pacientes com diabetes tipo 2 cuja hiperglicemia não pode ser controlada satisfatoriamente apenas com dieta e exercícios, a dose inicial recomendada de GLUCOVANCE 400 mg é 1,25 mg/250 mg uma vez ao dia com uma refeição. Como terapia inicial em pacientes com HbA1c inicial > 9% ou um FPG > 200 mg/dL, uma dose inicial de GLUCOVANCE 1,25 mg/250 mg duas vezes ao dia com as refeições da manhã e da noite pode ser usada. Os aumentos de dosagem devem ser feitos em incrementos de 1,25 mg/250 mg por dia a cada 2 semanas até a dose mínima eficaz necessária para alcançar o controle adequado da glicose no sangue. Em ensaios clínicos de GLUCOVANCE como terapia inicial, não houve experiência com doses diárias totais > 10 mg/2000 mg por dia. GLUCOVANCE 5 mg/500 mg não deve ser usado como terapia inicial devido ao risco aumentado de hipoglicemia.
GLUCOVANCE 500mg Uso em Pacientes com Controle Glicêmico Inadequado com Sulfonilureia e/ou Metformina
Dose inicial recomendada: 2,5 mg/500 mg ou 5 mg/500 mg duas vezes ao dia com as refeições.
Para pacientes não controlados adequadamente com gliburida (ou outra sulfonilureia) ou metformina isoladamente, a dose inicial recomendada de GLUCOVANCE é de 2,5 mg/500 mg ou 5 mg/500 mg duas vezes ao dia com as refeições da manhã e da noite. Para evitar hipoglicemia, a dose inicial de GLUCOVANCE 2,50mg não deve exceder as doses diárias de gliburida ou metformina já em uso. A dose diária deve ser titulada em incrementos não superiores a 5 mg/500 mg até a dose mínima eficaz para alcançar o controle adequado da glicemia ou até uma dose máxima de 20 mg/2000 mg por dia.
Para pacientes previamente tratados com terapia combinada de gliburida (ou outra sulfonilureia) mais metformina, se trocados para GLUCOVANCE, a dose inicial não deve exceder a dose diária de gliburida (ou dose equivalente de outra sulfonilureia) e metformina já em uso. Os pacientes devem ser monitorados de perto quanto a sinais e sintomas de hipoglicemia após tal troca e a dose de GLUCOVANCE deve ser titulada conforme descrito acima para alcançar o controle adequado da glicose no sangue.
Adição de tiazolidinedionas à terapia com GLUCOVANCE
Para pacientes não controlados adequadamente com GLUCOVANCE, uma tiazolidinediona pode ser adicionada à terapia com GLUCOVANCE 400mg. Quando uma tiazolidinediona é adicionada à terapia com GLUCOVANCE, a dose atual de GLUCOVANCE 500mg pode ser continuada e a tiazolidinediona iniciada na dose inicial recomendada. Para pacientes que necessitam de controle glicêmico adicional, a dose da tiazolidinediona pode ser aumentada com base no esquema de titulação recomendado. O aumento do controle glicêmico obtido com GLUCOVANCE mais uma tiazolidinediona pode aumentar o potencial de hipoglicemia a qualquer hora do dia. Em pacientes que desenvolvem hipoglicemia ao receber GLUCOVANCE 5mg e uma tiazolidinediona, deve-se considerar a redução da dose do componente gliburida de GLUCOVANCE. Conforme clinicamente justificado, o ajuste das dosagens dos outros componentes do regime antidiabético também deve ser considerado.
Pacientes que Recebem Colesevelam
Quando colesevelam é coadministrado com gliburida, a concentração plasmática máxima e a exposição total à gliburida são reduzidas. Portanto, GLUCOVANCE deve ser administrado pelo menos 4 horas antes do colesevelam.
Populações Específicas de Pacientes
GLUCOVANCE não é recomendado para uso durante a gravidez. A dosagem inicial e de manutenção de GLUCOVANCE deve ser conservadora em pacientes com idade avançada, devido ao potencial de diminuição da função renal nessa população. Qualquer ajuste de dose requer uma avaliação cuidadosa da função renal. Geralmente, pacientes idosos, debilitados e desnutridos não devem ser titulados para a dose máxima de GLUCOVANCE para evitar o risco de hipoglicemia. O monitoramento da função renal é necessário para auxiliar na prevenção da acidose láctica associada à metformina, particularmente em idosos. (Ver AVISOS .)
COMO FORNECIDO
GLUCOVANCE® (Gliburida e Metformina HCl) Comprimidos
GLUCOVANCE 1,25 mg/250 mg comprimido é amarelo pálido, em forma de cápsula, biconvexo, biconvexo, revestido por película com “ BMS ” gravado de um lado e “ 6072 ” gravado no lado oposto.
GLUCOVANCE 2,5 mg/500 mg O comprimido é um comprimido revestido por película laranja pálido, em forma de cápsula, com bordas biseladas, com “ BMS ” gravado de um lado e “ 6073 ” gravado no lado oposto.
GLUCOVANCE 5 mg/500 mg O comprimido é amarelo, em forma de cápsula, biconvexo, biconvexo, revestido por película com “ BMS ” gravado de um lado e “ 6074 ” gravado no lado oposto.
Armazenar
Armazenar em temperaturas de até 25°C (77°F). [Ver Temperatura ambiente controlada USP .]
Dispensar em recipientes resistentes à luz.
Distribuído por: Bristol-Myers Squibb Company, Princeton, NJ 08543 EUA 1158884A7. Rev Out 2013
EFEITOS COLATERAIS
GLUCOVANCE
Em ensaios clínicos duplo-cegos envolvendo GLUCOVANCE 2,50 mg como terapia inicial ou como terapia de segunda linha, um total de 642 pacientes receberam GLUCOVANCE 2,50 mg, 312 receberam terapia com metformina, 324 receberam terapia com gliburida e 161 receberam placebo. A porcentagem de pacientes que relataram eventos e tipos de eventos adversos relatados em ensaios clínicos de GLUCOVANCE (todas as dosagens) como terapia inicial e terapia de segunda linha estão listados na Tabela 6.
Em um ensaio clínico controlado de rosiglitazona versus placebo em pacientes tratados com GLUCOVANCE (n=365), 181 pacientes receberam GLUCOVANCE 5mg com rosiglitazona e 184 receberam GLUCOVANCE com placebo.
Edema foi relatado em 7,7% (14/181) dos pacientes tratados com rosiglitazona em comparação com 2,2% (4/184) dos pacientes tratados com placebo. Um ganho de peso médio de 3 kg foi observado em pacientes tratados com rosiglitazona.
Reações do tipo dissulfiram foram relatadas muito raramente em pacientes tratados com comprimidos de gliburida.
Hipoglicemia
Em ensaios clínicos controlados de GLUCOVANCE 5mg não houve episódios de hipoglicemia que necessitassem de intervenção médica e/ou terapia farmacológica; todos os eventos foram gerenciados pelos pacientes. A incidência de sintomas relatados de hipoglicemia (como tontura, tremores, sudorese e fome), no teste de terapia inicial de GLUCOVANCE 2,50 mg, está resumida na Tabela 7. A frequência de sintomas de hipoglicemia em pacientes tratados com GLUCOVANCE 1,25 mg/250 mg foi maior em pacientes com HbA1c basal 8%. Para pacientes com HbA1c basal entre 8% e 11% tratados com GLUCOVANCE 2,5 mg/500 mg como terapia inicial, a frequência de sintomas hipoglicêmicos foi de 30% a 35%. Como terapia de segunda linha em pacientes inadequadamente controlados apenas com sulfonilureia, aproximadamente 6,8% de todos os pacientes tratados com GLUCOVANCE 2,50mg apresentaram sintomas de hipoglicemia. Quando a rosiglitazona foi adicionada à terapia com GLUCOVANCE 2,50 mg, 22% dos pacientes relataram 1 ou mais medições de glicose por punção digital ≤ 50 mg/dL em comparação com 3,3% dos pacientes tratados com placebo. Todos os eventos hipoglicêmicos foram controlados pelos pacientes e apenas 1 paciente descontinuou por hipoglicemia. (Ver PRECAUÇÕES : Em geral : Adição de Tiazolidinedionas à Terapia GLUCOVANCE .)
Reações gastrointestinais
A incidência de efeitos colaterais gastrointestinais (GI) (diarreia, náusea/vômito e dor abdominal) no estudo de terapia inicial está resumida na Tabela 7. Em todos os estudos de GLUCOVANCE 500mg, os sintomas gastrointestinais foram os eventos adversos mais comuns com GLUCOVANCE 400mg e foram mais freqüente em níveis de dose mais elevados.
Em estudos controlados,
Em notificações pós-comercialização, icterícia colestática e hepatite podem ocorrer raramente, podendo progredir para insuficiência hepática; GLUCOVANCE 5mg deve ser descontinuado se isso ocorrer.
INTERAÇÕES MEDICAMENTOSAS
GLUCOVANCE
Certos medicamentos tendem a produzir hiperglicemia e podem levar à perda do controle da glicose no sangue. Esses medicamentos incluem tiazidas e outros diuréticos, corticosteroides, fenotiazinas, produtos da tireoide, estrogênios, contraceptivos orais, fenitoína, ácido nicotínico, simpaticomiméticos, medicamentos bloqueadores dos canais de cálcio e isoniazida. Quando esses medicamentos são administrados a um paciente recebendo GLUCOVANCE 400mg, o paciente deve ser observado atentamente quanto à perda do controle da glicose no sangue. Quando tais drogas são retiradas de um paciente recebendo GLUCOVANCE, o paciente deve ser observado atentamente quanto a hipoglicemia. A metformina liga-se de forma insignificante às proteínas plasmáticas e, portanto, é menos provável de interagir com drogas altamente ligadas às proteínas, como salicilatos, sulfonamidas, cloranfenicol e probenecida, em comparação com as sulfonilureias, que se ligam extensivamente às proteínas séricas.
Gliburida
ação hipoglicemiante das sulfonilureias pode ser potencializada por certos medicamentos, incluindo agentes anti-inflamatórios não esteroides e outros medicamentos altamente ligados a proteínas, salicilatos, sulfonamidas, cloranfenicol, probenecida, cumarinas, inibidores da monoaminoxidase e agentes bloqueadores beta-adrenérgicos. Quando esses medicamentos são administrados a um paciente recebendo GLUCOVANCE, o paciente deve ser observado atentamente quanto a hipoglicemia. Quando esses medicamentos são retirados de um paciente recebendo GLUCOVANCE 2,50mg, o paciente deve ser observado atentamente quanto à perda do controle da glicose no sangue.
Um risco aumentado de elevação das enzimas hepáticas foi observado em pacientes recebendo gliburida concomitantemente com bosentana. Portanto, a administração concomitante de GLUCOVANCE e bosentana é contraindicada.
Uma possível interação entre gliburida e ciprofloxacina, um antibiótico fluoroquinolona, foi relatada, resultando em uma potencialização da ação hipoglicêmica da gliburida. O mecanismo para esta interação não é conhecido.
Foi relatada uma potencial interação entre miconazol oral e agentes hipoglicemiantes orais levando a hipoglicemia grave. Não se sabe se essa interação também ocorre com as preparações intravenosas, tópicas ou vaginais de miconazol.
Colesevelam: a administração concomitante de colesevelam e gliburida resultou em reduções na AUC e Cmax da gliburida de 32% e 47%, respectivamente. As reduções na AUC e Cmax da gliburida foram de 20% e 15%, respectivamente, quando administradas 1 hora antes, e não mudaram significativamente (-7% e 4%, respectivamente) quando administradas 4 horas antes do colesevelam.
Cloridrato de Metformina
Furosemida
Um estudo de interação medicamentosa de dose única de metformina-furosemida em indivíduos saudáveis demonstrou que os parâmetros farmacocinéticos de ambos os compostos foram afetados pela coadministração. A furosemida aumentou a Cmax plasmática e sanguínea da metformina em 22% e a AUC sanguínea em 15%, sem qualquer alteração significativa na depuração renal da metformina. Quando administrado com metformina, a Cmax e a AUC da furosemida foram 31% e 12% menores, respectivamente, do que quando administradas isoladamente, e a meia-vida terminal foi reduzida em 32%, sem qualquer alteração significativa na depuração renal da furosemida. Não há informações disponíveis sobre a interação de metformina e furosemida quando coadministrados cronicamente.
Nifedipina
Um estudo de interação medicamentosa de dose única de metformina-nifedipina em voluntários saudáveis normais demonstrou que a coadministração de nifedipina aumentou a Cmax e a AUC plasmática da metformina em 20% e 9%, respectivamente, e aumentou a quantidade excretada na urina. Tmax e meia-vida não foram afetados. A nifedipina parece aumentar a absorção da metformina. A metformina teve efeitos mínimos sobre a nifedipina.
Drogas catiônicas
Drogas catiônicas (por exemplo, amilorida, digoxina, morfina, procainamida, quinidina, quinina, ranitidina, triantereno, trimetoprima ou vancomicina) que são eliminadas pela secreção tubular renal teoricamente têm o potencial de interação com a metformina por competir por sistemas de transporte tubular renal comuns. Essa interação entre a metformina e a cimetidina oral foi observada em voluntários saudáveis normais em estudos de interação medicamentosa metformina-cimetidina de dose única e múltipla, com um aumento de 60% no pico de metformina no plasma e nas concentrações de sangue total e um aumento de 40% no plasma e AUC de metformina de sangue total. Não houve alteração na meia-vida de eliminação no estudo de dose única. A metformina não teve efeito na farmacocinética da cimetidina. Embora tais interações permaneçam teóricas (exceto para cimetidina), recomenda-se monitoramento cuidadoso do paciente e ajuste de dose de GLUCOVANCE e/ou do medicamento interferente em pacientes que estejam tomando medicamentos catiônicos que são excretados através do sistema secretor tubular renal proximal.
Outro
Em voluntários saudáveis, a farmacocinética de metformina e propranolol e metformina e ibuprofeno não foi afetada quando coadministrados em estudos de interação de dose única.
AVISOS
Cloridrato de Metformina
Acidose láctica
A acidose láctica é uma complicação metabólica rara, mas grave, que pode ocorrer devido ao acúmulo de metformina durante o tratamento com GLUCOVANCE (Gliburida e Metformina HCl) comprimidos; quando ocorre, é fatal em aproximadamente 50% dos casos. A acidose láctica também pode ocorrer em associação com várias condições fisiopatológicas, incluindo diabetes mellitus, e sempre que houver hipoperfusão tecidual significativa e hipoxemia. A acidose láctica é caracterizada por níveis elevados de lactato no sangue (> 5 mmol/L), diminuição do pH sanguíneo, distúrbios eletrolíticos com aumento do anion gap e aumento da relação lactato/piruvato. Quando a metformina está implicada como causa da acidose láctica, geralmente são encontrados níveis plasmáticos de metformina > 5 μg/mL.
incidência relatada de acidose láctica em pacientes recebendo cloridrato de metformina é muito baixa (aproximadamente 0,03 casos/1.000 pacientes-ano, com aproximadamente 0,015 casos fatais/1.000 pacientes-ano). Em mais de 20.000 pacientes-ano de exposição à metformina em ensaios clínicos, não houve relatos de acidose láctica. Os casos relatados ocorreram principalmente em pacientes diabéticos com insuficiência renal significativa, incluindo doença renal intrínseca e hipoperfusão renal, muitas vezes no contexto de vários problemas médicos/cirúrgicos concomitantes e vários medicamentos concomitantes. Pacientes com insuficiência cardíaca congestiva que requerem tratamento farmacológico, em particular aqueles com insuficiência cardíaca congestiva instável ou aguda que correm risco de hipoperfusão e hipoxemia, apresentam risco aumentado de acidose lática. O risco de acidose láctica aumenta com o grau de disfunção renal e a idade do paciente. O risco de acidose láctica pode, portanto, ser significativamente diminuído pelo monitoramento regular da função renal em pacientes em uso de metformina e pelo uso da dose mínima eficaz de metformina. Em particular, o tratamento dos idosos deve ser acompanhado por uma monitorização cuidadosa da função renal. O tratamento com GLUCOVANCE 2,50 mg não deve ser iniciado em pacientes com idade ≥ 80 anos, a menos que a medição da depuração de creatinina demonstre que a função renal não está reduzida, pois esses pacientes são mais suscetíveis a desenvolver acidose láctica. Além disso, GLUCOVANCE deve ser imediatamente suspenso na presença de qualquer condição associada a hipoxemia, desidratação ou sepse. Como a função hepática prejudicada pode limitar significativamente a capacidade de eliminar o lactato, GLUCOVANCE geralmente deve ser evitado em pacientes com evidência clínica ou laboratorial de doença hepática. Os pacientes devem ser advertidos contra a ingestão excessiva de álcool, aguda ou crônica, ao tomar GLUCOVANCE 2,50 mg, uma vez que o álcool potencializa os efeitos do cloridrato de metformina no metabolismo do lactato. Além disso, GLUCOVANCE 5mg deve ser temporariamente descontinuado antes de qualquer estudo de radiocontraste intravascular e para qualquer procedimento cirúrgico (ver também PRECAUÇÕES).
início da acidose láctica geralmente é sutil e acompanhado apenas por sintomas inespecíficos, como mal-estar, mialgias, desconforto respiratório, aumento da sonolência e desconforto abdominal inespecífico. Pode haver hipotermia, hipotensão e bradiarritmias resistentes associadas com acidose mais acentuada. O paciente e o médico do paciente devem estar cientes da possível importância de tais sintomas e o paciente deve ser instruído a notificar o médico imediatamente se ocorrerem (ver também PRECAUÇÕES). GLUCOVANCE 500mg deve ser retirado até que a situação seja esclarecida. Eletrólitos séricos, cetonas, glicose no sangue e, se indicado, pH sanguíneo, níveis de lactato e até níveis de metformina no sangue podem ser úteis. Uma vez que o paciente esteja estabilizado com qualquer nível de dose de GLUCOVANCE, é improvável que os sintomas gastrointestinais, que são comuns durante o início da terapia com metformina, estejam relacionados ao medicamento. A ocorrência posterior de sintomas gastrointestinais pode ser devido a acidose láctica ou outra doença grave.
Níveis de lactato plasmático venoso em jejum acima do limite superior do normal, mas inferiores a 5 mmol/L em pacientes tomando GLUCOVANCE não indicam necessariamente acidose láctica iminente e podem ser explicáveis por outros mecanismos, como diabetes mal controlado ou obesidade, atividade física vigorosa, ou problemas técnicos no manuseio simples. (Veja também PRECAUÇÕES.)
Deve-se suspeitar de acidose lática em qualquer paciente diabético com acidose metabólica sem evidência de cetoacidose (cetonúria e cetonemia).
acidose láctica é uma emergência médica que deve ser tratada em ambiente hospitalar. Em um paciente com acidose lática que esteja tomando GLUCOVANCE 500mg, o medicamento deve ser descontinuado imediatamente e medidas gerais de suporte prontamente instituídas. Como o cloridrato de metformina é dialisável (com depuração de até 170 mL/min em boas condições hemodinâmicas), recomenda-se hemodiálise imediata para corrigir a acidose e remover a metformina acumulada. Esse manejo geralmente resulta na reversão imediata dos sintomas e na recuperação. (Veja também CONTRA-INDICAÇÕES e PRECAUÇÕES.)
AVISO ESPECIAL SOBRE O RISCO AUMENTADO DE MORTALIDADE CARDIOVASCULAR
administração de hipoglicemiantes orais tem sido associada ao aumento da mortalidade cardiovascular em comparação ao tratamento com dieta isolada ou dieta mais insulina. Este alerta é baseado no estudo realizado pelo University Group Diabetes Program (UGDP), um ensaio clínico prospectivo de longo prazo projetado para avaliar a eficácia de medicamentos hipoglicemiantes na prevenção ou retardo de complicações vasculares em pacientes com diabetes não insulinodependente. O estudo envolveu 823 pacientes que foram distribuídos aleatoriamente em 1 de 4 grupos de tratamento (Diabetes 19 (Suppl. 2):747-830, 1970).
UGDP relatou que os pacientes tratados por 5 a 8 anos com dieta mais uma dose fixa de tolbutamida (1,5 g por dia) tiveram uma taxa de mortalidade cardiovascular aproximadamente 2,5 vezes maior do que os pacientes tratados apenas com dieta. Não foi observado aumento significativo da mortalidade total, mas o uso de tolbutamida foi descontinuado com base no aumento da mortalidade cardiovascular, limitando a oportunidade de o estudo mostrar aumento da mortalidade geral. Apesar da controvérsia quanto à interpretação desses resultados , os achados do estudo UGDP fornecem uma base adequada para esse alerta. O paciente deve ser informado dos riscos e benefícios potenciais da gliburida e dos modos alternativos de terapia.
Embora apenas 1 fármaco da classe das sulfonilureias (tolbutamida) tenha sido incluído neste estudo, é prudente do ponto de vista da segurança considerar que esta advertência também pode ser aplicada a outros hipoglicemiantes desta classe, tendo em vista suas semelhanças no modo de ação e estrutura química.
PRECAUÇÕES
Em geral
Resultados Macrovasculares
Não houve estudos clínicos estabelecendo evidências conclusivas de redução do risco macrovascular com GLUCOVANCE 5mg ou qualquer outro medicamento antidiabético.
GLUCOVANCE
Hipoglicemia
GLUCOVANCE 400mg é capaz de produzir hipoglicemia ou sintomas hipoglicêmicos, portanto, a seleção, dosagem e instruções adequadas do paciente são importantes para evitar possíveis episódios de hipoglicemia. O risco de hipoglicemia aumenta quando a ingestão calórica é deficiente, quando o exercício extenuante não é compensado pela suplementação calórica ou durante o uso concomitante com outros agentes hipoglicemiantes ou etanol. A insuficiência renal ou hepática pode causar níveis elevados de gliburida e cloridrato de metformina, e a insuficiência hepática também pode diminuir a capacidade gliconeogênica, ambas aumentando o risco de reações hipoglicêmicas. Pacientes idosos, debilitados ou desnutridos e aqueles com insuficiência adrenal ou pituitária ou intoxicação alcoólica são particularmente suscetíveis a efeitos hipoglicêmicos. A hipoglicemia pode ser difícil de reconhecer em idosos e pessoas que estão tomando medicamentos bloqueadores beta-adrenérgicos.
Gliburida
Anemia hemolítica
tratamento de pacientes com deficiência de glicose-6-fosfato desidrogenase (G6PD) com sulfonilureias pode levar à anemia hemolítica. Como GLUCOVANCE 400mg pertence à classe de agentes de sulfonilureia, deve-se ter cautela em pacientes com deficiência de G6PD e uma alternativa não sulfonilureia deve ser considerada. Em relatórios pós-comercialização, anemia hemolítica também foi relatada em pacientes que não apresentavam deficiência de G6PD conhecida.
Cloridrato de Metformina
Monitoramento da Função Renal
metformina é conhecida por ser substancialmente excretada pelos rins, e o risco de acúmulo de metformina e acidose lática aumenta com o grau de comprometimento da função renal. Assim, pacientes com níveis de creatinina sérica acima do limite superior do normal para a idade não devem receber GLUCOVANCE. Em pacientes com idade avançada, GLUCOVANCE 400mg deve ser cuidadosamente titulado para estabelecer a dose mínima para efeito glicêmico adequado, pois o envelhecimento está associado à redução da função renal. Em pacientes idosos, particularmente aqueles ≥ 80 anos de idade, a função renal deve ser monitorada regularmente e, geralmente, GLUCOVANCE 2,50mg não deve ser titulado até a dose máxima (ver AVISOS e DOSAGEM E ADMINISTRAÇÃO ). Antes do início da terapia com GLUCOVANCE 2,50 mg e, posteriormente, pelo menos anualmente, a função renal deve ser avaliada e verificada como normal. Em pacientes nos quais o desenvolvimento de disfunção renal é antecipado, a função renal deve ser avaliada com mais frequência e GLUCOVANCE descontinuado se houver evidência de disfunção renal.
Uso de medicamentos concomitantes que podem afetar a função renal ou a disposição da metformina
Medicamentos concomitantes que podem afetar a função renal ou resultar em alterações hemodinâmicas significativas ou podem interferir na disposição da metformina, como medicamentos catiônicos que são eliminados por secreção tubular renal (ver INTERAÇÕES MEDICAMENTOSAS ), deve ser usado com cautela.
Estudos radiológicos envolvendo o uso de materiais de contraste iodado intravascular (por exemplo, urografia intravenosa, colangiografia intravenosa, angiografia e tomografia computadorizada (TC) com materiais de contraste intravascular)
Estudos de contraste intravascular com materiais iodados podem levar à alteração aguda da função renal e foram associados à acidose láctica em pacientes recebendo metformina (ver CONTRA-INDICAÇÕES ). Portanto, em pacientes nos quais tal estudo está planejado, GLUCOVANCE 400mg deve ser descontinuado temporariamente no momento ou antes do procedimento, e suspenso por 48 horas após o procedimento e reinstituído somente após a função renal ter sido reavaliada e comprovada. normal.
Estados hipóxicos
Colapso cardiovascular (choque) de qualquer causa, insuficiência cardíaca congestiva aguda, infarto agudo do miocárdio e outras condições caracterizadas por hipoxemia têm sido associados à acidose láctica e também podem causar azotemia pré-renal. Quando tais eventos ocorrem em pacientes em terapia com GLUCOVANCE 2,50mg, o medicamento deve ser imediatamente descontinuado.
Procedimentos cirúrgicos
terapia com GLUCOVANCE 400mg deve ser temporariamente suspensa para qualquer procedimento cirúrgico (exceto procedimentos menores não associados à ingestão restrita de alimentos e líquidos) e não deve ser reiniciada até que a ingestão oral do paciente seja retomada e a função renal tenha sido avaliada como normal.
Ingestão de álcool
O álcool é conhecido por potencializar o efeito da metformina no metabolismo do lactato. Os pacientes, portanto, devem ser alertados contra a ingestão excessiva de álcool, aguda ou crônica, enquanto estiverem recebendo GLUCOVANCE. Devido ao seu efeito sobre a capacidade gliconeogênica do fígado, o álcool também pode aumentar o risco de hipoglicemia.
Função hepática prejudicada
Uma vez que a função hepática comprometida foi associada a alguns casos de acidose láctica, GLUCOVANCE 500mg deve ser evitado em pacientes com evidência clínica ou laboratorial de doença hepática.
Níveis de Vitamina B12
Em ensaios clínicos controlados com metformina de 29 semanas de duração, foi observada uma diminuição para níveis subnormais de vitamina B12 sérica previamente normal, sem manifestações clínicas, em aproximadamente 7% dos pacientes. Essa diminuição, possivelmente devido à interferência na absorção de B12 do complexo B12-fator intrínseco, é, no entanto, muito raramente associada à anemia e parece ser rapidamente reversível com a descontinuação da suplementação de metformina ou vitamina B. A medição dos parâmetros hematológicos anualmente é aconselhada em pacientes em uso de metformina e quaisquer anormalidades aparentes devem ser adequadamente investigadas e tratadas (ver PRECAUÇÕES : Testes laboratoriais ).
Certos indivíduos (aqueles com ingestão ou absorção inadequada de vitamina B12 ou cálcio) parecem estar predispostos a desenvolver níveis subnormais de vitamina B12. Nesses pacientes, as dosagens de rotina da vitamina B12 sérica em intervalos de 2 a 3 anos podem ser úteis.
Mudança no estado clínico de pacientes com diabetes tipo 2 previamente controlada
Um paciente com diabetes tipo 2 previamente bem controlado com metformina que desenvolve anormalidades laboratoriais ou doença clínica (especialmente doença vaga e mal definida) deve ser avaliado imediatamente para evidência de cetoacidose ou acidose lática. A avaliação deve incluir eletrólitos e cetonas séricos, glicemia e, se indicado, pH sanguíneo, lactato, piruvato e níveis de metformina. Se ocorrer acidose de qualquer forma, GLUCOVANCE deve ser interrompido imediatamente e outras medidas corretivas apropriadas devem ser iniciadas (ver também AVISOS ).
Adição de Tiazolidinedionas à Terapia GLUCOVANCE 500mg
Hipoglicemia
Pacientes recebendo GLUCOVANCE 2,50 mg em combinação com uma tiazolidinediona podem estar em risco de hipoglicemia.
Ganho de peso
O ganho de peso foi observado com a adição de rosiglitazona a GLUCOVANCE 5mg, semelhante ao relatado para a terapia com tiazolidinediona isolada.
Efeitos hepáticos
Quando uma tiazolidinediona é usada em combinação com GLUCOVANCE 2,50mg, o monitoramento periódico dos testes de função hepática deve ser realizado de acordo com as recomendações do rótulo para a tiazolidinediona.
Informações para pacientes
GLUCOVANCE
Os pacientes devem ser informados sobre os riscos e benefícios potenciais de GLUCOVANCE 500mg e modos alternativos de terapia. Eles também devem ser informados sobre a importância da adesão às orientações alimentares; um programa regular de exercícios; e testes regulares de glicose no sangue, hemoglobina glicosilada, função renal e parâmetros hematológicos.
Os riscos de acidose láctica associados à terapia com metformina, seus sintomas e condições que predispõem ao seu desenvolvimento, conforme observado nas seções de ADVERTÊNCIAS e PRECAUÇÕES, devem ser explicados aos pacientes. Os pacientes devem ser aconselhados a descontinuar GLUCOVANCE imediatamente e notificar imediatamente seu médico se ocorrer hiperventilação inexplicável, mialgia, mal-estar, sonolência incomum ou outros sintomas inespecíficos. Uma vez que o paciente esteja estabilizado em qualquer nível de dose de GLUCOVANCE, é improvável que os sintomas gastrointestinais, que são comuns durante o início da terapia com metformina, estejam relacionados ao medicamento. A ocorrência posterior de sintomas gastrointestinais pode ser devido a acidose láctica ou outra doença grave.
Os riscos da hipoglicemia, seus sintomas e tratamento e as condições que predispõem ao seu desenvolvimento devem ser explicados aos pacientes e familiares responsáveis.
Os pacientes devem ser aconselhados contra a ingestão excessiva de álcool, aguda ou crônica, enquanto estiverem recebendo GLUCOVANCE. (Ver INFORMAÇÕES DO PACIENTE impressas abaixo de.)
Testes laboratoriais
Devem ser realizadas medições periódicas de glicemia de jejum (FBG) e HbA1c para monitorar a resposta terapêutica.
O monitoramento inicial e periódico dos parâmetros hematológicos (por exemplo, índices de hemoglobina/hematócrito e eritrócitos) e da função renal (creatinina sérica) deve ser realizado, pelo menos anualmente. Embora a anemia megaloblástica raramente tenha sido observada com a terapia com metformina, se houver suspeita, a deficiência de vitamina B12 deve ser excluída.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Não foram realizados estudos em animais com os produtos combinados de GLUCOVANCE. Os dados a seguir são baseados em descobertas em estudos realizados com os produtos individuais.
Gliburida
Estudos em ratos com gliburida isolada em doses de até 300 mg/kg/dia (aproximadamente 145 vezes a dose humana diária máxima recomendada [MRHD] de 20 mg para o componente gliburida de GLUCOVANCE 5mg com base em comparações de área de superfície corporal) por 18 meses revelaram sem efeitos cancerígenos. Em um estudo de oncogenicidade de 2 anos de gliburida em camundongos, não houve evidência de tumores relacionados ao tratamento.
Não houve evidência de potencial mutagênico da gliburida isoladamente nos seguintes testes in vitro: teste de microssoma de Salmonella (teste de Ames) e no teste de dano ao DNA/eluição alcalina.
Cloridrato de Metformina
Estudos de carcinogenicidade de longo prazo foram realizados com metformina isolada em ratos (duração da dosagem de 104 semanas) e camundongos (duração da dosagem de 91 semanas) em doses até e incluindo 900 mg/kg/dia e 1500 mg/kg/dia, respectivamente. Estas doses são aproximadamente 4 vezes a dose de MRHD de 2000 mg do componente metformina de GLUCOVANCE 400 mg com base em comparações da área de superfície corporal. Nenhuma evidência de carcinogenicidade com metformina isolada foi encontrada em camundongos machos ou fêmeas. Da mesma forma, não foi observado potencial tumorigênico com metformina isolada em ratos machos. Houve, no entanto, uma incidência aumentada de pólipos uterinos estromais benignos em ratas tratadas apenas com 900 mg/kg/dia de metformina.
Não houve evidência de potencial mutagênico da metformina isolada nos seguintes testes in vitro: teste de Ames (S. typhimurium), teste de mutação genética (células de linfoma de camundongo) ou teste de aberrações cromossômicas (linfócitos humanos). Os resultados no teste de micronúcleo em camundongos in vivo também foram negativos.
fertilidade de ratos machos ou fêmeas não foi afetada pela metformina isolada quando administrada em doses tão altas quanto 600 mg/kg/dia, que é aproximadamente 3 vezes a dose de MRHD do componente metformina de GLUCOVANCE 400 mg com base em comparações de área de superfície corporal.
Gravidez
Efeitos teratogênicos
Gravidez Categoria B
Informações recentes sugerem fortemente que níveis anormais de glicose no sangue durante a gravidez estão associados a uma maior incidência de anomalias congênitas. A maioria dos especialistas recomenda que a insulina seja usada durante a gravidez para manter a glicose no sangue o mais próximo possível do normal. Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, GLUCOVANCE 400mg não deve ser usado durante a gravidez, a menos que seja claramente necessário. (Veja abaixo.)

Não existem estudos adequados e bem controlados em mulheres grávidas com GLUCOVANCE ou seus componentes individuais. Não foram realizados estudos em animais com os produtos combinados de GLUCOVANCE. Os dados a seguir são baseados em descobertas em estudos realizados com os produtos individuais.
Gliburida
Estudos de reprodução foram realizados em ratos e coelhos com doses de até 500 vezes a dose de MRHD de 20 mg do componente gliburida de GLUCOVANCE 500 mg com base em comparações de área de superfície corporal e não revelaram evidências de fertilidade prejudicada ou danos ao feto devido à gliburida.
Cloridrato de Metformina
A metformina isolada não foi teratogênica em ratos ou coelhos em doses de até 600 mg/kg/dia. Isso representa uma exposição de cerca de 2 e 6 vezes a dose de MRHD de 2.000 mg do componente metformina de GLUCOVANCE 500 mg com base em comparações de área de superfície corporal para ratos e coelhos, respectivamente. A determinação das concentrações fetais demonstrou uma barreira placentária parcial à metformina.
Efeitos não teratogênicos
Hipoglicemia grave prolongada (4-10 dias) foi relatada em recém-nascidos de mães que estavam recebendo uma sulfonilureia no momento do parto. Isso tem sido relatado com mais frequência com o uso de agentes com meia-vida prolongada. Não é recomendado que GLUCOVANCE 400mg seja usado durante a gravidez. No entanto, se for utilizado, GLUCOVANCE deve ser descontinuado pelo menos 2 semanas antes da data prevista de entrega. (Ver Gravidez : Efeitos teratogênicos : Gravidez Categoria B .)
Mães que amamentam
Embora não se saiba se a gliburida é excretada no leite humano, sabe-se que algumas sulfonilureias são excretadas no leite humano. Estudos em ratas lactantes mostram que a metformina é excretada no leite e atinge níveis comparáveis aos do plasma. Estudos semelhantes não foram realizados em mães que amamentam. Como o potencial de hipoglicemia em lactentes pode existir, deve-se decidir entre descontinuar a amamentação ou descontinuar GLUCOVANCE, levando em consideração a importância do medicamento para a mãe. Se GLUCOVANCE for descontinuado e se a dieta por si só for inadequada para controlar a glicemia, a terapia com insulina deve ser considerada.
Uso Pediátrico
segurança e eficácia de GLUCOVANCE 500mg foram avaliadas em um estudo randomizado de 26 semanas, duplo-cego, controlado por ativo, envolvendo um total de 167 pacientes pediátricos (com idade variando de 9 a 16 anos) com diabetes tipo 2. GLUCOVANCE 500mg não demonstrou ser estatisticamente superior à metformina ou à gliburida no que diz respeito à redução da HbA1c desde o início (ver Tabela 5). Nenhum achado de segurança inesperado foi associado ao GLUCOVANCE 2,50mg neste estudo.
Uso Geriátrico
Dos 642 pacientes que receberam GLUCOVANCE em estudos clínicos duplo-cegos, 23,8% tinham 65 anos ou mais, enquanto 2,8% tinham 75 anos ou mais. Dos 1.302 pacientes que receberam GLUCOVANCE 500mg em estudos clínicos abertos, 20,7% tinham 65 anos ou mais, enquanto 2,5% tinham 75 anos ou mais. Não foram observadas diferenças gerais na eficácia ou segurança entre esses pacientes e pacientes mais jovens, e outras experiências clínicas relatadas não identificaram diferenças na resposta entre pacientes idosos e pacientes mais jovens, mas a maior sensibilidade de alguns indivíduos mais velhos não pode ser descartada.
O cloridrato de metformina é conhecido por ser substancialmente excretado pelos rins e, como o risco de reações adversas graves ao medicamento é maior em pacientes com função renal comprometida, GLUCOVANCE 500mg deve ser usado apenas em pacientes com função renal normal (ver CONTRA-INDICAÇÕES , AVISOS , e FARMACOLOGIA CLÍNICA : Farmacocinética ). Como o envelhecimento está associado à redução da função renal, GLUCOVANCE 5mg deve ser usado com cautela à medida que a idade aumenta. Deve-se ter cuidado na seleção da dose e deve ser baseado no monitoramento cuidadoso e regular da função renal. Geralmente, pacientes idosos não devem ser titulados para a dose máxima de GLUCOVANCE (ver também AVISOS e DOSAGEM E ADMINISTRAÇÃO ).
SOBREDOSAGEM
Gliburida
superdosagem de sulfonilureias, incluindo comprimidos de gliburida, pode produzir hipoglicemia. Sintomas hipoglicêmicos leves, sem perda de consciência ou achados neurológicos, devem ser tratados agressivamente com glicose oral e ajustes na dosagem do medicamento e/ou nos padrões de alimentação. O monitoramento cuidadoso deve continuar até que o médico tenha certeza de que o paciente está fora de perigo. Reações hipoglicêmicas graves com coma, convulsão ou outro comprometimento neurológico ocorrem com pouca frequência, mas constituem emergências médicas que requerem hospitalização imediata. Se houver suspeita ou diagnóstico de coma hipoglicêmico, o paciente deve receber uma injeção intravenosa rápida de solução concentrada de glicose (50%). Isso deve ser seguido por uma infusão contínua de uma solução de glicose mais diluída (10%) a uma taxa que manterá a glicose no sangue em um nível acima de 100 mg/dL. Os pacientes devem ser monitorados de perto por um período mínimo de 24 a 48 horas, pois a hipoglicemia pode recorrer após aparente recuperação clínica.
Cloridrato de Metformina
Ocorreu superdose de cloridrato de metformina, incluindo ingestão de quantidades > 50 g. Hipoglicemia foi relatada em aproximadamente 10% dos casos, mas nenhuma associação causal com o cloridrato de metformina foi estabelecida. Acidose láctica foi relatada em aproximadamente 32% dos casos de superdosagem de metformina (ver AVISOS ). A metformina é dialisável com depuração de até 170 mL/min em boas condições hemodinâmicas. Portanto, a hemodiálise pode ser útil para a remoção do fármaco acumulado de pacientes nos quais há suspeita de superdosagem de metformina.
CONTRA-INDICAÇÕES
GLUCOVANCE 2,50mg é contraindicado em pacientes com:
GLUCOVANCE 500mg deve ser descontinuado temporariamente em pacientes submetidos a estudos radiológicos envolvendo administração intravascular de materiais de contraste iodados, porque o uso de tais produtos pode resultar em alteração aguda da função renal. (Veja também PRECAUÇÕES .)
FARMACOLOGIA CLÍNICA
Mecanismo de ação
GLUCOVANCE combina gliburida e cloridrato de metformina, 2 agentes anti-hiperglicêmicos com mecanismos de ação complementares, para melhorar o controle glicêmico em pacientes com diabetes tipo 2.
gliburida parece diminuir a glicose no sangue de forma aguda, estimulando a liberação de insulina do pâncreas, um efeito dependente do funcionamento das células beta nas ilhotas pancreáticas. O mecanismo pelo qual a gliburida reduz a glicose no sangue durante a administração a longo prazo não foi claramente estabelecido. Com a administração crônica em pacientes com diabetes tipo 2, o efeito de redução da glicose no sangue persiste apesar de um declínio gradual na resposta secretora de insulina ao fármaco. Os efeitos extrapancreáticos podem estar envolvidos no mecanismo de ação dos hipoglicemiantes orais de sulfonilureia.
O cloridrato de metformina é um agente anti-hiperglicêmico que melhora a tolerância à glicose em pacientes com diabetes tipo 2, reduzindo a glicose plasmática basal e pós-prandial. O cloridrato de metformina diminui a produção hepática de glicose, diminui a absorção intestinal de glicose e melhora a sensibilidade à insulina ao aumentar a captação e utilização periférica de glicose.
Farmacocinética
Absorção e Biodisponibilidade
GLUCOVANCE
Em estudos de biodisponibilidade de GLUCOVANCE 2,5 mg/500 mg e 5 mg/500 mg, a área média sob a curva de concentração plasmática versus tempo (AUC) para o componente gliburida foi 18% e 7%, respectivamente, maior que a do Micronase® marca de gliburida coadministrada com metformina. O componente gliburida do GLUCOVANCE, portanto, não é bioequivalente ao Micronase®. O componente metformina de GLUCOVANCE 400mg é bioequivalente à metformina coadministrada com gliburida.
Após a administração de um único comprimido de GLUCOVANCE 5 mg/500 mg com uma solução de glicose a 20% ou uma solução de glicose a 20% com alimentos, não houve efeito dos alimentos na Cmax e um efeito relativamente pequeno dos alimentos na AUC da gliburida componente. O Tmax para o componente gliburida foi reduzido de 7,5 horas para 2,75 horas com alimentos em comparação com a mesma dosagem de comprimido administrada em jejum com uma solução de glicose a 20%. O significado clínico de um Tmax anterior para gliburida após a alimentação não é conhecido. O efeito dos alimentos na farmacocinética do componente metformina foi indeterminado.
Gliburida
Estudos de dose única com Micronase® comprimidos em indivíduos normais demonstram absorção significativa de gliburida em 1 hora, níveis máximos do medicamento em cerca de 4 horas e níveis baixos, mas detectáveis, em 24 horas. Os níveis séricos médios de gliburida, refletidos pelas áreas sob a curva de concentração sérica-tempo, aumentam proporcionalmente aos aumentos correspondentes na dose. A bioequivalência não foi estabelecida entre GLUCOVANCE 500mg e produtos de gliburida de ingrediente único.
Cloridrato de Metformina
biodisponibilidade absoluta de um comprimido de cloridrato de metformina de 500 mg administrado em jejum é de aproximadamente 50% a 60%. Estudos utilizando doses orais únicas de comprimidos de metformina de 500 mg e 1.500 mg e 850 mg a 2.550 mg indicam que há falta de proporcionalidade da dose com o aumento das doses, o que se deve à diminuição da absorção e não à alteração na eliminação. Os alimentos diminuem a extensão e atrasam levemente a absorção da metformina, conforme demonstrado por uma concentração de pico 40% menor e uma AUC plasmática 25% menor e um prolongamento de 35 minutos do tempo até a concentração plasmática máxima após a administração de uma dose única de 850 mg. comprimido de metformina com alimentos, em comparação com a mesma dosagem de comprimido administrado em jejum. A relevância clínica destas diminuições é desconhecida.
Distribuição
Gliburida
As sulfonilureias são extensivamente ligadas às proteínas séricas. O deslocamento dos sítios de ligação às proteínas por outras drogas pode levar a um aumento da ação hipoglicemiante. In vitro, a ligação proteica exibida pela gliburida é predominantemente não iônica, enquanto a de outras sulfonilureias (clorpropamida, tolbutamida, tolazamida) é predominantemente iônica. Drogas ácidas, como fenilbutazona, varfarina e salicilatos, deslocam as sulfonilureias de ligação iônica das proteínas séricas em uma extensão muito maior do que a gliburida de ligação não iônica. Não foi demonstrado que esta diferença na ligação às proteínas resulta em menos interações medicamentosas com comprimidos de gliburida em uso clínico.
Cloridrato de Metformina
volume aparente de distribuição (V/F) da metformina após doses orais únicas de 850 mg foi em média de 654±358 L. A metformina liga-se de forma insignificante às proteínas plasmáticas. A metformina se divide em eritrócitos, provavelmente em função do tempo. Em doses clínicas e esquemas de dosagem usuais de metformina, as concentrações plasmáticas de metformina no estado de equilíbrio são atingidas dentro de 24 a 48 horas e geralmente são
Metabolismo e eliminação
Gliburida
diminuição da gliburida no soro de indivíduos normais e saudáveis é bifásica; a meia-vida terminal é de cerca de 10 horas. O principal metabólito da gliburida é o derivado 4-trans-hidroxi. Um segundo metabólito, o derivado 3-cis-hidroxi, também ocorre. Esses metabólitos provavelmente não contribuem com ação hipoglicemiante significativa em humanos, uma vez que são apenas fracamente ativos (1/400 e 1/40 tão ativos, respectivamente, quanto gliburida) em coelhos. A gliburida é excretada como metabólitos na bile e na urina, aproximadamente 50% por cada via. Essa via de excreção dupla é qualitativamente diferente daquela de outras sulfonilureias, que são excretadas principalmente na urina.
Cloridrato de Metformina
Estudos de dose única intravenosa em indivíduos normais demonstram que a metformina é excretada inalterada na urina e não sofre metabolismo hepático (nenhum metabólito foi identificado em humanos) nem excreção biliar. A depuração renal (ver Tabela 1) é aproximadamente 3,5 vezes maior que a depuração da creatinina, o que indica que a secreção tubular é a principal via de eliminação da metformina. Após administração oral, aproximadamente 90% do fármaco absorvido é eliminado por via renal nas primeiras 24 horas, com meia-vida de eliminação plasmática de aproximadamente 6,2 horas. No sangue, a meia-vida de eliminação é de aproximadamente 17,6 horas, sugerindo que a massa eritrocitária pode ser um compartimento de distribuição.
Populações Especiais
Pacientes com diabetes tipo 2
Estudos de dose múltipla com gliburida em pacientes com diabetes tipo 2 demonstram curvas de concentração-tempo de nível de droga semelhantes a estudos de dose única, indicando que não há acúmulo de droga nos depósitos de tecidos.
Na presença de função renal normal, não há diferenças entre a farmacocinética de dose única ou múltipla de metformina entre pacientes com diabetes tipo 2 e indivíduos normais (consulte a Tabela 1), nem há acúmulo de metformina em nenhum dos grupos nas condições clínicas usuais. doses.
Insuficiência Hepática
Não foram realizados estudos farmacocinéticos em pacientes com insuficiência hepática para gliburida ou metformina.
Insuficiência renal
Não há informações disponíveis sobre a farmacocinética da gliburida em pacientes com insuficiência renal.
Em pacientes com função renal diminuída (com base na depuração de creatinina), a meia-vida plasmática e sanguínea da metformina é prolongada e a depuração renal é diminuída em proporção à diminuição da depuração de creatinina (ver Tabela 1; também, ver AVISOS ).
Geriatria
Não há informações sobre a farmacocinética da gliburida em pacientes idosos.
Dados limitados de estudos farmacocinéticos controlados de metformina em idosos saudáveis sugerem que a depuração plasmática total está diminuída, a meia-vida é prolongada e a Cmax está aumentada, quando comparados a indivíduos jovens saudáveis. A partir desses dados, parece que a alteração na farmacocinética da metformina com o envelhecimento é explicada principalmente por uma alteração na função renal (ver Tabela 1). O tratamento com metformina não deve ser iniciado em pacientes ≥ 80 anos de idade, a menos que a medição da depuração de creatinina demonstre que a função renal não está reduzida.
Pediatria
Após a administração de um comprimido oral único de GLUCOPHAGE® (cloridrato de metformina) 500 mg com alimentos, a média geométrica da Cmax e da AUC da metformina diferiu
Após a administração de um comprimido oral único de GLUCOVANCE com alimentos, a média geométrica normalizada da dose de gliburida C e AUC em pacientes pediátricos com diabetes tipo 2 (11-16 anos de idade, n=28, peso corporal médio de 97 kg) diferiram
Gênero
Não há informações sobre o efeito do sexo na farmacocinética da gliburida.
Os parâmetros farmacocinéticos da metformina não diferiram significativamente em indivíduos com ou sem diabetes tipo 2 quando analisados de acordo com o sexo (homens=19, mulheres=16). Da mesma forma, em estudos clínicos controlados em pacientes com diabetes tipo 2, o efeito anti-hiperglicêmico da metformina foi comparável em homens e mulheres.
Corrida
Não há informações disponíveis sobre diferenças raciais na farmacocinética da gliburida.
Não foram realizados estudos dos parâmetros farmacocinéticos da metformina de acordo com a raça. Em estudos clínicos controlados de metformina em pacientes com diabetes tipo 2, o efeito anti-hiperglicêmico foi comparável em brancos (n=249), negros (n=51) e hispânicos (n=24).
Estudos clínicos
Pacientes com controle glicêmico inadequado apenas com dieta e exercícios
Em um ensaio clínico multicêntrico, duplo-cego, de 20 semanas nos EUA, um total de 806 pacientes com diabetes tipo 2 virgens de tratamento com medicamentos, cuja hiperglicemia não foi adequadamente controlada com dieta e exercícios isolados (glicemia basal em jejum [FPG]
tratamento com GLUCOVANCE resultou em redução significativamente maior na HbA e na glicose plasmática pós-prandial (PPG) em comparação com gliburida, metformina ou placebo. Além disso, a terapia com GLUCOVANCE resultou em maior redução no FPG em comparação com gliburida, metformina ou placebo, mas as diferenças de gliburida e metformina não atingiram significância estatística.
As alterações no perfil lipídico associadas ao tratamento com GLUCOVANCE 2,50 mg foram semelhantes às observadas com gliburida, metformina e placebo.
estudo duplo-cego controlado por placebo descrito acima restringiu a inscrição a pacientes com HbA1c
Pacientes com controle glicêmico inadequado apenas com sulfoniluréia
Em um ensaio clínico de 16 semanas, duplo-cego, com controle ativo nos EUA, um total de 639 pacientes com diabetes tipo 2 não controlados adequadamente (HbA1c basal média de 9,5%, FPG basal médio de 213 mg/dL) enquanto estavam sendo tratados com pelo menos metade da dose máxima de uma sulfonilureia (p. /500mg. As doses de metformina e GLUCOVANCE foram tituladas para um máximo de 4 comprimidos por dia, conforme necessário, para atingir FPG
Após 16 semanas, não houve alteração significativa na HbA média em pacientes randomizados para terapia com gliburida ou metformina. O tratamento com GLUCOVANCE 2,50 mg em doses de até 20 mg/2000 mg por dia resultou em redução significativa de HbA, FPG e PPG desde o início em comparação com gliburida ou metformina isoladamente.
Adição de Tiazolidinedionas à Terapia GLUCOVANCE 400mg
Em um estudo clínico multicêntrico, duplo-cego, de 24 semanas nos EUA, pacientes com diabetes tipo 2 não adequadamente controlados com a terapia anti-hiperglicêmica oral atual (monoterapia ou terapia combinada) foram primeiramente trocados para comprimidos abertos de GLUCOVANCE 2,5 mg/500 mg e titulados até uma dose diária máxima de 10 mg/2000 mg. Um total de 365 pacientes inadequadamente controlados (HbA1c > 7,0% e ≤ 10%) após 10 a 12 semanas de uma dose diária de GLUCOVANCE 500 mg de pelo menos 7,5 mg/1500 mg foram randomizados para receber terapia adicional com rosiglitazona 4 mg ou placebo uma vez ao dia . Após 8 semanas, a dose de rosiglitazona foi aumentada para um máximo de 8 mg por dia, conforme necessário, para atingir uma meta de glicose diária média de 126 mg/dL ou HbA1c
Para os pacientes que não atingiram o controle glicêmico adequado com GLUCOVANCE 400mg, a adição de rosiglitazona, comparada ao placebo, resultou em redução significativa de HbA e FPG.
INFORMAÇÃO DO PACIENTE
GLUCOVANCE® (gliburida e metformina HCl) Comprimidos
AVISO: Um pequeno número de pessoas que tomaram cloridrato de metformina desenvolveu uma condição grave chamada acidose láctica. Os rins funcionando adequadamente são necessários para ajudar a prevenir a acidose láctica. A maioria das pessoas com problemas renais não deve tomar GLUCOVANCE. (Veja as questões nºs 9-13.)
Q1. Por que preciso tomar GLUCOVANCE 5mg?
O seu médico prescreveu GLUCOVANCE 500mg para tratar a sua diabetes tipo 2. Isso também é conhecido como diabetes mellitus não insulino-dependente.
Q2. O que é diabetes tipo 2?
Pessoas com diabetes não são capazes de produzir insulina suficiente e/ou respondem normalmente à insulina que seu corpo produz. Quando isso acontece, o açúcar (glicose) se acumula no sangue. Isso pode levar a sérios problemas médicos, incluindo danos nos rins, amputações e cegueira. A diabetes também está intimamente ligada a doenças cardíacas. O principal objetivo do tratamento do diabetes é reduzir o açúcar no sangue para um nível normal.
Q3. Por que é importante controlar o diabetes tipo 2?
O principal objetivo do tratamento do diabetes é reduzir o açúcar no sangue para um nível normal. Estudos mostraram que um bom controle do açúcar no sangue pode prevenir ou retardar complicações, como doenças cardíacas, doenças renais ou cegueira.
Q4. Como o diabetes tipo 2 geralmente é controlado?
O alto nível de açúcar no sangue pode ser reduzido por dieta e exercícios, vários medicamentos orais e injeções de insulina. Antes de tomar GLUCOVANCE 2,50mg deve primeiro tentar controlar a sua diabetes através de exercício e perda de peso. Mesmo se estiver tomando GLUCOVANCE, você ainda deve se exercitar e seguir a dieta recomendada para seu diabetes.
Q5. O GLUCOVANCE 400mg funciona de forma diferente de outros medicamentos de controle de glicose?
Sim. GLUCOVANCE 400mg combina 2 medicamentos para baixar a glicose, gliburida e metformina. Esses 2 medicamentos trabalham juntos para melhorar os diferentes defeitos metabólicos encontrados no diabetes tipo 2. A gliburida reduz o açúcar no sangue principalmente ao fazer com que mais insulina do próprio corpo seja liberada, e a metformina reduz o açúcar no sangue, em parte, ajudando seu corpo a usar sua própria insulina de forma mais eficaz. Juntos, eles são eficientes para ajudá-lo a obter um melhor controle da glicose.
Q6. O que acontece se meu açúcar no sangue ainda estiver muito alto?
Quando o açúcar no sangue não puder ser reduzido o suficiente com GLUCOVANCE, seu médico poderá prescrever insulina injetável ou tomar outras medidas para controlar seu diabetes.
Q7. GLUCOVANCE 400mg pode causar efeitos colaterais?
GLUCOVANCE 2,50mg, como todos os medicamentos para baixar o açúcar no sangue, pode causar efeitos colaterais em alguns pacientes. A maioria desses efeitos colaterais são menores. No entanto, também existem efeitos colaterais graves, mas raros, relacionados ao GLUCOVANCE (consulte Q9-Q13).
Q8. Quais são os efeitos colaterais mais comuns de GLUCOVANCE 500mg?
Os efeitos colaterais mais comuns de GLUCOVANCE 5mg são normalmente menores, como diarréia, náusea e dor de estômago. Se esses efeitos colaterais ocorrerem, eles geralmente ocorrem durante as primeiras semanas de terapia. Tomar GLUCOVANCE com as refeições pode ajudar a reduzir esses efeitos colaterais.
Com menos frequência, podem ocorrer sintomas de hipoglicemia (baixo nível de açúcar no sangue), como tontura, tontura, tremores ou fome. O risco de sintomas de hipoglicemia aumenta quando as refeições são omitidas, muito álcool é consumido ou exercícios pesados ocorrem sem comida suficiente. Seguir o conselho do seu médico pode ajudá-lo a evitar esses sintomas.
Q9. Existem efeitos colaterais graves que GLUCOVANCE pode causar?
As pessoas que têm uma condição conhecida como deficiência de glicose-6-fosfato desidrogenase (G6PD) e que tomam GLUCOVANCE podem desenvolver anemia hemolítica (quebra rápida dos glóbulos vermelhos). A deficiência de G6PD geralmente ocorre em famílias. Informe o seu médico se você ou algum membro da sua família foi diagnosticado com deficiência de G6PD antes de começar a tomar GLUCOVANCE.
GLUCOVANCE raramente causa efeitos colaterais graves. O efeito colateral mais grave que GLUCOVANCE 2,50mg pode causar é chamado de acidose láctica.
Q10. O que é acidos lácticos e pode acontecer comigo?
A acidose láctica é causada por um acúmulo de ácido lático no sangue. A acidose láctica associada à metformina é rara e ocorreu principalmente em pessoas cujos rins não estavam funcionando normalmente. A acidose láctica foi relatada em cerca de 1 em 33.000 pacientes tomando metformina ao longo de um ano. Embora rara, se ocorrer acidose lática, pode ser fatal em até metade dos casos.
Também é importante que seu fígado funcione normalmente quando você toma GLUCOVANCE. Seu fígado ajuda a remover o ácido lático da corrente sanguínea.
O seu médico irá monitorizar a sua diabetes e poderá realizar análises ao seu sangue de tempos a tempos para se certificar de que os seus rins e fígado estão a funcionar normalmente.
Não há evidências de que GLUCOVANCE cause danos aos rins ou ao fígado.
Q11. Existem outros fatores de risco para acidose láctica?
Seu risco de desenvolver acidose láctica ao tomar GLUCOVANCE 400mg é muito baixo, desde que seus rins e fígado estejam saudáveis. No entanto, alguns fatores podem aumentar seu risco porque podem afetar a função renal e hepática. Você deve discutir seu risco com seu médico.
Você não deve tomar GLUCOVANCE 400mg se:
- Você tem problemas renais ou hepáticos crônicos
- Você tem insuficiência cardíaca congestiva que é tratada com medicamentos, por exemplo, digoxina (Lanoxin®) ou furosemida (Lasix®)
- Você bebe álcool excessivamente (o tempo todo ou bebedeira de curto prazo)
- Você está seriamente desidratado (perdeu uma grande quantidade de fluidos corporais)
- Você vai ter certos procedimentos de raios-x com agentes de contraste injetáveis
- Você vai fazer uma cirurgia
- Você desenvolve uma condição grave, como ataque cardíaco, infecção grave ou acidente vascular cerebral
- Você tem ≥ 80 anos de idade e NÃO testou sua função renal
Q12. Quais são os sintomas da acidose láctica?
Alguns dos sintomas incluem: sentir-se muito fraco, cansado ou desconfortável; dor muscular incomum; Problemas respiratórios; desconforto estomacal incomum ou inesperado; sentindo frio; sentir-se tonto ou tonto; ou desenvolver subitamente um batimento cardíaco lento ou irregular.
Se notar estes sintomas, ou se a sua condição médica mudou subitamente, pare de tomar GLUCOVANCE comprimidos e contacte o seu médico imediatamente. A acidose láctica é uma emergência médica que deve ser tratada em um hospital.
Q13. O que meu médico precisa saber para diminuir meu risco de acidose láctica?
Informe o seu médico se tiver uma doença que resulte em vómitos graves, diarreia e/ou febre, ou se a ingestão de líquidos for significativamente reduzida. Estas situações podem levar a uma desidratação grave, e pode ser necessário parar de tomar GLUCOVANCE 400mg temporariamente.
Você deve informar o seu médico se for fazer alguma cirurgia ou procedimentos especializados de raios-x que exijam injeção de agentes de contraste. A terapia com GLUCOVANCE 2,50 mg precisará ser interrompida temporariamente nesses casos.
Q14. Posso tomar GLUCOVANCE 500mg com outros medicamentos?
Lembre o seu médico de que está a tomar GLUCOVANCE 2,50 mg quando for prescrito um novo medicamento ou quando for feita uma alteração na forma como toma um medicamento já prescrito. GLUCOVANCE 400mg pode interferir na forma como alguns medicamentos funcionam e alguns medicamentos podem interferir na ação de GLUCOVANCE.
Não tome GLUCOVANCE se estiver a tomar bosentano utilizado para hipertensão arterial pulmonar (HAP), que é a pressão arterial elevada nos vasos dos pulmões.
Q15. E se eu engravidar enquanto estiver tomando GLUCOVANCE 400mg?
Informe o seu médico se planeia engravidar ou ficou grávida. Assim como com outros medicamentos orais para controle da glicose, você não deve tomar GLUCOVANCE durante a gravidez.
Normalmente, o seu médico irá prescrever insulina enquanto estiver grávida. Como com todos os medicamentos, você e seu médico devem discutir o uso de GLUCOVANCE 5mg se estiver amamentando uma criança.
Q16. Como tomo GLUCOVANCE?
O seu médico irá dizer-lhe quantos comprimidos de GLUCOVANCE deve tomar e com que frequência. Isso também deve ser impresso no rótulo da sua receita. Você provavelmente começará com uma dose baixa de GLUCOVANCE 400mg e sua dosagem será aumentada gradualmente até que seu açúcar no sangue seja controlado.
Q17. Onde posso obter mais informações sobre GLUCOVANCE 400mg?
Este folheto é um resumo das informações mais importantes sobre GLUCOVANCE. Se você tiver dúvidas ou problemas, converse com seu médico ou outro profissional de saúde sobre diabetes tipo 2, GLUCOVANCE e seus efeitos colaterais. Há também um folheto (bula) escrito para profissionais de saúde que o seu farmacêutico pode deixar você ler.
