Effexor 37.5mg, 75mg Venlafaxine Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
INFORMAÇÃO DO PACIENTE
Effexor (venlafaxina) (ven-la-fax-een) Comprimidos, USP
Leia o Guia de Medicação que vem com os comprimidos de venlafaxina, USP antes de começar a tomá-lo e sempre que receber um reabastecimento. Pode haver novas informações. Este Guia de Medicação não substitui a conversa com seu médico sobre sua condição médica ou tratamento. Converse com seu médico se houver algo que você não entenda ou queira saber mais.
Qual é a informação mais importante que devo saber sobre Venlafaxina Comprimidos, USP?
Os comprimidos de venlafaxina, USP e outros medicamentos antidepressivos podem causar efeitos colaterais graves, incluindo:
1. Pensamentos ou ações suicidas:
- Os comprimidos de venlafaxina, USP e outros medicamentos antidepressivos podem aumentar os pensamentos ou ações suicidas em algumas crianças, adolescentes ou adultos jovens nos primeiros meses de tratamento ou quando a dose é alterada.
- Depressão ou outras doenças mentais graves são as causas mais importantes de pensamentos ou ações suicidas.
- Fique atento a essas mudanças e ligue para o seu médico imediatamente se notar:
- Mudanças novas ou repentinas no humor, comportamento, ações, pensamentos ou sentimentos, especialmente se forem graves.
- Preste atenção especial a essas alterações quando os comprimidos de venlafaxina, USP forem iniciados ou quando a dose for alterada.
Mantenha todas as visitas de acompanhamento com seu médico e ligue entre as visitas se estiver preocupado com os sintomas.
Ligue para o seu médico imediatamente se tiver algum dos seguintes sintomas ou ligue para o 911 em caso de emergência, especialmente se eles forem novos, piores ou se preocuparem:
- tentativas de suicídio
- agindo em impulsos perigosos
- agindo de forma agressiva ou violenta
- pensamentos sobre suicídio ou morte
- depressão nova ou pior
- ansiedade nova ou pior ou ataques de pânico
- sentindo-se agitado, inquieto, irritado ou irritado
- problemas para dormir
- um aumento na atividade ou falar mais do que o normal para você
- outras mudanças incomuns no comportamento ou humor
Ligue para o seu médico imediatamente se tiver algum dos seguintes sintomas ou ligue para o 911 em caso de emergência. Os comprimidos de venlafaxina, USP podem estar associados a estes efeitos colaterais graves:
2. Síndrome da serotonina
Esta condição pode ser fatal e pode incluir:
- agitação, alucinações, coma ou outras alterações no estado mental
- problemas de coordenação ou espasmos musculares (reflexos hiperativos)
- batimentos cardíacos acelerados, pressão arterial alta ou baixa
- sudorese ou febre
- náuseas, vômitos ou diarreia
- rigidez muscular
3. Alterações na pressão arterial. Os comprimidos de venlafaxina, USP podem:
- aumentar sua pressão arterial. Controle a pressão arterial elevada antes de iniciar o tratamento e monitore a pressão arterial regularmente
4. Pupilas aumentadas (midríase).
5. Ansiedade e insônia.
6. Alterações no apetite ou peso.
- crianças e adolescentes devem ter altura e peso monitorados durante o tratamento
7. Episódios maníacos/hipomaníacos:
- energia muito aumentada
- problemas graves para dormir
- pensamentos descontrolados
- comportamento imprudente
- ideias extraordinariamente grandes
- felicidade excessiva ou irritabilidade
- falando mais ou mais rápido do que o habitual
8. Baixos níveis de sal (sódio) no sangue.
Os idosos podem estar em maior risco para isso. Os sintomas podem incluir:
- dor de cabeça
- fraqueza ou sensação instável
- confusão, problemas de concentração ou pensamento ou problemas de memória
9. Convulsões ou convulsões.
10. Sangramento anormal: comprimidos de venlafaxina, USP e outros medicamentos antidepressivos podem aumentar o risco de sangramento ou hematomas, especialmente se você tomar o anticoagulante varfarina (Coumadin®, Jantoven®), um medicamento anti-inflamatório não esteróide (AINEs, como ibuprofeno ou naproxeno) ou aspirina.
11. Colesterol elevado.
12. Doença pulmonar e pneumonia: comprimidos de venlafaxina, USP podem causar problemas pulmonares raros. Os sintomas incluem:
- piora da falta de ar
- tosse
- desconforto no peito
13. Reações alérgicas graves:
- Problemas respiratórios
- inchaço da face, língua, olhos ou boca
- erupção cutânea, vergões com comichão (urticária) ou bolhas, sozinho ou com febre ou dor nas articulações
14. Problemas visuais:
- dor nos olhos
- mudanças na visão
- inchaço ou vermelhidão dentro ou ao redor do olho
Apenas algumas pessoas estão em risco para esses problemas. Você pode querer se submeter a um exame oftalmológico para ver se está em risco e receber tratamento preventivo, se estiver.
Não interrompa os comprimidos de Venlafaxina, USP sem primeiro falar com seu médico. Parar os comprimidos de venlafaxina, USP muito rapidamente ou mudar de outro antidepressivo muito rapidamente pode causar sintomas graves, incluindo:
- ansiedade, irritabilidade
- sentir-se cansado, inquieto ou problemas para dormir
- dor de cabeça, sudorese, tontura
- sensações de choque elétrico, tremores, confusão, pesadelos
- vómitos, náuseas, diarreia
O que é Venlafaxina Comprimidos, USP?
Comprimidos de venlafaxina, USP é um medicamento de prescrição usado para tratar a depressão. É importante conversar com seu médico sobre os riscos de tratar a depressão e também os riscos de não tratá-la. Você deve discutir todas as opções de tratamento com seu médico.
Converse com seu médico se achar que sua condição não está melhorando com comprimidos de venlafaxina, tratamento USP.
Quem não deve tomar comprimidos de venlafaxina, USP?
- Não tome comprimidos de venlafaxina, USP se você:
- são alérgicos a comprimidos de venlafaxina, USP ou a qualquer um dos ingredientes em comprimidos de venlafaxina, USP. Consulte o final deste Guia de Medicação para obter uma lista completa de ingredientes em comprimidos de venlafaxina, USP.
- tem glaucoma de ângulo estreito não controlado
- tomar um Inibidor da Monoamino Oxidase (IMAO). Pergunte ao seu médico ou farmacêutico se não tiver certeza se está tomando um IMAO, incluindo o antibiótico linezolida.
- Não tome um IMAO dentro de 7 dias após a interrupção dos comprimidos de venlafaxina, USP, a menos que seja orientado pelo seu médico.
- Não inicie comprimidos de venlafaxina, USP se você parou de tomar um IMAO nas últimas 2 semanas, a menos que seja orientado pelo seu médico.
As pessoas que tomam comprimidos de Venlafaxina, USP perto do tempo de um IMAO podem ter efeitos colaterais graves ou até mesmo fatais. Obtenha ajuda médica imediatamente se tiver algum destes sintomas:
- febre alta
- espasmos musculares descontrolados
- músculos fortes
- mudanças rápidas na frequência cardíaca ou pressão arterial
- confusão
- perda de consciência (desmaiar)
que devo dizer ao meu médico antes de tomar Venlafaxina Comprimidos, USP? Pergunte se não tiver certeza.
Antes de iniciar os comprimidos de venlafaxina, USP, informe o seu médico se você:
- Está tomando certos medicamentos, como:
- Medicamentos usados para tratar enxaquecas, tais como:
- triptanos
- Medicamentos usados para tratar distúrbios do humor, ansiedade, psicóticos ou do pensamento, tais como:
- antidepressivos tricíclicos
- lítio
- ISRS
- SNRIs
- drogas antipsicóticas
- Medicamentos usados para tratar a dor, tais como:
- tramadol
- Medicamentos usados para diluir o sangue, tais como:
- varfarina
- Medicamentos usados para tratar azia, tais como:
- Cimetidina
- Medicamentos de venda livre ou suplementos, tais como:
- Aspirina ou outros AINEs
- Triptofano
- Erva de São João
- tem problemas cardíacos
- tem diabetes
- tem problemas de fígado
- tem problemas renais
- tem problemas de tireóide
- tem glaucoma
- tem ou teve convulsões ou convulsões
- tem transtorno bipolar ou mania
- tem baixos níveis de sódio no sangue
- tem pressão alta
- tem colesterol alto
- tem ou teve problemas de sangramento
- estão grávidas ou planejam engravidar. Não se sabe se os comprimidos de venlafaxina, USP prejudicarão o feto. Converse com seu médico sobre os benefícios e riscos do tratamento da depressão durante a gravidez
- está amamentando ou planeja amamentar. Alguns comprimidos de venlafaxina, USP podem passar para o leite materno. Converse com seu médico sobre a melhor maneira de alimentar seu bebê enquanto estiver tomando comprimidos de venlafaxina, USP.
Informe o seu médico sobre todos os medicamentos que você toma, incluindo medicamentos prescritos e não prescritos, vitaminas e suplementos de ervas. Os comprimidos de venlafaxina, USP e alguns medicamentos podem interagir uns com os outros, podem não funcionar tão bem ou podem causar efeitos colaterais graves.
Seu médico ou farmacêutico pode dizer se é seguro tomar comprimidos de venlafaxina, USP com seus outros medicamentos. Não inicie ou interrompa qualquer medicamento enquanto estiver tomando comprimidos de venlafaxina, USP sem falar primeiro com seu médico.
Se você toma comprimidos de venlafaxina, USP, não deve tomar outros medicamentos que contenham (venlafaxina), incluindo: venlafaxina HCl.
Como devo tomar comprimidos de Venlafaxina, USP?
- Tome comprimidos de venlafaxina, USP exatamente como prescrito. Seu médico pode precisar alterar a dose dos comprimidos de venlafaxina, USP, até que seja a dose certa para você.
- Os comprimidos de venlafaxina, USP devem ser tomados com alimentos.
- Se você perder uma dose de comprimidos de venlafaxina, USP, tome a dose esquecida assim que se lembrar. Se estiver quase na hora da próxima dose, pule a dose esquecida e tome a próxima dose no horário regular. Não tome duas doses de comprimidos de venlafaxina, USP ao mesmo tempo.
- Se você tomar muitos comprimidos de venlafaxina, USP, ligue para seu médico ou centro de controle de veneno imediatamente ou obtenha tratamento de emergência.
- Ao mudar de outro antidepressivo para comprimidos de venlafaxina, USP, seu médico pode querer diminuir a dose do antidepressivo inicial primeiro para evitar efeitos colaterais
O que devo evitar ao tomar comprimidos de Venlafaxina, USP?
Os comprimidos de venlafaxina, USP podem causar sonolência ou afetar sua capacidade de tomar decisões, pensar com clareza ou reagir rapidamente.
Você não deve dirigir, operar máquinas pesadas ou fazer outras atividades perigosas até saber como os comprimidos de venlafaxina, USP o afetam. Não beba álcool enquanto estiver usando comprimidos de venlafaxina, USP.
Quais são os possíveis efeitos colaterais dos comprimidos de venlafaxina, USP?
Os comprimidos de venlafaxina, USP podem causar efeitos colaterais graves, incluindo:
- Consulte “Quais são as informações mais importantes que devo saber sobre os comprimidos de venlafaxina, USP?”
- Aumento do colesterol - verifique regularmente o seu colesterol
- Recém-nascidos cujas mães tomam comprimidos de venlafaxina, USP no terceiro trimestre podem ter problemas logo após o nascimento, incluindo:
- problemas de alimentação e respiração
- convulsões
- tremores, nervosismo ou choro constante
- Glaucoma de ângulo estreito/pupilas aumentadas.
Verifique a pressão ocular regularmente se você:
- tem um histórico de aumento da pressão ocular
- estão em risco de certos tipos de glaucoma
Os possíveis efeitos colaterais comuns em pessoas que tomam comprimidos de venlafaxina, USP incluem:
sonhos incomuns
- problemas sexuais
- perda de apetite, constipação, diarréia, náusea ou vômito ou boca seca
- sentindo-se cansado, fatigado ou excessivamente sonolento
- mudança nos hábitos de sono, problemas para dormir
- bocejando
- tremor ou tremor
- tonturas, visão turva
- sudorese
- sentindo-se ansioso, nervoso ou nervoso
- dor de cabeça
- aumento da frequência cardíaca
Informe o seu médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais dos comprimidos de venlafaxina, USP.
Para mais informações, pergunte ao seu médico ou farmacêutico.
LIGUE PARA O SEU MÉDICO PARA ACONSELHAMENTO MÉDICO SOBRE EFEITOS COLATERAIS. VOCÊ PODE DENUNCIAR EFEITOS COLATERAIS AO FDA EM 1-800-FDA-1088.
Como devo armazenar os comprimidos de Venlafaxina, USP?
- Armazenar a 20° a 25°C (68° a 77°F) excursões permitidas 15° a 30°C (59° a 86°F) [Consulte Temperatura ambiente controlada USP ].
- Mantenha os comprimidos de velafaxina, USP em local seco.
Mantenha os comprimidos de venlafaxina, USP e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre comprimidos de venlafaxina, USP Medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use comprimidos de venlafaxina, USP para uma condição para a qual não foi prescrito. Não dê comprimidos de venlafaxina, USP a outras pessoas, mesmo que tenham a mesma condição. Pode prejudicá-los.
Este Guia de Medicação resume as informações mais importantes sobre comprimidos de venlafaxina, USP. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre comprimidos de venlafaxina, USP que foi escrito para profissionais de saúde.
Para relatar REAÇÕES ADVERSAS SUSPEITAS, entre em contato com a Sun Pharmaceutical Industries, Inc. pelo telefone 1-800-818-4555.
Quais são os ingredientes dos comprimidos de venlafaxina, USP?
Princípio ativo: (venlafaxina)
Ingredientes inativos:
- Comprimidos: celulose microcristalina, lactose monohidratada, amido pré-gelatinizado, glicolato de amido sódico, óxido de ferro vermelho, óxido de ferro amarelo, dióxido de silício coloidal e estearato de magnésio
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA para todos os antidepressivos.
INDICAÇÕES
Transtorno Depressivo Maior
As cápsulas de liberação prolongada de Effexor XR (cloridrato de venlafaxina) são indicadas para o tratamento do transtorno depressivo maior (TDM). A eficácia foi estabelecida em três ensaios de manutenção de curto prazo (4, 8 e 12 semanas) e dois de longo prazo.
Distúrbio de ansiedade generalizada
Effexor XR é indicado para o tratamento do Transtorno de Ansiedade Generalizada (TAG). A eficácia foi estabelecida em dois ensaios controlados por placebo de 8 semanas e dois de 26 semanas.
Transtorno de ansiedade social
Effexor XR é indicado para o tratamento do Transtorno de Ansiedade Social (TAS), também conhecido como fobia social. A eficácia foi estabelecida em quatro ensaios de 12 semanas e um de 26 semanas, controlados por placebo.
Síndrome do pânico
Effexor XR é indicado para o tratamento do Transtorno do Pânico (TP), com ou sem agorafobia. A eficácia foi estabelecida em dois estudos controlados por placebo de 12 semanas.
DOSAGEM E ADMINISTRAÇÃO
Effexor 37,5mg XR deve ser administrado em dose única com alimentos, pela manhã ou à noite, aproximadamente no mesmo horário todos os dias [ver FARMACOLOGIA CLÍNICA ]. Cada cápsula deve ser engolida inteira com líquido e não dividida, esmagada, mastigada ou colocada em água ou pode ser administrada abrindo cuidadosamente a cápsula e polvilhando todo o conteúdo em uma colher de molho de maçã. Esta mistura de medicamento/alimento deve ser engolida imediatamente sem mastigar e seguida de um copo de água para garantir a deglutição completa dos pellets (esferóides).
Transtorno Depressivo Maior
Para a maioria dos pacientes, a dose inicial recomendada para Effexor 37,5 mg XR é de 75 mg por dia, administrada em dose única. Para alguns pacientes, pode ser desejável iniciar com 37,5 mg por dia por 4 a 7 dias para permitir que novos pacientes se ajustem à medicação antes de aumentar para 75 mg por dia. Os pacientes que não respondem à dose inicial de 75 mg por dia podem se beneficiar de aumentos de dose até um máximo de 225 mg por dia. Os aumentos de dose devem ser em incrementos de até 75 mg por dia, conforme necessário, e devem ser feitos em intervalos não inferiores a 4 dias, uma vez que os níveis plasmáticos de venlafaxina no estado de equilíbrio e seus principais metabólitos são alcançados na maioria dos pacientes no dia 4 [Vejo FARMACOLOGIA CLÍNICA ]. Nos estudos clínicos que estabeleceram a eficácia, a titulação ascendente foi permitida em intervalos de 2 semanas ou mais.
Deve-se notar que, embora a dose máxima recomendada para pacientes ambulatoriais moderadamente deprimidos também seja de 225 mg por dia para Effexor (liberação imediata), pacientes internados com depressão mais grave em um estudo do programa de desenvolvimento desse produto responderam a uma dose média de 350 mg por dia (intervalo de 150 a 375 mg por dia). Não se sabe se doses mais altas de Effexor 37,5mg XR são necessárias para pacientes com depressão mais grave; no entanto, a experiência com doses de Effexor 75mg XR superiores a 225 mg por dia é muito limitada.
Distúrbio de ansiedade generalizada
Para a maioria dos pacientes, a dose inicial recomendada de Effexor XR é de 75 mg por dia, administrada em dose única. Para alguns pacientes, pode ser desejável iniciar com 37,5 mg por dia por 4 a 7 dias para permitir que novos pacientes se ajustem à medicação antes de aumentar para 75 mg por dia. Os pacientes que não respondem à dose inicial de 75 mg por dia podem se beneficiar de aumentos de dose até um máximo de 225 mg por dia. Os aumentos de dose devem ser em incrementos de até 75 mg por dia, conforme necessário, e devem ser feitos em intervalos não inferiores a 4 dias, uma vez que os níveis plasmáticos de venlafaxina no estado de equilíbrio e seus principais metabólitos são alcançados na maioria dos pacientes no dia 4 [Vejo FARMACOLOGIA CLÍNICA ].
Transtorno de Ansiedade Social (Fobia Social)
A dose recomendada é de 75 mg por dia, administrada em dose única. Não houve evidência de que doses mais altas conferem qualquer benefício adicional.
Síndrome do pânico
dose inicial recomendada é de 37,5 mg por dia de Effexor 75 mg XR por 7 dias. Os pacientes que não respondem a 75 mg por dia podem se beneficiar de aumentos de dose até um máximo de aproximadamente 225 mg por dia. Os aumentos de dose devem ser em incrementos de até 75 mg por dia, conforme necessário, e devem ser feitos em intervalos não inferiores a 7 dias.
Trocando pacientes de comprimidos de Effexor 37,5mg
Pacientes deprimidos que estão atualmente sendo tratados com uma dose terapêutica com Effexor (liberação imediata) podem ser trocados para Effexor 37,5 mg XR na dose equivalente mais próxima (mg por dia), por exemplo, 37,5 mg de venlafaxina duas vezes ao dia para 75 mg Effexor 75 mg XR uma vez por dia. No entanto, ajustes de dose individuais podem ser necessários.
Populações Específicas
Pacientes com Insuficiência Hepática
A dose diária total deve ser reduzida em 50% em pacientes com insuficiência hepática leve (Child-Pugh=5-6) a moderada (Child-Pugh=7-9). Em pacientes com insuficiência hepática grave (Child-Pugh=10-15) ou cirrose hepática, pode ser necessário reduzir a dose em 50% ou mais [ver Uso em populações específicas ].
Pacientes com Insuficiência Renal
dose diária total deve ser reduzida em 25% a 50% em pacientes com insuficiência renal leve (CLcr= 60-89 mL/min) ou moderada (CLcr= 30-59 mL/min). Em pacientes em hemodiálise ou com insuficiência renal grave (CLcr Uso em populações específicas ].
Tratamento de manutenção
Não há evidências disponíveis de estudos controlados para indicar por quanto tempo pacientes com MDD, GAD, SAD ou PD devem ser tratados com Effexor 75mg XR.
É geralmente aceito que episódios agudos de TDM requerem vários meses ou mais de terapia farmacológica sustentada além da resposta ao episódio agudo. Effexor XR/Effexor demonstraram a continuação da resposta em estudos clínicos até 52 semanas, na mesma dose em que os pacientes responderam durante o tratamento inicial [ver Estudos clínicos ]. Não se sabe se a dose de Effexor XR necessária para o tratamento de manutenção é idêntica à dose necessária para obter uma resposta inicial. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção e a dose apropriada para tal tratamento.
Em pacientes com TAG e TAS, Effexor 37,5mg XR demonstrou ser eficaz em estudos clínicos de 6 meses. A necessidade de continuar a medicação em pacientes com TAG e TAS que melhoram com o tratamento com Effexor XR deve ser reavaliada periodicamente.
Em um estudo clínico para DP, os pacientes que continuaram com Effexor 75mg XR na mesma dose em que responderam durante as 12 semanas iniciais de tratamento tiveram um tempo de recaída estatisticamente significativamente maior do que os pacientes randomizados para placebo [ver Estudos clínicos ]. A necessidade de continuar a medicação em pacientes com DP que melhoram com o tratamento com Effexor XR deve ser reavaliada periodicamente.
Descontinuando Effexor XR
Recomenda-se uma redução gradual da dose, em vez de interrupção abrupta, ao descontinuar a terapia com Effexor 37,5mg XR. Em estudos clínicos com Effexor 37,5 mg XR, a redução gradual foi alcançada pela redução da dose diária em 75 mg em intervalos de uma semana. A individualização do afunilamento pode ser necessária [ver AVISOS E PRECAUÇÕES ]. Em alguns pacientes, a descontinuação pode ocorrer por um período de vários meses.
Troca de pacientes para ou de um inibidor da monoaminoxidase (IMAO) destinado a tratar distúrbios psiquiátricos
Devem decorrer pelo menos 14 dias entre a descontinuação de um IMAO (destinado a tratar distúrbios psiquiátricos) e o início da terapia com Effexor XR. Além disso, pelo menos 7 dias devem ser permitidos após a interrupção do Effexor XR antes de iniciar um IMAO destinado a tratar distúrbios psiquiátricos [ver CONTRA-INDICAÇÕES , AVISOS E PRECAUÇÕES , e INTERAÇÕES MEDICAMENTOSAS ].
Uso de Effexor XR com outros IMAOs, como Linezolida ou Azul de Metileno Intravenoso
Não inicie Effexor 75mg XR em um paciente que esteja sendo tratado com linezolida ou azul de metileno intravenoso, pois há um risco aumentado de síndrome serotoninérgica. Em um paciente que requer tratamento mais urgente de uma condição psiquiátrica, outras intervenções, incluindo hospitalização, devem ser consideradas [ver CONTRA-INDICAÇÕES ].
Em alguns casos, um paciente que já esteja recebendo terapia com Effexor 37,5mg XR pode necessitar de tratamento urgente com linezolida ou azul de metileno intravenoso. Se alternativas aceitáveis para linezolida ou azul de metileno intravenoso não estiverem disponíveis e os benefícios potenciais do tratamento com linezolida ou azul de metileno intravenoso forem considerados superiores aos riscos de síndrome serotoninérgica em um paciente em particular, Effexor XR deve ser interrompido imediatamente e linezolida ou azul de metileno intravenoso pode ser administrado. Monitorar o paciente quanto a sintomas de síndrome serotoninérgica por 7 dias ou até 24 horas após a última dose de linezolida ou azul de metileno intravenoso, o que ocorrer primeiro. A terapia com Effexor 75mg XR pode ser retomada 24 horas após a última dose de linezolida ou azul de metileno intravenoso [ver AVISOS E PRECAUÇÕES ].
risco de administrar azul de metileno por vias não intravenosas (como comprimidos orais ou por injeção local) ou em doses intravenosas muito inferiores a 1 mg/kg concomitantemente com Effexor XR não é claro. O clínico deve, no entanto, estar ciente da possibilidade de sintomas emergentes da síndrome serotoninérgica com tal uso [ver AVISOS E PRECAUÇÕES ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
As cápsulas de liberação prolongada Effexor 37,5mg XR® (cloridrato de venlafaxina) estão disponíveis nas seguintes dosagens:
- Cápsulas de 37,5 mg (tampa cinza/corpo pêssego com “W” e “Effexor 75mg XR” na tampa e “37,5” no corpo)
- Cápsulas de 75 mg (tampa e corpo pêssego com “W” e “Effexor 37,5mg XR” na tampa e “75” no corpo)
- Cápsulas de 150 mg (tampa laranja escuro e corpo com “W” e “Effexor 75mg XR” na tampa e “150” no corpo)
Armazenamento e manuseio
Effexor XR® (cloridrato de venlafaxina) cápsulas de liberação prolongada estão disponíveis da seguinte forma:
NDC 0008-0837-20, frasco de 15 cápsulas em embalagem unitária. NDC 0008-0837-21, frasco de 30 cápsulas em embalagem unitária. NDC 0008-0837-22, frasco de 90 cápsulas em embalagem unitária. NDC 0008-0837-03, embalagem de 10 blisters Redipak® de 10 cápsulas cada.
NDC 0008-0833-20, frasco de 15 cápsulas em embalagem unitária. NDC 0008-0833-21, frasco de 30 cápsulas em embalagem unitária. NDC 0008-0833-22, frasco de 90 cápsulas em embalagem unitária. NDC 0008-0833-03, embalagem de 10 blisters Redipak® de 10 cápsulas cada.
NDC 0008-0836-20, frasco de 15 cápsulas em embalagem unitária. NDC 0008-0836-21, frasco de 30 cápsulas em embalagem unitária. NDC 0008-0836-22, frasco de 90 cápsulas em embalagem unitária. NDC 0008-0836-03, embalagem de 10 blisters Redipak® de 10 cápsulas cada.
- 37,5 mg , tampa cinza/corpo pêssego com “W” e “Effexor XR” na tampa e “37.5” no corpo.
- 75 mg , tampa e corpo pêssego com “W” e “Effexor 37,5mg XR” na tampa e “75” no corpo.
- 150 mg tampa e corpo laranja escuro com “W” e “Effexor XR” na tampa e “150” no corpo.
Armazenar em temperatura ambiente controlada, 20° a 25°C (68° a 77°F).
A embalagem de unidade de uso destina-se a ser dispensada como uma unidade.
Distribuído por: Wyeth Pharmaceuticals LLC, uma subsidiária da Pfizer Inc, Philadelpia, PA 19101. Revisado: novembro de 2021
EFEITOS COLATERAIS
As seguintes reações adversas são discutidas em mais detalhes em outras seções do rótulo:
- Hipersensibilidade [ver CONTRA-INDICAÇÕES ]
- Pensamentos e Comportamentos Suicidas em Crianças, Adolescentes e Adultos [ver AVISOS E PRECAUÇÕES ]
- Síndrome serotoninérgica [ver AVISOS E PRECAUÇÕES ]
- Elevações na Pressão Arterial [ver AVISOS E PRECAUÇÕES ]
- Sangramento Anormal [ver AVISOS E PRECAUÇÕES ]
- Glaucoma de ângulo fechado [ver AVISOS E PRECAUÇÕES ]
- Ativação de Mania/Hipomania [ver AVISOS E PRECAUÇÕES ]
- Síndrome de descontinuação [ver AVISOS E PRECAUÇÕES ]
- Convulsão [ver AVISOS E PRECAUÇÕES ]
- Hiponatremia [ver AVISOS E PRECAUÇÕES ]
- Alterações de peso e altura em pacientes pediátricos [ver AVISOS E PRECAUÇÕES ]
- Alterações do Apetite em Pacientes Pediátricos [ver AVISOS E PRECAUÇÕES ]
- Doença Pulmonar Intersticial e Pneumonia Eosinofílica [ver AVISOS E PRECAUÇÕES ]
- Disfunção Sexual [ver AVISOS E PRECAUÇÕES ]
Experiência em Estudos Clínicos
Como os estudos clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos estudos clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos estudos clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
Reações Adversas Mais Comuns
As reações adversas mais comumente observadas no banco de dados de estudos clínicos em pacientes tratados com Effexor XR em MDD, GAD, SAD e DP (incidência ≥ 5% e pelo menos o dobro da taxa de placebo) foram: náusea (30,0%), sonolência (15,3 %), boca seca (14,8%), sudorese (11,4%), ejaculação anormal (9,9%), anorexia (9,8%), constipação (9,3%), impotência (5,3%) e diminuição da libido (5,1%).
Reações adversas relatadas como razões para descontinuação do tratamento
Combinado em estudos de pré-comercialização de curto prazo controlados por placebo para todas as indicações, 12% dos 3.558 pacientes que receberam Effexor XR (37,5-225 mg) descontinuaram o tratamento devido a uma experiência adversa, em comparação com 4% dos 2.197 pacientes tratados com placebo nesses estudos.As reações adversas mais comuns que levaram à descontinuação em ≥ 1% dos pacientes tratados com Effexor XR nos estudos de curto prazo (até 12 semanas) em todas as indicações são mostradas na Tabela 7.
Reações Adversas Comuns em Estudos Controlados por Placebo
número de pacientes que receberam múltiplas doses de Effexor XR durante a avaliação pré-comercialização para cada indicação aprovada é mostrado na Tabela 8. As condições e a duração da exposição à venlafaxina em todos os programas de desenvolvimento variaram muito e incluíram (em categorias sobrepostas) aberto e duplo estudos cegos, estudos não controlados e controlados, estudos de pacientes internados (somente Effexor) e estudos ambulatoriais, estudos de dose fixa e estudos de titulação.
As incidências de reações adversas comuns (aquelas que ocorreram em ≥ 2% dos pacientes tratados com Effexor XR [357 pacientes com MDD, 1.381 pacientes com TAG, 819 pacientes com TAS e 1.001 pacientes com DP] e mais frequentemente do que com placebo) em pacientes tratados com Effexor XR em resumo estudos clínicos de dose fixa e flexível, controlados por placebo, a termo (doses de 37,5 a 225 mg por dia) são mostrados na Tabela 9.
O perfil de reações adversas não diferiu substancialmente entre as diferentes populações de pacientes.
Outras reações adversas observadas em estudos clínicos
Corpo como um todo: Reação de fotossensibilidade, calafrios
Sistema cardiovascular: Hipotensão postural, síncope, hipotensão, taquicardia
Sistema digestivo: Hemorragia gastrointestinal [ver AVISOS E PRECAUÇÕES ],
bruxismo Sistema hemico/linfático: Equimose [ver AVISOS E PRECAUÇÕES ]
Metabólico/Nutricional: Hipercolesterolemia, ganho de peso [ver AVISOS E PRECAUÇÕES ], perda de peso [ver AVISOS E PRECAUÇÕES ]
Sistema nervoso: Convulsões [ver AVISOS E PRECAUÇÕES ], reação maníaca [ver AVISOS E PRECAUÇÕES ], agitação, confusão, acatisia, alucinações, hipertonia, mioclonia, despersonalização, apatia
Pele e anexos: Urticária, prurido, erupção cutânea, alopecia
Sentidos especiais: Midríase, anormalidade de acomodação, zumbido, alteração do paladar
Sistema urogenital: Retenção urinária, dificuldade para urinar, incontinência urinária, aumento da frequência urinária, distúrbios menstruais associados ao aumento do sangramento ou aumento do sangramento irregular (por exemplo, menorragia, metrorragia)
Mudanças nos sinais vitais
Em estudos de pré-comercialização controlados por placebo, houve aumentos na pressão arterial média (ver Tabela 10). Na maioria das indicações, um aumento relacionado à dose na pressão arterial sistólica e diastólica média em supino foi evidente em pacientes tratados com Effexor 37,5mg XRs. Em todos os estudos clínicos em MDD, GAD, SAD e PD, 1,4% dos pacientes nos grupos Effexor XR experimentaram um aumento no SDBP de ≥15 mm Hg juntamente com uma pressão arterial ≥ 105 mm Hg, em comparação com 0,9% dos pacientes no grupo grupos placebo. Da mesma forma, 1% dos pacientes nos grupos Effexor 37,5mg XR experimentaram um aumento na SSBP de ≥ 20 mm Hg com pressão arterial ≥ 180 mm Hg, em comparação com 0,3% dos pacientes nos grupos placebo.
tratamento com Effexor 37,5mg XR foi associado à hipertensão sustentada (definida como pressão arterial diastólica em decúbito dorsal [SDBP] ≥ 90 mmHg e ≥ 10 mmHg acima da linha de base para três consultas consecutivas de terapia (consulte a Tabela 11). Um número insuficiente dos pacientes receberam doses médias de Effexor XR acima de 300 mg por dia em estudos clínicos para avaliar completamente a incidência de aumentos sustentados da pressão arterial nessas doses mais altas.
Effexor 37,5mg XR foi associado a aumentos médios na frequência de pulso em comparação com placebo em estudos pré-comercialização controlados por placebo (ver Tabela 12) [ver AVISOS E PRECAUÇÕES ].
Alterações laboratoriais
Colesterol sérico
Effexor XR foi associado a aumentos finais médios nas concentrações séricas de colesterol em comparação com diminuições finais médias para placebo em estudos clínicos pré-comercialização de MDD, GAD, SAD e PD (Tabela 13).
tratamento com Effexor 75mg XR (cloridrato de venlafaxina) cápsulas de liberação prolongada por até 12 semanas em estudos pré-comercialização controlados por placebo para transtorno depressivo maior foi associado a um aumento médio final durante a terapia na concentração de colesterol sérico de aproximadamente 1,5 mg/dL em comparação com um redução final média de 7,4 mg/dL para placebo. O tratamento com Effexor XR por até 8 semanas e até 6 meses em estudos de GAD pré-comercialização controlados por placebo foi associado a aumentos médios finais na terapia na concentração de colesterol sérico de aproximadamente 1,0 mg/dL e 2,3 mg/dL, respectivamente, enquanto os indivíduos com placebo experimentaram decréscimos finais médios de 4,9 mg/dL e 7,7 mg/dL, respectivamente. O tratamento com Effexor XR por até 12 semanas e até 6 meses em estudos pré-comercialização de Transtorno de Ansiedade Social controlados por placebo foi associado a aumentos médios finais da terapia na concentração de colesterol sérico de aproximadamente 7,9 mg/dL e 5,6 mg/dL, respectivamente, em comparação com reduções finais médias de 2,9 e 4,2 mg/dL, respectivamente, para placebo. O tratamento com Effexor XR por até 12 semanas em estudos pré-comercialização de transtorno do pânico controlados por placebo foi associado a aumentos médios finais na terapia na concentração de colesterol sérico de aproximadamente 5,8 mg/dL em comparação com uma diminuição final média de 3,7 mg/dL para placebo.
Os pacientes tratados com Effexor (liberação imediata) por pelo menos 3 meses em estudos de extensão de 12 meses controlados por placebo tiveram um aumento médio final na terapia no colesterol total de 9,1 mg/dL em comparação com uma diminuição de 7,1 mg/dL entre placebo- pacientes tratados. Este aumento foi dependente da duração ao longo do período de estudo e tendeu a ser maior com doses mais altas. Aumentos clinicamente relevantes no colesterol sérico, definidos como 1) um aumento final durante a terapia no colesterol sérico ≥50 mg/dL desde a linha de base e para um valor ≥261 mg/dL, ou 2) um aumento médio durante a terapia no colesterol sérico ≥ 50 mg/dL da linha de base e para um valor ≥261 mg/dL, foram registrados em 5,3% dos pacientes tratados com venlafaxina e 0,0% dos pacientes tratados com placebo.
Triglicerídeos séricos
Effexor 75mg XR foi associado a aumentos médios finais da terapia nos triglicerídeos séricos em jejum em comparação com placebo em estudos clínicos pré-comercialização de SAD e PD até 12 semanas (dados agrupados) e 6 meses de duração (Tabela 14).
Pacientes pediátricos
Em geral, o perfil de reações adversas da venlafaxina (em estudos clínicos controlados por placebo) em crianças e adolescentes (6 a 17 anos) foi semelhante ao observado em adultos. Assim como em adultos, observou-se diminuição do apetite, perda de peso, aumento da pressão arterial e aumento do colesterol sérico [ver AVISOS E PRECAUÇÕES e Uso em populações específicas ].
Em estudos clínicos pediátricos, foi observada a reação adversa, ideação suicida.
Particularmente, as seguintes reações adversas foram observadas em pacientes pediátricos: dor abdominal, agitação, dispepsia, equimose, epistaxe e mialgia.
Reações Adversas Identificadas Durante o Uso Pós-aprovação
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de Effexor XR. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento:
Corpo como um todo: Anafilaxia, angioedema
Sistema cardiovascular: Prolongamento do intervalo QT, fibrilação ventricular, taquicardia ventricular (incluindo torsade de pointes), cardiomiopatia de takotsubo
Sistema digestivo: Pancreatite
Sistema hemico/linfático: Sangramento da membrana mucosa [ver AVISOS E PRECAUÇÕES ], discrasias sanguíneas (incluindo agranulocitose, anemia aplástica, neutropenia e pancitopenia), tempo de sangramento prolongado, trombocitopenia
Metabólico/Nutricional: Hiponatremia [ver AVISOS E PRECAUÇÕES ], Síndrome de secreção inadequada do hormônio antidiurético (SIADH) [ver AVISOS E PRECAUÇÕES ], testes de função hepática anormais, hepatite, aumento da prolactina
Musculoesquelético: Rabdomiólise
Sistema nervoso: Síndrome Neuroléptica Maligna (SNM) [ver AVISOS E PRECAUÇÕES ], síndrome serotoninérgica [ver AVISOS E PRECAUÇÕES ], delírio, reações extrapiramidais (incluindo distonia e discinesia), coordenação e equilíbrio prejudicados, discinesia tardia
Sistema respiratório: Dispneia, doença pulmonar intersticial, eosinofilia pulmonar [ver AVISOS E PRECAUÇÕES ]
Pele e anexos: Síndrome de Stevens-Johnson, necrólise epidérmica tóxica, eritema multiforme
Sentidos especiais: Glaucoma de ângulo fechado [ver AVISOS E PRECAUÇÕES ]
INTERAÇÕES MEDICAMENTOSAS
Drogas Ativas no Sistema Nervoso Central (SNC)
risco do uso de venlafaxina em combinação com outras drogas ativas no SNC não foi sistematicamente avaliado. Consequentemente, recomenda-se cautela quando Effexor XR é tomado em combinação com outros medicamentos ativos no SNC.
Inibidores da Monoamina Oxidase
Reações adversas, algumas das quais graves, foram relatadas em pacientes que descontinuaram recentemente um IMAO e iniciaram antidepressivos com propriedades farmacológicas semelhantes ao Effexor XR (SNRIs ou SSRIs), ou que tiveram recentemente a terapia SNRI ou SSRI descontinuada anteriormente. ao início de um IMAO [ver DOSAGEM E ADMINISTRAÇÃO , CONTRA-INDICAÇÕES e AVISOS E PRECAUÇÕES ].
Drogas serotoninérgicas
Com base no mecanismo de ação de Effexor XR e no potencial para síndrome serotoninérgica, recomenda-se cautela quando Effexor XR é coadministrado com outros medicamentos que podem afetar os sistemas de neurotransmissores serotoninérgicos, como triptanos, ISRSs, outros SNRIs, linezolida (um antibiótico que é um IMAO reversível não seletivo), lítio, tramadol ou erva de São João. Se o tratamento concomitante com Effexor XR e esses medicamentos for clinicamente justificado, recomenda-se a observação cuidadosa do paciente, particularmente durante o início do tratamento e aumentos de dose. O uso concomitante de Effexor 75mg XR com suplementos de triptofano não é recomendado [ver DOSAGEM E ADMINISTRAÇÃO , CONTRA-INDICAÇÕES , e AVISOS E PRECAUÇÕES ].
Medicamentos que interferem na hemostasia (por exemplo, AINEs, aspirina e varfarina)
A liberação de serotonina pelas plaquetas desempenha um papel importante na hemostasia. O uso de drogas psicotrópicas que interferem na recaptação de serotonina está associado à ocorrência de hemorragia digestiva alta e o uso concomitante de um AINE ou aspirina pode potencializar esse risco de sangramento. AVISOS E PRECAUÇÕES ]. Efeitos anticoagulantes alterados, incluindo aumento do sangramento, foram relatados quando SSRIs e SNRIs são coadministrados com varfarina. Pacientes recebendo terapia com varfarina devem ser cuidadosamente monitorados quando Effexor 37,5mg XR for iniciado ou descontinuado.
Agentes de perda de peso
A segurança e eficácia da terapia com venlafaxina em combinação com agentes para perda de peso, incluindo fentermina, não foram estabelecidas. A coadministração de Effexor XR e agentes de perda de peso não é recomendada. Effexor XR não é indicado para perda de peso sozinho ou em combinação com outros produtos.
Efeitos de outras drogas no Effexor XR
Figura 1: Efeito das drogas que interagem na farmacocinética da venlafaxina e do metabólito ativo O-desmetilvenlafaxina (ODV).
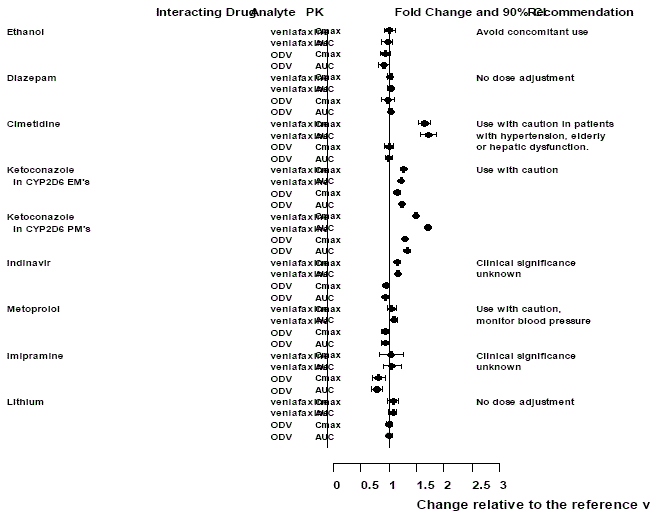
Efeitos do Effexor XR em outras drogas
Figura 2: Efeito da venlafaxina sobre os fármacos que interagem com a farmacocinética e seus metabólitos ativos.
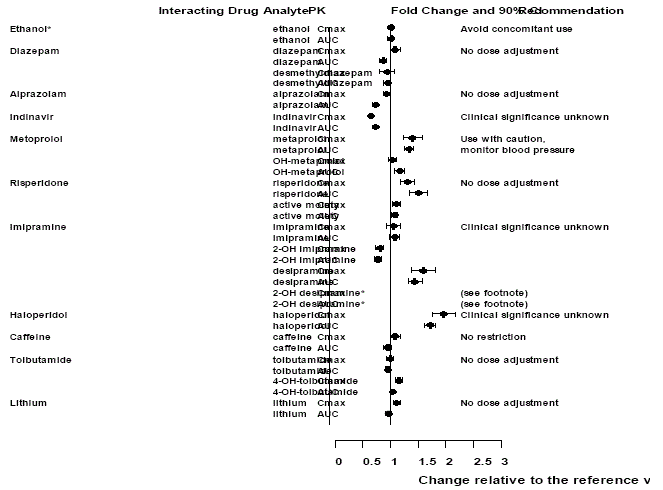
Observação
A administração de venlafaxina em regime estável não exagerou os efeitos psicomotores e psicométricos induzidos pelo etanol nesses mesmos indivíduos quando não estavam recebendo venlafaxina.
Interações de testes de laboratório de drogas
Testes de triagem de imunoensaio de urina falso-positivos para fenciclidina (PCP) e anfetamina foram relatados em pacientes tomando venlafaxina. Isso se deve à falta de especificidade dos testes de triagem. Podem ser esperados resultados falsos positivos nos testes por vários dias após a descontinuação da terapia com venlafaxina. Testes confirmatórios, como cromatografia gasosa/espectrometria de massa, distinguirão a venlafaxina de PCP e anfetamina.
Abuso e Dependência de Drogas
Substância controlada
Effexor 75mg XR não é uma substância controlada.
Abuso
Embora a venlafaxina não tenha sido sistematicamente estudada em estudos clínicos quanto ao seu potencial de abuso, não houve indicação de comportamento de busca de drogas nos estudos clínicos. No entanto, não é possível prever com base na experiência pré-comercialização até que ponto um medicamento ativo no SNC será mal utilizado, desviado e/ou abusado uma vez comercializado. Consequentemente, os médicos devem avaliar cuidadosamente os pacientes quanto ao histórico de abuso de drogas e acompanhá-los de perto, observando-os quanto a sinais de uso indevido ou abuso de venlafaxina (por exemplo, desenvolvimento de tolerância, aumento da dose, comportamento de busca de drogas).
Dependência
Estudos in vitro revelaram que a venlafaxina praticamente não tem afinidade para os receptores de opiáceos, benzodiazepínicos, fenciclidina (PCP) ou ácido N-metil-D-aspártico (NMDA).
A venlafaxina não apresentou atividade estimulante significativa do SNC em roedores. Em estudos de discriminação de drogas em primatas, a venlafaxina não mostrou nenhum risco significativo de abuso de estimulantes ou depressores.
Efeitos de descontinuação foram relatados em pacientes recebendo venlafaxina [ver DOSAGEM E ADMINISTRAÇÃO ].
AVISOS
Incluído como parte do "PRECAUÇÕES" Seção
PRECAUÇÕES
Pensamentos e Comportamentos Suicidas em Crianças, Adolescentes e Jovens Adultos
Pacientes com transtorno depressivo maior (TDM), adultos e pediátricos, podem apresentar piora de sua depressão e/ou surgimento de ideação e comportamento suicida (suicidalidade) ou mudanças incomuns de comportamento, estejam ou não tomando medicamentos antidepressivos, e isso risco pode persistir até que ocorra remissão significativa. O suicídio é um risco conhecido de depressão e alguns outros distúrbios psiquiátricos, e esses distúrbios são os mais fortes preditores de suicídio. Há uma preocupação de longa data, no entanto, de que os antidepressivos possam ter um papel na indução do agravamento da depressão e do surgimento de tendências suicidas em certos pacientes durante as fases iniciais do tratamento. Análises combinadas de estudos de curto prazo controlados por placebo de medicamentos antidepressivos (ISRSs e outros) mostraram que esses medicamentos aumentam o risco de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens (idades de 18 a 24 anos) com TDM e outros transtornos psiquiátricos. Estudos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução com antidepressivos em comparação com placebo em adultos com 65 anos ou mais.
As análises agrupadas de estudos controlados por placebo em crianças e adolescentes com TDM, Transtorno Obsessivo Compulsivo (TOC) ou outros transtornos psiquiátricos incluíram um total de 24 estudos de curto prazo de 9 medicamentos antidepressivos em mais de 4.400 pacientes. As análises agrupadas de estudos controlados por placebo em adultos com TDM ou outros transtornos psiquiátricos incluíram um total de 295 estudos de curto prazo (duração média de 2 meses) de 11 medicamentos antidepressivos em mais de 77.000 pacientes. Houve variação considerável no risco de suicídio entre as drogas, mas uma tendência de aumento nos pacientes mais jovens para quase todas as drogas estudadas. Houve diferenças no risco absoluto de suicídio entre as diferentes indicações, com maior incidência no TDM. As diferenças de risco (droga versus placebo), no entanto, foram relativamente estáveis dentro dos estratos de idade e entre as indicações. Essas diferenças de risco (diferença droga-placebo no número de casos de suicídio por 1.000 pacientes tratados) são fornecidas na Tabela 1.
Nenhum suicídio ocorreu em nenhum dos estudos pediátricos. Houve suicídios nos estudos com adultos, mas o número não foi suficiente para chegar a qualquer conclusão sobre o efeito da droga no suicídio.
Não se sabe se o risco de suicídio se estende ao uso de longo prazo, ou seja, além de vários meses. No entanto, há evidências substanciais de estudos de manutenção controlados por placebo em adultos com depressão de que o uso de antidepressivos pode retardar a recorrência da depressão.
Todos os pacientes em tratamento com antidepressivos para qualquer indicação devem ser monitorados adequadamente e observados de perto quanto a piora clínica, tendências suicidas e mudanças incomuns de comportamento, especialmente durante os primeiros meses de um curso de terapia medicamentosa, ou em momentos de mudanças de dose, ou aumentos ou diminui.
Os seguintes sintomas, ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia (agitação psicomotora), hipomania e mania, foram relatados em pacientes adultos e pediátricos tratados com antidepressivos para TDM, bem como para outras indicações, tanto psiquiátricas como não psiquiátricas. Embora não tenha sido estabelecida uma relação causal entre o surgimento de tais sintomas e o agravamento da depressão e/ou o surgimento de impulsos suicidas, existe a preocupação de que tais sintomas possam representar precursores de tendências suicidas emergentes.
Deve-se considerar a mudança do regime terapêutico, incluindo a possibilidade de descontinuação da medicação, em pacientes cuja depressão é persistentemente pior, ou que estão experimentando tendências suicidas emergentes ou sintomas que podem ser precursores de piora da depressão ou tendências suicidas, especialmente se esses sintomas forem graves, abruptos no início, ou não faziam parte dos sintomas de apresentação do paciente.
Se for tomada a decisão de descontinuar o tratamento, a medicação deve ser diminuída o mais rápido possível, mas com o reconhecimento de que a descontinuação abrupta pode estar associada a certos sintomas [ver Síndrome de descontinuação e DOSAGEM E ADMINISTRAÇÃO ].
Familiares e cuidadores de pacientes em tratamento com antidepressivos para TDM ou outras indicações, tanto psiquiátricas quanto não psiquiátricas, devem ser alertados sobre a necessidade de monitorar os pacientes quanto ao surgimento de agitação, irritabilidade, mudanças incomuns de comportamento e outros sintomas descritos acima, como bem como o surgimento de tendências suicidas, e relatar tais sintomas imediatamente aos profissionais de saúde. Tal monitoramento deve incluir observação diária por familiares e cuidadores. As prescrições de Effexor XR devem ser feitas para a menor quantidade de cápsulas consistente com o bom manejo do paciente, a fim de reduzir o risco de overdose.
Triagem de pacientes para transtorno bipolar
Um episódio depressivo maior pode ser a apresentação inicial do transtorno bipolar. Acredita-se geralmente (embora não estabelecido em estudos controlados) que tratar tal episódio com um antidepressivo isolado pode aumentar a probabilidade de precipitação de um episódio misto/maníaco em pacientes com risco de transtorno bipolar. Não se sabe se algum dos sintomas descritos acima representa tal conversão. No entanto, antes de iniciar o tratamento com um antidepressivo, os pacientes com sintomas depressivos devem ser examinados adequadamente para determinar se estão em risco de transtorno bipolar; essa triagem deve incluir uma história psiquiátrica detalhada, incluindo uma história familiar de suicídio, transtorno bipolar e depressão. Deve-se notar que Effexor XR não é aprovado para uso no tratamento da depressão bipolar.
Síndrome da serotonina
desenvolvimento de uma síndrome serotoninérgica potencialmente fatal foi relatado com inibidores da recaptação de serotonina-norepinefrina (SNRIs) e ISRSs, incluindo Effexor XR sozinho, mas particularmente com o uso concomitante de outros medicamentos serotoninérgicos (incluindo triptanos, antidepressivos tricíclicos, fentanil, lítio, tramadol, triptofano, buspirona, anfetaminas e erva de São João) e com medicamentos que prejudicam o metabolismo da serotonina em particular, IMAOs, tanto aqueles destinados a tratar distúrbios psiquiátricos como outros, como linezolida ou azul de metileno intravenoso).
Os sintomas da síndrome serotoninérgica podem incluir alterações do estado mental (p. , hiperreflexia, incoordenação); convulsões e sintomas gastrointestinais (por exemplo, náuseas, vômitos, diarréia). Os pacientes devem ser monitorados quanto ao surgimento de síndrome serotoninérgica.
uso concomitante de Effexor XR com IMAOs (destinados a tratar distúrbios psiquiátricos) é contraindicado. Effexor XR também não deve ser iniciado em pacientes que estejam sendo tratados com IMAOs, como linezolida ou azul de metileno intravenoso. Todos os relatos com azul de metileno que forneceram informações sobre a via de administração envolveram administração intravenosa na faixa de dose de 1 mg/kg a 8 mg/kg. Nenhum relato envolveu a administração de azul de metileno por outras vias (como comprimidos orais ou injeção local no tecido) ou em doses mais baixas. Pode haver circunstâncias em que seja necessário iniciar o tratamento com um IMAO, como linezolida ou azul de metileno intravenoso em um paciente tomando Effexor 37,5mg XR. Effexor XR deve ser descontinuado antes de iniciar o tratamento com o IMAO [ver CONTRA-INDICAÇÕES , DOSAGEM E ADMINISTRAÇÃO , e INTERAÇÕES MEDICAMENTOSAS ].
Se o uso concomitante de Effexor 37,5mg XR com outros medicamentos serotoninérgicos (por exemplo, triptanos, antidepressivos tricíclicos, mirtazapina, fentanil, lítio, tramadol, buspirona, anfetaminas, triptofano ou erva de São João) for clinicamente justificado, observação cuidadosa do paciente é aconselhado, particularmente durante o início do tratamento e aumentos de dose [ver INTERAÇÕES MEDICAMENTOSAS ]. Os pacientes devem ser informados sobre o risco potencial de síndrome serotoninérgica. O tratamento com Effexor XR e quaisquer agentes serotoninérgicos concomitantes deve ser descontinuado imediatamente se ocorrerem os eventos acima, e o tratamento sintomático de suporte deve ser iniciado.
Elevações da Pressão Arterial
Em estudos controlados, houve aumentos relacionados à dose na pressão arterial sistólica e diastólica, bem como casos de hipertensão sustentada [ver REAÇÕES ADVERSAS ].
Monitore a pressão arterial antes de iniciar o tratamento com Effexor 37,5mg XR e regularmente durante o tratamento. Controle a hipertensão pré-existente antes de iniciar o tratamento com Effexor 75mg XR. Tenha cuidado ao tratar pacientes com hipertensão pré-existente ou condições cardiovasculares ou cerebrovasculares que possam ser comprometidas pelo aumento da pressão arterial. A elevação sustentada da pressão arterial pode levar a resultados adversos. Casos de pressão arterial elevada que requerem tratamento imediato foram relatados com Effexor XR. Considerar a redução da dose ou a descontinuação do tratamento para pacientes que apresentarem um aumento sustentado da pressão arterial.
Em todos os estudos clínicos com Effexor 37,5mg, 1,4% dos pacientes nos grupos tratados com Effexor XR apresentaram um aumento ≥15 mmHg na pressão arterial diastólica supina (SDBP) ≥ 105 mmHg, em comparação com 0,9% dos pacientes nos grupos placebo. Da mesma forma, 1% dos pacientes nos grupos tratados com Effexor 75mg XR experimentaram um aumento ≥ 20 mm Hg na pressão arterial sistólica supina (SSBP) com pressão arterial ≥ 180 mm Hg, em comparação com 0,3% dos pacientes nos grupos placebo [ver Tabela 10 dentro REAÇÕES ADVERSAS ]. O tratamento com Effexor 75mg XR foi associado à hipertensão sustentada (definida como SDBP emergente do tratamento ≥ 90 mmHg e ≥ 10 mmHg acima da linha de base por três visitas consecutivas em terapia [ver Tabela 11 em REAÇÕES ADVERSAS ]. Um número insuficiente de pacientes recebeu doses médias de Effexor 37,5 mg XR acima de 300 mg por dia em estudos clínicos para avaliar completamente a incidência de aumentos sustentados da pressão arterial nessas doses mais altas.
Sangramento Anormal
ISRSs e SNRIs, incluindo Effexor 37,5mg XR, podem aumentar o risco de eventos hemorrágicos, variando de equimoses, hematomas, epistaxe, petéquias e hemorragia gastrointestinal a hemorragia com risco de vida. O uso concomitante de aspirina, anti-inflamatórios não esteroides (AINEs), varfarina e outros anticoagulantes ou outros medicamentos conhecidos por afetar a função plaquetária pode aumentar esse risco. Relatos de casos e estudos epidemiológicos (caso-controle e desenho de coorte) têm demonstrado associação entre o uso de drogas que interferem na recaptação de serotonina e a ocorrência de sangramento gastrointestinal. Alertar os pacientes sobre o risco de sangramento associado ao uso concomitante de Effexor 75mg XR e AINEs, aspirina ou outros medicamentos que afetem a coagulação.
Glaucoma de ângulo fechado
A dilatação pupilar que ocorre após o uso de muitos medicamentos antidepressivos, incluindo Effexor XR, pode desencadear um ataque de fechamento do ângulo em um paciente com ângulos anatomicamente estreitos que não tenha uma iridectomia patente.
Ativação de mania/hipomania
Mania ou hipomania foi relatada em pacientes tratados com Effexor 37,5mg XR nos estudos de pré-comercialização em MDD, SAD e DP (ver Tabela 2). Mania/hipomania também foi relatada em uma pequena proporção de pacientes com transtornos do humor que foram tratados com outros medicamentos comercializados para tratar o TDM. Effexor 37,5mg XR deve ser usado com cautela em pacientes com história de mania ou hipomania.
Síndrome de descontinuação
Os sintomas de descontinuação foram sistematicamente avaliados em pacientes em uso de venlafaxina, incluindo análises prospectivas de estudos clínicos em TAG e pesquisas retrospectivas de estudos em MDD e SAD. Descobriu-se que a interrupção abrupta ou redução da dose de venlafaxina em várias doses está associada ao aparecimento de novos sintomas, cuja frequência aumenta com o aumento da dose e com a duração mais longa do tratamento. Os sintomas relatados incluem agitação, anorexia, ansiedade, confusão, coordenação e equilíbrio prejudicados, diarreia, tontura, boca seca, humor disfórico, fasciculação, fadiga, sintomas semelhantes aos da gripe, dores de cabeça, hipomania, insônia, náusea, nervosismo, pesadelos, distúrbios sensoriais. incluindo sensações elétricas semelhantes a choque), sonolência, sudorese, tremores, vertigens e vômitos.
Houve relatos pós-comercialização de sintomas graves de descontinuação que podem ser prolongados e graves. Suicídio consumado, pensamentos suicidas, agressão e comportamento violento foram observados em pacientes durante a redução da dose de Effexor 75mg XR, inclusive durante a descontinuação. Outros relatos pós-comercialização descrevem alterações visuais (como visão turva ou dificuldade de focalização) e aumento da pressão arterial após a interrupção ou redução da dose de Effexor XR.
Durante a comercialização de Effexor XR, outros SNRIs e SSRIs, houve relatos espontâneos de outros eventos adversos que ocorreram após a descontinuação desses medicamentos, particularmente quando abruptos, incluindo os seguintes: irritabilidade, letargia, labilidade emocional, zumbido e convulsões.
Os pacientes devem ser monitorados quanto a esses sintomas ao descontinuar o tratamento com Effexor XR. Recomenda-se uma redução gradual da dose, em vez de interrupção abrupta. Se ocorrerem sintomas intoleráveis após a diminuição da dose ou após a descontinuação do tratamento, pode-se considerar a retomada da dose prescrita anteriormente. Subsequentemente, o profissional de saúde pode continuar diminuindo a dose, mas de forma mais gradual. Em alguns pacientes, a descontinuação pode precisar ocorrer por um período de vários meses [ver DOSAGEM E ADMINISTRAÇÃO ].
Convulsões
Ocorreram convulsões com a terapia com venlafaxina. Effexor 75mg XR, como muitos antidepressivos, deve ser usado com cautela em pacientes com histórico de convulsões e deve ser descontinuado em qualquer paciente que desenvolva convulsões. [Deve mitigar o risco: Fatores de risco, medicamentos concomitantes que diminuem o limiar convulsivo.]
Hiponatremia
hiponatremia pode ocorrer como resultado do tratamento com SSRIs e SNRIs, incluindo Effexor 37,5mg XR. Em muitos casos, a hiponatremia parece ser o resultado da Síndrome da Secreção Inapropriada do Hormônio Antidiurético (SIADH). Casos com sódio sérico inferior a 110 mmol/L foram relatados. Pacientes idosos podem estar em maior risco de desenvolver hiponatremia com ISRSs e SNRIs [ver Uso em populações específicas ]. Além disso, os pacientes em uso de diuréticos ou aqueles com depleção de volume podem estar em maior risco. Considerar a descontinuação de Effexor 37,5mg XR em pacientes com hiponatremia sintomática e instituir intervenção médica apropriada.
Sinais e sintomas de hiponatremia incluem dor de cabeça, dificuldade de concentração, comprometimento da memória, confusão, fraqueza e instabilidade, o que pode levar a quedas. Sinais e sintomas associados a casos mais graves e/ou agudos incluem alucinação, síncope, convulsão, coma, parada respiratória e morte.
Alterações de peso e altura em pacientes pediátricos
Alterações de peso
mudança média no peso corporal e a incidência de perda de peso (porcentagem de pacientes que perderam 3,5% ou mais) nos estudos pediátricos controlados por placebo em MDD, GAD e SAD são mostradas nas Tabelas 3 e 4.
A perda de peso não se limitou a pacientes com anorexia emergente do tratamento [ver Alterações do Apetite em Pacientes Pediátricos ].
Os riscos associados ao uso prolongado de Effexor 75mg XR foram avaliados em um estudo MDD aberto de crianças e adolescentes que receberam Effexor XR por até seis meses. As crianças e adolescentes do estudo tiveram aumentos de peso menores do que o esperado, com base em dados de pares pareados por idade e sexo. A diferença entre o ganho de peso observado e o ganho de peso esperado foi maior para crianças (
Alterações de Altura
Tabela 5 mostra o aumento médio da altura em pacientes pediátricos nos estudos de curto prazo MDD, GAD e SAD controlados por placebo. As diferenças nos aumentos de altura nos estudos GAD e MDD foram mais notáveis em pacientes com menos de doze anos.
No estudo MDD aberto de seis meses, crianças e adolescentes tiveram aumentos de altura menores do que o esperado, com base em dados de colegas de idade e sexo. A diferença entre as taxas de crescimento observadas e esperadas foi maior para crianças (
Alterações do Apetite em Pacientes Pediátricos
A diminuição do apetite (relatada como anorexia emergente do tratamento) foi mais comumente observada em pacientes tratados com Effexor XR versus pacientes tratados com placebo na avaliação pré-comercialização de Effexor XR para MDD, GAD e SAD (ver Tabela 6).
Doença Pulmonar Intersticial e Pneumonia Eosinofílica
Doença pulmonar intersticial e pneumonia eosinofílica associada à terapia com venlafaxina foram raramente relatadas. A possibilidade desses eventos adversos deve ser considerada em pacientes tratados com venlafaxina que apresentam dispneia progressiva, tosse ou desconforto torácico. Esses pacientes devem ser submetidos a uma avaliação médica imediata e a descontinuação da terapia com venlafaxina deve ser considerada.
Disfunção Sexual
O uso de SNRIs, incluindo Effexor XR, pode causar sintomas de disfunção sexual [ver REAÇÕES ADVERSAS ]. Em pacientes do sexo masculino, o uso de SNRI pode resultar em atraso ou falha ejaculatória, diminuição da libido e disfunção erétil. Em pacientes do sexo feminino, o uso de SNRI pode resultar em diminuição da libido e orgasmo atrasado ou ausente.
É importante que os prescritores perguntem sobre a função sexual antes do início de Effexor 37,5mg XR e perguntem especificamente sobre alterações na função sexual durante o tratamento, porque a função sexual pode não ser relatada espontaneamente. Ao avaliar as alterações na função sexual, é importante obter uma história detalhada (incluindo o momento do início dos sintomas) porque os sintomas sexuais podem ter outras causas, incluindo o transtorno psiquiátrico subjacente. Discutir estratégias de gestão potenciais para apoiar os pacientes na tomada de decisões informadas sobre o tratamento.
Informações de Aconselhamento do Paciente
Veja aprovado pela FDA INFORMAÇÃO DO PACIENTE ( Guia de Medicação ).
Os prescritores ou outros profissionais de saúde devem informar os pacientes, seus familiares e seus cuidadores sobre os benefícios e riscos associados ao tratamento com Effexor 37,5mg XR e devem aconselhá-los sobre seu uso adequado. Um Guia de Medicação do paciente sobre “Medicamentos Antidepressivos, Depressão e Outras Doenças Mentais Graves e Pensamentos ou Ações Suicidas” está disponível para Effexor 75mg XR. O prescritor ou profissional de saúde deve orientar os pacientes, seus familiares e seus cuidadores a ler o Guia de Medicação e auxiliá-los na compreensão de seu conteúdo. Os pacientes devem ter a oportunidade de discutir o conteúdo do Guia de Medicação e obter respostas para quaisquer dúvidas que possam ter. O texto completo do Guia de Medicação é reimpresso no final deste documento. Os pacientes devem ser informados sobre os seguintes problemas e devem ser solicitados a alertar seu prescritor se ocorrerem enquanto estiverem tomando Effexor XR.
Pensamentos e Comportamentos Suicidas
Orientar os pacientes, seus familiares e cuidadores a procurarem o surgimento de tendências suicidas, agravamento da depressão e outros sintomas psiquiátricos (ansiedade, agitação, ataques de pânico, insônia, irritabilidade, hostilidade, agressividade, impulsividade, acatisia, inquietação psicomotora, hipomania, mania, outras mudanças incomuns no comportamento), especialmente no início do tratamento e quando a dose é ajustada para cima ou para baixo. Tais sintomas devem ser relatados ao prescritor ou profissional de saúde do paciente, principalmente se forem graves, de início abrupto ou não fizerem parte dos sintomas apresentados pelo paciente. Sintomas como esses podem estar associados a um risco aumentado de pensamento e comportamento suicida e indicam a necessidade de monitoramento muito próximo [ver AVISO DE CAIXA e AVISOS E PRECAUÇÕES ].
Medicação concomitante
Aconselhe os pacientes tomando Effexor XR a não usar concomitantemente outros produtos contendo venlafaxina ou desvenlafaxina. Os profissionais de saúde devem instruir os pacientes a não tomar Effexor XR com um IMAO ou dentro de 14 dias após a interrupção de um IMAO e permitir 7 dias após a interrupção de Effexor XR antes de iniciar um IMAO [ver CONTRA-INDICAÇÕES ].
Síndrome da serotonina
Os pacientes devem ser alertados sobre o risco de síndrome serotoninérgica, com o uso concomitante de Effexor 75mg XR e triptanos, tramadol, anfetaminas, suplementos de triptofano, com antipsicóticos ou outros antagonistas da dopamina, ou outros agentes serotoninérgicos. AVISOS E PRECAUÇÕES e INTERAÇÕES MEDICAMENTOSAS ].
Pressão Arterial Elevada
Aconselhe os pacientes que eles devem ter monitoramento regular da pressão arterial ao tomar Effexor XR [ver AVISOS E PRECAUÇÕES ].
Sangramento Anormal
Os pacientes devem ser alertados sobre o uso concomitante de Effexor 75mg XR e AINEs, aspirina, varfarina ou outros medicamentos que afetem a coagulação, uma vez que o uso combinado de psicotrópicos que interferem na recaptação de serotonina e esses agentes tem sido associado a um risco aumentado de sangramento. AVISOS E PRECAUÇÕES ].
Glaucoma de ângulo fechado
Os pacientes devem ser alertados de que tomar Effexor XR pode causar dilatação pupilar leve, que em indivíduos suscetíveis pode levar a um episódio de glaucoma de ângulo fechado. O glaucoma pré-existente é quase sempre o glaucoma de ângulo aberto porque o glaucoma de ângulo fechado, quando diagnosticado, pode ser tratado definitivamente com iridectomia. O glaucoma de ângulo aberto não é um fator de risco para o glaucoma de ângulo fechado. Os pacientes podem querer ser examinados para determinar se são suscetíveis ao fechamento do ângulo e realizar um procedimento profilático (por exemplo, iridectomia), se forem suscetíveis [ver AVISOS E PRECAUÇÕES ].
Ativação de mania/hipomania
Aconselhe os pacientes, seus familiares e cuidadores a observarem sinais de ativação de mania/hipomania [ver AVISOS E PRECAUÇÕES ].
Doença cardiovascular/cerebrovascular
Recomenda-se cautela na administração de Effexor XR a pacientes com distúrbios cardiovasculares, cerebrovasculares ou do metabolismo lipídico [ver REAÇÕES ADVERSAS ].
Elevação de colesterol e triglicerídeos séricos
Avise os pacientes que podem ocorrer elevações no colesterol total, LDL e triglicerídeos e que a medição dos lipídios séricos pode ser considerada [ver AVISOS E PRECAUÇÕES ].
Síndrome de descontinuação
Aconselhe os pacientes a não parar de tomar Effexor 75mg XR sem falar primeiro com seu profissional de saúde. Os pacientes devem estar cientes de que podem ocorrer efeitos de descontinuação ao interromper Effexor XR [ver AVISOS E PRECAUÇÕES e REAÇÕES ADVERSAS ].
Disfunção Sexual
Avise os pacientes que o uso de Effexor XR pode causar sintomas de disfunção sexual em pacientes do sexo masculino e feminino. Informe os pacientes que eles devem discutir quaisquer alterações na função sexual e possíveis estratégias de manejo com seu médico [ver AVISOS E PRECAUÇÕES ].
Interferência com o desempenho cognitivo e motor
Alerte os pacientes sobre a operação de máquinas perigosas, incluindo automóveis, até que estejam razoavelmente certos de que a terapia com Effexor 37,5mg XR não afeta adversamente sua capacidade de se envolver em tais atividades.
Álcool
Aconselhe os pacientes a evitar o álcool enquanto estiverem tomando Effexor 37,5mg XR [ver INTERAÇÕES MEDICAMENTOSAS ].
Reações alérgicas
Aconselhe os pacientes a notificar seu médico se desenvolverem fenômenos alérgicos, como erupção cutânea, urticária, inchaço ou dificuldade para respirar.
Gravidez
Aconselhe as pacientes a notificarem seu médico se engravidarem ou pretenderem engravidar durante o tratamento [ver Uso em populações específicas ].
Enfermagem
Aconselhe as pacientes a notificarem seu médico se estiverem amamentando um bebê [ver Uso em populações específicas ].
Esferóides residuais
Effexor XR contém esferóides, que liberam a droga lentamente no trato digestivo. A porção insolúvel desses esferoides é eliminada, e os pacientes podem notar a passagem de esferoides nas fezes ou via colostomia. Os pacientes devem ser informados de que o medicamento ativo já foi absorvido no momento em que o paciente vê os esferóides.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Carcinogênese
Os tumores não foram aumentados pelo tratamento com venlafaxina em camundongos ou ratos. A venlafaxina foi administrada por gavagem oral a camundongos por 18 meses em doses de até 120 mg/kg por dia, que foi 1,7 vezes a dose humana máxima recomendada com base em mg/m2. A venlafaxina também foi administrada a ratos por gavagem oral por 24 meses em doses de até 120 mg/kg por dia. Em ratos que receberam a dose de 120 mg/kg, as concentrações plasmáticas de venlafaxina na necropsia foram 1 vezes (ratos machos) e 6 vezes (ratas fêmeas) as concentrações plasmáticas dos pacientes que receberam a dose humana máxima recomendada. Os níveis plasmáticos do metabólito O-desmetil (ODV) foram mais baixos em ratos do que em pacientes que receberam a dose máxima recomendada. A O-desmetilvenlafaxina (ODV), o principal metabólito humano da venlafaxina, administrada por gavagem oral a camundongos e ratos por 2 anos não aumentou a incidência de tumores em nenhum dos estudos. Os camundongos receberam ODV em dosagens de até 500/300 mg/kg/dia (dose reduzida após 45 semanas de dosagem). A exposição na dose de 300 mg/kg/dia é 9 vezes maior que a dose humana de 225 mg/dia. Os ratos receberam ODV em dosagens de até 300 mg/kg/dia (machos) ou 500 mg/kg/dia (fêmeas). A exposição na dose mais alta é aproximadamente 8 (homens) ou 11 (mulheres) vezes maior que uma dose humana de 225 mg/dia.
Mutagênese
venlafaxina e o principal metabólito humano, ODV, não foram mutagênicos no ensaio de mutação reversa de Ames em bactérias Salmonella ou no ensaio de mutação genética direta de células de mamíferos HGPRT/ovário de hamster chinês. A venlafaxina também não foi mutagênica ou clastogênica no ensaio in vitro de transformação de células de camundongo BALB/c-3T3, no ensaio de troca de cromátides irmãs em células cultivadas de ovário de hamster chinês ou no ensaio de aberração cromossômica in vivo em medula óssea de rato. ODV não foi clastogênico no ensaio in vitro de aberração cromossômica de células de ovário de hamster chinês ou no ensaio in vivo de aberração cromossômica em ratos.
Prejuízo da Fertilidade
Estudos de reprodução e fertilidade da venlafaxina em ratos não mostraram efeitos adversos da venlafaxina na fertilidade masculina ou feminina em doses orais de até 2 vezes a dose humana máxima recomendada de 225 mg/dia em uma base de mg/m2. No entanto, a fertilidade reduzida foi observada em um estudo no qual ratos machos e fêmeas foram tratados com O-desmetilvenlafaxina (ODV), o principal metabólito humano da venlafaxina, antes e durante o acasalamento e gestação. Isso ocorreu em uma exposição ao ODV (AUC) aproximadamente 2 a 3 vezes a associada a uma dose de venlafaxina humana de 225 mg/dia.
Uso em populações específicas
Gravidez
Efeitos teratogênicos
Gravidez Categoria C
venlafaxina não causou malformações em descendentes de ratos ou coelhos que receberam doses de até 2,5 vezes (rato) ou 4 vezes (coelho) a dose diária humana máxima recomendada em mg/m2. No entanto, em ratos, houve uma diminuição no peso dos filhotes, um aumento nos filhotes natimortos e um aumento nas mortes de filhotes durante os primeiros 5 dias de lactação, quando a dosagem começou durante a gravidez e continuou até o desmame. A causa dessas mortes não é conhecida. Estes efeitos ocorreram em 2,5 vezes (mg/m2) a dose diária humana máxima. A dose sem efeito para a mortalidade de filhotes de rato foi 0,25 vezes a dose humana em uma base de mg/m2. Em estudos de desenvolvimento reprodutivo em ratos e coelhos com O-desmetilvenlafaxina (ODV), o principal metabólito humano da venlafaxina, não foi observada evidência de teratogenicidade em margens de exposição de 13 em ratos e 0,3 em coelhos. Não existem estudos adequados e bem controlados em mulheres grávidas. Effexor XR deve ser usado durante a gravidez somente se o benefício potencial justificar o risco potencial para o feto. Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, este medicamento deve ser usado durante a gravidez somente se for claramente necessário.
Efeitos não teratogênicos
Recém-nascidos expostos a Effexor 37,5mg XR, outros SNRIs ou SSRIs, no final do terceiro trimestre, desenvolveram complicações que requerem hospitalização prolongada, suporte respiratório e alimentação por sonda. Tais complicações podem surgir imediatamente após o parto. Os achados clínicos relatados incluíram desconforto respiratório, cianose, apnéia, convulsões, instabilidade de temperatura, dificuldade de alimentação, vômitos, hipoglicemia, hipotonia, hipertonia, hiperreflexia, tremor, nervosismo, irritabilidade e choro constante. Essas características são consistentes com um efeito tóxico direto de SSRIs e SNRIs, ou possivelmente uma síndrome de descontinuação do medicamento. Deve-se notar que, em alguns casos, o quadro clínico é consistente com a síndrome serotoninérgica [ver AVISOS E PRECAUÇÕES e INTERAÇÕES MEDICAMENTOSAS ]. Ao tratar uma mulher grávida com Effexor XR durante o terceiro trimestre, o médico deve considerar cuidadosamente os potenciais riscos e benefícios do tratamento.
Trabalho e entrega
O efeito da venlafaxina no trabalho de parto e parto em humanos é desconhecido.
Mães que amamentam
Venlafaxina e ODV foram relatados como sendo excretados no leite humano. Devido ao potencial de reações adversas graves em lactentes de Effexor XR, deve-se decidir entre descontinuar a amamentação ou descontinuar o medicamento, levando em consideração a importância do medicamento para a mãe.
Uso Pediátrico
Dois estudos controlados por placebo em 766 pacientes pediátricos com TDM e dois estudos controlados por placebo em 793 pacientes pediátricos com TAG foram conduzidos com Effexor XR, e os dados não foram suficientes para sustentar uma alegação de uso em pacientes pediátricos.
Qualquer pessoa considerando o uso de Effexor XR em uma criança ou adolescente deve equilibrar os riscos potenciais com a necessidade clínica [ver AVISO DE CAIXA , AVISOS E PRECAUÇÕES e REAÇÕES ADVERSAS ].
Embora nenhum estudo tenha sido projetado para avaliar principalmente o impacto de Effexor 37,5mg XR no crescimento, desenvolvimento e maturação de crianças e adolescentes, os estudos realizados sugerem que Effexor XR pode afetar negativamente o peso e a altura [ver AVISOS E PRECAUÇÕES ]. Se for tomada a decisão de tratar um paciente pediátrico com Effexor XR, recomenda-se o monitoramento regular do peso e da altura durante o tratamento, principalmente se o tratamento for continuado a longo prazo [ver AVISOS E PRECAUÇÕES ]. A segurança do tratamento com Effexor 75mg XR para pacientes pediátricos não foi sistematicamente avaliada para tratamento crônico com duração superior a seis meses. Nos estudos realizados em doentes pediátricos (6-17 anos), a ocorrência de aumentos da pressão arterial e do colesterol considerados clinicamente relevantes em doentes pediátricos foi semelhante à observada em doentes adultos. Consequentemente, as precauções para adultos se aplicam a pacientes pediátricos [ver AVISOS E PRECAUÇÕES ].
Uso Geriátrico
A porcentagem de pacientes em estudos clínicos para Effexor 37,5mg XR para MDD, GAD, SAD e PD que tinham 65 anos de idade ou mais é mostrada na Tabela 15.
Não foram observadas diferenças globais na eficácia ou segurança entre pacientes geriátricos e pacientes mais jovens, e outras experiências clínicas relatadas geralmente não identificaram diferenças na resposta entre pacientes idosos e pacientes mais jovens. No entanto, uma maior sensibilidade de alguns indivíduos mais velhos não pode ser descartada. SSRIs e SNRIs, incluindo Effexor XR, foram associados a casos de hiponatremia clinicamente significativa em pacientes idosos, que podem estar em maior risco para esse evento adverso [ver AVISOS E PRECAUÇÕES ].
A farmacocinética da venlafaxina e da ODV não é substancialmente alterada em idosos [ver FARMACOLOGIA CLÍNICA ] (ver Figura 3). Nenhum ajuste de dose é recomendado para idosos com base apenas na idade, embora outras circunstâncias clínicas, algumas das quais podem ser mais comuns em idosos, como insuficiência renal ou hepática, possam justificar uma redução da dose [ver DOSAGEM E ADMINISTRAÇÃO ].
Idade e sexo
Uma análise farmacocinética populacional de 404 pacientes tratados com Effexor de dois estudos envolvendo regimes duas vezes ao dia e três vezes ao dia mostrou que os níveis plasmáticos mínimos de dose de venlafaxina ou ODV não foram alterados por diferenças de idade ou sexo. O ajuste da dose com base na idade ou sexo de um paciente geralmente não é necessário [ver DOSAGEM E ADMINISTRAÇÃO ] (ver Tabela 15).
Uso em subgrupos de pacientes
Figura 3: Farmacocinética da venlafaxina e seu metabólito O-desmetilvenlafaxina (ODV) em populações especiais.
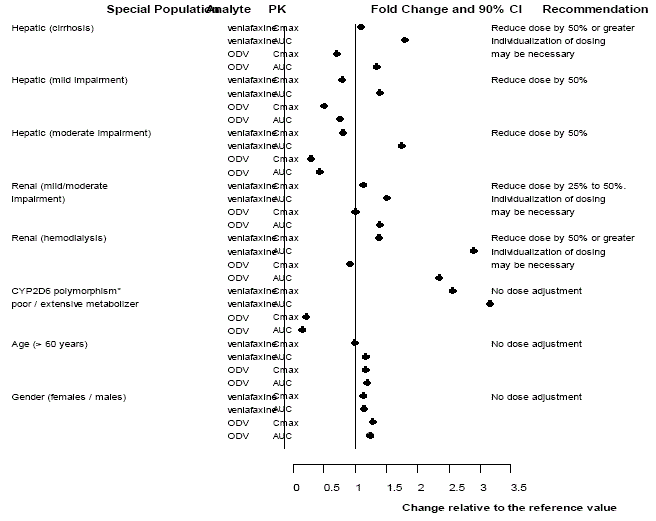
SOBREDOSAGEM
Experiência Humana
Durante as avaliações pré-comercialização de Effexor 75mg XR (para MDD, GAD, SAD e PD) e Effexor (para MDD), houve vinte notificações de superdosagem aguda com Effexor (6 e 14 notificações em pacientes com Effexor XR e Effexor 75mg, respectivamente) , sozinho ou em combinação com outras drogas e/ou álcool.
sonolência foi o sintoma mais comumente relatado. Entre os outros sintomas relatados estavam parestesia de todos os quatro membros, tontura moderada, náusea, dormência nas mãos e pés e crises de calor e frio 5 dias após a superdosagem. Na maioria dos casos, nenhum sinal ou sintoma foi associado à superdosagem. A maioria dos relatos envolveu ingestão na qual a dose total de venlafaxina tomada foi estimada em não mais do que várias vezes a dose terapêutica usual. Um paciente que ingeriu 2,75 g de venlafaxina apresentou duas convulsões generalizadas e um prolongamento do intervalo QTc para 500 mseg, em comparação com 405 mseg na linha de base. Taquicardia sinusal leve foi relatada em dois dos outros pacientes.
As ações tomadas para tratar a superdosagem incluíram não tratamento, hospitalização e tratamento sintomático e hospitalização mais tratamento com carvão ativado. Todos os pacientes se recuperaram.
Na experiência pós-comercialização, a superdosagem com venlafaxina ocorreu predominantemente em combinação com álcool e/ou outras drogas. Os eventos mais comumente relatados em superdosagem incluem taquicardia, alterações no nível de consciência (variando de sonolência a coma), midríase, convulsões e vômitos.
Foram relatadas alterações no eletrocardiograma (por exemplo, prolongamento do intervalo QT, bloqueio de ramo, prolongamento do QRS), taquicardia ventricular, bradicardia, hipotensão, rabdomiólise, vertigem, necrose hepática, síndrome serotoninérgica e morte.
Estudos retrospectivos publicados relatam que a superdosagem de venlafaxina pode estar associada a um risco aumentado de desfechos fatais em comparação ao observado com produtos antidepressivos ISRS, mas menor do que para antidepressivos tricíclicos. Estudos epidemiológicos mostraram que os pacientes tratados com venlafaxina têm uma carga preexistente maior de fatores de risco de suicídio do que os pacientes tratados com ISRS. A extensão em que a descoberta de um risco aumentado de desfechos fatais pode ser atribuída à toxicidade da venlafaxina em superdosagem, em oposição a algumas características de pacientes tratados com venlafaxina, não é clara. As prescrições de Effexor 75mg XR devem ser feitas para a menor quantidade de cápsulas consistente com um bom manejo do paciente, a fim de reduzir o risco de overdose.
Gerenciamento de superdosagem
Consulte um Centro de Controle de Intoxicações Certificado para obter orientações e conselhos atualizados (1-800-222-1222 ou www.poison.org). Em caso de superdosagem, forneça cuidados de suporte, incluindo supervisão médica e monitoramento. O tratamento deve consistir nas medidas gerais empregadas no manejo da superdosagem com qualquer droga. Considere a possibilidade de overdose de drogas múltiplas. Assegurar vias aéreas, oxigenação e ventilação adequadas. Monitorar o ritmo cardíaco e os sinais vitais. Fornecer medidas de suporte e sintomáticas.
CONTRA-INDICAÇÕES
Hipersensibilidade
Hipersensibilidade ao cloridrato de venlafaxina, succinato de desvenlafaxina ou a qualquer excipiente da formulação
Uso concomitante com inibidores da monoamina oxidase (IMAOs)
uso de IMAOs (destinados a tratar distúrbios psiquiátricos) concomitantemente com Effexor 75mg XR ou dentro de 7 dias após a interrupção do tratamento com Effexor XR é contraindicado devido ao risco aumentado de síndrome serotoninérgica. O uso de Effexor 37,5mg XR dentro de 14 dias após a descontinuação do tratamento com um IMAO (destinado a tratar distúrbios psiquiátricos) também é contraindicado [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES , e INTERAÇÕES MEDICAMENTOSAS ].
Iniciar Effexor XR em um paciente que está sendo tratado com um IMAO, como linezolida ou azul de metileno intravenoso, também é contraindicado, devido ao risco aumentado de síndrome serotoninérgica [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES , e INTERAÇÕES MEDICAMENTOSAS ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
mecanismo exato da ação antidepressiva da venlafaxina em humanos é desconhecido, mas acredita-se que esteja relacionado à potencialização da serotonina e da norepinefrina no sistema nervoso central, através da inibição de sua recaptação. Estudos não clínicos demonstraram que a venlafaxina e seu metabólito ativo, ODV, são inibidores potentes e seletivos da recaptação neuronal de serotonina e norepinefrina e inibidores fracos da recaptação de dopamina.
Farmacodinâmica
Venlafaxina e ODV não têm afinidade significativa para receptores muscarínico-colinérgicos, H1-histaminérgicos ou α1 adrenérgicos in vitro. Supõe-se que a atividade farmacológica nesses receptores esteja associada a vários efeitos anticolinérgicos, sedativos e cardiovasculares observados com outras drogas psicotrópicas. Venlafaxina e ODV não possuem atividade inibitória da monoaminoxidase (MAO).
Eletrofisiologia Cardíaca
efeito da venlafaxina no intervalo QT foi avaliado em um estudo QT cruzado de três períodos randomizado, duplo-cego, controlado por placebo e positivo, em 54 indivíduos adultos saudáveis. Nenhum efeito significativo de prolongamento do intervalo QT de 450 mg de venlafaxina foi detectado.
Farmacocinética
As concentrações de estado estacionário de venlafaxina e ODV no plasma são atingidas dentro de 3 dias de terapia oral de doses múltiplas. Venlafaxina e ODV exibiram cinética linear na faixa de dose de 75 a 450 mg por dia. A depuração plasmática média±DP no estado de equilíbrio da venlafaxina e ODV é 1,3±0,6 e 0,4±0,2 L/h/kg, respectivamente; a meia-vida de eliminação aparente é de 5±2 e 11±2 horas, respectivamente; e volume de distribuição aparente (estado estacionário) é 7,5±3,7 e 5,7±1,8 L/kg, respectivamente. Venlafaxina e ODV ligam-se minimamente em concentrações terapêuticas às proteínas plasmáticas (27% e 30%, respectivamente).
Absorção e Distribuição
venlafaxina é bem absorvida e extensamente metabolizada no fígado. ODV é o principal metabólito ativo. Com base em estudos de balanço de massa, pelo menos 92% de uma dose oral única de venlafaxina é absorvida. A biodisponibilidade absoluta da venlafaxina é de aproximadamente 45%.
A administração de Effexor 37,5 mg XR (150 mg uma vez ao dia) geralmente resultou em valores de Cmax e Tmax mais baixos do que para Effexor (liberação imediata) administrado duas vezes ao dia (Tabela 16). Quando doses diárias iguais de venlafaxina foram administradas na forma de comprimido de liberação imediata ou cápsula de liberação prolongada, a exposição tanto à venlafaxina quanto à ODV foi semelhante para os dois tratamentos, e a flutuação nas concentrações plasmáticas foi ligeiramente menor com o Effexor 37,5mg Cápsula XR. Portanto, Effexor XR fornece uma taxa de absorção mais lenta, mas a mesma extensão de absorção em comparação com o comprimido de liberação imediata.
Os alimentos não afetaram a biodisponibilidade da venlafaxina ou de seu metabólito ativo, ODV. O tempo de administração (AM versus PM) não afetou a farmacocinética da venlafaxina e ODV da cápsula de 75 mg de Effexor 75 mg XR.
A venlafaxina não se liga fortemente às proteínas plasmáticas; portanto, a administração de Effexor 37,5mg XR a um paciente que esteja tomando outro medicamento que seja altamente ligado a proteínas não deve causar aumento das concentrações livres do outro medicamento.
Metabolismo e eliminação
Após absorção, a venlafaxina sofre extenso metabolismo pré-sistêmico no fígado, principalmente para ODV, mas também para N-desmetilvenlafaxina, N,O-didesmetilvenlafaxina e outros metabólitos menores. Estudos in vitro indicam que a formação de ODV é catalisada por CYP2D6; isso foi confirmado em um estudo clínico mostrando que pacientes com níveis baixos de CYP2D6 (metabolizadores fracos) tinham níveis aumentados de venlafaxina e níveis reduzidos de ODV em comparação com pessoas com níveis normais de CYP2D6 (metabolizadores extensos) [ver Uso em populações específicas ].
Aproximadamente 87% de uma dose de venlafaxina é recuperada na urina dentro de 48 horas como venlafaxina inalterada (5%), ODV não conjugada (29%), ODV conjugada (26%) ou outros metabólitos inativos menores (27%). A eliminação renal da venlafaxina e seus metabólitos é, portanto, a principal via de excreção.
Estudos clínicos
Transtorno Depressivo Maior
eficácia de Effexor 75mg XR (cloridrato de venlafaxina) cápsulas de liberação prolongada como tratamento para Transtorno Depressivo Maior (TDM) foi estabelecida em dois medicamentos controlados por placebo, de curto prazo (8 semanas para o estudo 1; 12 semanas para o estudo 2), -estudos de dose, com doses começando em 75 mg por dia e variando até 225 mg por dia em pacientes ambulatoriais adultos que atendem aos critérios do DSM-III-R ou DSM-IV para TDM. Em pacientes ambulatoriais moderadamente deprimidos, a dose inicial de venlafaxina foi de 75 mg por dia. Em ambos os estudos, Effexor XR demonstrou superioridade em relação ao placebo na medida de eficácia primária definida como alteração desde a linha de base na pontuação total HAM-D-21 até a visita do endpoint, Effexor XR também demonstrou superioridade sobre o placebo no endpoint chave de eficácia secundária, o Clinical Escala de Gravidade da Doença de Impressões Globais (CGI). O exame dos subgrupos de gênero da população estudada não revelou qualquer responsividade diferencial com base no gênero.
Um estudo de 4 semanas de pacientes internados que atendem aos critérios do DSM-III-R para TDM com melancolia utilizando Effexor 37,5 mg em uma faixa de 150 a 375 mg por dia (dividido em um esquema de três vezes ao dia) demonstrou superioridade de Effexor sobre placebo com base na pontuação total HAM-D-21. A dose média em completadores foi de 350 mg por dia (estudo 3).
Em um estudo de longo prazo, pacientes ambulatoriais adultos com TDM que responderam durante um estudo aberto de 8 semanas com Effexor 37,5mg XR (75, 150 ou 225 mg, uma vez ao dia todas as manhãs) foram randomizados para a continuação do mesmo Effexor XR ou placebo, por até 26 semanas de observação para recaída. A resposta durante a fase de rótulo aberto foi definida como uma pontuação do item de gravidade da doença CGI de ≤3 e uma pontuação total HAM-D-21 de ≤10 na avaliação do dia 56. A recaída durante a fase duplo-cega foi definida da seguinte forma: (1) um reaparecimento de transtorno depressivo maior conforme definido pelos critérios do DSM-IV e uma pontuação do item de gravidade da doença CGI de ≥4 (doença moderada), (2) 2 CGI consecutivos Pontuação do item de Gravidade da Doença de ≥4, ou (3) uma pontuação final do item de Gravidade da Doença do CGI de ≥4 para qualquer paciente que desistiu do estudo por qualquer motivo. Os pacientes que receberam tratamento contínuo com Effexor 37,5 mg XR apresentaram taxas de recaída estatisticamente significativamente mais baixas nas 26 semanas subsequentes em comparação com aqueles que receberam placebo (estudo 4).
Em um segundo estudo de longo prazo, pacientes ambulatoriais adultos com TDM, tipo recorrente, que responderam (pontuação total HAM-D21 ≤ 12 na avaliação do dia 56) e continuaram a melhorar [definido como os seguintes critérios atendidos nos dias 56 a 180 : (1) sem pontuação total HAM-D-21 ≥ 20; (2) não mais de 2 pontuações totais HAM39 D-21 > 10, e (3) nenhuma pontuação de item de gravidade de doença única CGI ≥ 4 (moderadamente doente)] durante as 26 semanas iniciais de tratamento com Effexor [100 a 200 mg por dia, em um esquema de duas vezes ao dia] foram randomizados para a continuação da mesma dose de Effexor ou placebo. O período de acompanhamento para observar pacientes para recaída, definido como uma pontuação do item de gravidade da doença CGI ≥ 4, foi de até 52 semanas. Os pacientes que receberam tratamento contínuo com Effexor apresentaram taxas de recaída estatisticamente significativamente mais baixas nas 52 semanas subsequentes em comparação com aqueles que receberam placebo (estudo 5).
Distúrbio de ansiedade generalizada
eficácia de Effexor XR como tratamento para Transtorno de Ansiedade Generalizada (TAG) foi estabelecida em dois estudos de 8 semanas, controlados por placebo, de dose fixa (75 a 225 mg por dia), um de 6 meses, controlado por placebo, flexível - estudo de dose (75 a 225 mg por dia) e um estudo de dose fixa de 6 meses, controlado por placebo (37,5, 75 e 150 mg por dia) em pacientes ambulatoriais adultos que atendem aos critérios do DSM-IV para TAG.
Em um estudo de 8 semanas, Effexor XR demonstrou superioridade em relação ao placebo para as doses de 75, 150 e 225 mg por dia, conforme medido pela pontuação total da Escala de Avaliação de Hamilton para Ansiedade (HAM-A), tanto a ansiedade quanto a tensão da HAM-A itens e a escala Clinical Global Impressions (CGI). No entanto, as doses de 75 e 150 mg por dia não foram tão consistentemente eficazes quanto a dose mais alta (estudo 1). Um segundo estudo de 8 semanas avaliando doses de 75 e 150 mg por dia e placebo mostrou que ambas as doses foram mais eficazes do que placebo em alguns desses mesmos resultados; no entanto, a dose de 75 mg por dia foi mais consistentemente eficaz do que a dose de 150 mg por dia (estudo 2). Uma relação dose-resposta para eficácia no GAD não foi claramente estabelecida na faixa de dose de 75 a 225 mg por dia estudada.
Dois estudos de 6 meses, um avaliando doses de Effexor 75mg XR de 37,5, 75 e 150 mg por dia (estudo 3) e o outro avaliando doses de Effexor XR de 75 a 225 mg por dia (estudo 4), mostraram que doses diárias de 75 mg ou mais foram mais eficazes do que placebo no total de HAM-A, tanto os itens de ansiedade e tensão de HAM-A quanto a escala CGI durante 6 meses de tratamento. Embora também houvesse evidência de superioridade em relação ao placebo para a dose de 37,5 mg por dia, essa dose não foi tão consistentemente eficaz quanto as doses mais altas.
O exame dos subgrupos de gênero da população estudada não revelou qualquer responsividade diferencial com base no gênero.
Transtorno de Ansiedade Social (também conhecido como Fobia Social)
eficácia de Effexor 37,5mg XR como tratamento para Transtorno de Ansiedade Social (TAS) foi estabelecida em quatro estudos duplo-cegos, de grupos paralelos, de 12 semanas, multicêntricos, controlados por placebo, de dose flexível (estudos 1-4) e um estudo duplo-cego, de grupos paralelos, de 6 meses, controlado por placebo, de dose fixa/flexível, que incluiu doses na faixa de 75 a 225 mg por dia em pacientes ambulatoriais adultos que atendem aos critérios do DSM-IV para TAS (estudo 5 ).
Nestes cinco estudos, Effexor 75mg XR foi estatisticamente significativamente mais eficaz do que o placebo na mudança da linha de base para o ponto final na pontuação total da Escala de Ansiedade Social de Liebowitz (LSAS). Não houve evidência de maior eficácia do grupo de 150 a 225 mg por dia em comparação com o grupo de 75 mg por dia no estudo de 6 meses.
O exame de subconjuntos da população estudada não revelou qualquer responsividade diferencial com base no gênero. Não havia informações suficientes para determinar o efeito da idade ou raça no resultado nestes estudos.
Síndrome do pânico
eficácia de Effexor XR como tratamento para Transtorno de Pânico (TP) foi estabelecida em dois estudos duplo-cegos, multicêntricos, de 12 semanas, controlados por placebo em pacientes ambulatoriais adultos que atendem aos critérios do DSM-IV para TP, com ou sem agorafobia. Os pacientes receberam doses fixas de 75 ou 150 mg por dia em um estudo (estudo 1) e 75 ou 225 mg por dia no outro estudo (estudo 2).
A eficácia foi avaliada com base nos resultados em três variáveis: (1) porcentagem de pacientes livres de ataques de pânico com sintomas completos na Escala de Pânico e Ansiedade Antecipatória (PAAS); (2) alteração média da linha de base ao ponto final na pontuação total da Escala de Gravidade do Transtorno do Pânico (PDSS); e (3) porcentagem de pacientes classificados como respondedores (muito melhorados ou muito melhorados) na escala de Melhoria de Impressões Globais Clínicas (CGI). Nestes dois estudos, Effexor XR foi estatisticamente significativamente mais eficaz do que placebo (para cada dose fixa) em todos os três parâmetros, mas uma relação dose-resposta não foi claramente estabelecida.
O exame de subconjuntos da população estudada não revelou qualquer responsividade diferencial com base no gênero. Não havia informações suficientes para determinar o efeito da idade ou raça no resultado nestes estudos.
Em um estudo de longo prazo (estudo 3), pacientes ambulatoriais adultos que atenderam aos critérios do DSM-IV para DP que responderam durante uma fase aberta de 12 semanas com Effexor 75mg XR (75 a 225 mg por dia) foram aleatoriamente designados para continuar o mesmo Effexor 75mg Dose de XR (75, 150 ou 225 mg) ou mude para placebo para observação de recaída em condições duplo-cegas. A resposta durante a fase aberta foi definida como ≤ 1 ataque de pânico com sintomas completos por semana durante as últimas 2 semanas da fase aberta e uma pontuação de melhora CGI de 1 (muito melhorada) ou 2 (muito melhorada). A recaída durante a fase duplo-cega foi definida como tendo 2 ou mais ataques de pânico com sintomas completos por semana durante 2 semanas consecutivas ou interrupção devido à perda de eficácia conforme determinado pelos investigadores durante o estudo. Os pacientes randomizados estavam em estado de resposta por um tempo médio de 34 dias antes de serem randomizados. Na fase randomizada após o período aberto de 12 semanas, os pacientes que receberam Effexor 75mg XR contínuo tiveram um tempo estatisticamente significativamente maior para recaída.
Pacientes pediátricos
Dois estudos controlados por placebo em 766 pacientes pediátricos com TDM e dois estudos controlados por placebo em 793 pacientes pediátricos com TAG foram conduzidos com Effexor XR, e os dados não foram suficientes para sustentar uma alegação de uso em pacientes pediátricos.
O que é Effexor e como é usado?
Effexor é um medicamento de prescrição usado para tratar os sintomas de depressão, ansiedade generalizada, ansiedade social e transtorno do pânico. Effexor pode ser usado sozinho ou com outros medicamentos.
Effexor pertence a uma classe de medicamentos chamados Antidepressivos, Inibidores Seletivos da Recaptação de Serotonina e Norepinefrina (SNRIs).
Quais são os possíveis efeitos colaterais do Effexor 37,5mg?
Effexor pode causar efeitos colaterais graves, incluindo:
- visão embaçada,
- visão de túnel,
- dor ou inchaço nos olhos,
- vendo halos redondos de luzes,
- hematomas ou sangramentos fáceis (sangramento nasal, sangramento nas gengivas),
- sangue na urina ou fezes,
- tossindo sangue,
- tosse,
- aperto no peito,
- Problemas respiratórios,
- convulsões (convulsão),
- dor de cabeça,
- confusão,
- fala arrastada,
- fraqueza severa,
- vômito,
- perda de coordenação,
- sentindo-se instável,
- músculo muito rígido (rígido),
- febre alta,
- sudorese,
- confusão,
- batimentos cardíacos rápidos ou irregulares,
- tremores, e
- tontura
- Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
- Os efeitos colaterais mais comuns do Effexor incluem:
- tontura,
- sonolência,
- ansiedade,
- sentindo nervoso,
- problemas de sono (insônia),
- alterações na visão,
- náusea,
- vômito,
- diarréia,
- alterações de peso ou apetite,
- boca seca,
- bocejando,
- aumento da sudorese,
- diminuição do desejo sexual,
- impotência,
- ejaculação anormal e
- dificuldade em ter um orgasmo
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Effexor. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
Suicídio e drogas antidepressivas
Os antidepressivos aumentaram o risco em comparação ao placebo de pensamento e comportamento suicida (suicidalidade) em crianças, adolescentes e adultos jovens em estudos de curto prazo de Transtorno Depressivo Maior (TDM) e outros transtornos psiquiátricos. Qualquer pessoa que considere o uso de comprimidos de venlafaxina, USP ou qualquer outro antidepressivo em uma criança, adolescente ou adulto jovem deve equilibrar esse risco com a necessidade clínica. Estudos de curto prazo não mostraram um aumento no risco de suicídio com antidepressivos em comparação com placebo em adultos com mais de 24 anos; houve uma redução no risco com antidepressivos em comparação com placebo em adultos com 65 anos ou mais. A depressão e alguns outros transtornos psiquiátricos estão associados ao aumento do risco de suicídio. Pacientes de todas as idades que iniciam terapia antidepressiva devem ser monitorados adequadamente e observados de perto quanto a piora clínica, suicídio ou mudanças incomuns no comportamento. As famílias e os cuidadores devem ser avisados da necessidade de observação atenta e comunicação com o prescritor. Comprimidos de venlafaxina, USP não é aprovado para uso em pacientes pediátricos. (Ver AVISOS : Agravamento clínico e risco de suicídio , INFORMAÇÃO DO PACIENTE , e PRECAUÇÕES : Uso Pediátrico ).
DESCRIÇÃO
Comprimidos de venlafaxina, USP é um antidepressivo estruturalmente novo para administração oral. É designado cloridrato de (R/S)-1-[2-(dimetilamino)-1-(4-metoxifenil)etil]ciclohexanol ou (±)-1-[α-[(dimetil-amino)metil]-p- cloridrato de metoxibenzil]ciclohexanol e tem a fórmula empírica de C17H27NO2 HCl. Seu peso molecular é 313,87. A fórmula estrutural é mostrada abaixo.
O cloridrato de venlafaxina é um sólido cristalino branco a esbranquiçado com uma solubilidade de 572 mg/mL em água (ajustada para força iônica de 0,2 M com cloreto de sódio). Seu coeficiente de partição octanol:água (cloreto de sódio 0,2 M) é 0,43.
Os comprimidos comprimidos contêm cloridrato de venlafaxina, USP equivalente a 25 mg, 37,5 mg, 50 mg, 75 mg ou 100 mg de venlafaxina base e os seguintes ingredientes inativos: celulose microcristalina, lactose monohidratada, amido pré-gelatinizado, amidoglicolato de sódio, óxido de ferro vermelho, óxido de ferro amarelo, dióxido de silício coloidal e estearato de magnésio.
