Zyprexa 2.5mg, 5mg, 7.5mg, 10mg, 15mg, 20mg Olanzapine Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Zyprexa 10mg e como é usado?
O Zyprexa é um medicamento sujeito a receita médica utilizado para tratar os sintomas da esquizofrenia e da perturbação bipolar (depressão maníaca). Zyprexa pode ser usado sozinho ou com outros medicamentos.
- Zyprexa pertence a uma classe de medicamentos chamados Antipsicóticos, 2ª Geração, Agentes Antimaníacos.
- Não se sabe se Zyprexa é seguro e eficaz em crianças com menos de 13 anos de idade.
Quais são os possíveis efeitos colaterais do Zyprexa 15mg?
Zyprexa pode causar efeitos colaterais graves, incluindo:
- movimentos musculares descontrolados em seu rosto (mastigação, estalar os lábios, franzir a testa, movimento da língua, piscar ou movimento dos olhos),
- dificuldade para falar ou engolir,
- inchaço nas mãos ou pés,
- confusão,
- pensamentos ou comportamentos incomuns,
- alucinações,
- pensamentos sobre se machucar,
- fraqueza súbita ou mal-estar,
- febre,
- arrepios,
- dor de garganta,
- gengivas inflamadas,
- feridas dolorosas na boca,
- dor ao engolir,
- feridas na pele,
- sintomas de resfriado ou gripe,
- tosse,
- sentindo muita sede ou calor,
- incapacidade de urinar,
- suor intenso,
- pele quente ou seca,
- dor de estômago superior,
- coceira,
- perda de apetite,
- urina escura,
- fezes cor de barro,
- amarelecimento da pele ou dos olhos (icterícia),
- aumento da sede,
- aumento da micção,
- fome,
- boca seca,
- odor de hálito frutado,
- sonolência,
- visão embaçada,
- perda de peso,
- músculos muito rígidos,
- febre alta,
- confusão,
- batimentos cardíacos rápidos ou irregulares,
- tremores, e
- tontura
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Zyprexa incluem:
- ganho de peso (mais comum em adolescentes),
- aumento do apetite,
- dores de cabeça,
- tontura,
- sonolência,
- sentir-se cansado ou inquieto,
- problemas com a fala ou memória,
- tremores ou tremores,
- sensação de dormência ou formigamento,
- mudanças de personalidade,
- boca seca,
- salivação aumentada,
- dor de estômago,
- constipação, e
- dor em seus braços ou pernas
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Zyprexa. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
MORTALIDADE AUMENTADA EM PACIENTES IDOSOS COM PSICOSE RELACIONADA À DEMÊNCIA
Pacientes idosos com psicose relacionada à demência tratados com medicamentos antipsicóticos apresentam risco aumentado de morte. Análises de dezessete estudos controlados por placebo (duração modal de 10 semanas), em grande parte em pacientes tomando antipsicóticos atípicos, revelaram um risco de morte em pacientes tratados com drogas entre 1,6 a 1,7 vezes o risco de morte em pacientes tratados com placebo. Ao longo de um estudo controlado típico de 10 semanas, a taxa de morte em pacientes tratados com drogas foi de cerca de 4,5%, em comparação com uma taxa de cerca de 2,6% no grupo placebo. Embora as causas de morte fossem variadas, a maioria das mortes parecia ser de natureza cardiovascular (por exemplo, insuficiência cardíaca, morte súbita) ou infecciosa (por exemplo, pneumonia). Estudos observacionais sugerem que, semelhante aos antipsicóticos atípicos, o tratamento com antipsicóticos convencionais pode aumentar a mortalidade. A extensão em que os achados de aumento da mortalidade em estudos observacionais podem ser atribuídos ao medicamento antipsicótico em oposição a algumas características dos pacientes não é clara. ZYPREXA (olanzapina) não é aprovado para o tratamento de pacientes com psicose relacionada à demência [ver AVISOS E PRECAUÇÕES e INFORMAÇÃO DO PACIENTE ].
Ao usar ZYPREXA 15mg e fluoxetina em combinação, consulte também a seção Aviso na embalagem do folheto informativo do Symbyax.
DESCRIÇÃO
ZYPREXA (olanzapina) é um antipsicótico atípico que pertence à classe tienobenzodiazepina. A designação química é 2-metil-4-(4-metil-1-piperazinil)-10H-tieno[2,3-b][1,5]benzodiazepina. A fórmula molecular é C17H20N4S, que corresponde a um peso molecular de 312,44. A estrutura química é:
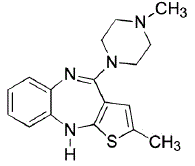
A olanzapina é um sólido cristalino amarelo, praticamente insolúvel em água.
Os comprimidos de ZYPREXA 7,5 mg destinam-se apenas à administração oral.
Cada comprimido contém olanzapina equivalente a 2,5 mg (8 μmol), 5 mg (16 μmol), 7,5 mg (24 μmol), 10 mg (32 μmol), 15 mg (48 μmol) ou 20 mg (64 μmol). Os ingredientes inativos são cera de carnaúba, crospovidona, hidroxipropilcelulose, hipromelose, lactose, estearato de magnésio, celulose microcristalina e outros ingredientes inativos. O revestimento colorido contém Dióxido de Titânio (todas as concentrações), Laca de Alumínio Azul FD&C No. 2 (15 mg) ou Óxido de Ferro Vermelho Sintético (20 mg). Os comprimidos de 2,5, 5, 7,5 e 10 mg são impressos com tinta comestível que contém FD&C Blue No. 2 Aluminum Lake.
ZYPREXA 2,5 mg ZYDIS (comprimidos de desintegração oral de olanzapina) destina-se apenas à administração oral.
Cada comprimido de desintegração oral contém olanzapina equivalente a 5 mg (16 μmol), 10 mg (32 μmol), 15 mg (48 μmol) ou 20 mg (64 μmol). Ele começa a se desintegrar na boca em segundos, permitindo que seu conteúdo seja posteriormente engolido com ou sem líquido. ZYPREXA 15mg ZYDIS (olanzapina comprimidos de desintegração oral) também contém os seguintes ingredientes inativos: gelatina, manitol, aspartame, metilparabeno sódico e propilparabeno sódico.
ZYPREXA 2,5 mg IntraMuscular (olanzapina injetável) destina-se apenas ao uso intramuscular.
Cada frasco para injetáveis prevê a administração de 10 mg (32 μmol) de olanzapina com ingredientes inativos, 50 mg de lactose monohidratada e 3,5 mg de ácido tartárico. Ácido clorídrico e/ou hidróxido de sódio podem ter sido adicionados durante a fabricação para ajustar o pH.
INDICAÇÕES
Esquizofrenia
ZYPREXA oral é indicado para o tratamento da esquizofrenia. A eficácia foi estabelecida em três ensaios clínicos em pacientes adultos com esquizofrenia: dois ensaios de 6 semanas e um ensaio de manutenção. Em pacientes adolescentes com esquizofrenia (13-17 anos), a eficácia foi estabelecida em um estudo de 6 semanas [ver Estudos clínicos ].
Ao decidir entre os tratamentos alternativos disponíveis para adolescentes, os médicos devem considerar o aumento do potencial (em adolescentes em comparação com adultos) para ganho de peso e dislipidemia. Os médicos devem considerar os riscos potenciais a longo prazo ao prescrever a adolescentes e, em muitos casos, isso pode levá-los a considerar a prescrição de outros medicamentos primeiro em adolescentes [ver AVISOS E PRECAUÇÕES ].
Transtorno Bipolar I (Episódios Maníacos ou Mistos)
Monoterapia
ZYPREXA oral é indicado para o tratamento agudo de episódios maníacos ou mistos associados ao transtorno bipolar I e tratamento de manutenção do transtorno bipolar I. A eficácia foi estabelecida em três ensaios clínicos em doentes adultos com episódios maníacos ou mistos de perturbação bipolar I: dois ensaios de 3 a 4 semanas e um ensaio de manutenção em monoterapia. Em pacientes adolescentes com episódios maníacos ou mistos associados ao transtorno bipolar I (13-17 anos), a eficácia foi estabelecida em um estudo de 3 semanas [ver Estudos clínicos ].
Ao decidir entre os tratamentos alternativos disponíveis para adolescentes, os médicos devem considerar o aumento do potencial (em adolescentes em comparação com adultos) para ganho de peso e dislipidemia. Os médicos devem considerar os riscos potenciais a longo prazo ao prescrever a adolescentes e, em muitos casos, isso pode levá-los a considerar a prescrição de outros medicamentos primeiro em adolescentes [ver AVISOS E PRECAUÇÕES ].
Terapia adjuvante ao lítio ou valproato
ZYPREXA oral 5mg é indicado para o tratamento de episódios maníacos ou mistos associados ao transtorno bipolar I como adjuvante ao lítio ou valproato. A eficácia foi estabelecida em dois ensaios clínicos de 6 semanas em adultos. A eficácia da terapia adjuvante para uso a longo prazo não foi sistematicamente avaliada em estudos controlados [ver Estudos clínicos ].
Considerações Especiais no Tratamento da Esquizofrenia Pediátrica e do Transtorno Bipolar I
esquizofrenia pediátrica e o transtorno bipolar I são transtornos mentais graves; no entanto, o diagnóstico pode ser um desafio. Para esquizofrenia pediátrica, os perfis de sintomas podem ser variáveis, e para transtorno bipolar I, pacientes pediátricos podem ter padrões variáveis de periodicidade de sintomas maníacos ou mistos. Recomenda-se que a terapia medicamentosa para esquizofrenia pediátrica e transtorno bipolar I seja iniciada somente após uma avaliação diagnóstica completa e consideração cuidadosa dos riscos associados ao tratamento medicamentoso. O tratamento medicamentoso para esquizofrenia pediátrica e transtorno bipolar I deve fazer parte de um programa de tratamento total que geralmente inclui intervenções psicológicas, educacionais e sociais.
ZYPREXA 15mg Intra Muscular: Agitação Associada à Esquizofrenia e Bipolar I Mania
ZYPREXA 15mg IntraMuscular é indicado para o tratamento da agitação aguda associada à esquizofrenia e mania bipolar I.
eficácia foi demonstrada em 3 estudos controlados por placebo de curto prazo (24 horas de tratamento IM) em pacientes adultos agitados internados com: esquizofrenia ou transtorno bipolar I (episódios maníacos ou mistos) [ver Estudos clínicos ].
“Agitação psicomotora” é definida no DSM-IV como “atividade motora excessiva associada a uma sensação de tensão interna”. Pacientes que experimentam agitação frequentemente manifestam comportamentos que interferem em seu diagnóstico e tratamento, por exemplo, comportamentos ameaçadores, comportamento crescente ou urgentemente angustiante ou comportamento autoexaustivo, levando os médicos ao uso de medicamentos antipsicóticos intramusculares para obter o controle imediato da agitação.
ZYPREXA e fluoxetina em combinação: episódios depressivos associados ao transtorno bipolar I
ZYPREXA oral e fluoxetina em combinação é indicado para o tratamento de episódios depressivos associados ao transtorno bipolar I, com base em estudos clínicos. Ao usar ZYPREXA 10mg e fluoxetina em combinação, consulte a seção de Estudos Clínicos do folheto informativo do Symbyax.
A monoterapia com ZYPREXA não é indicada para o tratamento de episódios depressivos associados ao transtorno bipolar I.
ZYPREXA e fluoxetina em combinação: depressão resistente ao tratamento
ZYPREXA oral e fluoxetina em combinação é indicado para o tratamento da depressão resistente ao tratamento (transtorno depressivo maior em pacientes que não respondem a 2 ensaios separados de diferentes antidepressivos de dose e duração adequadas no episódio atual), com base em estudos clínicos em pacientes adultos . Ao usar ZYPREXA e fluoxetina em combinação, consulte a seção de Estudos Clínicos do folheto informativo do Symbyax.
monoterapia com ZYPREXA 5mg não é indicada para o tratamento da depressão resistente ao tratamento.
DOSAGEM E ADMINISTRAÇÃO
Esquizofrenia
Adultos
Seleção de Dose
A olanzapina oral deve ser administrada uma vez ao dia, independentemente das refeições, geralmente começando com 5 a 10 mg inicialmente, com uma dose alvo de 10 mg/dia em vários dias. Ajustes de dose adicionais, se indicados, geralmente devem ocorrer em intervalos não inferiores a 1 semana, uma vez que o estado de equilíbrio da olanzapina não seria alcançado por aproximadamente 1 semana no paciente típico. Quando são necessários ajustes de dose, são recomendados aumentos/diminuições de dose de 5 mg QD.
eficácia na esquizofrenia foi demonstrada em uma faixa de dose de 10 a 15 mg/dia em ensaios clínicos. No entanto, doses acima de 10 mg/dia não demonstraram ser mais eficazes do que a dose de 10 mg/dia. Um aumento para uma dose superior à dose alvo de 10 mg/dia (ou seja, para uma dose de 15 mg/dia ou superior) é recomendado somente após avaliação clínica. A olanzapina não é indicada para uso em doses acima de 20 mg/dia.
Dosagem em Populações Especiais
A dose inicial recomendada é de 5 mg em pacientes debilitados, com predisposição a reações hipotensivas, que exibem uma combinação de fatores que podem resultar em metabolismo mais lento da olanzapina (p. que podem ser farmacodinamicamente mais sensíveis à olanzapina [ver AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS , e FARMACOLOGIA CLÍNICA ]. Quando indicado, o aumento da dose deve ser realizado com cautela nesses pacientes.
Tratamento de manutenção
eficácia da olanzapina oral, 10 mg/dia a 20 mg/dia, na manutenção da resposta ao tratamento em pacientes esquizofrênicos que permaneceram estáveis com ZYPREXA por aproximadamente 8 semanas e foram então acompanhados para recidiva foi demonstrada em um estudo controlado por placebo [ver Estudos clínicos ]. O profissional de saúde que optar por usar ZYPREXA por períodos prolongados deve reavaliar periodicamente a utilidade a longo prazo do medicamento para o paciente individual.
Adolescentes
Seleção de Dose
A olanzapina oral deve ser administrada uma vez ao dia, independentemente das refeições, com uma dose inicial recomendada de 2,5 ou 5 mg, com uma dose alvo de 10 mg/dia. A eficácia em adolescentes com esquizofrenia foi demonstrada com base em um intervalo de dose flexível de 2,5 a 20 mg/dia em ensaios clínicos, com uma dose modal média de 12,5 mg/dia (dose média de 11,1 mg/dia). Quando são necessários ajustes de dose, são recomendados aumentos/diminuições de dose de 2,5 ou 5 mg.
segurança e eficácia de doses acima de 20 mg/dia não foram avaliadas em ensaios clínicos [ver Estudos clínicos ].
Tratamento de manutenção
A eficácia de ZYPREXA para o tratamento de manutenção da esquizofrenia na população adolescente não foi sistematicamente avaliada; no entanto, a eficácia de manutenção pode ser extrapolada a partir de dados de adultos juntamente com comparações dos parâmetros farmacocinéticos da olanzapina em pacientes adultos e adolescentes. Assim, geralmente é recomendado que os pacientes responsivos continuem além da resposta aguda, mas na dose mais baixa necessária para manter a remissão. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção.
Transtorno Bipolar I (Episódios Maníacos ou Mistos)
Adultos
Seleção de dose para monoterapia
olanzapina oral deve ser administrada uma vez ao dia, independentemente das refeições, geralmente começando com 10 ou 15 mg. Os ajustes de dose, se indicados, geralmente devem ocorrer em intervalos não inferiores a 24 horas, refletindo os procedimentos dos estudos controlados por placebo. Quando são necessários ajustes de dose, são recomendados aumentos/diminuições de dose de 5 mg QD.
A eficácia antimaníaca de curto prazo (3-4 semanas) foi demonstrada em uma faixa de dose de 5 mg a 20 mg/dia em ensaios clínicos. A segurança de doses acima de 20 mg/dia não foi avaliada em ensaios clínicos [ver Estudos clínicos ].
Monoterapia de Manutenção
O benefício de manter pacientes bipolares I em monoterapia com ZYPREXA 10mg oral na dose de 5 a 20 mg/dia, após atingir um status de resposta por uma duração média de 2 semanas, foi demonstrado em um estudo controlado [ver Estudos clínicos ]. O profissional de saúde que optar por usar ZYPREXA por períodos prolongados deve reavaliar periodicamente a utilidade a longo prazo do medicamento para o paciente individual.
Seleção de dose para tratamento adjuvante
Quando administrado como tratamento adjuvante ao lítio ou valproato, a dosagem oral de olanzapina deve geralmente começar com 10 mg uma vez ao dia, independentemente das refeições.
A eficácia antimaníaca foi demonstrada em uma faixa de dose de 5 mg a 20 mg/dia em ensaios clínicos [ver Estudos clínicos ]. A segurança de doses acima de 20 mg/dia não foi avaliada em ensaios clínicos.
Adolescentes
Seleção de Dose
olanzapina oral deve ser administrada uma vez ao dia, independentemente das refeições, com uma dose inicial recomendada de 2,5 ou 5 mg, com uma dose alvo de 10 mg/dia. A eficácia em adolescentes com transtorno bipolar I (episódios maníacos ou mistos) foi demonstrada com base em uma faixa de dose flexível de 2,5 a 20 mg/dia em ensaios clínicos, com uma dose modal média de 10,7 mg/dia (dose média de 8,9 mg/dia ). Quando são necessários ajustes de dose, são recomendados aumentos/diminuições de dose de 2,5 ou 5 mg.
A segurança e eficácia de doses acima de 20 mg/dia não foram avaliadas em ensaios clínicos [ver Estudos clínicos ].
Tratamento de manutenção
eficácia de ZYPREXA 7,5mg para o tratamento de manutenção do transtorno bipolar I na população adolescente não foi avaliada; no entanto, a eficácia de manutenção pode ser extrapolada a partir de dados de adultos juntamente com comparações dos parâmetros farmacocinéticos da olanzapina em pacientes adultos e adolescentes. Assim, geralmente é recomendado que os pacientes responsivos continuem além da resposta aguda, mas na dose mais baixa necessária para manter a remissão. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção.
Administração de ZYPREXA ZYDIS (comprimidos de desintegração oral de olanzapina)
Depois de abrir a saqueta, retire a película do blister. Não empurre o comprimido através do papel alumínio. Imediatamente após a abertura do blister, com as mãos secas, retire o comprimido e coloque todo o ZYPREXA 15mg ZYDIS na boca. A desintegração do comprimido ocorre rapidamente na saliva para que possa ser facilmente engolido com ou sem líquido.
ZYPREXA Intra Muscular: Agitação Associada à Esquizofrenia e Bipolar I Mania
Seleção de dose para pacientes adultos agitados com esquizofrenia e mania bipolar I
A eficácia da olanzapina intramuscular para injeção no controle da agitação nesses distúrbios foi demonstrada em uma faixa de dose de 2,5 mg a 10 mg. A dose recomendada nestes doentes é de 10 mg. Uma dose mais baixa de 5 ou 7,5 mg pode ser considerada quando os fatores clínicos justificarem [ver Estudos clínicos ]. Se a agitação que justifica doses intramusculares adicionais persistir após a dose inicial, doses subsequentes de até 10 mg podem ser administradas. No entanto, a eficácia de doses repetidas de olanzapina intramuscular para injeção em pacientes agitados não foi sistematicamente avaliada em ensaios clínicos controlados. Além disso, a segurança de doses diárias totais superiores a 30 mg ou injeções de 10 mg administradas com mais frequência do que 2 horas após a dose inicial e 4 horas após a segunda dose não foi avaliada em ensaios clínicos. A dosagem máxima de olanzapina intramuscular (por exemplo, 3 doses de 10 mg administradas com 2-4 horas de intervalo) pode estar associada a uma ocorrência substancial de hipotensão ortostática significativa [ver AVISOS E PRECAUÇÕES ]. Assim, recomenda-se que os pacientes que necessitam de injeções intramusculares subsequentes sejam avaliados quanto à hipotensão ortostática antes da administração de quaisquer doses subsequentes de olanzapina intramuscular para injeção. A administração de uma dose adicional a um paciente com alteração postural clinicamente significativa na pressão arterial sistólica não é recomendada.
Se a terapia contínua com olanzapina for clinicamente indicada, a olanzapina oral pode ser iniciada na faixa de 5-20 mg/dia assim que clinicamente apropriado [ver Esquizofrenia e Transtorno Bipolar I (Episódios Maníacos ou Mistos) ].
Dosagem Intramuscular em Populações Especiais
Uma dose de 5 mg/injeção deve ser considerada para pacientes geriátricos ou quando outros fatores clínicos o justifiquem. Uma dose mais baixa de 2,5 mg/injeção deve ser considerada para pacientes que de outra forma poderiam estar debilitados, predispostos a reações hipotensivas ou serem mais sensíveis farmacodinamicamente à olanzapina [ver AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS , e FARMACOLOGIA CLÍNICA ].
Administração de ZYPREXA Intra Muscular
ZYPREXA Intra Muscular destina-se apenas ao uso intramuscular. Não administrar por via intravenosa ou subcutânea. Injete lentamente, profundamente na massa muscular. Os medicamentos parenterais devem ser inspecionados visualmente quanto a partículas e descoloração antes da administração, sempre que a solução e o recipiente permitirem.
Instruções para preparação de ZYPREXA 2,5mg intramuscular com água estéril para injeção
Dissolva o conteúdo do frasco usando 2,1 mL de água estéril para injeção para fornecer uma solução contendo aproximadamente 5 mg/mL de olanzapina. A solução resultante deve parecer límpida e amarela. ZYPREXA 7,5 mg intramuscular reconstituído com água estéril para injeção deve ser usado imediatamente (dentro de 1 hora) após a reconstituição. Descarte qualquer porção não utilizada.
A tabela a seguir fornece os volumes de injeção para administração de várias doses de olanzapina intramuscular para injeção reconstituída com água estéril para injeção.
Informações de incompatibilidade física
ZYPREXA 15mg IntraMuscular deve ser reconstituído apenas com água estéril para injeção. ZYPREXA 20mg IntraMuscular não deve ser combinado em uma seringa com injeção de diazepam porque ocorre precipitação quando esses produtos são misturados. A injeção de lorazepam não deve ser usada para reconstituir ZYPREXA IntraMuscular, pois esta combinação resulta em um atraso no tempo de reconstituição. ZYPREXA IntraMuscular não deve ser combinado em uma seringa com injeção de haloperidol porque o pH baixo resultante demonstrou degradar a olanzapina ao longo do tempo.
ZYPREXA 20mg e fluoxetina em combinação: episódios depressivos associados ao transtorno bipolar I
Ao usar ZYPREXA 7,5 mg e fluoxetina em combinação, consulte também a seção de Estudos Clínicos do folheto informativo do Symbyax.
Adultos
olanzapina oral deve ser administrada em combinação com fluoxetina uma vez ao dia à noite, independentemente das refeições, geralmente começando com 5 mg de olanzapina oral e 20 mg de fluoxetina. Ajustes de dose, se indicados, podem ser feitos de acordo com a eficácia e tolerabilidade dentro dos intervalos de dose de olanzapina oral 5 a 12,5 mg e fluoxetina 20 a 50 mg. A eficácia antidepressiva foi demonstrada com ZYPREXA 10 mg e fluoxetina em combinação em pacientes adultos com uma faixa de dose de olanzapina 6 a 12 mg e fluoxetina 25 a 50 mg. A segurança da administração concomitante de doses acima de 18 mg de olanzapina com 75 mg de fluoxetina não foi avaliada em estudos clínicos.
Crianças e Adolescentes (10-17 anos)
olanzapina oral deve ser administrada em combinação com fluoxetina uma vez ao dia à noite, independentemente das refeições, geralmente começando com 2,5 mg de olanzapina oral e 20 mg de fluoxetina. Ajustes de dosagem, se indicados, podem ser feitos de acordo com a eficácia e tolerabilidade. A segurança da administração concomitante de doses acima de 12 mg de olanzapina com 50 mg de fluoxetina não foi avaliada em estudos clínicos pediátricos.
A segurança e eficácia de ZYPREXA e fluoxetina em combinação foram determinadas em ensaios clínicos que apoiam a aprovação de Symbyax (combinação de dose fixa de ZYPREXA e fluoxetina). Symbyax é administrado entre 3 mg/25 mg (olanzapina/fluoxetina) por dia e 12 mg/50 mg (olanzapina/fluoxetina) por dia. A tabela a seguir demonstra as doses de componentes individuais apropriadas de ZYPREXA 10mg e fluoxetina versus Symbyax. Ajustes de dosagem, se indicados, devem ser feitos com os componentes individuais de acordo com a eficácia e tolerabilidade.
Embora não haja evidências para responder à questão de quanto tempo um paciente tratado com ZYPREXA e fluoxetina em combinação deve permanecer com o medicamento, é geralmente aceito que o transtorno bipolar I, incluindo os episódios depressivos associados ao transtorno bipolar I, é uma doença crônica doença que requer tratamento crônico. O profissional de saúde deve reexaminar periodicamente a necessidade de continuação da farmacoterapia.
A monoterapia com ZYPREXA 5mg não é indicada para o tratamento de episódios depressivos associados ao transtorno bipolar I.
ZYPREXA 7,5 mg e fluoxetina em combinação: depressão resistente ao tratamento
Ao usar ZYPREXA e fluoxetina em combinação, consulte também a seção de Estudos Clínicos do folheto informativo do Symbyax.
olanzapina oral deve ser administrada em combinação com fluoxetina uma vez ao dia à noite, independentemente das refeições, geralmente começando com 5 mg de olanzapina oral e 20 mg de fluoxetina. Ajustes de dosagem, se indicados, podem ser feitos de acordo com a eficácia e tolerabilidade dentro dos intervalos de dose de olanzapina oral 5 a 20 mg e fluoxetina 20 a 50 mg. A eficácia antidepressiva foi demonstrada com olanzapina e fluoxetina em combinação em pacientes adultos com uma faixa de dose de olanzapina de 6 a 18 mg e fluoxetina de 25 a 50 mg.
segurança e a eficácia da olanzapina em combinação com a fluoxetina foram determinadas em ensaios clínicos que apoiam a aprovação de Symbyax (combinação de dose fixa de olanzapina e fluoxetina). Symbyax é administrado entre 3 mg/25 mg (olanzapina/fluoxetina) por dia e 12 mg/50 mg (olanzapina/fluoxetina) por dia. A Tabela 1 acima demonstra as doses apropriadas de componentes individuais de ZYPREXA e fluoxetina versus Symbyax. Ajustes de dosagem, se indicados, devem ser feitos com os componentes individuais de acordo com a eficácia e tolerabilidade.
Embora não haja evidências para responder à questão de quanto tempo um paciente tratado com ZYPREXA e fluoxetina em combinação deve permanecer com ele, é geralmente aceito que a depressão resistente ao tratamento (transtorno depressivo maior em pacientes adultos que não respondem a 2 ensaios de diferentes antidepressivos de dose e duração adequadas no episódio atual) é uma doença crônica que requer tratamento crônico. O profissional de saúde deve reexaminar periodicamente a necessidade de continuação da farmacoterapia.
A segurança da administração concomitante de doses acima de 18 mg de olanzapina com 75 mg de fluoxetina não foi avaliada em estudos clínicos.
ZYPREXA 7,5 mg em monoterapia não é indicado para o tratamento da depressão resistente ao tratamento (transtorno depressivo maior em pacientes que não respondem a 2 antidepressivos de dose e duração adequadas no episódio atual).
ZYPREXA 10mg e fluoxetina em combinação: dosagem em populações especiais
dose inicial de olanzapina oral 2,5-5 mg com fluoxetina 20 mg deve ser usada para pacientes com predisposição a reações hipotensivas, pacientes com insuficiência hepática ou pacientes que apresentam uma combinação de fatores que podem retardar o metabolismo de olanzapina ou fluoxetina em combinação (sexo feminino, idade geriátrica, status de não fumante), ou aqueles pacientes que podem ser farmacodinamicamente sensíveis à olanzapina. A modificação da dosagem pode ser necessária em pacientes que apresentam uma combinação de fatores que podem retardar o metabolismo. Quando indicado, o aumento da dose deve ser realizado com cautela nesses pacientes. ZYPREXA e fluoxetina em combinação não foram sistematicamente estudados em pacientes com mais de 65 anos de idade ou em pacientes com menos de 10 anos de idade [ver AVISOS E PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS , e FARMACOLOGIA CLÍNICA ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
Os comprimidos de ZYPREXA 2,5 mg, 5 mg, 7,5 mg e 10 mg são brancos, redondos e impressos em tinta azul com LILLY e o número do comprimido. Os comprimidos de 15 mg são elípticos, azuis e gravados com LILLY e o número do comprimido. Os comprimidos de 20 mg são elípticos, cor-de-rosa e gravados com LILLY e o número do comprimido. Os comprimidos não são pontuados. Os comprimidos estão disponíveis da seguinte forma:
ZYPREXA 10mg ZYDIS (comprimidos de desintegração oral de olanzapina) são amarelos, redondos e gravados com a dosagem do comprimido. Os comprimidos não são pontuados. Os comprimidos estão disponíveis da seguinte forma:
ZYPREXA 15mg intramuscular está disponível em frascos de 10 mg (1s).
Os comprimidos de ZYPREXA 2,5 mg, 5 mg, 7,5 mg e 10 mg são brancos, redondos e impressos em tinta azul com LILLY e o número do comprimido. Os comprimidos de 15 mg são elípticos, azuis e gravados com LILLY e o número do comprimido. Os comprimidos de 20 mg são elípticos, cor-de-rosa e gravados com LILLY e o número do comprimido. Os comprimidos estão disponíveis da seguinte forma:
ZYPREXA 2,5mg ZYDIS (comprimidos de desintegração oral de olanzapina) são amarelos, redondos e gravados com a dosagem do comprimido. Os comprimidos estão disponíveis da seguinte forma:
ZYPREXA Intramuscular está disponível em:
NDC 0002-7597-01 (Nº VL7597) - frasco de 10 mg (1s)
Armazenamento e manuseio
Armazene os comprimidos de ZYPREXA, ZYPREXA ZYDIS e frascos de ZYPREXA IntraMuscular (antes da reconstituição) em temperatura ambiente controlada, 20° a 25°C (68° a 77°F) [ver USP ]. O ZYPREXA 20mg IntraMuscular reconstituído pode ser armazenado em temperatura ambiente controlada, 20° a 25°C (68° a 77°F) [ver USP por até 1 hora, se necessário. Descarte qualquer porção não utilizada de ZYPREXA IntraMuscular reconstituído. A USP define temperatura ambiente controlada como uma temperatura mantida termostaticamente que abrange o ambiente de trabalho usual e habitual de 20° a 25°C (68° a 77°F); que resulte em uma temperatura cinética média calculada não superior a 25°C; e que permite excursões entre 15° e 30°C (59° e 86°F) que são experimentadas em farmácias, hospitais e armazéns.
Proteja os comprimidos ZYPREXA e ZYPREXA ZYDIS da luz e da umidade. Proteja o ZYPREXA IntraMuscular da luz, não congele.
Comercializado por: Lilly USA, LLC, Indianápolis, IN 46285, EUA. Revisado: outubro de 2019
EFEITOS COLATERAIS
Ao usar ZYPREXA 2,5 mg e fluoxetina em combinação, consulte também a seção Reações Adversas do folheto informativo do Symbyax.
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos sob condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos ensaios clínicos de outro medicamento e podem não refletir ou prever as taxas observadas na prática.
Ensaios Clínicos em Adultos
As informações abaixo para a olanzapina são derivadas de um banco de dados de ensaios clínicos para a olanzapina consistindo de 10.504 pacientes adultos com aproximadamente 4.765 pacientes-ano de exposição à olanzapina mais 722 pacientes com exposição à olanzapina intramuscular para injeção. Esse banco de dados inclui: (1) 2.500 pacientes que participaram de ensaios de pré-comercialização de olanzapina oral com doses múltiplas em esquizofrenia e doença de Alzheimer, representando aproximadamente 1.122 pacientes-ano de exposição em 14 de fevereiro de 1995; (2) 182 pacientes que participaram de estudos pré-comercialização de transtorno bipolar I de olanzapina oral (episódios maníacos ou mistos), representando aproximadamente 66 pacientes-ano de exposição; (3) 191 pacientes que participaram de um estudo de olanzapina oral de pacientes com vários sintomas psiquiátricos associados à doença de Alzheimer, representando aproximadamente 29 pacientes-ano de exposição; (4) 5.788 pacientes adicionais de 88 ensaios clínicos de olanzapina oral em 31 de dezembro de 2001; (5) 1.843 pacientes adicionais de 41 ensaios clínicos de olanzapina em 31 de outubro de 2011; e (6) 722 pacientes que participaram de ensaios de pré-comercialização de olanzapina intramuscular para injeção em pacientes agitados com esquizofrenia, transtorno bipolar I (episódios maníacos ou mistos) ou demência. Também estão incluídas abaixo informações do banco de dados de estudos clínicos de 6 semanas de pré-comercialização para olanzapina em combinação com lítio ou valproato, consistindo de 224 pacientes que participaram de estudos de transtorno bipolar I (episódios maníacos ou mistos) com aproximadamente 22 pacientes-ano de exposição.
As condições e a duração do tratamento com olanzapina variaram muito e incluíram (em categorias sobrepostas) fases de estudos abertos e duplo-cegos, pacientes internados e ambulatoriais, estudos de dose fixa e titulação de dose e exposição de curto ou longo prazo . As reações adversas foram avaliadas pela coleta de reações adversas, resultados de exames físicos, sinais vitais, pesos, análises laboratoriais, ECGs, radiografias de tórax e resultados de exames oftalmológicos.
Certas partes da discussão abaixo relacionadas a parâmetros de segurança objetivos ou numéricos, a saber, reações adversas dependentes da dose, alterações de sinais vitais, ganho de peso, alterações laboratoriais e alterações de ECG são derivadas de estudos em pacientes com esquizofrenia e não foram duplicadas para transtorno bipolar I (episódios maníacos ou mistos) ou agitação. No entanto, esta informação também é geralmente aplicável ao transtorno bipolar I (episódios maníacos ou mistos) e agitação.
As reações adversas durante a exposição foram obtidas por notificação espontânea e registradas por investigadores clínicos usando terminologia de sua própria escolha. Consequentemente, não é possível fornecer uma estimativa significativa da proporção de indivíduos que apresentam reações adversas sem primeiro agrupar tipos semelhantes de reações em um número menor de categorias de reações padronizadas. Nas tabelas e tabulações que se seguem, a terminologia do Dicionário MedDRA e COSTART foi utilizada para classificar as reações adversas notificadas.
As frequências declaradas de reações adversas representam a proporção de indivíduos que sofreram, pelo menos uma vez, uma reação adversa emergente do tratamento do tipo listado. Uma reação foi considerada emergente do tratamento se ocorreu pela primeira vez ou piorou durante o tratamento após a avaliação inicial. As reações relatadas não incluem os termos de reação que foram tão gerais que não foram informativos. As reações listadas em outras partes do rótulo não podem ser repetidas abaixo. É importante ressaltar que, embora as reações tenham ocorrido durante o tratamento com olanzapina, não necessariamente foram causadas por ela. O rótulo inteiro deve ser lido para obter uma compreensão completa do perfil de segurança da olanzapina.
prescritor deve estar ciente de que os números das tabelas e tabulações não podem ser usados para prever a incidência de efeitos colaterais no curso da prática médica habitual, onde as características do paciente e outros fatores diferem daqueles que prevaleceram nos ensaios clínicos. Da mesma forma, as frequências citadas não podem ser comparadas com números obtidos de outras investigações clínicas envolvendo diferentes tratamentos, usos e pesquisadores. Os números citados, no entanto, fornecem ao médico prescritor alguma base para estimar a contribuição relativa de fatores medicamentosos e não medicamentosos para a incidência de reações adversas na população estudada.
Incidência de reações adversas em ensaios de curto prazo, controlados por placebo e de combinação
Os achados a seguir são baseados em estudos pré-comercialização de (1) olanzapina oral para esquizofrenia, transtorno bipolar I (episódios maníacos ou mistos), um estudo subsequente de pacientes com vários sintomas psiquiátricos associados à doença de Alzheimer e estudos combinados pré-comercialização e (2 ) olanzapina intramuscular para injeção em pacientes agitados com esquizofrenia ou mania bipolar I.
Reações Adversas Associadas à Descontinuação do Tratamento em Ensaios de Curto Prazo Controlados por Placebo
Esquizofrenia
No geral, não houve diferença na incidência de descontinuação devido a reações adversas (5% para olanzapina oral versus 6% para placebo). No entanto, as descontinuações devido a aumentos na ALT foram consideradas relacionadas ao medicamento (2% para olanzapina oral versus 0% para placebo).
Transtorno Bipolar I (Episódios Maníacos ou Mistos) Monoterapia
No geral, não houve diferença na incidência de descontinuação devido a reações adversas (2% para olanzapina oral versus 2% para placebo).
Agitação
No geral, não houve diferença na incidência de descontinuação devido a reações adversas (0,4% para olanzapina intramuscular para injeção versus 0% para placebo).
Reações Adversas Associadas à Descontinuação do Tratamento em Ensaios de Combinação de Curto Prazo
Transtorno Bipolar I (Episódios Maníacos ou Mistos), Olanzapina Como Adjuvante ao Lítio ou Valproato
Em um estudo de pacientes que já toleravam lítio ou valproato como monoterapia, as taxas de descontinuação devido a reações adversas foram de 11% para a combinação de olanzapina oral com lítio ou valproato em comparação com 2% para pacientes que permaneceram em monoterapia com lítio ou valproato. As interrupções com a combinação de olanzapina oral e lítio ou valproato que ocorreram em mais de 1 paciente foram: sonolência (3%), ganho de peso (1%) e edema periférico (1%).
Reações Adversas Comumente Observadas em Ensaios de Curto Prazo Controlados por Placebo
As reações adversas mais comumente observadas associadas ao uso de olanzapina oral (incidência de 5% ou mais) e não observadas em uma incidência equivalente entre os pacientes tratados com placebo (incidência de olanzapina pelo menos duas vezes a do placebo) foram:
Olanzapina Intramuscular
Houve 1 reação adversa (sonolência) observada em uma incidência de 5% ou mais entre olanzapina intramuscular para pacientes tratados com injeção e não observada em uma incidência equivalente entre os pacientes tratados com placebo (incidência de olanzapina pelo menos duas vezes a do placebo) durante o placebo -estudos de pré-comercialização controlados. A incidência de sonolência durante o período de tratamento de 24 horas IM em ensaios clínicos em pacientes agitados com esquizofrenia ou mania bipolar I foi de 6% para olanzapina intramuscular para injeção e 3% para placebo.
Reações adversas que ocorrem com uma incidência de 2% ou mais entre pacientes tratados com olanzapina oral em estudos de curto prazo controlados por placebo
Tabela 11 enumera a incidência, arredondada para o percentual mais próximo, de reações adversas emergentes do tratamento que ocorreram em 2% ou mais dos pacientes tratados com olanzapina oral (doses ≥2,5 mg/dia) e com incidência maior do que placebo que participaram do tratamento agudo fase de ensaios controlados por placebo.
Dependência de Dose de Reações Adversas
Uma diferença de grupo de dose foi observada para fadiga, tontura, ganho de peso e elevação de prolactina. Em um único estudo randomizado, duplo-cego, de dose fixa de 8 semanas comparando 10 (N=199), 20 (N=200) e 40 (N=200) mg/dia de olanzapina oral em pacientes adultos com esquizofrenia ou esquizoafetiva distúrbio, a incidência de fadiga (10 mg/dia: 1,5%; 20 mg/dia: 2,1%; 40 mg/dia: 6,6%) foi observada com diferenças significativas entre 10 vs 40 e 20 vs 40 mg/dia. A incidência de tontura (10 mg/dia: 2,6%; 20 mg/dia: 1,6%; 40 mg/dia: 6,6%) foi observada com diferenças significativas entre 20 vs 40 mg. As diferenças entre os grupos de dose também foram observadas para ganho de peso e elevação de prolactina [ver AVISOS E PRECAUÇÕES ].
tabela a seguir aborda a relação de dose para outras reações adversas usando dados de um estudo de esquizofrenia envolvendo faixas de dosagem fixas de olanzapina oral. Ele enumera a porcentagem de pacientes com reações adversas emergentes do tratamento para os 3 grupos de faixa de dose fixa e placebo. Os dados foram analisados pelo teste de Cochran-Armitage, excluindo o grupo placebo, e a tabela inclui apenas as reações adversas para as quais houve tendência.
Reações adversas comumente observadas em ensaios de curto prazo de olanzapina oral como adjuvante ao lítio ou valproato
Nos estudos adjuntos controlados por placebo para transtorno bipolar I (episódios maníacos ou mistos), as reações adversas mais comumente observadas associadas à combinação de olanzapina e lítio ou valproato (incidência ≥5% e pelo menos duas vezes placebo) foram:
Reações adversas que ocorrem com uma incidência de 2% ou mais entre pacientes tratados com olanzapina oral em ensaios de curto prazo de olanzapina como adjuvante ao lítio ou valproato
A Tabela 14 enumera a incidência, arredondada para o percentual mais próximo, de reações adversas emergentes do tratamento que ocorreram em 2% ou mais dos pacientes tratados com a combinação de olanzapina (doses ≥5 mg/dia) e lítio ou valproato e com incidência maior que lítio ou valproato sozinhos que participaram da fase aguda de ensaios de combinação controlados por placebo.
Para obter informações específicas sobre as reações adversas observadas com lítio ou valproato, consulte a seção Reações Adversas das bulas desses outros produtos.
Reações adversas que ocorrem com uma incidência de 1% ou mais entre olanzapina intramuscular para pacientes tratados com injeção em ensaios de curto prazo controlados por placebo
Tabela 15 enumera a incidência, arredondada para o percentual mais próximo, de reações adversas emergentes do tratamento que ocorreram em 1% ou mais dos pacientes tratados com olanzapina intramuscular para injeção (intervalo de dose de 2,5-10 mg/injeção) e com incidência maior do que placebo que participaram de estudos controlados por placebo de curto prazo em pacientes agitados com esquizofrenia ou mania bipolar I.
Sintomas extrapiramidais
A tabela a seguir enumera a porcentagem de pacientes com sintomas extrapiramidais emergentes do tratamento, conforme avaliado por análises categóricas de escalas formais de classificação durante a terapia aguda em um ensaio clínico controlado comparando olanzapina oral em 3 doses fixas com placebo no tratamento da esquizofrenia em um período de 6 semanas tentativas.
tabela a seguir enumera a porcentagem de pacientes com sintomas extrapiramidais emergentes do tratamento, conforme avaliado por reações adversas relatadas espontaneamente durante a terapia aguda no mesmo ensaio clínico controlado comparando olanzapina em 3 doses fixas com placebo no tratamento da esquizofrenia em um estudo de 6 semanas.
A tabela a seguir enumera a porcentagem de pacientes adolescentes com sintomas extrapiramidais emergentes do tratamento, conforme avaliado por reações adversas relatadas espontaneamente durante a terapia aguda (intervalo de dose: 2,5 a 20 mg/dia).
A tabela a seguir enumera a porcentagem de pacientes com sintomas extrapiramidais emergentes do tratamento, conforme avaliado por análises categóricas de escalas formais de classificação durante ensaios clínicos controlados comparando doses fixas de olanzapina intramuscular para injeção com placebo em agitação. Os pacientes em cada grupo de dose podem receber até 3 injeções durante os ensaios [ver Estudos clínicos ]. As avaliações dos pacientes foram realizadas durante as 24 horas após a dose inicial de olanzapina intramuscular para injeção.
A tabela a seguir enumera a porcentagem de pacientes com sintomas extrapiramidais emergentes do tratamento, conforme avaliado por reações adversas relatadas espontaneamente no mesmo ensaio clínico controlado, comparando doses fixas de olanzapina intramuscular para injeção com placebo em pacientes agitados com esquizofrenia.
Distonia, Efeito de Classe
Sintomas de distonia, contrações anormais prolongadas de grupos musculares, podem ocorrer em indivíduos suscetíveis durante os primeiros dias de tratamento. Os sintomas distônicos incluem: espasmo dos músculos do pescoço, algumas vezes progredindo para aperto na garganta, dificuldade para engolir, dificuldade para respirar e/ou protrusão da língua. Embora esses sintomas possam ocorrer em doses baixas, a frequência e a gravidade são maiores com alta potência e em doses mais altas de medicamentos antipsicóticos de primeira geração. Em geral, um risco elevado de distonia aguda pode ser observado em homens e grupos etários mais jovens recebendo antipsicóticos; no entanto, eventos de distonia foram relatados com pouca frequência (
Outras reações adversas
Outras reações adversas observadas durante a avaliação do ensaio clínico de olanzapina oral
seguir está uma lista de reações adversas emergentes do tratamento relatadas por pacientes tratados com olanzapina oral (em doses múltiplas ≥1 mg/dia) em estudos clínicos. Esta lista não pretende incluir reações (1) já listadas em tabelas anteriores ou em qualquer outro lugar na bula, (2) para as quais a causa do medicamento era remota, (3) que eram tão gerais que não eram informativas, (4) que não eram considerados como tendo implicações clínicas significativas, ou (5) que ocorreram a uma taxa igual ou inferior ao placebo. As reações são classificadas por sistema corporal usando as seguintes definições: reações adversas frequentes são aquelas que ocorrem em pelo menos 1/100 pacientes; reações adversas infrequentes são aquelas que ocorrem em 1/100 a 1/1.000 pacientes; reações raras são aquelas que ocorrem em menos de 1/1.000 pacientes.
Corpo como um todo - Infrequentes: calafrios, edema facial, reação de fotossensibilidade, tentativa de suicídio1; Raros: calafrios e febre, efeito de ressaca, morte súbita1.
Sistema cardiovascular - Infrequentes: acidente vascular cerebral, vasodilatação.
Sistema digestivo - Infrequentes: distensão abdominal, náuseas e vômitos, edema de língua; Raros: íleo, obstrução intestinal, depósito de gordura no fígado.
Sistema Hemico e Linfático - Infrequente: trombocitopenia.
Distúrbios metabólicos e nutricionais - Frequentes: aumento da fosfatase alcalina; Infrequentes: bilirrubinemia, hipoproteinemia.
Sistema musculo-esquelético - Raros: osteoporose.
Sistema nervoso - Infrequentes: ataxia, disartria, diminuição da libido, estupor; Raro: coma.
Sistema respiratório - Infrequente: epistaxe; Raros: edema pulmonar.
Pele e Anexos - Infrequente: alopecia.
Sentidos Especiais - Infrequente: anormalidade de acomodação, olhos secos; Raros: midríase.
Sistema Urogenital - Infrequentes: amenorreia2, dor mamária, menstruação diminuída, impotência2, menstruação aumentada2, menorragia2, metrorragia2, poliúria2, frequência urinária, retenção urinária, urgência urinária, dificuldade para urinar.
1 Esses termos representam eventos adversos graves, mas não atendem à definição de reações adversas a medicamentos. Eles estão incluídos aqui por causa de sua seriedade. 2 Ajustado por gênero.
Outras reações adversas observadas durante a avaliação do ensaio clínico de olanzapina intramuscular para injeção
A seguir está uma lista de reações adversas emergentes do tratamento relatadas por pacientes tratados com olanzapina intramuscular para injeção (em 1 ou mais doses ≥2,5 mg/injeção) em estudos clínicos. Esta lista não pretende incluir reações (1) já listadas em tabelas anteriores ou em qualquer outro lugar na bula, (2) para as quais a causa do medicamento era remota, (3) que eram tão gerais que não eram informativas, (4) que não eram considerados como tendo implicações clínicas significativas, ou (5) para os quais ocorreram em uma taxa igual ou inferior ao placebo. As reações são classificadas por sistema corporal usando as seguintes definições: reações adversas frequentes são aquelas que ocorrem em pelo menos 1/100 pacientes; reações adversas infrequentes são aquelas que ocorrem em 1/100 a 1/1.000 pacientes.
Corpo como um todo - Frequentes: dor no local da injeção.
Sistema cardiovascular - Infrequente: síncope.
Sistema digestivo - Infrequente: náusea.
Distúrbios metabólicos e nutricionais - Infrequente: aumento da creatina fosfoquinase.
Ensaios Clínicos em Pacientes Adolescentes (13 a 17 anos)
Reações Adversas Comumente Observadas em Ensaios Orais de Curto Prazo com Olanzapina, Controlados por Placebo
As reações adversas em pacientes adolescentes tratados com olanzapina oral (doses ≥2,5 mg) relatadas com incidência de 5% ou mais e relatadas com pelo menos duas vezes mais frequência do que pacientes tratados com placebo estão listadas na Tabela 21.
Reações adversas que ocorrem com uma incidência de 2% ou mais entre pacientes tratados com olanzapina oral em curto prazo (3-6 semanas), ensaios controlados por placebo
As reações adversas em pacientes adolescentes tratados com olanzapina oral (doses ≥2,5 mg) relatadas com uma incidência de 2% ou mais e maior que o placebo estão listadas na Tabela 22.
Sinais vitais e estudos laboratoriais
Mudanças nos sinais vitais
olanzapina oral foi associada a hipotensão ortostática e taquicardia em ensaios clínicos. A olanzapina intramuscular para injeção foi associada a bradicardia, hipotensão e taquicardia em ensaios clínicos [ver AVISOS E PRECAUÇÕES ].
Alterações laboratoriais
Monoterapia com Olanzapina em Adultos
Uma avaliação da experiência pré-comercialização da olanzapina revelou uma associação com aumentos assintomáticos de ALT, AST e GGT. No banco de dados original de pré-comercialização de cerca de 2.400 pacientes adultos com ALT basal ≤ 90 UI/L, a incidência de elevações de ALT para > 200 UI/L foi de 2% (50/2381). Nenhum desses pacientes apresentou icterícia ou outros sintomas atribuíveis a insuficiência hepática e a maioria apresentou alterações transitórias que tenderam a se normalizar enquanto o tratamento com olanzapina foi continuado.
Em estudos de monoterapia com olanzapina controlados por placebo em adultos, foram observadas elevações clinicamente significativas de ALT (alteração de
A partir de uma análise dos dados laboratoriais em um banco de dados integrado de 41 estudos clínicos concluídos em pacientes adultos tratados com olanzapina oral, níveis elevados de GGT foram registrados em ≥1% (88/5245) dos pacientes.
Deve-se ter cautela em pacientes com sinais e sintomas de insuficiência hepática, em pacientes com condições preexistentes associadas à reserva funcional hepática limitada e em pacientes que estão sendo tratados com drogas potencialmente hepatotóxicas.
A administração de olanzapina também foi associada a aumentos na prolactina sérica [ver AVISOS E PRECAUÇÕES ], com elevação assintomática da contagem de eosinófilos em 0,3% dos pacientes e com aumento da CPK.
A partir de uma análise dos dados laboratoriais em um banco de dados integrado de 41 estudos clínicos completos em pacientes adultos tratados com olanzapina oral, o ácido úrico elevado foi registrado em ≥3% (171/4641) dos pacientes.
Monoterapia com Olanzapina em Adolescentes
Em ensaios clínicos controlados por placebo de pacientes adolescentes com esquizofrenia ou transtorno bipolar I (episódios maníacos ou mistos), foram observadas frequências maiores para os seguintes achados emergentes do tratamento, a qualquer momento, em analitos laboratoriais em comparação com placebo: ALT elevada (≥3X ULN em pacientes com ALT na linha de base
Em estudos de monoterapia com olanzapina controlados por placebo em adolescentes, foram observadas elevações clinicamente significativas de ALT (alteração de
Alterações de ECG
Em estudos agrupados de adultos, bem como estudos agrupados de adolescentes, não houve diferenças significativas entre olanzapina e placebo nas proporções de pacientes que apresentaram alterações potencialmente importantes nos parâmetros de ECG, incluindo intervalos QT, QTc (corrigido por Fridericia) e PR. O uso de olanzapina foi associado a um aumento médio da frequência cardíaca em comparação com placebo (adultos: +2,4 batimentos por minuto vs sem alteração com placebo; adolescentes: +6,3 batimentos por minuto vs -5,1 batimentos por minuto com placebo). Esse aumento na frequência cardíaca pode estar relacionado ao potencial da olanzapina para induzir alterações ortostáticas [ver AVISOS E PRECAUÇÕES ].
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de ZYPREXA. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, é difícil estimar com segurança sua frequência ou avaliar uma relação causal com a exposição ao medicamento.
As reações adversas relatadas desde a introdução no mercado que foram temporariamente (mas não necessariamente causalmente) relacionadas à terapia com ZYPREXA incluem as seguintes: reação alérgica (por exemplo, reação anafilactóide, angioedema, prurido ou urticária), lesão hepática colestática ou mista, coma diabético, cetoacidose diabética, reação de descontinuação (diaforese, náusea ou vômito), reação ao medicamento com eosinofilia e sintomas sistêmicos (DRESS), hepatite, icterícia, neutropenia, pancreatite, priapismo, erupção cutânea, síndrome das pernas inquietas, rabdomiólise, gagueira1 e eventos tromboembólicos venosos (incluindo embolia pulmonar e trombose venosa profunda). Níveis aleatórios de colesterol ≥240 mg/dL e níveis aleatórios de triglicerídeos ≥1000 mg/dL foram relatados.
1 A gagueira só foi estudada em formulações de injeção oral e de longa ação (LAI).
INTERAÇÕES MEDICAMENTOSAS
Os riscos do uso de olanzapina em combinação com outros medicamentos não foram amplamente avaliados em estudos sistemáticos.
Potencial para outras drogas afetarem a olanzapina
Diazepam
A coadministração de diazepam com olanzapina potencializou a hipotensão ortostática observada com olanzapina.
Cimetidina e Antiácidos
Doses únicas de cimetidina (800 mg) ou antiácidos contendo alumínio e magnésio não afetaram a biodisponibilidade oral da olanzapina.
Indutores de CYP1A2
A terapia com carbamazepina (200 mg bid) causa um aumento de aproximadamente 50% na depuração da olanzapina. Este aumento é provavelmente devido ao fato de que a carbamazepina é um potente indutor da atividade do CYP1A2. Doses diárias mais altas de carbamazepina podem causar um aumento ainda maior na depuração da olanzapina.
Álcool
O etanol (dose única de 45 mg/70 kg) não teve efeito na farmacocinética da olanzapina. A coadministração de álcool (isto é, etanol) com olanzapina potencializou a hipotensão ortostática observada com olanzapina [ver INTERAÇÕES MEDICAMENTOSAS ].
Inibidores de CYP1A2
Fluvoxamina
fluvoxamina, um inibidor do CYP1A2, diminui a depuração da olanzapina. Isso resulta em um aumento médio na Cmax da olanzapina após a fluvoxamina de 54% em mulheres não fumantes e 77% em homens fumantes. O aumento médio da AUC da olanzapina é de 52% e 108%, respectivamente. Doses mais baixas de olanzapina devem ser consideradas em pacientes recebendo tratamento concomitante com fluvoxamina.
Inibidores de CYP2D6
Fluoxetina
A fluoxetina (dose única de 60 mg ou dose diária de 60 mg por 8 dias) causa um pequeno aumento (média de 16%) na concentração máxima de olanzapina e uma pequena diminuição (média de 16%) na depuração da olanzapina. A magnitude do impacto desse fator é pequena em comparação com a variabilidade geral entre os indivíduos e, portanto, a modificação da dose não é recomendada rotineiramente. Ao usar ZYPREXA e fluoxetina em combinação, consulte também a seção Interações medicamentosas do folheto informativo do Symbyax.
Varfarina
A varfarina (dose única de 20 mg) não afetou a farmacocinética da olanzapina.
Indutores de CYP1A2 ou glucuronil transferase
Omeprazol e rifampicina podem causar um aumento na depuração da olanzapina.
Carvão
A administração de carvão ativado (1 g) reduziu a Cmax e a AUC da olanzapina oral em cerca de 60%. Como os níveis máximos de olanzapina não são normalmente obtidos até cerca de 6 horas após a dosagem, o carvão pode ser um tratamento útil para a superdosagem de olanzapina.
Potencial para a Olanzapina Afetar Outros Medicamentos
Drogas que Agem no SNC
Dados os efeitos primários da olanzapina no SNC, deve-se ter cautela quando a olanzapina é administrada em combinação com outras drogas de ação central e álcool.
Agentes anti-hipertensivos
A olanzapina, devido ao seu potencial para induzir hipotensão, pode potencializar os efeitos de certos agentes anti-hipertensivos.
Agonistas de levodopa e dopamina
A olanzapina pode antagonizar os efeitos da levodopa e dos agonistas da dopamina.
Lorazepam (IM)
administração de lorazepam intramuscular (2 mg) 1 hora após a injeção intramuscular de olanzapina (5 mg) não afetou significativamente a farmacocinética da olanzapina, lorazepam não conjugado ou lorazepam total. No entanto, esta coadministração de lorazepam intramuscular e olanzapina intramuscular para injeção aumentou a sonolência observada com qualquer uma das drogas isoladamente [ver AVISOS E PRECAUÇÕES ].
Lítio
Doses múltiplas de olanzapina (10 mg por 8 dias) não influenciaram a cinética do lítio. Portanto, a administração concomitante de olanzapina não requer ajuste de dose de lítio [ver AVISOS E PRECAUÇÕES ].
Valproato
A olanzapina (10 mg por dia durante 2 semanas) não afetou as concentrações plasmáticas de valproato no estado de equilíbrio. Portanto, a administração concomitante de olanzapina não requer ajuste de dose de valproato [ver AVISOS E PRECAUÇÕES ].
Efeito da olanzapina nas enzimas metabolizadoras de drogas
Estudos in vitro utilizando microssomas hepáticos humanos sugerem que a olanzapina tem pouco potencial para inibir CYP1A2, CYP2C9, CYP2C19, CYP2D6 e CYP3A. Assim, é improvável que a olanzapina cause interações medicamentosas clinicamente importantes mediadas por essas enzimas.
Imipramina
Doses únicas de olanzapina não afetaram a farmacocinética da imipramina ou de seu metabólito ativo desipramina.
Varfarina
Doses únicas de olanzapina não afetaram a farmacocinética da varfarina.
Diazepam
A olanzapina não influenciou a farmacocinética do diazepam ou seu metabólito ativo Ndesmetildiazepam. No entanto, diazepam coadministrado com olanzapina aumentou a hipotensão ortostática observada com qualquer um dos medicamentos administrados isoladamente.
Álcool
Doses múltiplas de olanzapina não influenciaram a cinética do etanol.
Biperideno
Doses múltiplas de olanzapina não influenciaram a cinética do biperideno.
Teofilina
Doses múltiplas de olanzapina não afetaram a farmacocinética da teofilina ou seus metabólitos.
Abuso e Dependência de Drogas
Dependência
Em estudos projetados prospectivamente para avaliar o potencial de abuso e dependência, a olanzapina demonstrou ter efeitos depressivos agudos no SNC, mas pouco ou nenhum potencial de abuso ou dependência física em ratos administrados em doses orais até 15 vezes a MRHD oral diária (20 mg) e macacos rhesus administraram doses orais até 8 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal.
olanzapina não foi sistematicamente estudada em humanos por seu potencial de abuso, tolerância ou dependência física. Embora os ensaios clínicos não tenham revelado qualquer tendência para qualquer comportamento de procura de drogas, estas observações não foram sistemáticas e não é possível prever com base nesta experiência limitada até que ponto uma droga activa no SNC será mal utilizada, desviada , e/ou abusado uma vez comercializado. Consequentemente, os pacientes devem ser avaliados cuidadosamente para uma história de abuso de drogas, e esses pacientes devem ser observados atentamente quanto a sinais de uso indevido ou abuso de olanzapina (por exemplo, desenvolvimento de tolerância, aumento da dose, comportamento de busca de drogas).
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Ao usar ZYPREXA 7,5 mg e fluoxetina em combinação, consulte também a seção de Advertências e Precauções do folheto informativo do Symbyax.
Pacientes idosos com psicose relacionada à demência
Aumento da mortalidade
Pacientes idosos com psicose relacionada à demência tratados com medicamentos antipsicóticos apresentam risco aumentado de morte. ZYPREXA 20mg não é aprovado para o tratamento de pacientes com psicose relacionada à demência [ver ADVERTÊNCIA NA CAIXA, Uso em pacientes com doença concomitante e INFORMAÇÕES AO PACIENTE].
Em estudos clínicos controlados com placebo em pacientes idosos com psicose relacionada à demência, a incidência de morte em pacientes tratados com olanzapina foi significativamente maior do que em pacientes tratados com placebo (3,5% vs 1,5%, respectivamente).
Eventos Adversos Cerebrovasculares (ECV), Incluindo AVC
Eventos adversos cerebrovasculares (por exemplo, acidente vascular cerebral, ataque isquêmico transitório), incluindo fatalidades, foram relatados em pacientes em estudos com olanzapina em pacientes idosos com psicose relacionada à demência. Em estudos controlados com placebo, houve uma incidência significativamente maior de eventos adversos cerebrovasculares em pacientes tratados com olanzapina em comparação com pacientes tratados com placebo. A olanzapina não é aprovada para o tratamento de pacientes com psicose relacionada à demência [ver AVISO EM CAIXA e INFORMAÇÃO DO PACIENTE ].
Suicídio
A possibilidade de tentativa de suicídio é inerente à esquizofrenia e ao transtorno bipolar I, e a supervisão cuidadosa de pacientes de alto risco deve acompanhar a terapia medicamentosa. As prescrições de olanzapina devem ser feitas para a menor quantidade de comprimidos compatível com o bom manejo do paciente, a fim de reduzir o risco de superdosagem.
Síndrome Neuroléptica Maligna (SNM)
Um complexo de sintomas potencialmente fatal, algumas vezes referido como Síndrome Neuroléptica Maligna (SNM), foi relatado em associação com a administração de medicamentos antipsicóticos, incluindo a olanzapina. As manifestações clínicas da SNM são hiperpirexia, rigidez muscular, estado mental alterado e evidência de instabilidade autonômica (pulso ou pressão arterial irregulares, taquicardia, diaforese e arritmia cardíaca). Sinais adicionais podem incluir creatinina fosfoquinase elevada, mioglobinúria (rabdomiólise) e insuficiência renal aguda.
avaliação diagnóstica de pacientes com esta síndrome é complicada. Ao chegar a um diagnóstico, é importante excluir casos em que a apresentação clínica inclui doença médica grave (por exemplo, pneumonia, infecção sistêmica, etc.) e sinais e sintomas extrapiramidais (SEP) não tratados ou tratados inadequadamente. Outras considerações importantes no diagnóstico diferencial incluem toxicidade anticolinérgica central, insolação, febre medicamentosa e patologia primária do sistema nervoso central.
O manejo da SNM deve incluir: 1) descontinuação imediata de drogas antipsicóticas e outras drogas não essenciais à terapia concomitante; 2) tratamento sintomático intensivo e acompanhamento médico; e 3) tratamento de quaisquer problemas médicos graves concomitantes para os quais existam tratamentos específicos disponíveis. Não há acordo geral sobre regimes de tratamento farmacológico específico para SNM.
Se um paciente necessitar de tratamento medicamentoso antipsicótico após a recuperação da SNM, a potencial reintrodução da terapia medicamentosa deve ser cuidadosamente considerada. O paciente deve ser cuidadosamente monitorado, uma vez que foram relatadas recorrências de SNM [ver INFORMAÇÃO DO PACIENTE ].
Reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS)
Reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS) foi relatada com a exposição à olanzapina. DRESS pode apresentar uma reação cutânea (como erupção cutânea ou dermatite esfoliativa), eosinofilia, febre e/ou linfadenopatia com complicações sistêmicas como hepatite, nefrite, pneumonite, miocardite e/ou pericardite. DRESS às vezes é fatal. Descontinuar a olanzapina se houver suspeita de DRESS [ver INFORMAÇÃO DO PACIENTE ].
Alterações metabólicas
Os antipsicóticos atípicos têm sido associados a alterações metabólicas, incluindo hiperglicemia, dislipidemia e ganho de peso. Alterações metabólicas podem estar associadas ao aumento do risco cardiovascular/cerebrovascular. O perfil metabólico específico da olanzapina é apresentado abaixo.
Hiperglicemia e Diabetes Mellitus
Os profissionais de saúde devem considerar os riscos e benefícios ao prescrever olanzapina a pacientes com diagnóstico estabelecido de diabetes mellitus ou com nível de glicose no sangue limítrofe aumentado (jejum 100-126 mg/dL, sem jejum 140-200 mg/dL). Pacientes em uso de olanzapina devem ser monitorados regularmente quanto ao agravamento do controle da glicose. Os pacientes que iniciam o tratamento com olanzapina devem ser submetidos a testes de glicemia de jejum no início do tratamento e periodicamente durante o tratamento. Qualquer paciente tratado com antipsicóticos atípicos deve ser monitorado quanto a sintomas de hiperglicemia, incluindo polidipsia, poliúria, polifagia e fraqueza. Os pacientes que desenvolvem sintomas de hiperglicemia durante o tratamento com antipsicóticos atípicos devem ser submetidos ao teste de glicemia em jejum. Em alguns casos, a hiperglicemia foi resolvida quando o antipsicótico atípico foi descontinuado; no entanto, alguns pacientes necessitaram de continuação do tratamento antidiabético apesar da descontinuação do medicamento suspeito [ver INFORMAÇÃO DO PACIENTE ].
Hiperglicemia, em alguns casos extrema e associada a cetoacidose ou coma hiperosmolar ou morte, foi relatada em pacientes tratados com antipsicóticos atípicos, incluindo olanzapina. A avaliação da relação entre o uso de antipsicóticos atípicos e anormalidades da glicose é complicada pela possibilidade de um risco aumentado de diabetes mellitus em pacientes com esquizofrenia e o aumento da incidência de diabetes mellitus na população em geral. Estudos epidemiológicos sugerem um risco aumentado de reações adversas relacionadas à hiperglicemia emergentes do tratamento em pacientes tratados com antipsicóticos atípicos. Embora as estimativas de risco relativo sejam inconsistentes, a associação entre antipsicóticos atípicos e aumentos nos níveis de glicose parece cair em um continuum e a olanzapina parece ter uma associação maior do que alguns outros antipsicóticos atípicos.
Aumentos médios da glicemia foram observados em pacientes tratados (exposição mediana de 9,2 meses) com olanzapina na fase 1 dos Ensaios Clínicos Antipsicóticos de Eficácia de Intervenção (CATIE). O aumento médio da glicose sérica (amostras em jejum e sem jejum) desde a linha de base até a média das 2 concentrações séricas mais altas foi de 15,0 mg/dL.
Em um estudo com voluntários saudáveis, os indivíduos que receberam olanzapina (N=22) por 3 semanas tiveram um aumento médio em comparação com a linha de base na glicemia de jejum de 2,3 mg/dL. Indivíduos tratados com placebo (N = 19) tiveram um aumento médio na glicemia de jejum em comparação com a linha de base de 0,34 mg/dL.
Monoterapia com Olanzapina em Adultos
Em uma análise de 5 estudos de monoterapia com olanzapina em adultos controlados por placebo com duração mediana de tratamento de aproximadamente 3 semanas, a olanzapina foi associada a uma alteração média maior nos níveis de glicose em jejum em comparação ao placebo (2,76 mg/dL versus 0,17 mg/dL). A diferença nas alterações médias entre olanzapina e placebo foi maior em pacientes com evidência de desregulação da glicose no início do estudo (pacientes diagnosticados com diabetes mellitus ou reações adversas relacionadas, pacientes tratados com agentes antidiabéticos, pacientes com nível basal de glicose aleatório ≥200 mg/ dL e/ou um nível basal de glicose em jejum ≥126 mg/dL). Os pacientes tratados com olanzapina tiveram um aumento médio maior de HbA1c desde a linha de base de 0,04% (exposição mediana de 21 dias), em comparação com uma diminuição média de HbA1c de 0,06% em indivíduos tratados com placebo (exposição mediana de 17 dias).
Em uma análise de 8 estudos controlados com placebo (exposição mediana ao tratamento 4-5 semanas), 6,1% dos indivíduos tratados com olanzapina (N=855) tiveram glicosúria emergente do tratamento em comparação com 2,8% dos indivíduos tratados com placebo (N=599) . A Tabela 2 mostra as alterações de curto e longo prazo nos níveis de glicose em jejum de estudos de monoterapia com olanzapina em adultos.
A alteração média na glicemia de jejum para pacientes expostos por pelo menos 48 semanas foi de 4,2 mg/dL (N=487). Em análises de pacientes que completaram 9-12 meses de terapia com olanzapina, a alteração média nos níveis de glicose em jejum e sem jejum continuou a aumentar ao longo do tempo.
Monoterapia com Olanzapina em Adolescentes
segurança e eficácia da olanzapina não foram estabelecidas em pacientes com idade inferior a 13 anos. Em uma análise de 3 estudos de monoterapia com olanzapina controlados por placebo em pacientes adolescentes, incluindo aqueles com esquizofrenia (6 semanas) ou transtorno bipolar I (episódios maníacos ou mistos) (3 semanas), a olanzapina foi associada a uma alteração média maior da linha de base em jejum níveis de glicose em comparação com placebo (2,68 mg/dL versus -2,59 mg/dL). A alteração média na glicemia de jejum para adolescentes expostos por pelo menos 24 semanas foi de 3,1 mg/dL (N=121). A Tabela 3 mostra as alterações de curto e longo prazo na glicemia de jejum de estudos de monoterapia com olanzapina em adolescentes.
Dislipidemia
Alterações indesejáveis nos lipídios foram observadas com o uso de olanzapina. Recomenda-se o monitoramento clínico, incluindo avaliações lipídicas iniciais e periódicas de acompanhamento em pacientes em uso de olanzapina [ver INFORMAÇÃO DO PACIENTE ].
Clinicamente significativas, e às vezes muito altas (> 500 mg/dL), foram observadas elevações nos níveis de triglicerídeos com o uso de olanzapina. Aumentos médios modestos no colesterol total também foram observados com o uso de olanzapina.
Monoterapia com Olanzapina em Adultos
Em uma análise de 5 estudos de monoterapia com olanzapina controlados por placebo com duração de tratamento de até 12 semanas, os pacientes tratados com olanzapina tiveram aumentos da linha de base no colesterol total médio em jejum, colesterol LDL e triglicerídeos de 5,3 mg/dL, 3,0 mg/dL e 20,8 mg/dL, respectivamente, em comparação com as diminuições da linha de base no colesterol total médio em jejum, colesterol LDL e triglicerídeos de 6,1 mg/dL, 4,3 mg/dL e 10,7 mg/dL para pacientes tratados com placebo. Para o colesterol HDL em jejum, não foram observadas diferenças clinicamente significativas entre os pacientes tratados com olanzapina e os pacientes tratados com placebo. Os aumentos médios nos valores lipídicos em jejum (colesterol total, colesterol LDL e triglicerídeos) foram maiores em pacientes sem evidência de desregulação lipídica no início do estudo, onde a desregulação lipídica foi definida como pacientes diagnosticados com dislipidemia ou reações adversas relacionadas, pacientes tratados com agentes hipolipemiantes, ou pacientes com níveis lipídicos basais elevados.
Em estudos de longo prazo (pelo menos 48 semanas), os pacientes tiveram aumentos da linha de base na média de colesterol total em jejum, colesterol LDL e triglicerídeos de 5,6 mg/dL, 2,5 mg/dL e 18,7 mg/dL, respectivamente, e uma média diminuição do colesterol HDL em jejum de 0,16 mg/dL. Em uma análise de pacientes que completaram 12 meses de terapia, o colesterol total médio sem jejum não aumentou mais após aproximadamente 4-6 meses.
A proporção de pacientes que tiveram alterações (pelo menos uma vez) no colesterol total, colesterol LDL ou triglicerídeos de normal ou limítrofe para alto, ou alterações no colesterol HDL de normal ou limítrofe para baixo, foi maior em estudos de longo prazo (pelo menos 48 semanas) em comparação com estudos de curta duração. A Tabela 4 mostra as mudanças categóricas nos valores de lipídios em jejum.
Na fase 1 do Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE), ao longo de uma exposição mediana de 9,2 meses, o aumento médio dos triglicerídeos em pacientes em uso de olanzapina foi de 40,5 mg/dL. Na fase 1 do CATIE, o aumento médio do colesterol total foi de 9,4 mg/dL.
Monoterapia com Olanzapina em Adolescentes
segurança e eficácia da olanzapina não foram estabelecidas em pacientes com idade inferior a 13 anos. Em uma análise de 3 estudos de monoterapia com olanzapina controlados por placebo em adolescentes, incluindo aqueles com esquizofrenia (6 semanas) ou transtorno bipolar I (episódios maníacos ou mistos) (3 semanas), os adolescentes tratados com olanzapina tiveram aumentos em relação à linha de base no colesterol total médio em jejum, LDL colesterol e triglicerídeos de 12,9 mg/dL, 6,5 mg/dL e 28,4 mg/dL, respectivamente, em comparação com aumentos da linha de base no colesterol total médio em jejum e colesterol LDL de 1,3 mg/dL e 1,0 mg/dL, e uma diminuição em triglicerídeos de 1,1 mg/dL para adolescentes tratados com placebo. Para o colesterol HDL em jejum, não foram observadas diferenças clinicamente significativas entre adolescentes tratados com olanzapina e adolescentes tratados com placebo.
Em estudos de longo prazo (pelo menos 24 semanas), os adolescentes tiveram aumentos desde a linha de base na média de colesterol total em jejum, colesterol LDL e triglicerídeos de 5,5 mg/dL, 5,4 mg/dL e 20,5 mg/dL, respectivamente, e uma média diminuição do colesterol HDL em jejum de 4,5 mg/dL. A Tabela 5 mostra as mudanças categóricas nos valores de lipídios em jejum em adolescentes.
Ganho de peso
As consequências potenciais do ganho de peso devem ser consideradas antes de iniciar a olanzapina. Os pacientes que recebem olanzapina devem receber monitoramento regular do peso [ver Informações de Aconselhamento do Paciente ].
Monoterapia com Olanzapina em Adultos
Em uma análise de 13 estudos de monoterapia com olanzapina controlados por placebo, os pacientes tratados com olanzapina ganharam uma média de 2,6 kg (5,7 lb) em comparação com uma perda de peso média de 0,3 kg (0,6 lb) em pacientes tratados com placebo com uma exposição mediana de 6 semanas ; 22,2% dos pacientes tratados com olanzapina ganharam pelo menos 7% do seu peso inicial, em comparação com 3% dos pacientes tratados com placebo, com exposição mediana ao evento de 8 semanas; 4,2% dos pacientes tratados com olanzapina ganharam pelo menos 15% do seu peso inicial, em comparação com 0,3% dos pacientes tratados com placebo, com uma exposição mediana ao evento de 12 semanas. O ganho de peso clinicamente significativo foi observado em todas as categorias de base do Índice de Massa Corporal (IMC). A descontinuação devido ao ganho de peso ocorreu em 0,2% dos pacientes tratados com olanzapina e em 0% dos pacientes tratados com placebo.
Em estudos de longo prazo (pelo menos 48 semanas), o ganho de peso médio foi de 5,6 kg (12,3 lb) (exposição mediana de 573 dias, N = 2021). As porcentagens de pacientes que ganharam pelo menos 7%, 15% ou 25% de seu peso corporal basal com exposição a longo prazo foram de 64%, 32% e 12%, respectivamente. A descontinuação devido ao ganho de peso ocorreu em 0,4% dos pacientes tratados com olanzapina após pelo menos 48 semanas de exposição.
A Tabela 6 inclui dados sobre ganho de peso em adultos com olanzapina agrupados de 86 ensaios clínicos. Os dados em cada coluna representam dados para os pacientes que completaram os períodos de tratamento das durações especificadas.
Foram observadas diferenças entre os grupos de dose em relação ao ganho de peso. Em um único estudo randomizado, duplo-cego, de dose fixa de 8 semanas comparando 10 (N=199), 20 (N=200) e 40 (N=200) mg/dia de olanzapina oral em pacientes adultos com esquizofrenia ou transtorno esquizoafetivo, Foi observado aumento médio de linha de base até o ponto final no peso (10 mg/dia: 1,9 kg; 20 mg/dia: 2,3 kg; 40 mg/dia: 3 kg) com diferenças significativas entre 10 vs 40 mg/dia.
Monoterapia com Olanzapina em Adolescentes
A segurança e eficácia da olanzapina não foram estabelecidas em pacientes com idade inferior a 13 anos. O aumento médio de peso em adolescentes foi maior do que em adultos. Em 4 estudos controlados com placebo, a descontinuação devido ao ganho de peso ocorreu em 1% dos pacientes tratados com olanzapina, em comparação com 0% dos pacientes tratados com placebo.
Em estudos de longo prazo (pelo menos 24 semanas), o ganho de peso médio foi de 11,2 kg (24,6 lb); (exposição mediana de 201 dias, N=179). As porcentagens de adolescentes que ganharam pelo menos 7%, 15% ou 25% de seu peso corporal basal com exposição a longo prazo foram de 89%, 55% e 29%, respectivamente. Entre os pacientes adolescentes, o ganho de peso médio por categoria de IMC basal foi de 11,5 kg (25,3 lb), 12,1 kg (26,6 lb) e 12,7 kg (27,9 lb), respectivamente, para normal (N = 106), excesso de peso (N = 26) e obesos (N=17). A descontinuação devido ao ganho de peso ocorreu em 2,2% dos pacientes tratados com olanzapina após pelo menos 24 semanas de exposição.
A Tabela 8 mostra dados sobre ganho de peso em adolescentes com olanzapina agrupados de 6 ensaios clínicos. Os dados em cada coluna representam dados para os pacientes que completaram os períodos de tratamento das durações especificadas. Existem poucos dados de ensaios clínicos disponíveis sobre ganho de peso em adolescentes com olanzapina após 6 meses de tratamento.
Discinesia tardia
Uma síndrome de movimentos discinéticos involuntários e potencialmente irreversíveis pode se desenvolver em pacientes tratados com drogas antipsicóticas. Embora a prevalência da síndrome pareça ser maior entre os idosos, especialmente as mulheres idosas, é impossível confiar nas estimativas de prevalência para prever, no início do tratamento antipsicótico, quais pacientes provavelmente desenvolverão a síndrome. Se os medicamentos antipsicóticos diferem em seu potencial para causar discinesia tardia é desconhecido.
Acredita-se que o risco de desenvolver discinesia tardia e a probabilidade de que se torne irreversível aumente à medida que a duração do tratamento e a dose cumulativa total de drogas antipsicóticas administradas ao paciente aumentam. No entanto, a síndrome pode se desenvolver, embora muito menos comumente, após períodos de tratamento relativamente breves em doses baixas ou pode até surgir após a descontinuação do tratamento.
discinesia tardia pode regredir, parcial ou completamente, se o tratamento antipsicótico for retirado. O tratamento antipsicótico, no entanto, pode suprimir (ou suprimir parcialmente) os sinais e sintomas da síndrome e, assim, pode mascarar o processo subjacente. O efeito que a supressão sintomática tem sobre o curso a longo prazo da síndrome é desconhecido.
Dadas essas considerações, a olanzapina deve ser prescrita da maneira mais provável de minimizar a ocorrência de discinesia tardia. O tratamento antipsicótico crônico geralmente deve ser reservado para pacientes (1) que sofrem de uma doença crônica que responde aos medicamentos antipsicóticos e (2) para os quais tratamentos alternativos igualmente eficazes, mas potencialmente menos prejudiciais, não estão disponíveis ou são apropriados. Em pacientes que necessitam de tratamento crônico, deve-se buscar a menor dose e a menor duração do tratamento que produza uma resposta clínica satisfatória. A necessidade de continuação do tratamento deve ser reavaliada periodicamente.
Se surgirem sinais e sintomas de discinesia tardia em um paciente em uso de olanzapina, a descontinuação do medicamento deve ser considerada. No entanto, alguns pacientes podem necessitar de tratamento com olanzapina apesar da presença da síndrome.
Para obter informações específicas sobre os avisos de lítio ou valproato, consulte a seção Avisos dos folhetos informativos desses outros produtos.
Hipotensão ortostática
A olanzapina pode induzir hipotensão ortostática associada a tontura, taquicardia, bradicardia e, em alguns pacientes, síncope, especialmente durante o período inicial de titulação da dose, provavelmente refletindo suas propriedades antagônicas α1-adrenérgicas. Informações de Aconselhamento do Paciente ].
A partir de uma análise dos dados de sinais vitais em um banco de dados integrado de 41 estudos clínicos completos em pacientes adultos tratados com olanzapina oral, foi registrada hipotensão ortostática em ≥20% (1277/6030) dos pacientes.
Para a terapia oral com olanzapina, o risco de hipotensão ortostática e síncope pode ser minimizado iniciando a terapia com 5 mg QD [ver DOSAGEM E ADMINISTRAÇÃO ]. Uma titulação mais gradual para a dose alvo deve ser considerada se ocorrer hipotensão.
Hipotensão, bradicardia com ou sem hipotensão, taquicardia e síncope também foram relatados durante os ensaios clínicos com olanzapina intramuscular para injeção. Em um estudo de farmacologia clínica aberto em pacientes não agitados com esquizofrenia, no qual a segurança e a tolerabilidade da olanzapina intramuscular foram avaliadas sob um regime de dosagem máxima (três doses de 10 mg administradas com 4 horas de intervalo), aproximadamente um terço desses pacientes apresentou diminuição ortostática na pressão arterial sistólica (ou seja, diminuição ≥30 mmHg) [ver DOSAGEM E ADMINISTRAÇÃO ]. Síncope foi relatada em 0,6% (15/2500) dos pacientes tratados com olanzapina em estudos de fase 2-3 com olanzapina oral e em 0,3% (2/722) dos pacientes tratados com olanzapina com agitação nos estudos de olanzapina intramuscular para injeção. Três voluntários normais em estudos de fase 1 com olanzapina intramuscular experimentaram hipotensão, bradicardia e pausas sinusais de até 6 segundos que se resolveram espontaneamente (em 2 casos as reações ocorreram com olanzapina intramuscular e em 1 caso com olanzapina oral). O risco para esta sequência de hipotensão, bradicardia e pausa sinusal pode ser maior em pacientes não psiquiátricos em comparação com pacientes psiquiátricos que possivelmente são mais adaptados a certos efeitos de drogas psicotrópicas. Para a terapia de injeção de olanzapina intramuscular, os pacientes devem permanecer em decúbito se estiverem sonolentos ou tontos após a injeção até que o exame indique que eles não estão apresentando hipotensão postural, bradicardia e/ou hipoventilação.
olanzapina deve ser usada com cuidado especial em pacientes com doença cardiovascular conhecida (história de infarto do miocárdio ou isquemia, insuficiência cardíaca ou anormalidades de condução), doença cerebrovascular e condições que predisponham os pacientes à hipotensão (desidratação, hipovolemia e tratamento com medicamentos anti-hipertensivos). ) onde a ocorrência de síncope, ou hipotensão e/ou bradicardia pode colocar o paciente em risco médico aumentado.
É necessária cautela em pacientes que recebem tratamento com outros medicamentos que tenham efeitos que possam induzir hipotensão, bradicardia, depressão respiratória ou do sistema nervoso central. INTERAÇÕES MEDICAMENTOSAS ]. A administração concomitante de olanzapina intramuscular e benzodiazepina parenteral não é recomendada devido ao potencial de sedação excessiva e depressão cardiorrespiratória.
Cataratas
ZYPREXA pode causar sonolência, hipotensão postural, instabilidade motora e sensorial, podendo levar a quedas e, consequentemente, fraturas ou outras lesões. Para pacientes com doenças, condições ou medicamentos que possam exacerbar esses efeitos, complete as avaliações de risco de queda ao iniciar o tratamento antipsicótico e recorrentemente para pacientes em terapia antipsicótica de longo prazo.
Leucopenia, neutropenia e agranulocitose
Efeito de classe
Em ensaios clínicos e/ou experiência pós-comercialização, eventos de leucopenia/neutropenia foram relatados temporariamente relacionados a agentes antipsicóticos, incluindo ZYPREXA. Agranulocitose também foi relatada.
Possíveis fatores de risco para leucopenia/neutropenia incluem baixa contagem de glóbulos brancos (WBC) pré-existente e história de leucopenia/neutropenia induzida por drogas. Pacientes com história de leucograma baixo clinicamente significativo ou leucopenia/neutropenia induzida por drogas devem ter seu hemograma completo monitorado frequentemente durante os primeiros meses de terapia e a descontinuação de ZYPREXA deve ser considerada ao primeiro sinal de declínio clinicamente significativo em leucócitos na ausência de outros fatores causais.
Pacientes com neutropenia clinicamente significativa devem ser cuidadosamente monitorados quanto a febre ou outros sintomas ou sinais de infecção e tratados imediatamente se tais sintomas ou sinais ocorrerem. Pacientes com neutropenia grave (contagem absoluta de neutrófilos
Disfagia
dismotilidade esofágica e a aspiração têm sido associadas ao uso de drogas antipsicóticas. A pneumonia aspirativa é uma causa comum de morbidade e mortalidade em pacientes com doença de Alzheimer avançada. A olanzapina não está aprovada para o tratamento de pacientes com doença de Alzheimer.
Convulsões
Durante os testes de pré-comercialização, ocorreram convulsões em 0,9% (22/2500) dos pacientes tratados com olanzapina. Houve fatores de confusão que podem ter contribuído para a ocorrência de convulsões em muitos desses casos. A olanzapina deve ser usada com cautela em pacientes com histórico de convulsões ou com condições que potencialmente diminuem o limiar convulsivo, por exemplo, demência de Alzheimer. A olanzapina não está aprovada para o tratamento de pacientes com doença de Alzheimer. Condições que diminuem o limiar convulsivo podem ser mais prevalentes em uma população de 65 anos ou mais.
Potencial para comprometimento cognitivo e motor
sonolência foi uma reação adversa comumente relatada associada ao tratamento com olanzapina, ocorrendo em uma incidência de 26% em pacientes com olanzapina em comparação com 15% em pacientes com placebo. Esta reação adversa também foi relacionada à dose. A sonolência levou à descontinuação em 0,4% (9/2.500) dos pacientes no banco de dados de pré-comercialização.
Como a olanzapina tem o potencial de prejudicar o julgamento, o pensamento ou as habilidades motoras, os pacientes devem ser advertidos sobre a operação de máquinas perigosas, incluindo automóveis, até que tenham certeza razoável de que a terapia com olanzapina não os afeta adversamente [ver Informações de Aconselhamento do Paciente ].
Regulação da temperatura corporal
interrupção da capacidade do corpo de reduzir a temperatura corporal central tem sido atribuída a agentes antipsicóticos. Recomenda-se o cuidado apropriado ao prescrever olanzapina para pacientes que apresentarão condições que possam contribuir para a elevação da temperatura corporal central, por exemplo, exercício intenso, exposição a calor extremo, uso concomitante de medicação com atividade anticolinérgica ou estar sujeito a desidratação. INFORMAÇÃO DO PACIENTE ].
Uso em pacientes com doenças concomitantes
A experiência clínica com olanzapina em pacientes com certas doenças sistêmicas concomitantes é limitada. FARMACOLOGIA CLÍNICA ].
olanzapina exibe afinidade para o receptor muscarínico in vitro. Em ensaios clínicos pré-comercialização com olanzapina, a olanzapina foi associada a constipação, boca seca e taquicardia, todas as reações adversas possivelmente relacionadas ao antagonismo colinérgico. Tais reações adversas não foram frequentemente a base para a descontinuação da olanzapina, mas a olanzapina deve ser usada com cautela em pacientes com hipertrofia prostática clinicamente significativa, glaucoma de ângulo estreito ou histórico de íleo paralítico ou condições relacionadas.
Em 5 estudos controlados por placebo de olanzapina em pacientes idosos com psicose relacionada à demência (n = 1.184), as seguintes reações adversas emergentes do tratamento foram relatadas em pacientes tratados com olanzapina com uma incidência de pelo menos 2% e significativamente maior do que placebo pacientes tratados: quedas, sonolência, edema periférico, marcha anormal, incontinência urinária, letargia, aumento de peso, astenia, pirexia, pneumonia, boca seca e alucinações visuais. A taxa de descontinuação devido a reações adversas foi maior com olanzapina do que com placebo (13% vs 7%). Pacientes idosos com psicose relacionada à demência tratados com olanzapina apresentam risco aumentado de morte em comparação ao placebo. A olanzapina não é aprovada para o tratamento de pacientes com psicose relacionada à demência [ver AVISO EM CAIXA , Pacientes Idosos com Psicose Relacionada à Demência , e INFORMAÇÃO DO PACIENTE ].
olanzapina não foi avaliada ou utilizada em extensão apreciável em pacientes com história recente de infarto do miocárdio ou doença cardíaca instável. Os pacientes com esses diagnósticos foram excluídos dos estudos clínicos pré-comercialização. Devido ao risco de hipotensão ortostática com olanzapina, deve-se ter cautela em pacientes cardíacos [ver Hipotensão ortostática ].
Hiperprolactinemia
Assim como outras drogas que antagonizam os receptores D2 da dopamina, a olanzapina eleva os níveis de prolactina e a elevação persiste durante a administração crônica. A hiperprolactinemia pode suprimir o GnRH hipotalâmico, resultando em secreção reduzida de gonadotrofina hipofisária. Isso, por sua vez, pode inibir a função reprodutiva, prejudicando a esteroidogênese gonadal em pacientes do sexo feminino e masculino. Galactorreia, amenorreia, ginecomastia e impotência foram relatadas em pacientes recebendo compostos que aumentam a prolactina. A hiperprolactinemia de longa duração quando associada ao hipogonadismo pode levar à diminuição da densidade óssea em indivíduos do sexo feminino e masculino.
Experimentos em cultura de tecidos indicam que aproximadamente um terço dos cânceres de mama humanos são dependentes de prolactina in vitro, um fator de potencial importância se a prescrição desses medicamentos for contemplada em uma paciente com câncer de mama previamente detectado. Como é comum com compostos que aumentam a liberação de prolactina, um aumento na neoplasia da glândula mamária foi observado nos estudos de carcinogenicidade da olanzapina realizados em camundongos e ratos [ver Toxicologia não clínica ]. Nem os estudos clínicos nem os estudos epidemiológicos realizados até o momento mostraram associação entre a administração crônica dessa classe de medicamentos e a tumorigênese em humanos; a evidência disponível é considerada muito limitada para ser conclusiva neste momento.
Em estudos clínicos de olanzapina controlados por placebo (até 12 semanas), foram observadas alterações de normal para alta nas concentrações de prolactina em 30% dos adultos tratados com olanzapina, em comparação com 10,5% dos adultos tratados com placebo. Em uma análise agrupada de estudos clínicos incluindo 8.136 adultos tratados com olanzapina, as manifestações clínicas potencialmente associadas incluíram eventos relacionados à menstruação1 (2% [49/3240] das mulheres), eventos relacionados à função sexual2 (2% [150/8136] das mulheres e homens) e eventos relacionados à mama3 (0,7% [23/3240] das mulheres, 0,2% [9/4896] dos homens).
Em estudos de monoterapia com olanzapina controlados por placebo em pacientes adolescentes (até 6 semanas) com esquizofrenia ou transtorno bipolar I (episódios maníacos ou mistos), foram observadas alterações de normal para alta nas concentrações de prolactina em 47% dos pacientes tratados com olanzapina em comparação com 7 % de pacientes tratados com placebo. Em uma análise agrupada de ensaios clínicos incluindo 454 adolescentes tratados com olanzapina, as manifestações clínicas potencialmente associadas incluíram eventos relacionados à menstruação1 (1% [2/168] das mulheres), eventos relacionados à função sexual2 (0,7% [3/454] das mulheres e homens ) e eventos relacionados à mama3 (2% [3/168] das mulheres, 2% [7/286] dos homens) [ver Uso em populações específicas ].
1 Com base na busca dos seguintes termos: amenorréia, hipomenorréia, menstruação atrasada e oligomenorréia.
2 Com base na busca dos seguintes termos: anorgasmia, ejaculação retardada, disfunção erétil, diminuição da libido, perda da libido, orgasmo anormal e disfunção sexual.
Com base na pesquisa dos seguintes termos: corrimento mamário, aumento ou inchaço, galactorreia, ginecomastia e distúrbio da lactação.
Foram observadas diferenças entre os grupos de dose em relação à elevação da prolactina. Em um único estudo randomizado, duplo-cego, de dose fixa de 8 semanas comparando 10 (N=199), 20 (N=200) e 40 (N=200) mg/dia de olanzapina oral em pacientes adultos com esquizofrenia ou esquizoafetiva distúrbio, incidência de elevação de prolactina >24,2 ng/mL (mulheres) ou >18,77 ng/mL (homens) em qualquer momento durante o estudo (10 mg/dia: 31,2%; 20 mg/dia: 42,7%; 40 mg/dia : 61,1%) indicaram diferenças significativas entre 10 vs 40 mg/dia e 20 vs 40 mg/dia.
Use em combinação com fluoxetina, lítio ou valproato
Ao usar ZYPREXA e fluoxetina em combinação, o prescritor também deve consultar a seção de Advertências e Precauções do folheto informativo do Symbyax. Ao usar ZYPREXA em combinação com lítio ou valproato, o prescritor deve consultar as seções de Advertências e Precauções das bulas de lítio ou valproato [ver INTERAÇÕES MEDICAMENTOSAS ].
Testes laboratoriais
Recomenda-se o teste de glicemia em jejum e o perfil lipídico no início e periodicamente durante o tratamento [ver Alterações metabólicas e INFORMAÇÃO DO PACIENTE ].
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( Guia de Medicação ) para as formulações orais.
Os pacientes devem ser avisados sobre os seguintes problemas e solicitados a alertar seu prescritor se ocorrerem enquanto estiverem tomando ZYPREXA 15mg como monoterapia ou em combinação com fluoxetina. Se você achar que não está melhorando ou se tiver dúvidas sobre sua condição enquanto estiver tomando ZYPREXA 2,5 mg, ligue para o seu médico. Ao usar ZYPREXA e fluoxetina em combinação, consulte também a seção Informações de aconselhamento ao paciente do folheto informativo do Symbyax.
Pacientes idosos com psicose relacionada à demência: aumento da mortalidade e eventos adversos cerebrovasculares (ECV), incluindo acidente vascular cerebral
Pacientes e cuidadores devem ser informados de que pacientes idosos com psicose relacionada à demência tratados com drogas antipsicóticas apresentam risco aumentado de morte. Pacientes e cuidadores devem ser informados de que pacientes idosos com psicose relacionada à demência tratados com ZYPREXA tiveram uma incidência significativamente maior de eventos adversos cerebrovasculares (por exemplo, acidente vascular cerebral, ataque isquêmico transitório) em comparação com placebo.
ZYPREXA não é aprovado para pacientes idosos com psicose relacionada à demência [ver AVISO EM CAIXA e AVISOS E PRECAUÇÕES ].
Síndrome Neuroléptica Maligna (SNM)
Pacientes e cuidadores devem ser informados de que um complexo de sintomas potencialmente fatal, algumas vezes referido como SNM, foi relatado em associação com a administração de medicamentos antipsicóticos, incluindo ZYPREXA. Os sinais e sintomas da SNM incluem hiperpirexia, rigidez muscular, estado mental alterado e evidência de instabilidade autonômica (pulso ou pressão arterial irregulares, taquicardia, sudorese e arritmia cardíaca) [ver AVISOS E PRECAUÇÕES ].
Reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS)
Os pacientes devem ser aconselhados a relatar ao seu médico, o mais cedo possível, quaisquer sinais e sintomas que possam estar associados à Reação ao Medicamento com Eosinofilia e Sintomas Sistêmicos (DRESS) [ver AVISOS E PRECAUÇÕES ].
Hiperglicemia e Diabetes Mellitus
Os pacientes devem ser alertados sobre o risco potencial de reações adversas relacionadas à hiperglicemia. Os pacientes devem ser monitorados regularmente quanto ao agravamento do controle da glicose. Pacientes que têm diabetes devem seguir as instruções de seu médico sobre a frequência de verificação de açúcar no sangue enquanto estiverem tomando ZYPREXA [ver AVISOS E PRECAUÇÕES ].
Dislipidemia
Os pacientes devem ser informados de que ocorreu dislipidemia durante o tratamento com ZYPREXA. Os pacientes devem ter seu perfil lipídico monitorado regularmente [ver AVISOS E PRECAUÇÕES ].
Ganho de peso
Os pacientes devem ser informados de que ocorreu ganho de peso durante o tratamento com ZYPREXA. Os pacientes devem ter seu peso monitorado regularmente [ver AVISOS E PRECAUÇÕES ].
Hipotensão ortostática
Os pacientes devem ser alertados sobre o risco de hipotensão ortostática, especialmente durante o período de titulação da dose inicial e em associação com o uso concomitante de medicamentos que podem potencializar o efeito ortostático de ZYPREXA, por exemplo, diazepam ou álcool. AVISOS E PRECAUÇÕES e INTERAÇÕES MEDICAMENTOSAS ]. Os pacientes devem ser aconselhados a mudar de posição com cuidado para ajudar a prevenir a hipotensão ortostática e a deitar-se se sentirem tonturas ou desmaios, até que se sintam melhor. Os doentes devem ser aconselhados a contactar o seu médico se sentirem algum dos seguintes sinais e sintomas associados à hipotensão ortostática: tonturas, batimentos cardíacos rápidos ou lentos ou desmaios.
Potencial para comprometimento cognitivo e motor
Como o ZYPREXA tem o potencial de prejudicar o julgamento, o pensamento ou as habilidades motoras, os pacientes devem ser alertados sobre a operação de máquinas perigosas, incluindo automóveis, até que tenham certeza razoável de que a terapia com ZYPREXA não os afeta adversamente [ver AVISOS E PRECAUÇÕES ].
Regulação da temperatura corporal
Os pacientes devem ser avisados sobre os cuidados apropriados para evitar superaquecimento e desidratação. Os pacientes devem ser aconselhados a ligar para o médico imediatamente se ficarem gravemente doentes e apresentarem alguns ou todos estes sintomas de desidratação: sudorese demais ou nada, boca seca, sensação de muito calor, sede, incapacidade de produzir urina. Vejo AVISOS E PRECAUÇÕES ].
Medicação concomitante
Os pacientes devem ser aconselhados a informar seus profissionais de saúde se estiverem tomando ou planejam tomar Symbyax. Os pacientes também devem ser aconselhados a informar seus profissionais de saúde se estiverem tomando, planejam tomar ou pararam de tomar qualquer medicamento prescrito ou de venda livre, incluindo suplementos de ervas, uma vez que existe potencial para interações [ver INTERAÇÕES MEDICAMENTOSAS ].
Álcool
Os pacientes devem ser aconselhados a evitar o álcool enquanto estiverem tomando ZYPREXA [ver INTERAÇÕES MEDICAMENTOSAS ].
Fenilcetonúricos
ZYPREXA 10 mg ZYDIS (comprimidos de desintegração oral de olanzapina) contém fenilalanina (0,34, 0,45, 0,67 ou 0,90 mg por comprimido de 5, 10, 15 ou 20 mg, respectivamente) [ver DESCRIÇÃO ].
Uso em populações específicas
Gravidez
Aconselhe as mulheres a notificarem seu médico se engravidarem ou pretendem engravidar durante o tratamento com ZYPREXA. Avise os pacientes de que ZYPREXA pode causar sintomas extrapiramidais e/ou de abstinência (agitação, hipertonia, hipotonia, tremor, sonolência, desconforto respiratório e distúrbio alimentar) em um recém-nascido. Avisar as pacientes que existe um registro de exposição na gravidez que monitora os resultados da gravidez em mulheres expostas a ZYPREXA 7,5 mg durante a gravidez [ver Uso em populações específicas ].
Lactação
Aconselhe as mulheres que amamentam usando ZYPREXA 20mg a monitorar os bebês quanto a sedação excessiva, irritabilidade, má alimentação e sintomas extrapiramidais (tremores e movimentos musculares anormais) e a procurar atendimento médico se notar esses sinais. [Vejo Uso em populações específicas ].
Infertilidade
Avise as mulheres com potencial reprodutivo que ZYPREXA pode prejudicar a fertilidade devido ao aumento dos níveis séricos de prolactina. Os efeitos sobre a fertilidade são reversíveis [ver Uso em populações específicas ].
Uso Pediátrico
ZYPREXA 15mg é indicado para o tratamento da esquizofrenia e episódios maníacos ou mistos associados ao transtorno bipolar I em adolescentes de 13 a 17 anos de idade. Em comparação com pacientes de estudos clínicos em adultos, os adolescentes provavelmente ganharam mais peso, experimentaram maior sedação e tiveram maiores aumentos nos níveis de colesterol total, triglicerídeos, colesterol LDL, prolactina e aminotransferase hepática. Os pacientes devem ser aconselhados sobre os potenciais riscos a longo prazo associados ao ZYPREXA e informados de que esses riscos podem levá-los a considerar outros medicamentos primeiro [ver INDICAÇÕES E USO ]. A segurança e eficácia de ZYPREXA 5mg em pacientes com menos de 13 anos de idade não foram estabelecidas. A segurança e eficácia de ZYPREXA 15mg e fluoxetina em combinação em pacientes de 10 a 17 anos de idade foram estabelecidas para o tratamento agudo de episódios depressivos associados ao transtorno bipolar I. A segurança e eficácia de ZYPREXA e fluoxetina em combinação em pacientes AVISOS E PRECAUÇÕES e Uso em populações específicas ].
Necessidade de programa de tratamento abrangente em pacientes pediátricos
ZYPREXA 20mg é indicado como parte integrante de um programa de tratamento total para pacientes pediátricos com esquizofrenia e transtorno bipolar que pode incluir outras medidas (psicológicas, educacionais, sociais) para pacientes com o transtorno. A eficácia e a segurança de ZYPREXA 7,5mg não foram estabelecidas em pacientes pediátricos com menos de 13 anos de idade. Os antipsicóticos atípicos não se destinam ao uso em pacientes pediátricos que apresentam sintomas secundários a fatores ambientais e/ou outros distúrbios psiquiátricos primários. A colocação educacional apropriada é essencial e a intervenção psicossocial é muitas vezes útil. A decisão de prescrever medicação antipsicótica atípica dependerá da avaliação do profissional de saúde quanto à cronicidade e gravidade dos sintomas do paciente [ver INDICAÇÕES E USO ].
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Carcinogênese
Estudos de carcinogenicidade oral foram realizados em camundongos e ratos. A olanzapina foi administrada a camundongos em dois estudos de 78 semanas em doses de 3, 10, 30/20 mg/kg/dia (equivalente a 0,8-5 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal) e 0,25, 2 , 8 mg/kg/dia (equivalente a 0,06-2 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal). Os ratos foram administrados durante 2 anos em doses de 0,25, 1, 2,5, 4 mg/kg/dia (machos) e 0,25, 1, 4, 8 mg/kg/dia (fêmeas) (equivalente a 0,13-2 e 0,13-4 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal, respectivamente). A incidência de hemangiomas e hemangiossarcomas do fígado aumentou significativamente em 1 estudo em camundongos fêmeas com 2 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal. Esses tumores não foram aumentados em outro estudo em camundongos em fêmeas com doses de até 2-5 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal; neste estudo, houve alta incidência de mortalidade precoce em homens do grupo 30/20 mg/kg/dia. A incidência de adenomas e adenocarcinomas da glândula mamária foi significativamente aumentada em camundongos fêmeas com doses ≥2 mg/kg/dia e em ratas com doses ≥4 mg/kg/dia (0,5 e 2 vezes a MRHD oral diária com base em mg/m² superfície corporal, respectivamente). Fármacos antipsicóticos demonstraram elevar cronicamente os níveis de prolactina em roedores. Os níveis séricos de prolactina não foram medidos durante os estudos de carcinogenicidade da olanzapina; entretanto, medições durante estudos de toxicidade subcrônica mostraram que a olanzapina elevou os níveis séricos de prolactina em até 4 vezes em ratos nas mesmas doses usadas no estudo de carcinogenicidade. Um aumento nas neoplasias da glândula mamária foi encontrado em roedores após a administração crônica de outras drogas antipsicóticas e é considerado mediado pela prolactina. A relevância para o risco humano da descoberta de tumores endócrinos mediados por prolactina em roedores é desconhecida [ver AVISOS E PRECAUÇÕES ].
Mutagênese
Nenhuma evidência de potencial genotóxico para olanzapina foi encontrada no teste de mutação reversa de Ames, teste de micronúcleo in vivo em camundongos, teste de aberração cromossômica em células de ovário de hamster chinês, teste de síntese de DNA não programado em hepatócitos de rato, teste de indução de mutação direta em células de linfoma de camundongo , ou teste de troca de cromátides irmãs in vivo na medula óssea de hamsters chineses.
Prejuízo da Fertilidade
Em um estudo de fertilidade oral e desempenho reprodutivo em ratos, o desempenho de acasalamento dos machos, mas não a fertilidade, foi prejudicado com uma dose de 22,4 mg/kg/dia e a fertilidade feminina foi diminuída com uma dose de 3 mg/kg/dia (11 e 1,5 mg/kg/dia). vezes a MRHD oral diária com base em mg/m² de área de superfície corporal, respectivamente). A descontinuação do tratamento com olanzapina reverteu os efeitos no desempenho de acasalamento dos machos. Em ratas, o período pré-coital foi aumentado e o índice de acasalamento reduzido em 5 mg/kg/dia (2,5 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal). O diestro foi prolongado e o estro atrasado em 1,1 mg/kg/dia (0,6 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal); portanto, a olanzapina pode produzir um atraso na ovulação.
Uso em populações específicas
Ao usar ZYPREXA e fluoxetina em combinação, consulte também a seção Uso em populações específicas do folheto informativo do Symbyax.
Gravidez
Registro de Exposição à Gravidez
Existe um registro de exposição à gravidez que monitora os resultados da gravidez em mulheres expostas a antipsicóticos atípicos, incluindo ZYPREXA, durante a gravidez. Os profissionais de saúde são incentivados a registrar pacientes entrando em contato com o Registro Nacional de Gravidez para Antipsicóticos Atípicos em 1-866-961-2388 ou visite http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/.
Resumo do risco
Recém-nascidos expostos a medicamentos antipsicóticos, incluindo ZYPREXA, durante o terceiro trimestre estão em risco de sintomas extrapiramidais e/ou de abstinência após o parto (ver Considerações Clínicas ). Os dados gerais disponíveis de estudos epidemiológicos publicados de mulheres grávidas expostas à olanzapina não estabeleceram um risco associado ao medicamento de defeitos congênitos graves, aborto espontâneo ou resultados maternos ou fetais adversos (ver Dados ). Existem riscos para a mãe associados à esquizofrenia não tratada ou transtorno bipolar I e à exposição a antipsicóticos, incluindo ZYPREXA 7,5 mg, durante a gravidez (ver Considerações Clínicas ).
A olanzapina não foi teratogênica quando administrada oralmente a ratas e coelhas grávidas em doses que são 9 e 30 vezes a dose oral máxima diária recomendada para humanos (MRHD), com base em mg/m² de área de superfície corporal; algumas toxicidades fetais foram observadas com essas doses (ver Dados ).
O risco de fundo estimado de grandes defeitos congênitos e aborto para as populações indicadas é desconhecido. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, o risco de fundo estimado de defeitos congênitos graves e aborto espontâneo em gestações clinicamente reconhecidas é de 2% a 4% e 15% a 20%, respectivamente.
Considerações Clínicas
Risco Materno e Embrio/Fetal Associado à Doença
Existe um risco para a mãe de esquizofrenia não tratada ou transtorno bipolar I, incluindo aumento do risco de recaída, hospitalização e suicídio. A esquizofrenia e o transtorno bipolar I estão associados ao aumento de resultados perinatais adversos, incluindo parto prematuro. Não se sabe se isso é resultado direto da doença ou de outros fatores comórbidos.
Reações Adversas Fetais/Neonatais
Sintomas extrapiramidais e/ou de abstinência, incluindo agitação, hipertonia, hipotonia, tremor, sonolência, dificuldade respiratória e distúrbios alimentares foram relatados em recém-nascidos que foram expostos a medicamentos antipsicóticos, incluindo ZYPREXA 2,5 mg, durante o terceiro trimestre de gravidez. Esses sintomas têm variado em gravidade. Monitore os neonatos quanto a sintomas extrapiramidais e/ou de abstinência e gerencie os sintomas adequadamente. Alguns neonatos se recuperaram em horas ou dias sem tratamento específico; outros necessitaram de hospitalização prolongada.
Dados
Dados humanos
passagem placentária foi relatada em relatórios de estudos publicados; no entanto, a taxa de passagem placentária foi altamente variável, variando entre 7% a 167% no nascimento após a exposição durante a gravidez. A relevância clínica deste achado é desconhecida.
Dados publicados de estudos observacionais, registros de nascimento e relatos de casos que avaliaram o uso de antipsicóticos atípicos durante a gravidez não estabelecem um risco aumentado de defeitos congênitos maiores. Um estudo de coorte retrospectivo de um banco de dados Medicaid de 9.258 mulheres expostas a antipsicóticos durante a gravidez não indicou um aumento geral do risco de defeitos congênitos graves.
Dados de animais
Em estudos de reprodução oral em ratos com doses de até 18 mg/kg/dia e em coelhos com doses de até 30 mg/kg/dia (9 e 30 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal, respectivamente), nenhuma evidência de teratogenicidade foi observada. Em um estudo de teratologia oral em ratos, reabsorções precoces e aumento do número de fetos inviáveis foram observados com uma dose de 18 mg/kg/dia (9 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal), e a gestação foi prolongada em 10 mg/kg/dia (5 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal). Em um estudo de teratologia oral em coelhos, a toxicidade fetal manifestada como reabsorções aumentadas e diminuição do peso fetal ocorreu com uma dose tóxica materna de 30 mg/kg/dia (30 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal).
Lactação
Resumo do risco
olanzapina está presente no leite humano. Existem relatos de sedação excessiva, irritabilidade, má alimentação e sintomas extrapiramidais (tremores e movimentos musculares anormais) em lactentes expostos à olanzapina através do leite materno (ver Considerações Clínicas ). Não há informações sobre os efeitos da olanzapina na produção de leite.
Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica de ZYPREXA da mãe e quaisquer efeitos adversos potenciais do ZYPREXA na criança amamentada ou da condição subjacente da mãe.
Considerações Clínicas
Lactentes expostos a ZYPREXA 7,5mg devem ser monitorados quanto a sedação excessiva, irritabilidade, má alimentação e sintomas extrapiramidais (tremores e movimentos musculares anormais).
Fêmeas e Machos com Potencial Reprodutivo
Infertilidade
Mulheres
Com base na ação farmacológica da olanzapina (antagonismo do receptor D2), o tratamento com ZYPREXA pode resultar em aumento nos níveis séricos de prolactina, o que pode levar a uma redução reversível da fertilidade em mulheres com potencial reprodutivo [ver AVISOS E PRECAUÇÕES ].
Uso Pediátrico
A segurança e eficácia de ZYPREXA oral no tratamento da esquizofrenia e episódios maníacos ou mistos associados ao transtorno bipolar I foram estabelecidas em estudos de curto prazo em adolescentes (idades de 13 a 17 anos). O uso de ZYPREXA em adolescentes é apoiado por evidências de estudos adequados e bem controlados de ZYPREXA 5mg nos quais 268 adolescentes receberam ZYPREXA 20mg em uma faixa de 2,5 a 20 mg/dia [ver Estudos clínicos ]. A dose inicial recomendada para adolescentes é menor do que para adultos [ver DOSAGEM E ADMINISTRAÇÃO ]. Em comparação com pacientes de estudos clínicos em adultos, os adolescentes provavelmente ganharam mais peso, experimentaram aumento da sedação e tiveram maiores aumentos nos níveis de colesterol total, triglicerídeos, colesterol LDL, prolactina e aminotransferase hepática. AVISOS E PRECAUÇÕES e REAÇÕES ADVERSAS ]. Ao decidir entre os tratamentos alternativos disponíveis para adolescentes, os médicos devem considerar o aumento do potencial (em adolescentes em comparação com adultos) para ganho de peso e dislipidemia. Os médicos devem considerar os riscos potenciais a longo prazo ao prescrever a adolescentes e, em muitos casos, isso pode levá-los a considerar a prescrição de outros medicamentos primeiro em adolescentes [ver INDICAÇÕES E USO ].
A segurança e eficácia da olanzapina em crianças INFORMAÇÃO DO PACIENTE ].
segurança e eficácia de ZYPREXA 7,5 mg e fluoxetina em combinação em crianças e adolescentes (10 a 17 anos de idade) foram estabelecidas para o tratamento agudo de episódios depressivos associados ao transtorno bipolar I.
A segurança e eficácia de ZYPREXA e fluoxetina em combinação em crianças
Uso Geriátrico
Dos 2.500 pacientes em estudos clínicos pré-comercialização com olanzapina oral, 11% (263) tinham 65 anos de idade ou mais. Em pacientes com esquizofrenia, não houve indicação de qualquer tolerabilidade diferente da olanzapina em idosos em comparação com pacientes mais jovens. Estudos em pacientes idosos com psicose relacionada à demência sugeriram que pode haver um perfil de tolerabilidade diferente nessa população em comparação com pacientes mais jovens com esquizofrenia. Pacientes idosos com psicose relacionada à demência tratados com olanzapina apresentam risco aumentado de morte em comparação ao placebo. Em estudos controlados com placebo de olanzapina em pacientes idosos com psicose relacionada à demência, houve uma maior incidência de eventos adversos cerebrovasculares (por exemplo, acidente vascular cerebral, ataque isquêmico transitório) em pacientes tratados com olanzapina em comparação com pacientes tratados com placebo. A olanzapina não está aprovada para o tratamento de pacientes com psicose relacionada à demência. Além disso, a presença de fatores que podem diminuir a depuração farmacocinética ou aumentar a resposta farmacodinâmica à olanzapina deve levar à consideração de uma dose inicial mais baixa para qualquer paciente geriátrico [ver AVISO EM CAIXA , DOSAGEM E ADMINISTRAÇÃO , e AVISOS E PRECAUÇÕES ].
Os estudos clínicos de ZYPREXA e fluoxetina em combinação não incluíram um número suficiente de pacientes ≥65 anos de idade para determinar se eles respondem de forma diferente dos pacientes mais jovens.
SOBREDOSAGEM
Experiência Humana
Em estudos de pré-comercialização envolvendo mais de 3.100 pacientes e/ou indivíduos normais, a superdosagem aguda acidental ou intencional de olanzapina foi identificada em 67 pacientes. No paciente que tomou a maior quantidade identificada, 300 mg, os únicos sintomas relatados foram sonolência e fala arrastada. No número limitado de pacientes que foram avaliados em hospitais, incluindo o paciente tomando 300 mg, não houve observações indicando uma alteração adversa nos analitos laboratoriais ou no ECG. Os sinais vitais estavam geralmente dentro dos limites normais após superdosagem.
Em notificações pós-comercialização de superdosagem com olanzapina isolada, os sintomas foram relatados na maioria dos casos. Em pacientes sintomáticos, os sintomas com incidência ≥10% incluíram agitação/agressividade, disartria, taquicardia, vários sintomas extrapiramidais e redução do nível de consciência variando de sedação a coma. Entre os sintomas menos comumente relatados estavam as seguintes reações potencialmente graves do ponto de vista médico: aspiração, parada cardiorrespiratória, arritmias cardíacas (como taquicardia supraventricular e 1 paciente apresentando pausa sinusal com retomada espontânea do ritmo normal), delírio, possível síndrome neuroléptica maligna, depressão/parada respiratória , convulsão, hipertensão e hipotensão. Eli Lilly and Company recebeu relatos de fatalidade em associação com overdose de olanzapina isoladamente. Em 1 caso de morte, a quantidade de olanzapina ingerida agudamente foi relatada como sendo possivelmente tão baixa quanto 450 mg de olanzapina oral; entretanto, em outro caso, foi relatado que um paciente sobreviveu a uma ingestão aguda de olanzapina de aproximadamente 2 g de olanzapina oral.
Gerenciamento de overdose
Para obter informações atualizadas sobre o manejo da overdose de ZYPREXA (olanzapina), entre em contato com um centro de controle de envenenamento certificado (1-800-222-1222 ou www.poison.org). A possibilidade de envolvimento de múltiplas drogas deve ser considerada. Em caso de superdosagem aguda, estabeleça e mantenha uma via aérea e assegure oxigenação e ventilação adequadas, que podem incluir intubação. Deve-se considerar a lavagem gástrica (após a intubação, se o paciente estiver inconsciente) e a administração de carvão ativado junto com um laxante. A administração de carvão ativado (1 g) reduziu a Cmax e a AUC da olanzapina oral em cerca de 60%. Como os níveis máximos de olanzapina não são normalmente obtidos até cerca de 6 horas após a dosagem, o carvão pode ser um tratamento útil para a superdosagem de olanzapina.
possibilidade de obnubilação, convulsões ou reação distônica da cabeça e pescoço após superdosagem pode criar risco de aspiração com vômito induzido. O monitoramento cardiovascular deve começar imediatamente e deve incluir monitoramento eletrocardiográfico contínuo para detectar possíveis arritmias.
Não há antídoto específico para a olanzapina. Portanto, medidas de suporte apropriadas devem ser iniciadas. Hipotensão e colapso circulatório devem ser tratados com medidas apropriadas, como fluidos intravenosos e/ou agentes simpaticomiméticos. (Não use epinefrina, dopamina ou outros simpaticomiméticos com atividade beta-agonista, pois a estimulação beta pode piorar a hipotensão no contexto de bloqueio alfa induzido por olanzapina). Supervisão médica e monitoramento rigorosos devem continuar até que o paciente se recupere.
Para obter informações específicas sobre superdosagem com lítio ou valproato, consulte a seção Superdosagem das bulas desses produtos. Para informações específicas sobre superdosagem com olanzapina e fluoxetina em combinação, consulte a seção Superdosagem do folheto informativo de Symbyax.
CONTRA-INDICAÇÕES
- Nenhum com monoterapia com ZYPREXA.
- Ao usar ZYPREXA e fluoxetina em combinação, consulte também a seção Contra-indicações do folheto informativo do Symbyax.
- Para obter informações específicas sobre as contraindicações do lítio ou valproato, consulte a seção Contraindicações das bulas desses outros produtos.
FARMACOLOGIA CLÍNICA
Mecanismo de ação
O mecanismo de ação da olanzapina, nas indicações listadas, não é claro. No entanto, a eficácia da olanzapina na esquizofrenia pode ser mediada por uma combinação de antagonismo de dopamina e serotonina tipo 2 (5HT2).
Farmacodinâmica
olanzapina se liga com alta afinidade aos seguintes receptores: serotonina 5HT2A/2C, 5HT6 (Ki=4, 11 e 5 nM, respectivamente), dopamina D1-4 (Ki=11-31 nM), histamina H1 (Ki=7 nM ), e receptores adrenérgicos α1 (Ki = 19 nM). A olanzapina é um antagonista com afinidade moderada de ligação para serotonina 5HT3 (Ki=57 nM) e M1-5 muscarínico (Ki=73, 96, 132, 32 e 48 nM, respectivamente). A olanzapina liga-se com baixa afinidade aos receptores GABAA, BZD e β-adrenérgicos (Ki>10 μM).
Farmacocinética
Administração Oral, Monoterapia
A olanzapina é bem absorvida e atinge o pico de concentração em aproximadamente 6 horas após uma dose oral. É eliminado extensivamente por metabolismo de primeira passagem, com aproximadamente 40% da dose metabolizada antes de atingir a circulação sistêmica. Os alimentos não afetam a taxa ou extensão da absorção da olanzapina. Os estudos farmacocinéticos mostraram que as formas farmacêuticas de ZYPREXA 5mg comprimidos e ZYPREXA ZYDIS (comprimidos de desintegração oral de olanzapina) de olanzapina são bioequivalentes.
olanzapina apresenta cinética linear ao longo da faixa de dosagem clínica. Sua meia-vida varia de 21 a 54 horas (5º a 95º percentil; média de 30 horas), e a depuração plasmática aparente varia de 12 a 47 L/h (5º a 95º percentil; média de 25 L/h).
A administração de olanzapina uma vez ao dia leva a concentrações no estado de equilíbrio em cerca de 1 semana que são aproximadamente o dobro das concentrações após doses únicas. As concentrações plasmáticas, a meia-vida e a depuração da olanzapina podem variar entre os indivíduos com base no tabagismo, sexo e idade.
A olanzapina é amplamente distribuída por todo o corpo, com um volume de distribuição de aproximadamente 1.000 L. Liga-se 93% às proteínas plasmáticas na faixa de concentração de 7 a 1.100 ng/mL, ligando-se principalmente à albumina e α1-glicoproteína ácida.
Metabolismo e eliminação
Após uma dose oral única de olanzapina marcada com 14C, 7% da dose de olanzapina foi recuperada na urina como droga inalterada, indicando que a olanzapina é altamente metabolizada. Aproximadamente 57% e 30% da dose foi recuperada na urina e nas fezes, respectivamente. No plasma, a olanzapina representou apenas 12% da AUC da radioatividade total, indicando exposição significativa a metabólitos. Após doses múltiplas, os principais metabólitos circulantes foram o 10-N-glicuronídeo, presente em estado de equilíbrio em 44% da concentração de olanzapina, e 4´-N-desmetil olanzapina, presente em estado de equilíbrio em 31% da concentração de olanzapina. . Ambos os metabolitos carecem de actividade farmacológica nas concentrações observadas.
glucuronidação direta e a oxidação mediada pelo citocromo P450 (CYP) são as principais vias metabólicas da olanzapina. Estudos in vitro sugerem que os CYPs 1A2 e 2D6 e o sistema monooxigenase contendo flavina estão envolvidos na oxidação da olanzapina. A oxidação mediada por CYP2D6 parece ser uma via metabólica menor in vivo, porque a depuração da olanzapina não é reduzida em indivíduos com deficiência dessa enzima.
Administração intramuscular
ZYPREXA IntraMuscular resulta em rápida absorção com picos de concentração plasmática ocorrendo em 15 a 45 minutos. Com base em um estudo farmacocinético em voluntários saudáveis, uma dose de 5 mg de olanzapina intramuscular para injeção produz, em média, uma concentração plasmática máxima aproximadamente 5 vezes maior do que a concentração plasmática máxima produzida por uma dose de 5 mg de olanzapina oral. A área sob a curva obtida após uma dose intramuscular é semelhante à obtida após a administração oral da mesma dose. A meia-vida observada após administração intramuscular é semelhante à observada após administração oral. A farmacocinética é linear ao longo da faixa de dosagem clínica. Os perfis metabólicos após administração intramuscular são qualitativamente semelhantes aos perfis metabólicos após administração oral.
Populações Específicas
Insuficiência renal
Como a olanzapina é altamente metabolizada antes da excreção e apenas 7% do fármaco é excretado inalterado, é improvável que a disfunção renal isolada tenha um grande impacto na farmacocinética da olanzapina. As características farmacocinéticas da olanzapina foram semelhantes em pacientes com insuficiência renal grave e indivíduos normais, indicando que não é necessário ajuste de dose com base no grau de insuficiência renal. Além disso, a olanzapina não é removida por diálise. O efeito da insuficiência renal na eliminação de metabólitos não foi estudado.
Insuficiência hepática
Embora a presença de insuficiência hepática possa reduzir a depuração da olanzapina, um estudo do efeito da insuficiência hepática em indivíduos (n=6) com cirrose clinicamente significativa (classificação de Childs Pugh A e B) revelou pouco efeito sobre a farmacocinética de olanzapina.
Geriátrico
Em um estudo envolvendo 24 indivíduos saudáveis, a meia-vida média de eliminação da olanzapina foi cerca de 1,5 vezes maior em idosos (≥65 anos) do que em não idosos ( DOSAGEM E ADMINISTRAÇÃO ].
Gênero
A depuração da olanzapina é aproximadamente 30% menor nas mulheres do que nos homens. Não houve, no entanto, diferenças aparentes entre homens e mulheres na eficácia ou efeitos adversos. Modificações de dosagem com base no sexo não devem ser necessárias.
Condição de fumante
A depuração da olanzapina é cerca de 40% maior em fumantes do que em não fumantes, embora modificações de dosagem não sejam rotineiramente recomendadas.
Corrida
Estudos in vivo mostraram que as exposições são semelhantes entre japoneses, chineses e caucasianos, especialmente após a normalização das diferenças de peso corporal. Modificações de dosagem para raça não são, portanto, recomendadas.
Efeitos combinados
Os efeitos combinados de idade, tabagismo e sexo podem levar a diferenças farmacocinéticas substanciais nas populações. A depuração em homens jovens fumantes, por exemplo, pode ser 3 vezes maior do que em mulheres idosas não fumantes. A modificação da dosagem pode ser necessária em pacientes que apresentam uma combinação de fatores que podem resultar em metabolismo mais lento da olanzapina [ver DOSAGEM E ADMINISTRAÇÃO ].
Adolescentes (13 a 17 anos)
Em estudos clínicos, a maioria dos adolescentes não era fumante e essa população tinha um peso corporal médio mais baixo, o que resultou em uma exposição média à olanzapina mais alta em comparação com os adultos.
Toxicologia e/ou Farmacologia Animal
Em estudos em animais com olanzapina, os principais achados hematológicos foram citopenias periféricas reversíveis em cães individuais com dose de 10 mg/kg (17 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal), diminuições relacionadas à dose em linfócitos e neutrófilos em camundongos , e linfopenia em ratos. Alguns cães tratados com 10 mg/kg desenvolveram neutropenia reversível e/ou anemia hemolítica reversível entre 1 e 10 meses de tratamento. Foram observadas diminuições relacionadas com a dose em linfócitos e neutrófilos em ratinhos que receberam doses de 10 mg/kg (igual a 2 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal) em estudos de 3 meses de duração. Linfopenia inespecífica, consistente com diminuição do ganho de peso corporal, ocorreu em ratos que receberam 22,5 mg/kg (11 vezes a MRHD oral diária com base em mg/m² de área de superfície corporal) por 3 meses ou 16 mg/kg (8 vezes a MRHD oral diária com base em em mg/m² de superfície corporal) por 6 ou 12 meses. Nenhuma evidência de citotoxicidade da medula óssea foi encontrada em nenhuma das espécies examinadas. As medulas ósseas eram normocelulares ou hipercelulares, indicando que as reduções nas células sanguíneas circulantes eram provavelmente devidas a fatores periféricos (não medulares).
Estudos clínicos
Ao usar ZYPREXA 7,5 mg e fluoxetina em combinação, consulte também a seção de Estudos Clínicos do folheto informativo do Symbyax.
Esquizofrenia
Adultos
eficácia da olanzapina oral no tratamento da esquizofrenia foi estabelecida em 2 estudos controlados de curto prazo (6 semanas) de pacientes adultos internados que preenchiam os critérios do DSM III-R para esquizofrenia. Um único braço de haloperidol foi incluído como tratamento comparativo em 1 dos 2 estudos, mas este estudo não comparou esses 2 medicamentos em toda a gama de doses clinicamente relevantes para ambos.
Vários instrumentos foram utilizados para avaliar sinais e sintomas psiquiátricos nesses estudos, entre eles a Escala de Avaliação Psiquiátrica Breve (BPRS), um inventário multi-item de psicopatologia geral tradicionalmente usado para avaliar os efeitos do tratamento medicamentoso na esquizofrenia. O cluster de psicose BPRS (desorganização conceitual, comportamento alucinatório, suspeita e conteúdo de pensamento incomum) é considerado um subconjunto particularmente útil para avaliar pacientes esquizofrênicos ativamente psicóticos. Uma segunda avaliação tradicional, a Impressão Clínica Global (CGI), reflete a impressão de um observador habilidoso, totalmente familiarizado com as manifestações da esquizofrenia, sobre o estado clínico geral do paciente. Além disso, foram empregadas 2 escalas desenvolvidas mais recentemente; estes incluíram a Escala de Sintomas Positivos e Negativos de 30 itens (PANSS), na qual estão incorporados os 18 itens da BPRS, e a Escala de Avaliação de Sintomas Negativos (SANS). Os resumos dos ensaios abaixo se concentram nos seguintes resultados: total de PANSS e/ou total de BPRS; cluster de psicose BPRS; subescala negativa PANSS ou SANS; e Gravidade CGI. Seguem os resultados dos testes:
(1) Em um estudo controlado por placebo de 6 semanas (n = 149) envolvendo 2 doses fixas de olanzapina de 1 e 10 mg/dia (uma vez ao dia), olanzapina, a 10 mg/dia (mas não a 1 mg/dia). dia), foi superior ao placebo na pontuação total da PANSS (também no total da BPRS extraída), no grupo de psicose BPRS, na subescala negativa da PANSS e na gravidade CGI.
(2) Em um estudo controlado por placebo de 6 semanas (n=253) envolvendo 3 faixas de doses fixas de olanzapina (5 ± 2,5 mg/dia, 10 ± 2,5 mg/dia e 15 ± 2,5 mg/dia) em um uma vez ao dia, os 2 grupos de dose mais alta de olanzapina (doses médias reais de 12 e 16 mg/dia, respectivamente) foram superiores ao placebo no escore total de BPRS, cluster de psicose BPRS e escore de gravidade CGI; o grupo de dose mais alta de olanzapina foi superior ao placebo no SANS. Não houve vantagem clara para o grupo de alta dose sobre o grupo de dose média.
(3) Em um estudo de longo prazo, pacientes ambulatoriais adultos (n=326) que preenchiam predominantemente os critérios do DSM-IV para esquizofrenia e que permaneceram estáveis com olanzapina durante o tratamento aberto por pelo menos 8 semanas foram randomizados para continuar com a olanzapina atual doses (variando de 10 a 20 mg/dia) ou ao placebo. O período de acompanhamento para observar pacientes para recidiva, definido em termos de aumento nos sintomas positivos de BPRS ou hospitalização, foi planejado para 12 meses, no entanto, os critérios foram atendidos para interromper o estudo precocemente devido a um excesso de recaídas de placebo em comparação com recaídas de olanzapina , e a olanzapina foi superior ao placebo no momento da recaída, o desfecho primário para este estudo. Assim, a olanzapina foi mais eficaz que o placebo na manutenção da eficácia em pacientes estabilizados por aproximadamente 8 semanas e acompanhados por um período de observação de até 8 meses.
O exame de subconjuntos populacionais (raça e gênero) não revelou qualquer responsividade diferencial com base nesses subgrupos.
Adolescentes
eficácia da olanzapina oral no tratamento agudo da esquizofrenia em adolescentes (idades de 13 a 17 anos) foi estabelecida em um estudo duplo-cego, controlado por placebo, randomizado de 6 semanas de pacientes internados e ambulatoriais com esquizofrenia (n = 107) que atenderam critérios diagnósticos de acordo com o DSM-IV-TR e confirmados pelo Kiddie Schedule for Affective Disorders and Schizophrenia for School Aged Children-Present and Lifetime Version (K-SADS-PL).
O instrumento de classificação primário usado para avaliar sinais e sintomas psiquiátricos neste estudo foi a versão ancorada da pontuação total da Escala de Avaliação Psiquiátrica Breve para Crianças (BPRS-C).
Neste ensaio de dose flexível, a olanzapina 2,5 a 20 mg/dia (dose modal média 12,5 mg/dia, dose média de 11,1 mg/dia) foi mais eficaz do que o placebo no tratamento de adolescentes diagnosticados com esquizofrenia, conforme corroborado pelo estudo estatístico redução média significativamente maior na pontuação total de BPRS-C para pacientes no grupo de tratamento com olanzapina do que no grupo placebo.
Embora não haja evidências disponíveis para responder à questão de quanto tempo o paciente adolescente tratado com ZYPREXA deve ser mantido, a eficácia de manutenção pode ser extrapolada a partir de dados de adultos juntamente com comparações dos parâmetros farmacocinéticos da olanzapina em pacientes adultos e adolescentes. Geralmente, é recomendado que os pacientes que responderam continuem além da resposta aguda, mas na dose mais baixa necessária para manter a remissão. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção.
Transtorno Bipolar I (episódios maníacos ou mistos)
Adultos
Monoterapia
eficácia da olanzapina oral no tratamento de episódios maníacos ou mistos foi estabelecida em 2 estudos controlados por placebo de curto prazo (um de 3 semanas e um de 4 semanas) em pacientes adultos que preencheram os critérios do DSM-IV para transtorno bipolar I com episódios maníacos ou mistos. Esses estudos incluíram pacientes com ou sem características psicóticas e com ou sem ciclo rápido.
O instrumento de classificação primário usado para avaliar os sintomas maníacos nesses estudos foi a Young Mania Rating Scale (Y-MRS), uma escala de 11 itens tradicionalmente usada para avaliar o grau de sintomatologia maníaca (irritabilidade, comportamento disruptivo/agressivo, sono , humor elevado, fala, atividade aumentada, interesse sexual, transtorno de linguagem/pensamento, conteúdo de pensamento, aparência e insight) em uma faixa de 0 (sem características maníacas) a 60 Â (pontuação máxima). O resultado primário nestes estudos foi a alteração da linha de base no escore total Y-MRS. Seguem os resultados dos testes:
(1) Em um estudo controlado por placebo de 3 semanas (n=67) que envolveu uma faixa de dose de olanzapina (5-20 mg/dia, uma vez ao dia, começando com 10 mg/dia), a olanzapina foi superior ao placebo no redução do escore total Y-MRS. Em um estudo de desenho idêntico realizado simultaneamente com o primeiro estudo, a olanzapina demonstrou uma diferença de tratamento semelhante, mas possivelmente devido ao tamanho da amostra e à variabilidade do local, não se mostrou superior ao placebo nesse desfecho.
(2) Em um estudo controlado por placebo de 4 semanas (n=115) que envolveu uma faixa de dose de olanzapina (5-20 mg/dia, uma vez ao dia, começando com 15 mg/dia), a olanzapina foi superior ao placebo no redução do escore total Y-MRS.
(3) Em outro estudo, 361 pacientes que preencheram os critérios do DSM-IV para um episódio maníaco ou misto de transtorno bipolar I que responderam durante uma fase inicial de tratamento aberto por cerca de 2 semanas, em média, à olanzapina 5 a 20 mg/ dia foram randomizados para a continuação da olanzapina na mesma dose (n=225) ou placebo (n=136), para observação de recaída. Aproximadamente 50% dos pacientes descontinuaram o grupo olanzapina no dia 59 e 50% do grupo placebo descontinuaram no dia 23 do tratamento duplo-cego. A resposta durante a fase de rótulo aberto foi definida por uma diminuição do escore total Y-MRS para ≤12 e HAM-D 21 para ≤8. A recaída durante a fase duplo-cega foi definida como um aumento do escore total Y-MRS ou HAM-D 21 para ≥15, ou hospitalização por mania ou depressão. Na fase randomizada, os pacientes que receberam olanzapina contínua apresentaram um tempo significativamente maior para recaída.
Adjuvante ao lítio ou valproato
eficácia da olanzapina oral com lítio ou valproato concomitante no tratamento de episódios maníacos ou mistos foi estabelecida em 2 estudos controlados em pacientes que preenchiam os critérios do DSM-IV para transtorno bipolar I com episódios maníacos ou mistos. Esses estudos incluíram pacientes com ou sem características psicóticas e com ou sem ciclo rápido. Seguem os resultados dos testes:
(1) Em um estudo de combinação controlado por placebo de 6 semanas, 175 pacientes ambulatoriais em terapia com lítio ou valproato com sintomas maníacos ou mistos inadequadamente controlados (Y-MRS ≥16) foram randomizados para receber olanzapina ou placebo, em combinação com sua terapia original . Olanzapina (em uma faixa de dose de 5-20 mg/dia, uma vez ao dia, começando com 10 mg/dia) combinada com lítio ou valproato (em uma faixa terapêutica de 0,6 mEq/L a 1,2 mEq/L ou 50 μg/mL a 125 μg/mL, respectivamente) foi superior ao lítio ou valproato sozinho na redução do escore total Y-MRS.
(2) Em um segundo estudo de combinação placebo-controlado de 6 semanas, 169 pacientes ambulatoriais em terapia com lítio ou valproato com sintomas maníacos ou mistos inadequadamente controlados (Y-MRS ≥16) foram randomizados para receber olanzapina ou placebo, em combinação com o tratamento original. terapia. Olanzapina (em uma faixa de dose de 5-20 mg/dia, uma vez ao dia, começando com 10 mg/dia) combinada com lítio ou valproato (em uma faixa terapêutica de 0,6 mEq/L a 1,2 mEq/L ou 50 μg/mL a 125 μg/mL, respectivamente) foi superior ao lítio ou valproato sozinho na redução do escore total Y-MRS.
Adolescentes
Monoterapia Aguda
eficácia da olanzapina oral no tratamento de episódios maníacos agudos ou mistos em adolescentes (idades de 13 a 17 anos) foi estabelecida em um estudo randomizado, duplo-cego, controlado por placebo, de 3 semanas com adolescentes internados e ambulatoriais que preencheram o diagnóstico critérios para episódios maníacos ou mistos associados ao transtorno bipolar I (com ou sem características psicóticas) de acordo com o DSM-IV-TR (n=161). O diagnóstico foi confirmado pelo K-SADS-PL.
O instrumento de classificação primário usado para avaliar os sintomas maníacos neste estudo foi a pontuação total da Escala de Classificação de Young-Mania Estruturada do Adolescente (Y-MRS).
Neste ensaio de dose flexível, a olanzapina 2,5 a 20 mg/dia (dose modal média 10,7 mg/dia, dose média de 8,9 mg/dia) foi mais eficaz do que o placebo no tratamento de adolescentes com episódios maníacos ou mistos associados ao transtorno bipolar I transtorno, como apoiado pela redução média estatisticamente significativamente maior no escore total Y-MRS para pacientes no grupo de tratamento com olanzapina do que no grupo placebo.
Embora não haja evidências disponíveis para responder à questão de quanto tempo o paciente adolescente tratado com ZYPREXA deve ser mantido, a eficácia de manutenção pode ser extrapolada a partir de dados de adultos juntamente com comparações dos parâmetros farmacocinéticos da olanzapina em pacientes adultos e adolescentes. Geralmente, é recomendado que os pacientes que responderam continuem além da resposta aguda, mas na dose mais baixa necessária para manter a remissão. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de tratamento de manutenção.
Agitação associada à esquizofrenia e mania bipolar I
eficácia da injeção intramuscular de olanzapina para o tratamento da agitação foi estabelecida em 3 estudos controlados por placebo de curto prazo (24 horas de tratamento IM) em pacientes adultos agitados internados de 2 grupos de diagnóstico: esquizofrenia e transtorno bipolar I (episódios maníacos ou mistos) . Cada um dos ensaios incluiu um único braço de tratamento comparador ativo de injeção de haloperidol (estudos de esquizofrenia) ou injeção de lorazepam (estudo de mania bipolar I). Os pacientes inscritos nos estudos precisavam ser: (1) julgados pelos investigadores clínicos como clinicamente agitados e candidatos clinicamente apropriados para tratamento com medicação intramuscular e (2) exibindo um nível de agitação que atingisse ou excedesse uma pontuação limite de ≥14 em os 5 itens que compõem o Componente Excitado da Escala de Síndrome Positiva e Negativa (PANSS) (ou seja, itens de controle de impulso ruim, tensão, hostilidade, falta de cooperação e excitação) com pelo menos 1 item individual pontuação ≥4 usando um sistema de pontuação de 1-7 (1 = ausente, 4=moderado, 7=extremo). Nos estudos, a pontuação média inicial do PANSS Excited Component foi de 18,4, com pontuações variando de 13 a 32 (de uma pontuação máxima de 35), sugerindo níveis predominantemente moderados de agitação com alguns pacientes apresentando níveis leves ou graves de agitação. A medida de eficácia primária utilizada para avaliar os sinais e sintomas de agitação nestes ensaios foi a alteração da linha de base no Componente Excitado PANSS 2 horas após a injeção. Os pacientes podem receber até 3 injeções durante os períodos de tratamento IM de 24 horas; no entanto, os pacientes não puderam receber a segunda injeção até após o período inicial de 2 horas, quando a medida de eficácia primária foi avaliada. Seguem os resultados dos testes:
(1) Em um estudo controlado por placebo em pacientes agitados que atendem aos critérios do DSM-IV para esquizofrenia (n=270), foram avaliadas 4 doses fixas de olanzapina intramuscular para injeção de 2,5 mg, 5 mg, 7,5 mg e 10 mg. Todas as doses foram estatisticamente superiores ao placebo no PANSS Excited Component 2 horas após a injeção. No entanto, o efeito foi maior e mais consistente para as 3 doses mais altas. Não houve diferenças significativas aos pares para as doses de 7,5 e 10 mg em relação à dose de 5 mg.
(2) Em um segundo estudo controlado por placebo em pacientes internados agitados que atendem aos critérios do DSM-IV para esquizofrenia (n=311), foi avaliada 1 olanzapina intramuscular fixa para injeção de 10 mg. A olanzapina injetável foi estatisticamente superior ao placebo no PANSS Excited Component 2 horas após a injeção.
(3) Em um estudo controlado por placebo em pacientes internados agitados que atendem aos critérios do DSM-IV para transtorno bipolar I (e atualmente apresentando um episódio maníaco agudo ou misto com ou sem características psicóticas) (n=201), 1 olanzapina intramuscular fixa para dose injetável de 10 mg foi avaliada. A olanzapina injetável foi estatisticamente superior ao placebo no PANSS Excited Component 2 horas após a injeção.
O exame de subconjuntos populacionais (idade, raça e sexo) não revelou qualquer responsividade diferencial com base nesses subgrupos.
INFORMAÇÃO DO PACIENTE
ZYPREXA® (zy-PREX-a) (olanzapina) Comprimido
ZYPREXA® ZYDIS® (zy-PREX-a ZY-dis) (olanzapina) Comprimido, Desintegrante Oral
Leia o Guia de Medicação que acompanha o ZYPREXA antes de começar a tomá-lo e sempre que receber um reabastecimento. Pode haver novas informações. Este Guia de Medicação não substitui a conversa com seu médico sobre sua condição médica ou tratamento. Converse com seu médico ou farmacêutico se houver algo que você não entenda ou se quiser saber mais sobre ZYPREXA.
Quais são as informações mais importantes que devo saber sobre ZYPREXA?
ZYPREXA 20mg pode causar efeitos colaterais graves, incluindo:
Esses efeitos colaterais graves são descritos abaixo.
1. Aumento do risco de morte em idosos confusos, com perda de memória e perda de contato com a realidade (psicose relacionada à demência). ZYPREXA não está aprovado para o tratamento de psicose em idosos com demência.
2. Açúcar elevado no sangue (hiperglicemia). Açúcar elevado no sangue pode acontecer se você já tem diabetes ou se nunca teve diabetes. Açúcar elevado no sangue pode levar a:
- um acúmulo de ácido no sangue devido a cetonas (cetoacidose)
- coma
- morte
seu médico deve fazer testes para verificar o seu nível de açúcar no sangue antes de começar a tomar ZYPREXA 7,5 mg e durante o tratamento. Em pessoas que não têm diabetes, às vezes o açúcar elevado no sangue desaparece quando ZYPREXA 7,5 mg é interrompido. Pessoas com diabetes e algumas pessoas que não tinham diabetes antes de tomar ZYPREXA precisam tomar remédios para açúcar elevado no sangue mesmo depois de parar de tomar ZYPREXA.
Se você tem diabetes, siga as instruções do seu médico sobre a frequência de checagem do seu açúcar no sangue enquanto estiver tomando ZYPREXA.
Ligue para o seu médico se tiver algum destes sintomas de açúcar elevado no sangue (hiperglicemia) enquanto estiver a tomar ZYPREXA:
- sinto muita sede
- necessidade de urinar mais do que o habitual
- sinto muita fome
- sentir-se fraco ou cansado
- sentir-se mal do estômago
- sente-se confuso ou seu hálito cheira a fruta
3. Níveis elevados de gordura no sangue (colesterol e triglicérides). Níveis elevados de gordura podem ocorrer em pessoas tratadas com ZYPREXA 10mg, especialmente em adolescentes (13 a 17 anos), ou quando usado em combinação com fluoxetina em crianças (10 a 17 anos). Você pode não ter nenhum sintoma, portanto, seu médico deve fazer exames de sangue para verificar seus níveis de colesterol e triglicerídeos antes de começar a tomar ZYPREXA e durante o tratamento.
4. Ganho de peso. O ganho de peso é muito comum em pessoas que tomam ZYPREXA. Adolescentes (13 a 17 anos) são mais propensos a ganhar peso e ganhar mais peso do que os adultos. As crianças (10 a 17 anos) também são mais propensas a ganhar peso e a ganhar mais peso do que os adultos quando ZYPREXA 7,5 mg é usado em combinação com fluoxetina. Algumas pessoas podem ganhar muito peso enquanto tomam ZYPREXA, então você e seu médico devem verificar seu peso regularmente. Converse com seu médico sobre maneiras de controlar o ganho de peso, como comer uma dieta saudável e equilibrada e se exercitar.
O que é ZYPREXA?
ZYPREXA é um medicamento de prescrição usado para tratar:
- esquizofrenia em pessoas com 13 anos ou mais.
- transtorno bipolar, incluindo:
- episódios maníacos ou mistos que ocorrem com transtorno bipolar I em pessoas com 13 anos ou mais.
- episódios maníacos ou mistos que ocorrem com transtorno bipolar I, quando usado com o medicamento lítio ou valproato, em adultos.
- tratamento a longo prazo do transtorno bipolar I em adultos.
- episódios de depressão que ocorrem com transtorno bipolar I, quando usado com o medicamento fluoxetina (Prozac®) em pessoas com 10 anos ou mais.
- episódios de depressão que não melhoram após 2 outros medicamentos, também chamados de depressão resistente ao tratamento, quando usados com o medicamento fluoxetina (Prozac), em adultos.
ZYPREXA 7,5 mg não foi aprovado para uso em crianças com menos de 13 anos de idade. ZYPREXA 10mg em combinação com fluoxetina não foi aprovado para uso em crianças com menos de 10 anos de idade.
Os sintomas da esquizofrenia incluem ouvir vozes, ver coisas que não existem, ter crenças que não são verdadeiras e ser desconfiado ou retraído.
Os sintomas do transtorno bipolar I incluem períodos alternados de depressão e humor elevado ou irritável, aumento da atividade e inquietação, pensamentos acelerados, fala rápida, comportamento impulsivo e diminuição da necessidade de sono.
Os sintomas da depressão resistente ao tratamento incluem diminuição do humor, diminuição do interesse, aumento dos sentimentos de culpa, diminuição da energia, diminuição da concentração, alterações no apetite e pensamentos ou comportamentos suicidas.
Alguns dos seus sintomas podem melhorar com o tratamento. Se você acha que não está melhorando, ligue para o seu médico.
O que devo dizer ao meu médico antes de tomar ZYPREXA?
ZYPREXA pode não ser adequado para você. Antes de iniciar ZYPREXA, informe o seu médico se você tem ou teve:
- Problemas cardíacos
- convulsões
- diabetes ou níveis elevados de açúcar no sangue (hiperglicemia)
- níveis elevados de colesterol ou triglicérides no sangue
- problemas de fígado
- pressão arterial baixa ou alta
- AVCs ou “mini-derrames” também chamados de ataques isquêmicos transitórios (TIAs)
- Doença de Alzheimer
- glaucoma de ângulo estreito
- próstata aumentada em homens
- obstrução intestinal
- fenilcetonúria, porque ZYPREXA 5mg ZYDIS contém fenilalanina
- câncer de mama
- pensamentos de suicídio ou de se machucar
- qualquer outra condição médica
- estão grávidas ou planejam engravidar. Não se sabe se ZYPREXA 2,5 mg prejudicará o feto.
- Se você engravidar enquanto estiver recebendo ZYPREXA 20mg, converse com seu médico sobre o registro no Registro Nacional de Gravidez para Antipsicóticos Atípicos. Você pode se registrar ligando para 1-866-961-2388 ou acesse http://womensmentalhealth.org/clinical-andresearch-programs/pregnancyregistry/.
- está amamentando ou planeja amamentar. ZYPREXA passa para o leite materno. Fale com o seu médico sobre a melhor forma de alimentar o seu bebé se estiver a tomar ZYPREXA.
Informe o seu médico se você se exercita muito ou está em lugares quentes com frequência.
Os sintomas do transtorno bipolar I, depressão resistente ao tratamento ou esquizofrenia podem incluir pensamentos de suicídio ou de ferir a si mesmo ou aos outros. Se você tiver esses pensamentos a qualquer momento, informe seu médico ou dirija-se a uma sala de emergência imediatamente.
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos e não prescritos, vitaminas e suplementos de ervas. ZYPREXA 20mg e alguns medicamentos podem interagir entre si e não funcionar tão bem, ou causar possíveis efeitos colaterais graves. O seu médico pode dizer-lhe se é seguro tomar ZYPREXA com outros medicamentos. Não inicie ou pare qualquer medicamento enquanto estiver a tomar ZYPREXA sem falar primeiro com o seu médico.
Como devo tomar ZYPREXA 7,5mg?
- Tome ZYPREXA exatamente como prescrito. Seu médico pode precisar alterar (ajustar) a dose de ZYPREXA 15mg até que seja adequada para você.
- Se você esquecer de uma dose de ZYPREXA 20mg, tome a dose esquecida assim que se lembrar. Se estiver quase na hora da próxima dose, simplesmente pule a dose esquecida e tome a próxima dose no horário regular. Não tome duas doses de ZYPREXA 10mg ao mesmo tempo.
- Para evitar efeitos colaterais graves, não pare de tomar ZYPREXA repentinamente. Se você precisar parar de tomar ZYPREXA, seu médico pode lhe dizer como parar de tomá-lo com segurança.
- Se você tomar muito ZYPREXA, ligue para o seu médico ou centro de controle de envenenamento em 1-800-222-1222 imediatamente, ou obtenha tratamento de emergência.
- ZYPREXA 10mg pode ser tomado com ou sem alimentos.
- ZYPREXA é geralmente tomado uma vez por dia.
- Tome ZYPREXA 20mg ZYDIS da seguinte forma:
- Certifique-se de que suas mãos estejam secas.
- Abra a saqueta e retire a película do blister. Não empurre o comprimido através da folha.
- Assim que abrir o blister, retire o comprimido e coloque-o na boca.
- comprimido se desintegrará rapidamente em sua saliva para que você possa engoli-lo facilmente com ou sem beber líquido.
- Ligue para o seu médico se achar que não está melhorando ou se tiver dúvidas sobre sua condição enquanto estiver tomando ZYPREXA.
O que devo evitar ao tomar ZYPREXA?
- ZYPREXA pode causar sonolência e afetar sua capacidade de tomar decisões, pensar com clareza ou reagir rapidamente. Você não deve dirigir, operar máquinas pesadas ou realizar outras atividades perigosas até saber como ZYPREXA 7,5mg o afeta.
- Evite beber álcool enquanto estiver tomando ZYPREXA. Beber álcool enquanto você toma ZYPREXA pode deixá-lo mais sonolento do que se você tomasse ZYPREXA 15mg sozinho.
Quais são os possíveis efeitos colaterais do ZYPREXA 5mg?
Efeitos colaterais graves podem ocorrer quando você toma ZYPREXA 5mg, incluindo:
- Consulte “Qual é a informação mais importante que devo saber sobre ZYPREXA?”, que descreve o risco aumentado de morte em idosos com psicose relacionada à demência e os riscos de açúcar elevado no sangue, níveis elevados de colesterol e triglicérides e ganho de peso.
- Aumento da incidência de acidente vascular cerebral ou “mini-derrames” chamados ataques isquêmicos transitórios (AITs) em idosos com psicose relacionada à demência (idosos que perderam o contato com a realidade devido à confusão e perda de memória). ZYPREXA não está aprovado para esses pacientes.
- Síndrome Neuroléptica Maligna (SNM): A SNM é uma condição rara, mas muito grave, que pode ocorrer em pessoas que tomam medicamentos antipsicóticos, incluindo ZYPREXA. NMS pode causar a morte e deve ser tratado em um hospital. Ligue para o seu médico imediatamente se ficar gravemente doente e tiver algum destes sintomas:
- febre alta
- suor excessivo
- músculos rígidos
- confusão
- alterações na respiração, batimentos cardíacos e pressão arterial.
- Reação Medicamentosa com Eosinofilia e Sintomas Sistêmicos (DRESS): DRESS pode ocorrer com ZYPREXA. As características do DRESS podem incluir erupção cutânea, febre, glândulas inchadas e envolvimento de outros órgãos internos, como fígado, rim, pulmão e coração. DRESS às vezes é fatal; portanto, informe imediatamente o seu médico se sentir algum destes sinais.
- Discinesia tardia: Essa condição causa movimentos corporais que continuam acontecendo e que você não pode controlar. Esses movimentos geralmente afetam a face e a língua. A discinesia tardia pode não desaparecer, mesmo que você pare de tomar ZYPREXA. Também pode começar depois que você parar de tomar ZYPREXA. Informe o seu médico se tiver quaisquer movimentos corporais que não consiga controlar.
- Diminuição da pressão arterial quando você muda de posição, com sintomas de tontura, batimentos cardíacos rápidos ou lentos ou desmaios.
- Dificuldade em engolir, que pode fazer com que alimentos ou líquidos entrem nos pulmões.
- Convulsões: Informe o seu médico se tiver convulsões durante o tratamento com ZYPREXA.
- Problemas com o controle da temperatura corporal: Você pode ficar muito quente, por exemplo, quando se exercita muito ou fica em uma área muito quente. É importante que você beba água para evitar a desidratação. Ligue para o seu médico imediatamente se ficar gravemente doente e tiver algum destes sintomas de desidratação:
- suando muito ou nada
- boca seca
- sentindo muito calor
- sentindo sede
- incapaz de produzir urina.
Os efeitos colaterais comuns do ZYPREXA incluem: falta de energia, boca seca, aumento do apetite, sonolência, tremores, fezes duras ou pouco frequentes, tonturas, alterações de comportamento ou inquietação.
Outros efeitos colaterais comuns em adolescentes (13-17 anos) incluem: dor de cabeça, dor na área do estômago (abdominal), dor nos braços ou pernas ou cansaço. Os adolescentes experimentaram maiores aumentos na prolactina, enzimas hepáticas e sonolência, em comparação com os adultos.
Informe o seu médico sobre qualquer efeito colateral que o incomode ou que não desapareça.
Estes não são todos os efeitos colaterais possíveis com ZYPREXA. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar o ZYPREXA?
- Armazene ZYPREXA em temperatura ambiente, entre 20°C e 25°C (68°F a 77°F).
- Mantenha ZYPREXA longe da luz.
- Mantenha ZYPREXA 15mg seco e longe da umidade.
Mantenha ZYPREXA 5mg e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre ZYPREXA
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use ZYPREXA para uma condição para a qual não foi prescrito. Não dê ZYPREXA 5mg a outras pessoas, mesmo que tenham a mesma condição. Pode prejudicá-los.
Este Guia de Medicação resume as informações mais importantes sobre ZYPREXA. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre ZYPREXA 20mg que foram escritas para profissionais de saúde. Para obter mais informações sobre o ZYPREXA, ligue para 1-800-Lilly-Rx (1-800-545-5979).
Quais são os ingredientes de ZYPREXA?
Ingrediente ativo: olanzapina
Ingredientes inativos:
cera de carnaúba, crospovidona, hidroxipropilcelulose, hipromelose, lactose, estearato de magnésio, celulose microcristalina e outros ingredientes inativos. O revestimento colorido contém: Dióxido de Titânio, Laca de Alumínio Azul FD&C No. 2 ou Óxido de Ferro Vermelho Sintético.
ZYDIS - gelatina, manitol, aspartame, metil parabeno de sódio e propil parabeno de sódio.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
