Cipro 1000mg, 250mg, 500mg, 750mg Ciprofloxacin Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Cipro 750mg e como é usado?
Cipro 500mg é um medicamento de prescrição usado para tratar os sintomas de infecções bacterianas. Cipro pode ser usado sozinho ou com outros medicamentos.
Cipro pertence a uma classe de medicamentos chamados fluoroquinolonas.
Não se sabe se Cipro 750mg é seguro e eficaz em crianças menores de 1 ano de idade.
Quais são os possíveis efeitos colaterais do Cipro?
Cipro pode causar efeitos colaterais graves, incluindo:
- Baixo teor de açúcar no sangue,
- dor de cabeça,
- fome,
- sudorese,
- irritabilidade,
- tontura,
- náusea,
- ritmo cardíaco acelerado,
- sentindo-se ansioso ou trêmulo,
- dormência nas mãos, braços, pernas ou pés,
- fraqueza,
- formigamento ou dor ardente,
- nervosismo,
- confusão,
- agitação,
- paranóia,
- alucinações,
- problemas de memória,
- dificuldade de concentração,
- pensamentos de suicídio,
- dor repentina,
- inchaço,
- contusões,
- ternura,
- rigidez,
- problemas de movimento,
- estalando ou estalando em qualquer articulação,
- dor forte ou constante no peito, estômago ou costas,
- diarreia aquosa ou sanguinolenta,
- vibrando em seu peito,
- falta de ar,
- tontura,
- irritação na pele,
- problemas respiratórios,
- pouca ou nenhuma micção,
- amarelecimento da pele ou dos olhos,
- dor de cabeça severa,
- zumbido em seus ouvidos,
- problemas de visão e
- dor atrás de seus olhos
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Cipro 1000mg incluem:
- náusea,
- vômito,
- diarréia,
- dor de estômago,
- coceira ou corrimento vaginal,
- dor de cabeça, e
- testes de função hepática anormais
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Cipro. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
REAÇÕES ADVERSAS GRAVES, INCLUINDO TENDINITE, RUPTURA DE TENDÃO, NEUROPATIA PERIFÉRICA, EFEITOS DO SISTEMA NERVOSO CENTRAL E EXACERBAÇÃO DE MIASTENIA GRAVIS
- As fluoroquinolonas, incluindo Cipro 250mg, foram associadas a reações adversas graves incapacitantes e potencialmente irreversíveis que ocorreram em conjunto [ver ADVERTÊNCIAS E PRECAUÇÕES], incluindo:
- Tendinite e ruptura de tendão [ver ADVERTÊNCIAS E PRECAUÇÕES]
- Neuropatia periférica [ver ADVERTÊNCIAS E PRECAUÇÕES]
- Efeitos no sistema nervoso central [ver ADVERTÊNCIAS E PRECAUÇÕES]
Descontinue Cipro 750mg imediatamente e evite o uso de fluoroquinolonas, incluindo Cipro, em pacientes que apresentarem qualquer uma dessas reações adversas graves [ver AVISOS E PRECAUÇÕES ]
- Fluoroquinolonas, incluindo Cipro 750mg, podem exacerbar a fraqueza muscular em pacientes com miastenia gravis. Evite Cipro em pacientes com história conhecida de miastenia gravis. [ver ADVERTÊNCIAS E PRECAUÇÕES]
- Como as fluoroquinolonas, incluindo CIPRO 500mg, foram associadas a reações adversas graves [ver ADVERTÊNCIAS E PRECAUÇÕES], reserve CIPRO para uso em pacientes que não têm opções alternativas de tratamento para infecções do trato urinário não complicadas [ver INDICAÇÕES]
DESCRIÇÃO
Cipro (cipro 750mgfloxacina*) comprimidos de liberação prolongada contém cipro 500mgfloxacina, um agente antimicrobiano sintético para administração oral. Os comprimidos de Cipro 1000mg são comprimidos revestidos de duas camadas que consistem em uma camada de liberação imediata e uma camada de liberação controlada do tipo matriz de erosão. Os comprimidos contêm uma combinação de dois tipos de substância medicamentosa ciprofloxacina, cloridrato de ciprofloxacina e ciprofloxacina betaína (base). Cipro 750 mg de cloridrato de floxacina é cloridrato de ácido 1-ciclopropil-6-fluoro-1,4di-hidro-4-oxo-7-(1-piperazinil)-3-quinolinocarboxílico. É fornecido como uma mistura do monohidrato e do sesquihidrato. A fórmula empírica do monohidrato é C17H18FN3O3. HCl. H2O e seu peso molecular é 385,8. A fórmula empírica do sesquihidrato é C17H18FN3O3. HCl. 1,5 H2O e seu peso molecular é 394,8. A substância do fármaco é uma substância cristalina levemente amarelada a amarela clara. A estrutura química do monohidrato é a seguinte:
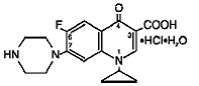
Cipro 1000mgfloxacina betaína é ácido 1-ciclopropil-6-fluoro-1, 4-di-hidro-4-oxo-7-(1-piperazinil)-3-quinolinocarboxílico. Como hidrato, sua fórmula empírica é C17H18FN3O3. 3,5 H2O e seu peso molecular é 394,3. É uma substância cristalina amarela clara a amarela clara e sua estrutura química é a seguinte:
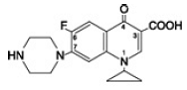
Cipro está disponível nas dosagens de comprimidos de 500 mg e 1000 mg (equivalente a 500 mg de floxacina de cipro). Os comprimidos de Cipro são comprimidos oblongos, revestidos por película, quase brancos a ligeiramente amarelados. Cada comprimido de Cipro 500 mg contém 500 mg de ciprofloxacina sob a forma de ciprofloxacina HCl (287,5 mg, calculado como ciprofloxacina em base seca) e cipro 1000 mgfloxacina† (212,6 mg, calculado em base seca). Cada comprimido de Cipro 1000 mg contém 1000 mg de ciprofloxacina sob a forma de ciprofloxacina HCl (574,9 mg, calculado como ciprofloxacina em base seca) e cipro 750 mgfloxacina† (425,2 mg, calculado em base seca). Os ingredientes inativos são crospovidona, hipromelose, estearato de magnésio, polietilenoglicol, sílica coloidal anidra, ácido succínico e dióxido de titânio.
* uma vez que cipro 500mgfloxacina† e cipro 250mgfloxacina cloridrato † não está em conformidade com o teste de perda por secagem e resíduo no teste de ignição da monografia da USP.
INDICAÇÕES
Infecções da pele e da estrutura da pele
CIPRO 1000mg é indicado em pacientes adultos para o tratamento de infecções da pele e estruturas da pele causadas por Escherichia coli, Klebsiella pneumoniae, Enterobacter cloacae, Proteus mirabilis, Proteus vulgaris, Providencia stuartii, Morganella morganii, Citrobacter freundii, Pseudomonas aeruginosa, Staphylococcus aureus sensível à meticilina, Staphylococcus epidermidis sensível à meticilina ou Streptococcus pyogenes.
Infecções ósseas e articulares
CIPRO 750mg é indicado em pacientes adultos para o tratamento de infecções ósseas e articulares causadas por Enterobacter cloacae, Serratia marcescens ou Pseudomonas aeruginosa.
Infecções Intra-Abdominais Complicadas
CIPRO 250mg é indicado em pacientes adultos para o tratamento de infecções intra-abdominais complicadas (usadas em combinação com metronidazol) causadas por Escherichia coli, Pseudomonas aeruginosa, Proteus mirabilis, Klebsiella pneumoniae ou Bacteroides fragilis.
Diarréia Infecciosa
CIPRO 500mg é indicado em pacientes adultos para tratamento de diarreia infecciosa causada por Escherichia coli (isolados enterotoxigênicos), Campylobacter jejuni, Shigella boydii †, Shigella dysenteriae, Shigella flexneri ou Shigella sonnei† quando a terapia antibacteriana é indicada.
†Embora o tratamento de infecções causadas por este organismo neste sistema de órgãos tenha demonstrado um resultado clinicamente significativo, a eficácia foi estudada em menos de 10 pacientes.
Febre tifóide (febre entérica)
CIPRO 1000mg é indicado em pacientes adultos para o tratamento da febre tifoide (febre entérica) causada por Salmonella typhi. A eficácia da ciprofloxacina na erradicação do estado de portador de febre tifóide crônica não foi demonstrada.
Gonorreia Cervical e Uretral Não Complicada
CIPRO é indicado em pacientes adultos para tratamento de gonorreia cervical e uretral não complicada por Neisseria gonorrhoeae [ver AVISOS E PRECAUÇÕES ].
Antraz por inalação (pós-exposição)
CIPRO 250mg é indicado em pacientes adultos e pediátricos desde o nascimento até 17 anos de idade para antraz por inalação (pós-exposição) para reduzir a incidência ou progressão da doença após exposição ao Bacillus anthracis aerossolizado.
As concentrações séricas de cipro 500 mgfloxacina alcançadas em humanos serviram como um desfecho substituto razoavelmente provável para prever o benefício clínico e forneceram a base inicial para a aprovação desta indicação. 2001 [ver Estudos clínicos ].
Praga
CIPRO 1000mg é indicado para o tratamento da peste, incluindo peste pneumônica e septicêmica, por Yersinia pestis (Y. pestis) e profilaxia da peste em adultos e pacientes pediátricos desde o nascimento até os 17 anos de idade. Estudos de eficácia de cipro 250mgfloxacina não puderam ser realizados em humanos com peste por razões de viabilidade. Portanto, esta indicação é baseada em um estudo de eficácia realizado apenas em animais [ver Estudos clínicos ].
Prostatite Bacteriana Crônica
CIPRO é indicado em pacientes adultos para tratamento de prostatite bacteriana crônica causada por Escherichia coli ou Proteus mirabilis.
Infecções do Trato Respiratório Inferior
CIPRO 750mg é indicado em pacientes adultos para o tratamento de infecções do trato respiratório inferior causadas por Escherichia coli, Klebsiella pneumoniae, Enterobacter cloacae, Proteus mirabilis, Pseudomonas aeruginosa, Haemophilus influenzae, Haemophilus parainfluenzae ou Streptococcus pneumoniae.
CIPRO não é uma droga de primeira escolha no tratamento de pneumonia presumida ou confirmada secundária a Streptococcus pneumoniae.
CIPRO é indicado para o tratamento de exacerbações agudas de bronquite crônica (AECB) causadas por Moraxella catarrhalis.
Como as fluoroquinolonas, incluindo CIPRO, foram associadas a reações adversas graves [ver AVISOS E PRECAUÇÕES ] e para alguns pacientes o ACE é autolimitado, reserve CIPRO 750mg para tratamento do ACE em pacientes que não têm opções alternativas de tratamento.
Infecções do trato urinário
Infecções do Trato Urinário em Adultos
CIPRO 500mg é indicado em pacientes adultos para o tratamento de infecções do trato urinário causadas por Escherichia coli, Klebsiella pneumoniae, Enterobacter cloacae, Serratia marcescens, Proteus mirabilis, Providencia rettgeri, Morganella morganii, Citrobacter koseri, Citrobacter freundii, Pseudomonas aeruginosa, Staphylococcus epidermidis sensível à meticilina , Staphylococcus saprophyticus ou Enterococcus faecalis.
Cistite Aguda Não Complicada
CIPRO 750mg é indicado em pacientes adultas do sexo feminino para tratamento de cistite aguda não complicada causada por Escherichia coli ou Staphylococcus saprophyticus.
Como as fluoroquinolonas, incluindo CIPRO, foram associadas a reações adversas graves [ver AVISOS E PRECAUÇÕES ] e para alguns pacientes a cistite aguda não complicada é autolimitada, reserve CIPRO para o tratamento da cistite aguda não complicada em pacientes que não têm opções alternativas de tratamento.
Infecção urinária complicada e pielonefrite em pacientes pediátricos
CIPRO é indicado em pacientes pediátricos de 1 a 17 anos de idade para o tratamento de infecções complicadas do trato urinário (ITUc) e pielonefrite por Escherichia coli. Uso em populações específicas ].
Embora eficaz em ensaios clínicos, CIPRO não é um medicamento de primeira escolha na população pediátrica devido ao aumento da incidência de reações adversas em comparação com os controles, incluindo reações relacionadas às articulações e/ou tecidos circundantes. CIPRO 250mg, como outras fluoroquinolonas, está associado a artropatia e alterações histopatológicas nas articulações de sustentação de peso de animais juvenis [ver AVISOS E PRECAUÇÕES , REAÇÕES ADVERSAS , Uso em populações específicas e Toxicologia não clínica ].
Sinusite aguda
CIPRO é indicado em pacientes adultos para o tratamento de sinusite aguda causada por Haemophilus influenzae, Streptococcus pneumoniae ou Moraxella catarrhalis.
Como as fluoroquinolonas, incluindo CIPRO, foram associadas a reações adversas graves [ver AVISOS E PRECAUÇÕES ] e para alguns pacientes a sinusite aguda é autolimitada, reserve CIPRO para o tratamento da sinusite aguda em pacientes que não têm opções alternativas de tratamento.
Uso
Para reduzir o desenvolvimento de bactérias resistentes a medicamentos e manter a eficácia de CIPRO 1000mg e outros medicamentos antibacterianos, CIPRO 500mg deve ser usado apenas para tratar ou prevenir infecções comprovadas ou fortemente suspeitas de serem causadas por bactérias suscetíveis. Quando as informações de cultura e suscetibilidade estiverem disponíveis, elas devem ser consideradas na seleção ou modificação da terapia antibacteriana. Na ausência de tais dados, a epidemiologia local e os padrões de suscetibilidade podem contribuir para a seleção empírica da terapia.
Se houver suspeita de organismos anaeróbios que contribuem para a infecção, deve ser administrada terapia apropriada. Cultura apropriada e testes de sensibilidade devem ser realizados antes do tratamento para isolar e identificar organismos causadores de infecção e determinar sua suscetibilidade ao ciprofloxacino. A terapia com CIPRO pode ser iniciada antes que os resultados desses testes sejam conhecidos; assim que os resultados estiverem disponíveis, a terapia apropriada deve ser continuada.
Assim como com outras drogas, alguns isolados de Pseudomonas aeruginosa podem desenvolver resistência rapidamente durante o tratamento com cipro 1000mgfloxacino. A cultura e os testes de suscetibilidade realizados periodicamente durante a terapia fornecerão informações não apenas sobre o efeito terapêutico do agente antimicrobiano, mas também sobre o possível surgimento de resistência bacteriana.
DOSAGEM E ADMINISTRAÇÃO
CIPRO 1000mg Comprimidos e Suspensão Oral devem ser administrados por via oral conforme descrito nas tabelas de Diretrizes de Dosagem apropriadas.
Dosagem em Adultos
determinação da dosagem e duração para qualquer paciente em particular deve levar em consideração a gravidade e natureza da infecção, a suscetibilidade do microrganismo causador, a integridade dos mecanismos de defesa do paciente e o estado da função renal e hepática. . CIPRO Tablets ou CIPRO para Suspensão Oral pode ser administrado a pacientes adultos quando clinicamente indicado a critério do médico. Administre CIPRO para Suspensão Oral usando a colher graduada embalada em conjunto [ver DOSAGEM E ADMINISTRAÇÃO ].
Conversão da dosagem IV para oral em adultos
Os pacientes cuja terapia é iniciada com CIPRO IV podem ser trocados para CIPRO 750mg Comprimidos ou Suspensão Oral quando clinicamente indicado a critério do médico (Tabela 2) [ver FARMACOLOGIA CLÍNICA ].
Dosagem em pacientes pediátricos
dosagem e a via inicial de terapia (isto é, IV ou oral) para ITUc ou pielonefrite devem ser determinadas pela gravidade da infecção. CIPRO deve ser administrado conforme descrito na Tabela 3. Administrar CIPRO para Suspensão Oral usando a colher graduada embalada em conjunto [ver DOSAGEM E ADMINISTRAÇÃO ].
Modificações de dosagem em pacientes com insuficiência renal
Cipro 250mgfloxacino é eliminado principalmente por excreção renal; entretanto, a droga também é metabolizada e parcialmente eliminada pelo sistema biliar do fígado e pelo intestino. Essas vias alternativas de eliminação do fármaco parecem compensar a excreção renal reduzida em pacientes com insuficiência renal. No entanto, algumas modificações de dosagem são recomendadas, particularmente para pacientes com disfunção renal grave. As diretrizes de dosagem para uso em pacientes com insuficiência renal são mostradas na Tabela 4.
Quando apenas a concentração de creatinina sérica é conhecida, as seguintes fórmulas podem ser usadas para estimar a depuração de creatinina:
creatinina sérica deve representar um estado de equilíbrio da função renal.
Em pacientes com infecções graves e insuficiência renal grave, uma dose unitária de 750 mg pode ser administrada nos intervalos indicados acima. Os pacientes devem ser cuidadosamente monitorados.
Pacientes pediátricos com insuficiência renal moderada a grave foram excluídos do ensaio clínico de ITUc e pielonefrite. Não há informações disponíveis sobre ajustes de dose necessários para pacientes pediátricos com insuficiência renal moderada a grave (ou seja, depuração de creatinina
Instruções importantes de administração
Com Cátions Multivalentes
Administrar CIPRO pelo menos 2 horas antes ou 6 horas após antiácidos de magnésio/alumínio; ligantes de fosfato poliméricos (por exemplo, sevelâmero, carbonato de lantânio) ou sucralfato; Comprimidos mastigáveis/tamponados Videx® (didanosina) ou pó pediátrico para solução oral; outras drogas altamente tamponadas; ou outros produtos que contenham cálcio, ferro ou zinco.
Com produtos lácteos
administração concomitante de CIPRO 500mg com produtos lácteos (como leite ou iogurte) ou apenas sucos fortificados com cálcio deve ser evitada, pois é possível diminuir a absorção; no entanto, CIPRO pode ser tomado com uma refeição que contenha esses produtos.
Hidratação de Pacientes Recebendo CIPRO
Assegurar a hidratação adequada dos pacientes que recebem CIPRO 1000mg para evitar a formação de urina altamente concentrada. Cristalúria foi relatada com quinolonas.
Instrua o paciente sobre a administração apropriada de CIPRO 1000mg [ver Informações de Aconselhamento do Paciente ].
Doses Perdidas
Se uma dose for esquecida, ela deve ser tomada a qualquer momento, mas não depois de 6 horas antes da próxima dose programada. Se faltarem menos de 6 horas para a próxima dose, a dose esquecida não deve ser tomada e o tratamento deve ser continuado conforme prescrito com a próxima dose programada. Doses duplas não devem ser tomadas para compensar uma dose esquecida.
Divisão de comprimidos CIPRO 1000mg
CIPRO 750mg comprimidos, 250 mg e 500 mg são comprimidos com ranhuras funcionais que podem ser divididos ao meio na linha ranhurada para fornecer uma dosagem de 125 mg e 250 mg, respectivamente.
Instruções para reconstituição das microcápsulas CIPRO 500mg para suspensão oral
CIPRO 750mg Suspensão Oral é fornecido em 5% (5 g de ciprofloxacina em 100 mL) e 10% (10 g de cipro 750mgfloxacina em 100 mL). CIPRO 250mg suspensão oral é composto por dois componentes (microcápsulas e diluente) que devem ser combinados antes da dispensação.
Preparação da suspensão
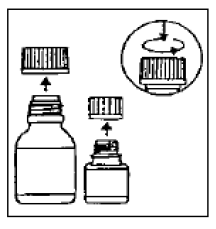
Passo 1
O frasco pequeno contém as microcápsulas, o frasco grande contém o diluente.

Passo 2
Abra as duas garrafas. Tampa à prova de crianças: Pressione para baixo de acordo com as instruções na tampa enquanto gira para a esquerda.

etapa 3
 Despeje as microcápsulas completamente no frasco maior de diluente. Não adicione água à suspensão .
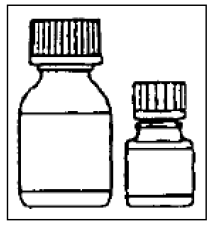
Passo 4
 Remova a camada superior do rótulo do frasco de diluente (para revelar o rótulo CIPRO 1000mg Oral Suspension). Feche o frasco grande completamente de acordo com as instruções na tampa e agite vigorosamente por cerca de 15 segundos. A suspensão está pronta para uso.
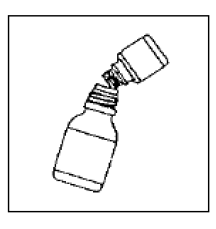
Etapa 5
Escreva a data de validade da suspensão oral reconstituída no rótulo do frasco.
O produto reconstituído pode ser armazenado abaixo de 30°C (86°F) por 14 dias. Proteger do congelamento.
Não devem ser feitas adições à suspensão final mista de ciprofloxacina. CIPRO 1000mg Suspensão Oral não deve ser administrado através de alimentação ou sondas NG (nasogástricas) devido às suas características físicas.
Instruções de administração para CIPRO para suspensão oral após reconstituição
- Agite a Suspensão Oral CIPRO 750mg vigorosamente cada vez antes de usar por aproximadamente 15 segundos.
- Administre a Suspensão Oral CIPRO usando a colher de chá graduada fornecida para o paciente (consulte a Figura 1)
Figura 1: colher de chá graduada de 5 mL embalada conjuntamente
A colher de chá graduada embalada em conjunto (5mL) é fornecida, com marcações para ½ (2,5 mL) e 1/1 (5 mL)
- Após o uso, lave a colher graduada em água corrente com detergente e seque bem.
- Não mastigue as microcápsulas da Suspensão Oral CIPRO 250mg, mas engula-as inteiras.
- A água pode ser tomada depois.
- Feche o frasco corretamente após cada uso de acordo com as instruções na tampa.
- Após a conclusão do tratamento, CIPRO 1000mg Suspensão Oral não deve ser reutilizado.
Dosagem de CIPRO para suspensão oral usando a colher co-embalada em adultos e pacientes pediátricos
COMO FORNECIDO
Formas de dosagem e pontos fortes
Comprimidos
- 250 mg, levemente amarelado, revestido por película, redondo, com ranhura funcional, impresso com “BAYER” de um lado e “CIP 250” do outro.
- 500 mg, levemente amarelado, revestido por película, em forma de cápsula, com ranhura funcional, impresso com “BAYER” de um lado e “CIP 500” do outro.
Suspensão oral
- Suspensão Oral 5%: 250 mg de cipro 750 mg de floxacina por 5 mL após reconstituição
- Suspensão Oral 10%: 500 mg de cipro 250 mg de floxacina por 5 mL após reconstituição
Armazenamento e manuseio
Os comprimidos CIPRO (cloridrato de cipro 750mgfloxacina) estão disponíveis na forma de comprimidos revestidos por película redondos, ligeiramente amarelados, contendo 250 mg de cipro 500mgfloxacina. O comprimido de 250 mg está codificado com a palavra “BAYER” de um lado e funcionalmente marcado e gravado com “CIP 250” no verso. CIPRO também está disponível em comprimidos revestidos por película em forma de cápsula, ligeiramente amarelados, contendo 500 mg de ciprofloxacina. O comprimido de 500 mg está codificado com a palavra “BAYER” de um lado e funcionalmente marcado e gravado com “CIP 500” no verso. CIPRO 250 mg e 500 mg estão disponíveis em frascos de 100.
Armazenar a 20° a 25°C (68° a 77°F); excursões permitidas de 15° a 30°C (59° a 86°F) [ver Temperatura ambiente controlada USP ].
CIPRO Suspensão Oral é fornecido em dosagens de 5% e 10%. O medicamento é composto por dois componentes (microcápsulas contendo o princípio ativo e diluente) que devem ser misturados pelo farmacêutico [ver DOSAGEM E ADMINISTRAÇÃO ].
Armazene as microcápsulas e o diluente abaixo de 25°C (77°F); são permitidas excursões de 15°C a 30°C (59°F a 86°F) [ver Temperatura ambiente controlada USP ]. Proteger do congelamento.
O produto reconstituído pode ser armazenado a 25°C (77°F) por 14 dias; são permitidas excursões de 15°C a 30°C (59°F a 86°F) [ver Temperatura ambiente controlada USP ]. Proteger do congelamento.
Uma colher de chá graduada (5mL) com marcações ½ (2,5 mL) e 1/1 (5 mL) é fornecida ao paciente.
REFERÊNCIAS
1. 21 CFR 314.510 (Subparte H – Aprovação acelerada de novos medicamentos para doenças que ameaçam a vida).
2. Friedman J, Polifka J. Efeitos teratogênicos de drogas: um recurso para clínicos (TERIS). Baltimore, Maryland: Johns Hopkins University Press, 2000:149-195.
3. Loebstein R, Addis A, Ho E, et al. Resultado da gravidez após exposição gestacional a fluoroquinolonas: um estudo multicêntrico prospectivo controlado. Agentes Antimicrobianos Quimioterápicos. 1998;42(6):1336-1339.
Fabricado para: Bayer HealthCare Pharmaceuticals Inc. Whippany, NJ 07981. Revisado: novembro de 2021
EFEITOS COLATERAIS
As seguintes reações adversas graves e importantes a medicamentos são discutidas em mais detalhes em outras seções da rotulagem:
- Reações adversas graves incapacitantes e potencialmente irreversíveis [consulte AVISOS E PRECAUÇÕES ]
- Tendinite e Ruptura de Tendão [ver AVISOS E PRECAUÇÕES ]
- Neuropatia periférica [ver AVISOS E PRECAUÇÕES ]
- Efeitos do Sistema Nervoso Central [ver AVISOS E PRECAUÇÕES ] Exacerbação da Miastenia Gravis [ver AVISOS E PRECAUÇÕES ]
- Outras reações adversas graves e às vezes fatais [ver AVISOS E PRECAUÇÕES ]
- Reações de hipersensibilidade [ver AVISOS E PRECAUÇÕES ]
- Hepatotoxicidade [ver AVISOS E PRECAUÇÕES ]
- Risco de aneurisma e dissecção da aorta [ver AVISOS E PRECAUÇÕES ]
- Reações Adversas Graves com Teofilina Concomitante [ver AVISOS E PRECAUÇÕES ]
- Diarreia Associada a Clostridioides difficile [ver AVISOS E PRECAUÇÕES ]
- Prolongamento do intervalo QT [ver AVISOS E PRECAUÇÕES ]
- Distúrbios musculoesqueléticos em pacientes pediátricos [ver AVISOS E PRECAUÇÕES ]
- Fotossensibilidade/fototoxicidade [ver AVISOS E PRECAUÇÕES ]
- Desenvolvimento de Bactérias Resistentes a Medicamentos [ver AVISOS E PRECAUÇÕES ]
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
Pacientes adultos
Durante as investigações clínicas com CIPRO oral e parenteral 750mg, 49.038 pacientes receberam cursos da droga.
As reações adversas relatadas com mais frequência, de ensaios clínicos de todas as formulações, todas as dosagens, todas as durações da terapia medicamentosa e para todas as indicações da terapia com ciprofloxacina foram náusea (2,5%), diarreia (1,6%), testes de função hepática anormais (1,3% ), vômitos (1%) e erupção cutânea (1%).
Em ensaios clínicos randomizados, duplo-cegos controlados comparando comprimidos CIPRO [500 mg duas vezes ao dia (BID)] com cefuroxima axetil (250 mg–500 mg BID) e claritromicina (500 mg BID) em pacientes com infecções do trato respiratório, CIPRO demonstrou um perfil de reações adversas do SNC comparável aos medicamentos de controle.
Pacientes pediátricos
segurança musculoesquelética e neurológica de curto (6 semanas) e longo prazo (1 ano) da ciprofloxacina oral/intravenosa foi comparada a uma cefalosporina para o tratamento de ITU ou pielonefrite em pacientes pediátricos de 1 a 17 anos de idade (idade média de 6 ± 4 anos ) em um estudo multicêntrico internacional. A duração da terapia foi de 10 a 21 dias (duração média do tratamento foi de 11 dias com intervalo de 1 a 88 dias). Um total de 335 pacientes tratados com cipro 250mgfloxacina e 349 com comparador foram inscritos.
Um Comitê Independente de Segurança Pediátrica (IPSC) revisou todos os casos de reações adversas musculoesqueléticas, incluindo marcha anormal ou exame articular anormal (inicial ou emergente do tratamento). Dentro de 6 semanas do início do tratamento, as taxas de reações adversas musculoesqueléticas foram de 9,3% (31/335) no grupo tratado com cipro 750mgfloxacina versus 6% (21/349) nos pacientes tratados com o comparador. Todas as reações adversas musculoesqueléticas que ocorreram em 6 semanas foram resolvidas (resolução clínica dos sinais e sintomas), geralmente dentro de 30 dias após o término do tratamento. As avaliações radiológicas não foram usadas rotineiramente para confirmar a resolução das reações adversas. Os pacientes tratados com Cipro 500mgfloxacino foram mais propensos a relatar mais de uma reação adversa e em mais de uma ocasião em comparação com os pacientes controle. A taxa de reações adversas musculoesqueléticas foi consistentemente maior no grupo da ciprofloxacina em comparação com o grupo controle em todos os subgrupos de idade. Ao final de 1 ano, a taxa dessas reações adversas relatadas a qualquer momento durante esse período foi de 13,7% (46/335) no grupo tratado com cipro 250mgfloxacina versus 9,5% (33/349) nos pacientes tratados com o comparador ( Tabela 9).
As taxas de incidência de reações adversas neurológicas dentro de 6 semanas do início do tratamento foram de 3% (9/335) no grupo CIPRO versus 2% (7/349) no grupo comparador e incluíram tontura, nervosismo, insônia e sonolência.
Neste estudo, as taxas globais de incidência de reações adversas dentro de 6 semanas após o início do tratamento foram de 41% (138/335) no grupo de cipro 250mgfloxacina versus 31% (109/349) no grupo comparador. As reações adversas mais frequentes foram gastrointestinais: 15% (50/335) dos pacientes com ciprofloxacina em comparação com 9% (31/349) dos pacientes comparadores. Reações adversas graves foram observadas em 7,5% (25/335) dos pacientes tratados com ciprofloxacina em comparação com 5,7% (20/349) dos pacientes de controle. A descontinuação do medicamento devido a uma reação adversa foi observada em 3% (10/335) dos pacientes tratados com ciprofloxacina versus 1,4% (5/349) dos pacientes comparadores. Outras reações adversas que ocorreram em pelo menos 1% dos pacientes com ciprofloxacina foram diarreia 4,8%, vômitos 4,8%, dor abdominal 3,3%, dispepsia 2,7%, náusea 2,7%, febre 2,1%, asma 1,8% e erupção cutânea 1,8%.
Dados de segurança de curto prazo para cipro 1000mgfloxacino também foram coletados em um ensaio clínico randomizado e duplo-cego para o tratamento de exacerbações pulmonares agudas em pacientes com fibrose cística (idades de 5 a 17 anos). Sessenta e sete pacientes receberam CIPRO IV 10 mg/kg/dose a cada 8 horas por uma semana seguido de CIPRO 250 mg comprimidos 20 mg/kg/dose a cada 12 horas para completar o tratamento de 10 a 21 dias e 62 pacientes receberam a combinação de ceftazidima intravenosa 50 mg/kg/dose a cada 8 horas e tobramicina intravenosa 3 mg/kg/dose a cada 8 horas por um total de 10-21 dias. Avaliações musculoesqueléticas periódicas foram conduzidas por examinadores cegos ao tratamento. Os pacientes foram acompanhados por uma média de 23 dias após o término do tratamento (intervalo de 0 a 93 dias). Reações adversas musculoesqueléticas foram relatadas em 22% dos pacientes no grupo da ciprofloxacina e 21% no grupo de comparação. A diminuição da amplitude de movimento foi relatada em 12% dos indivíduos do grupo ciprofloxacina e 16% no grupo de comparação. Artralgia foi relatada em 10% dos pacientes no grupo cipro 500mgfloxacino e 11% no grupo de comparação. Outras reações adversas foram semelhantes em natureza e frequência entre os braços de tratamento. A eficácia do CIPRO para o tratamento de exacerbações pulmonares agudas em pacientes pediátricos com fibrose cística não foi estabelecida.
Além das reações adversas relatadas em pacientes pediátricos em estudos clínicos, deve-se esperar que reações adversas relatadas em adultos durante os estudos clínicos ou experiência pós-comercialização também possam ocorrer em pacientes pediátricos.
Experiência pós-marketing
As seguintes reações adversas foram relatadas a partir da experiência de marketing mundial com fluoroquinolonas, incluindo CIPRO. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento (Tabela 10).
Alterações laboratoriais adversas
As alterações nos parâmetros laboratoriais durante o CIPRO 250mg estão listadas abaixo:
Hepático –Elevações de ALT (SGPT), AST (SGOT), fosfatase alcalina, LDH, bilirrubina sérica.
Hematologico –Eosinofilia, leucopenia, plaquetas sanguíneas diminuídas, plaquetas sanguíneas elevadas, pancitopenia.
Renal –Elevações de creatinina sérica, BUN, cristalúria, cilindrúria e hematúria foram relatadas.
Outras alterações que ocorreram foram: elevação da gamaglutamil transferase sérica, elevação da amilase sérica, redução da glicemia, elevação do ácido úrico, diminuição da hemoglobina, anemia, diátese hemorrágica, aumento dos monócitos no sangue e leucocitose.
INTERAÇÕES MEDICAMENTOSAS
A ciprofloxacina é um inibidor do metabolismo humano mediado pelo citocromo P450 1A2 (CYP1A2). A coadministração de CIPRO com outros medicamentos metabolizados principalmente pelo CYP1A2 resulta em aumento das concentrações plasmáticas desses medicamentos e pode levar a eventos adversos clinicamente significativos do medicamento coadministrado.
AVISOS
Incluído como parte do PRECAUÇÕES seção.
PRECAUÇÕES
Reações adversas graves incapacitantes e potencialmente irreversíveis, incluindo tendinite e ruptura de tendão, neuropatia periférica e efeitos no sistema nervoso central
As fluoroquinolonas, incluindo CIPRO, têm sido associadas a reações adversas graves incapacitantes e potencialmente irreversíveis de diferentes sistemas corporais que podem ocorrer em conjunto no mesmo paciente. As reações adversas comumente observadas incluem tendinite, ruptura de tendão, artralgia, mialgia, neuropatia periférica e efeitos no sistema nervoso central (alucinações, ansiedade, depressão, insônia, fortes dores de cabeça e confusão). Essas reações podem ocorrer dentro de horas a semanas após o início do CIPRO. Pacientes de qualquer idade ou sem fatores de risco pré-existentes apresentaram essas reações adversas [ver AVISOS E PRECAUÇÕES ].
Interrompa o CIPRO 250mg imediatamente aos primeiros sinais ou sintomas de qualquer reação adversa grave. Além disso, evite o uso de fluoroquinolonas, incluindo CIPRO 500mg, em pacientes que sofreram alguma dessas reações adversas graves associadas às fluoroquinolonas.
Tendinite e Ruptura de Tendão
As fluoroquinolonas, incluindo CIPRO, foram associadas a um risco aumentado de tendinite e ruptura de tendão em todas as idades [ver AVISOS E PRECAUÇÕES e REAÇÕES ADVERSAS ]. Esta reação adversa envolve mais frequentemente o tendão de Aquiles e também foi relatada com o manguito rotador (ombro), a mão, o bíceps, o polegar e outros tendões. Tendinite ou ruptura de tendão podem ocorrer horas ou dias após o início do CIPRO 500mg, ou até vários meses após a conclusão da terapia com fluoroquinolonas. Tendinite e ruptura de tendão podem ocorrer bilateralmente.
risco de desenvolver tendinite associada à fluoroquinolona e ruptura de tendão é maior em pacientes com mais de 60 anos de idade, em pacientes em uso de corticosteróides e em pacientes com transplante de rim, coração ou pulmão. Outros fatores que podem aumentar independentemente o risco de ruptura do tendão incluem atividade física extenuante, insuficiência renal e distúrbios anteriores do tendão, como artrite reumatóide. Tendinite e ruptura de tendão também ocorreram em pacientes em uso de fluoroquinolonas que não apresentam os fatores de risco acima. Interrompa o CIPRO 250mg imediatamente se o paciente sentir dor, inchaço, inflamação ou ruptura de um tendão. Evite fluoroquinolonas, incluindo CIPRO 250mg, em pacientes com histórico de distúrbios do tendão ou que sofreram tendinite ou ruptura do tendão [ver REAÇÕES ADVERSAS ].
Neuropatia periférica
As fluoroquinolonas, incluindo CIPRO, foram associadas a um risco aumentado de neuropatia periférica. Casos de polineuropatia axonal sensorial ou sensório-motora afetando axônios pequenos e/ou grandes resultando em parestesias, hipoestesias, disestesias e fraqueza foram relatados em pacientes recebendo fluoroquinolonas, incluindo CIPRO. Os sintomas podem ocorrer logo após o início do CIPRO e podem ser irreversíveis em alguns pacientes [ver AVISOS E PRECAUÇÕES e REAÇÕES ADVERSAS ].
Interrompa o CIPRO imediatamente se o paciente apresentar sintomas de neuropatia periférica, incluindo dor, queimação, formigamento, dormência e/ou fraqueza, ou outras alterações nas sensações, incluindo toque leve, dor, temperatura, sensação de posição e sensação vibratória e/ou força motora em para minimizar o desenvolvimento de uma condição irreversível. Evite fluoroquinolonas, incluindo CIPRO 500mg, em pacientes que já apresentaram neuropatia periférica [ver REAÇÕES ADVERSAS ].
Efeitos do sistema nervoso central
Reações Adversas Psiquiátricas
As fluoroquinolonas, incluindo CIPRO, têm sido associadas a um risco aumentado de reações adversas psiquiátricas, incluindo: psicose tóxica, reações psicóticas que progridem para ideias/pensamentos suicidas, alucinações ou paranóia; depressão ou comportamento autolesivo, como tentativa ou suicídio consumado; ansiedade, agitação ou nervosismo; confusão, delírio, desorientação ou distúrbios da atenção; insônia ou pesadelos; comprometimento da memória. Estas reações podem ocorrer após a primeira dose. Aconselhe os pacientes que recebem CIPRO a informar imediatamente seu médico se essas reações ocorrerem, descontinuar o medicamento e instituir os cuidados adequados.
Reações Adversas do Sistema Nervoso Central
As fluoroquinolonas, incluindo CIPRO 750mg, foram associadas a um risco aumentado de convulsões, aumento da pressão intracraniana (pscudotumor cerebral), tontura e tremores. CIPRO, como outras fluoroquinolonas, é conhecido por desencadear convulsões ou diminuir o limiar convulsivo. Casos de status epilepticus foram relatados. Como com todas as fluoroquinolonas, use CIPRO com cautela em pacientes epilépticos e pacientes com distúrbios do SNC conhecidos ou suspeitos que podem predispor a convulsões ou diminuir o limiar convulsivo (por exemplo, arteriosclerose cerebral grave, história prévia de convulsão, fluxo sanguíneo cerebral reduzido, alterações cerebrais ou acidente vascular cerebral), ou na presença de outros fatores de risco que podem predispor a convulsões ou diminuir o limiar convulsivo (por exemplo, certas terapias medicamentosas, disfunção renal). Se ocorrerem convulsões, descontinuar CIPRO 500mg e instituir cuidados apropriados [ver REAÇÕES ADVERSAS e INTERAÇÕES MEDICAMENTOSAS ].
Exacerbação da Miastenia Gravis
Fluoroquinolonas, incluindo CIPRO, têm atividade de bloqueio neuromuscular e podem exacerbar a fraqueza muscular em pacientes com miastenia gravis. Reações adversas graves pós-comercialização, incluindo mortes e necessidade de suporte ventilatório, foram associadas ao uso de fluoroquinolonas em pacientes com miastenia gravis. Evite CIPRO em pacientes com história conhecida de miastenia gravis [ver REAÇÕES ADVERSAS ].
Outras reações adversas graves e às vezes fatais
Outras reações adversas graves e às vezes fatais, algumas devido à hipersensibilidade e outras devido à etiologia incerta, foram relatadas em pacientes recebendo terapia com quinolonas, incluindo CIPRO. Esses eventos podem ser graves e geralmente ocorrem após a administração de doses múltiplas. As manifestações clínicas podem incluir um ou mais dos seguintes:
- Febre, erupção cutânea ou reações dermatológicas graves (por exemplo, necrólise epidérmica tóxica, síndrome de Stevens-Johnson);
- Vasculite; artralgia; mialgia; doença do soro;
- Pneumonite alérgica;
- nefrite intersticial; insuficiência ou insuficiência renal aguda;
- Hepatite; icterícia; necrose ou falência hepática aguda;
- Anemia, incluindo hemolítica e aplástica; trombocitopenia, incluindo púrpura trombocitopênica trombótica; leucopenia; agranulocitose; pancitopenia; e/ou outras anormalidades hematológicas.
Interrompa o CIPRO 500mg imediatamente ao primeiro aparecimento de erupção cutânea, icterícia ou qualquer outro sinal de hipersensibilidade e medidas de suporte instituídas [ver REAÇÕES ADVERSAS ].
Reações de hipersensibilidade
Reações de hipersensibilidade (anafiláticas) graves e ocasionalmente fatais, algumas após a primeira dose, foram relatadas em pacientes recebendo terapia com fluoroquinolonas, incluindo CIPRO. Algumas reações foram acompanhadas de colapso cardiovascular, perda de consciência, formigamento, edema faríngeo ou facial, dispneia, urticária e coceira. Apenas alguns pacientes tinham histórico de reações de hipersensibilidade. Reações anafiláticas graves requerem tratamento de emergência imediato com epinefrina e outras medidas de ressuscitação, incluindo oxigênio, fluidos intravenosos, anti-histamínicos intravenosos, corticosteroides, aminas pressoras e manejo das vias aéreas, incluindo intubação, conforme indicado [ver REAÇÕES ADVERSAS ].
Hepatotoxicidade
Casos de hepatotoxicidade grave, incluindo necrose hepática, insuficiência hepática com risco de vida e eventos fatais, foram relatados com CIPRO. A lesão hepática aguda tem início rápido (intervalo de 1 a 39 dias) e está frequentemente associada à hipersensibilidade. O padrão de lesão pode ser hepatocelular, colestático ou misto. A maioria dos pacientes com desfechos fatais tinha mais de 55 anos. No caso de quaisquer sinais e sintomas de hepatite (como anorexia, icterícia, urina escura, prurido ou abdome sensível), interrompa o tratamento imediatamente.
Pode haver um aumento temporário das transaminases, fosfatase alcalina ou icterícia colestática, especialmente em pacientes com lesão hepática prévia, que são tratados com CIPRO [ver REAÇÕES ADVERSAS ].
Risco de aneurisma e dissecção da aorta
Estudos epidemiológicos relatam um aumento da taxa de aneurisma e dissecção da aorta dentro de dois meses após o uso de fluoroquinolonas, particularmente em pacientes idosos. A causa para o aumento do risco não foi identificada. Em pacientes com aneurisma de aorta conhecido ou pacientes com maior risco de aneurisma de aorta, reserve CIPRO 750mg para uso somente quando não houver tratamentos antibacterianos alternativos disponíveis.
Reações adversas graves com teofilina concomitante
Reações graves e fatais foram relatadas em pacientes recebendo administração concomitante de CIPRO 250mg e teofilina. Essas reações incluíram parada cardíaca, convulsão, estado de mal epiléptico e insuficiência respiratória. Também ocorreram casos de náusea, vômito, tremor, irritabilidade ou palpitação.
Embora reações adversas graves semelhantes tenham sido relatadas em pacientes recebendo apenas teofilina, a possibilidade de que essas reações possam ser potencializadas pelo CIPRO não pode ser eliminada. Se o uso concomitante não puder ser evitado, monitore os níveis séricos de teofilina e ajuste a dosagem conforme apropriado. INTERAÇÕES MEDICAMENTOSAS ].
Diarreia Associada a Clostridioides Difficile
Diarreia associada a Clostridioides difficile (C. difficile) (CDAD) foi relatada com o uso de quase todos os agentes antibacterianos, incluindo CIPRO, e pode variar em gravidade de diarreia leve a colite fatal. O tratamento com agentes antibacterianos altera a flora normal do cólon levando ao crescimento excessivo de C. difficile.
C. difficile produz toxinas A e B que contribuem para o desenvolvimento de CDAD. Isolados produtores de hipertoxina de C. difficile causam aumento da morbidade e mortalidade, pois essas infecções podem ser refratárias à terapia antimicrobiana e podem exigir colectomia. CDAD deve ser considerado em todos os pacientes que apresentam diarreia após o uso de antibacterianos. É necessário um histórico médico cuidadoso, pois foi relatado que a CDAD ocorre mais de dois meses após a administração de agentes antibacterianos.
Se houver suspeita ou confirmação de CDAD, o uso contínuo de antibacterianos não direcionados contra C. difficile pode precisar ser descontinuado. Gerenciamento adequado de fluidos e eletrólitos, suplementação de proteína, tratamento antibacteriano de C. difficile e instituição de avaliação cirúrgica conforme indicação clínica [ver REAÇÕES ADVERSAS ].
Prolongamento do intervalo QT
Algumas fluoroquinolonas, incluindo CIPRO 750mg, têm sido associadas ao prolongamento do intervalo QT no eletrocardiograma e a casos de arritmia. Casos de torsade de pointes foram relatados durante a vigilância pós-comercialização em pacientes recebendo fluoroquinolonas, incluindo CIPRO.
Evite CIPRO 1000mg em pacientes com prolongamento conhecido do intervalo QT, fatores de risco para prolongamento QT ou torsade de pointes (por exemplo, síndrome congênita do QT longo, desequilíbrio eletrolítico não corrigido, como hipocalemia ou hipomagnesemia e doença cardíaca, como insuficiência cardíaca, infarto ou bradicardia) e pacientes recebendo agentes antiarrítmicos de classe IA (quinidina, procainamida) ou agentes antiarrítmicos de classe III (amiodarona, sotalol), antidepressivos tricíclicos, macrolídeos e antipsicóticos. Pacientes idosos também podem ser mais suscetíveis a efeitos associados a drogas no intervalo QT [ver REAÇÕES ADVERSAS , Uso em populações específicas ].
Distúrbios musculoesqueléticos em pacientes pediátricos e efeitos artropáticos em animais
CIPRO 250mg é indicado em pacientes pediátricos (com menos de 18 anos de idade) apenas para ITUc, prevenção de antraz inalatório (pós-exposição) e peste [ver INDICAÇÕES E USO ]. Foi observado um aumento da incidência de reações adversas em comparação com os controles, incluindo reações relacionadas às articulações e/ou tecidos circundantes [ver REAÇÕES ADVERSAS ].
Em estudos pré-clínicos, a administração oral de CIPRO causou claudicação em cães imaturos. O exame histopatológico das articulações de sustentação de peso desses cães revelou lesões permanentes da cartilagem. Drogas da classe das quinolonas relacionadas também produzem erosões da cartilagem das articulações que suportam peso e outros sinais de artropatia em animais imaturos de várias espécies. Uso em populações específicas e Toxicologia não clínica ].
Fotossensibilidade/Fototoxicidade
Reações moderadas a graves de fotossensibilidade/fototoxicidade, a última das quais pode se manifestar como reações exageradas de queimadura solar (por exemplo, queimação, eritema, exsudação, vesículas, bolhas, edema) envolvendo áreas expostas à luz (tipicamente a face, área “V” do pescoço, superfícies extensoras dos antebraços, dorso das mãos), pode ser associado ao uso de quinolonas incluindo CIPRO após exposição ao sol ou à luz UV. Portanto, evite a exposição excessiva a essas fontes de luz. Descontinuar CIPRO 250mg se ocorrer fototoxicidade [ver REAÇÕES ADVERSAS ].
Desenvolvimento de bactérias resistentes a drogas
Prescrever CIPRO 250mg Comprimidos e CIPRO Suspensão Oral na ausência de infecção bacteriana comprovada ou fortemente suspeita ou indicação profilática provavelmente não trará benefícios ao paciente e aumenta o risco de desenvolvimento de bactérias resistentes aos medicamentos.
Riscos potenciais com o uso concomitante de drogas metabolizadas pelas enzimas do citocromo P450 1A2
CIPRO 750mg é um inibidor da via hepática da enzima CYP1A2. A coadministração de CIPRO e outros medicamentos metabolizados principalmente pelo CYP1A2 (por exemplo, teofilina, metilxantinas, cafeína, tizanidina, ropinirol, clozapina, olanzapina e zolpidem), resulta em aumento das concentrações plasmáticas do medicamento coadministrado e pode levar a reações adversas farmacodinâmicas do medicamento coadministrado [ver INTERAÇÕES MEDICAMENTOSAS e FARMACOLOGIA CLÍNICA ].
Interferência no diagnóstico oportuno da sífilis
CIPRO 1000mg não demonstrou ser eficaz no tratamento da sífilis. Agentes antimicrobianos usados em altas doses por curtos períodos de tempo para tratar a gonorreia podem mascarar ou retardar os sintomas da incubação da sífilis. Realizar um teste sorológico para sífilis em todos os pacientes com gonorreia no momento do diagnóstico. Realizar teste sorológico de acompanhamento para sífilis três meses após o tratamento com CIPRO.
Cristalúria
Cristais de ciprofloxacina foram observados raramente na urina de seres humanos, mas com mais frequência na urina de animais de laboratório, que geralmente é alcalina. Toxicologia não clínica ]. Cristalúria relacionada ao CIPRO foi relatada apenas raramente em humanos porque a urina humana é geralmente ácida. Evitar a alcalinidade da urina em pacientes recebendo CIPRO. Hidrate bem os pacientes para evitar a formação de urina altamente concentrada [ver DOSAGEM E ADMINISTRAÇÃO ].
Distúrbios da glicose no sangue
As fluoroquinolonas, incluindo CIPRO, têm sido associadas a distúrbios da glicemia, incluindo hiperglicemia e hipoglicemia sintomática, geralmente em pacientes diabéticos recebendo tratamento concomitante com um agente hipoglicemiante oral (por exemplo, gliburida) ou com insulina. Nestes doentes, recomenda-se a monitorização cuidadosa da glicemia. Casos graves de hipoglicemia resultando em coma ou morte foram relatados. Se ocorrer uma reação hipoglicêmica em um paciente em tratamento com CIPRO, descontinue CIPRO 750mg e inicie a terapia apropriada imediatamente [ver REAÇÕES ADVERSAS , INTERAÇÕES MEDICAMENTOSAS ].
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( Guia de Medicação )
Reações Adversas Graves
Aconselhe os pacientes a parar de tomar CIPRO 250mg se apresentarem uma reação adversa e a ligar para seu médico para aconselhamento sobre a conclusão do tratamento completo com outro medicamento antibacteriano.
Informe os pacientes sobre as seguintes reações adversas graves que foram associadas ao uso de CIPRO ou outras fluoroquinolonas:
- Reações adversas graves incapacitantes e potencialmente irreversíveis que podem ocorrer em conjunto: Informar os pacientes que reações adversas graves incapacitantes e potencialmente irreversíveis, incluindo tendinite e ruptura de tendão, neuropatias periféricas e efeitos no sistema nervoso central, foram associadas ao uso de CIPRO 1000mg e podem ocorrer juntas no mesmo paciente. Informe os pacientes para parar de tomar CIPRO imediatamente se apresentarem uma reação adversa e ligar para seu médico.
- Tendinite e ruptura de tendão: Instrua os pacientes a entrar em contato com seu médico se sentirem dor, inchaço ou inflamação de um tendão, ou fraqueza ou incapacidade de usar uma de suas articulações; descansar e abster-se de exercícios; e descontinuar o tratamento com CIPRO 750mg. Os sintomas podem ser irreversíveis. O risco de doença grave do tendão com fluoroquinolonas é maior em pacientes mais velhos, geralmente com mais de 60 anos de idade, em pacientes em uso de corticosteróides e em pacientes com transplantes de rim, coração ou pulmão.
- Neuropatias periféricas: Informe os pacientes que neuropatias periféricas foram associadas ao uso de ciprofloxacina, os sintomas podem ocorrer logo após o início da terapia e podem ser irreversíveis. Se surgirem sintomas de neuropatia periférica, incluindo dor, queimação, formigamento, dormência e/ou fraqueza, interrompa imediatamente o CIPRO e diga-lhes para entrar em contato com seu médico.
- Efeitos no sistema nervoso central (por exemplo, convulsões, tonturas, vertigens, aumento da pressão intracraniana): Informe os pacientes que convulsões foram relatadas em pacientes recebendo fluoroquinolonas, incluindo Ciprofloxacina. Instrua os pacientes a notificar seu médico antes de tomar este medicamento se tiverem histórico de convulsões. Informe aos pacientes que eles devem saber como reagem ao CIPRO antes de operar um automóvel ou máquina ou se envolver em outras atividades que exijam agilidade mental e coordenação. Instrua os pacientes a notificar seu médico se ocorrer dor de cabeça persistente com ou sem visão turva.
- Exacerbação da Miastenia Gravis: Instrua os pacientes a informar seu médico sobre qualquer história de miastenia gravis. Instrua os pacientes a notificarem seu médico se apresentarem quaisquer sintomas de fraqueza muscular, incluindo dificuldades respiratórias.
- Reações de hipersensibilidade: Informar os pacientes que o ciprofloxacino pode causar reações de hipersensibilidade, mesmo após uma dose única, e descontinuar o medicamento ao primeiro sinal de erupção cutânea, urticária ou outras reações cutâneas, batimentos cardíacos acelerados, dificuldade em engolir ou respirar, qualquer inchaço sugestivo de angioedema. por exemplo, inchaço dos lábios, língua, face, aperto na garganta, rouquidão) ou outros sintomas de uma reação alérgica.
- Hepatotoxicidade: Informe os pacientes que hepatotoxicidade grave (incluindo hepatite aguda e eventos fatais) foi relatada em pacientes tomando CIPRO. Instrua os pacientes a informar seu médico se apresentarem quaisquer sinais ou sintomas de lesão hepática, incluindo: perda de apetite, náusea, vômito, febre, fraqueza, cansaço, sensibilidade no quadrante superior direito, coceira, amarelecimento da pele e dos olhos, movimentos intestinais de cor clara ou urina de cor escura.
- Aneurisma e dissecção da aorta: Informe os pacientes para procurar atendimento médico de emergência se sentirem dor súbita no peito, no estômago ou nas costas.
- Diarréia: A diarreia é um problema comum causado por antibióticos que geralmente termina quando o antibiótico é descontinuado. Às vezes, após o início do tratamento com antibióticos, os pacientes podem desenvolver fezes aquosas e sanguinolentas (com ou sem cólicas estomacais e febre), mesmo dois ou mais meses após a última dose do antibiótico. Se isso ocorrer, instrua os pacientes a entrar em contato com seu médico o mais rápido possível.
- Prolongamento do intervalo QT: Instruir os pacientes a informar seu médico sobre qualquer história pessoal ou familiar de prolongamento do intervalo QT ou condições pró-arrítmicas, como hipocalemia, bradicardia ou isquemia miocárdica recente; se estiverem tomando qualquer agente antiarrítmico Classe IA (quinidina, procainamida) ou Classe III (amiodarona, sotalol). Instrua os pacientes a notificar seu médico se apresentarem quaisquer sintomas de prolongamento do intervalo QT, incluindo palpitações cardíacas prolongadas ou perda de consciência.
- Distúrbios Musculoesqueléticos em Pacientes Pediátricos: Instrua os pais a informar o médico de seus filhos se a criança tiver um histórico de problemas relacionados às articulações antes de tomar este medicamento. Informe os pais de pacientes pediátricos para notificar o médico de seus filhos sobre quaisquer problemas relacionados às articulações que ocorram durante ou após a terapia com cipro 1000mgfloxacina [ver AVISOS E PRECAUÇÕES e Uso em populações específicas ].
- Tizanidina: Instruir os pacientes a não usarem cipro 250mgfloxacino se já estiverem tomando tizanidina. CIPRO aumenta os efeitos da tizanidina (Zanaflex®).
- Teofilina: Informe os pacientes que cipro 250mgfloxacina CIPRO 1000mg pode aumentar os efeitos da teofilina. Podem ocorrer efeitos do SNC com risco de vida e arritmias. Aconselhe os pacientes a procurarem imediatamente ajuda médica se tiverem convulsões, palpitações ou dificuldade em respirar.
- Cafeína: Informe os pacientes que CIPRO 500mg pode aumentar os efeitos da cafeína. Existe a possibilidade de acúmulo de cafeína quando produtos que contêm cafeína são consumidos enquanto se toma quinolonas.
- Fotossensibilidade/Fototoxicidade: Informe os pacientes que fotossensibilidade/fototoxicidade foram relatadas em pacientes recebendo fluoroquinolonas. Informe os pacientes para minimizar ou evitar a exposição à luz solar natural ou artificial (camas de bronzeamento artificial ou tratamento UVA/B) enquanto estiver tomando quinolonas. Se os pacientes precisarem ficar ao ar livre enquanto estiverem usando quinolonas, instrua-os a usar roupas folgadas que protejam a pele da exposição ao sol e discuta outras medidas de proteção solar com seu médico. Se ocorrer uma reação do tipo queimadura solar ou erupção cutânea, instrua os pacientes a entrar em contato com seu médico.
- Distúrbios da glicose no sangue: Informar aos pacientes que se forem diabéticos e estiverem sendo tratados com insulina ou hipoglicemiante oral e ocorrer uma reação hipoglicêmica, devem descontinuar CIPRO 250mg e consultar um médico.
- Lactação: Para outras indicações além do antraz por inalação (pós-exposição), informe à mulher que a amamentação não é recomendada durante o tratamento com Cipro e por mais 2 dias após a última dose. Alternativamente, uma mulher pode bombear e descartar durante o tratamento e por mais 2 dias após a última dose [ver Uso em populações específicas ].
Resistência Antibacteriana
Informe os pacientes que os medicamentos antibacterianos, incluindo CIPRO 250mg Comprimidos e CIPRO 1000mg Suspensão Oral, devem ser usados apenas para tratar infecções bacterianas. Eles não tratam infecções virais (por exemplo, o resfriado comum). Quando CIPRO 500mg Comprimidos e CIPRO 500mg Suspensão Oral são prescritos para tratar uma infecção bacteriana, os pacientes devem ser informados de que, embora seja comum sentir-se melhor no início do tratamento, a medicação deve ser tomada exatamente como indicado. Pular doses ou não completar o curso completo da terapia pode (1) diminuir a eficácia do tratamento imediato e (2) aumentar a probabilidade de que as bactérias desenvolvam resistência e não sejam tratáveis por CIPRO 500mg Comprimidos e CIPRO 250mg Suspensão Oral ou outro antibacteriano drogas no futuro.
Instruções de administração
Instruir o paciente
- Agitar vigorosamente a Suspensão Oral CIPRO todas as vezes antes de usar por aproximadamente 15 segundos.
- Utilizar sempre a colher graduada embalada com marcações para ½ (2,5 mL) e 1/1 (5 mL), para obter a dose exata.
- Após o uso, a colher de medição graduada deve ser limpa em água corrente com detergente e seca bem.
- Não mastigar as microcápsulas, mas engoli-las inteiras.
- Essa água pode ser tomada depois.
- Feche o frasco corretamente após cada uso de acordo com as instruções na tampa.
- Após a conclusão do tratamento, CIPRO 1000mg Suspensão Oral não deve ser reutilizado.
Informe os pacientes que CIPRO 250mg pode ser tomado com ou sem alimentos.
Informe os pacientes para beberem líquidos livremente enquanto estiverem tomando CIPRO para evitar a formação de urina altamente concentrada e a formação de cristais na urina.
Informe os pacientes que antiácidos contendo magnésio ou alumínio, bem como sucralfato, cátions metálicos como ferro e preparações multivitamínicas com zinco ou didanosina devem ser tomados pelo menos duas horas antes ou seis horas após a administração de CIPRO 1000mg. CIPRO não deve ser tomado com produtos lácteos (como leite ou iogurte) ou sucos enriquecidos com cálcio, pois a absorção de ciprofloxacina pode ser significativamente reduzida; no entanto, CIPRO 500mg pode ser tomado com uma refeição que contenha esses produtos.
Aconselhe os pacientes que, se uma dose for esquecida, ela deve ser tomada a qualquer momento, mas não depois de 6 horas antes da próxima dose programada. Se faltarem menos de 6 horas para a próxima dose, a dose esquecida não deve ser tomada e o tratamento deve ser continuado conforme prescrito com a próxima dose programada. Doses duplas não devem ser tomadas para compensar uma dose esquecida.
Informe os pacientes que os comprimidos de CIPRO 500mg (250 mg e 500 mg) são marcados e podem ser divididos ao meio na linha marcada para fornecer uma dosagem de 125 mg ou 250 mg, respectivamente.
Interações Medicamentosas Antidiabéticos Orais
Informar os pacientes que hipoglicemia foi relatada quando cipro 250mgfloxacino e agentes antidiabéticos orais foram coadministrados; se ocorrer baixo nível de açúcar no sangue com CIPRO 750mg, instrua-os a consultar seu médico e que seu medicamento antibacteriano pode precisar ser trocado.
Estudos de antraz e pestes
Informe os pacientes que receberam CIPRO para essas condições que os estudos de eficácia não podem ser realizados em humanos por motivos de viabilidade. Portanto, a aprovação para essas condições foi baseada em estudos de eficácia realizados em animais.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Oito testes de mutagenicidade in vitro foram realizados com cipro 500mgfloxacina, e os resultados dos testes estão listados abaixo:
- Teste de Salmonela/Microssoma (Negativo)
- Ensaio de Reparo de DNA de E. coli (Negativo)
- Ensaio de mutação direta de células de linfoma de camundongo (positivo)
- Teste HGPRT de Célula V79 do Hamster Chinês (Negativo)
- Ensaio de Transformação de Células de Embriões de Hamster Sírio (Negativo)
- Ensaio de Mutação de Ponto de Saccharomyces cerevisiae (Negativo)
- Ensaio de Crossover Mitótico e Conversão de Genes de Saccharomyces cerevisiae (Negativo)
- Ensaio de reparo de DNA de hepatócitos de rato (positivo)
Assim, 2 dos 8 testes foram positivos, mas os resultados dos 3 seguintes sistemas de teste in vivo deram resultados negativos:
- Ensaio de reparo de DNA de hepatócitos de rato
- Teste de micronúcleo (camundongos)
- Teste Letal Dominante (Camundongos)
Estudos de carcinogenicidade de longo prazo em ratos e camundongos não resultaram em efeitos carcinogênicos ou tumorigênicos devido ao cipro 500mgfloxacino em doses orais diárias de até 250mg/kg e 750mg/kg para ratos e camundongos, respectivamente (aproximadamente 1,7 e 2,5 vezes a dose terapêutica mais alta recomendada com base na área de superfície corporal, respectivamente).
Os resultados dos testes de fotoco-carcinogenicidade indicam que o cipro 1000mgfloxacino não reduz o tempo de aparecimento de tumores cutâneos induzidos por UV em comparação com o controle do veículo. Camundongos sem pêlos (Skh-1) foram expostos à luz UVA por 3,5 horas cinco vezes a cada duas semanas por até 78 semanas enquanto eram administrados simultaneamente ciprofloxacina. O tempo para o desenvolvimento dos primeiros tumores de pele foi de 50 semanas em camundongos tratados concomitantemente com UVA e cipro 1000mgfloxacina (dose de camundongo aproximadamente igual à dose humana máxima recomendada com base na área de superfície corporal), em oposição a 34 semanas quando os animais foram tratados com UVA e veículo. Os tempos para o desenvolvimento de tumores de pele variaram de 16 semanas a 32 semanas em camundongos tratados concomitantemente com UVA e outras quinolonas.5
Neste modelo, camundongos tratados apenas com ciprofloxacina não desenvolveram tumores de pele ou sistêmicos. Não há dados de modelos semelhantes usando camundongos pigmentados e/ou camundongos totalmente peludos. O significado clínico desses achados para humanos é desconhecido.
Estudos de fertilidade realizados em ratos machos e fêmeas com doses orais de cipro 250mgfloxacino até 100mg/kg (aproximadamente 0,6 vezes a dose oral terapêutica mais alta recomendada com base na área de superfície corporal) não revelaram evidência de comprometimento. Ratos machos receberam ciprofloxacina oral por 10 semanas antes do acasalamento e as fêmeas foram dosadas por 3 semanas antes do acasalamento até o 7º dia de gestação.
Uso em populações específicas
Gravidez
Resumo do risco
A experiência prolongada com cipro 1000mgfloxacino em mulheres grávidas ao longo de várias décadas, com base em informações publicadas disponíveis de relatos de casos, estudos de caso-controle e estudos observacionais sobre cipro 1000mgfloxacino administrado durante a gravidez, não identificou nenhum risco associado ao medicamento de defeitos congênitos maiores, aborto espontâneo ou efeitos adversos resultados maternos ou fetais (ver Dados ). A administração oral de cipro 500mgfloxacino durante a organogênese em doses de até 100mg/kg em camundongos e ratas grávidas e até 30mg/kg em coelhas grávidas não causou malformações fetais (ver Dados ). Essas doses foram de até 0,3, 0,6 e 0,4 vezes a dose oral clínica máxima recomendada em camundongos, ratos e coelhos, respectivamente, com base na área de superfície corporal. O risco de fundo estimado de defeitos congênitos graves e aborto espontâneo para a população indicada é desconhecido. Todas as gestações têm um risco histórico de defeitos congênitos, perda ou outros resultados adversos. Na população geral dos EUA, os riscos de fundo estimados de defeitos congênitos graves e aborto espontâneo em gestações clinicamente reconhecidas são de 2 a 4% e 15 a 20%, respectivamente.
Dados
Dados humanos
Embora os estudos disponíveis não possam estabelecer definitivamente a ausência de risco, os dados publicados de estudos observacionais prospectivos ao longo de várias décadas não estabeleceram uma associação com o uso de cipro 250mgfloxacino durante a gravidez e defeitos congênitos graves, aborto espontâneo ou resultados maternos ou fetais adversos. Os estudos disponíveis têm limitações metodológicas, incluindo o pequeno tamanho da amostra e alguns deles não são específicos para ciprofloxacina. Um estudo observacional prospectivo controlado acompanhou 200 mulheres expostas a fluoroquinolonas (52,5% expostas a cipro 250mgfloxacina e 68% exposições no primeiro trimestre) durante a gestação. A exposição in utero a fluoroquinolonas durante a embriogênese não foi associada a aumento do risco de malformações maiores. As taxas relatadas de malformações congênitas maiores foram de 2,2% para o grupo fluoroquinolona e 2,6% para o grupo controle (a incidência de fundo de malformações maiores é de 1 a 5%). As taxas de abortos espontâneos, prematuridade e baixo peso ao nascer não diferiram entre os grupos e não houve disfunções musculoesqueléticas clinicamente significativas até um ano de idade nas crianças expostas ao cipro 500mgfloxacino.
Outro estudo prospectivo de acompanhamento relatou 549 gestações com exposição à fluoroquinolona (93% das exposições no primeiro trimestre). Houve 70 exposições de cipro 500mgfloxacina, todas no primeiro trimestre. As taxas de malformação entre bebês nascidos vivos expostos a cipro 750mgfloxacina e a fluoroquinolonas em geral estavam dentro das faixas de incidência de fundo. Não foram encontrados padrões específicos de anomalias congênitas. O estudo não revelou quaisquer reações adversas claras devido à exposição in utero à ciprofloxacina.
Não foram observadas diferenças nas taxas de prematuridade, abortos espontâneos ou peso ao nascer em mulheres expostas ao ciprofloxacino durante a gravidez. No entanto, esses pequenos estudos epidemiológicos pós-comercialização, dos quais a maior parte da experiência é de exposição de curto prazo no primeiro trimestre, são insuficientes para avaliar o risco de defeitos menos comuns ou para permitir conclusões confiáveis e definitivas sobre a segurança do ciprofloxacino em mulheres grávidas e seus fetos em desenvolvimento. .
Dados de animais
Estudos de toxicologia do desenvolvimento foram realizados com cipro 500mgfloxacina em ratos, camundongos e coelhos. Em ratos e camundongos, doses orais de até 100 mg/kg administradas durante a organogênese (dias de gestação, GD, 6-17) não foram associadas a resultados adversos no desenvolvimento, incluindo toxicidade embriofetal ou malformações. Em ratos e camundongos, uma dose de 100 mg/kg é aproximadamente 0,6 e 0,3 vezes a dose oral humana diária máxima (1500 mg/dia) com base na área de superfície corporal, respectivamente. Em uma série de estudos de toxicologia do desenvolvimento em coelhos, recebeu cipro oral ou intravenosa 250mgfloxacina por um dos seguintes períodos de 5 dias: GD 6 a 10, GD 10 a 14, ou GD 14 a 18, destinados a cobrir o período de organogênese. Esta foi uma tentativa de mitigar a intolerância gastrointestinal observada em coelhos que recebem antibacterianos manifestada pela redução do consumo alimentar materno e perda de peso, que pode levar à reabsorção embriofetal ou aborto espontâneo. Uma dose oral de cipro 750 mg de floxacina de 100 mg/kg (aproximadamente 1,3 vezes a dose oral clínica mais alta recomendada com base na área de superfície corporal) causou toxicidade materna excessiva, confundindo a avaliação dos fetos. Uma dose oral de 30 mg/kg (aproximadamente 0,4 vezes a dose oral clínica mais alta recomendada) foi associada à supressão do ganho de peso corporal materno e fetal, mas não foram observadas malformações fetais. A administração intravenosa de doses de até 20 mg/kg (aproximadamente 0,3 vezes a dose oral clínica mais alta recomendada com base na área de superfície corporal) a coelhas grávidas não foi tóxica para a mãe e nem toxicidade embriofetal nem malformações fetais foram observadas.
Em estudos peri e pós-natais, ratos receberam doses de cipro 1000mgfloxacino até 200mg/kg/dia (oral) ou até 30mg/kg/dia (subcutâneo) do DG 16 a 22 dias após o parto. A dose de 200 mg/kg é aproximadamente 1,3 vezes a dose oral clínica máxima recomendada com base na área de superfície corporal. Nem toxicidade materna nem efeitos adversos no crescimento e desenvolvimento dos filhotes foram observados, incluindo nenhum sinal de artropatia nas articulações das pernas traseiras dos filhotes. A ciprofloxacina e outras quinolonas demonstraram causar artropatia em animais imaturos da maioria das espécies testadas quando administradas diretamente [ver AVISOS E PRECAUÇÕES e Toxicologia não clínica ].
Lactação
Resumo do risco
A literatura publicada relata que a cipro 1000mgfloxacina está presente no leite humano após administração intravenosa e oral. Não há informações sobre os efeitos do CIPRO na produção de leite ou no lactente. Devido ao risco potencial de reações adversas graves em lactentes amamentados, incluindo artropatia demonstrada em estudos com animais juvenis [ver Uso em populações específicas (Considerações Clínicas)], para a maioria das indicações, uma mulher lactante pode considerar bombear e descartar o leite materno durante o tratamento com CIPRO 500mg e mais dois dias (cinco meias-vidas) após a última dose. Alternativamente, informe a mulher que a amamentação não é recomendada durante o tratamento com CIPRO e por mais dois dias (cinco meias-vidas) após a última dose.
No entanto, para antraz por inalação (pós-exposição), durante um incidente que resulte em exposição ao antraz, a avaliação de risco-benefício de continuar a amamentação enquanto a mãe (e potencialmente o bebê) está (estão) em CIPRO pode ser aceitável [ver DOSAGEM E ADMINISTRAÇÃO , Uso Pediátrico , e Estudos clínicos ]. Os benefícios do aleitamento materno para o desenvolvimento e para a saúde devem ser considerados juntamente com a necessidade clínica da mãe de CIPRO e quaisquer potenciais efeitos adversos na criança amamentada de CIPRO 1000mg ou da condição materna subjacente.
Considerações Clínicas
Cipro 1000mgfloxacina pode causar alteração da flora intestinal do lactente. Aconselhe a mulher a monitorar o bebê amamentado quanto a fezes soltas ou com sangue e candidíase (aftas, assaduras).
Uso Pediátrico
Embora eficaz em ensaios clínicos, CIPRO 750mg não é um medicamento de primeira escolha na população pediátrica devido ao aumento da incidência de reações adversas em relação aos controles. As quinolonas, incluindo CIPRO, causam artropatia (artralgia, artrite), em animais juvenis [ver AVISOS E PRECAUÇÕES e Toxicologia não clínica ].
Infecção urinária complicada e pielonefrite
CIPRO 250mg é indicado para o tratamento de ITU e pielonefrite por Escherichia coli em pacientes pediátricos de 1 a 17 anos de idade. Embora eficaz em ensaios clínicos, CIPRO 500mg não é a droga de primeira escolha na população pediátrica devido ao aumento da incidência de reações adversas em comparação com os controles, incluindo eventos relacionados às articulações e/ou tecidos circundantes [ver REAÇÕES ADVERSAS e Estudos clínicos ].
Antraz por inalação (pós-exposição)
CIPRO 750mg é indicado em pacientes pediátricos do nascimento aos 17 anos de idade, para antraz inalatório (pós-exposição). A avaliação risco-benefício indica que a administração de ciprofloxacina a pacientes pediátricos é apropriada [ver DOSAGEM E ADMINISTRAÇÃO e Estudos clínicos ].
Praga
CIPRO 500mg é indicado em pacientes pediátricos do nascimento aos 17 anos de idade, para tratamento de peste, incluindo peste pneumônica e septicêmica por Yersinia pestis (Y. pestis) e profilaxia para peste. Os estudos de eficácia do CIPRO não puderam ser realizados em humanos com peste pneumônica por razões de viabilidade. Portanto, a aprovação desta indicação foi baseada em um estudo de eficácia realizado em animais. A avaliação risco-benefício indica que a administração de CIPRO a pacientes pediátricos é apropriada [ver INDICAÇÕES E USO , DOSAGEM E ADMINISTRAÇÃO e Estudos clínicos ].
Uso Geriátrico
Pacientes geriátricos correm maior risco de desenvolver distúrbios graves do tendão, incluindo ruptura do tendão, quando tratados com uma fluoroquinolona, como CIPRO. Este risco é ainda maior em pacientes recebendo terapia concomitante com corticosteróides. A tendinite ou ruptura do tendão pode envolver o tendão de Aquiles, mão, ombro ou outros locais e pode ocorrer durante ou após a conclusão da terapia; foram relatados casos que ocorreram até vários meses após o tratamento com fluoroquinolona. Deve-se ter cuidado ao prescrever CIPRO 500mg para pacientes idosos, especialmente aqueles em uso de corticosteroides. Os pacientes devem ser informados desta potencial reação adversa e aconselhados a descontinuar CIPRO 500mg e entrar em contato com seu médico se ocorrerem quaisquer sintomas de tendinite ou ruptura de tendão [ver AVISO EM CAIXA , AVISOS E PRECAUÇÕES , e REAÇÕES ADVERSAS ].
Estudos epidemiológicos relatam um aumento da taxa de aneurisma e dissecção da aorta dentro de dois meses após o uso de fluoroquinolonas, particularmente em pacientes idosos. AVISOS E PRECAUÇÕES ].
Em uma análise retrospectiva de 23 ensaios clínicos controlados de dose múltipla de CIPRO abrangendo mais de 3.500 pacientes tratados com ciprofloxacina, 25% dos pacientes tinham idade maior ou igual a 65 anos e 10% tinham idade maior ou igual a 75 anos. Não foram observadas diferenças gerais na segurança ou eficácia entre esses indivíduos e indivíduos mais jovens, e outras experiências clínicas relatadas não identificaram diferenças nas respostas entre pacientes idosos e pacientes mais jovens, mas uma maior sensibilidade de alguns indivíduos mais velhos em qualquer terapia medicamentosa não pode ser descartada. A ciprofloxacina é substancialmente excretada pelos rins e o risco de reações adversas pode ser maior em pacientes com insuficiência renal. Nenhuma alteração de dosagem é necessária para pacientes com mais de 65 anos de idade com função renal normal. No entanto, como alguns indivíduos idosos apresentam função renal reduzida em virtude da idade avançada, deve-se ter cuidado na seleção da dose para pacientes idosos, e o monitoramento da função renal pode ser útil nesses pacientes [ver DOSAGEM E ADMINISTRAÇÃO e FARMACOLOGIA CLÍNICA ].
Em geral, os pacientes idosos podem ser mais suscetíveis aos efeitos associados aos medicamentos no intervalo QT. Portanto, deve-se ter precaução ao usar CIPRO 500mg com medicamentos concomitantes que podem resultar em prolongamento do intervalo QT (por exemplo, antiarrítmicos classe IA ou classe III) ou em pacientes com fatores de risco para torsade de pointes (por exemplo, prolongamento QT conhecido , hipocalemia não corrigida) [ver AVISOS E PRECAUÇÕES ].
Insuficiência renal
Cipro 500mgfloxacino é eliminado principalmente por excreção renal; entretanto, a droga também é metabolizada e parcialmente eliminada pelo sistema biliar do fígado e pelo intestino. Essas vias alternativas de eliminação do fármaco parecem compensar a excreção renal reduzida em pacientes com insuficiência renal. No entanto, algumas modificações na dosagem são recomendadas, particularmente para pacientes com disfunção renal grave [ver DOSAGEM E ADMINISTRAÇÃO e FARMACOLOGIA CLÍNICA ].
Insuficiência hepática
Em estudos preliminares em pacientes com cirrose hepática crônica estável, não foram observadas alterações significativas na farmacocinética da ciprofloxacina. A farmacocinética do cipro 500mgfloxacino em pacientes com insuficiência hepática aguda não foi estudada.
SOBREDOSAGEM
No caso de superdosagem aguda, toxicidade renal reversível foi relatada em alguns casos. Esvazie o estômago induzindo o vômito ou por lavagem gástrica. Observe o paciente cuidadosamente e dê tratamento de suporte, incluindo monitoramento da função renal, pH urinário e acidificação, se necessário, para prevenir cristalúria e administração de antiácidos contendo magnésio, alumínio ou cálcio que podem reduzir a absorção de cipro 750mgfloxacino. A hidratação adequada deve ser mantida. Apenas uma pequena quantidade de cipro 250mgfloxacina (menos de 10%) é removida do corpo após hemodiálise ou diálise peritoneal.
CONTRA-INDICAÇÕES
Hipersensibilidade
CIPRO 1000mg é contraindicado em pessoas com histórico de hipersensibilidade ao cipro 750mgfloxacino, a qualquer membro da classe de antibacterianos das quinolonas ou a qualquer um dos componentes do produto. AVISOS E PRECAUÇÕES ].
Tizanidina
A administração concomitante com tizanidina é contraindicada [ver INTERAÇÕES MEDICAMENTOSAS ].
FARMACOLOGIA CLÍNICA
Mecanismo de ação
A ciprofloxacina é um membro da classe de agentes antibacterianos das fluoroquinolonas [ver Microbiologia ].
Farmacocinética
Absorção
A biodisponibilidade absoluta do cipro 500mgfloxacino quando administrado na forma de comprimido oral é de aproximadamente 70% sem perda substancial pelo metabolismo de primeira passagem. As concentrações séricas máximas de ciprofloxacina (Cmax) e a área sob a curva (AUC) são mostradas no gráfico para o intervalo de dose de 250 mg a 1000 mg (Tabela 12).
As concentrações séricas máximas são atingidas 1 a 2 horas após a administração oral. As concentrações médias 12 horas após a dosagem com 250, 500 ou 750 mg são 0,1, 0,2 e 0,4 mcg/mL, respectivamente. A meia-vida de eliminação sérica em indivíduos com função renal normal é de aproximadamente 4 horas. As concentrações séricas aumentam proporcionalmente com doses até 1000 mg.
Uma dose oral de 500 mg administrada a cada 12 horas demonstrou produzir uma AUC equivalente àquela produzida por uma infusão intravenosa de 400 mg de CIPRO 1000 mg administrada durante 60 minutos a cada 12 horas. Uma dose oral de 750 mg administrada a cada 12 horas mostrou produzir uma AUC no estado de equilíbrio equivalente àquela produzida por uma infusão intravenosa de 400 mg administrada durante 60 minutos a cada 8 horas. Uma dose oral de 750 mg resulta em uma Cmax semelhante à observada com uma dose intravenosa de 400 mg (Tabela 13). Uma dose oral de 250 mg administrada a cada 12 horas produz uma AUC equivalente àquela produzida por uma infusão de 200 mg de CIPRO 1000 mg administrada a cada 12 horas.
Comida
Quando CIPRO Tablet é administrado concomitantemente com alimentos, há um atraso na absorção do medicamento, resultando em picos de concentração que ocorrem mais perto de 2 horas após a administração em vez de 1 hora, enquanto não há atraso observado quando CIPRO 750mg Suspensão é administrado com alimentos . A absorção geral de CIPRO 1000mg Tablet ou CIPRO 500mg Suspension, entretanto, não é substancialmente afetada. A farmacocinética do cipro 750mgfloxacino administrado como suspensão também não é afetada pelos alimentos. Evite a administração concomitante de CIPRO com produtos lácteos (como leite ou iogurte) ou sucos fortificados com cálcio, pois é possível diminuir a absorção; no entanto, CIPRO 1000mg pode ser tomado com uma refeição que contenha esses produtos
Com administração oral, uma dose de 500 mg, administrada como 10 mL da Suspensão CIPRO 5% (contendo 250 mg de ciprofloxacina/5 mL) é bioequivalente ao comprimido de 500 mg. Um volume de 10 mL da Suspensão CIPRO 1000mg a 5% (contendo 250 mg de ciprofloxacina/5mL) é bioequivalente a um volume de 5 mL da Suspensão CIPRO 750mg a 10% (contendo 500 mg de cipro 1000mgfloxacina/5mL).
Distribuição
A ligação da ciprofloxacina às proteínas séricas é de 20% a 40%, o que provavelmente não é alto o suficiente para causar interações significativas de ligação às proteínas com outros medicamentos.
Após administração oral, o cipro 250mgfloxacino é amplamente distribuído por todo o corpo. As concentrações nos tecidos geralmente excedem as concentrações séricas em homens e mulheres, particularmente no tecido genital, incluindo a próstata. A ciprofloxacina está presente na forma ativa na saliva, secreções nasais e brônquicas, mucosa dos seios da face, escarro, fluido da bolha cutânea, linfa, fluido peritoneal, bile e secreções prostáticas. Cipro 500mgfloxacina também foi detectado no pulmão, pele, gordura, músculo, cartilagem e osso. A droga difunde-se no líquido cefalorraquidiano (LCR); no entanto, as concentrações no LCR são geralmente inferiores a 10% das concentrações séricas de pico. Baixos níveis da droga foram detectados nos humores aquoso e vítreo do olho.
Metabolismo
Quatro metabólitos foram identificados na urina humana que juntos representam aproximadamente 15% de uma dose oral. Os metabólitos têm atividade antimicrobiana, mas são menos ativos que o cipro 500mgfloxacino inalterado. Cipro 500mgfloxacina é um inibidor do metabolismo humano mediado pelo citocromo P450 1A2 (CYP1A2). A coadministração de ciprofloxacina com outros medicamentos metabolizados principalmente pelo CYP1A2 resulta em aumento das concentrações plasmáticas desses medicamentos e pode levar a eventos adversos clinicamente significativos do medicamento coadministrado [ver CONTRA-INDICAÇÕES , AVISOS E PRECAUÇÕES , e INTERAÇÕES MEDICAMENTOSAS ].
Excreção
meia-vida de eliminação sérica em indivíduos com função renal normal é de aproximadamente 4 horas. Aproximadamente 40 a 50% de uma dose administrada por via oral é excretada na urina como droga inalterada. Após uma dose oral de 250 mg, as concentrações urinárias de cipro 500 mg floxacina geralmente excedem 200 mcg/mL durante as primeiras duas horas e são aproximadamente 30 mcg/mL em 8 a 12 horas após a administração. A excreção urinária da ciprofloxacina é praticamente completa dentro de 24 horas após a administração. A depuração renal do cipro 250mgfloxacino, que é de aproximadamente 300 mL/minuto, excede a taxa de filtração glomerular normal de 120 mL/minuto. Assim, a secreção tubular ativa parece desempenhar um papel significativo na sua eliminação. A coadministração de probenecida com ciprofloxacina resulta em cerca de 50% de redução na depuração renal de ciprofloxacina e um aumento de 50% em sua concentração na circulação sistêmica.
Embora as concentrações biliares de cipro 250mgfloxacina sejam várias vezes maiores do que as concentrações séricas após a administração oral, apenas uma pequena quantidade da dose administrada é recuperada da bile como droga inalterada. Um adicional de 1% a 2% da dose é recuperado da bile na forma de metabólitos. Aproximadamente 20% a 35% de uma dose oral é recuperada das fezes dentro de 5 dias após a administração. Isso pode surgir da depuração biliar ou da eliminação transintestinal.
Populações Específicas
Idoso
Estudos farmacocinéticos das formas oral (dose única) e intravenosa (dose única e múltipla) de cipro 250mgfloxacino indicam que as concentrações plasmáticas de ciprofloxacino são mais altas em indivíduos idosos (mais de 65 anos) em comparação com adultos jovens. Embora a Cmax esteja aumentada em 16% a 40%, o aumento na AUC média é de aproximadamente 30% e pode ser pelo menos parcialmente atribuído à diminuição da depuração renal em idosos. A meia-vida de eliminação é apenas ligeiramente (~20%) prolongada em idosos. Essas diferenças não são consideradas clinicamente significativas [ver Uso em populações específicas ].
Insuficiência renal
Em pacientes com função renal reduzida, a meia-vida da ciprofloxacina é ligeiramente prolongada. Ajustes de dosagem podem ser necessários [ver Uso em populações específicas e DOSAGEM E ADMINISTRAÇÃO ].
Insuficiência hepática
Em estudos preliminares em pacientes com cirrose hepática crônica estável, não foram observadas alterações significativas na farmacocinética da ciprofloxacina. A cinética do cipro 750mgfloxacino em pacientes com insuficiência hepática aguda não foi totalmente estudada.
Pediatria
Tabela 14 resume os parâmetros farmacocinéticos em pacientes pediátricos com menos de 1 a menos de 12 anos de idade recebendo tratamento intravenoso.
Esses valores estão dentro da faixa relatada para adultos em doses terapêuticas. Com base na análise farmacocinética populacional de pacientes pediátricos com várias infecções, a meia-vida média prevista em crianças é de aproximadamente 4 horas – 5 horas, e a biodisponibilidade da suspensão oral é de aproximadamente 60%.
Interações Medicamentosas
Antiácidos
A administração concomitante de antiácidos contendo hidróxido de magnésio ou hidróxido de alumínio pode reduzir a biodisponibilidade de cipro 500mgfloxacino em até 90% [ver DOSAGEM E ADMINISTRAÇÃO e INTERAÇÕES MEDICAMENTOSAS ].
Antagonistas do Receptor H2 da Histamina
Os antagonistas do receptor H2 da histamina parecem não ter efeito significativo sobre a biodisponibilidade de cipro 250mgfloxacina.
Metronidazol
As concentrações séricas de ciprofloxacina e metronidazol não foram alteradas quando esses dois medicamentos foram administrados concomitantemente.
Tizanidina
Em um estudo farmacocinético, a exposição sistêmica de tizanidina (dose única de 4 mg) aumentou significativamente (Cmax 7 vezes, AUC 10 vezes) quando o medicamento foi administrado concomitantemente com CIPRO (500 mg duas vezes ao dia por 3 dias). A administração concomitante de tizanidina e CIPRO é contraindicada devido à potencialização dos efeitos hipotensores e sedativos da tizanidina [ver CONTRA-INDICAÇÕES ].
Ropinirol
Em um estudo realizado em 12 pacientes com doença de Parkinson aos quais foram administrados 6 mg de ropinirol uma vez ao dia com 500 mg de CIPRO 250 mg duas vezes ao dia, a Cmax média e a AUC média do ropinirol aumentaram em 60% e 84%, respectivamente. Recomenda-se o monitoramento de reações adversas relacionadas ao ropinirol e o ajuste adequado da dose de ropinirol durante e logo após a coadministração com CIPRO [ver AVISOS E PRECAUÇÕES ].
Clozapina
Após a administração concomitante de 250 mg de CIPRO 500 mg com 304 mg de clozapina por 7 dias, as concentrações séricas de clozapina e N-desmetilclozapina aumentaram 29% e 31%, respectivamente. Aconselha-se a monitorização cuidadosa das reações adversas associadas à clozapina e o ajuste adequado da dose de clozapina durante e logo após a coadministração com CIPRO.
Sildenafila
Após a administração concomitante de uma dose oral única de 50 mg de sildenafil com 500 mg de CIPRO 1000 mg a indivíduos saudáveis, a Cmax média e a AUC média de sildenafil aumentaram aproximadamente duas vezes. Use sildenafil com cautela quando coadministrado com CIPRO 500mg devido ao aumento esperado de duas vezes na exposição de sildenafil após a coadministração de CIPRO.
Duloxetina
Em estudos clínicos, foi demonstrado que o uso concomitante de duloxetina com fortes inibidores da isoenzima CYP450 1A2, como a fluvoxamina, pode resultar em um aumento de 5 vezes na AUC média e um aumento de 2,5 vezes na Cmax média da duloxetina.
Lidocaína
Em um estudo realizado em 9 voluntários saudáveis, o uso concomitante de 1,5 mg/kg de lidocaína IV com CIPRO 500 mg duas vezes ao dia resultou em um aumento da Cmax e AUC da lidocaína em 12% e 26%, respectivamente. Embora o tratamento com lidocaína tenha sido bem tolerado nesta exposição elevada, uma possível interação com CIPRO e um aumento nas reações adversas relacionadas à lidocaína podem ocorrer após a administração concomitante.
Metoclopramida
A metoclopramida acelera significativamente a absorção de cipro 750mgfloxacina oral, resultando em um tempo mais curto para atingir as concentrações plasmáticas máximas. Nenhum efeito significativo foi observado na biodisponibilidade da ciprofloxacina.
Omeprazol
Quando CIPRO foi administrado como uma dose única de 1.000 mg concomitantemente com omeprazol (40 mg uma vez ao dia por três dias) a 18 voluntários saudáveis, a AUC e Cmax médias de ciprofloxacina foram reduzidas em 20% e 23%, respectivamente. O significado clínico desta interação não foi determinado.
Microbiologia
Mecanismo de ação
A ação bactericida do cipro 750mgfloxacino resulta da inibição das enzimas topoisomerase II (DNA girase) e topoisomerase IV (ambas topoisomerases Tipo II), que são necessárias para a replicação, transcrição, reparo e recombinação do DNA bacteriano.
Mecanismo de resistência
mecanismo de ação das fluoroquinolonas, incluindo o ciprofloxacino, é diferente do das penicilinas, cefalosporinas, aminoglicosídeos, macrolídeos e tetraciclinas; portanto, microrganismos resistentes a essas classes de medicamentos podem ser suscetíveis à ciprofloxacina. A resistência às fluoroquinolonas ocorre principalmente por mutações nas girases de DNA, diminuição da permeabilidade da membrana externa ou efluxo de drogas. A resistência in vitro à ciprofloxacina desenvolve-se lentamente por mutações em várias etapas. A resistência à ciprofloxacina devido a mutações espontâneas ocorre com uma frequência geral entre
Resistência Cruzada
Não há resistência cruzada conhecida entre cipro 1000mgfloxacina e outras classes de antimicrobianos.
A ciprofloxacina demonstrou ser ativa contra a maioria dos isolados das seguintes bactérias, tanto in vitro quanto em infecções clínicas [ver INDICAÇÕES E USO ].
Bactérias Gram-positivas
Bacillus anthracis Enterococcus faecalis Staphylococcus aureus (somente isolados sensíveis à meticilina) Staphylococcus epidermidis (somente isolados sensíveis à meticilina) Staphylococcus saprophyticus Streptococcus pneumoniae Streptococcus pyogenes
Bactérias Gram-negativas
Campylobacter jejuni Citrobacter koseri Citrobacter freundii Enterobacter cloacae Escherichia coli Haemophilus influenza Haemophilus parainfluenzae Klebsiella pneumonia Moraxella catarrhalis Morganella morganii Neisseria gonorrhoeae Proteus mirabilis Proteus vulgaris Providencia rettgeri Providencia stuartii Pseudomonas aeruginosa Salmonella typhi Serratia marcescens Shigella boydii Shigella dysenteriae Shigella flexneri Shigella sonnei Yersinia pestis
Os seguintes dados in vitro estão disponíveis, mas seu significado clínico é desconhecido. Pelo menos 90 por cento das seguintes bactérias exibem uma concentração inibitória mínima in vitro (CIM) menor ou igual ao ponto de ruptura suscetível para cipro 750mgfloxacina contra isolados de gênero ou grupo de organismos semelhantes. No entanto, a eficácia do cipro 500mgfloxacino no tratamento de infecções clínicas causadas por essas bactérias não foi estabelecida em ensaios clínicos adequados e bem controlados.
Bactérias Gram-positivas
Staphylococcus haemolyticus (somente isolados sensíveis à meticilina) Staphylococcus hominis (somente isolados sensíveis à meticilina)
Bactérias Gram-negativas
Acinetobacter lwoffi Aeromonas hydrophila Edwardsiella tarda Enterobacter aerogenes Klebsiella oxytoca Legionella pneumophila Pasteurella multocida Salmonella enteritidis Vibrio cholera Vibrio parahaemolyticus Vibrio vulnificus Yersinia enterocolitica
Teste de suscetibilidade
Para obter informações específicas sobre os critérios interpretativos do teste de suscetibilidade e métodos de teste associados e padrões de controle de qualidade reconhecidos pela FDA para este medicamento, consulte: https://www.fda.gov/STIC.
Estudos clínicos
Infecção Complicada do Trato Urinário e Pielonefrite – Eficácia em Pacientes Pediátricos
CIPRO administrado por via intravenosa e/ou oral foi comparado a uma cefalosporina para tratamento de ITU e pielonefrite em pacientes pediátricos de 1 a 17 anos de idade (idade média de 6 ± 4 anos). O estudo foi realizado nos EUA, Canadá, Argentina, Peru, Costa Rica, México, África do Sul e Alemanha. A duração da terapia foi de 10 a 21 dias (duração média do tratamento foi de 11 dias com intervalo de 1 a 88 dias). O objetivo primário do estudo foi avaliar a segurança musculoesquelética e neurológica.
Os pacientes foram avaliados quanto ao sucesso clínico e erradicação bacteriológica do(s) organismo(s) de linha de base sem nova infecção ou superinfecção em 5 a 9 dias após a terapia (Teste de Cura ou TOC). A população Por Protocolo tinha organismo(s) causador(es) com contagem(ões) de colônias especificadas pelo protocolo na linha de base, sem violação de protocolo e sem interrupção prematura ou perda de acompanhamento (entre outros critérios).
As taxas de sucesso clínico e erradicação bacteriológica na população Por Protocolo foram semelhantes entre CIPRO 250mg e o grupo comparador, conforme mostrado abaixo.
Antraz por inalação em adultos e pediatria
As concentrações séricas médias de ciprofloxacina associadas a uma melhora estatisticamente significativa na sobrevida no modelo de macaco rhesus de antraz por inalação são atingidas ou excedidas em pacientes adultos e pediátricos recebendo regimes orais e intravenosos. A farmacocinética do Cipro 500mgfloxacino foi avaliada em várias populações humanas. A concentração sérica máxima média alcançada no estado de equilíbrio em humanos adultos recebendo 500 mg por via oral a cada 12 horas é de 2,97 mcg/mL e 4,56 mcg/mL após 400 mg por via intravenosa a cada 12 horas. A concentração sérica mínima média no estado de equilíbrio para ambos os regimes é de 0,2 mcg/mL. Em um estudo com 10 pacientes pediátricos entre 6 e 16 anos de idade, o pico médio de concentração plasmática alcançada é de 8,3 mcg/mL e as concentrações mínimas variam de 0,09 mcg/mL a 0,26 mcg/mL, após duas infusões intravenosas de 30 minutos de 10 mg/kg administrados com 12 horas de intervalo. Após a segunda infusão intravenosa, os pacientes mudaram para 15 mg/kg por via oral a cada 12 horas atingiram um pico médio de concentração de 3,6 mcg/mL após a dose oral inicial. Os dados de segurança a longo prazo, incluindo efeitos na cartilagem, após a administração de CIPRO a pacientes pediátricos são limitados. As concentrações séricas de Cipro 1000mgfloxacina alcançadas em humanos servem como um desfecho substituto razoavelmente provável para prever o benefício clínico e fornecer a base para esta indicação.1
Foi realizado um estudo em animais controlado por placebo em macacos rhesus expostos a uma dose média inalada de 11 LD50 (~5,5 x 105 esporos (intervalo 5-30 LD50) de B. anthracis. A concentração inibitória mínima (CIM) de cipro 250mgfloxacina para a cepa de antraz usada neste estudo foi de 0,08 mcg/mL. Nos animais estudados, as concentrações séricas médias de cipro 1000mgfloxacina alcançadas no Tmax esperado (1 hora pós-dose) após a dosagem oral até o estado de equilíbrio variaram de 0,98 mcg/mL a 1,69 mcg/mL. As concentrações médias de vale no estado de equilíbrio em 12 horas após a dose variaram de 0,12 mcg/mL a 0,19 mcg/mL.6 Mortalidade devido ao antraz para animais que receberam um regime de 30 dias de cipro 750mgfloxacina oral começando 24 horas após - a exposição foi significativamente menor (1/9), em comparação com o grupo placebo (9/10) [p= 0,001]. O único animal tratado com CIPRO que morreu de antraz o fez após o período de administração do medicamento de 30 dias.7
Mais de 9.300 pessoas foram recomendadas para completar um mínimo de 60 dias de profilaxia antibacteriana contra possível exposição inalatória a B. anthracis durante 2001. CIPRO 250mg foi recomendado para a maioria desses indivíduos para todo ou parte do regime de profilaxia. Algumas pessoas também receberam a vacina contra o antraz ou foram trocadas para drogas antibacterianas alternativas. Ninguém que recebeu CIPRO 1000mg ou outras terapias como tratamento profilático desenvolveu posteriormente antraz por inalação. O número de pessoas que receberam CIPRO como todo ou parte de seu regime de profilaxia pós-exposição é desconhecido.
Praga
Foi realizado um estudo em animais controlado por placebo em macacos verdes africanos expostos a uma dose média inalada de 110 LD50 (intervalo de 92 a 127 LD50) de Yersinia pestis (estirpe CO92). A concentração inibitória mínima (CIM) de ciprofloxacina para a cepa de Y. pestis utilizada neste estudo foi de 0,015 mcg/mL. As concentrações séricas máximas médias de ciprofloxacina alcançadas no final de uma única infusão de 60 minutos foram 3,49 ± mcg/mL 0,55 mcg/mL, 3,91 mcg/mL ± 0,58 mcg/mL e 4,03 mcg/mL ± 1,22 mcg/mL no Dia 2, Dia 6 e Dia 10 de tratamento em macacos verdes africanos, respectivamente Todas as concentrações mínimas (Dia 2, Dia 6 e Dia 10) foram
Toxicologia e/ou Farmacologia Animal
Cipro 250mgfloxacina e outras quinolonas demonstraram causar artropatia em animais imaturos da maioria das espécies testadas [ver AVISOS E PRECAUÇÕES ]. Danos nas articulações de suporte de peso foram observados em cães e ratos juvenis. Em beagles jovens, 100 mg/kg de ciprofloxacina, administrados diariamente por 4 semanas, causaram alterações articulares degenerativas da articulação do joelho. A 30 mg/kg, o efeito na articulação foi mínimo. Em um estudo subsequente em cães beagle jovens, doses orais de cipro 750 mg de floxacina de 30 mg/kg e 90 mg/kg de cipro 750 mg de floxacina (aproximadamente 1,3 vezes e 3,5 vezes a dose pediátrica com base nas AUCs plasmáticas comparativas) administradas diariamente por 2 semanas causaram alterações que ainda foram observadas por histopatologia após um período sem tratamento de 5 meses. Na dose de 10 mg/kg (aproximadamente 0,6 vezes a dose pediátrica com base nas AUCs plasmáticas comparativas), não foram observados efeitos nas articulações. Esta dose também não foi associada a artrotoxicidade após um período adicional de 5 meses sem tratamento. Em outro estudo, a remoção do peso da articulação reduziu as lesões, mas não as preveniu totalmente.
cristalúria, às vezes associada à nefropatia secundária, ocorre em animais de laboratório que receberam ciprofloxacina. Isso está relacionado principalmente à solubilidade reduzida da ciprofloxacina em condições alcalinas, que predominam na urina dos animais de teste; no homem, a cristalúria é rara, pois a urina humana é tipicamente ácida. Em macacos rhesus, foi observada cristalúria sem nefropatia após doses orais únicas tão baixas quanto 5 mg/kg. (aproximadamente 0,07 vezes a dose terapêutica mais alta recomendada com base na área de superfície corporal). Após 6 meses de administração intravenosa de 10 mg/kg/dia, não foram observadas alterações nefropatológicas; no entanto, observou-se nefropatia após administração de 20 mg/kg/dia pela mesma duração (aproximadamente 0,2 vezes a dose terapêutica mais elevada recomendada com base na área de superfície corporal).
Em cães, ciprofloxacina a 3 mg/kg e 10 mg/kg por injeção intravenosa rápida (15 seg.) produz efeitos hipotensores pronunciados. Esses efeitos são considerados relacionados à liberação de histamina, pois são parcialmente antagonizados pela pirilamina, um anti-histamínico. Em macacos rhesus, a injeção intravenosa rápida também produz hipotensão, mas o efeito nesta espécie é inconsistente e menos pronunciado.
Em camundongos, foi relatado que a administração concomitante de drogas anti-inflamatórias não esteróides, como fenilbutazona e indometacina com quinolonas, aumenta o efeito estimulador do SNC das quinolonas.
A toxicidade ocular observada com alguns medicamentos relacionados não foi observada em animais tratados com ciprofloxacina
REFERÊNCIAS
1. 21 CFR 314.510 (Subparte H – Aprovação acelerada de novos medicamentos para doenças que ameaçam a vida).
5. Relatório apresentado na reunião do Comitê Consultivo de Medicamentos Anti-Infecciosos e Medicamentos Dermatológicos da FDA, 31 de março de 1993, Silver Spring, MD. Relatório disponível da FDA, CDER, Advisors and Consultants Staff, HFD-21, 1901 Chapman Avenue, Room 200, Rockville, MD 20852, EUA.
6. Kelly DJ, et ai. Concentrações séricas de penicilina, doxiciclina e ciprofloxacina durante terapia prolongada em macacos rhesus. J Infect Dis 1992; 166:1184-7.
7. Friedlander AM, et ai. Profilaxia pós-exposição contra antraz experimental por inalação. J Infect Dis 1993; 167:1239-42.
8. Reunião do Comitê Consultivo de Medicamentos Antiinfecciosos, 3 de abril de 2012 - A eficácia do Ciprofloxacino no tratamento da Peste Pneumônica.
INFORMAÇÃO DO PACIENTE
CIPRO® Comprimidos (Sip-row) (cloridrato de ciprofloxacina), para uso oral
CIPRO® (Sip-row) (cipro 1000mgfloxacina) para suspensão oral
Leia este Guia de Medicação antes de começar a tomar CIPRO 500mg e sempre que receber um refil. Pode haver novas informações. Esta informação não substitui a conversa com seu médico sobre sua condição médica ou seu tratamento.
Qual é a informação mais importante que devo saber sobre CIPRO 500mg?
CIPRO, um medicamento antibacteriano fluoroquinolona, pode causar sérios efeitos colaterais. Alguns desses efeitos colaterais graves podem ocorrer ao mesmo tempo e resultar em morte.
Se você tiver algum dos seguintes efeitos colaterais graves enquanto estiver tomando CIPRO, pare de tomar CIPRO 750mg imediatamente e procure ajuda médica imediatamente.
1. Ruptura do tendão ou inchaço do tendão (tendinite).
- Problemas de tendão podem acontecer em pessoas de todas as idades que tomam CIPRO. Os tendões são cordões de tecido resistentes que conectam os músculos aos ossos. Os sintomas de problemas de tendão podem incluir:
- dor
- inchaço
- lágrimas e inchaço dos tendões, incluindo a parte de trás do tornozelo (Aquiles), ombro, mão, polegar ou outros locais do tendão.
- O risco de ter problemas de tendão enquanto você toma CIPRO é maior se você:
- tem mais de 60 anos
- está tomando esteróides (corticosteróides)
- teve um transplante de rim, coração ou pulmão.
- Problemas de tendão podem acontecer em pessoas que não têm os fatores de risco acima quando tomam CIPRO.
- Outras razões que podem aumentar o risco de problemas nos tendões podem incluir:
- atividade física ou exercício
- falência renal
- problemas de tendão no passado, como em pessoas com artrite reumatóide (AR).
- Pare de tomar CIPRO imediatamente e procure ajuda médica imediatamente ao primeiro sinal de dor no tendão, inchaço ou inflamação. A área mais comum de dor e inchaço é o tendão de Aquiles na parte de trás do tornozelo. Isso também pode acontecer com outros tendões.
- A ruptura do tendão pode ocorrer enquanto você estiver tomando ou após terminar de tomar CIPRO. As rupturas de tendão podem ocorrer dentro de horas ou dias após o uso do CIPRO e ocorreram até vários meses após as pessoas terem terminado de tomar a fluoroquinolona.
- Pare de tomar CIPRO 500mg imediatamente e procure ajuda médica imediatamente se tiver algum dos seguintes sinais ou sintomas de ruptura de tendão:
- ouvir ou sentir um estalo ou estalo em uma área do tendão
- hematomas logo após uma lesão em uma área do tendão
- incapaz de mover a área afetada ou suportar peso
Os problemas de tendão podem ser permanentes.
2. Alterações na sensação e possíveis danos nos nervos (neuropatia periférica). Danos aos nervos dos braços, mãos, pernas ou pés podem ocorrer em pessoas que tomam fluoroquinolonas, incluindo CIPRO. Pare de tomar CIPRO 750mg imediatamente e fale com seu médico imediatamente se tiver algum dos seguintes sintomas de neuropatia periférica em seus braços, mãos, pernas ou pés:
- dor
- dormência
- queimando
- fraqueza
- formigamento
CIPRO 500mg pode precisar ser interrompido para evitar danos permanentes nos nervos.
3. Efeitos no Sistema Nervoso Central (SNC). Problemas de saúde mental e convulsões foram relatados em pessoas que tomam medicamentos antibacterianos de fluoroquinolona, incluindo CIPRO. Informe o seu médico se tiver histórico de convulsões antes de começar a tomar CIPRO. Os efeitos colaterais do SNC podem ocorrer assim que tomar a primeira dose de CIPRO. Pare de tomar CIPRO imediatamente e converse com seu médico imediatamente se tiver algum desses efeitos colaterais ou outras alterações de humor ou comportamento:
- convulsões
- problemas para dormir
- ouvir vozes, ver coisas ou sentir coisas que não estão lá (alucinações)
- pesadelos
- sentir-se tonto ou tonto
- sinta-se agitado
- sentir-se mais desconfiado (paranóia)
- tremores
- pensamentos ou atos suicidas
- sente-se ansioso ou nervoso
- dores de cabeça que não vão embora, com ou sem
- confusão visão turva
- depressão
- problemas de memória
- consciência reduzida do ambiente
- pensamentos ou crenças falsos ou estranhos (delírios)
Essas mudanças podem ser permanentes.
4. Agravamento da miastenia gravis (um problema que causa fraqueza muscular). Fluoroquinolonas como CIPRO 500mg podem causar agravamento dos sintomas de miastenia gravis, incluindo fraqueza muscular e problemas respiratórios. Informe o seu médico se você tem histórico de miastenia gravis antes de começar a tomar CIPRO. Ligue para o seu médico imediatamente se tiver algum agravamento da fraqueza muscular ou problemas respiratórios.
O que é CIPRO 750mg?
CIPRO é um medicamento antibacteriano fluoroquinolona usado em adultos com 18 anos ou mais para tratar certas infecções causadas por certos germes chamados bactérias. Essas infecções bacterianas incluem:
-
- infecção do trato urinário
- infecção óssea e articular
- gonorreia cervical e uretral, não complicada
- infecção crônica da próstata
- pneumonia nosocomial
- pessoas com baixa contagem de glóbulos brancos e febre
- infecção do trato respiratório inferior
- infecção intra-abdominal, complicada
- antraz por inalação
- infecção do sinus
- diarreia infecciosa
- praga
- Infecção de pele
- febre tifóide (entérica)
- Estudos de CIPRO 1000mg para uso no tratamento de peste e antraz foram feitos apenas em animais, porque peste e antraz não podiam ser estudados em pessoas.
- CIPRO 250mg não deve ser usado em pessoas com exacerbação aguda de bronquite crônica, cistite aguda não complicada e sinusite, se houver outras opções de tratamento disponíveis.
- CIPRO 750mg não deve ser usado como primeira escolha de medicamento antibacteriano para tratar infecções do trato respiratório inferior causadas por um certo tipo de bactéria chamada Streptococcus pneumoniae.
- CIPRO 1000mg também é usado em crianças menores de 18 anos de idade para tratar infecções complicadas do trato urinário e renais ou que podem ter inalado germes de antraz, ter peste ou ter sido exposto a germes da peste.
- Crianças com menos de 18 anos de idade têm uma chance maior de ter problemas ósseos, articulares ou tendinosos (musculoesqueléticos), como dor ou inchaço, enquanto tomam CIPRO. CIPRO 500mg não deve ser usado como primeira escolha de medicamento antibacteriano em crianças menores de 18 anos.
Quem não deve tomar CIPRO 1000mg?
Não tome CIPRO 500mg se você:
- já teve uma reação alérgica grave a um medicamento antibacteriano conhecido como fluoroquinolona, ou é alérgico ao cloridrato de cipro 500mgfloxacina ou a qualquer um dos ingredientes do CIPRO. Consulte o final deste Guia de Medicação para obter uma lista completa dos ingredientes do CIPRO.
- tome também um medicamento chamado tizanidina (Zanaflex®). Pergunte ao seu médico se não tiver certeza.
O que devo dizer ao meu médico antes de tomar CIPRO?
Antes de tomar CIPRO, informe o seu médico sobre todas as suas condições médicas, incluindo se você:
- tem problemas de tendão. CIPRO não deve ser usado em pessoas com histórico de problemas nos tendões.
- tem uma doença que causa fraqueza muscular (miastenia gravis). CIPRO não deve ser usado em pessoas com histórico conhecido de miastenia gravis.
- tem problemas de fígado.
- tem problemas no sistema nervoso central (como epilepsia).
- tem problemas nervosos. CIPRO 500mg não deve ser usado em pessoas que tenham histórico de um problema nervoso chamado neuropatia periférica ou qualquer pessoa da sua família tenha batimentos cardíacos irregulares ou ataque cardíaco, especialmente uma condição chamada “prolongamento do intervalo QT”.
- tem baixo nível de potássio no sangue (hipocalemia) ou baixo nível de magnésio (hipomagnesemia).
- tem ou teve convulsões.
- tem problemas renais. Você pode precisar de uma dose menor de CIPRO 500mg se seus rins não funcionarem bem.
- tem diabetes ou problemas com baixo nível de açúcar no sangue (hipoglicemia).
- tem problemas nas articulações, incluindo artrite reumatóide (AR).
- tem problemas para engolir comprimidos.
- estão grávidas ou planejam engravidar. Não se sabe se CIPRO 250mg prejudicará o feto.
- está amamentando ou planeja amamentar. CIPRO 250mg passa para o leite materno.
- Você não deve amamentar durante o tratamento com CIPRO 500mg e por 2 dias após tomar sua última dose de CIPRO. Você pode bombear seu leite materno e jogá-lo fora durante o tratamento com CIPRO e por 2 dias após tomar sua última dose de CIPRO.
- Se você estiver tomando CIPRO para antraz por inalação, você e seu médico devem decidir se você pode continuar amamentando enquanto estiver tomando CIPRO.
Informe o seu médico sobre todos os medicamentos que toma, incluindo medicamentos prescritos e de venda livre, vitaminas e suplementos de ervas.
- CIPRO 1000mg e outros medicamentos podem afetar uns aos outros causando efeitos colaterais.
- Informe especialmente o seu médico se você tomar:
- um medicamento esteróide.
- um medicamento antipsicótico.
- um antidepressivo tricíclico.
- uma pílula de água (diurético).
- teofilina (como Theo-24®, Elixophyllin®, Theochron®, Uniphyl®, Theolair®).
- um medicamento para controlar a sua frequência ou ritmo cardíaco (antiarrítmicos).
- um medicamento oral anti-diabetes.
- fenitoína (Fosphenytoin Sodium®, Cerebyx®, Dilantin-125®, Dilantin®, Extended Phenytoin Sodium®, Prompt Phenytoin Sodium®, Phenytek®).
- ciclosporina (Gengraf®, Neoral®, Sandimmune®, Sangcya®).
- um anticoagulante (como varfarina, Coumadin®, Jantoven®).
- metotrexato (Trexall®).
- ropinirol (Requip®).
- clozapina (Clozaril®, Fazaclo® ODT®).
- um medicamento anti-inflamatório não esteróide (AINE). Muitos medicamentos comuns para alívio da dor são AINEs. Tomar um AINE enquanto toma CIPRO 500mg ou outras fluoroquinolonas pode aumentar o risco de convulsões e efeitos no sistema nervoso central.
- sildenafil (Viagra®, Revatio®).
- duloxetina.
- produtos que contenham cafeína.
- probenecida (Probalan®, Col-probenecid®).
- Certos medicamentos podem impedir que os comprimidos CIPRO e a suspensão oral CIPRO funcionem corretamente. Tome CIPRO Comprimidos e Suspensão Oral 2 horas antes ou 6 horas depois de tomar estes medicamentos, vitaminas ou suplementos:
- um antiácido, multivitamínico ou outro medicamento ou suplementos que contenha magnésio, cálcio, alumínio, ferro ou zinco.
- sucralfato (Carafate®).
- didanosina (Videx®, Videx EC®).
Peça ao seu médico uma lista desses medicamentos se não tiver certeza.
Conheça os medicamentos que você toma. Mantenha uma lista deles para mostrar ao seu médico e farmacêutico quando receber um novo medicamento.
Como devo tomar CIPRO 500mg?
- Tome CIPRO exatamente como seu médico lhe disser para tomá-lo.
- Seu médico lhe dirá quanto CIPRO tomar e quando tomá-lo.
- CIPRO pode ser tomado com ou sem alimentos.
- CIPRO não deve ser tomado com produtos lácteos (como leite ou iogurte) ou sucos enriquecidos com cálcio, mas pode ser tomado com uma refeição que contenha esses produtos.
- Beba bastante líquido enquanto estiver tomando CIPRO.
- Não pule nenhuma dose de CIPRO ou pare de tomá-lo, mesmo que comece a se sentir melhor, até terminar o tratamento prescrito, a menos que:
- você tem problemas de tendão. Ver “Qual é a informação mais importante que devo saber sobre o CIPRO?”
- você tem problemas nervosos. Ver “Qual é a informação mais importante que devo saber sobre o CIPRO?”
- você tem problemas no sistema nervoso central. Ver “Qual é a informação mais importante que devo saber sobre CIPRO 1000mg?”
- você tem uma reação alérgica grave. Ver “Quais são os possíveis efeitos colaterais do CIPRO 750mg?”
- seu médico lhe diz para parar de tomar CIPRO.
Tomar todas as suas doses de CIPRO ajudará a garantir que todas as bactérias sejam mortas. Tomar todas as suas doses de CIPRO ajudará a diminuir a chance de que as bactérias se tornem resistentes ao CIPRO. Se você se tornar resistente ao CIPRO, CIPRO 1000mg e outros medicamentos antibacterianos podem não funcionar para você no futuro.
-
Se você tomar muito CIPRO 750mg, ligue para seu médico ou procure ajuda médica imediatamente.
-
CIPRO é fornecido na forma de comprimido marcado (CIPRO 1000mg comprimidos), suspensão oral (CIPRO 750mg suspensão oral), comprimido de liberação prolongada (CIPRO XR) e injeção para infusão intravenosa (CIPRO IV). Leia e siga as instruções abaixo para o tipo de CIPRO 500mg que seu médico prescreveu para você.
CIPRO Comprimidos:
- Os comprimidos CIPRO vêm em comprimidos com ranhuras de 250 mg e 500 mg que podem ser tomados inteiros ou podem ser partidos ao meio na linha ranhurada. Seu médico lhe dirá a quantidade de comprimidos de CIPRO 500mg e se você precisará quebrar os comprimidos de CIPRO 1000mg pela metade para obter a dose prescrita.
- Tome os comprimidos CIPRO de manhã e à noite aproximadamente à mesma hora todos os dias. Não esmague ou mastigue o comprimido. Informe o seu médico se não conseguir engolir o comprimido.
- Se você esquecer uma dose de CIPRO 500mg Comprimidos e for:
- 6 horas ou mais até a próxima dose programada, tome a dose esquecida imediatamente. Em seguida, tome a próxima dose no horário habitual.
- menos de 6 horas até a próxima dose programada, não tome a dose esquecida. Tome a próxima dose no horário habitual.
- Não tome 2 doses de CIPRO 750mg comprimidos de uma vez para compensar uma dose esquecida. Se você não tiver certeza sobre quando tomar CIPRO 500mg comprimidos após uma dose esquecida, pergunte ao seu médico ou farmacêutico.
CIPRO Suspensão Oral:
- Tome CIPRO 1000mg Suspensão Oral de manhã e à noite aproximadamente à mesma hora todos os dias. Agite bem o frasco de Suspensão Oral CIPRO 750mg cada vez antes de usar por cerca de 15 segundos para garantir que a suspensão esteja bem misturada. Feche o frasco completamente após o uso.
- Se você perder uma dose de CIPRO Suspensão Oral e for:
- 6 horas ou mais até a próxima dose programada, tome a dose esquecida imediatamente. Em seguida, tome a próxima dose no horário habitual.
- menos de 6 horas até a próxima dose programada, não tome a dose esquecida. Tome a próxima dose no horário habitual.
- Não tome 2 doses de CIPRO 750mg Suspensão Oral de uma só vez para compensar uma dose esquecida. Se você não tiver certeza sobre quando tomar CIPRO Suspensão Oral após uma dose esquecida, pergunte ao seu médico ou farmacêutico.
O que devo evitar ao tomar CIPRO?
- CIPRO 250mg pode fazer você se sentir tonto e tonto. Não dirija, opere máquinas ou faça outras atividades que exijam alerta ou coordenação mental até saber como o CIPRO 250mg o afeta.
- Evite lâmpadas solares, camas de bronzeamento e tente limitar seu tempo ao sol. CIPRO 500mg pode tornar sua pele sensível ao sol (fotossensibilidade) e à luz de lâmpadas solares e camas de bronzeamento. Você pode ter queimaduras solares graves, bolhas ou inchaço da pele. Se você tiver algum desses sintomas enquanto estiver tomando CIPRO 250mg, ligue para o seu médico imediatamente. Você deve usar um protetor solar e usar um chapéu e roupas que cubram a pele se tiver que ficar na luz solar.
Quais são os possíveis efeitos colaterais do CIPRO?
CIPRO pode causar efeitos colaterais graves, incluindo:
- Ver “Qual é a informação mais importante que devo saber sobre o CIPRO?”
- Reações alérgicas graves. Reações alérgicas graves, incluindo morte, podem ocorrer em pessoas que tomam fluoroquinolonas, incluindo CIPRO, mesmo após apenas 1 dose. Pare de tomar CIPRO e procure ajuda médica de emergência imediatamente se tiver algum dos seguintes sintomas de uma reação alérgica grave:
- urticária
- batimento cardíaco acelerado
- dificuldade para respirar ou engolir
- desmaiar
- inchaço dos lábios, língua, rosto
- erupção cutânea
- aperto na garganta, rouquidão
A erupção cutânea pode ocorrer em pessoas que tomam CIPRO 1000mg mesmo após apenas 1 dose. Pare de tomar CIPRO 500mg ao primeiro sinal de erupção cutânea e ligue para o seu médico. A erupção cutânea pode ser um sinal de uma reação mais grave ao CIPRO.
- Danos no fígado (hepatotoxicidade). A hepatotoxicidade pode ocorrer em pessoas que tomam CIPRO. Ligue para o seu médico imediatamente se tiver sintomas inexplicáveis, como:
- náusea ou vômito
- cansaço incomum
- dor de estômago
- perda de apetite
- febre
- movimentos intestinais de cor clara
- fraqueza
- urina de cor escura
- dor ou sensibilidade abdominal
- amarelecimento da pele e do branco dos olhos
- coceira
Pare de tomar CIPRO 750mg e informe o seu médico imediatamente se tiver amarelamento da pele ou parte branca dos olhos, ou se tiver urina escura. Estes podem ser sinais de uma reação grave ao CIPRO (um problema no fígado).
- Aneurisma e dissecção da aorta. Informe o seu médico se alguma vez lhe foi dito que tem um aneurisma da aorta, um inchaço da grande artéria que transporta sangue do coração para o corpo. Obtenha ajuda médica de emergência imediatamente se tiver dor súbita no peito, no estômago ou nas costas.
- Infecção intestinal (Clostridioides difficile – diarreia associada). diarreia associada ao Clostridioides difficile (CDAD) pode ocorrer com muitos medicamentos antibacterianos, incluindo o CIPRO. Ligue para o seu médico imediatamente se tiver diarreia aquosa, diarreia que não desaparece ou fezes com sangue. Você pode ter cólicas estomacais e febre. CDAD pode ocorrer 2 ou mais meses após você ter terminado seu medicamento antibacteriano.
- Alterações graves do ritmo cardíaco (prolongamento do intervalo QT e torsade de pointes). Informe o seu médico imediatamente se tiver uma alteração no seu batimento cardíaco (batimento cardíaco rápido ou irregular) ou se desmaiar. CIPRO pode causar um problema cardíaco raro conhecido como prolongamento do intervalo QT. Esta condição pode causar um batimento cardíaco anormal e pode ser muito perigoso. As chances desse evento são maiores nas pessoas:
- que são idosos.
- com história familiar de intervalo QT prolongado.
- com baixo nível de potássio no sangue (hipocalemia) ou baixo nível de magnésio (hipomagnesemia).
- que tomam certos medicamentos para controlar o ritmo cardíaco (antiarrítmicos).
- Problemas comuns. Aumento da chance de problemas com articulações e tecidos ao redor das articulações em crianças menores de 18 anos pode acontecer. Informe o profissional de saúde do seu filho se ele tiver algum problema articular durante ou após o tratamento com CIPRO.
- Sensibilidade à luz solar (fotossensibilidade). Consulte “O que devo evitar ao tomar CIPRO 250mg?”
- Alterações no açúcar no sangue. As pessoas que tomam CIPRO e outros medicamentos de fluoroquinolona com medicamentos antidiabéticos orais ou com insulina podem apresentar níveis baixos de açúcar no sangue (hipoglicemia) e níveis elevados de açúcar no sangue (hiperglicemia). Siga as instruções do seu médico sobre com que frequência verificar o açúcar no sangue. Se você tem diabetes e tem baixo nível de açúcar no sangue enquanto toma CIPRO, pare de tomar CIPRO e ligue para seu médico imediatamente. Seu medicamento antibiótico pode precisar ser alterado.
Os efeitos colaterais mais comuns do CIPRO 750mg incluem:
- náusea
- diarréia
- alterações nos testes de função hepática
- vômito
- irritação na pele
Informe o seu médico sobre qualquer efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do CIPRO. Para mais informações, pergunte ao seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar o CIPRO?
CIPRO 500mg Comprimidos
- Armazenar em temperatura ambiente entre 68°F a 77°F (20°C a 25°C).
CIPRO 750mg Suspensão Oral
- Armazene as microcápsulas e o diluente em temperatura ambiente até 25°C (77°F).
- Não congele.
- Após o término do tratamento com CIPRO, jogue fora com segurança qualquer suspensão oral não utilizada.
Mantenha CIPRO 250mg e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre o uso seguro e eficaz do CIPRO.
Os medicamentos às vezes são prescritos para outros fins que não os listados em um Guia de Medicamentos. Não use CIPRO para uma condição para a qual não foi prescrito. Não dê CIPRO a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Este Guia de Medicação resume as informações mais importantes sobre o CIPRO. Se você quiser mais informações sobre o CIPRO, fale com seu médico. Você pode pedir ao seu médico ou farmacêutico informações sobre CIPRO 250mg que foram escritas para profissionais de saúde.
Quais são os ingredientes do CIPRO 500mg?
CIPRO 1000mg Comprimidos:
- Ingrediente ativo: Cipro 250mg cloridrato de floxacina
- Ingredientes inativos: amido de milho, crospovidona, hipromelose, estearato de magnésio, celulose microcristalina, polietilenoglicol, dióxido de silício e dióxido de titânio.
CIPRO Suspensão Oral:
- Ingrediente ativo: ciprofloxacina
- Ingredientes inativos:
- Microcápsulas contém: hipromelose, estearato de magnésio, copolímero de ácido metacrílico e polissorbato 20 e povidona.
- Diluente contém: triglicerídeos de cadeia média, sacarose, lecitina de soja, água e aroma de morango.
Este Guia de Medicação foi aprovado pela Food and Drug Administration dos EUA.
