Duricef 250mg, 500mg Cefadroxil Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Duricef e como é usado?
Duricef (cefadroxil) é um antibiótico cefalosporínico usado para tratar muitos tipos diferentes de infecções causadas por bactérias. A marca Duricef foi descontinuada e o cefadroxil está disponível na forma genérica.
Quais são os efeitos colaterais do Duricef?
Os efeitos colaterais comuns de Duricef (cefadroxil) incluem:
- dor de estômago ou dor,
- náusea,
- vômito,
- diarréia,
- músculos rígidos ou tensos,
- dores nas articulações,
- sentindo-se inquieto ou hiperativo,
- gosto incomum ou desagradável na boca,
- comichão ou erupção cutânea, ou
- coceira ou corrimento vaginal.
Informe o seu médico se tiver efeitos secundários improváveis mas muito graves de Duricef (cefadroxil), incluindo:
- náuseas ou vômitos persistentes,
- olhos ou pele amarelados,
- urina escura,
- novos sinais de infecção (por exemplo, dor de garganta persistente ou febre),
- hematomas ou sangramentos fáceis,
- alterações na quantidade de urina, ou
- alterações mentais/de humor (como confusão).
DESCRIÇÃO
DURICEF (cefadroxil) é um antibiótico cefalosporínico semissintético destinado à administração oral. É um pó cristalino branco a branco amarelado. É solúvel em água e é ácido-estável. É quimicamente designado como ácido 5-tia-l-azabiciclo[4.2.0]oct-2-eno-2-carboxílico, 7-[[amino(4-hidroxifenil)acetil]amino]-3-metil-8-oxo -, monohidrato[6R-[6α,7β(R*)]]-. Tem a fórmula C16H17N3O5S•H20 e o peso molecular de 381,40. Tem a seguinte fórmula estrutural:
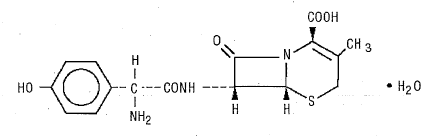
DURICEF (cefadroxil) comprimidos revestidos por película, 1 g, contém os seguintes ingredientes inativos: celulose microcristalina, hidroxipropilmetilcelulose, estearato de magnésio, polietilenoglicol, polissorbato 80, emulsão de simeticona e dióxido de titânio.
DURICEF (cefadroxil) para Suspensão Oral contém os seguintes ingredientes inativos: FD&C Amarelo Nº 6, aromas (naturais e artificiais), polissorbato 80, benzoato de sódio, sacarose e goma xantana.
As cápsulas de DURICEF (cefadroxil) contêm os seguintes ingredientes inativos: D&C Red No. 28, FD&C Blue No. 1, FD&C Red No. 40, gelatina, estearato de magnésio e dióxido de titânio.
INDICAÇÕES
DURICEF (cefadroxil) é indicado para o tratamento de pacientes com infecção causada por cepas sensíveis dos organismos designados nas seguintes doenças:
Infecções do trato urinário causadas por E. coli; P. mirabilis e espécies de Klebsiella.
Infecções da pele e da estrutura da pele causadas por estafilococos e/ou estreptococos.
Faringite e/ou amigdalite causadas por Streptococcus pyogenes (estreptococos beta-hemolíticos do Grupo A).
Observação: Apenas a penicilina por via intramuscular de administração demonstrou ser eficaz na profilaxia da febre reumática. DURICEF (cefadroxil) é geralmente eficaz na erradicação de estreptococos da orofaringe. No entanto, os dados que estabelecem a eficácia de DURICEF (cefadroxil) para a profilaxia da febre reumática subsequente não estão disponíveis.
Observação: Os testes de cultura e sensibilidade devem ser iniciados antes e durante a terapia. Estudos de função renal devem ser realizados quando indicado.
Para reduzir o desenvolvimento de bactérias resistentes a medicamentos e manter a eficácia de DURICEF (cefadroxil) e outros medicamentos antibacterianos, DURICEF (cefadroxil) deve ser usado apenas para tratar ou prevenir infecções comprovadas ou fortemente suspeitas de serem causadas por bactérias suscetíveis. Quando as informações de cultura e suscetibilidade estiverem disponíveis, elas devem ser consideradas na seleção ou modificação da terapia antibacteriana. Na ausência de tais dados, a epidemiologia local e os padrões de suscetibilidade podem contribuir para a seleção empírica da terapia.
DOSAGEM E ADMINISTRAÇÃO
DURICEF (cefadroxil) é ácido-estável e pode ser administrado por via oral independentemente das refeições. A administração com alimentos pode ser útil para diminuir potenciais queixas gastrointestinais ocasionalmente associadas à terapia oral com cefalosporina.
Adultos
Infecções do trato urinário: Para infecções não complicadas do trato urinário inferior (isto é, cistite), a dosagem usual é de 1 ou 2 g por dia em doses únicas (qd) ou divididas (bid).
Para todas as outras infecções do trato urinário, a dosagem usual é de 2 g por dia em doses divididas (bid).
Infecções da pele e da estrutura da pele: Para infecções da pele e estruturas da pele, a dosagem usual é de 1 g por dia em doses únicas (qd) ou divididas (bid).
Faringite e Amigdalite: Tratamento da faringite e amigdalite estreptocócica beta-hemolítica do grupo A - 1 g por dia em doses únicas (qd) ou divididas (bid) por 10 dias.
Crianças
Para infecções do trato urinário, a dose diária recomendada para crianças é de 30 mg/kg/dia em doses divididas a cada 12 horas. Para faringite, amigdalite e impetigo, a dose diária recomendada para crianças é de 30 mg/kg/dia em dose única ou em doses igualmente divididas a cada 12 horas. Para outras infecções da pele e estruturas da pele, a dose diária recomendada é de 30 mg/kg/dia em doses igualmente divididas a cada 12 horas. No tratamento de infecções estreptocócicas beta-hemolíticas, uma dose terapêutica de DURICEF (cefadroxil) deve ser administrada por pelo menos 10 dias.
Consulte a tabela para a dosagem diária total para crianças.
Insuficiência renal
Em pacientes com insuficiência renal, a dosagem de monohidrato de cefadroxil deve ser ajustada de acordo com as taxas de depuração de creatinina para evitar o acúmulo do fármaco. A seguinte programação é sugerida. Em adultos, a dose inicial é de 1000 mg de DURICEF (cefadroxil) e a dose de manutenção (baseada na taxa de depuração de creatinina [mL/min/1,73 M2]) é de 500 mg nos intervalos de tempo listados abaixo.
Pacientes com taxas de depuração de creatinina acima de 50 mL/min podem ser tratados como se fossem pacientes com função renal normal.
COMO FORNECIDO
DURICEF® (cefadroxil monohidratado, USP) 500 mg Cápsulas: cápsulas de gelatina dura opacas, marrons e brancas, impressas com "PPP" e "784" em uma extremidade e com "DURICEF (cefadroxil)" e "500 mg" na outra extremidade .
As cápsulas são fornecidas da seguinte forma:
N 0430-0780-19...................Garrafa de 50
Armazenar em temperatura ambiente controlada 15° - 30° C (59° - 86° F).
DURICEF® (cefadroxil) 1 grama Comprimidos: brancos a esbranquiçados, bissectados na parte superior, ovais, impressos com "PPP" de um lado da bissetriz e "785" do outro lado da bissetriz. Os comprimidos são fornecidos da seguinte forma:
N 0430-0781-19...................Garrafa de 50
Armazenar em temperatura ambiente controlada 15° - 30° C (59° - 86° F).
DURICEF® (cefadroxil) para Suspensão Oral tem sabor de laranja-abacaxi e é fornecido da seguinte forma:
250mg/5mL................................N 0430-2782-15 Frasco de 50 mL
Antes da reconstituição: Armazenar em temperatura ambiente controlada 15° - 30° C (59° - 86° F).
Fabricado por Bristol-Myers Squibb Co. Princeton, NJ 08543. Para Warner Chilcott Company, Inc. Fajardo, PR 00738. Comercializado por Warner Chilcott (EUA), Inc. Rockaway, NJ 07866. Revisado em abril de 2007. FDA Rev date: 6/ 5/2007
EFEITOS COLATERAIS
Gastrointestinal
O início dos sintomas de colite pseudomembranosa pode ocorrer durante ou após o tratamento com antibióticos (ver AVISOS ). Dispepsia, náuseas e vômitos foram relatados raramente. A diarreia também ocorreu.
Hipersensibilidade
Alergias (na forma de erupção cutânea, urticária, angioedema e prurido) foram observadas. Essas reações geralmente desaparecem com a descontinuação do medicamento. Anafilaxia também foi relatada.
Outro
Outras reações incluíram disfunção hepática incluindo colestase e elevações nas transaminases séricas, prurido genital, monilíase genital, vaginite, neutropenia transitória moderada, febre. Agranulocitose, trombocitopenia, insuficiência hepática idiossincrática, eritema multiforme, síndrome de Stevens-Johnson, doença do soro e artralgia foram raramente relatados.
Além das reações adversas listadas acima que foram observadas em pacientes tratados com cefadroxil, as seguintes reações adversas e testes laboratoriais alterados foram relatados para antibióticos da classe das cefalosporinas:
Necrólise epidérmica tóxica, dor abdominal, superinfecção, disfunção renal, nefropatia tóxica, anemia aplástica, anemia hemolítica, hemorragia, tempo de protrombina prolongado, teste de Coombs positivo, BUN aumentado, creatinina aumentada, fosfatase alcalina elevada, aspartato aminotransferase (AST), elevada alanina aminotransferase (ALT), bilirrubina elevada, LDH elevada, eosinofilia, pancitopenia, neutropenia.
Várias cefalosporinas foram implicadas no desencadeamento de convulsões, particularmente em pacientes com insuficiência renal, quando a dosagem não foi reduzida (ver DOSAGEM E ADMINISTRAÇÃO E SOBREDOSAGEM ). Se ocorrerem convulsões associadas à terapia medicamentosa, o medicamento deve ser descontinuado. A terapia anticonvulsivante pode ser administrada se clinicamente indicada.
INTERAÇÕES MEDICAMENTOSAS
Interações Medicamentos/Testes Laboratoriais
Testes de Coombs diretos positivos foram relatados durante o tratamento com antibióticos cefalosporínicos. Em estudos hematológicos ou em procedimentos de prova cruzada de transfusão quando testes de antiglobulina são realizados no lado menor ou em testes de Coombs de recém-nascidos cujas mães receberam antibióticos cefalosporínicos antes do parto, deve-se reconhecer que um teste de Coombs positivo pode ser devido à medicamento.
AVISOS
ANTES DE INSTITUIR A TERAPIA COM DURICEF (cefadroxil), DEVE-SE FAZER CUIDADOSA PESQUISA PARA DETERMINAR SE O PACIENTE TEVE REAÇÕES ANTERIORES DE HIPERSENSIBILIDADE A CEFADROXTL, CEFALOSPORINAS, PENICILINAS OU OUTRAS DROGAS. SE ESTE PRODUTO DEVE SER ADMINISTRADO A PACIENTES SENSÍVEIS À PENICILINA, DEVE-SE TER CUIDADO, POIS A SENSIBILIDADE CRUZADA ENTRE ANTIBIÓTICOS BETA-LACTAM FOI CLARAMENTE DOCUMENTADA E PODE OCORRER EM ATÉ 10% DOS PACIENTES COM HISTÓRICO DE ALERGIA À PENICILINA.
SE OCORRER UMA REAÇÃO ALÉRGICA A DURICEF (cefadroxil), INTERROMPA O MEDICAMENTO. REAÇÕES DE HIPERSENSIBILIDADE AGUDAS GRAVES PODEM REQUER TRATAMENTO COM EPINEFRINA E OUTRAS MEDIDAS DE EMERGÊNCIA, INCLUINDO OXIGÊNIO, LÍQUIDOS INTRAVENOSOS, ANTI-HISTAMÍNICOS INTRAVENOSOS, CORTICOSTEROIDES, AMINAS PRESSORA E MANEJO DAS VIAS RESPIRATÓRIAS, CONFORME INDICADO CLÍNICAMENTE.
Diarreia associada ao Clostridium difficile (CDAD) foi relatada com o uso de quase todos os agentes antibacterianos, incluindo DURICEF (cefadroxil), e pode variar em gravidade de diarreia leve a colite fatal. O tratamento com agentes antibacterianos altera a flora normal do cólon levando ao crescimento excessivo de C. difficile.
C. difficile produz toxinas A e B que contribuem para o desenvolvimento de CD AD. Cepas produtoras de hipertoxina de C. difficile causam aumento da morbidade e mortalidade, pois essas infecções podem ser refratárias à terapia antimicrobiana e podem exigir colectomia. A DC AD deve ser considerada em todos os pacientes que apresentam diarreia após o uso de antibióticos. É necessário um histórico médico cuidadoso, pois foi relatado que a DC AD ocorre mais de dois meses após a administração de agentes antibacterianos.
Se houver suspeita ou confirmação de DC AD, o uso contínuo de antibióticos não direcionados contra C. difficile pode precisar ser descontinuado. O manejo adequado de fluidos e eletrólitos, suplementação proteica, tratamento antibiótico de C. difficile e avaliação cirúrgica devem ser instituídos conforme indicação clínica.
PRECAUÇÕES
Em geral
DURICEF (cefadroxil) deve ser usado com cautela na presença de função renal marcadamente comprometida (taxa de depuração de creatinina inferior a 50 mL/min/1,73 M2). (Ver DOSAGEM E ADMINISTRAÇÃO .) Em pacientes com insuficiência renal conhecida ou suspeita, uma observação clínica cuidadosa e estudos laboratoriais apropriados devem ser feitos antes e durante a terapia.
A prescrição de DURICEF (cefadroxil) na ausência de infecção bacteriana comprovada ou fortemente suspeita ou indicação profilática provavelmente não trará benefícios ao paciente e aumenta o risco de desenvolvimento de bactérias resistentes aos medicamentos.
O uso prolongado de DURICEF (cefadroxil) pode resultar no crescimento excessivo de organismos honsusceptíveis. A observação cuidadosa do paciente é essencial. Se ocorrer superinfecção durante a terapia, medidas apropriadas devem ser tomadas.
DURICEF (cefadroxil) deve ser prescrito com cautela em indivíduos com histórico de doença gastrointestinal, particularmente colite.
Carcinogênese, Mutagênese e Prejuízo da Fertilidade
Não foram realizados estudos de longo prazo para determinar o potencial carcinogênico. Não foram realizados testes de toxicidade genética.
Gravidez: Gravidez Categoria B
Estudos de reprodução foram realizados em camundongos e ratos com doses de até 11 vezes a dose humana e não revelaram evidências de diminuição da fertilidade ou danos ao feto devido ao monohidrato de cefadroxil. No entanto, não existem estudos adequados e bem controlados em mulheres grávidas. Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, este medicamento deve ser usado durante a gravidez somente se for claramente necessário.
Trabalho e entrega
DURICEF (cefadroxil) não foi estudado para uso durante o trabalho de parto e parto. O tratamento só deve ser administrado se for claramente necessário.
Mães que amamentam
Deve-se ter cautela quando cefadroxil monohidratado é administrado a uma mãe que amamenta.
Uso Pediátrico
(Ver DOSAGEM E ADMINISTRAÇÃO. )
Uso Geriátrico
De aproximadamente 650 pacientes que receberam cefadroxil para o tratamento de infecções do trato urinário em três ensaios clínicos, 28% tinham 60 anos ou mais, enquanto 16% tinham 70 anos ou mais. De aproximadamente 1.000 pacientes que receberam cefadroxil para o tratamento de infecções da pele e estruturas da pele em 14 ensaios clínicos, 12% tinham 60 anos ou mais, enquanto 4% tinham 70 anos ou mais. Não foram observadas diferenças globais na segurança entre os pacientes idosos nestes estudos e os pacientes mais jovens. Estudos clínicos de cefadroxil para o. o tratamento da faringite ou amigdalite não incluiu um número suficiente de pacientes com 65 anos ou mais para determinar se eles respondem de forma diferente dos pacientes mais jovens. Outras experiências clínicas relatadas com cefadroxil não identificaram diferenças nas respostas entre pacientes idosos e mais jovens, mas a maior sensibilidade de alguns indivíduos mais velhos não pode ser descartada.
Cefadroxil é substancialmente excretado pelo rim, e o ajuste de dose é indicado para pacientes com insuficiência renal (ver DOSAGEM E ADMINISTRAÇÃO: Insuficiência Renal ). Como os pacientes idosos são mais propensos a ter função renal diminuída, deve-se ter cuidado na seleção da dose e pode ser útil monitorar a função renal.
SOBREDOSAGEM
Um estudo com crianças menores de seis anos sugeriu que a ingestão de menos de 250 mg/kg de cefalosporinas não está associada a desfechos significativos. Nenhuma ação é necessária além de apoio geral e observação. Para quantidades superiores a 250 mg/kg, induzir o esvaziamento gástrico.
Em cinco pacientes anúricos, foi demonstrado que uma média de 63% de uma dose oral de 1 g é extraída do corpo durante uma sessão de hemodiálise de 6 a 8 horas.
CONTRA-INDICAÇÕES
DURICEF (cefadroxil) é contraindicado em pacientes com alergia conhecida ao grupo de antibióticos das cefalosporinas.
FARMACOLOGIA CLÍNICA
DURICEF (cefadroxil) é rapidamente absorvido após administração oral. Após doses únicas de 500 mg e 1000 mg, as concentrações séricas máximas médias foram de aproximadamente 16 e 28 |ag/mL, respectivamente. Os níveis mensuráveis estavam presentes 12 horas após a administração. Mais de 90% da droga é excretada inalterada na urina em 24 horas. As concentrações máximas na urina são de aproximadamente 1800 pg/mL durante o período após uma dose oral única de 500 mg. Aumentos na dosagem geralmente produzem um aumento proporcional na concentração urinária de DURICEF (cefadroxil monohidratado, USP). A concentração de antibiótico na urina, após uma dose de 1 g, foi mantida bem acima da CIM de patógenos urinários suscetíveis por 20 a 22 horas.
Microbiologia
Testes in vitro demonstram que as cefalosporinas são bactericidas devido à inibição da síntese da parede celular. Cefadroxil demonstrou ser ativo contra os seguintes organismos tanto in vitro quanto em infecções clínicas (ver INDICAÇÕES ):
Estreptococos beta-hemolíticos Estafilococos, incluindo cepas produtoras de penicilinase Streptococcus (Diplococcus) pneumoniae Escherichia coli Proteus mirabilis Klebsiella species Moraxella (Branhamella) catarrhalis
Observação: A maioria das cepas de Entervcoccus faecalis (anteriormente Streptococcus faecalis) e Enterococcus faecium (anteriormente Streptococcus faecium) são resistentes ao DURICEF (cefadroxil). Não é ativo contra a maioria das cepas de espécies de Enterobacter, Morganella morganii (anteriormente Proteus morganii) e P. vulgaris. Não tem atividade contra espécies de Pseudomonas e Acinetobacter calcoaceticus (anteriormente espécies de Mima e Herellea).
Testes de suscetibilidade: Técnicas de difusão
uso de métodos de teste de suscetibilidade de disco a antibióticos que medem o diâmetro da zona fornece uma estimativa precisa da suscetibilidade a antibióticos. Um desses procedimentos padrão1 que foi recomendado para uso com discos para testar a suscetibilidade de organismos ao cefadroxil usa o disco da classe das cefalosporinas (cefalotina). A interpretação envolve a correlação dos diâmetros obtidos no teste do disco com a concentração inibitória mínima (CIM) para cefadroxil.
Os relatórios do laboratório com resultados do teste de sensibilidade padrão de disco único com um disco de cefalotina de 30 µg devem ser interpretados de acordo com os seguintes critérios:
Um relatório de "Susceptível" indica que o patógeno provavelmente será inibido por níveis sanguíneos geralmente alcançáveis. Um relato de "suscetibilidade intermediária" sugere que o organismo seria suscetível se for usada alta dosagem ou se a infecção estiver confinada a tecidos e fluidos (por exemplo, urina) nos quais altos níveis de antibióticos são atingidos. Um relatório de "Resistente" indica que é improvável que as concentrações alcançáveis do antibiótico sejam inibitórias e outra terapia deve ser selecionada.
Procedimentos padronizados requerem o uso de organismos de controle de laboratório. O disco de cefalotina de 30 µg deve fornecer os seguintes diâmetros de zona:
Técnicas de diluição
Ao usar o método de diluição em ágar NCCLS ou diluição em caldo (incluindo microdiluição)2 ou equivalente, um isolado bacteriano pode ser considerado suscetível se o valor de MIC (concentração inibitória mínima) para cefalotina for 8 µg/mL ou menos. Os organismos são considerados resistentes se a CIM for 32 µg/mL ou maior. Organismos com um valor de MIC inferior a 32 µg/mL, mas superior a 8 µg/mL são intermediários.
Tal como acontece com os métodos de difusão padrão, os procedimentos de diluição requerem o uso de organismos de controle de laboratório. O pó de cefalotina padrão deve fornecer valores de CIM na faixa de 0,12 µg/mL e 0,5 µg/mL para Staphylococcus aureus ATCC 29213. Vox Escherichia coli ATCC 25922, a faixa de CIM deve estar entre 4,0 µg/mL e 16,0 µg/mL. Para Streptococcus faecalis ATCC 29212, a faixa de CIM deve estar entre 8,0 e 32,0 µg/mL.
REFERÊNCIAS
1. Comitê Nacional de Padrões de Laboratório Clínico, Padrão Aprovado, Padrões de Desempenho para Teste de Susceptibilidade de Disco Antimicrobiano, 4ª Edição, Vol. 10 (7): M2-A4, Villanova, PA, abril de 1990.
2. Comitê Nacional de Padrões de Laboratório Clínico, Padrão Aprovado: Métodos para Testes de Susceptibilidade Antimicrobiana de Diluição para Bactérias que Crescem Aerobicamente, 2ª Edição, Vol. 10 (8): M7-A2, Villanova, PA, abril de 1990.
INFORMAÇÃO DO PACIENTE
Os pacientes devem ser informados de que medicamentos antibacterianos, incluindo DURICEF (cefadroxil), devem ser usados apenas para tratar infecções bacterianas. Eles não tratam infecções virais (por exemplo, o resfriado comum). Quando DURICEF (cefadroxil) é prescrito para tratar uma infecção bacteriana, os pacientes devem ser informados de que, embora seja comum sentir-se melhor no início do tratamento, a medicação deve ser tomada exatamente como indicado. Pular doses ou não completar o curso completo da terapia pode (1) diminuir a eficácia do tratamento imediato e (2) aumentar a probabilidade de que as bactérias desenvolvam resistência e não sejam tratáveis por DURICEF (cefadroxil) ou outros medicamentos antibacterianos no futuro .
diarreia é um problema comum causado por antibióticos que geralmente termina quando o antibiótico é descontinuado. Às vezes, após o início do tratamento com antibióticos, os pacientes podem desenvolver fezes aquosas e sanguinolentas (com ou sem cólicas estomacais e febre), mesmo dois ou mais meses após a última dose do antibiótico. Se isso ocorrer, os pacientes devem entrar em contato com seu médico o mais rápido possível.
