Flagyl 200mg, 400mg Metronidazole Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Flagyl e como é usado?
Flagyl é um medicamento de prescrição usado para tratar os sintomas de infecções bacterianas da vagina, estômago, fígado, pele, articulações, cérebro e trato respiratório. Flagyl pode ser usado sozinho ou com outros medicamentos.
Flagyl é um nitroimidazóis, inibidor de CYP3A4, moderado.
Quais são os possíveis efeitos colaterais do Flagyl 200mg?
Flagyl 400mg pode causar efeitos colaterais graves, incluindo:
- diarréia,
- dor ou dificuldade em urinar,
- problemas para dormir,
- depressão,
- irritabilidade,
- dor de cabeça,
- tontura
- fraqueza,
- tontura,
- bolhas ou úlceras na boca,
- gengivas vermelhas ou inchadas, e
- dificuldade para engolir
Informe o seu médico se tiver efeitos secundários graves de Flagyl, incluindo:
- dormência,
- formigamento,
- dor ardente nas mãos ou pés,
- problemas de visão,
- dor atrás de seus olhos,
- vendo flashes ou luz,
- fraqueza muscular,
- dificuldade de coordenação,
- dificuldade em falar ou entender o que é dito a você,
- apreensão,
- febre,
- rigidez de nuca e
- aumento da sensibilidade à luz
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Estes não são todos os possíveis efeitos colaterais do Flagyl. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Para reduzir o desenvolvimento de bactérias resistentes a medicamentos e manter a eficácia de FLAGYL® e de outros medicamentos antibacterianos, FLAGYL® deve ser usado apenas para tratar ou prevenir infecções comprovadas ou fortemente suspeitas de serem causadas por bactérias.
AVISO
O metronidazol demonstrou ser carcinogênico em camundongos e ratos (ver PRECAUÇÕES ). O uso desnecessário do medicamento deve ser evitado. Seu uso deve ser reservado para as condições descritas no INDICAÇÕES E USO seção abaixo.
DESCRIÇÃO
FLAGYL (metronidazol) comprimidos, 250 mg ou 500 mg é uma formulação oral do antimicrobiano sintético nitroimidazol, 2-metil-5-nitro-1H-imidazol-1-etanol, que possui a seguinte fórmula estrutural:
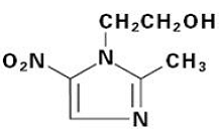
Os comprimidos de FLAGYL (metronidazol) contêm 250 mg ou 500 mg de metronidazol. Os ingredientes inativos incluem celulose, FD&C Blue No. 2 Lake, hidroxipropilcelulose, hipromelose, polietilenoglicol, ácido esteárico e dióxido de titânio.
INDICAÇÕES
Tricomoníase Sintomática. FLAGYL é indicado para o tratamento da infecção por T. vaginalis em mulheres e homens quando a presença do tricomonad foi confirmada por procedimentos laboratoriais apropriados (esfregaços úmidos e/ou culturas).
Tricomoníase Assintomática. FLAGYL 400mg é indicado no tratamento da infecção assintomática por T. vaginalis em mulheres quando o organismo está associado a endocervicite, cervicite ou erosão cervical. Como há evidências de que a presença do tricomonad pode interferir na avaliação precisa de esfregaços citológicos anormais, esfregaços adicionais devem ser realizados após a erradicação do parasita.
Tratamento de Parceiros Sexuais Assintomáticos. infecção por T. vaginalis é uma doença venérea. Portanto, parceiros sexuais assintomáticos de pacientes tratados devem ser tratados simultaneamente se o organismo estiver presente, a fim de evitar a reinfecção do parceiro. A decisão de tratar um parceiro masculino assintomático que tenha uma cultura negativa ou para quem nenhuma cultura foi tentada é individual. Ao tomar esta decisão, deve-se notar que há evidências de que uma mulher pode se reinfectar se seu parceiro sexual não for tratado. Além disso, uma vez que pode haver uma dificuldade considerável em isolar o organismo do portador assintomático do sexo masculino, esfregaços e culturas negativas não podem ser confiáveis a esse respeito. Em qualquer caso, o parceiro sexual deve ser tratado com FLAGYL em casos de reinfecção.
Amebíase. FLAGYL é indicado no tratamento da amebíase intestinal aguda (disenteria amebiana) e abscesso hepático amebiano.
No abscesso hepático amebiano, a terapia com FLAGYL não elimina a necessidade de aspiração ou drenagem de pus.
Infecções Bacterianas Anaeróbias. FLAGYL 200mg é indicado no tratamento de infecções graves causadas por bactérias anaeróbicas sensíveis. Os procedimentos cirúrgicos indicados devem ser realizados em conjunto com a terapia com FLAGYL. Em uma infecção mista aeróbica e anaeróbica, antimicrobianos apropriados para o tratamento da infecção aeróbia devem ser usados em adição ao FLAGYL.
INFECÇÕES INTRA-ABDOMINAIS, incluindo peritonite, abscesso intra-abdominal e abscesso hepático, causadas por espécies de Bacteroides, incluindo o grupo B. fragilis (B. fragilis, B. distasonis, B. ovatus, B. thetaiotaomicron, B. vulgatus), Clostridium espécies, espécies de Eubacterium, espécies de Peptococcus e espécies de Peptostreptococcus.
INFECÇÕES DA PELE E DA ESTRUTURA DA PELE causadas por espécies de Bacteroides, incluindo o grupo B. fragilis, espécies de Clostridium, espécies de Peptococcus, espécies de Peptostreptococcus e espécies de Fusobacterium.
INFECÇÕES GINECOLÓGICAS, incluindo endometrite, endomiometrite, abscesso tubo-ovariano e infecção do manguito vaginal pós-cirúrgico, causadas por espécies de Bacteroides, incluindo o grupo B. fragilis, espécies de Clostridium, espécies de Peptococcus, espécies de Peptostreptococcus e espécies de Fusobacterium.
SEPTICICEMIA BACTERIANA causada por espécies de Bacteroides incluindo o grupo B. fragilis e espécies de Clostridium.
INFECÇÕES ÓSSEAS E ARTICULARES, (como terapia adjuvante), causadas por espécies de Bacteroides incluindo o grupo B. fragilis.
INFECÇÕES DO SISTEMA NERVOSO CENTRAL (SNC), incluindo meningite e abscesso cerebral, causadas por espécies de Bacteroides, incluindo o grupo B. fragilis.
INFECÇÕES DO TRATO RESPIRATÓRIO INFERIOR, incluindo pneumonia, empiema e abscesso pulmonar, causadas por espécies de Bacteroides, incluindo o grupo B. fragilis.
ENDOCARDITE causada por espécies de Bacteroides incluindo o grupo B. fragilis.
Para reduzir o desenvolvimento de bactérias resistentes a medicamentos e manter a eficácia de FLAGYL 400mg e outros medicamentos antibacterianos, FLAGYL deve ser usado apenas para tratar ou prevenir infecções comprovadas ou fortemente suspeitas de serem causadas por bactérias suscetíveis. Quando as informações de cultura e suscetibilidade estiverem disponíveis, elas devem ser consideradas na seleção ou modificação da terapia antibacteriana. Na ausência de tais dados, a epidemiologia local e os padrões de suscetibilidade podem contribuir para a seleção empírica da terapia.
DOSAGEM E ADMINISTRAÇÃO
Tricomoníase
Na Fêmea
Tratamento de um dia - dois gramas de FLAGYL, administrados em dose única ou em duas doses divididas de um grama cada, administradas no mesmo dia.
Curso de sete dias de tratamento - 250 mg três vezes ao dia durante sete dias consecutivos. Há alguma indicação de estudos comparativos controlados de que as taxas de cura determinadas por esfregaços vaginais e sinais e sintomas podem ser maiores após um curso de tratamento de sete dias do que após um regime de tratamento de um dia.
O regime de dosagem deve ser individualizado. O tratamento de dose única pode garantir a adesão, especialmente se administrado sob supervisão, naqueles pacientes que não podem continuar com o regime de sete dias. Um curso de sete dias de tratamento pode minimizar a reinfecção, protegendo o paciente por tempo suficiente para que os contatos sexuais obtenham o tratamento adequado. Além disso, alguns pacientes podem tolerar um regime de tratamento melhor do que o outro.
Pacientes grávidas não devem ser tratadas durante o primeiro trimestre (ver CONTRA-INDICAÇÕES ). Em pacientes grávidas para as quais o tratamento alternativo foi inadequado, o curso de um dia de terapia não deve ser usado, pois resulta em níveis séricos mais elevados que podem atingir a circulação fetal (ver PRECAUÇÕES , Gravidez ).
Quando forem necessários ciclos repetidos do medicamento, recomenda-se um intervalo de quatro a seis semanas entre os ciclos e que a presença do tricomonad seja reconfirmada por medidas laboratoriais apropriadas. As contagens de leucócitos totais e diferenciais devem ser feitas antes e após o novo tratamento.
No Masculino: O tratamento deve ser individualizado como é para a mulher.
Amebíase
Adultos
Para amebíase intestinal aguda (disenteria amebiana aguda): 750 mg por via oral três vezes ao dia por 5 a 10 dias.
Para abscesso hepático amebiano: 500 mg ou 750 mg por via oral três vezes ao dia por 5 a 10 dias.
Pacientes pediátricos: 35 a 50 mg/kg/24 horas, divididas em três doses, via oral por 10 dias.
Infecções Bacterianas Anaeróbias
No tratamento das infecções anaeróbicas mais graves, o metronidazol intravenoso é geralmente administrado inicialmente.
A dosagem oral habitual para adultos é de 7,5 mg/kg a cada seis horas (aproximadamente 500 mg para um adulto de 70 kg). Um máximo de 4 g não deve ser excedido durante um período de 24 horas.
A duração usual da terapia é de 7 a 10 dias; entretanto, infecções ósseas e articulares, do trato respiratório inferior e do endocárdio podem exigir um tratamento mais prolongado.
Ajustes de dosagem
Pacientes com Insuficiência Hepática Grave
Para pacientes com insuficiência hepática grave (Child-Pugh C), a dose de FLAGYL deve ser reduzida em 50% (ver FARMACOLOGIA CLÍNICA e PRECAUÇÕES ).
Pacientes em Hemodiálise
hemodiálise remove quantidades significativas de metronidazol e seus metabólitos da circulação sistêmica. A depuração do metronidazol dependerá do tipo de membrana de diálise utilizada, da duração da sessão de diálise e de outros fatores. Se a administração de metronidazol não puder ser separada da sessão de hemodiálise, a suplementação da dose de metronidazol após a sessão de hemodiálise deve ser considerada, dependendo da situação clínica do paciente (ver FARMACOLOGIA CLÍNICA ).
COMO FORNECIDO
FLAGYL 250 mg os comprimidos são redondos, azuis, revestidos por película, com SEARLE e 1831 gravados numa das faces e FLAGYL e 250 na outra; fornecidos em garrafas de 50 e 100.
FLAGYL 500 mg os comprimidos são oblongos, azuis, revestidos por película, com FLAGYL gravado numa das faces e 500 na outra; garrafas de 50 e 100.
Armazenamento e estabilidade
Armazenar abaixo de 25°C (77°F) e proteger da luz.
Distribuído por: Pfizer Labs, Division of Pfizre Inc., NY, NY 10017. Revisado: dezembro de 2021
EFEITOS COLATERAIS
As seguintes reações foram relatadas durante o tratamento com metronidazol:
Sistema nervoso central
As reações adversas mais graves relatadas em pacientes tratados com metronidazol foram convulsões, encefalopatia, meningite asséptica, neuropatia óptica e periférica, esta última caracterizada principalmente por dormência ou parestesia de uma extremidade. Uma vez que neuropatia periférica persistente foi relatada em alguns pacientes que receberam administração prolongada de metronidazol, os pacientes devem ser especificamente alertados sobre essas reações e devem ser instruídos a interromper o medicamento e relatar imediatamente a seus médicos se ocorrerem quaisquer sintomas neurológicos. Além disso, os pacientes relataram dor de cabeça, síncope, tontura, vertigem, incoordenação, ataxia, confusão, disartria, irritabilidade, depressão, fraqueza e insônia (ver AVISOS ).
Gastrointestinal
As reações adversas mais comuns relatadas referem-se ao trato gastrointestinal, particularmente náuseas, algumas vezes acompanhadas de cefaleia, anorexia e, ocasionalmente, vômitos; diarréia; desconforto epigástrico; e cólicas abdominais e constipação.
Boca
Um gosto metálico acentuado e desagradável não é incomum. Língua peluda, glossite e estomatite ocorreram; estes podem estar associados a um crescimento súbito de Candida que pode ocorrer durante o tratamento.
Dermatológico
Erupção eritematosa e prurido.
Hematopoiético
Neutropenia reversível (leucopenia); raramente, trombocitopenia reversível.
Cardiovascular
Foi relatado prolongamento do intervalo QT, particularmente quando o metronidazol foi administrado com drogas com potencial para prolongar o intervalo QT. O achatamento da onda T pode ser visto nos traçados eletrocardiográficos.
Hipersensibilidade
Urticária, erupção cutânea eritematosa, síndrome de Stevens-Johnson, necrólise epidérmica tóxica, rubor, congestão nasal, secura da boca (ou vagina ou vulva) e febre.
Renal
Disúria, cistite, poliúria, incontinência e sensação de pressão pélvica. Casos de urina escurecida foram relatados por aproximadamente um paciente em 100.000. Embora o pigmento que provavelmente seja responsável por esse fenômeno não tenha sido identificado positivamente, é quase certamente um metabólito do metronidazol e parece não ter significado clínico.
Hepático
Casos de hepatotoxicidade irreversível grave/insuficiência hepática aguda, incluindo casos com desfechos fatais com início muito rápido após o início do uso sistêmico de metronidazol, foram relatados em pacientes com síndrome de Cockayne (latência desde o início do medicamento até os sinais de insuficiência hepática em até 2 dias). ) (Vejo CONTRA-INDICAÇÕES ).
Outro
Proliferação de Candida na vagina, dispareunia, diminuição da libido, proctite e dores articulares passageiras, às vezes lembrando “doença do soro”. Casos raros de pancreatite, que geralmente diminuíram com a retirada do medicamento, foram relatados.
Sabe-se que os pacientes com doença de Crohn têm uma incidência aumentada de cânceres gastrointestinais e certos extraintestinais. Houve alguns relatos na literatura médica de câncer de mama e cólon em pacientes com doença de Crohn que foram tratados com metronidazol em altas doses por longos períodos de tempo. Uma relação de causa e efeito não foi estabelecida. A doença de Crohn não é uma indicação aprovada para comprimidos de FLAGYL 200mg.
INTERAÇÕES MEDICAMENTOSAS
Dissulfiram
Reações psicóticas foram relatadas em pacientes alcoólatras que estão usando metronidazol e dissulfiram concomitantemente. O metronidazol não deve ser administrado a pacientes que tomaram dissulfiram nas últimas duas semanas (ver CONTRA-INDICAÇÕES ).
Bebidas Alcoólicas
Cólicas abdominais, náuseas, vômitos, dores de cabeça e rubor podem ocorrer se bebidas alcoólicas ou produtos contendo propilenoglicol forem consumidos durante ou após a terapia com metronidazol. CONTRA-INDICAÇÕES ).
Varfarina e outros anticoagulantes orais
Foi relatado que o metronidazol potencializa o efeito anticoagulante da varfarina e de outros anticoagulantes cumarínicos orais, resultando em prolongamento do tempo de protrombina. Quando FLAGYL é prescrito para pacientes em uso deste tipo de terapia anticoagulante, o tempo de protrombina e o INR devem ser cuidadosamente monitorados.

Lítio
Em pacientes estabilizados com doses relativamente altas de lítio, a terapia de curto prazo com metronidazol tem sido associada à elevação do lítio sérico e, em alguns casos, a sinais de toxicidade do lítio. Os níveis séricos de lítio e creatinina sérica devem ser obtidos vários dias após o início do metronidazol para detectar qualquer aumento que possa preceder os sintomas clínicos de intoxicação por lítio.
Bussulfan
Foi relatado que o metronidazol aumenta as concentrações plasmáticas de bussulfano, o que pode resultar em um risco aumentado de toxicidade grave por bussulfano. O metronidazol não deve ser administrado concomitantemente com bussulfano, a menos que o benefício supere o risco. Se não estiverem disponíveis alternativas terapêuticas ao metronidazol e a administração concomitante com bussulfano for clinicamente necessária, deve ser realizada monitorização frequente da concentração plasmática de bussulfano e a dose de bussulfano deve ser ajustada em conformidade.
Medicamentos que inibem as enzimas CYP450
A administração simultânea de medicamentos que diminuem a atividade das enzimas hepáticas microssomais, como a cimetidina, pode prolongar a meia-vida e diminuir a depuração plasmática do metronidazol.
Drogas que Induzem Enzimas CYP450
administração simultânea de drogas que induzem enzimas microssomais hepáticas, como fenitoína ou fenobarbital, pode acelerar a eliminação do metronidazol, resultando em níveis plasmáticos reduzidos; também foi relatada deficiência na depuração da fenitoína.
Medicamentos que prolongam o intervalo QT
Foi relatado prolongamento do intervalo QT, particularmente quando o metronidazol foi administrado com drogas com potencial para prolongar o intervalo QT.
AVISOS
Efeitos do sistema nervoso central e periférico
Encefalopatia e neuropatia periférica: Casos de encefalopatia e neuropatia periférica (incluindo neuropatia óptica) foram relatados com metronidazol.
Encefalopatia foi relatada em associação com toxicidade cerebelar caracterizada por ataxia, tontura e disartria. As lesões do SNC vistas na RM foram descritas em relatos de encefalopatia. Os sintomas do SNC são geralmente reversíveis dentro de dias a semanas após a descontinuação do metronidazol. As lesões do SNC vistas na ressonância magnética também foram descritas como reversíveis.
A neuropatia periférica, principalmente do tipo sensorial, tem sido relatada e é caracterizada por dormência ou parestesia de uma extremidade.
Crises convulsivas foram relatadas em pacientes tratados com metronidazol.
Meningite asséptica: Casos de meningite asséptica foram relatados com metronidazol. Os sintomas podem ocorrer horas após a administração da dose e geralmente desaparecem após a descontinuação da terapia com metronidazol.
O aparecimento de sinais e sintomas neurológicos anormais exige a avaliação imediata da relação benefício/risco da continuação da terapia (ver REAÇÕES ADVERSAS ).
PRECAUÇÕES
Em geral
Insuficiência hepática
Pacientes com insuficiência hepática metabolizam o metronidazol lentamente, com consequente acúmulo de metronidazol no plasma. Para pacientes com insuficiência hepática grave (Child-Pugh C), é recomendada uma dose reduzida de FLAGYL 400mg. Para pacientes com insuficiência hepática leve a moderada, nenhum ajuste de dose é necessário, mas esses pacientes devem ser monitorados para eventos adversos associados ao metronidazol (ver FARMACOLOGIA CLÍNICA e DOSAGEM E ADMINISTRAÇÃO ).
Insuficiência renal
Pacientes com doença renal terminal podem excretar metronidazol e metabólitos lentamente na urina, resultando em acúmulo significativo de metabólitos do metronidazol. Recomenda-se o monitoramento de eventos adversos associados ao metronidazol (ver FARMACOLOGIA CLÍNICA ).
Superinfecções fúngicas
A candidíase conhecida ou não reconhecida anteriormente pode apresentar sintomas mais proeminentes durante a terapia com FLAGYL e requer tratamento com um agente candidato.
Uso em pacientes com discrasias sanguíneas
metronidazol é um nitroimidazol e deve ser usado com cautela em pacientes com evidência ou histórico de discrasia sanguínea. Uma leve leucopenia foi observada durante sua administração; entretanto, nenhuma anormalidade hematológica persistente atribuível ao metronidazol foi observada em estudos clínicos. As contagens totais e diferenciais de leucócitos são recomendadas antes e após a terapia.
Bactérias e parasitas resistentes a drogas
A prescrição de FLAGYL na ausência de uma infecção bacteriana ou parasitária comprovada ou fortemente suspeita ou uma indicação profilática provavelmente não trará benefícios ao paciente e aumenta o risco de desenvolvimento de bactérias e parasitas resistentes aos medicamentos.
Interações Medicamentos/Testes Laboratoriais
metronidazol pode interferir com certos tipos de determinações de valores químicos séricos, como aspartato aminotransferase (AST, SGOT), alanina aminotransferase (ALT, SGPT), lactato desidrogenase (LDH), triglicerídeos e glicose hexoquinase. Valores de zero podem ser observados. Todos os ensaios nos quais foi relatada interferência envolvem acoplamento enzimático do ensaio à oxidação-redução do dinucleotídeo de nicotinamida adenina (NAD + NADH). A interferência se deve à semelhança nos picos de absorbância de NADH (340 nm) e metronidazol (322 nm) em pH 7.
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Tumores que afetam o fígado, pulmões, tecidos mamários e linfáticos foram detectados em vários estudos de metronidazol em ratos e camundongos, mas não em hamsters.
Tumores pulmonares foram observados em todos os seis estudos relatados no camundongo, incluindo um estudo em que os animais receberam doses em um esquema intermitente (administração apenas a cada quatro semanas). Os tumores malignos do fígado foram aumentados em camundongos machos tratados com aproximadamente 1500 mg/m² (semelhante à dose diária máxima recomendada, com base em comparações da área de superfície corporal). Linfomas malignos e neoplasias pulmonares também foram aumentados com a alimentação ao longo da vida da droga para camundongos. Tumores mamários e hepáticos foram aumentados entre ratas que receberam metronidazol oral em comparação com controles concomitantes. Dois estudos de tumorigenicidade ao longo da vida em hamsters foram realizados e relatados como negativos.
O metronidazol mostrou atividade mutagênica em sistemas de ensaio in vitro, incluindo o teste de Ames. Estudos em mamíferos in vivo não conseguiram demonstrar um potencial para danos genéticos.
metronidazol falhou em produzir quaisquer efeitos adversos na fertilidade ou na função testicular em ratos machos em doses de até 400 mg/kg/dia (semelhante à dose clínica máxima recomendada, com base em comparações de área de superfície corporal) por 28 dias. No entanto, os ratos tratados com a mesma dose por 6 semanas ou mais eram inférteis e mostraram degeneração grave do epitélio seminífero nos testículos, bem como diminuições acentuadas na contagem de espermátides testiculares e na contagem de espermatozóides do epidídimo. A fertilidade foi restaurada na maioria dos ratos após um período de recuperação sem drogas de oito semanas.
Gravidez
Efeitos teratogênicos
Não existem estudos adequados e bem controlados de FLAGYL em mulheres grávidas. Existem dados publicados de estudos caso-controle, estudos de coorte e 2 meta-análises que incluem mais de 5.000 gestantes que usaram metronidazol durante a gravidez. Muitos estudos incluíram exposições no primeiro trimestre. Um estudo mostrou um risco aumentado de lábio leporino, com ou sem fenda palatina, em lactentes expostos ao metronidazol in-utero; no entanto, esses achados não foram confirmados. Além disso, mais de dez ensaios clínicos randomizados controlados por placebo envolveram mais de 5.000 mulheres grávidas para avaliar o uso de tratamento com antibióticos (incluindo metronidazol) para vaginose bacteriana na incidência de parto prematuro. A maioria dos estudos não mostrou um risco aumentado de anomalias congênitas ou outros resultados fetais adversos após a exposição ao metronidazol durante a gravidez. Três estudos conduzidos para avaliar o risco de câncer infantil após a exposição ao metronidazol durante a gravidez não mostraram um risco aumentado; no entanto, a capacidade desses estudos para detectar tal sinal foi limitada.
metronidazol atravessa a barreira placentária e seus efeitos na organogênese fetal humana não são conhecidos. Estudos de reprodução foram realizados em ratos, coelhos e camundongos em doses semelhantes à dose humana máxima recomendada com base em comparações de área de superfície corporal. Não houve evidência de dano ao feto devido ao metronidazol.
Mães que amamentam
O metronidazol está presente no leite humano em concentrações semelhantes aos níveis séricos maternos, e os níveis séricos infantis podem ser próximos ou comparáveis aos níveis terapêuticos infantis. Devido ao potencial de tumorigenicidade mostrado para metronidazol em camundongos e ratos
estudos, deve-se decidir entre descontinuar a amamentação ou descontinuar o medicamento, levando em consideração a importância do medicamento para a mãe. Alternativamente, uma mãe que amamenta pode optar por bombear e descartar o leite humano durante a terapia com metronidazol e por 24 horas após o término da terapia e alimentar seu bebê com leite humano armazenado ou fórmula.
Uso Geriátrico
Em pacientes geriátricos idosos, recomenda-se o monitoramento de eventos adversos associados ao metronidazol (ver FARMACOLOGIA CLÍNICA , PRECAUÇÕES ). A função hepática diminuída em pacientes geriátricos pode resultar em concentrações aumentadas de metronidazol que podem necessitar de ajuste da dose de metronidazol (ver DOSAGEM E ADMINISTRAÇÃO ).
Uso Pediátrico
A segurança e eficácia em pacientes pediátricos não foram estabelecidas, exceto para o tratamento da amebíase.
SOBREDOSAGEM
Doses orais únicas de metronidazol, até 15 g, foram relatadas em tentativas de suicídio e overdoses acidentais. Os sintomas relatados incluem náuseas, vômitos e ataxia.
O metronidazol oral tem sido estudado como sensibilizador de radiação no tratamento de tumores malignos. Efeitos neurotóxicos, incluindo convulsões e neuropatia periférica, foram relatados após 5 a 7 dias de doses de 6 a 10,4 g em dias alternados.
Tratamento de superdosagem
Não há antídoto específico para superdosagem de metronidazol; portanto, o manejo do paciente deve consistir em terapia sintomática e de suporte.
CONTRA-INDICAÇÕES
Hipersensibilidade
FLAGYL Tablets é contraindicado em pacientes com história prévia de hipersensibilidade ao metronidazol ou a outros derivados do nitroimidazol.
Em pacientes com tricomoníase, FLAGYL 200mg comprimidos é contraindicado durante o primeiro trimestre de gravidez (ver PRECAUÇÕES ).
Reação psicótica com dissulfiram
O uso de metronidazol oral está associado a reações psicóticas em pacientes alcoólatras que estavam usando dissulfiram concomitantemente. Não administre metronidazol a pacientes que tomaram dissulfiram nas últimas duas semanas (ver PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS ).
Interação com álcool
O uso de metronidazol oral está associado a uma reação do tipo dissulfiram ao álcool, incluindo cólicas abdominais, náuseas, vômitos, dores de cabeça e rubor. Descontinuar o consumo de álcool ou produtos contendo propilenoglicol durante e por pelo menos três dias após a terapia com metronidazol (ver PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS ).
Síndrome de Cockayne
Os comprimidos de FLAGYL 400mg são contraindicados em pacientes com síndrome de Cockayne. Hepatotoxicidade irreversível grave/insuficiência hepática aguda com desfechos fatais foram relatados após o início do metronidazol em pacientes com síndrome de Cockayne (ver REAÇÕES ADVERSAS ).
FARMACOLOGIA CLÍNICA
Absorção
A disposição do metronidazol no corpo é semelhante para as formas de dosagem oral e intravenosa. Após administração oral, o metronidazol é bem absorvido, com picos de concentração plasmática ocorrendo entre uma e duas horas após a administração.
As concentrações plasmáticas de metronidazol são proporcionais à dose administrada. A administração oral de 250 mg, 500 mg ou 2.000 mg produziu concentrações plasmáticas máximas de 6 mcg/mL, 12 mcg/mL e 40 mcg/mL, respectivamente. Os estudos não revelam diferenças significativas de biodisponibilidade entre machos e fêmeas; no entanto, devido às diferenças de peso, os níveis plasmáticos resultantes nos homens são geralmente mais baixos.
Distribuição
metronidazol é o principal componente que aparece no plasma, estando também presentes quantidades menores de metabolitos. Menos de 20% do metronidazol circulante está ligado às proteínas plasmáticas. O metronidazol aparece no líquido cefalorraquidiano, saliva e leite materno em concentrações semelhantes às encontradas no plasma. Concentrações bactericidas de metronidazol também foram detectadas em pus de abscessos hepáticos.
Metabolismo/Excreção
A principal via de eliminação do metronidazol e seus metabólitos é a urina (60% a 80% da dose), sendo a excreção fecal responsável por 6% a 15% da dose. Os metabólitos que aparecem na urina resultam principalmente da oxidação da cadeia lateral [1-(ßhidroxietil)-2-hidroximetil-5-nitroimidazol e ácido 2-metil-5-nitroimidazol-1-ilacético] e conjugação de glicuronídeos, com contagem de metronidazol inalterada aproximadamente 20% do total. Tanto o composto original quanto o metabólito hidroxila possuem atividade antimicrobiana in vitro.
depuração renal do metronidazol é de aproximadamente 10 mL/min/1,73 m². A meia-vida média de eliminação do metronidazol em indivíduos saudáveis é de oito horas.
Insuficiência renal
A diminuição da função renal não altera a farmacocinética de dose única do metronidazol.
Indivíduos com doença renal terminal (ESRD; CLCR = 8,1±9,1 mL/min) e que receberam uma única infusão intravenosa de metronidazol 500 mg não tiveram alteração significativa na farmacocinética do metronidazol, mas tiveram Cmax 2 vezes maior de hidroximetronidazol e 5 - vezes maior Cmax do acetato de metronidazol, em comparação com indivíduos saudáveis com função renal normal (CLCR= 126±16 mL/min). Assim, devido ao potencial acúmulo de metabólitos do metronidazol em pacientes com insuficiência renal terminal, recomenda-se o monitoramento de eventos adversos associados ao metronidazol (ver PRECAUÇÕES ).
Efeito da diálise
Após uma única infusão intravenosa ou dose oral de metronidazol 500 mg, a depuração do metronidazol foi investigada em indivíduos com insuficiência renal terminal submetidos a hemodiálise ou diálise peritoneal ambulatorial contínua (CAPD). Uma sessão de hemodiálise com duração de 4 a 8 horas removeu 40% a 65% da dose administrada de metronidazol, dependendo do tipo de membrana dialisadora utilizada e da duração da sessão de diálise. Se a administração de metronidazol não puder ser separada da sessão de diálise, a suplementação da dose de metronidazol após a hemodiálise deve ser considerada (ver DOSAGEM E ADMINISTRAÇÃO ). Uma sessão de diálise peritoneal com duração de 7,5 horas removeu aproximadamente 10% da dose de metronidazol administrada. Nenhum ajuste na dose de metronidazol é necessário em pacientes com DRT submetidos a CAPD.
Insuficiência hepática
Após uma única infusão intravenosa de 500 mg de metronidazol, a AUC24 média do metronidazol foi maior em 114% em pacientes com insuficiência hepática grave (Child-Pugh C) e em 54% e 53% em pacientes com insuficiência hepática leve (Child-Pugh A) e insuficiência hepática moderada (Child-Pugh B), respectivamente, em comparação com indivíduos controles saudáveis. Não houve alterações significativas na AUC24 do hidroxil-metronidazol nesses pacientes com insuficiência hepática. Recomenda-se uma redução na dose de metronidazol em 50% em pacientes com insuficiência hepática grave (Child-Pugh C) (ver DOSAGEM E ADMINISTRAÇÃO ). Não é necessário ajuste de dose para pacientes com insuficiência hepática leve a moderada. Pacientes com insuficiência hepática leve a moderada devem ser monitorados quanto a eventos adversos associados ao metronidazol (ver PRECAUÇÕES e DOSAGEM E ADMINISTRAÇÃO ).
Pacientes Geriátricos
Após uma dose única de 500 mg oral ou IV de metronidazol, indivíduos >70 anos sem disfunção renal ou hepática aparente tiveram uma AUC média 40% a 80% maior de hidroximetronidazol (metabólito ativo), sem aumento aparente na média AUC do metronidazol (composto original), em comparação com controles saudáveis jovens PRECAUÇÕES ).
Pacientes pediátricos
Em um estudo, recém-nascidos pareciam demonstrar capacidade diminuída de eliminar o metronidazol. A meia-vida de eliminação, medida durante os primeiros 3 dias de vida, foi inversamente relacionada à idade gestacional. Em bebês com idade gestacional entre 28 e 40 semanas, as meias-vidas de eliminação correspondentes variaram de 109 a 22,5 horas.
Microbiologia
Mecanismo de ação
metronidazol, um nitroimidazol, exerce efeitos antibacterianos em um ambiente anaeróbico contra a maioria dos anaeróbios obrigatórios. Uma vez que o metronidazol entra no organismo por difusão passiva e é ativado no citoplasma de bactérias anaeróbicas suscetíveis, ele é reduzido; esse processo inclui proteínas de transporte intracelular de elétrons, como ferredoxina, transferência de um elétron para o grupo nitro do metronidazol e formação de um radical livre nitroso de curta duração. Devido a essa alteração da molécula do metronidazol, é criado e mantido um gradiente de concentração que promove o transporte intracelular do fármaco. A forma reduzida de metronidazol e radicais livres podem interagir com o DNA levando à inibição da síntese de DNA e degradação do DNA levando à morte das bactérias. O mecanismo preciso de ação do metronidazol não é claro.
Resistência
Existe um potencial para o desenvolvimento de resistência contra o metronidazol.
resistência pode ser devida a múltiplos mecanismos que incluem diminuição da absorção do fármaco, eficiência de redução alterada, superexpressão das bombas de efluxo, inativação do fármaco e/ou aumento do reparo de danos ao DNA.
O metronidazol não possui atividade clinicamente relevante contra anaeróbios facultativos ou aeróbios obrigatórios.
Actividade antimicrobiana
O metronidazol demonstrou ser ativo contra a maioria dos isolados das seguintes bactérias, tanto in vitro quanto em infecções clínicas, conforme descrito na seção INDICAÇÕES E USO.
Anaeróbios Gram-positivos
Espécies de Clostridium Espécies de Eubacterium Espécies de Peptococcus Espécies de Peptostreptococcus
Aeróbios Gram-negativos
Grupo Bacteroides fragilis (B. fragilis, B. distasonis, B. ovatus, B. thetaiotaomicron, B.vulgatus) Espécies de Fusobacterium
Parasitas Protozoários
Entamoeba histolytica Trichomonas vaginalis
Os seguintes dados in vitro estão disponíveis, mas seu significado clínico é desconhecido:
metronidazol exibe in vitro concentrações inibitórias mínimas (CIM's) de 8 mcg/mL ou menos contra a maioria (≥ 90%) dos isolados das seguintes bactérias; no entanto, a segurança e a eficácia do metronidazol no tratamento de infecções clínicas causadas por essas bactérias não foram estabelecidas em ensaios clínicos adequados e bem controlados.
Anaeróbios Gram-negativos
Grupo Bacteroides fragilis (B. caccae, B. uniformis) Espécies de Prevotella (P. bivia, P. buccae, P. disiens)
Teste de suscetibilidade
Para obter informações específicas sobre os critérios interpretativos do teste de suscetibilidade e métodos de teste associados e padrões de controle de qualidade reconhecidos pela FDA para este medicamento, consulte: https://www.fda.gov/STIC.
INFORMAÇÃO DO PACIENTE
Interação com álcool
Interrompa o consumo de bebidas alcoólicas ou produtos que contenham propilenoglicol enquanto estiver tomando FLAGYL 400mg e por pelo menos três dias depois, pois podem ocorrer cólicas abdominais, náuseas, vômitos, dores de cabeça e rubor. CONTRA-INDICAÇÕES e PRECAUÇÕES , INTERAÇÕES MEDICAMENTOSAS ).
Tratamento de infecções bacterianas e parasitárias
Os pacientes devem ser informados de que FLAGYL 400mg deve ser usado apenas para tratar infecções bacterianas e parasitárias. FLAGYL 400mg não trata infecções virais (por exemplo, resfriado comum). Quando FLAGYL é prescrito para tratar uma infecção bacteriana, os pacientes devem ser informados de que, embora seja comum sentir-se melhor no início do tratamento, a medicação deve ser tomada exatamente como indicado. Pular doses ou não completar o curso completo da terapia pode (1) diminuir a eficácia do tratamento imediato e (2) aumentar a probabilidade de que as bactérias desenvolvam resistência e não sejam tratáveis com FLAGYL 400mg no futuro.
