Catapres 100mcg Clonidine Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Catapres e como é usado?
Catapres é um medicamento de prescrição usado para tratar sintomas de pressão alta, transtorno de déficit de atenção e hiperatividade (TDAH) e dor de câncer. Catapres 100mcg pode ser usado sozinho ou com outros medicamentos.
Catapres 100mcg pertence a uma classe de medicamentos chamados Alpha2 Agonists, Central-Acting, ADHD Agents.
Não se sabe se Catapres 100mcg é seguro e eficaz em crianças menores de 12 anos.
Quais são os possíveis efeitos colaterais do Catapres?
Catapres pode causar efeitos colaterais graves, incluindo:
- sintomas de abstinência,
- nervosismo,
- agitação,
- dor de cabeça,
- tremor, e
- rápido aumento da pressão arterial
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Catapres 100mcg incluem:
- boca seca,
- tontura,
- sonolência,
- fadiga,
- constipação,
- dor de cabeça,
- náusea, e
- problemas para dormir (insônia)
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Catapres. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
DESCRIÇÃO
Catapres® (cloridrato de clonidina, USP) é um agente hipotensor alfa-agonista de ação central disponível na forma de comprimidos para administração oral em três dosagens: 0,1 mg, 0,2 mg e 0,3 mg. O comprimido de 0,1 mg é equivalente a 0,087 mg da base livre.
Os ingredientes inativos são dióxido de silício coloidal, amido de milho, fosfato de cálcio dibásico, FD&C Yellow No. 6, gelatina, glicerina, lactose e estearato de magnésio. O comprimido de Catapres 0,1 mg também contém FD&C Blue No.1 e FD&C Red No.3.
O cloridrato de clonidina é um derivado de imidazolina e existe como um composto mesomérico. O nome químico é cloridrato de 2-(2,6-diclorofenilamino)-2-imidazolina. Segue a fórmula estrutural:
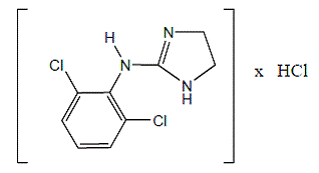 C9H9Cl2N3 · HCl Mol. Peso 266,56
C9H9Cl2N3 · HCl Mol. Peso 266,56 O cloridrato de clonidina é uma substância inodora, amarga, branca e cristalina, solúvel em água e álcool.
INDICAÇÕES
Os comprimidos de CATAPRES são indicados no tratamento da hipertensão. Os comprimidos de CATAPRES podem ser utilizados isoladamente ou concomitantemente com outros agentes anti-hipertensivos.
DOSAGEM E ADMINISTRAÇÃO
Adultos
A dose dos comprimidos de Catapres® (cloridrato de clonidina, USP) deve ser ajustada de acordo com a resposta individual da pressão arterial do paciente. O seguinte é um guia geral para a sua administração.
Dose inicial
Comprimido de 0,1 mg duas vezes ao dia (de manhã e ao deitar). Os doentes idosos podem beneficiar de uma dose inicial mais baixa.
Dose de Manutenção
Aumentos adicionais de 0,1 mg por dia podem ser feitos em intervalos semanais, se necessário, até que a resposta desejada seja alcançada. Tomar a maior porção da dose oral diária na hora de dormir pode minimizar os efeitos transitórios de ajuste de boca seca e sonolência. As doses terapêuticas mais comumente empregadas variam de 0,2 mg a 0,6 mg por dia, administradas em doses divididas. Estudos indicaram que 2,4 mg é a dose diária efetiva máxima, mas doses tão altas como esta raramente foram empregadas.
Insuficiência renal
Pacientes com insuficiência renal podem se beneficiar de uma dose inicial mais baixa. Os pacientes devem ser cuidadosamente monitorados. Uma vez que apenas uma quantidade mínima de clonidina é removida durante a hemodiálise de rotina, não há necessidade de administrar clonidina suplementar após a diálise.
COMO FORNECIDO
Os comprimidos Catapres® (cloridrato de clonidina, USP) são fornecidos da seguinte forma:
Armazenar a 25°C (77°F); excursões permitidas para 15°-30°C (59°-86°F) [Vejo Temperatura ambiente controlada USP ].
Dispensar em recipiente hermético e resistente à luz.
Distribuído por: Boehringer Ingelheim Pharmaceuticals, Inc., Ridgefield, CT 06877 EUA. Fabricado por: Boehringer Ingelheim Promeco SA de CV, Cidade do México, México. Licenciado de: Boehringer Ingelheim, International GmbH, Envie consultas médicas para: (800) 542-6257 ou (800) 459-9906. Revisado: maio de 2012
EFEITOS COLATERAIS
A maioria dos efeitos adversos são leves e tendem a diminuir com a continuação da terapia. Os mais frequentes (que parecem estar relacionados com a dose) são boca seca, ocorrendo em cerca de 40 de 100 pacientes; sonolência, cerca de 33 em 100; tonturas, cerca de 16 em 100; constipação e sedação, cada uma cerca de 10 em 100.
As seguintes experiências adversas menos frequentes também foram relatadas em pacientes recebendo CATAPRES 100mcg comprimidos, mas em muitos casos os pacientes estavam recebendo medicação concomitante e uma relação causal não foi estabelecida.
Corpo como um todo: Fadiga, febre, dor de cabeça, palidez, fraqueza e síndrome de abstinência. Também foram relatados um teste de Coombs fracamente positivo e aumento da sensibilidade ao álcool.
Cardiovascular: Bradicardia, insuficiência cardíaca congestiva, anormalidades eletrocardiográficas (ou seja, parada do nó sinusal, bradicardia juncional, bloqueio AV de alto grau e arritmias), sintomas ortostáticos, palpitações, fenômeno de Raynaud, síncope e taquicardia. Casos de bradicardia sinusal e bloqueio atrioventricular foram relatados, com e sem o uso concomitante de digitálicos.
Sistema nervoso central: Agitação, ansiedade, delírio, percepção delirante, alucinações (incluindo visuais e auditivas), insônia, depressão mental, nervosismo, outras alterações comportamentais, parestesia, inquietação, distúrbio do sono e sonhos ou pesadelos vívidos.
Dermatológico: Alopecia, edema angioneurótico, urticária, prurido, erupção cutânea e urticária.
Gastrointestinal: Dor abdominal, anorexia, constipação, hepatite, mal-estar, anormalidades transitórias leves nos testes de função hepática, náusea, parotidite, pseudo-obstrução (incluindo pseudo-obstrução colônica), dor nas glândulas salivares e vômitos.
Geniturinário: Diminuição da atividade sexual, dificuldade de micção, disfunção erétil, perda de libido, noctúria e retenção urinária.
Hematologico: Trombocitopenia.
Metabólico: Ginecomastia, elevação transitória da glicemia ou creatina fosfoquinase sérica e ganho de peso.
Musculoesquelético: Cãibras nas pernas e dores musculares ou articulares.
Oro-otolaríngeo: Secura da mucosa nasal.
Oftalmológico: Distúrbio de acomodação, visão turva, ardor nos olhos, diminuição do lacrimejamento e secura dos olhos.
INTERAÇÕES MEDICAMENTOSAS
A clonidina pode potencializar os efeitos depressivos do SNC do álcool, barbitúricos ou outras drogas sedativas. Se um paciente recebendo cloridrato de clonidina também estiver tomando antidepressivos tricíclicos, o efeito hipotensor da clonidina pode ser reduzido, necessitando de um aumento na dose de clonidina. Se um paciente recebendo clonidina também estiver tomando neurolépticos, distúrbios da regulação ortostática (por exemplo, hipotensão ortostática, tontura, fadiga) podem ser induzidos ou exacerbados.
Monitorar a frequência cardíaca em pacientes recebendo clonidina concomitantemente com agentes conhecidos por afetar a função do nó sinusal ou a condução nodal AV, por exemplo, digitálicos, bloqueadores dos canais de cálcio e betabloqueadores. Bradicardia sinusal resultando em hospitalização e inserção de marcapasso tem sido relatada em associação com o uso de clonidina concomitantemente com diltiazem ou verapamil.
Amitriptilina em combinação com clonidina aumenta a manifestação de lesões da córnea em ratos (ver Toxicologia ).
Com base em observações em pacientes em estado de delírio alcoólico, foi sugerido que altas doses intravenosas de clonidina podem aumentar o potencial arritmogênico (prolongamento QT, fibrilação ventricular) de altas doses intravenosas de haloperidol. A relação causal e relevância para os comprimidos orais de clonidina não foram estabelecidas.
AVISOS
Cancelamento
Os pacientes devem ser instruídos a não descontinuar a terapia sem consultar seu médico. A interrupção repentina do tratamento com clonidina resultou, em alguns casos, em sintomas como nervosismo, agitação, dor de cabeça e tremores acompanhados ou seguidos por um rápido aumento da pressão arterial e concentrações elevadas de catecolaminas no plasma. A probabilidade de tais reações à descontinuação da terapia com clonidina parece ser maior após a administração de doses mais altas ou a continuação do tratamento concomitante com betabloqueador e, portanto, recomenda-se cautela especial nessas situações. Raros casos de encefalopatia hipertensiva, acidentes vasculares cerebrais e morte foram relatados após a retirada da clonidina. Ao descontinuar a terapia com CATAPRES comprimidos, o médico deve reduzir a dose gradualmente ao longo de 2 a 4 dias para evitar sintomas de abstinência.
Um aumento excessivo da pressão arterial após a descontinuação da terapia com CATAPRES 100mcg comprimidos pode ser revertido pela administração de cloridrato de clonidina oral ou por fentolamina intravenosa. Se a terapia for descontinuada em pacientes recebendo um betabloqueador e clonidina concomitantemente, o betabloqueador deve ser descontinuado vários dias antes da descontinuação gradual de CATAPRES 100mcg comprimidos.
Como as crianças geralmente têm doenças gastrointestinais que levam ao vômito, elas podem ser particularmente suscetíveis a episódios hipertensivos resultantes da incapacidade abrupta de tomar medicamentos.
PRECAUÇÕES
Em geral
Em pacientes que desenvolveram sensibilização de contato localizada ao Catapres-TTS® (clonidina), a continuação do Catapres-TTS ou a substituição da terapia oral com cloridrato de clonidina pode estar associada ao desenvolvimento de erupção cutânea generalizada.
Em pacientes que desenvolvem uma reação alérgica ao Catapres-TTS, a substituição de cloridrato de clonidina oral também pode provocar uma reação alérgica (incluindo erupção cutânea generalizada, urticária ou angioedema).
A ação simpatolítica da clonidina pode piorar a disfunção do nó sinusal e o bloqueio atrioventricular (AV), especialmente em pacientes em uso de outras drogas simpatolíticas. Há relatos pós-comercialização de pacientes com anormalidades de condução e/ou tomando outras drogas simpatolíticas que desenvolveram bradicardia grave necessitando de atropina IV, isoproterenol IV e estimulação cardíaca temporária enquanto tomavam clonidina.
Na hipertensão causada por feocromocitoma, nenhum efeito terapêutico de CATAPRES 100mcg comprimidos pode ser esperado.
Uso perioperatório
administração dos comprimidos de Catapres® (cloridrato de clonidina, USP) deve ser continuada até 4 horas após a cirurgia e retomada o mais rápido possível a partir de então. A pressão arterial deve ser cuidadosamente monitorada durante a cirurgia e medidas adicionais para controlar a pressão arterial devem estar disponíveis, se necessário.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
A administração dietética crônica de clonidina não foi carcinogênica para ratos (132 semanas) ou camundongos (78 semanas) com doses, respectivamente, de até 46 ou 70 vezes a dose humana diária máxima recomendada em mg/kg (9 ou 6 vezes o MRDHD em um base mg/m²). Não houve evidência de genotoxicidade no teste de Ames para mutagenicidade ou teste de micronúcleo em camundongo para clastogenicidade.
A fertilidade de ratos machos ou fêmeas não foi afetada por doses de clonidina tão altas quanto 150 μg/kg (aproximadamente 3 vezes MRDHD). Em um experimento separado, a fertilidade de ratas parece ser afetada em níveis de dose de 500 a 2.000 μg/kg (10 a 40 vezes o MRDHD oral com base em mg/kg; 2 a 8 vezes o MRDHD com base em mg/m² ).
Gravidez
Efeitos teratogênicos
Gravidez Categoria C
Estudos de reprodução realizados em coelhos com doses de até aproximadamente 3 vezes a dose oral máxima diária recomendada para humanos (MRDHD) de comprimidos de Catapres® (cloridrato de clonidina, USP) não produziram evidência de potencial teratogênico ou embriotóxico em coelhos. Em ratos, no entanto, doses tão baixas quanto 1/3 do MRDHD oral (1/15 do MRDHD em uma base de mg/m²) de clonidina foram associadas a reabsorções aumentadas em um estudo no qual as mães foram tratadas continuamente a partir de 2 meses antes do acasalamento . Reabsorções aumentadas não foram associadas ao tratamento ao mesmo tempo ou em níveis de dose mais altos (até 3 vezes o MRDHD oral) quando as mães foram tratadas nos dias de gestação 6 a 15. Aumentos na reabsorção foram observados em níveis de dose muito mais altos (40 vezes o MRDHD oral em uma base de mg/kg; 4 a 8 vezes o MRDHD em uma base de mg/m²) em camundongos e ratos tratados nos dias de gestação 1 a 14 (a dose mais baixa empregada no estudo foi de 500 μg/kg).
Não foram realizados estudos adequados e bem controlados em mulheres grávidas. A clonidina atravessa a barreira placentária (ver FARMACOLOGIA CLÍNICA , Farmacocinética ). Como os estudos de reprodução em animais nem sempre são preditivos da resposta humana, este medicamento deve ser usado durante a gravidez somente se for claramente necessário.
Mães que amamentam
Como o cloridrato de clonidina é excretado no leite humano, deve-se ter cautela quando os comprimidos de CATAPRES 100 mcg são administrados a uma lactante.
Uso Pediátrico
A segurança e a eficácia em pacientes pediátricos não foram estabelecidas em estudos adequados e bem controlados (ver AVISOS , Cancelamento ).
SOBREDOSAGEM
hipertensão pode se desenvolver precocemente e pode ser seguida de hipotensão, bradicardia, depressão respiratória, hipotermia, sonolência, diminuição ou ausência de reflexos, fraqueza, irritabilidade e miose. A frequência de depressão do SNC pode ser maior em crianças do que em adultos. Grandes overdoses podem resultar em defeitos reversíveis de condução cardíaca ou arritmias, apnéia, coma e convulsões. Os sinais e sintomas de superdosagem geralmente ocorrem dentro de 30 minutos a duas horas após a exposição. Apenas 0,1 mg de clonidina produziu sinais de toxicidade em crianças.
Não há antídoto específico para superdosagem de clonidina. A superdosagem de clonidina pode resultar no rápido desenvolvimento de depressão do SNC; portanto, a indução do vômito com xarope de ipeca não é recomendada. A lavagem gástrica pode ser indicada após ingestões recentes e/ou grandes. A administração de carvão ativado e/ou catártico pode ser benéfica. Os cuidados de suporte podem incluir sulfato de atropina para bradicardia, fluidos intravenosos e/ou agentes vasopressores para hipotensão e vasodilatadores para hipertensão. A naloxona pode ser um adjuvante útil para o manejo da depressão respiratória, hipotensão e/ou coma induzidos por clonidina; a pressão arterial deve ser monitorada, pois a administração de naloxona ocasionalmente resultou em hipertensão paradoxal. Não é provável que a diálise aumente significativamente a eliminação da clonidina.
maior overdose relatada até o momento envolveu um homem de 28 anos que ingeriu 100 mg de pó de cloridrato de clonidina. Este paciente desenvolveu hipertensão seguida de hipotensão, bradicardia, apnéia, alucinações, semicoma e contrações ventriculares prematuras. O paciente se recuperou totalmente após tratamento intensivo. Os níveis de clonidina no plasma foram de 60 ng/ml após 1 hora, 190 ng/ml após 1,5 horas, 370 ng/ml após 2 horas e 120 ng/ml após 5,5 e 6,5 horas. Em camundongos e ratos, a LD50 oral da clonidina é de 206 e 465 mg/kg, respectivamente.
CONTRA-INDICAÇÕES
Os comprimidos de Catapres® (cloridrato de clonidina, USP) não devem ser usados em pacientes com hipersensibilidade conhecida à clonidina (ver PRECAUÇÕES ).
FARMACOLOGIA CLÍNICA
clonidina estimula alfa-adrenorreceptores no tronco cerebral. Essa ação resulta na redução do fluxo simpático do sistema nervoso central e na diminuição da resistência periférica, da resistência vascular renal, da frequência cardíaca e da pressão arterial. Os comprimidos CATAPRES 100mcg agem de forma relativamente rápida. A pressão arterial do paciente diminui dentro de 30 a 60 minutos após uma dose oral, a diminuição máxima ocorrendo dentro de 2 a 4 horas. O fluxo sanguíneo renal e a taxa de filtração glomerular permanecem essencialmente inalterados. Os reflexos posturais normais estão intactos; portanto, os sintomas ortostáticos são leves e infrequentes.
Estudos agudos com cloridrato de clonidina em humanos demonstraram redução moderada (15% a 20%) do débito cardíaco na posição supina sem alteração da resistência periférica: na inclinação de 45° há menor redução do débito cardíaco e diminuição de resistência periférica. Durante a terapia de longo prazo, o débito cardíaco tende a retornar aos valores de controle, enquanto a resistência periférica permanece diminuída. A diminuição da frequência de pulso foi observada na maioria dos pacientes que receberam clonidina, mas a droga não altera a resposta hemodinâmica normal ao exercício.
A tolerância ao efeito anti-hipertensivo pode se desenvolver em alguns pacientes, necessitando de uma reavaliação da terapia.
Outros estudos em pacientes forneceram evidências de redução na atividade da renina plasmática e na excreção de aldosterona e catecolaminas. A relação exata dessas ações farmacológicas com o efeito anti-hipertensivo da clonidina não foi totalmente elucidada.
clonidina estimula agudamente a liberação do hormônio do crescimento em crianças e adultos, mas não produz uma elevação crônica do hormônio do crescimento com o uso prolongado.
Farmacocinética
A farmacocinética da clonidina é proporcional à dose na faixa de 100 a 600 μg. A biodisponibilidade absoluta da clonidina na administração oral é de 70% a 80%. Os níveis plasmáticos máximos de clonidina são atingidos em aproximadamente 1 a 3 horas.
Após administração intravenosa, a clonidina apresenta disposição bifásica com meia-vida de distribuição de cerca de 20 minutos e meia-vida de eliminação variando de 12 a 16 horas. A meia-vida aumenta até 41 horas em pacientes com insuficiência grave da função renal. A clonidina atravessa a barreira placentária. Demonstrou-se que atravessa a barreira hematoencefálica em ratos.
Após administração oral, cerca de 40% a 60% da dose absorvida é recuperada na urina como droga inalterada em 24 horas. Cerca de 50% da dose absorvida é metabolizada no fígado. Nem a alimentação nem a raça do paciente influenciam a farmacocinética da clonidina.
O efeito anti-hipertensivo é alcançado em concentrações plasmáticas entre cerca de 0,2 e 2,0 ng/mL em pacientes com função excretora normal. Um aumento adicional dos níveis plasmáticos não aumentará o efeito anti-hipertensivo.
Toxicologia
Em vários estudos com cloridrato de clonidina oral, um aumento dependente da dose na incidência e gravidade da degeneração retiniana espontânea foi observado em ratos albinos tratados por seis meses ou mais. Estudos de distribuição tecidual em cães e macacos mostraram uma concentração de clonidina na coróide.
Em vista da degeneração da retina observada em ratos, foram realizados exames oftalmológicos durante os ensaios clínicos em 908 pacientes antes e periodicamente após o início da terapia com clonidina. Em 353 desses 908 pacientes, os exames oftalmológicos foram realizados em períodos de 24 meses ou mais. Exceto por alguma secura dos olhos, nenhum achado oftalmológico anormal relacionado ao medicamento foi registrado e, de acordo com testes especializados, como eletrorretinografia e deslumbramento macular, a função da retina permaneceu inalterada.
Em combinação com amitriptilina, a administração de cloridrato de clonidina levou ao desenvolvimento de lesões da córnea em ratos em 5 dias.
INFORMAÇÃO DO PACIENTE
Os pacientes devem ser advertidos contra a interrupção da terapia com CATAPRES 100mcg comprimidos sem o conselho de seu médico.
Como os pacientes podem apresentar um possível efeito sedativo, tontura ou distúrbio de acomodação com o uso de clonidina, alerte os pacientes sobre a realização de atividades como dirigir veículos ou operar aparelhos ou máquinas. Além disso, informe os pacientes que este efeito sedativo pode ser aumentado pelo uso concomitante de álcool, barbitúricos ou outros medicamentos sedativos.
Os pacientes que usam lentes de contato devem ser advertidos de que o tratamento com CATAPRES comprimidos pode causar secura nos olhos.
