Hyzaar 12.5mg Hydrochlorothiazide Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Hyzaar e como é usado?
Hyzaar 12,5mg é um medicamento de prescrição usado para tratar os sintomas da pressão alta (hipertensão). Hyzaar pode ser usado sozinho ou com outros medicamentos.
Hyzaar pertence a uma classe de medicamentos chamados ARB/HCTZ Combos.
Não se sabe se Hyzaar é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Hyzaar 12,5mg?
Hyzaar pode causar efeitos colaterais graves, incluindo:
- tontura,
- batimentos cardíacos irregulares,
- dor nos olhos,
- problemas de visão,
- pouca ou nenhuma micção,
- ganho de peso rápido,
- inchaço nas mãos, pés ou tornozelos,
- dores nas articulações,
- erupção cutânea nas bochechas ou braços que piora com a luz solar,
- aumento da sede,
- aumento da micção,
- confusão,
- vômito,
- constipação,
- dor muscular,
- cãibras nas pernas,
- fraqueza severa,
- dormência ou formigamento,
- perda de movimento e
- sentindo-se nervoso ou instável
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns do Hyzaar incluem:
- tontura,
- dores nas costas e
- sintomas de resfriado (nariz entupido, espirros, dor de garganta)
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Hyzaar. Para mais informações, consulte seu médico ou farmacêutico.
Ligue para o seu médico para aconselhamento médico sobre os efeitos colaterais. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
AVISO
TOXICIDADE FETAL
Quando a gravidez for detectada, descontinue HYZAAR o mais rápido possível. Drogas que agem diretamente no sistema renina-angiotensina podem causar lesão e morte do feto em desenvolvimento [ver AVISOS E PRECAUÇÕES ].
DESCRIÇÃO
Os comprimidos de HYZAAR 50/12.5 (losartana potássica-hidroclorotiazida), HYZAAR 100/12.5 (losartana potássica hidroclorotiazida) e HYZAAR 100/25 (losartana potássica-hidroclorotiazida) combinam um bloqueador do receptor da angiotensina II que atua no subtipo do receptor AT1 e um diurético, a hidroclorotiazida.
losartana potássica, uma molécula não peptídica, é quimicamente descrita como sal monopotássico de 2-butil-4-cloro-1-[p-(o-1H-tetrazol-5-ilfenil)benzil]imidazol-5-metanol. Sua fórmula empírica é C22H22ClKN6O, e sua fórmula estrutural é:
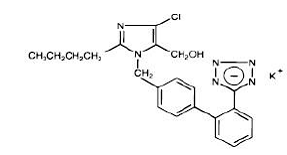
Losartana potássica é um pó cristalino de fluxo livre branco a esbranquiçado com um peso molecular de 461,01. É livremente solúvel em água, solúvel em álcoois e ligeiramente solúvel em solventes orgânicos comuns, como acetonitrila e metiletilcetona.
A oxidação do grupo 5-hidroximetil no anel imidazol resulta no metabólito ativo do losartan.
Hidroclorotiazida é 1,1-dióxido de 6-cloro-3,4-di-hidro-2H-1,2,4-benzotiadiazina-7-sulfonamida. Sua fórmula empírica é C7H8ClN3O4S2 e sua fórmula estrutural é:
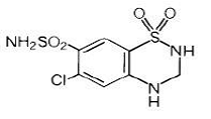
A hidroclorotiazida é um pó cristalino branco, ou praticamente branco, com um peso molecular de 297,74, que é ligeiramente solúvel em água, mas livremente solúvel em solução de hidróxido de sódio.
HYZAAR está disponível para administração oral em três combinações de comprimidos de losartana e hidroclorotiazida. HYZAAR 50/12.5 contém 50 mg de losartana potássica e 12,5 mg de hidroclorotiazida. HYZAAR 100/12.5 contém 100 mg de losartana potássica e 12,5 mg de hidroclorotiazida. HYZAAR 100/25 contém 100 mg de losartana potássica e 25 mg de hidroclorotiazida. Os ingredientes inativos são celulose microcristalina, lactose hidratada, amido pré-gelatinizado, estearato de magnésio, hidroxipropilcelulose, hipromelose e dióxido de titânio.
HYZAAR 50/12.5 e HYZAAR 100/25 também contêm laca de alumínio D&C amarela nº 10. HYZAAR 50/12.5, HYZAAR 100/12.5 e HYZAAR 100/25 também podem conter cera de carnaúba.
HYZAAR 50/12.5 contém 4,24 mg (0,108 mEq) de potássio, HYZAAR 100/12,5 contém 8,48 mg (0,216 mEq) de potássio e HYZAAR 100/25 contém 8,48 mg (0,216 mEq) de potássio.
INDICAÇÕES
Hipertensão
HYZAAR® é indicado para o tratamento da hipertensão, para baixar a pressão arterial. A redução da pressão arterial reduz o risco de eventos cardiovasculares (CV) fatais e não fatais, principalmente derrames e infarto do miocárdio. Esses benefícios foram observados em estudos controlados de medicamentos anti-hipertensivos de uma ampla variedade de classes farmacológicas, incluindo losartana e hidroclorotiazida.
controle da hipertensão arterial deve fazer parte do gerenciamento abrangente do risco cardiovascular, incluindo, conforme apropriado, controle lipídico, controle do diabetes, terapia antitrombótica, cessação do tabagismo, exercícios e ingestão limitada de sódio. Muitos pacientes precisarão de mais de 1 medicamento para atingir as metas de pressão arterial. Para obter conselhos específicos sobre metas e gerenciamento, consulte as diretrizes publicadas, como as do Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC) do National High Blood Pressure Education Program.
Numerosos medicamentos anti-hipertensivos, de várias classes farmacológicas e com diferentes mecanismos de ação, têm demonstrado em ensaios clínicos randomizados reduzir a morbimortalidade cardiovascular, podendo-se concluir que é a redução da pressão arterial, e não alguma outra propriedade farmacológica do medicamento. os medicamentos, que é o grande responsável por esses benefícios. O maior e mais consistente benefício de resultado cardiovascular tem sido a redução do risco de acidente vascular cerebral, mas reduções no infarto do miocárdio e na mortalidade cardiovascular também foram observadas regularmente.
pressão sistólica ou diastólica elevada causa aumento do risco cardiovascular, e o aumento do risco absoluto por mmHg é maior em pressões sanguíneas mais altas, de modo que mesmo reduções modestas da hipertensão grave podem proporcionar benefícios substanciais. A redução do risco relativo da redução da pressão arterial é semelhante em populações com risco absoluto variável, portanto, o benefício absoluto é maior em pacientes que estão em maior risco independentemente de sua hipertensão (por exemplo, pacientes com diabetes ou hiperlipidemia), e esses pacientes seriam esperados beneficiar de um tratamento mais agressivo para uma meta de pressão arterial mais baixa.
Alguns medicamentos anti-hipertensivos têm efeitos menores na pressão arterial (como monoterapia) em pacientes negros, e muitos medicamentos anti-hipertensivos têm indicações e efeitos adicionais aprovados (por exemplo, na angina, insuficiência cardíaca ou doença renal diabética). Essas considerações podem orientar a seleção da terapia.
Esta combinação de dose fixa não é indicada para terapia inicial de hipertensão, exceto quando a hipertensão é grave o suficiente para que o valor de alcançar o controle imediato da pressão arterial exceda o risco de iniciar a terapia de combinação nesses pacientes [ver Estudos clínicos e DOSAGEM E ADMINISTRAÇÃO ].
HYZAAR pode ser administrado com outros agentes anti-hipertensivos.
Pacientes hipertensos com hipertrofia ventricular esquerda
HYZAAR é indicado para reduzir o risco de acidente vascular cerebral em pacientes com hipertensão e hipertrofia ventricular esquerda, mas há evidências de que esse benefício não se aplica a pacientes negros. [Ver Uso em populações específicas , FARMACOLOGIA CLÍNICA , e DOSAGEM E ADMINISTRAÇÃO .]
DOSAGEM E ADMINISTRAÇÃO
Hipertensão
A dose inicial usual de HYZAAR é 50/12,5 (losartana 50 mg/hidroclorotiazida 12,5 mg) uma vez ao dia. A dosagem pode ser aumentada após 3 semanas de terapia até um máximo de 100/25 (losartana 100 mg/hidroclorotiazida 25 mg) uma vez ao dia, conforme necessário para controlar a pressão arterial [ver Estudos clínicos ].
Inicie um paciente cuja pressão arterial não esteja adequadamente controlada com losart uma monoterapia de 50 mg com HYZAAR 50/12,5 uma vez ao dia. Se a pressão arterial permanecer descontrolada após cerca de 3 semanas de terapia, a dosagem pode ser aumentada para dois comprimidos de HYZAAR 50/12,5 uma vez ao dia ou um comprimido de HYZAAR 100/25 uma vez ao dia.
Iniciar um paciente cuja pressão arterial não esteja adequadamente controlada com losartana 100 mg em monoterapia com HYZAAR 100/12,5 (losartana 100 mg/hidroclorotiazida 12,5 mg) uma vez ao dia. Se a pressão arterial permanecer descontrolada após cerca de 3 semanas de terapia, aumente a dose para dois comprimidos de HYZAAR 50/12,5 uma vez ao dia ou um comprimido de HYZAAR 100/25 uma vez ao dia.
Iniciar um paciente cuja pressão arterial esteja inadequadamente controlada com hidroclorotiazida 25 mg uma vez ao dia, ou esteja controlada, mas que apresente hipocalemia com este regime, com HYZAAR 50/12,5 uma vez ao dia, reduzindo a dose de hidroclorotiazida sem reduzir a resposta anti-hipertensiva global esperada. Avalie a resposta clínica ao HYZAAR 50/12.5 e, se a pressão arterial permanecer descontrolada após cerca de 3 semanas de terapia, aumente a dose para dois comprimidos de HYZAAR 50/12.5 uma vez ao dia ou um comprimido de HYZAAR 100/25 uma vez ao dia.
Pacientes hipertensos com hipertrofia ventricular esquerda
Em pacientes cuja pressão arterial não é adequadamente controlada com 50 mg de losartana potássica, inicie o tratamento com HYZAAR 50/12.5. Se for necessária redução adicional da pressão arterial, aumente a dose para HYZAAR 100/12,5, seguido de HYZAAR 100/25. Para uma redução adicional da pressão arterial, adicione outros anti-hipertensivos [ver Estudos clínicos ].
COMO FORNECIDO
Formas de dosagem e pontos fortes
- HYZAAR 50/12.5 são comprimidos revestidos por película amarelos, ovais, com o código 717 numa das faces.
- HYZAAR 100/12.5 são comprimidos revestidos por película brancos, ovais, com o código 745 numa das faces.
- HYZAAR 100/25 são comprimidos revestidos por película, amarelo-claros, ovais, com o código 747 numa das faces.
Armazenamento e manuseio
HYZAAR é fornecido como um comprimido revestido por película.
Armazenar a 25°C (77°F); excursões permitidas para 15-30°C (59-86°F) [ver Temperatura ambiente controlada USP ]. Mantenha o recipiente bem fechado. Proteja da luz.
Fabricado para: Organon LLC, uma subsidiária da ORGANON & Co., Jersey City, NJ 07302, EUA. Revisado: junho de 2021
EFEITOS COLATERAIS
Experiência de Ensaios Clínicos
Como os ensaios clínicos são conduzidos em condições muito variadas, as taxas de reações adversas observadas nos ensaios clínicos de um medicamento não podem ser diretamente comparadas às taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática.
losartana potássica-hidroclorotiazida foi avaliada quanto à segurança em 858 pacientes tratados para hipertensão essencial e 3.889 pacientes tratados para hipertensão e hipertrofia ventricular esquerda. A maioria das reações adversas foram de natureza leve e transitória e não exigiram a descontinuação da terapia. Em ensaios clínicos controlados, a descontinuação da terapia devido a eventos adversos clínicos foi necessária em apenas 2,8% e 2,3% dos pacientes tratados com a combinação e placebo, respectivamente.
Nestes ensaios clínicos controlados em dupla ocultação, as reações adversas que ocorreram em mais de 2% dos indivíduos tratados com losartan-hidroclorotiazida e a uma taxa superior ao placebo foram: dor nas costas (2,1% vs 0,6%), tonturas (5,7% vs 2,9%) , e infecção do trato respiratório superior (6,1% vs 4,6%).
As seguintes reações adversas adicionais foram relatadas em estudos clínicos com HYZAAR e/ou os componentes individuais:
Distúrbios do sangue e do sistema linfático: Anemia, anemia aplástica, anemia hemolítica, leucopenia, agranulocitose.
Distúrbios do metabolismo e da nutrição: Anorexia, hiperglicemia, hiperuricemia, desequilíbrio eletrolítico incluindo hiponatremia e hipocalemia.
Distúrbios psiquiátricos: Insônia, inquietação.
Distúrbios do sistema nervoso: Disgeusia, cefaleia, enxaqueca, parestesias.
Distúrbios oculares: Xantopsia, visão turva transitória.
Distúrbios cardíacos: Palpitação, taquicardia.
Distúrbios vasculares: Efeitos ortostáticos relacionados com a dose, angeíte necrosante (vasculite, vasculite cutânea).
Distúrbios respiratórios, torácicos e mediastinais: Congestão nasal.
Problemas gastrointestinais: Dispepsia, dor abdominal, irritação gástrica, cólicas, náuseas, vômitos, pancreatite, sialoadenite.
Distúrbios hepatobiliares: Icterícia (icterícia colestática intra-hepática).
Distúrbios da pele e tecidos subcutâneos: Erupção cutânea, prurido, púrpura, necrólise epidérmica tóxica, urticária, fotossensibilidade, lúpus eritematoso cutâneo.
Distúrbios musculoesqueléticos e do tecido conjuntivo: Cãibras musculares, espasmo muscular.
Distúrbios renais e urinários: Glicosúria, disfunção renal, nefrite intersticial, insuficiência renal.
Distúrbios do sistema reprodutor e da mama: Disfunção erétil/impotência.
Distúrbios gerais e condições do local de administração: Dor no peito, mal-estar, fraqueza.
Investigações: Anormalidades da função hepática.
Tosse
tosse seca persistente tem sido associada ao uso de inibidores da ECA e, na prática, pode ser uma causa de descontinuação da terapia com inibidores da ECA. Dois estudos prospectivos, de grupos paralelos, duplo-cegos, randomizados e controlados foram conduzidos para avaliar os efeitos da losartana na incidência de tosse em pacientes hipertensos que apresentaram tosse durante o tratamento com inibidor da ECA. Os pacientes que apresentaram tosse típica do inibidor da ECA quando desafiados com lisinopril, cuja tosse desapareceu com placebo, foram randomizados para losartana 50 mg, lisinopril 20 mg ou placebo (um estudo, n=97) ou 25 mg de hidroclorotiazida (n=135). O período de tratamento duplo-cego durou até 8 semanas. A incidência de tosse é mostrada na Tabela 1 abaixo.
Esses estudos demonstram que a incidência de tosse associada à terapia com losartana, em uma população em que todos tiveram tosse associada à terapia com inibidor da ECA, é semelhante à associada à terapia com hidroclorotiazida ou placebo.
Casos de tosse, incluindo reexposição positiva, foram relatados com o uso de losartana na experiência pós-comercialização.
Experiência pós-marketing
As seguintes reações adversas foram identificadas durante o uso pós-aprovação de HYZAAR. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar sua frequência de forma confiável ou estabelecer uma relação causal com a exposição ao medicamento.
Digestivo: Hepatite foi relatada raramente em pacientes tratados com losartana.
Hematologico: Trombocitopenia.
Hipersensibilidade: Angioedema, incluindo inchaço da laringe e glote, causando obstrução das vias aéreas e/ou inchaço da face, lábios, faringe e/ou língua foi relatado raramente em pacientes tratados com losartana; alguns desses pacientes já apresentaram angioedema com outros medicamentos, incluindo inibidores da ECA. Vasculite, incluindo púrpura de Henoch-Schönlein, foi relatada com losartana. Reações anafiláticas foram relatadas.
Musculoesquelético: Rabdomiólise.
Pele: Eritrodermia.
Câncer de pele não melanoma: hidroclorotiazida está associada a um risco aumentado de câncer de pele não melanoma. Em um estudo realizado no Sentinel System, o risco aumentado foi predominantemente para carcinoma de células escamosas (CEC) e em pacientes brancos tomando grandes doses cumulativas. O risco aumentado para CEC na população geral foi de aproximadamente 1 caso adicional por 16.000 pacientes por ano, e para pacientes brancos tomando uma dose cumulativa ≥50.000mg o aumento do risco foi de aproximadamente 1 caso adicional de CEC para cada 6.700 pacientes por ano.
INTERAÇÕES MEDICAMENTOSAS
Agentes que aumentam o potássio sérico
A coadministração de losartana com outros medicamentos que elevam os níveis séricos de potássio pode resultar em hipercalemia. Monitorar o potássio sérico nesses pacientes.
Lítio
Aumentos nas concentrações séricas de lítio e toxicidade do lítio foram relatados com o uso concomitante de antagonistas dos receptores da angiotensina II ou diuréticos tiazídicos. Monitore os níveis de lítio em pacientes recebendo 12,5 mg de HYZAAR e lítio.
Agentes anti-inflamatórios não esteroides, incluindo inibidores seletivos da ciclooxigenase-2
Losartana Potássica
Em pacientes idosos, com depleção de volume (incluindo aqueles em terapia diurética) ou com função renal comprometida, a coadministração de AINEs, incluindo inibidores seletivos da COX-2, com antagonistas dos receptores da angiotensina II (incluindo losartana) pode resultar em deterioração da função renal, incluindo possível insuficiência renal aguda. Estes efeitos são geralmente reversíveis. Monitorar a função renal periodicamente em pacientes recebendo terapia com losartana e AINEs.
O efeito anti-hipertensivo dos antagonistas dos receptores da angiotensina II, incluindo losartana, pode ser atenuado por AINEs, incluindo inibidores seletivos de COX-2.
Hidroclorotiazida
A administração de um agente anti-inflamatório não esteroidal, incluindo um inibidor seletivo da COX-2, pode reduzir os efeitos diuréticos, natriuréticos e anti-hipertensivos dos diuréticos de alça, poupadores de potássio e tiazídicos. Portanto, quando HYZAAR e agentes anti-inflamatórios não esteroides, incluindo inibidores seletivos de COX-2, são usados concomitantemente, observe atentamente para determinar se o efeito desejado do diurético é obtido.
Em pacientes recebendo terapia diurética, a coadministração de AINEs com bloqueadores dos receptores da angiotensina, incluindo losartana, pode resultar em deterioração da função renal, incluindo possível insuficiência renal aguda. Estes efeitos são geralmente reversíveis. Monitorar a função renal periodicamente em pacientes recebendo terapia com hidroclorotiazida, losartana e AINEs.
Duplo bloqueio do sistema renina-angiotensina (RAS)
O bloqueio duplo do SRA com bloqueadores dos receptores da angiotensina, inibidores da ECA ou alisquireno está associado a riscos aumentados de hipotensão, síncope, hipercalemia e alterações na função renal (incluindo insuficiência renal aguda) em comparação com a monoterapia.
estudo Veterans Affairs Nephropathy in Diabetes (VA NEPHRON-D) recrutou 1.448 pacientes com diabetes tipo 2, razão albumina-creatinina elevada e diminuição da taxa de filtração glomerular estimada (TFG 30 a 89,9 mL/min), randomizando-os para lisinopril ou placebo em um histórico de terapia com losartana e os acompanhou por uma média de 2,2 anos. Os pacientes que receberam a combinação de losartana e lisinopril não obtiveram nenhum benefício adicional em comparação com a monoterapia para o desfecho combinado de declínio da TFG, doença renal em estágio final ou morte, mas experimentaram um aumento da incidência de hipercalemia e lesão renal aguda em comparação com a monoterapia grupo.
Monitore de perto a pressão arterial, função renal e eletrólitos em pacientes em uso de HYZAAR 12,5 mg e outros agentes que afetam o RAS.
Não coadministre alisquireno com HYZAAR 12,5mg em pacientes com diabetes. Evite o uso de alisquireno com HYZAAR 12,5mg em pacientes com insuficiência renal (TFG
uso de hidroclorotiazida com outras drogas
Quando administrados concomitantemente, os seguintes medicamentos podem interagir com os diuréticos tiazídicos [ver FARMACOLOGIA CLÍNICA ]:
Medicamentos antidiabéticos (agentes orais e insulina) - pode ser necessário ajuste da dose do medicamento antidiabético.
Resinas de colestiramina e colestipol - A absorção de hidroclorotiazida é prejudicada na presença de resinas de troca aniônica. Doses únicas de resinas de colestiramina ou colestipol ligam a hidroclorotiazida e reduzem sua absorção no trato gastrointestinal em até 85 e 43 por cento, respectivamente.
Escalonar a dosagem de hidroclorotiazida e da resina de modo que a hidroclorotiazida seja administrada pelo menos 4 horas antes ou 4 a 6 horas após a administração da resina.
AVISOS
Incluído como parte do "PRECAUÇÕES" Seção
PRECAUÇÕES
Toxicidade Fetal
uso de drogas que atuam no sistema renina-angiotensina durante o segundo e terceiro trimestres de gestação reduz a função renal fetal e aumenta a morbidade e morte fetal e neonatal. O oligoidrâmnio resultante pode estar associado a hipoplasia pulmonar fetal e deformações esqueléticas. Os potenciais efeitos adversos neonatais incluem hipoplasia do crânio, anúria, hipotensão, insuficiência renal e morte. Quando a gravidez for detectada, descontinue HYZAAR 12,5mg o mais rápido possível.
As tiazidas atravessam a barreira placentária e aparecem no sangue do cordão umbilical. As reações adversas incluem icterícia fetal ou neonatal, trombocitopenia [ver Uso em populações específicas ].
Hipotensão em pacientes com depleção de volume ou sal
Em pacientes com um sistema renina-angiotensina ativado, como pacientes com depleção de volume ou sal (por exemplo, aqueles que estão sendo tratados com altas doses de diuréticos), pode ocorrer hipotensão sintomática após o início do tratamento com HYZAAR. Corrija a depleção de volume ou sal antes da administração de HYZAAR. Não use HYZAAR como terapia inicial em pacientes com depleção de volume intravascular.
Função Renal Prejudicada
Alterações na função renal, incluindo insuficiência renal aguda, podem ser causadas por drogas que inibem o sistema reninangiotensina e por diuréticos. Pacientes cuja função renal pode depender em parte da atividade do sistema renina-angiotensina (p. HYZAAR. Monitore a função renal periodicamente nesses pacientes. Considere suspender ou descontinuar a terapia em pacientes que desenvolvem uma diminuição clinicamente significativa da função renal com HYZAAR [ver INTERAÇÕES MEDICAMENTOSAS e Uso em populações específicas ].
Hipersensibilidade
As reações de hipersensibilidade à hidroclorotiazida podem ocorrer em pacientes com ou sem histórico de alergia ou asma brônquica, mas são mais prováveis em pacientes com esse histórico.
Efeitos eletrolíticos e metabólicos
Em ensaios clínicos duplo-cegos de várias doses de losartana potássica e hidroclorotiazida, a incidência de pacientes hipertensos que desenvolveram hipocalemia (potássio sérico 5,7 mEq/L) foi de 0,4% versus 0% para placebo.
HYZAAR contém hidroclorotiazida que pode causar hipocalemia, hiponatremia e hipomagnesemia. A hipomagnesemia pode resultar em hipocalemia que pode ser difícil de tratar apesar da reposição de potássio. HYZAAR 12,5mg também contém losartana, que pode causar hipercalemia. Monitore os eletrólitos séricos periodicamente [ver INTERAÇÕES MEDICAMENTOSAS ].
O uso concomitante de outros medicamentos que podem aumentar o potássio sérico pode levar à hipercalemia [ver INTERAÇÕES MEDICAMENTOSAS ].
A hidroclorotiazida pode alterar a tolerância à glicose e aumentar os níveis séricos de colesterol e triglicerídeos.
Hiperuricemia pode ocorrer ou gota franca pode ser precipitada em pacientes recebendo terapia com tiazida. Como o losartan diminui o ácido úrico, o losartan em combinação com a hidroclorotiazida atenua a hiperuricemia induzida por diuréticos.
hidroclorotiazida diminui a excreção urinária de cálcio e pode causar elevações do cálcio sérico. Monitorar os níveis de cálcio.
Miopia aguda e glaucoma secundário de ângulo fechado
A hidroclorotiazida, uma sulfonamida, pode causar uma reação idiossincrática, resultando em miopia transitória aguda e glaucoma agudo de ângulo fechado. Os sintomas incluem início agudo de diminuição da acuidade visual ou dor ocular e geralmente ocorrem dentro de horas a semanas após o início da droga. O glaucoma agudo de ângulo fechado não tratado pode levar à perda permanente da visão. O tratamento primário é descontinuar a hidroclorotiazida o mais rápido possível. Tratamentos médicos ou cirúrgicos imediatos podem precisar ser considerados se a pressão intraocular permanecer descontrolada. Os fatores de risco para o desenvolvimento de glaucoma agudo de ângulo fechado podem incluir história de alergia à sulfonamida ou à penicilina.
Lúpus Eritematoso Sistêmico
Diuréticos tiazídicos podem causar exacerbação ou ativação do lúpus eritematoso sistêmico.
Pacientes pós-simpatectomia
Os efeitos anti-hipertensivos da droga podem ser aumentados no paciente pós-simpatectomia.
Informações de Aconselhamento do Paciente
Aconselhe o paciente a ler o rótulo do paciente aprovado pela FDA ( INFORMAÇÃO DO PACIENTE ).
Gravidez
Aconselhe as pacientes do sexo feminino em idade fértil sobre as consequências da exposição a HYZAAR 12,5mg durante a gravidez. Discuta as opções de tratamento com as mulheres que planejam engravidar. Diga às pacientes para relatar a gravidez a seus médicos o mais rápido possível [ver AVISOS E PRECAUÇÕES e Uso em populações específicas ].

Hipotensão sintomática
Aconselhe os pacientes que tonturas podem ocorrer, especialmente durante os primeiros dias de terapia, e informe esse sintoma a um profissional de saúde. Informe os pacientes que a desidratação por ingestão inadequada de líquidos, transpiração excessiva, vômitos ou diarreia pode levar a uma queda excessiva da pressão arterial. Se ocorrer síncope, aconselhe os pacientes a entrar em contato com seu médico [ver AVISOS E PRECAUÇÕES ].
Suplementos de potássio
Aconselhar os pacientes a não usar suplementos de potássio ou substitutos do sal contendo potássio sem consultar seu médico [ver INTERAÇÕES MEDICAMENTOSAS ].
Miopia aguda e glaucoma secundário de ângulo fechado
Aconselhe os pacientes a descontinuar HYZAAR 12,5 mg e procurar atendimento médico imediato se apresentarem sintomas de miopia aguda ou glaucoma secundário de ângulo fechado [ver AVISOS E PRECAUÇÕES ].
Toxicologia não clínica
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
Losartan Potássio-Hidroclorotiazida
Não foram realizados estudos de carcinogenicidade com a combinação losartana potássica-hidroclorotiazida.
A losartana potássica-hidroclorotiazida, quando testada na proporção de peso de 4:1, foi negativa no ensaio de mutagênese microbiana de Ames e no ensaio de mutagênese em células pulmonares de hamster chinês V-79. Além disso, não houve evidência de genotoxicidade direta no ensaio de eluição alcalina in vitro em hepatócitos de ratos e no ensaio de aberração cromossômica in vitro em células de ovário de hamster chinês em concentrações não citotóxicas.
losartana potássica, coadministrada com hidroclorotiazida, não teve efeito sobre a fertilidade ou comportamento de acasalamento de ratos machos em doses de até 135 mg/kg/dia de losartana e 33,75 mg/kg/dia de hidroclorotiazida. Essas dosagens demonstraram fornecer as respectivas exposições sistêmicas (AUCs) para losartana, seu metabólito ativo e hidroclorotiazida que são aproximadamente 60, 60 e 30 vezes maiores do que aquelas alcançadas em humanos com 100 mg de losartana potássica em combinação com 25 mg de hidroclorotiazida. Em ratas, entretanto, a coadministração de doses tão baixas quanto 10 mg/kg/dia de losartana e 2,5 mg/kg/dia de hidroclorotiazida foi associada a reduções leves, mas estatisticamente significativas, nos índices de fecundidade e fertilidade. Os valores de AUC para losartana, seu metabólito ativo e hidroclorotiazida, extrapolados de dados obtidos com losartana administrada a ratos na dose de 50 mg/kg/dia em combinação com 12,5 mg/kg/dia de hidroclorotiazida, foram aproximadamente 6, 2 e 2 vezes maiores do que as alcançadas em humanos com 100 mg de losartana em combinação com 25 mg de hidroclorotiazida.
Losartana Potássica
losartana potássica não foi carcinogênica quando administrada em doses máximas toleradas a ratos e camundongos por 105 e 92 semanas, respectivamente. Ratas fêmeas que receberam a dose mais alta (270 mg/kg/dia) tiveram uma incidência ligeiramente maior de adenoma acinar pancreático. As dosagens máximas toleradas (270 mg/kg/dia em ratos, 200 mg/kg/dia em camundongos) forneceram exposições sistêmicas para losartana e seu metabólito farmacologicamente ativo que foram aproximadamente 160 e 90 vezes (ratos) e 30 e 15 vezes (camundongos). ) a exposição de um ser humano de 50 kg que recebeu 100 mg por dia.
A losartana potássica foi negativa nos ensaios de mutagênese microbiana e mutagênese em células de mamíferos V-79 e na eluição alcalina in vitro e nos ensaios de aberração cromossômica in vitro e in vivo. Além disso, o metabólito ativo não mostrou evidência de genotoxicidade na mutagênese microbiana, eluição alcalina in vitro e ensaios de aberração cromossômica in vitro.
fertilidade e o desempenho reprodutivo não foram afetados em estudos com ratos machos que receberam doses orais de losartana potássica até aproximadamente 150 mg/kg/dia. A administração de doses tóxicas em fêmeas (300/200 mg/kg/dia) foi associada a uma diminuição significativa (p
Hidroclorotiazida
Estudos de alimentação de dois anos em camundongos e ratos conduzidos sob os auspícios do Programa Nacional de Toxicologia (NTP) não revelaram evidência de potencial carcinogênico da hidroclorotiazida em camundongos fêmeas (em doses de até aproximadamente 600 mg/kg/dia) ou em machos e ratos fêmeas (em doses até aproximadamente 100 mg/kg/dia). O NTP, no entanto, encontrou evidências ambíguas de hepatocarcinogenicidade em camundongos machos.
hidroclorotiazida não foi genotóxica in vitro no ensaio de mutagenicidade de Ames das cepas de Salmonella typhimurium TA 98, TA 100, TA 1535, TA 1537 e TA 1538 e no teste de ovário de hamster chinês (CHO) para aberrações cromossômicas, ou in vivo em ensaios usando cromossomos de células germinais de camundongos, cromossomos de medula óssea de hamster chinês e o gene recessivo de traço letal ligado ao sexo de Drosophila. Os resultados positivos dos testes foram obtidos apenas nos ensaios in vitro CHO Sister Chromatid Exchange (clastogenicidade) e nos ensaios de células de linfoma de camundongo (mutagenicidade), usando concentrações de hidroclorotiazida de 43 a 1300 mcg/mL, e no ensaio de não disjunção de Aspergillus nidulans em uma concentração não especificada.
A hidroclorotiazida não teve efeitos adversos na fertilidade de camundongos e ratos de ambos os sexos em estudos em que essas espécies foram expostas, por meio de sua dieta, a doses de até 100 e 4 mg/kg, respectivamente, antes do acasalamento e durante a gestação.
Uso em populações específicas
Gravidez
Gravidez Categoria D
uso de drogas que atuam no sistema renina-angiotensina durante o segundo e terceiro trimestres de gestação reduz a função renal fetal e aumenta a morbidade e morte fetal e neonatal. O oligoidrâmnio resultante pode estar associado a hipoplasia pulmonar fetal e deformações esqueléticas. Os potenciais efeitos adversos neonatais incluem hipoplasia do crânio, anúria, hipotensão, insuficiência renal e morte. Quando a gravidez for detectada, interrompa a losartana o mais rápido possível. Esses desfechos adversos geralmente estão associados ao uso desses medicamentos no segundo e terceiro trimestre da gravidez. A maioria dos estudos epidemiológicos examinando anormalidades fetais após exposição ao uso de anti-hipertensivos no primeiro trimestre não distinguiu drogas que afetam o sistema renina-angiotensina de outros agentes anti-hipertensivos. O manejo adequado da hipertensão materna durante a gravidez é importante para otimizar os resultados tanto para a mãe quanto para o feto.
No caso incomum de não haver alternativa adequada à terapia com drogas que afetem o sistema reninaangiotensina para um paciente em particular, informar a mãe sobre o risco potencial para o feto. Realizar exames ultrassonográficos seriados para avaliar o ambiente intra-amniótico. Se for observado oligoidrâmnio, descontinuar HYZAAR, a menos que seja considerado salva-vidas para a mãe. O teste fetal pode ser apropriado, com base na semana de gravidez. Pacientes e médicos devem estar cientes, entretanto, de que o oligoidrâmnio pode não aparecer até que o feto tenha sofrido lesão irreversível. Observar de perto bebês com história de exposição in utero a HYZAAR 12,5 mg para hipotensão, oligúria e hipercalemia [ver Uso Pediátrico ].
Não houve evidência de teratogenicidade em ratos ou coelhos tratados com uma dose máxima de losartana potássica de 10 mg/kg/dia em combinação com 2,5 mg/kg/dia de hidroclorotiazida. Nessas dosagens, as respectivas exposições (AUCs) de losartana, seu metabólito ativo e hidroclorotiazida em coelhos foram aproximadamente 5, 1,5 e 1,0 vezes aquelas alcançadas em humanos com 100 mg de losartana em combinação com 25 mg de hidroclorotiazida. Os valores de AUC para losartana, seu metabólito ativo e hidroclorotiazida, extrapolados de dados obtidos com losartana administrada a ratos na dose de 50 mg/kg/dia em combinação com 12,5 mg/kg/dia de hidroclorotiazida, foram aproximadamente 6, 2 e 2 vezes maiores do que as alcançadas em humanos com 100 mg de losartana em combinação com 25 mg de hidroclorotiazida. A toxicidade fetal em ratos, evidenciada por um ligeiro aumento nas costelas supranumerárias, foi observada quando as fêmeas foram tratadas antes e durante a gestação com 10 mg/kg/dia de losartana em combinação com 2,5 mg/kg/dia de hidroclorotiazida. Como também observado em estudos com losartana isoladamente, efeitos adversos fetais e neonatais, incluindo diminuição do peso corporal, toxicidade renal e mortalidade, ocorreram quando ratas grávidas foram tratadas durante o final da gestação e/ou lactação com 50 mg/kg/dia de losartana em combinação com 12,5 mg/kg/dia de hidroclorotiazida. As respectivas AUCs para losartana, seu metabólito ativo e hidroclorotiazida nessas dosagens em ratos foram aproximadamente 35, 10 e 10 vezes maiores do que aquelas alcançadas em humanos com a administração de 100 mg de losartana em combinação com 25 mg de hidroclorotiazida. Quando a hidroclorotiazida foi administrada sem losartana a camundongos e ratas grávidas durante seus respectivos períodos de organogênese principal, em doses de até 3.000 e 1.000 mg/kg/dia, respectivamente, não houve evidência de dano ao feto.
As tiazidas atravessam a barreira placentária e aparecem no sangue do cordão umbilical. Existe o risco de icterícia fetal ou neonatal, trombocitopenia e possivelmente outras reações adversas que ocorreram em adultos.
Mães que amamentam
Não se sabe se a losartana é excretada no leite humano, mas níveis significativos de losartana e seu metabólito ativo mostraram-se presentes no leite de rato. As tiazidas aparecem no leite humano. Devido ao potencial de efeitos adversos no lactente, deve-se decidir entre descontinuar a amamentação ou descontinuar o medicamento, levando em consideração a importância do medicamento para a mãe.
Uso Pediátrico
A segurança e eficácia de HYZAAR em pacientes pediátricos não foram estabelecidas.
Recém-nascidos com histórico de exposição in utero ao HYZAAR
Se ocorrer oligúria ou hipotensão, dirigir a atenção para o suporte da pressão arterial e perfusão renal. A exsanguineotransfusão ou diálise pode ser necessária como meio de reverter a hipotensão e/ou substituir a função renal desordenada.
Uso Geriátrico
Em um estudo clínico controlado para a redução do risco combinado de morte cardiovascular, acidente vascular cerebral e infarto do miocárdio em pacientes hipertensos com hipertrofia ventricular esquerda, 2.857 pacientes (62%) tinham 65 anos ou mais, enquanto 808 pacientes (18%) tinham 75 anos e acabou. Em um esforço para controlar a pressão arterial neste estudo, os pacientes foram coadministrados com losartana e hidroclorotiazida 74% do tempo total em que estiveram no medicamento do estudo. Não foram observadas diferenças globais na eficácia entre estes doentes e os doentes mais jovens. Os eventos adversos foram um pouco mais frequentes em idosos do que em pacientes não idosos tanto para o grupo losartana-hidroclorotiazida quanto para o grupo controle [ver FARMACOLOGIA CLÍNICA ].
Corrida
No estudo Losartan Intervention For Endpoint redução na hipertensão (LIFE), pacientes negros com hipertensão e hipertrofia ventricular esquerda tratados com atenolol apresentaram menor risco de acidente vascular cerebral, o desfecho composto primário, em comparação com pacientes negros tratados com losartana (ambos co-tratados com hidroclorotiazida na maioria dos pacientes). No subgrupo de pacientes negros (n=533, 6% dos pacientes do estudo LIFE), houve 29 desfechos primários entre 263 pacientes em uso de atenolol (11%, 26 por 1.000 pacientes-ano) e 46 desfechos primários entre 270 pacientes (17 %, 42 por 1.000 pacientes-ano) com losartana. Este achado não pode ser explicado com base em diferenças nas populações além da raça ou em quaisquer desequilíbrios entre os grupos de tratamento. Além disso, as reduções da pressão arterial em ambos os grupos de tratamento foram consistentes entre pacientes negros e não negros. Dada a dificuldade em interpretar diferenças de subconjuntos em grandes ensaios, não se pode saber se a diferença observada é resultado do acaso. No entanto, o estudo LIFE não fornece evidências de que os benefícios da losartana na redução do risco de eventos cardiovasculares em pacientes hipertensos com hipertrofia ventricular esquerda se apliquem a pacientes negros [ver FARMACOLOGIA CLÍNICA ].
Insuficiência hepática
início de 12,5 mg de HYZAAR não é recomendado para pacientes com insuficiência hepática porque a dose inicial apropriada de losartana, 25 mg, não está disponível.
Insuficiência renal
Alterações na função renal foram relatadas em indivíduos suscetíveis [ver DOSAGEM E ADMINISTRAÇÃO , AVISOS E PRECAUÇÕES , e FARMACOLOGIA CLÍNICA ]. A segurança e eficácia de HYZAAR em pacientes com insuficiência renal grave (clearance de creatinina
SOBREDOSAGEM
Losartana Potássica
Foi observada letalidade significativa em camundongos e ratos após administração oral de 1.000 mg/kg e 2.000 mg/kg, respectivamente, cerca de 44 e 170 vezes a dose humana máxima recomendada em uma base de mg/m.
Dados limitados estão disponíveis em relação à superdosagem em humanos. A manifestação mais provável de superdosagem seria hipotensão e taquicardia; bradicardia pode ocorrer por estimulação parassimpática (vagal). Se ocorrer hipotensão sintomática, deve ser instituído tratamento de suporte.
Nem a losartana nem seu metabólito ativo podem ser removidos por hemodiálise.
Hidroclorotiazida
LD oral da hidroclorotiazida é superior a 10 g/kg em camundongos e ratos. Os sinais e sintomas mais comuns observados são aqueles causados por depleção eletrolítica (hipocalemia, hipocloremia, hiponatremia) e desidratação por diurese excessiva. Se digitálicos também foram administrados, a hipocalemia pode acentuar as arritmias cardíacas. O grau de remoção da hidroclorotiazida por hemodiálise não foi estabelecido.
CONTRA-INDICAÇÕES
HYZAAR 12,5mg é contraindicado:
- Em pacientes com hipersensibilidade a qualquer componente deste produto.
- Em pacientes com anúria
- Para coadministração com alisquireno em pacientes com diabetes
FARMACOLOGIA CLÍNICA
Mecanismo de ação
Losartana Potássica
angiotensina II [formada a partir da angiotensina I em uma reação catalisada pela enzima conversora da angiotensina (ECA, cininase II)], é um potente vasoconstritor, o hormônio vasoativo primário do sistema renina-angiotensina e um importante componente na fisiopatologia da hipertensão. Também estimula a secreção de aldosterona pelo córtex adrenal. A losartana e seu principal metabólito ativo bloqueiam os efeitos vasoconstritores e secretores de aldosterona da angiotensina II bloqueando seletivamente a ligação da angiotensina II ao receptor AT1 encontrado em muitos tecidos (p. ex., músculo liso vascular, glândula adrenal). Há também um receptor AT2 encontrado em muitos tecidos, mas não se sabe que esteja associado à homeostase cardiovascular. Nem a losartana nem seu principal metabólito ativo exibem qualquer atividade agonista parcial no receptor AT1, e ambos têm afinidade muito maior (cerca de 1.000 vezes) para o receptor AT1 do que para o receptor AT2. Estudos de ligação in vitro indicam que a losartana é um inibidor competitivo e reversível do receptor AT1. O metabólito ativo é 10 a 40 vezes mais potente em peso do que a losartana e parece ser um inibidor reversível e não competitivo do receptor AT1.
Nem a losartana nem seu metabólito ativo inibem a ECA (cininase II, a enzima que converte a angiotensina I em angiotensina II e degrada a bradicinina), nem se ligam ou bloqueiam outros receptores hormonais ou canais iônicos conhecidos por serem importantes na regulação cardiovascular.
Hidroclorotiazida
hidroclorotiazida é um diurético tiazídico. As tiazidas afetam os mecanismos tubulares renais de reabsorção de eletrólitos, aumentando diretamente a excreção de sódio e cloreto em quantidades aproximadamente equivalentes. Indiretamente, a ação diurética da hidroclorotiazida reduz o volume plasmático, com conseqüente aumento da renina renina plasmática, aumento da secreção de aldosterona, aumento da perda urinária de potássio e diminuição do potássio sérico. A ligação renina-aldosterona é mediada pela angiotensina II, de modo que a coadministração de um antagonista do receptor da angiotensina II tende a reverter a perda de potássio associada a esses diuréticos. O mecanismo do efeito anti-hipertensivo das tiazidas é desconhecido.
Farmacodinâmica
Losartana Potássica
losartana inibe o efeito pressor de infusões de angiotensina II (assim como de angiotensina I). Uma dose de 100 mg inibe o efeito pressor em cerca de 85% no pico com 25-40% de inibição persistindo por 24 horas. A remoção do feedback negativo da angiotensina II causa uma duplicação ou triplicação da atividade da renina plasmática e conseqüente aumento na concentração plasmática de angiotensina II em pacientes hipertensos. A losartana não afeta a resposta à bradicinina, enquanto os inibidores da ECA aumentam a resposta à bradicinina. As concentrações plasmáticas de aldosterona caem após a administração de losartana. Apesar do efeito do losartan na secreção de aldosterona, foi observado muito pouco efeito no potássio sérico.
efeito da losartana está substancialmente presente em uma semana, mas em alguns estudos o efeito máximo ocorreu em 3-6 semanas. Em estudos de acompanhamento de longo prazo (com controle de outplacebo), o efeito da losartana pareceu ser mantido por até um ano. Não há efeito rebote aparente após a retirada abrupta de losartana. Não houve essencialmente nenhuma alteração na frequência cardíaca média em pacientes tratados com losartana em estudos controlados.
Hidroclorotiazida
Após a administração oral de hidroclorotiazida, a diurese começa em 2 horas, atinge o pico em cerca de 4 horas e dura cerca de 6 a 12 horas.
Interações medicamentosas
Hidroclorotiazida
Álcool, barbitúricos ou narcóticos - pode ocorrer potenciação da hipotensão ortostática.
Outros medicamentos anti-hipertensivos - efeito aditivo ou potenciação.
Relaxantes do músculo esquelético, não despolarizantes (por exemplo, tubocurarina) - possível aumento da responsividade ao relaxante muscular.
Corticosteróides, ACTH ou glicirrizina (encontrado no alcaçuz) - depleção eletrolítica intensificada, particularmente hipocalemia.
Aminas pressoras (por exemplo, norepinefrina) - possível resposta diminuída às aminas pressoras, mas não suficiente para impedir seu uso.
Farmacocinética
Losartana Potássica
Absorção
Após administração oral, a losartana é bem absorvida e sofre substancial metabolismo de primeira passagem. A biodisponibilidade sistêmica da losartana é de aproximadamente 33%. As concentrações máximas médias de losartana e seu metabólito ativo são atingidas em 1 hora e em 3-4 horas, respectivamente. Embora as concentrações plasmáticas máximas de losartana e de seu metabólito ativo sejam aproximadamente iguais, a AUC (área sob a curva) do metabólito é cerca de 4 vezes maior que a de losartana. Uma refeição retarda a absorção de losartana e diminui sua Cmax, mas tem apenas efeitos menores na AUC de losartana ou na AUC do metabólito (diminuição de ~10%). A farmacocinética do losartan e do seu metabolito ativo é linear com doses orais de losartan até 200 mg e não se altera ao longo do tempo.
Distribuição
volume de distribuição da losartana e do metabólito ativo é de cerca de 34 litros e 12 litros, respectivamente. Tanto a losartana quanto seu metabólito ativo estão altamente ligados às proteínas plasmáticas, principalmente a albumina, com frações plasmáticas livres de 1,3% e 0,2%, respectivamente. A ligação às proteínas plasmáticas é constante ao longo do intervalo de concentração alcançado com as doses recomendadas. Estudos em ratos indicam que o losartan atravessa mal a barreira hematoencefálica, se é que o atravessa.
Metabolismo
losartana é um agente oralmente ativo que sofre substancial metabolismo de primeira passagem pelas enzimas do citocromo P450. É convertido, em parte, em um metabólito ativo de ácido carboxílico que é responsável pela maior parte do antagonismo do receptor de angiotensina II que segue o tratamento com losartana. Cerca de 14% de uma dose de losartana administrada por via oral é convertida no metabólito ativo. Além do metabólito ativo do ácido carboxílico, vários metabólitos inativos são formados. Estudos in vitro indicam que o citocromo P450 2C9 e 3A4 estão envolvidos na biotransformação do losartan em seus metabólitos.
Eliminação
depuração plasmática total de losartana e do metabólito ativo é de cerca de 600 mL/min e 50 mL/min, respectivamente, com depuração renal de cerca de 75 mL/min e 25 mL/min, respectivamente. A meia-vida terminal do losartan é de cerca de 2 horas e do metabólito é de cerca de 6-9 horas. Após administração oral de doses únicas de losartana, cerca de 4% da dose é excretada inalterada na urina e cerca de 6% é excretada na urina como metabólito ativo. A excreção biliar contribui para a eliminação da losartana e seus metabólitos. Após losartana marcada com 14C oral, cerca de 35% da radioatividade é recuperada na urina e cerca de 60% nas fezes. Após uma dose intravenosa de losartana marcada com 14C, cerca de 45% da radioatividade é recuperada na urina e 50% nas fezes. Nem o losartan nem o seu metabolito acumulam-se no plasma com doses repetidas uma vez por dia.
Hidroclorotiazida
hidroclorotiazida não é metabolizada, mas é rapidamente eliminada pelo rim. Quando os níveis plasmáticos foram acompanhados por pelo menos 24 horas, observou-se que a meia-vida plasmática variou entre 5,6 e 14,8 horas. Pelo menos 61 por cento da dose oral é eliminada inalterada em 24 horas. A hidroclorotiazida atravessa a barreira placentária, mas não a barreira hematoencefálica e é excretada no leite materno.
Populações Específicas
Geriatria e Gênero
A farmacocinética da losartana tem sido investigada em idosos (65-75 anos) e em ambos os sexos. As concentrações plasmáticas de losartana e seu metabólito ativo são semelhantes em idosos e hipertensos jovens. As concentrações plasmáticas de losartana foram cerca de duas vezes maiores em hipertensos do sexo feminino do que nos hipertensos do sexo masculino, mas as concentrações do metabólito ativo foram semelhantes em homens e mulheres.
Corrida
As diferenças farmacocinéticas devido à raça não foram estudadas [ver também Uso em populações específicas ].
Insuficiência Hepática
Após administração oral em pacientes com cirrose hepática alcoólica leve a moderada, as concentrações plasmáticas de losartana e seu metabólito ativo foram, respectivamente, 5 vezes e cerca de 1,7 vezes maiores que em voluntários jovens do sexo masculino. Em comparação com indivíduos normais, a depuração plasmática total de losartana em pacientes com insuficiência hepática foi cerca de 50% menor, e a biodisponibilidade oral foi aproximadamente o dobro. A dose inicial mais baixa de losartana recomendada para uso em pacientes com insuficiência hepática não pode ser administrada com HYZAAR. Seu uso em tais pacientes como meio de titulação de losartana não é, portanto, recomendado [ver AVISOS E PRECAUÇÕES e Uso em populações específicas ].
Insuficiência renal
Losartana
Após administração oral, as concentrações plasmáticas e AUCs de losartana e seu metabólito ativo aumentam em 50-90% em pacientes com insuficiência renal leve (depuração de creatinina de 50 a 74 mL/min) ou moderada (depuração de creatinina de 30 a 49 mL/min). Neste estudo, a depuração renal foi reduzida em 55-85% tanto para losartana quanto para seu metabólito ativo em pacientes com insuficiência renal leve ou moderada. Nem a losartana nem seu metabólito ativo podem ser removidos por hemodiálise.
Hidroclorotiazida
Após a administração oral, a AUC da hidroclorotiazida é aumentada em 70 e 700% para pacientes com insuficiência renal leve e moderada, respectivamente. Neste estudo, a depuração renal da hidroclorotiazida diminuiu em 45 e 85% em pacientes com insuficiência renal leve e moderada, respectivamente.
Use os regimes usuais de terapia com HYZAAR desde que a depuração de creatinina do paciente seja maior que 30 mL/min. A segurança e a eficácia de HYZAAR 12,5 mg em pacientes com insuficiência renal grave (clearance de creatinina inferior a 30 mL/min) não foram estabelecidas [ver Uso em populações específicas ].
Interações medicamentosas
Losartana Potássica
Não foram encontradas interações medicamentosas clinicamente significativas em estudos de losartana potássica com hidroclorotiazida, digoxina, varfarina, cimetidina e fenobarbital. No entanto, a rifampicina demonstrou diminuir a AUC de losartana e seu metabólito ativo em 30% e 40%, respectivamente. O fluconazol, um inibidor do citocromoP450 2C9, diminuiu a AUC do metabólito ativo em aproximadamente 40%, mas aumentou a AUC de losartana em aproximadamente 70% após doses múltiplas. A conversão de losartana em seu metabólito ativo após administração intravenosa não é afetada pelo cetoconazol, um inibidor de P450 3A4. A AUC do metabólito ativo após losartana oral não foi afetada pela eritromicina, um inibidor de P450 3A4, mas a AUC de losartana foi aumentada por 30%.
As consequências farmacodinâmicas do uso concomitante de losartana e inibidores de P450 2C9 não foram examinadas. Indivíduos que não metabolizam losartana em metabólito ativo demonstraram ter um defeito específico e raro no citocromo P450 2C9. Esses dados sugerem que a conversão de losartana em seu metabólito ativo é mediada principalmente por P450 2C9 e não por P450 3A4.
Estudos clínicos
Monoterapia com Losartana
Redução do risco de acidente vascular cerebral
estudo LIFE foi um estudo multinacional, duplo-cego, comparando losartana e atenolol em 9.193 pacientes hipertensos com hipertrofia ventricular esquerda documentada por ECG. Pacientes com infarto do miocárdio ou acidente vascular cerebral nos seis meses anteriores à randomização foram excluídos. Os pacientes foram randomizados para receber losartana 50 mg ou atenolol 50 mg uma vez ao dia. Se a meta de pressão arterial (
Nos esforços para controlar a pressão arterial, os pacientes em ambos os braços do estudo LIFE foram coadministrados com hidroclorotiazida na maior parte do tempo em que estiveram no medicamento do estudo (73,9% e 72,4% dos dias nos braços de losartana e atenolol, respectivamente).
Dos pacientes randomizados, 4.963 (54%) eram do sexo feminino e 533 (6%) eram negros. A idade média foi de 67 anos com 5704 (62%) idade ≥65. No início do estudo, 1.195 (13%) tinham diabetes, 1.326 (14%) tinham hipertensão sistólica isolada, 1.469 (16%) tinham doença coronariana e 728 (8%) tinham doença cerebrovascular. A pressão arterial média basal foi de 174/98 mmHg em ambos os grupos de tratamento. O tempo médio de seguimento foi de 4,8 anos. No final do estudo ou na última visita antes de um desfecho primário, 77% do grupo tratado com losartana e 73% do grupo tratado com atenolol ainda estavam tomando a medicação do estudo. Dos pacientes que ainda tomavam a medicação do estudo, as doses médias de losartana e atenolol foram de cerca de 80 mg/dia, e 15% estavam tomando atenolol ou losartana como monoterapia, enquanto 77% também estavam recebendo hidroclorotiazida (na dose média de 20 mg/dia em cada grupo). A redução da pressão arterial medida no vale foi semelhante para ambos os grupos de tratamento, mas a pressão arterial não foi medida em nenhum outro momento do dia. No final do estudo ou na última visita antes de um desfecho primário, as pressões sanguíneas médias foram de 144,1/81,3 mmHg para o grupo tratado com losartana e 145,4/80,9 mmHg para o grupo tratado com atenolol [a diferença na PAS de 1,3 mmHg foi significativa (p
desfecho primário foi a primeira ocorrência de morte cardiovascular, acidente vascular cerebral não fatal ou infarto do miocárdio não fatal. Os pacientes com eventos não fatais permaneceram no estudo, de modo que também houve um exame do primeiro evento de cada tipo, mesmo que não fosse o primeiro evento (por exemplo, um acidente vascular cerebral após um infarto do miocárdio inicial seria contado na análise do acidente vascular cerebral) . O tratamento com losartana resultou em redução de 13% (p=0,021) no risco do desfecho primário comparado ao grupo atenolol; essa diferença foi principalmente o resultado de um efeito no acidente vascular cerebral fatal e não fatal. O tratamento com losartana reduziu o risco de acidente vascular cerebral em 25% em relação ao atenolol (p=0,001).
Losartan Potássio-Hidroclorotiazida
Os 3 estudos controlados de losartana e hidroclorotiazida incluíram mais de 1300 pacientes avaliando a eficácia anti-hipertensiva de várias doses de losartana (25, 50 e 100 mg) e hidroclorotiazida concomitante (6,25, 12,5 e 25 mg). Um estudo fatorial comparou a combinação de losartana/hidroclorotiazida 50/12,5 mg com seus componentes e placebo. A combinação de losartana/hidroclorotiazida 50/12,5 mg resultou em uma resposta sistólica/diastólica ajustada ao placebo aproximadamente aditiva (15,5/9,0 mmHg para a combinação em comparação com 8,5/5,0 mmHg para losartana isoladamente e 7,0/3,0 mmHg para hidroclorotiazida sozinha). Outro estudo investigou a relação dose-resposta de várias doses de hidroclorotiazida (6,25, 12,5 e 25 mg) ou placebo em um fundo de losartana (50 mg) em pacientes não controlados adequadamente (pressão arterial diastólica sentada [SiDBP] 93-120 mmHg) em losartana (50 mg) isoladamente. O terceiro estudo investigou a relação dose-resposta de várias doses de losartana (25, 50 e 100 mg) ou placebo em um fundo de hidroclorotiazida (25 mg) em pacientes não adequadamente controlados (SiDBP93-120 mmHg) em hidroclorotiazida (25 mg) sozinho. Esses estudos mostraram uma resposta anti-hipertensiva adicional no vale (24 horas após a administração) de hidroclorotiazida 12,5 ou 25 mg adicionados a losartana 50 mg de 5,5/3,5 e 10,0/6,0 mmHg, respectivamente. Da mesma forma, houve uma resposta anti-hipertensiva adicional quando losartana 50 ou 100 mg foi adicionada a hidroclorotiazida 25 mg de 9,0/5,5 e 12,5/6,5 mmHg, respectivamente. Não houve efeito significativo sobre a frequência cardíaca.
Não houve diferença na resposta para homens e mulheres ou em pacientes com mais ou menos de 65 anos de idade.
Pacientes negros tiveram uma resposta maior à hidroclorotiazida do que pacientes não negros e uma resposta menor à losartana. A resposta geral à combinação foi semelhante para pacientes negros e não negros.
Hipertensão grave (SiDBP ≥110 mmHg)
segurança e eficácia de HYZAAR como terapia inicial para hipertensão grave (definida como média SiDBP ≥ 110 mmHg confirmada em 2 ocasiões separadas de todas as terapias anti-hipertensivas) foi estudada em um estudo multicêntrico, randomizado, duplo-cego de 6 semanas. Os pacientes foram randomizados para losartana e hidroclorotiazida (50/12,5 mg, uma vez ao dia) ou losartana (50 mg, uma vez ao dia) e acompanhados quanto à resposta da pressão arterial. Os pacientes foram titulados em intervalos de 2 semanas se a SiDBP não atingisse a meta (
estudo envolveu 585 pacientes, incluindo 264 (45%) mulheres, 124 (21%) negros e 21 (4%) ≥65 anos de idade. A pressão arterial média no início do estudo para a população total foi de 171/113 mmHg. A média de idade foi de 53 anos. Após 4 semanas de terapia, a SiDBP média foi 3,1 mmHg menor e a SiSBP média foi 5,6 mmHg menor no grupo tratado com HYZAAR. Como resultado, uma maior proporção de pacientes em uso de HYZAAR 12,5mg atingiu a pressão arterial diastólica alvo (17,6% para HYZAAR 12,5mg, 9,4% para losartana; p=0,006). Tendências semelhantes foram observadas quando os pacientes foram agrupados de acordo com sexo, raça ou idade (
Após 6 semanas de terapia, mais pacientes que receberam o regime de combinação atingiram a pressão arterial diastólica alvo do que aqueles que receberam o regime de monoterapia (29,8% versus 12,5%).
INFORMAÇÃO DO PACIENTE
HYZAAR® (HY-zar) (comprimidos de losartana potássica e hidroclorotiazida) 50/12,5 mg, 100/12,5 mg, 100/25 mg
Leia as informações do paciente que acompanham o HYZAAR ® antes de começar a tomá-lo e sempre que receber um reabastecimento. Pode haver novas informações. Este folheto não substitui a conversa com o seu médico sobre a sua condição e tratamento.
Qual é a informação mais importante que devo saber sobre HYZAAR?
- HYZAAR pode causar danos ou morte ao feto.
- Fale com o seu médico sobre outras formas de baixar a pressão arterial se planeia engravidar.
- Se engravidar enquanto estiver a tomar HYZAAR 12,5 mg informe o seu médico imediatamente.
O que é HYZAAR 12,5mg?
HYZAAR 12,5 mg contém 2 medicamentos prescritos, um bloqueador do receptor de angiotensina (BRA) e um diurético (pílula de água). É usado para:
- baixar a pressão arterial elevada (hipertensão). HYZAAR geralmente não é o primeiro medicamento usado para tratar a pressão alta.
- diminuir a chance de acidente vascular cerebral em pacientes com pressão alta e um problema cardíaco chamado hipertrofia ventricular esquerda (HVE). HYZAAR pode não ajudar pacientes negros com este problema.
HYZAAR não foi estudado em crianças com menos de 18 anos.
Pressão Arterial Alta (hipertensão). A pressão arterial é a força nos vasos sanguíneos quando o coração bate e quando o coração descansa. Você tem pressão alta quando a força é demais. O ingrediente losartana em HYZAAR 12,5 mg pode ajudar seus vasos sanguíneos a relaxarem para que sua pressão arterial seja mais baixa. A hidroclorotiazida em gredientin HYZAAR funciona fazendo com que seus rins eliminem mais água e sal.
Hipertrofia Ventricular Esquerda (HVE) é um alargamento das paredes da câmara esquerda do coração (a principal câmara de bombeamento do coração). LVH pode acontecer de várias coisas. A hipertensão arterial é a causa mais comum de HVE.
Quem não deve tomar HYZAAR?
Não tome HYZAAR 12,5 mg se você:
- são alérgicos a qualquer componente de HYZAAR. Veja uma lista completa de ingredientes em HYZAAR no final deste folheto.
- não estão urinando.
- tem diabetes e está tomando um medicamento chamado alisquireno para reduzir a pressão arterial.
O que devo dizer ao meu médico antes de tomar HYZAAR?
Informe o seu médico sobre todas as suas condições médicas, incluindo se você:
- está grávida ou planejando engravidar. Consulte “Quais são as informações mais importantes que devo saber sobre HYZAAR?”
- está amamentando ou planeja amamentar. HYZAAR pode passar para o seu leite e pode prejudicar o seu bebé. Você e seu médico devem decidir se você vai tomar HYZAAR ou amamentar. Você não deve fazer ambos.
- esteve vomitando (vômito), tendo diarréia, suando muito ou não bebendo líquidos suficientes. Estes podem fazer com que você tenha pressão arterial baixa.
- tem problemas de fígado
- tem problemas renais
- tem lúpus eritematoso sistêmico (Lúpus; LES)
- tem diabetes
- ter gota
- tem alguma alergia
- teve câncer de pele ou se desenvolver uma nova lesão de pele durante o tratamento. O tratamento com hidroclorotiazida pode aumentar o risco de alguns tipos de câncer de pele (câncer de pele não melanoma). Discuta com seu médico como proteger sua pele da exposição ao sol e com que frequência você deve se submeter a exames de câncer de pele.
Informe o seu médico sobre todos os medicamentos que você toma, incluindo medicamentos prescritos e não prescritos, vitaminas e suplementos de ervas.
HYZAAR 12,5 mg e alguns outros medicamentos podem interagir entre si. Informe especialmente o seu médico se estiver a tomar:
- suplementos de potássio
- substitutos do sal contendo potássio
- outros medicamentos que podem aumentar o potássio sérico
- pílulas de água (diuréticos)
- lítio (um medicamento usado para tratar um certo tipo de depressão)
- medicamentos usados para tratar a dor e a artrite, chamados anti-inflamatórios não esteroides (AINEs), incluindo inibidores da COX-2
- outros medicamentos para reduzir a pressão arterial.
Conheça os medicamentos que você toma. Mantenha uma lista dos seus medicamentos e mostre-a ao seu médico e farmacêutico quando receber um novo medicamento.
Como devo tomar HYZAAR 12,5mg?
- Tome HYZAAR 12,5 mg exatamente como prescrito pelo seu médico. O seu médico pode alterar a sua dose, se necessário.
- HYZAAR pode ser tomado com ou sem alimentos.
- Se você esquecer de uma dose, tome-a assim que se lembrar. Se estiver próximo da próxima dose, não tome a dose esquecida. Apenas tome a próxima dose no horário habitual.
- Se você tomar HYZAAR 12,5mg demais, ligue para o seu médico ou para o Centro de Controle de Intoxicações, ou dirija-se imediatamente ao pronto-socorro do hospital mais próximo.
- O seu médico pode fazer análises ao sangue de tempos a tempos enquanto estiver a tomar HYZAAR.
Quais são os possíveis efeitos colaterais do HYZAAR?
HYZAAR pode causar os seguintes efeitos colaterais que podem ser graves:
- Lesão ou morte de bebês não nascidos. Consulte “Quais são as informações mais importantes que devo saber sobre HYZAAR?”
- Reação alérgica. Os sintomas de uma reação alérgica são inchaço da face, lábios, garganta ou língua. Obtenha ajuda médica de emergência imediatamente e pare de tomar HYZAAR.
- Pressão arterial baixa (hipotensão). A pressão arterial baixa pode fazer com que você se sinta fraco ou tonto. Deite-se se você se sentir fraco ou tonto. Ligue para o seu médico imediatamente.
- Se você tiver problemas renais, poderá observar uma piora no funcionamento dos rins. Ligue para o seu médico se tiver inchaço nos pés, tornozelos ou mãos ou ganho de peso inexplicável.
- Uma condição nova ou agravada chamada lúpus eritematoso sistêmico (Lúpus; LES)
- Problemas oculares. Um dos medicamentos de HYZAAR 12,5 mg pode causar problemas oculares que, se não forem tratados, podem levar à perda de visão. Os sintomas de problemas oculares podem ocorrer dentro de horas a semanas após o início do HYZAAR. Informe o seu médico imediatamente se tiver:
- diminuição da visão
- dor nos olhos
- Sensibilidade da pele ao sol e risco de câncer de pele.
Os efeitos colaterais mais comuns de HYZAAR 12,5mg em pessoas com pressão alta são:
- “resfriados” (infecção respiratória superior)
- tontura
- nariz entupido
- dor nas costas
Informe o seu médico se tiver algum efeito colateral que o incomode ou que não vá embora. Esta não é uma lista completa de efeitos colaterais. Para obter uma lista completa, pergunte ao seu médico ou farmacêutico.
Como devo armazenar HYZAAR 12,5mg?
- Armazene HYZAAR em temperatura ambiente de 59°F a 86°F (15°C a 30°C).
- Mantenha HYZAAR em um recipiente bem fechado e mantenha HYZAAR longe da luz.
- Mantenha HYZAAR 12,5mg e todos os medicamentos fora do alcance das crianças.
Informações gerais sobre HYZAAR
Às vezes, medicamentos são prescritos para condições que não são mencionadas nos folhetos informativos do paciente. Não use HYZAAR para uma condição para a qual não foi prescrito. Não dê HYZAAR a outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los.
Este folheto resume as informações mais importantes sobre HYZAAR. Se você quiser mais informações, converse com seu médico. Você pode pedir ao seu farmacêutico ou médico informações escritas para profissionais de saúde.
Quais são os ingredientes de HYZAAR?
Ingredientes ativos: losartana potássica, hidroclorotiazida
Ingredientes inativos:
celulose microcristalina, lactose hidratada, amido pré-gelatinizado, estearato de magnésio, hidroxipropilcelulose, hipromelose, dióxido de titânio. HYZAAR 50/12.5 e HYZAAR 100/25 também contêm laca de alumínio D&C amarela nº 10.
HYZAAR 50/12.5, HYZAAR 100/12.5 e HYZAAR 100/25 também podem conter cera de carnaúba.
