Procardia 30mg Nifedipine Uso, efeitos colaterais e dosagem. Preço na farmácia online. Medicamentos genericos sem receita.
O que é Procardia 30mg e como é usado?
Procardia é um medicamento de prescrição usado para tratar os sintomas de dor no peito (angina), pressão alta (hipertensão) e hipertensão pulmonar. Procardia 30mg pode ser usado sozinho ou com outros medicamentos.
Procardia pertence a uma classe de medicamentos chamados bloqueadores dos canais de cálcio; Bloqueadores dos canais de cálcio, diidrofiridina.
Não se sabe se Procardia é seguro e eficaz em crianças.
Quais são os possíveis efeitos colaterais do Procardia?
Procardia pode causar efeitos colaterais graves, incluindo:
- febre,
- dor de garganta,
- Olhos queimando,
- dor de pele,
- erupção cutânea vermelha ou roxa com bolhas e descamação,
- agravamento da dor no peito,
- batimentos cardíacos acelerados,
- vibrando em seu peito,
- tontura,
- inchaço nas mãos ou pernas,
- dor de estômago superior e
- amarelecimento da pele ou dos olhos (icterícia)
Obtenha ajuda médica imediatamente, se tiver algum dos sintomas listados acima.
Os efeitos colaterais mais comuns de Procardia 30mg incluem:
- inchaço,
- rubor (calor, vermelhidão ou sensação de formigamento),
- dor de cabeça,
- tontura,
- náusea,
- azia, e
- sentindo-se fraco ou cansado
Informe o médico se tiver algum efeito colateral que o incomode ou que não desapareça.
Estes não são todos os possíveis efeitos colaterais do Procardia. Para mais informações, consulte seu médico ou farmacêutico.
DESCRIÇÃO
PROCARDIA® (nifedipina) é um medicamento antianginoso pertencente a uma classe de agentes farmacológicos, os bloqueadores dos canais de cálcio. A nifedipina é ácido 3,5-piridinadicarboxílico, 1,4-di-hidro-2,6-dimetil-4-(2-nitrofenil)-, éster dimetílico, C17H18N2O6, e tem a fórmula estrutural:
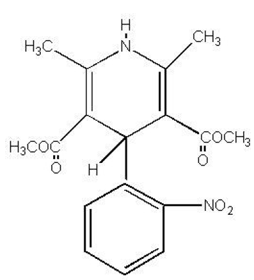
A nifedipina é uma substância cristalina amarela, praticamente insolúvel em água, mas solúvel em etanol. Tem um peso molecular de 346,3. As cápsulas de PROCARDIA são formuladas como cápsulas de gelatina mole para administração oral, cada uma contendo 10 mg de nifedipina.
Os ingredientes inertes da formulação são: glicerina; óleo de menta; polietileno glicol; cápsulas de gelatina mole (que contêm Amarelo 6 e podem conter óxido férrico vermelho e outros ingredientes inertes); e água. As cápsulas de 10 mg também contêm sacarina sódica.
INDICAÇÕES
Angina Vasospástica
PROCARDIA (nifedipina) é indicado para o manejo da angina vasoespástica confirmada por qualquer um dos seguintes critérios: 1) padrão clássico de angina em repouso acompanhada de supradesnivelamento do segmento ST, 2) angina ou espasmo da artéria coronária provocado por ergonovina, ou 3) demonstrado angiograficamente espasmo da artéria coronária. Nos pacientes que fizeram angiografia, a presença de doença obstrutiva fixa significativa não é incompatível com o diagnóstico de angina vasoespástica, desde que os critérios acima sejam satisfeitos. PROCARDIA 30mg também pode ser usado quando a apresentação clínica sugere um possível componente vasoespástico, mas onde o vasoespasmo não foi confirmado, por exemplo, quando a dor tem um limiar variável ao esforço ou quando a angina é refratária a nitratos e/ou doses adequadas de betabloqueadores.
Angina Crônica Estável (Angina Associada ao Esforço Clássica)
PROCARDIA 30mg é indicado para o tratamento da angina crônica estável (angina associada ao esforço) sem evidência de vasoespasmo em pacientes que permanecem sintomáticos apesar de doses adequadas de betabloqueadores e/ou nitratos orgânicos ou que não toleram esses agentes.
Na angina crônica estável (angina associada ao esforço), PROCARDIA foi eficaz em estudos controlados de até oito semanas de duração na redução da frequência da angina e no aumento da tolerância ao exercício, mas a confirmação da eficácia sustentada e a avaliação da segurança a longo prazo nesses pacientes são incompletas. .
Estudos controlados em um pequeno número de pacientes sugerem que o uso concomitante de PROCARDIA 30mg e agentes betabloqueadores pode ser benéfico em pacientes com angina crônica estável, mas as informações disponíveis não são suficientes para prever com confiança os efeitos do tratamento concomitante, especialmente em pacientes com função ventricular esquerda comprometida ou anormalidades de condução cardíaca. Ao introduzir tal terapia concomitante, deve-se ter cuidado para monitorar a pressão arterial de perto, pois pode ocorrer hipotensão grave devido aos efeitos combinados dos medicamentos. (Ver AVISOS .)
DOSAGEM E ADMINISTRAÇÃO
A dosagem de PROCARDIA 30mg necessária para suprimir a angina e que pode ser tolerada pelo paciente deve ser estabelecida por titulação. Doses excessivas podem resultar em hipotensão.
terapia deve ser iniciada com a cápsula de 10 mg. A dose inicial é uma cápsula de 10 mg, engolida inteira, 3 vezes/dia. A faixa de dose efetiva usual é de 10 a 20 mg três vezes ao dia. Alguns pacientes, especialmente aqueles com evidência de espasmo da artéria coronária, respondem apenas a doses mais altas, administração mais frequente ou ambos. Nesses pacientes, doses de 20 a 30 mg três ou quatro vezes ao dia podem ser eficazes. Doses acima de 120 mg por dia raramente são necessárias. Mais de 180 mg por dia não é recomendado.
Na maioria dos casos, a titulação de PROCARDIA deve ser realizada durante um período de 7 a 14 dias para que o médico possa avaliar a resposta a cada nível de dose e monitorar a pressão arterial antes de prosseguir com doses mais altas.
Se os sintomas assim o justificarem, a titulação pode prosseguir mais rapidamente, desde que o paciente seja avaliado com frequência. Com base no nível de atividade física do paciente, na frequência das crises e no consumo de nitroglicerina sublingual, a dose de PROCARDIA 30mg pode ser aumentada de 10 mg tid para 20 mg tid e depois para 30 mg tid durante um período de três dias.
Em pacientes hospitalizados sob observação cuidadosa, a dose pode ser aumentada em incrementos de 10 mg em períodos de quatro a seis horas, conforme necessário para controlar a dor e as arritmias devido à isquemia. Uma dose única raramente deve exceder 30 mg.
Evite a coadministração de nifedipina com sumo de toranja (ver FARMACOLOGIA CLÍNICA e INTERAÇÕES MEDICAMENTOSAS ).
Nenhum “efeito rebote” foi observado após a descontinuação de PROCARDIA. No entanto, se for necessária a descontinuação de PROCARDIA, a prática clínica sólida sugere que a dosagem deve ser diminuída gradualmente com supervisão médica rigorosa.
Coadministração com outros medicamentos antianginosos
nitroglicerina sublingual pode ser administrada conforme necessário para o controle de manifestações agudas de angina, particularmente durante a titulação de PROCARDIA. Ver INTERAÇÕES MEDICAMENTOSAS , para obter informações sobre a coadministração de PROCARDIA 30mg com betabloqueadores ou nitratos de ação prolongada.
COMO FORNECIDO
PROCÁRDIA cápsulas de gelatina mole são fornecidas em:
Frascos de 100: 10 mg ( NDC 0069-2600-66)
As cápsulas devem ser protegidas da luz e da umidade e armazenadas em temperatura ambiente controlada, 59° a 77°F (15° a 25°C) na embalagem original do fabricante.
Distribuído por: Pfizer Labs, Division of Pfizer Inc, NY, NY 10017. Revisado: julho de 2016
EFEITOS COLATERAIS
Em estudos controlados de dose múltipla nos Estados Unidos e no exterior, nos quais as reações adversas foram relatadas espontaneamente, os efeitos adversos foram frequentes, mas geralmente não graves e raramente exigiram a descontinuação da terapia ou ajuste de dose. A maioria eram consequências esperadas dos efeitos vasodilatadores de PROCARDIA.
Há também uma grande experiência não controlada em mais de 2.100 pacientes nos Estados Unidos. A maioria dos pacientes apresentou angina pectoris vasoespástica ou resistente, e cerca de metade recebeu tratamento concomitante com agentes bloqueadores betaadrenérgicos. Os eventos adversos mais comuns foram:
Incidência Aproximadamente 10%
Cardiovascular: edema periférico
Sistema nervoso central: tontura ou vertigem
Gastrointestinal: náusea
Sistêmico: dor de cabeça e rubor, fraqueza
Incidência Aproximadamente 5%
Cardiovascular: hipotensão transitória
Incidência de 2% ou menos
Cardiovascular: palpitação
Respiratório: congestão nasal e torácica, falta de ar
Gastrointestinal: diarréia, constipação, cólicas, flatulência
Musculoesquelético: inflamação, rigidez articular, cãibras musculares
Sistema nervoso central: tremores, nervosismo, nervosismo, distúrbios do sono, visão turva, dificuldades de equilíbrio
Outro: dermatite, prurido, urticária, febre, sudorese, calafrios, dificuldades sexuais
Incidência Aproximadamente 0,5%
Cardiovascular: síncope (principalmente com a dosagem inicial e/ou aumento da dose), eritromelalgia
Incidência inferior a 0,5%
Hematologico: trombocitopenia, anemia, leucopenia, púrpura
Gastrointestinal: hepatite alérgica
Rosto e garganta: angioedema (principalmente edema orofaríngeo com dificuldade respiratória em alguns pacientes), hiperplasia gengival
SNC: depressão, síndrome paranoide
Sentidos Especiais: cegueira transitória no pico do nível plasmático, zumbido
Urogenital: noctúria, poliúria
Outro: artrite com ANA (+), dermatite esfoliativa, ginecomastia
Musculoesquelético: mialgia
Vários desses efeitos colaterais parecem estar relacionados à dose. Edema periférico ocorreu em cerca de um em 25 pacientes com doses inferiores a 60 mg por dia e em cerca de um paciente em oito com 120 mg por dia ou mais. Hipotensão transitória, geralmente de gravidade leve a moderada e raramente exigindo descontinuação da terapia, ocorreu em um dos 50 pacientes com menos de 60 mg por dia e em um dos 20 pacientes com 120 mg por dia ou mais.
Muito raramente, a introdução da terapêutica com PROCARDIA 30 mg foi associada a um aumento da dor anginosa, possivelmente devido à hipotensão associada. A perda unilateral transitória da visão também ocorreu.
Além disso, eventos adversos mais graves foram observados, não facilmente distinguíveis da história natural da doença nesses pacientes. Ainda é possível, no entanto, que alguns ou muitos desses eventos estejam relacionados a drogas. Infarto do miocárdio ocorreu em cerca de 4% dos pacientes e insuficiência cardíaca congestiva ou edema pulmonar em cerca de 2%. Arritmias ventriculares ou distúrbios de condução ocorreram em menos de 0,5% dos pacientes.
Em um subgrupo de mais de 1.000 pacientes recebendo PROCARDIA 30mg com terapia concomitante com betabloqueador, o padrão e a incidência de reações adversas não foram diferentes daqueles de todo o grupo de pacientes tratados com PROCARDIA (nifedipina). (Ver PRECAUÇÕES .)
Em um subgrupo de aproximadamente 250 pacientes com diagnóstico de insuficiência cardíaca congestiva, bem como angina pectoris (cerca de 10% da população total de pacientes), tonturas ou vertigens, edema periférico, dor de cabeça ou rubor ocorreram em um em cada oito pacientes. Hipotensão ocorreu em cerca de um em cada 20 pacientes. Ocorreu síncope em aproximadamente um paciente em 250. Infarto do miocárdio ou sintomas de insuficiência cardíaca congestiva ocorreram em cerca de um paciente em cada 15. Arritmias atriais ou ventriculares ocorreram em cerca de um paciente em 150.
Na experiência pós-comercialização, houve relatos raros de dermatite esfoliativa causada por nifedipina. Houve relatos raros de eventos adversos cutâneos esfoliativos ou bolhosos (como eritema multiforme, síndrome de Stevens-Johnson e necrólise epidérmica tóxica) e reações de fotossensibilidade. Pustulose exantemática generalizada aguda também foi relatada.
INTERAÇÕES MEDICAMENTOSAS
Agentes bloqueadores beta-adrenérgicos
(Ver INDICAÇÕES E USO e AVISOS experiência em mais de 1.400 pacientes em um ensaio clínico não comparativo mostrou que a administração concomitante de PROCARDIA 30mg e agentes betabloqueadores geralmente é bem tolerada, mas houve relatos ocasionais na literatura sugerindo que a combinação pode aumentar a probabilidade de insuficiência cardíaca congestiva, hipotensão grave ou exacerbação da angina.
Nitratos de ação prolongada
PROCARDIA 30mg pode ser coadministrado com segurança com nitratos, mas não há estudos controlados para avaliar a eficácia antianginosa dessa combinação.
Digital
Como houve relatos isolados de pacientes com níveis elevados de digoxina e como existe uma possível interação entre digoxina e nifedipina, recomenda-se que os níveis de digoxina sejam monitorados ao iniciar, ajustar e descontinuar a nifedipina para evitar uma possível super ou subdigitalização .
Quinidina
Houve relatos raros de interação entre quinidina e nifedipina (com uma diminuição do nível plasmático de quinidina).
Anticoagulantes cumarínicos
Houve relatos raros de aumento do tempo de protrombina em pacientes tomando anticoagulantes cumarínicos aos quais PROCARDIA foi administrado. No entanto, a relação com a terapia com PROCARDIA é incerta.
Cimetidina
Um estudo em seis voluntários saudáveis mostrou um aumento significativo nos níveis plasmáticos de pico de nifedipina (80%) e na área sob a curva (74%) após um curso de uma semana de cimetidina a 1000 mg por dia e nifedipina a 40 mg por dia. dia. A ranitidina produziu aumentos menores e não significativos. O efeito pode ser mediado pela conhecida inibição da cimetidina no citocromo P-450 hepático, o sistema enzimático provavelmente responsável pelo metabolismo de primeira passagem da nifedipina. Se a terapia com nifedipina for iniciada em um paciente que está recebendo cimetidina, recomenda-se uma titulação cautelosa.
nifedipina é metabolizada pelo CYP3A4. A coadministração de nifedipina com fenitoína, um indutor do CYP3A4, reduz a exposição sistêmica à nifedipina em aproximadamente 70%. Evite a coadministração de nifedipina com fenitoína ou qualquer indutor conhecido do CYP3A4 ou considere uma terapia anti-hipertensiva alternativa.
Inibidores do CYP3A como fluconazol, itraconazol, claritromicina, eritromicina, nefazodona, fluoxetina, saquinavir, indinavir e nelfinavir podem resultar em aumento da exposição à nifedipina quando coadministrados. Monitoramento cuidadoso e ajuste de dose podem ser necessários; considerar iniciar nifedipina na dose mais baixa disponível se administrada concomitantemente com esses medicamentos.
Outras interações
Suco de toranja
coadministração de nifedipina com sumo de toranja resultou na duplicação da AUC e Cmax da nifedipina sem alteração da semivida. As concentrações plasmáticas aumentadas provavelmente resultam da inibição do metabolismo de primeira passagem relacionado ao CYP 3A4. Evite a ingestão de toranja e sumo de toranja enquanto estiver a tomar nifedipina.
AVISOS
Hipotensão excessiva
Embora, na maioria dos pacientes, o efeito hipotensor de PROCARDIA 30mg seja modesto e bem tolerado, alguns pacientes tiveram hipotensão excessiva e mal tolerada. Essas respostas geralmente ocorreram durante a titulação inicial ou no momento do ajuste posológico subsequente. Embora os pacientes raramente tenham experimentado hipotensão excessiva com PROCARDIA 30mg isolado, isso pode ser mais comum em pacientes em terapia concomitante com betabloqueadores. Embora não aprovado para esta finalidade, PROCARDIA e outras cápsulas de nifedipina de liberação imediata têm sido usadas (por via oral e sublingual) para redução aguda da pressão arterial. Vários relatos bem documentados descrevem casos de hipotensão profunda, infarto do miocárdio e morte quando a nifedipina de liberação imediata foi usada dessa maneira. As cápsulas de PROCARDIA não devem ser utilizadas para a redução aguda da pressão arterial.
Hipotensão grave e/ou aumento da necessidade de volume de líquidos foram relatados em pacientes que receberam PROCARDIA 30mg em conjunto com um agente betabloqueador que foram submetidos a cirurgia de revascularização do miocárdio usando altas doses de anestesia com fentanil. A interação com altas doses de fentanil parece ser devido à combinação de PROCARDIA e um betabloqueador, mas a possibilidade de que possa ocorrer com PROCARDIA 30mg isoladamente, com baixas doses de fentanil, em outros procedimentos cirúrgicos ou com outros analgésicos narcóticos não pode ser descartado. Em pacientes tratados com PROCARDIA, nos quais a cirurgia com altas doses de anestesia com fentanil é contemplada, o médico deve estar ciente desses problemas potenciais e, se a condição do paciente permitir, deve haver tempo suficiente (pelo menos 36 horas) para que PROCARDIA 30mg seja lavado do o corpo antes da cirurgia.
Aumento da Angina e/ou Infarto do Miocárdio
Raramente, os pacientes, particularmente aqueles com doença arterial coronariana obstrutiva grave, desenvolveram um aumento bem documentado da frequência, duração e/ou gravidade da angina ou infarto agudo do miocárdio ao iniciar PROCARDIA 30mg ou no momento do aumento da dose. O mecanismo deste efeito não está estabelecido.
Vários ensaios clínicos randomizados e bem controlados estudaram o uso de nifedipina de liberação imediata em pacientes que acabaram de sofrer infarto do miocárdio. Em nenhum destes ensaios a nifedipina de libertação imediata pareceu proporcionar qualquer benefício. Em alguns dos ensaios, os pacientes que receberam nifedipina de liberação imediata tiveram resultados significativamente piores do que os pacientes que receberam placebo. As cápsulas de PROCARDIA 30mg não devem ser administradas na primeira ou duas semanas após o infarto do miocárdio e também devem ser evitadas no contexto de síndrome coronariana aguda (quando o infarto pode ser iminente).
Uso na hipertensão essencial
PROCARDIA 30mg e outras cápsulas de nifedipina de liberação imediata também têm sido usadas para o controle a longo prazo da hipertensão essencial, embora as cápsulas de PROCARDIA 30mg não tenham sido aprovadas para esse fim e não tenham sido realizados estudos adequadamente controlados para definir uma dose ou intervalo de dose apropriados. para tal tratamento. PROCARDIA 30mg cápsulas não deve ser usado para o controle da hipertensão essencial.
Retirada do Beta Bloqueador
Pacientes recentemente retirados de betabloqueadores podem desenvolver uma síndrome de abstinência com aumento da angina, provavelmente relacionada ao aumento da sensibilidade às catecolaminas. O início do tratamento com PROCARDIA 30mg não previne esta ocorrência e pode-se esperar que a exacerbe ao provocar a liberação reflexa de catecolaminas. Houve relatos ocasionais de aumento da angina em um cenário de retirada de betabloqueador e início de PROCARDIA. É importante diminuir gradualmente os betabloqueadores, se possível, em vez de interrompê-los abruptamente antes de iniciar PROCARDIA.
Insuficiência Cardíaca Congestiva
Raramente, os pacientes, geralmente aqueles que recebem um betabloqueador, desenvolveram insuficiência cardíaca após o início do PROCARDIA. Pacientes com estenose aórtica apertada podem estar em maior risco para tal evento, pois o efeito de descarga de PROCARDIA 30mg seria menos benéfico para esses pacientes, devido à sua impedância fixa para fluir através da válvula aórtica.
PRECAUÇÕES
Em geral
Hipotensão
Como PROCARDIA diminui a resistência vascular periférica, sugere-se o monitoramento cuidadoso da pressão arterial durante a administração inicial e a titulação de PROCARDIA 30mg. A observação cuidadosa é especialmente recomendada para pacientes que já tomam medicamentos conhecidos por reduzir a pressão arterial. (Ver AVISOS .)
Edema periférico
Edema periférico leve a moderado, tipicamente associado à vasodilatação arterial e não devido à disfunção ventricular esquerda, ocorre em cerca de um em cada dez pacientes tratados com PROCARDIA (nifedipina). Esse edema ocorre principalmente nas extremidades inferiores e geralmente responde à terapia diurética. Em pacientes cuja angina é complicada por insuficiência cardíaca congestiva, deve-se ter cuidado para diferenciar esse edema periférico dos efeitos da disfunção ventricular esquerda crescente.
Testes laboratoriais
Foram observadas elevações raras, geralmente transitórias, mas ocasionalmente significativas de enzimas como fosfatase alcalina, CPK, LDH, SGOT e SGPT. A relação com a terapia com PROCARDIA é incerta na maioria dos casos, mas provável em alguns. Essas anormalidades laboratoriais raramente foram associadas a sintomas clínicos; entretanto, colestase com ou sem icterícia foi relatada. Raros casos de hepatite alérgica foram relatados.
PROCARDIA 30mg, como outros bloqueadores dos canais de cálcio, diminui a agregação plaquetária in vitro. Estudos clínicos limitados demonstraram uma diminuição moderada, mas estatisticamente significativa, na agregação plaquetária e um aumento no tempo de sangramento em alguns pacientes com PROCARDIA. Acredita-se que isso seja uma função da inibição do transporte de cálcio através da membrana plaquetária. Nenhum significado clínico para esses achados foi demonstrado.
Teste de Coombs direto positivo com/sem anemia hemolítica foi relatado, mas não foi possível determinar uma relação causal entre a administração de PROCARDIA e a positividade deste teste laboratorial, incluindo hemólise.
Embora PROCARDIA 30mg tenha sido usado com segurança em pacientes com disfunção renal e tenha sido relatado que exerce um efeito benéfico, em certos casos, elevações raras e reversíveis de BUN e creatinina sérica foram relatadas em pacientes com insuficiência renal crônica pré-existente. A relação com a terapia com PROCARDIA é incerta na maioria dos casos, mas provável em alguns.
Carcinogênese, Mutagênese, Prejuízo da Fertilidade
nifedipina foi administrada por via oral a ratos durante dois anos e não se mostrou cancerígena. Quando administrado a ratos antes do acasalamento, a nifedipina causou redução da fertilidade em uma dose aproximadamente 5 vezes a dose humana máxima recomendada. Há um relato na literatura de redução reversível na capacidade do esperma humano obtido de um número limitado de homens inférteis tomando as doses recomendadas de nifedipina para se ligar e fertilizar um óvulo in vitro. Os estudos de mutagenicidade in vivo foram negativos.
Gravidez
nifedipina demonstrou produzir achados teratogênicos em ratos e coelhos, incluindo anomalias digitais semelhantes às relatadas para a fenitoína. Anomalias digitais foram relatadas como ocorrendo com outros membros da classe das diidropiridinas e são possivelmente resultado de comprometimento do fluxo sanguíneo uterino. A administração de nifedipina foi associada a uma variedade de efeitos embriotóxicos, placentotóxicos e fetotóxicos, incluindo fetos atrofiados (ratos, camundongos, coelhos), deformidades nas costelas (camundongos), fenda palatina (camundongos), placentas pequenas e vilosidades coriônicas subdesenvolvidas (macacos), e óbitos fetais (ratos, camundongos, coelhos) e gravidez prolongada/sobrevivência neonatal diminuída (ratos; não avaliado em outras espécies). Numa base de mg/kg, todas as doses associadas aos efeitos embriotóxicos ou fetotóxicos teratogénicos em animais foram superiores (5 a 50 vezes) à dose humana máxima recomendada de 120 mg/dia. Em uma base de mg/m², algumas doses foram maiores e outras menores do que a dose humana máxima recomendada, mas todas estavam dentro de uma ordem de magnitude dela. As doses associadas a efeitos placentotóxicos em macacos foram equivalentes ou inferiores à dose humana máxima recomendada em mg/m².
Não existem estudos adequados e bem controlados em mulheres grávidas. PROCARDIA deve ser usado durante a gravidez apenas se o benefício potencial justificar o risco potencial.
Lactação
A nifedipina é transferida através do leite materno. PROCARDIA deve ser usado durante a amamentação apenas se o benefício potencial justificar o risco potencial.
Uso Pediátrico
A segurança e eficácia em pacientes pediátricos não foram estabelecidas. O uso na população pediátrica não é recomendado.
Uso Geriátrico
A idade parece ter um efeito significativo na farmacocinética da nifedipina. A depuração é diminuída resultando em uma AUC mais alta em idosos. Estas alterações não são devidas a alterações na função renal (ver FARMACOLOGIA CLÍNICA , Farmacocinética ).
SOBREDOSAGEM
experiência com superdosagem de nifedipina é limitada. Geralmente, a superdosagem com nifedipina levando a hipotensão pronunciada requer suporte cardiovascular ativo, incluindo monitoramento da função cardiovascular e respiratória, elevação das extremidades e uso criterioso de infusão de cálcio, agentes vasopressores e fluidos. Espera-se que a depuração da nifedipina seja prolongada em pacientes com função hepática prejudicada. Como a nifedipina é altamente ligada às proteínas, a diálise provavelmente não trará nenhum benefício; no entanto, a plasmaférese pode ser benéfica.
CONTRA-INDICAÇÕES
Reação de hipersensibilidade conhecida ao PROCARDIA.
FARMACOLOGIA CLÍNICA
PROCARDIA é um inibidor do influxo de iões de cálcio (bloqueador dos canais lentos ou antagonista do ião de cálcio) e inibe o influxo transmembranar de iões de cálcio no músculo cardíaco e no músculo liso. Os processos contráteis do músculo cardíaco e do músculo liso vascular são dependentes do movimento de íons cálcio extracelulares para dentro dessas células por meio de canais iônicos específicos. PROCARDIA 30mg inibe seletivamente o influxo de íons cálcio através da membrana celular do músculo cardíaco e do músculo liso vascular sem alterar as concentrações séricas de cálcio.
Mecanismo de ação
O meio preciso pelo qual essa inibição alivia a angina não foi totalmente determinado, mas inclui pelo menos os dois mecanismos a seguir:
Relaxamento e prevenção do espasmo da artéria coronária
PROCARDIA dilata as principais artérias coronárias e arteríolas coronárias, tanto em regiões normais como isquêmicas, e é um potente inibidor do espasmo da artéria coronária, seja espontâneo ou induzido por ergonovina. Esta propriedade aumenta o fornecimento de oxigênio ao miocárdio em pacientes com espasmo da artéria coronária e é responsável pela eficácia de PROCARDIA 30mg na angina vasoespástica (de Prinzmetal ou variante). Se esse efeito desempenha algum papel na angina clássica não está claro, mas estudos de tolerância ao exercício não mostraram um aumento no produto máximo da taxa de exercício-pressão, uma medida amplamente aceita da utilização de oxigênio. Isso sugere que, em geral, o alívio do espasmo ou dilatação das artérias coronárias não é um fator importante na angina clássica.
Redução da utilização de oxigênio
PROCARDIA reduz regularmente a pressão arterial em repouso e em um determinado nível de exercício, dilatando as arteríolas periféricas e reduzindo a resistência periférica total (pós-carga) contra a qual o coração trabalha. Essa descarga do coração reduz o consumo de energia do miocárdio e as necessidades de oxigênio e provavelmente é responsável pela eficácia do PROCARDIA na angina crônica estável.
Farmacocinética e Metabolismo
PROCARDIA é rápida e totalmente absorvido após administração oral. A droga é detectável no soro 10 minutos após a administração oral, e os níveis sanguíneos de pico ocorrem em aproximadamente 30 minutos. A biodisponibilidade é proporcional à dose de 10 a 30 mg; a meia-vida não muda significativamente com a dose. Há pouca diferença na biodisponibilidade relativa quando as cápsulas de PROCARDIA são administradas por via oral e deglutidas inteiras, mordidas e deglutidas ou mordidas e mantidas sublingualmente. No entanto, morder a cápsula antes de engolir resulta em concentrações plasmáticas ligeiramente mais precoces (27 ng/mL 10 minutos após 10 mg) do que se as cápsulas forem engolidas intactas. PROCARDIA 30mg é altamente ligado às proteínas séricas. PROCARDIA é extensivamente convertido em metabólitos inativos e aproximadamente 80% de PROCARDIA 30mg e metabólitos são eliminados pelos rins. A meia-vida de eliminação da nifedipina é de aproximadamente duas horas. Como a biotransformação hepática é a via predominante para a eliminação da nifedipina, a farmacocinética pode ser alterada em pacientes com doença hepática crônica. Pacientes com insuficiência hepática (cirrose hepática) têm uma meia-vida de disposição mais longa e maior biodisponibilidade de nifedipina do que voluntários saudáveis. O grau de ligação da nifedipina às proteínas séricas é alto (92-98%). A ligação às proteínas pode ser bastante reduzida em pacientes com insuficiência renal ou hepática.
Após administração intravenosa, a depuração da nifedipina foi diminuída em 33% em indivíduos idosos saudáveis em relação a indivíduos jovens saudáveis.
Hemodinâmica
Como outros bloqueadores de canais lentos, PROCARDIA exerce um efeito inotrópico negativo no tecido miocárdico isolado. Isso raramente, ou nunca, é visto em animais intactos ou no homem, provavelmente devido a respostas reflexas aos seus efeitos vasodilatadores. No homem, PROCARDIA 30mg causa diminuição da resistência vascular periférica e queda na pressão sistólica e diastólica, geralmente modesta (5-10 mmHg sistólica), mas às vezes maior. Geralmente há um pequeno aumento da frequência cardíaca, uma resposta reflexa à vasodilatação. As medições da função cardíaca em pacientes com função ventricular normal geralmente encontraram um pequeno aumento no índice cardíaco sem grandes efeitos na fração de ejeção, pressão diastólica final do ventrículo esquerdo (LVEDP) ou volume (LVEDV). Em pacientes com função ventricular prejudicada, a maioria dos estudos agudos mostrou algum aumento na fração de ejeção e redução na pressão de enchimento do ventrículo esquerdo.
Efeitos eletrofisiológicos
Embora, como outros membros de sua classe, PROCARDIA diminua a função do nó sinoatrial e a condução atrioventricular em preparações miocárdicas isoladas, tais efeitos não foram observados em estudos em animais intactos ou no homem. Em estudos eletrofisiológicos formais, predominantemente em pacientes com sistemas de condução normais, PROCARDIA 30mg não apresentou tendência a prolongar a condução atrioventricular, prolongar o tempo de recuperação do nó sinusal ou diminuir a frequência sinusal.
INFORMAÇÃO DO PACIENTE
Nenhuma informação fornecida. Por favor, consulte o AVISOS e PRECAUÇÕES Seções.
